MỤC LỤC CHƯƠNG
|
Cấu trúc
Kiểm soát thần kinh của Đường thở
Chức năng
Sức cản đường thở Gắng sức thở ra tối đa
|
Trên đường đi từ mũi hoặc miệng đến vùng trao đổi khí của phổi, không khí đi qua thanh quản và sau đó dọc theo một loạt các cấu trúc hình ống phân nhánh dần từ khí quản xuống các tiểu phế quản nhỏ nhất. Để chuẩn bị cho việc thảo luận về các bệnh lý ảnh hưởng đến đường thở, chương này mô tả cấu trúc của các đường thở này và sau đó xem xét cách chúng hoạt động.
CẤU TRÚC
Khí quản, phế quản và các tiểu phế quản cho đến tiểu phế quản tận tạo thành đường thở dẫn khí. Chức năng của chúng là vận chuyển khí và bảo vệ phần phổi ở xa khỏi các chất ô nhiễm hít vào, nhưng chúng không trực tiếp tham gia vào quá trình trao đổi khí. Vượt qua tiểu phế quản tận là các tiểu phế quản hô hấp. Chúng đánh dấu sự khởi đầu của vùng hô hấp của phổi, nơi diễn ra quá trình trao đổi khí. Các tiểu phế quản hô hấp được coi là một phần của vùng trao đổi khí của phổi vì có một số phế nang hiện diện dọc theo một phần thành của chúng. Với các thế hệ kế tiếp của tiểu phế quản hô hấp, ngày càng có nhiều phế nang xuất hiện dọc theo thành cho đến vị trí các ống phế nang, vốn được “phế nang hóa” hoàn toàn (Hình 4.1). Cuộc thảo luận trong chương này chỉ giới hạn ở các đường thở dẫn khí và những khía cạnh của các đường thở ở xa hơn có ảnh hưởng đến sự di chuyển của không khí nhưng không ảnh hưởng đến trao đổi khí. Cấu trúc phế nang được thảo luận thêm trong Chương 8.
|
Đường thở dẫn khí: khí quản, phế quản, các tiểu phế quản cho đến tiểu phế quản tận
Vùng hô hấp: tiểu phế quản hô hấp, ống phế nang và phế nang
|
Đường thở được cấu tạo bởi nhiều lớp mô (Hình 4.2). Liền kề với lòng đường thở là lớp niêm mạc, bên dưới là màng đáy ngăn cách các tế bào biểu mô của niêm mạc với lớp dưới niêm mạc. Bên trong lớp dưới niêm mạc có các tuyến nhầy (chất chứa bên trong được tiết qua niêm mạc vào lòng đường thở), cơ trơn, và mô liên kết lỏng lẻo với một số dây thần kinh và mạch bạch huyết. Bao quanh lớp dưới niêm mạc là một lớp sụn-sợi chứa các vòng sụn nâng đỡ cho nhiều thế hệ đường thở. Cuối cùng, một lớp mô quanh phế quản với mỡ, mạch bạch huyết, mạch máu và dây thần kinh bao quanh phần còn lại của thành đường thở. Mỗi lớp này sẽ được xem xét ở đây, với mô tả về các tế bào thành phần và cách cấu trúc thay đổi trong quá trình đi xuống xa hơn qua cây khí-phế quản.
Lớp bề mặt (niêm mạc) chủ yếu bao gồm các tế bào biểu mô trụ giả tầng. Nó được gọi là “giả tầng” vì ở khí quản và các phế quản lớn, niêm mạc có vẻ dày bằng nhiều tế bào, do hình dạng trụ và vị trí khác nhau của các nhân; tuy nhiên, mỗi tế bào thực sự đều nằm trên màng đáy (xem Hình 4.2A). Các lông chuyển lót trong lòng đường thở chịu trách nhiệm bảo vệ các đường thở sâu hơn bằng cách đẩy các chất tiết của khí-phế quản (và các hạt hít vào bị mắc kẹt trong đó) về phía hầu họng. Các lông chuyển của tế bào biểu mô đường thở có cấu trúc siêu vi đặc trưng thấy ở các tế bào có lông chuyển khác: một cặp vi ống trung tâm và một vòng ngoài gồm chín vi ống kép (xem Hình 22.1). Các nhánh bên nhỏ gọi là tay dynein, chứa adenosine triphosphatase (ATPase) dynein, được tìm thấy trên các vi ống kép bên ngoài. Cấu hình và chức năng phù hợp của các tay dynein là cần thiết cho hoạt động bình thường của lông chuyển, và những bệnh nhân có lông chuyển thiếu các tay dynein hoạt động đầy đủ sẽ bị suy giảm hoạt động lông chuyển và do đó phát triển các bệnh nhiễm trùng phế quản-phổi tái phát.
Rải rác giữa các tế bào biểu mô có lông chuyển là các tế bào biểu mô tiết mucin gọi là tế bào hình đài, có chức năng sản xuất và tiết mucin vào lòng đường thở. Thông thường, tế bào hình đài phổ biến hơn ở các đường thở gần. Số lượng của chúng giảm dần về phía ngoại vi và chúng không có mặt ở các tiểu phế quản tận. Mucin là các glycoprotein rất lớn, một số trong đó liên kết với màng tế bào biểu mô đường thở, trong khi những loại khác được tiết vào đường thở. Mucin được tiết ra có thể polyme hóa, giãn nở lớn về mặt vật lý, và liên kết với nước, chất điện giải và các phân tử khác để tạo thành một lớp gel nhầy nhớt, điều này cần thiết cho sự chuyển động bình thường của lông chuyển và do đó cần thiết cho việc làm sạch các hạt và vi sinh vật hít vào khỏi đường thở. Ở người, có bảy loại mucin chính của đường thở; hai loại quan trọng nhất dường như là MUC5AC, được sản xuất chủ yếu bởi các tế bào hình đài, và MUC5B, được sản xuất chủ yếu bởi các tế bào trong các tuyến dưới niêm mạc (xem phần sau). Trong các chất tiết đường thở khỏe mạnh bình thường, MUC5AC là mucin có nhiều nhất.
Lớp niêm mạc của các đường thở lớn bao gồm các tế bào biểu mô trụ giả tầng có lông chuyển. Biểu mô bề mặt dường như có các chức năng quan trọng khác có thể bị thay đổi trong một số tình trạng lâm sàng nhất định. Nhờ các liên kết chặt chẽ giữa các tế bào biểu mô ở bề mặt lòng ống, biểu mô ngăn chặn sự xâm nhập của vật lạ hít vào đến các lớp sâu hơn của thành đường thở. Có bằng chứng cho thấy sự phá vỡ chức năng hàng rào này do viêm, cho phép các kháng nguyên xâm nhập qua bề mặt biểu mô, là một yếu tố quan trọng trong bệnh hen suyễn. Một chức năng quan trọng khác của biểu mô liên quan đến việc vận chuyển và điều hòa tích cực các ion, đặc biệt là clorua và bicarbonate, để duy trì một môi trường ion thuận lợi trong lớp nhầy lót thành đường thở. Trong bệnh xơ nang, sự bất thường trong vận chuyển clorua của các tế bào biểu mô bề mặt đóng một vai trò quan trọng trong cơ chế bệnh sinh (xem Chương 7).
Các tế bào đáy nằm xen kẽ sâu trong lớp biểu mô, tiếp giáp với màng đáy. Chức năng của tế bào đáy là biệt hóa và bổ sung cho các tế bào bề mặt hơn của niêm mạc, có thể là tế bào có lông chuyển hoặc tế bào hình đài tiết dịch. Ở các đường thở xa hơn và tiểu phế quản tận, các tế bào Club được tìm thấy xen kẽ giữa các tế bào biểu mô có lông chuyển. Các tế bào Club, hoạt động như tế bào tiền thân cho chính chúng và cho các tế bào có lông chuyển, có một số chức năng bảo vệ, bao gồm tổng hợp các phân tử miễn dịch và một lượng nhỏ chất nhầy và protein surfactant, cũng như chuyển hóa các hóa chất hít vào. Một loại tế bào quan trọng khác được tìm thấy trong biểu mô đường thở là tế bào nội tiết thần kinh phổi (tế bào Kulchitsky). Những tế bào này là một phần của hệ thống hấp thụ và khử carboxyl tiền chất amin (amine precursor uptake and decarboxylation – APUD) và do đó có khả năng sản xuất các hormone amin (serotonin, dopamine, norepinephrine) và các sản phẩm polypeptide. Ngoài ra, các tế bào nội tiết thần kinh phổi có các bào tương mở rộng đến bề mặt lòng ống. Do đó, các tế bào này có thể tham gia vào việc cảm nhận thành phần của khí hít vào và đã được giả thuyết là đóng một vai trò trong việc kiểm soát thông khí và tưới máu theo vùng. Các loại tế bào khác nhau trong niêm mạc đường thở có ý nghĩa không chỉ vì vai trò sinh lý bình thường của chúng mà còn vì cách chúng phản ứng với sự kích thích đường thở và khả năng trở thành khối u.
Lớp dưới niêm mạc có hai thành phần chính: tuyến nhầy phế quản và cơ trơn phế quản. Chất nhầy là một chất giống như gel bao gồm chủ yếu là nước (97%) và mucin. Các protein khác bao gồm các chất điều hòa miễn dịch cũng có mặt, cũng như các chất điện giải, lipid và mảnh vỡ tế bào. Các tuyến nhầy nằm giữa các dải cơ trơn. Đáy của các tuyến được lót bởi các tế bào nhầy và tế bào thanh dịch và được nối với đường thở bằng các ống dẫn lót bởi các tế bào có lông chuyển. Ống dẫn này vận chuyển các chất tiết qua niêm mạc và đổ chúng vào lòng đường thở. Như đã lưu ý trước đó, mucin chính được sản xuất bởi các tuyến nhầy là MUC5B. Trong các tình trạng bệnh lý như bệnh phổi tắc nghẽn mạn tính và xơ nang, nơi có sự tăng sản và phì đại tuyến nhầy, MUC5B trở nên nổi bật hơn MUC5AC trong dịch tiết phế quản. Tuy nhiên, chức năng của MUC5AC và MUC5B có khác nhau hay không vẫn chưa được hiểu rõ. Ngoài ra, một đa hình phổ biến trong gen MUC5B có liên quan đến tính nhạy cảm với bệnh xơ phổi vô căn (idiopathic pulmonary fibrosis – IPF), một bệnh của nhu mô phổi được thảo luận trong Chương 11. Các tế bào thanh dịch cũng lót các tuyến nhầy; các tế bào này tiết ra proteoglycan và nhiều chất kháng khuẩn tham gia vào hệ miễn dịch bẩm sinh (xem Chương 22). Cơ trơn đường thở có mặt từ khí quản xuống đến tiểu phế quản và thậm chí cả ống phế nang. Sự rối loạn về số lượng và chức năng của cơ trơn là quan trọng trong bệnh tật, đặc biệt là trong trường hợp hen phế quản.
| Dịch tiết phế quản được sản xuất bởi các tuyến dưới niêm mạc và các tế bào hình đài trong niêm mạc. |
Lớp sụn-sợi rất quan trọng vì sụn cung cấp sự hỗ trợ cấu trúc cho đường thở. Hình dạng của sụn thay đổi đáng kể ở các cấp độ khác nhau của cây khí-phế quản, nhưng chức năng ở tất cả các cấp độ có lẽ là tương tự nhau.
Cấu trúc đường thở thay đổi đáng kể khi đi xuống xa hơn trong cây khí-phế quản. Chúng ta đã mô tả cấu trúc chung của đường thở, nhưng cấu trúc thay đổi đáng kể ở các cấp độ khác nhau. Một số khác biệt này được minh họa trong Hình 4.2. Trong quá trình đi xuống xa hơn qua cây khí-phế quản, các thay đổi sau đây thường được thấy:
- Lớp tế bào biểu mô trở nên mỏng dần cho đến khi chỉ còn một lớp tế bào hình khối ở cấp độ tiểu phế quản tận.
- Tế bào hình đài giảm số lượng cho đến khi chúng biến mất ở khoảng cấp độ tiểu phế quản tận. Các tế bào Club hình vòm xuất hiện ở các đường thở nhỏ hơn, nơi chúng góp phần vào việc sản xuất chất nhầy và các chức năng khác.
- Các tuyến nhầy, có mặt trong khí quản và các phế quản lớn, có số lượng nhiều nhất ở các phế quản cỡ trung bình. Chúng trở nên ít dần về phía xa và không có ở các tiểu phế quản.
- Cơ trơn thay đổi hình dạng ở các cấp độ khác nhau của cây khí-phế quản. Trong khí quản và các phế quản lớn, cơ trơn được tìm thấy dưới dạng các dải hoặc một mạng lưới xoắn ốc, trong khi ở các phế quản nhỏ hơn và tiểu phế quản, một lớp cơ trơn liên tục bao quanh đường thở. Khi kích thước đường thở giảm dần về phía xa trong cây khí-phế quản, cơ trơn thường chiếm một phần lớn hơn trong tổng độ dày của thành đường thở. Tỷ lệ cơ trơn so với độ dày thành đường thở trở nên tối đa ở cấp độ tiểu phế quản tận.
- Sụn cũng thay đổi hình dạng. Trong khí quản, các vòng sụn có hình móng ngựa, với mặt sau của khí quản không có sụn. Trong các phế quản, các mảng sụn trở nên nhỏ hơn và ít hơn về phía xa cho đến khi sụn không còn ở các tiểu phế quản.
Phần thảo luận trên mô tả nhiều đặc điểm cấu trúc của đường thở bình thường. Tuy nhiên, một loạt các thay đổi xảy ra khi tiếp xúc mãn tính với một chất kích thích như khói thuốc lá. Một số thay đổi này, đặc biệt là ở các tế bào biểu mô, rất quan trọng vì có khả năng dẫn đến ác tính sau này (xem Chương 20). Các thay đổi khác thể hiện rõ ở các cấu trúc tiết chất nhầy (tuyến nhầy phế quản và tế bào hình đài) và là những đặc điểm quan trọng của viêm phế quản mạn tính. Khi bị kích thích mạn tính, các tuyến nhầy phì đại, và các tế bào hình đài trở nên nhiều hơn và được tìm thấy ở xa hơn bình thường, ngay cả trong các tiểu phế quản tận. Các hàm ý của những thay đổi này trong các tình trạng bệnh lý được thảo luận trong Chương 6.
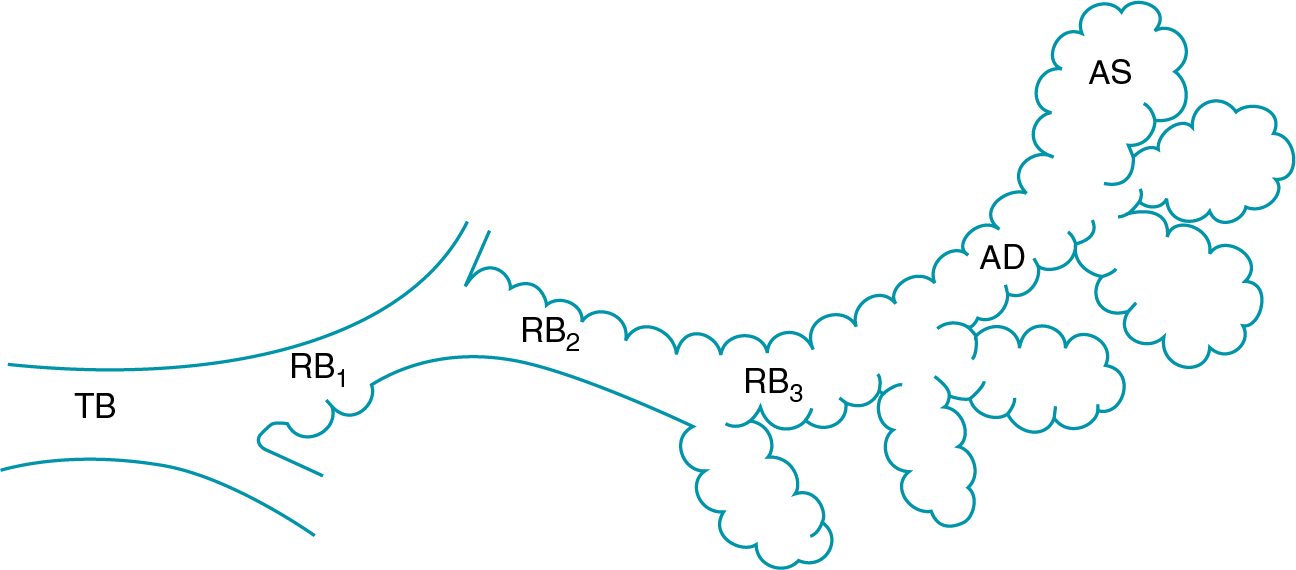
Hình 4.1 Sơ đồ phần xa nhất của cây hô hấp. Mỗi tiểu phế quản tận (TB) cung cấp cho nhiều thế hệ tiểu phế quản hô hấp (RB, từ RB₁ đến RB₃) có lớp biểu mô hô hấp (phế nang) lót thành ngày càng nhiều. Các ống phế nang (AD) được lót hoàn toàn bằng biểu mô phế nang, cũng như các túi phế nang (AS). Vùng phổi ở phía xa và được cung cấp bởi tiểu phế quản tận được gọi là chùm phế nang.
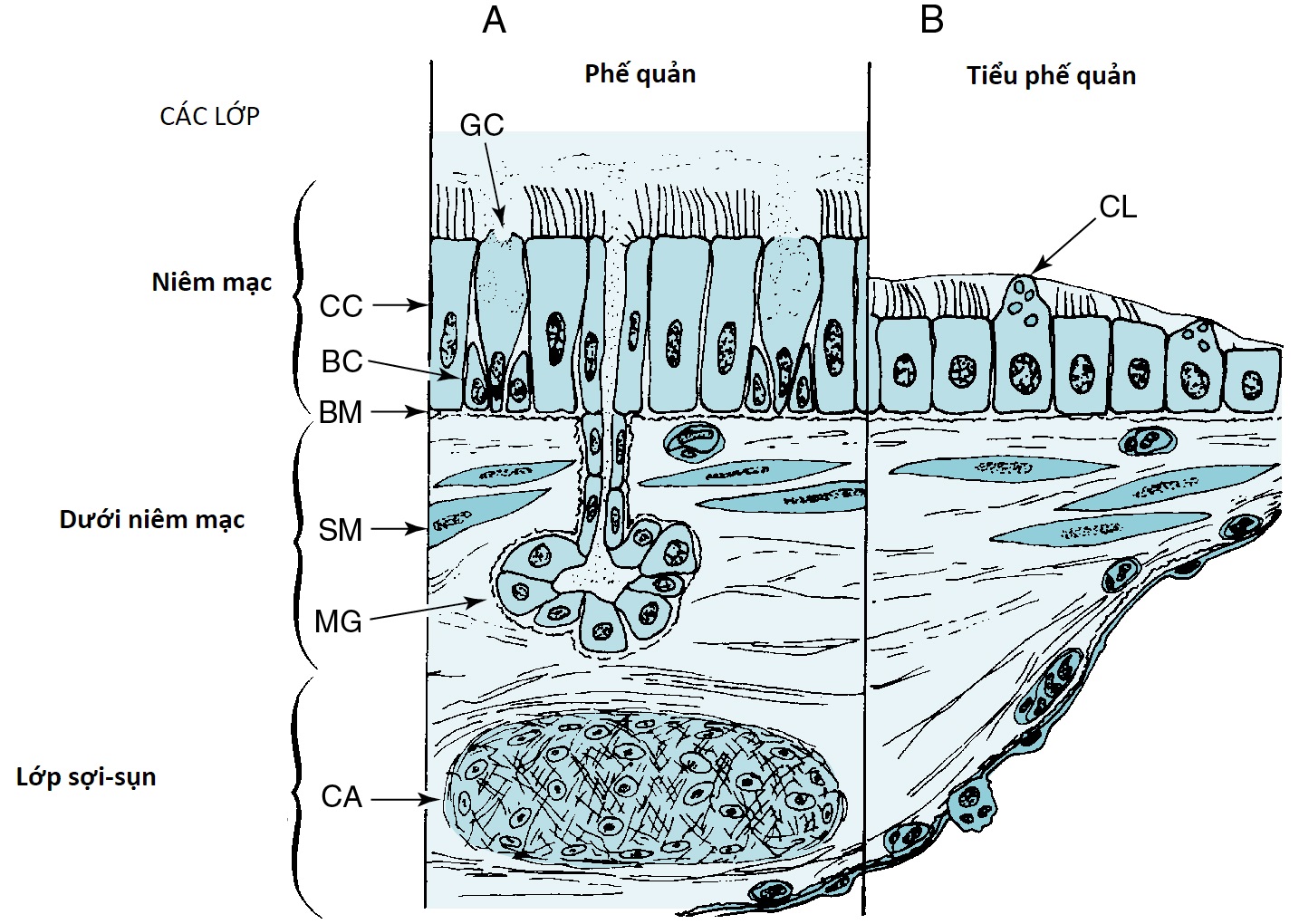
Hình 4.2 Sơ đồ các thành phần của thành đường thở. A, Cấp độ đường thở lớn (khí quản và phế quản). B, Cấp độ đường thở nhỏ (tiểu phế quản). BC, tế bào đáy; BM, màng đáy; CA, sụn; CC, tế bào biểu mô trụ có lông chuyển; CL, tế bào Club; GC, tế bào hình đài; MG, tuyến nhầy; SM, cơ trơn.
Kiểm soát thần kinh của Đường thở
Sự chi phối thần kinh (kiểm soát thần kinh) của đường thở là một khía cạnh quan trọng của cấu trúc đường thở, có liên quan lâm sàng đặc biệt trong bệnh hen suyễn (xem Chương 5). Kiểm soát thần kinh của đường thở ảnh hưởng đến sự co và giãn của cơ trơn phế quản và hoạt động của các tuyến nhầy phế quản. Việc hiểu rõ về sự chi phối thần kinh, các thụ thể và các chất trung gian tham gia vào việc kiểm soát chức năng đường thở là quan trọng cả vì vai trò tiềm tàng của kiểm soát thần kinh trong cơ chế bệnh sinh của hen suyễn và vì vai trò đã được xác lập của dược lý trị liệu trong việc kích thích hoặc phong bế các thụ thể đường thở. Phần thảo luận sau đây tập trung vào ba thành phần của việc kiểm soát thần kinh đường thở: hệ phó giao cảm (cholinergic), hệ giao cảm (adrenergic), và hệ ức chế không adrenergic, không cholinergic (Hình 4.3).
Hệ thần kinh phó giao cảm cung cấp trương lực co thắt phế quản chính cho đường thở thông qua các nhánh của dây thần kinh phế vị (dây thần kinh sọ X, còn được gọi là dây thần kinh phế vị-dạ dày). Sự kích thích các nhánh phế vị này gây ra co cơ trơn trong thành đường thở; ngoài ra, các sợi phế vị còn chi phối các tuyến nhầy phế quản và các tế bào hình đài, dẫn đến tăng tiết từ cả hai thành phần của bộ máy tiết chất nhầy. Các thụ thể trên cơ trơn và bộ máy tiết chất nhầy là các thụ thể muscarinic cholinergic; chất dẫn truyền thần kinh là acetylcholine. Các thụ thể cholinergic này có mật độ dày đặc hơn ở các đường thở trung tâm so với các đường thở ngoại vi. Việc xác định nhiều phân nhóm của thụ thể muscarinic, làm sáng tỏ một loạt các tác động lên cả cơ trơn đường thở và các dây thần kinh cung cấp cho cơ trơn, và bằng chứng về sự “tương tác chéo” giữa các thụ thể muscarinic và adrenergic đã chứng minh rằng tín hiệu thụ thể muscarinic thực sự phức tạp hơn nhiều. Tuy nhiên, sơ đồ đơn giản hóa được mô tả trước đó cung cấp một khuôn khổ thực tế cho các cuộc thảo luận sau này về sinh lý bệnh và điều trị các bệnh đường thở. Ví dụ, các loại thuốc kháng cholinergic dạng hít như ipratropium và tiotropium phong bế các thụ thể muscarinic cholinergic, dẫn đến giãn phế quản và giảm sản xuất chất nhầy (xem Chương 6).
Vai trò của hệ thần kinh giao cảm (adrenergic) trong việc kiểm soát trương lực đường thở ít rõ ràng hơn nhiều vì sự chi phối thần kinh adrenergic ở đường thở của con người rất thưa thớt, nếu có. Mặc dù sự chi phối của các dây thần kinh giao cảm rất ít, nhưng có các thụ thể adrenergic, chủ yếu là β₂, trên cơ trơn phế quản được kích thích bởi các catecholamine lưu hành. Khi được kích thích, các thụ thể β₂ kích hoạt adenylate cyclase, làm tăng nồng độ cyclic adenosine monophosphate (cAMP) nội bào và gây giãn cơ trơn phế quản. Ngược lại, sự kích thích các thụ thể α-adrenergic ít nhiều hơn dẫn đến một mức độ co thắt phế quản. Mật độ thụ thể của các thụ thể β₂-adrenergic ngược lại với các thụ thể cholinergic; các thụ thể β₂-adrenergic có mật độ dày đặc hơn ở các đường thở ngoại vi so với các đường thở trung tâm. Các chất chủ vận β-adrenergic dạng hít gây giãn phế quản và là một phần quan trọng trong điều trị hen suyễn và COPD (xem Chương 6).
Việc tìm kiếm sự chi phối thần kinh của đường thở với tác dụng giãn cơ trơn (giãn phế quản) đã chứng minh một thành phần thứ ba của kiểm soát thần kinh, thường được gọi là hệ ức chế không adrenergic, không cholinergic. Tương tự như các dây thần kinh phó giao cảm của đường thở, các sợi thần kinh này chạy trong thân dây phế vị, nhưng khi được kích thích, chúng làm cho cơ trơn phế quản giãn ra, không co lại. Bằng chứng cho thấy các chất truyền dẫn giãn phế quản quan trọng cho các dây thần kinh này là nitric oxide và polypeptide vận mạch ruột (vasoactive intestinal peptide).
| Sự chi phối thần kinh phó giao cảm cung cấp trương lực co thắt phế quản cho đường thở; sự chi phối thần kinh ức chế không adrenergic, không cholinergic cung cấp trương lực giãn phế quản. Các thụ thể adrenergic có mặt trên cơ trơn phế quản mặc dù không có sự chi phối thần kinh giao cảm đáng kể. |
Cho đến nay, chỉ có sự điều khiển thần kinh đầu ra (tức là, kiểm soát ly tâm) đến đường thở được thảo luận. Ngoài ra, có các thụ thể đường thở với sự chi phối thần kinh cảm giác (hướng tâm). Các thụ thể này, nằm trong lớp biểu mô đường thở và phản ứng với các kích thích hóa học và cơ học khác nhau, bao gồm các thụ thể ho (“kích thích”) có myelin và các sợi C không myelin. Tín hiệu thần kinh được truyền từ các đầu dây cảm giác này trong các sợi hướng tâm của dây thần kinh phế vị. Thông tin cảm giác này không chỉ được truyền đến hệ thần kinh trung ương thông qua các sợi phế vị hướng tâm mà còn chịu trách nhiệm kích hoạt các phản xạ cục bộ gây giải phóng các chất trung gian gọi là tachykinin từ các đầu dây thần kinh trong thành đường thở. Các tachykinin, bao gồm chất P và neurokinin A, có thể gây co thắt phế quản, tăng tiết tuyến dưới niêm mạc, và tăng tính thấm thành mạch (xem Hình 4.3). Tuy nhiên, mức độ quan trọng của chúng trong các tình trạng bệnh lý như hen suyễn vẫn chưa được biết chắc chắn.
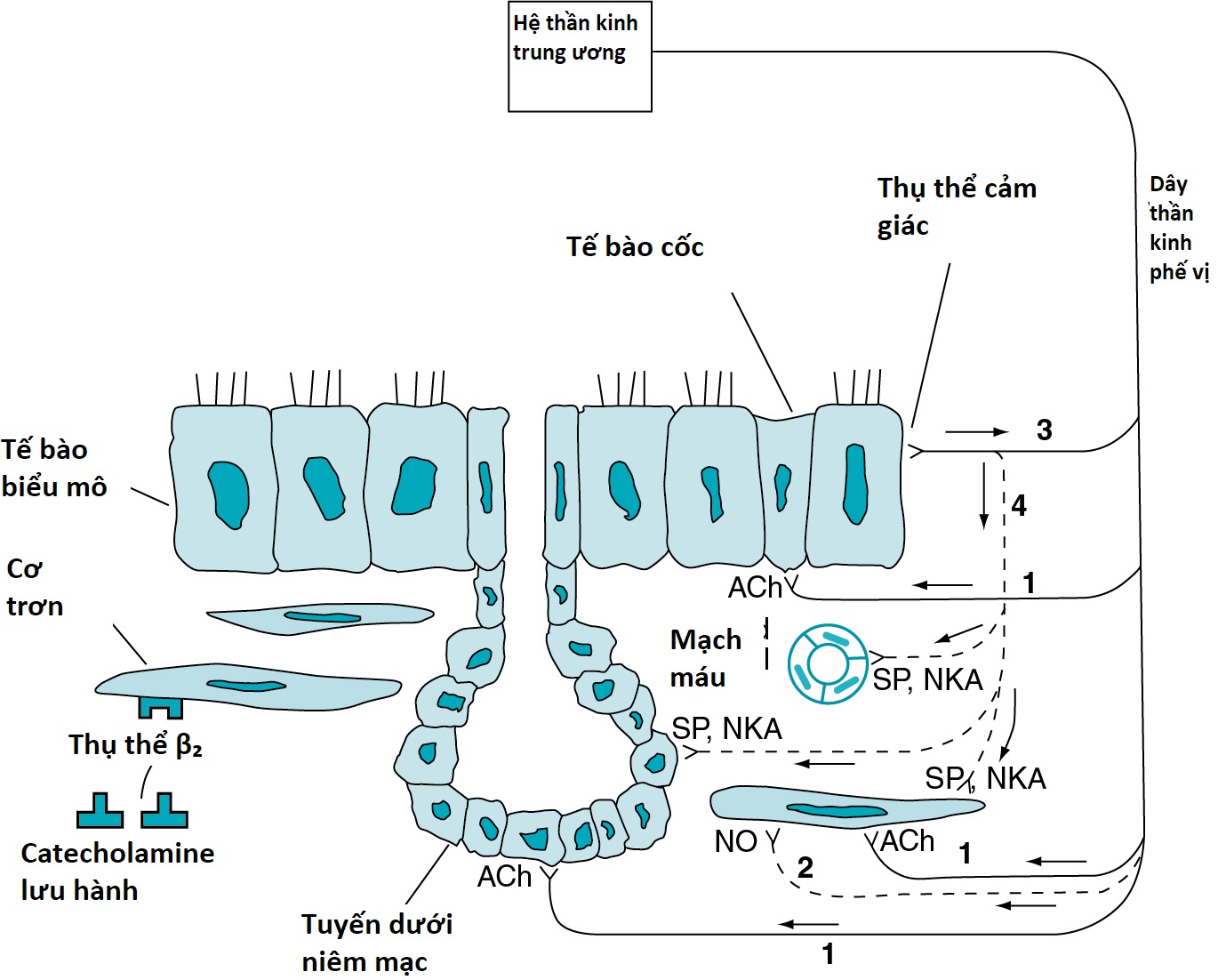
Hình 4.3 Sơ đồ kiểm soát thần kinh của đường thở. Các sợi phó giao cảm chi phối tế bào cơ trơn đường thở, tuyến dưới niêm mạc, và tế bào hình đài được đánh số 1; sự chi phối không adrenergic, không cholinergic của tế bào cơ trơn đường thở được đánh số 2; sự chi phối hướng tâm của tế bào biểu mô đường thở được đánh số 3; và luồng thần kinh dọc theo con đường được đánh số 4 đi đến dây thần kinh phế vị nhưng cũng có tác động lên tế bào cơ trơn đường thở, tuyến dưới niêm mạc, và mạch máu thông qua các phản xạ cục bộ. ACh, acetylcholine; NKA, neurokinin A; NO, nitric oxide; SP, chất P (substance P).
CHỨC NĂNG
Với mỗi nhịp thở, không khí chảy từ mũi hoặc miệng, qua cây phế quản, đến các vùng của phổi chịu trách nhiệm trao đổi khí. Để tạo ra luồng không khí này trong quá trình hít vào, áp lực trong các phế nang phải thấp hơn áp lực ở mũi hoặc miệng vì không khí chảy từ vùng có áp lực cao hơn đến vùng có áp lực thấp hơn. Cơ hoành và các cơ hít vào của thành ngực gây ra sự giãn nở của ngực và phổi, tạo ra áp lực âm trong khoang màng phổi và trong các phế nang, do đó khởi đầu luồng không khí.
Luồng khí trong đường thở có thể được coi là tương tự như dòng điện trong một hệ thống điện. Tuy nhiên, thay vì sự sụt áp khi các electron chảy qua một điện trở, đường thở có sự chênh lệch áp suất giữa hai điểm của luồng không khí, và sức cản đối với luồng khí chủ yếu được cung cấp bởi diện tích mặt cắt ngang hạn chế của chính các đường thở. Tốc độ của luồng không khí một phần phụ thuộc vào sự chênh lệch áp suất giữa hai điểm và một phần phụ thuộc vào sức cản của đường thở. Trong quá trình hít vào, áp lực phế nang là âm so với áp lực mũi hoặc miệng (là áp suất khí quyển), và không khí chảy vào trong. Ngược lại, trong quá trình thở ra, áp lực phế nang là dương so với áp lực mũi hoặc miệng, và không khí chảy ra ngoài từ các phế nang về phía mũi và miệng.
Sức cản đường thở
Luồng khí thực tế là một hiện tượng phức tạp hơn nhiều so với những gì chúng ta vừa mô tả. Ví dụ, hãy xem xét chi tiết hơn về vấn đề sức cản. Sức cản đường thở bình thường là khoảng 0.5 đến 2 cm H2O/L/s — nghĩa là, cần có sự chênh lệch áp suất từ 0.5 đến 2 cm H2O giữa mũi hoặc miệng và các phế nang để không khí chảy với tốc độ 1 L/s giữa hai điểm này. Đường thở nào cung cấp phần lớn sức cản? Mặc dù một đường thở nhỏ đơn lẻ cung cấp nhiều sức cản hơn cho luồng không khí so với một đường thở lớn hơn, nhưng điều đó không có nghĩa là tổng hợp các đường thở nhỏ hơn cung cấp phần lớn sức cản. Trên thực tế, điều ngược lại là đúng. Ví dụ, mặc dù khí quản lớn, nhưng chỉ có một khí quản, và tổng diện tích mặt cắt ngang của các đường thở ở cấp độ này là khá nhỏ. Ngược lại, ở cấp độ các đường thở nhỏ (ví dụ, <2 mm đường kính), số lượng khổng lồ của các đường thở này bù đắp cho đường kính nhỏ của mỗi đường thở và dẫn đến tổng diện tích mặt cắt ngang rất lớn.
Hình 4.4 cho thấy mức độ sức cản đối với luồng không khí được cung cấp bởi các đường thở ở các cấp độ khác nhau của cây khí-phế quản. Vị trí có sức cản lớn nhất (tổng diện tích mặt cắt ngang nhỏ nhất) là ở cấp độ các phế quản cỡ trung bình. Các đường thở nhỏ hoặc ngoại vi, thường được định nghĩa là các đường thở có đường kính dưới 2 mm, chỉ đóng góp khoảng 10% đến 20% tổng sức cản. Do đó, các đường thở này thường được gọi là “vùng im lặng” vì bệnh ở chúng có thể ảnh hưởng đến kích thước của chúng mà không làm thay đổi đáng kể tổng sức cản đường thở. Thật không may, mặc dù các nhà sinh lý học đã nỗ lực rất nhiều để phát triển các phương pháp có khả năng phát hiện sự gia tăng sức cản trong các đường thở nhỏ, nhưng tính hữu dụng của các xét nghiệm đó đã không đáp ứng được kỳ vọng ban đầu. Sự tương quan giữa các nghiên cứu chức năng này và xác nhận mô bệnh học của bệnh ở các đường thở nhỏ đã không nhất quán; do đó, các xét nghiệm này ít được sử dụng.
| Bởi vì sức cản đối với luồng không khí trong cây khí-phế quản phụ thuộc vào tổng diện tích mặt cắt ngang của các đường thở, các đường thở lớn và trung bình cung cấp sức cản lớn hơn so với các đường thở nhỏ có số lượng nhiều hơn. |
Gắng sức thở ra tối đa
Khía cạnh quan trọng tiếp theo của sinh lý luồng không khí là sự phân biệt giữa thở bình thường và các nỗ lực hô hấp gắng sức hoặc tối đa. Rất nhiều thông tin có thể thu được bằng cách xem xét luồng khí trong một lần thở ra gắng sức (tức là, thở ra từ tổng dung tích phổi xuống thể tích khí cặn càng mạnh và càng nhanh càng tốt). Trong một cuộc thảo luận về khái niệm này, sẽ hữu ích khi xem xét đường cong lưu lượng-thể tích đã được đề cập trong Chương 3 và được hiển thị lại trong Hình 4.5. Trong hình này, một loạt các đường cong thở ra cho thấy loại tốc độ dòng khí được tạo ra bởi các nỗ lực thở ra ngày càng lớn. Đường cong A cho thấy luồng khí thở ra với nỗ lực tương đối thấp, trong khi đường cong D cho thấy luồng khí với nỗ lực thở ra tối đa. Trong phần đầu của đường cong này, cho đến khi khoảng 30% dung tích sống đã được thở ra, tốc độ dòng khí khá phụ thuộc vào nỗ lực bỏ ra—nghĩa là, các nỗ lực thở ra lớn hơn gây ra sự gia tăng liên tục của tốc độ dòng khí thở ra, điều này là kết quả của việc tăng áp lực màng phổi và do đó tăng lực đẩy cho luồng không khí thở ra. Vùng này của dung tích sống trong quá trình thở ra gắng sức tối đa thường được gọi là phần phụ thuộc vào gắng sức.
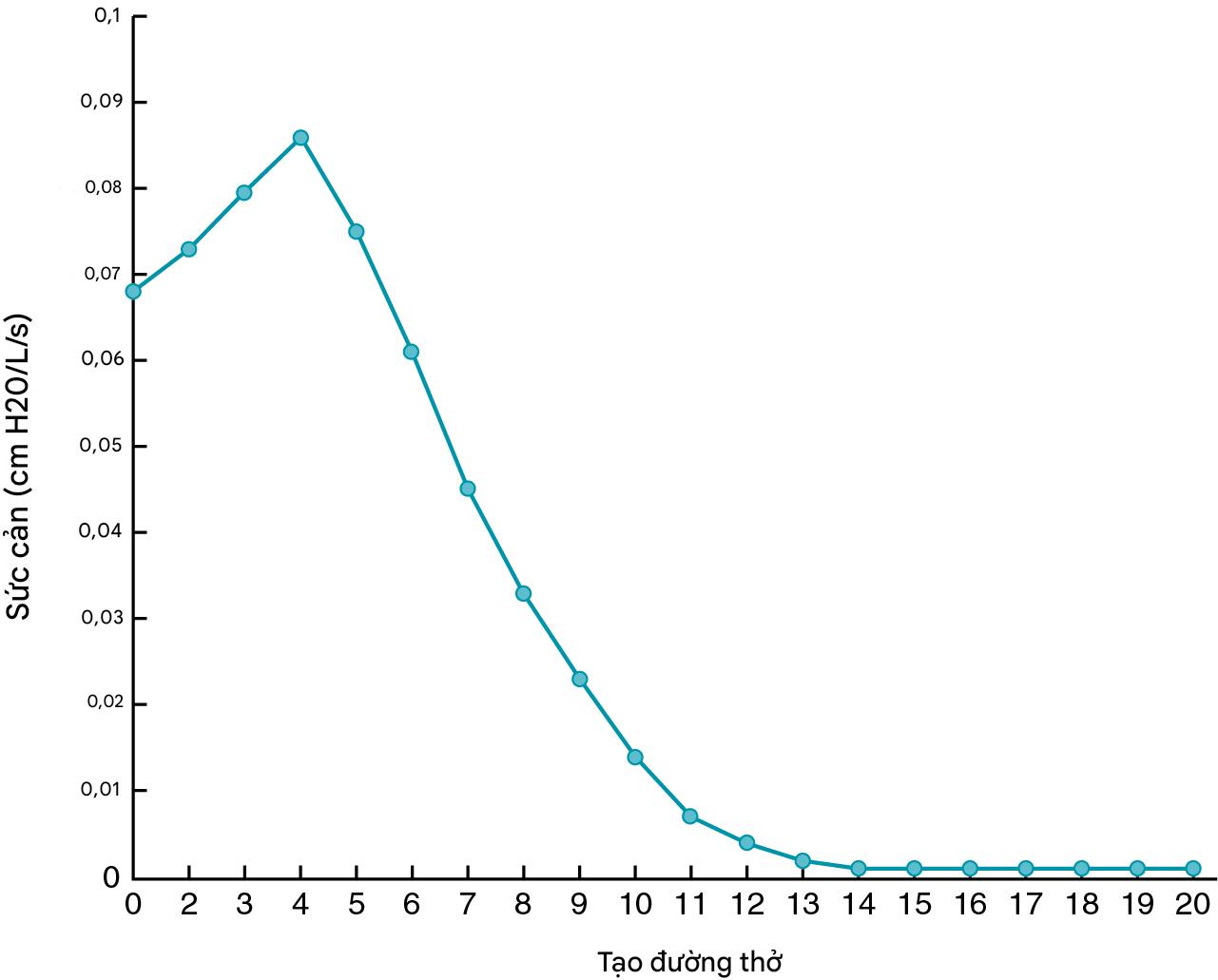
Hình 4.4 Sự đóng góp vào sức cản của các đường thở ở các cấp độ khác nhau của cây khí-phế quản. Sự đóng góp lớn nhất vào sức cản được cung cấp bởi các phế quản cỡ trung bình (thế hệ 3-5), trong khi các đường thở nhỏ hơn (khoảng thế hệ 9 trở đi) đóng góp ít hơn đáng kể vào tổng sức cản vì tổng diện tích mặt cắt ngang của chúng lớn hơn nhiều.
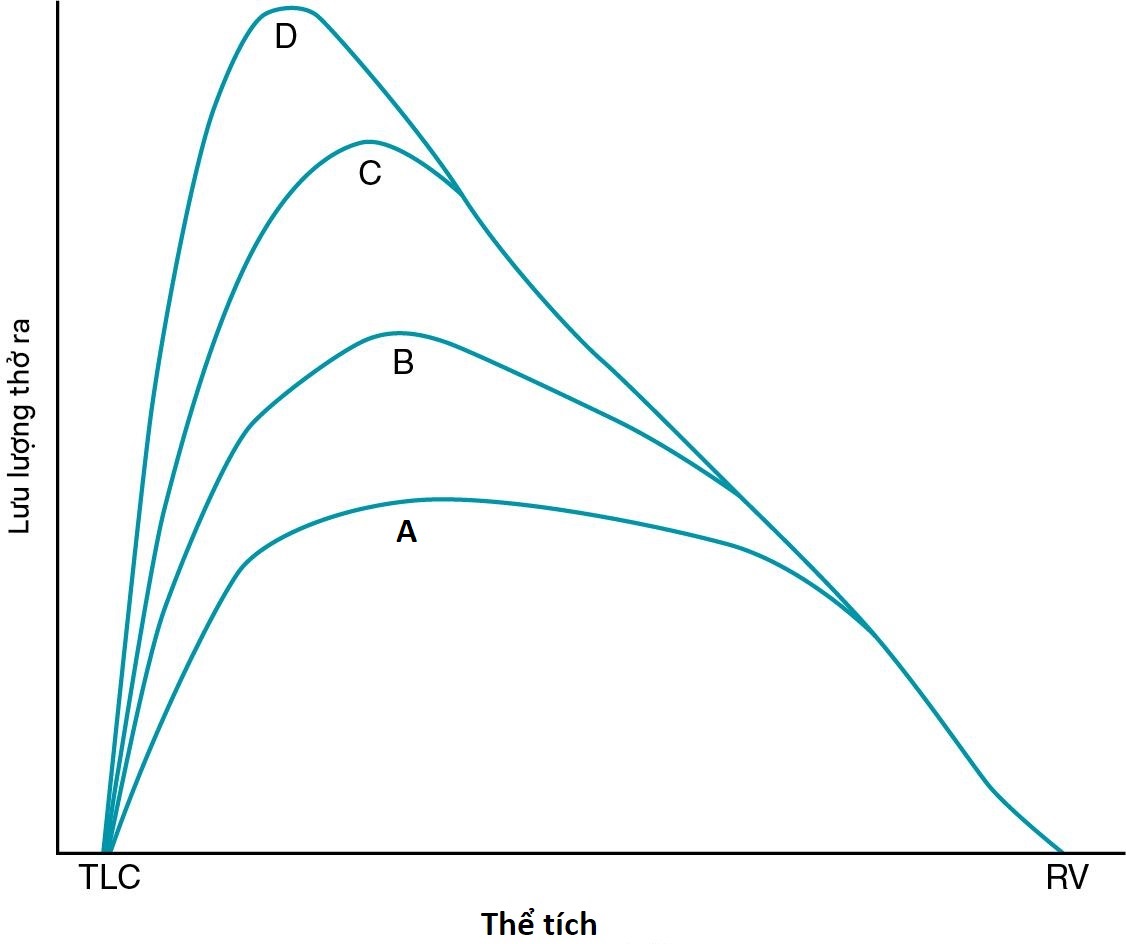
Hình 4.5 Các đường cong lưu lượng-thể tích thở ra với nỗ lực tăng dần. Đường cong A đại diện cho nỗ lực ít nhất; đường cong D đại diện cho nỗ lực thở ra tối đa. Trên phần dốc xuống của đường cong, vượt qua điểm mà khoảng 30% dung tích sống đã được thở ra, luồng khí bị giới hạn bởi các đặc tính cơ học của đường thở và phổi, không phải bởi nỗ lực của cơ. RV, thể tích khí cặn; TLC, tổng dung tích phổi.
Dưới 70% dung tích sống là điểm mà tại đó chúng ta không thể tăng tốc độ dòng khí bằng cách tăng nỗ lực. Một thứ gì đó khác ngoài sức mạnh cơ bắp của chúng ta (do đó, khác với áp lực màng phổi dương mà chúng ta có thể tạo ra) giới hạn luồng khí. Trên thực tế, yếu tố giới hạn là sự hẹp lại tới hạn của đường thở. Khi chúng ta cố gắng mạnh hơn, tất cả những gì chúng ta làm là nén đường thở thêm nữa mà không có bất kỳ sự gia tăng nào về tốc độ dòng khí. Phần này của đường cong lưu lượng-thể tích thường được gọi là phần không phụ thuộc vào gắng sức vì vượt qua một mức nỗ lực nhất định, nỗ lực hơn nữa không dẫn đến tốc độ dòng khí tăng thêm.
| Trong phần lớn quá trình thở ra gắng sức, luồng khí bị giới hạn bởi sự hẹp lại tới hạn của đường thở; nỗ lực hơn nữa không dẫn đến luồng khí tăng thêm. |
Hai câu hỏi chưa được trả lời về luồng khí thở ra tối đa vẫn còn. Thứ nhất, tại sao sự hẹp tới hạn của đường thở lại xảy ra đến mức nỗ lực ngày càng tăng tỏ ra vô ích trong việc tăng luồng khí? Thứ hai, sự hẹp tới hạn này xảy ra ở cấp độ nào trong đường thở? Câu trả lời cho những câu hỏi này, vốn được các nhà sinh lý học phổi rất quan tâm, phải được chắt lọc từ một lượng lớn lý thuyết và nghiên cứu.*
Trong một lần thở ra gắng sức, có một số yếu tố quyết định đường kính đường thở. Đầu tiên và rõ ràng nhất là kích thước vốn có của đường thở, phụ thuộc vào cấp độ của nó trong cây khí-phế quản và trương lực của cơ trơn đường thở. Trong bệnh tật, trương lực cơ trơn có thể tăng lên (như trong bệnh hen suyễn), hoặc các chất tiết trong đường thở có thể làm hẹp lòng ống (như trong bệnh hen suyễn hoặc viêm phế quản mạn tính). Thứ hai là khả năng xẹp của đường thở, ở các đường thở nhỏ, bị ảnh hưởng bởi mức độ lực kéo xuyên tâm do mô phổi xung quanh tác động lên thành đường thở. Khí quản và các phế quản lớn hơn được nâng đỡ bởi sụn, nhưng các đường thở nhỏ được bao quanh bởi một khung nâng đỡ gồm các thành phế nang liên tục “kéo” hoặc “giằng” mở các đường thở. Khi nhu mô phổi bị phá hủy, như trong bệnh khí phế thũng, các đường thở nhỏ mất đi một phần sự hỗ trợ bình thường này và có nhiều khả năng bị xẹp trong một lần thở ra gắng sức (xem Chương 6). Thứ ba là sự kết hợp của các áp lực bên ngoài và bên trong tác động lên các đường thở nhỏ. Sự cân bằng áp lực này là rất quan trọng trong việc xác định xem một đường thở cụ thể có còn mở hay đóng trong một lần thở ra gắng sức.
| Đường kính đường thở phụ thuộc vào cấp độ của đường thở trong cây khí-phế quản, trương lực cơ trơn đường thở, lực kéo xuyên tâm lên đường thở từ mô phổi xung quanh, và các áp lực bên trong và bên ngoài lên đường thở. |
Áp lực bên ngoài tác động lên một đường thở được xác định bởi áp lực màng phổi (Hình 4.6). Khi áp lực màng phổi dương mạnh, như khi thở ra gắng sức, đường thở bị nén lại. Chỉ nhờ có một áp lực đối kháng bên trong đường thở mà chúng vẫn mở khi đối mặt với một áp lực bên ngoài dương mạnh. Hai yếu tố góp phần vào áp lực bên trong đường thở: (1) lực đàn hồi của phổi và (2) áp lực màng phổi truyền đến các phế nang và đường thở.
Hình 4.6 cho thấy thành phế nang giống như một quả bóng bay bị kéo căng đang cố gắng đẩy không khí ra ngoài. Giống như cách một quả bóng bay, khi cố gắng xẹp lại, tạo áp lực lên không khí bên trong, thành phế nang có lực đàn hồi tác động áp lực lên khí bên trong. Áp lực này dẫn đến luồng khí từ các phế nang qua các đường thở. Tuy nhiên, hãy nhớ rằng luồng khí qua một đường thở đi kèm với sự sụt giảm áp suất dọc theo đường thở. Tại một điểm nhất định dọc theo đường thở, áp suất giảm đủ để áp suất bên trong đường thở trở nên bằng với áp suất bên ngoài đường thở (tức là áp lực màng phổi). Điểm mà áp suất bên trong đường thở bằng với áp suất bên ngoài đường thở được gọi là điểm áp lực bằng nhau. Nỗ lực tăng lên gây ra tăng áp lực màng phổi, được tác động cả lên phế nang và lên thành đường thở. Do đó, áp lực tăng lên trên các phế nang (sẽ làm tăng luồng khí) được cân bằng bởi áp lực bên ngoài tăng lên trên đường thở. Do đó, áp lực đẩy (tức là, sự khác biệt giữa áp lực phế nang và áp lực tại điểm áp lực bằng nhau) chỉ được quyết định bởi áp lực đàn hồi của phổi. Với nỗ lực thêm, áp lực đẩy phế nang tăng lên được cân bằng chính xác bởi áp lực bên ngoài tăng lên trên đường thở, điều này thúc đẩy sự xẹp đường thở (xem Hình 4.6). Kết quả cuối cùng là, áp lực đàn hồi, chứ không phải áp lực màng phổi được tạo ra bởi một nỗ lực thở ra tối đa, là yếu tố quyết định quan trọng của luồng khí thở ra tối đa, ít nhất là trong phần không phụ thuộc vào gắng sức hoặc phần sau của một lần thở ra gắng sức. Các chương sau sẽ cho thấy rằng trong các bệnh có lực đàn hồi bị thay đổi, tốc độ luồng khí thở ra tối đa bị ảnh hưởng bởi sự thay đổi này trong áp lực đẩy hiệu dụng cho luồng không khí.
| Tại điểm áp lực bằng nhau, áp lực bên trong và bên ngoài trên đường thở là bằng nhau. Áp lực đẩy thực từ phế nang đến điểm áp lực bằng nhau là áp lực đàn hồi của phổi. |
Câu hỏi cuối cùng cần được giải quyết ở đây là cấp độ mà sự hẹp tới hạn này (tức là điểm áp lực bằng nhau) xảy ra. Câu trả lời phụ thuộc vào thể tích phổi. Điểm áp lực bằng nhau không ở một vị trí không đổi khi một cá nhân thở ra đến thể tích khí cặn. Ở các thể tích phổi cao hơn, áp lực đàn hồi lớn hơn (các phế nang bị kéo căng hơn), và một khoảng cách dài hơn ngăn cách các phế nang với điểm áp lực bằng nhau. Ở các thể tích phổi trên dung tích cặn chức năng, điểm hẹp tới hạn này nằm trong các đường thở tương đối lớn, các phế quản phân thùy hoặc lớn hơn. Ở các thể tích phổi thấp hơn, áp lực đàn hồi thấp hơn, khoảng cách từ phế nang đến điểm áp lực bằng nhau nhỏ hơn, và sự hẹp tới hạn xảy ra ở các đường thở nhỏ hơn, ngoại vi hơn. Bởi vì luồng khí tối đa phụ thuộc vào lực đàn hồi và sức cản của các đường thở ở phía ngoại vi (“thượng nguồn”) so với điểm áp lực bằng nhau, sức cản của các đường thở nhỏ là một thành phần lớn hơn của sức cản thượng nguồn ở các thể tích phổi nhỏ và do đó là một yếu tố quyết định lớn hơn của luồng khí thở ra tối đa ở các thể tích thấp hơn dọc theo đường cong lưu lượng-thể tích.
| Điểm áp lực bằng nhau di chuyển về phía ngoại vi (hướng tới các đường thở nhỏ hơn) khi thể tích phổi giảm trong quá trình thở ra gắng sức; do đó, sức cản của các đường thở nhỏ giới hạn luồng khí thở ra tối đa nhiều hơn ở thể tích phổi thấp so với thể tích phổi cao. |
Tóm lại, luồng khí qua cây khí-phế quản phản ánh sự kết hợp của các yếu tố: kích thước đường thở, sự nâng đỡ hoặc lực kéo xuyên tâm do nhu mô phổi xung quanh tác động, và áp lực đẩy được cung cấp bởi lực đàn hồi của phổi. Mặc dù áp lực màng phổi góp phần vào áp lực đẩy cho luồng không khí, nó cũng tác động một áp lực bên ngoài đối trọng lên đường thở, thúc đẩy sự xẹp đường thở. Thảo luận sau này về các rối loạn cụ thể sẽ cho thấy các yếu tố khác nhau này liên quan với nhau như thế nào như là các yếu tố quyết định luồng khí thở ra tối đa và chúng có thể bị thay đổi như thế nào trong các tình trạng bệnh lý.
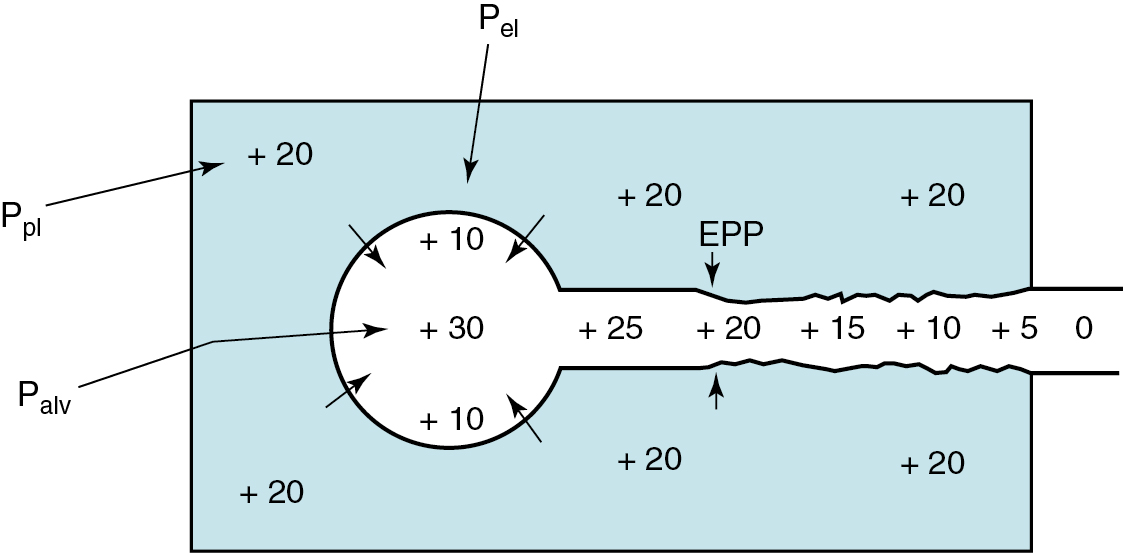
Hình 4.6 Sơ đồ khái niệm điểm áp lực bằng nhau trong một lần thở ra gắng sức (tối đa). Phế nang và đường thở của nó được hiển thị bên trong hộp, đại diện cho khoang màng phổi. Áp lực phế nang (Palv) có hai thành phần góp phần: áp lực màng phổi (Ppl) và áp lực đàn hồi của phổi (Pel). Trong sơ đồ này, Ppl=20 cm H2O và Pel=10 cm H2O, do đó Palv là tổng của Ppl và Pel, là 30 cm H2O.
* Thảo luận này sử dụng một mô hình dựa trên khái niệm điểm áp lực bằng nhau. Một mô hình khác dựa trên lý thuyết tốc độ sóng có lẽ cung cấp một khuôn khổ khái niệm chính xác hơn cho giới hạn luồng khí thở ra, nhưng nó phức tạp hơn nhiều và nằm ngoài phạm vi của cuộc thảo luận này.
TÀI LIỆU THAM KHẢO ĐỀ XUẤT
- Albertine K.H.: Anatomy of the lungs.Broaddus V.C.Mason R.J.Ernst J.D. et. al.Murray and Nadel’s textbook of respiratory medicine.2016.ElsevierPhiladelphia:pp. 3-21.
- Barnes P.J.: Neurogenic inflammation in the airways. Respiration Physiology 2001; 125: pp. 145-154.
- Fahy J.V., Dickey B.F.: Airway mucus function and dysfunction. New England Journal of Medicine 2010; 363: pp. 2233-2247.
- Gohy S.T., Hupin C., Pilette C., Ladjemi M.Z.: Chronic inflammatory airway diseases: The central role of the epithelium revisited. Clinical and Experimental Allergy 2016; 46: pp. 529-542.
- Kajstura J., Rota M., Hall S.R., Hosoda T., D’Amario D., Sanada F., et. al.: Evidence for human lung stem cells. New England Journal of Medicine 2011; 364: pp. 1795-1806.
- Leslie K.O., Wick M.R.: Lung anatomy.Leslie K.O.Wick M.R.Practical pulmonary pathology: A diagnostic approach.2018.ElsevierPhiladelphia:pp. 1-13.
- Ma J., Rubin B.K., Voynow J.A.: Mucins, mucus, and goblet cells. Chest 2017; 154: pp. 169-176.
- Mazzone S.B., Canning B.J.: Autonomic neural control of the airways. Handbook of Clinical Neurology 2013; 117: pp. 215-228.
- Mazzone S.B., Undem B.J.: Vagal afferent innervation of the airways in health and disease. Physiological Reviews 2016; 96: pp. 975-1024.
- Mehran R.J.: Fundamental and practical aspects of airway anatomy: From glottis to segmental bronchus. Thoracic Surgery Clinics 2018; 28: pp. 117-125.
- Parker D., Prince A.: Innate immunity in the respiratory epithelium. American Journal of Respiratory Cell and Molecular Biology 2011; 45: pp. 189-201.
- Pincus A.B., Fryer A.D., Jacoby D.B.: Mini review: Neural mechanisms underlying airway hyperresponsiveness. Neuroscience Letters 2021; 751: pp. 135795.
- Proskocil B.J., Fryer A.D.2-Agonist and anticholinergic drugs in the treatment of lung disease. Proceedings of the American Thoracic Society 2005; 2: pp. 305-310.
- Schwartzstein R.M., Parker M.J.: 2006.Lippincott Williams & WilkinsPhiladelphia
- Tam A., Wadsworth S., Dorscheid D., Man S.F., Sin D.D.: The airway epithelium: More than just a structural barrier. Therapeutic Advances in Respiratory Disease 2011; 5: pp. 255-273.
- Voynow J.A., Rubin B.K.: Mucins, mucus, and sputum. Chest 2009; 135: pp. 505-512.
- West J.B., Luks A.M.: 11th ed.2021.Wolters KluwerPhiladelphia
- Widdicombe J.G.: Autonomic regulation. i-NANC/e-NANC. American Journal of Respiratory and Critical Care Medicine 1998; 158: pp. S171-S175.
- Widdicombe J.H., Wine J.J.: Airway gland structure and function. Physiological Reviews 2015; 95: pp. 1241-1319






