[Sách dịch] Sổ tay Bệnh Gan – Handbook of Liver Disease – (C) NXB Elsevier, 2022
Dịch và chú giải: Ths.Bs. Lê Đình Sáng
CHƯƠNG 16: VIÊM ĐƯỜNG MẬT TIÊN PHÁT
Primary Biliary Cholangitis
Gwilym J. Webb BM BCh, MA, MRCP and Gideon M. Hirschfield MB BChir, PhD, FRCP
Handbook of Liver Disease, Chapter 16, 217-232
NHỮNG ĐIỂM CHÍNH
|
Thay đổi danh pháp
Các tuyên bố đồng thuận dựa trên phản hồi của bệnh nhân đã hỗ trợ việc thay đổi tên từ xơ gan ứ mật tiên phát (primary biliary cirrhosis) thành viêm đường mật tiên phát (primary biliary cholangitis). Cuối cùng, một tỷ lệ cao bệnh nhân vẫn tiến triển đến xơ gan và cần được theo dõi tầm soát ung thư biểu mô tế bào gan (hepatocellular carcinoma – HCC).
Dịch tễ học
- PBC là một bệnh chiếm ưu thế ở nữ (90% đến 95%) được ghi nhận ở tất cả các dân tộc. Bệnh dường như ít gặp hơn ở người Mỹ gốc Phi nhưng được báo cáo là thường xuyên hơn ở một số quần thể như các bộ lạc bản địa Canada (Canadian First Nations).
- Ước tính cứ 1000 phụ nữ trên 40 tuổi thì có 1 người mắc PBC. Một phân tích tổng hợp đã cho thấy tỷ lệ mắc mới từ 0,33 đến 5,8 trên 100.000 người/năm và tỷ lệ hiện mắc từ 1,91 đến 40,2 trên 100.000 người, với tỷ lệ hiện mắc ngày càng tăng theo thời gian.
- Tuổi khởi phát dao động từ 30 đến 70 tuổi, và chẩn đoán PBC ngày càng được thực hiện khi sàng lọc hoặc khảo sát các bệnh lý khác phát hiện các chỉ số xét nghiệm sinh hóa gan bất thường. Mặc dù phản ứng AMA ở trẻ em đã được ghi nhận, chẩn đoán PBC trước tuổi dậy thì chưa được báo cáo. Tuổi khởi phát trẻ hơn (<50) thường liên quan đến bệnh tiến triển nhanh hơn và không đáp ứng với UDCA.
- Tỷ lệ ghép gan cho PBC đã giảm nhờ việc sử dụng rộng rãi UDCA, nhưng một số bệnh nhân, thường là những người khởi phát ở tuổi trẻ hơn, vẫn tiếp tục tiến triển đến mất bù.
Di truyền học
- Các yếu tố di truyền đóng một vai trò trong PBC, mặc dù rối loạn này không chỉ là hậu quả của một đột biến gen duy nhất.
- Khoảng 1 trong 20 bệnh nhân có một thành viên trong gia đình bị ảnh hưởng bởi PBC. Bệnh nhân và các thành viên gia đình của họ có nhiều khả năng mắc các bệnh tự miễn khác, đặc biệt là bệnh celiac và xơ cứng bì.
- Sự thiếu tương hợp hoàn toàn đối với PBC ở các cặp song sinh cùng trứng cho thấy các yếu tố môi trường cũng quan trọng; các yếu tố hợp lý được đề xuất bao gồm phơi nhiễm với xenobiotic và sự bắt chước phân tử từ nhiễm trùng. Hút thuốc là một yếu tố nguy cơ quan trọng đối với mức độ nặng và sự tiến triển của bệnh.
- Mối liên quan với các biến thể trong locus HLA lớp II đã được xác định nhưng chưa được hiểu rõ về mặt cơ chế.
- Các xét nghiệm liên kết toàn bộ bộ gen (genome-wide association testing) và các nghiên cứu lặp lại đã xác định các biến thể trong các gen quan trọng trong con đường Th1/interleukin-12 (IL12A, IL12RB2, IRF5, NFKB1, TYK2, STAT4) là đặc biệt liên quan đến sinh bệnh học của PBC. Các biến thể trong các gen khác liên quan đến hoạt hóa tế bào T, phát triển tế bào B và T, định vị tế bào B, và trình diện kháng nguyên cũng được báo cáo.
- Nhiều mối liên kết di truyền của PBC – bao gồm các kháng nguyên HLA – được chia sẻ với các bệnh tự miễn khác (ví dụ: đa xơ cứng, viêm loét đại tràng, viêm khớp dạng thấp, đái tháo đường typ 1, bệnh celiac).
- Các đề xuất cho rằng những thay đổi trong chức năng và số lượng nhiễm sắc thể X ảnh hưởng đến tính nhạy cảm với bệnh chưa được hỗ trợ bởi các nghiên cứu toàn bộ bộ gen; tuy nhiên, sự khác biệt về mức độ nặng của bệnh giữa nam và nữ đã được báo cáo.
Miễn dịch học
Các nghiên cứu di truyền về PBC ủng hộ quan điểm rằng các bất thường miễn dịch là nền tảng của căn bệnh tự miễn điển hình này. Các thay đổi miễn dịch được xác định ở bệnh nhân PBC bao gồm:
- Kháng thể kháng ty thể (AMA)
a. Được phát hiện ở 95% bệnh nhân PBC.
b. Không ảnh hưởng đến diễn tiến hoặc đáp ứng điều trị của PBC.
c. Có thể thấy trong các bệnh gan khác, bao gồm suy gan cấp, tổn thương do thuốc, và viêm gan tự miễn.
d. Tồn tại dai dẳng sau ghép gan.
e. Là một họ các kháng thể phản ứng với các kháng nguyên khác nhau bên trong ty thể.- AMA PDH-E2
- Tự kháng thể chính được tìm thấy trong PBC.
- Chủ yếu chống lại thành phần dihydrolipoamide acyltransferase (E2) của các phức hợp ketoacid dehydrogenase trên màng trong ty thể.
- Pyruvate dehydrogenase là phức hợp enzyme được biết đến nhiều nhất trong số này.
- Anti-M4, anti-M8, và anti-M9
- Các AMA khác được mô tả trong PBC nhưng không được coi là có liên quan đến chăm sóc lâm sàng.
- Sự tồn tại của chúng không được xác nhận trong một nghiên cứu sử dụng các protein ty thể người được nhân bản vô tính có độ tinh khiết cao làm kháng nguyên.
- AMA PDH-E2
f. Ý nghĩa
-
- Mối quan hệ giữa AMA và tổn thương ống mật qua trung gian miễn dịch vẫn chưa rõ ràng.
- AMA thường có trước khi bệnh biểu hiện lâm sàng.
- Các thay đổi sinh hóa đối với phức hợp pyruvate dehydrogenase trong quá trình apoptosis của tế bào biểu mô đường mật dường như quan trọng trong việc giải thích sự liên quan của AMA trong PBC.
- Pyruvate dehydrogenase và các kháng nguyên ty thể khác được biểu hiện bất thường trên bề mặt lòng ống của các tế bào biểu mô đường mật từ bệnh nhân PBC nhưng không có ở các đối tượng đối chứng hoặc bệnh nhân viêm đường mật xơ hóa tiên phát.
- Pyruvate dehydrogenase E2 được biểu hiện trong các tế bào biểu mô ống mật trước khi xảy ra độc tế bào T-lymphocyte.
- Các kháng nguyên ty thể không đặc hiệu cho mô.
- Không có sự tương quan nào giữa sự hiện diện hoặc hiệu giá của AMA và mức độ nặng của diễn tiến PBC; hiệu giá kháng thể có thể giảm khi điều trị.
- Hiệu giá cao của AMA có thể được gây ra ở động vật thí nghiệm bằng cách tiêm chủng với pyruvate dehydrogenase tinh khiết của người, nhưng những động vật này không phát triển bệnh gan; việc gây ra viêm đường mật tự miễn với AMA sau khi tiêm chủng xenobiotic hóa học (axit 2-octynoic) hoặc nhiễm Escherichia coli ở những con chuột dễ bị tự miễn đã được báo cáo.
- Thao tác di truyền trên chuột (ví dụ, chuột NOD.c3c4 đồng gen hoặc nhiều khuyết tật khác nhau ảnh hưởng đến con đường T-điều hòa bao gồm thiếu hụt FOXP3; rối loạn chức năng thụ thể IL2 alpha; biểu hiện của thụ thể yếu tố tăng trưởng biến đổi [TGF] β dạng trội âm trên tế bào T CD4+; knockout chất trao đổi anion 2) dẫn đến sản xuất AMA và bệnh đường mật tự miễn với một số đặc điểm gợi nhớ đến PBC.
- Các tự kháng thể lưu hành khác
a. Kháng thể kháng nhân (Antinuclear antibodies – ANA)
* Kiểu hình huỳnh quang miễn dịch rất đặc hiệu cho PBC, do đó sự hiện diện của ANA dạng chấm nhân đa dạng (sp100) hoặc ANA dạng viền màng (gp210) có thể có giá trị chẩn đoán ở những bệnh nhân âm tính với AMA.
b. Kháng thể kháng tâm động (Anticentromere antibodies)
* Các nghiên cứu cho thấy những bệnh nhân dương tính với gp210 có xu hướng có diễn tiến bệnh nặng hơn với suy gan, trong khi những bệnh nhân dương tính với kháng thể kháng tâm động có xu hướng có kiểu hình tăng áp lực tĩnh mạch cửa. - Immunoglobulin huyết thanh
a. Nồng độ immunoglobulin M (IgM) huyết thanh tăng, có tính phản ứng miễn dịch và dễ kết tủa lạnh cao.
b. Có thể có kết quả dương tính giả với các xét nghiệm phát hiện phức hợp miễn dịch. - Liên quan với các bệnh tự miễn khác
a. Xơ cứng bì
b. Hội chứng Sjögren
c. Bệnh celiac
d. Viêm tuyến giáp hoặc suy giáp
e. Viêm khớp dạng thấp hoặc lupus ban đỏ hệ thống - Bất thường về miễn dịch tế bào
a. Giảm chức năng và số lượng tế bào T-điều hòa đã được báo cáo.
b. Giảm số lượng tế bào T-lymphocyte lưu hành nhưng tăng số lượng tế bào T hỗ trợ nang lympho.
c. Tăng tế bào Th17 trong gan.
d. Tích tụ các tế bào T-lymphocyte trong các khoảng cửa của gan.
Sinh bệnh học
- Viêm đường mật u hạt không sinh mủ mạn tính là một mô tả chính xác hơn về bệnh so với PBC, với ít nhất hai quá trình liên quan dẫn đến tổn thương gan (Hình 16.1).
- Quá trình đầu tiên là sự phá hủy mạn tính, thường là dạng u hạt, của các ống mật nhỏ, có lẽ do các tế bào lympho hoạt hóa qua trung gian. Tổn thương ống mật phá hủy ban đầu trong PBC là do các tế bào T-lymphocyte gây độc tế bào. Viêm gan vùng chuyển tiếp có thể hiện diện (5% đến 10%), nhưng liệu đây chỉ là một khía cạnh của PBC hay là viêm gan tự miễn cùng tồn tại vẫn còn gây tranh cãi. Tuy nhiên, rõ ràng là những bệnh nhân trẻ hơn, không đáp ứng với UDCA có thể có biểu hiện bệnh nặng hơn về gan, mặc dù thường không đáp ứng với glucocorticoid.
- Tế bào ống mật ở bệnh nhân PBC biểu hiện tăng lượng kháng nguyên HLA lớp I (HLA-A, HLA-B, HLA-C) và lớp II (HLA-DR).
- Tổn thương ống mật giống với các rối loạn qua trung gian tế bào T-lymphocyte gây độc tế bào, chẳng hạn như bệnh mảnh ghép chống chủ và thải ghép gan đồng loại.
- Quá trình thứ hai bao gồm tổn thương hóa học đối với các tế bào gan ở những vùng gan có dòng chảy mật bị cản trở do sự phá hủy các ống mật nhỏ.
- Xảy ra sự ứ đọng axit mật, bilirubin, đồng và các chất khác thường được bài tiết vào mật; sự hấp thu lipid và các chất hòa tan trong lipid cũng bị suy giảm.
- Nồng độ tăng của một số chất này, chẳng hạn như axit mật, có thể làm tổn thương thêm các tế bào gan.
- Hậu quả của sự phá hủy ống mật bao gồm viêm và sẹo ở khoảng cửa, tiến triển đến xơ gan và cuối cùng là suy gan.
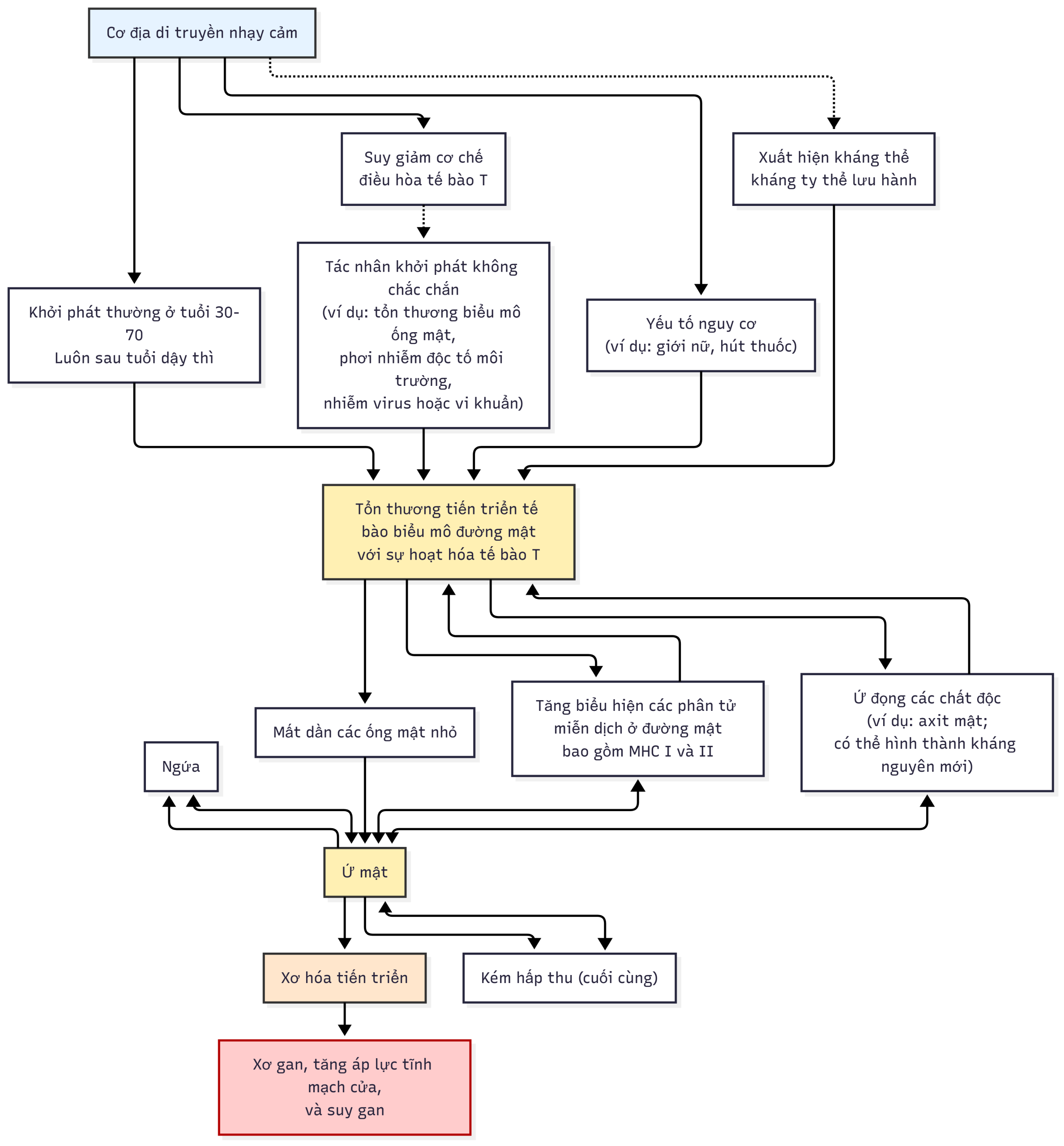
Hình 16.1 Trình tự các sự kiện trong sinh bệnh học có thể có của viêm đường mật tiên phát (PBC). Nguyên nhân của PBC vẫn chưa được biết, mặc dù các yếu tố di truyền và miễn dịch dường như đóng một vai trò. MHC, Phức hợp tương hợp mô chính.*
Giải phẫu bệnh học
TỔN THƯƠNG ĐẠI THỂ
- Gan ban đầu to ra nhưng bề mặt nhẵn.
- Khi bệnh tiến triển, gan to hơn nữa, trở nên nốt và có hình ảnh xơ gan đại thể với sự nhiễm mật. Cuối cùng, kích thước gan có thể giảm trong giai đoạn cuối của bệnh.
- Tần suất sỏi mật tăng được ghi nhận (khoảng 40% bệnh nhân).
- Tần suất tăng sản nốt tái tạo (nodular regenerative hyperplasia – NRH) tăng được quan sát thấy trong giai đoạn đầu của PBC. Mặc dù giãn tĩnh mạch thực quản và tăng áp lực tĩnh mạch cửa thường phản ánh xơ gan, tăng áp lực tĩnh mạch cửa trước xoang có thể phát triển do NRH ở những bệnh nhân PBC chưa bị xơ gan.
- Các hạch bạch huyết to do tăng sản phản ứng lành tính có thể được thấy ở rốn gan và xung quanh động mạch chủ và tĩnh mạch chủ dưới; phát hiện này cần được phân biệt với u lympho.
TỔN THƯƠNG MÔ HỌC
- Bốn giai đoạn mô học của PBC được công nhận.
- Phân giai đoạn mô học đã bị thay thế bởi đáp ứng sinh hóa với điều trị như một công cụ tiên lượng, do đó làm giảm nhu cầu sinh thiết gan, và vì vậy không được khuyến nghị trong thực hành lâm sàng. Các dấu ấn không xâm lấn của xơ hóa, đặc biệt là đo độ đàn hồi gan bằng siêu âm, đang ngày càng được sử dụng.
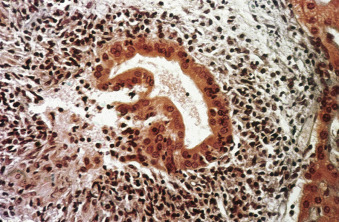
Hình 16.2 Mô bệnh học tổn thương ống mật điển hình giai đoạn I của viêm đường mật tiên phát. Lớp tế bào biểu mô lót một ống mật nhỏ bị thâm nhiễm bởi các tế bào lympho (nhuộm hematoxylin và eosin [H&E]).
- Những cân nhắc khi diễn giải phân giai đoạn sinh thiết gan
a. Sự liên quan của bệnh có thể không đồng nhất và có thể bị ảnh hưởng bởi sự thay đổi do lấy mẫu.
b. Một vài giai đoạn có thể được thấy trên cùng một mẫu sinh thiết; theo quy ước, phân giai đoạn dựa trên tổn thương tiến triển nhất được thấy trên mẫu sinh thiết.
c. Vì PBC ngày càng được chẩn đoán ở giai đoạn sớm, nên hiện nay ít có khả năng tìm thấy các phát hiện bệnh học đặc trưng trên các mẫu sinh thiết kim hơn so với trước đây. - Các giai đoạn mô học tiêu chuẩn
a. Giai đoạn I
* Các ống mật bị tổn thương thường được bao quanh bởi một đám thâm nhiễm dày đặc các tế bào đơn nhân, hầu hết là tế bào lympho (Hình 16.2).
* Những tổn thương phá hủy không đối xứng, điển hình của các ống mật gian tiểu thùy này nằm rải rác không đều khắp các khoảng cửa và thường chỉ được thấy trên các mẫu sinh thiết phẫu thuật lớn của gan, nơi có sự hiện diện đầy đủ của các ống mật nhỏ.
* Viêm chỉ giới hạn trong các khoảng cửa.
b. Giai đoạn II
* Tổn thương lan rộng hơn nhưng ít đặc hiệu hơn.
* Có thể thấy rõ sự giảm số lượng các ống mật bình thường trong các khoảng cửa và tăng số lượng các ống mật không điển hình, hình thành kém với lòng ống có hình dạng không đều (Hình 16.3).
* Xơ hóa khoảng cửa lan tỏa và thâm nhiễm tế bào đơn nhân được thấy trong các khoảng cửa. Viêm có thể lan vào các khu vực quanh khoảng cửa xung quanh.
* Số lượng ống mật giảm trong một mẫu sinh thiết kim gan không có gì đặc biệt khác nên cảnh báo về khả năng mắc PBC.
c. Giai đoạn III
* Tương tự như giai đoạn II, ngoại trừ các vách xơ kéo dài ra ngoài các khoảng cửa và hình thành các cầu nối từ khoảng cửa đến khoảng cửa (Hình 16.4).
d. Giai đoạn IV
* Đại diện cho giai đoạn cuối của tổn thương, với xơ gan rõ và các nốt tái tạo (Hình 16.5).
* Các phát hiện có thể không thể phân biệt được với các loại xơ gan khác; tuy nhiên, sự khan hiếm các ống mật bình thường trong các khu vực sẹo gợi ý khả năng mắc PBC. - Các hệ thống tính điểm bệnh học mới hơn đánh giá mức độ xơ hóa (xơ hóa khoảng cửa/quanh khoảng cửa/ít vách ngăn/nhiều vách ngăn/xơ gan); các mức độ viêm gan vùng chuyển tiếp tế bào lympho và giảm ống mật (tỷ lệ ống mật—tức là, tỷ lệ giữa số lượng khoảng cửa có ống mật so với tổng số khoảng cửa); hoặc giai đoạn PBC (xơ hóa, mất ống mật, và sự lắng đọng protein gắn đồng) và mức độ hoạt động hoại tử-viêm (viêm đường mật và viêm gan).
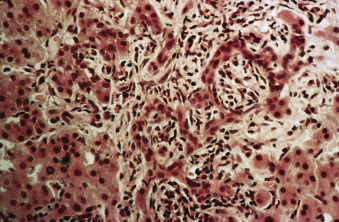
Hình 16.3 Mô bệnh học giai đoạn II của viêm đường mật tiên phát. Tăng sản ống mật không điển hình được thấy. Các ống mật ngoằn ngoèo có thể nhìn thấy, với thâm nhiễm tế bào viêm bao gồm chủ yếu là tế bào lympho và một vài bạch cầu trung tính (nhuộm H&E).
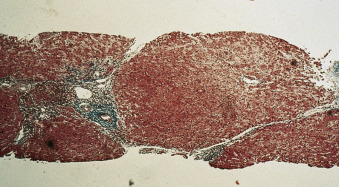
Hình 16.4 Mô bệnh học giai đoạn III của viêm đường mật tiên phát. Một vách xơ từ khoảng cửa đến khoảng cửa được thể hiện trên hình ảnh độ phóng đại thấp này (nhuộm Masson trichrome).
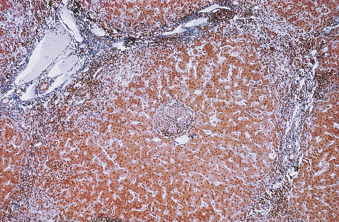
Hình 16.5 Mô bệnh học giai đoạn IV của viêm đường mật tiên phát. Một u hạt không hoại tử bã đậu có thể nhìn thấy ở trung tâm của một nốt. Các khoảng cửa được nối với nhau bằng các dải mô liên kết và tế bào viêm (nhuộm Masson trichrome).
Đặc điểm lâm sàng
TRIỆU CHỨNG
Khoảng hai phần ba bệnh nhân không có triệu chứng tại thời điểm chẩn đoán ban đầu. Các triệu chứng và dấu hiệu của PBC một phần phản ánh tình trạng ứ mật.
- Mệt mỏi
- Triệu chứng phổ biến nhất, nhưng được báo cáo khác nhau tùy thuộc vào phương pháp xác định.
- Không đặc hiệu cho PBC; thấy trong các bệnh gan và không do gan khác.
- Cần xem xét các giải thích khác, chẳng hạn như trầm cảm, thiếu máu, ngưng thở khi ngủ, suy giáp, thiếu sắt và suy thượng thận.
- Ngứa
- Sinh bệnh học chưa rõ; ngứa không chỉ do sự ứ đọng của các axit mật chính và phụ tự nhiên mà có khả năng do một chất khác thường được bài tiết vào mật gây ra.
- Tăng trương lực hệ opioid liên quan đến ứ mật mạn tính đã được đề xuất là một yếu tố căn nguyên tiềm năng.
- Hoạt động autotaxin huyết thanh và nồng độ lysophosphatidic đã được chứng minh có tương quan với cường độ ngứa và có thể là mục tiêu điều trị tiềm năng.
- Đặc trưng là ngứa nặng hơn vào giờ đi ngủ.
- Ban đầu có thể phát triển trong ba tháng cuối của thai kỳ và kéo dài sau khi sinh.
- Nghịch lý là, ngứa thường cải thiện khi bệnh tiến triển.
- UDCA không phải là một phương pháp điều trị ngứa và có thể làm ngứa trầm trọng hơn. Các chất chủ vận thụ thể Farnesoid X như axit obeticholic cũng có thể làm ngứa trầm trọng hơn; việc điều chỉnh liều và điều trị triệu chứng ngứa đồng thời đã được chứng minh là có hiệu quả trong việc cải thiện ngứa ở những bệnh nhân dùng axit obeticholic.
- Loãng xương
- Bệnh xương giảm mật độ (osteopenic) xảy ra ở ít nhất 25% bệnh nhân PBC; sinh bệnh học vẫn chưa rõ ràng nhưng dường như phản ánh sự giảm chu chuyển xương cũng như mức độ nặng của bệnh gan.
- Nhuyễn xương (osteomalacia) không phổ biến.
- Các triệu chứng lâm sàng của loãng xương không thường gặp, nhưng khi có, chúng liên quan đến gãy xương tự phát hoặc do va chạm nhẹ.
- Kém hấp thu
- Hiện là một biểu hiện lâm sàng không phổ biến; trước đây nó được ghi nhận ở những bệnh nhân bị ứ mật kéo dài.
- Sự suy giảm bài tiết mật dẫn đến giảm nồng độ axit mật trong lòng ruột; nồng độ axit mật có thể giảm xuống dưới nồng độ micelle tới hạn và không đủ để tiêu hóa và hấp thu hoàn toàn các triglyceride trung tính trong chế độ ăn.
- Bệnh nhân có thể bị tiêu chảy về đêm, phân có mùi hôi, khối lượng lớn, hoặc sụt cân mặc dù ăn ngon miệng và tăng lượng calo nạp vào.
- Có thể có tình trạng kém hấp thu các vitamin tan trong chất béo A, D, E, K và canxi; quáng gà là một triệu chứng đặc biệt quan trọng của thiếu vitamin A.
- Suy tụy cũng có thể góp phần vào tình trạng kém hấp thu; điều này rất có thể xảy ra ở những bệnh nhân có hội chứng sicca đồng thời.
- Phức hợp Sicca
- Sự kết hợp giữa khô mắt, khô miệng và khô âm đạo này là một phàn nàn thường gặp ở bệnh nhân PBC.
- Một số bệnh nhân có hội chứng Sjögren tiên phát, mặc dù hầu hết những người có phức hợp sicca thì không.
- Đau bụng hạ sườn phải
- Cơn đau không đặc hiệu được mô tả bởi tới một phần ba bệnh nhân mà không có giải thích lâm sàng hoặc X-quang rõ ràng.
- Đau khớp và đau xương
- Thường được báo cáo; cũng có thể chỉ ra viêm khớp viêm đồng thời.
KHÁM THỰC THỂ
- Các phát hiện thay đổi tùy thuộc vào giai đoạn của bệnh; việc thăm khám thường không có gì đặc biệt ở những bệnh nhân không có triệu chứng.
- Gan to và lách to được phát hiện khi bệnh tiến triển; một vài bệnh nhân có thể có lách to sớm do tăng áp lực tĩnh mạch cửa liên quan đến NRH.
- Bất thường ở da
- Tăng sắc tố da, nếu thấy, có thể giống như rám nắng và do melanin gây ra, không phải do bilirubin, trong giai đoạn đầu của PBC.
- Vết trầy xước có thể lan tỏa do gãi vì ngứa khó chữa.
- Vàng da thường biểu hiện muộn hơn trong diễn tiến của bệnh.
- U vàng mí mắt (xanthelasma) và u vàng (xanthomata) phản ánh tình trạng tăng cholesterol máu; u vàng mí mắt phổ biến hơn u vàng (Hình 16.6 và Hình 16.7). Ít hơn 5% bệnh nhân cuối cùng sẽ phát triển u vàng, được tìm thấy trên lòng bàn tay và lòng bàn chân, trên các bề mặt duỗi của khuỷu tay và đầu gối, trong gân của mắt cá chân và cổ tay, và trên mông.
- Bất thường ở mắt: Vòng Kayser-Fleischer hiếm khi được phát hiện và là kết quả của sự ứ đọng đồng do ứ mật kéo dài.
- PBC giai đoạn cuối: Sao mạch, teo cơ thái dương và cơ gốc chi, cổ trướng, và phù thường xảy ra khi có xơ gan và tăng áp lực tĩnh mạch cửa.
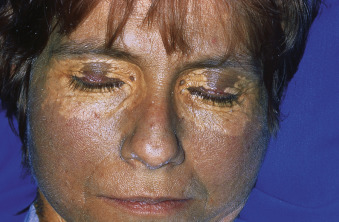
Hình 16.6 U vàng mí mắt (xanthelasma) lan rộng hai bên ở một phụ nữ trung niên.
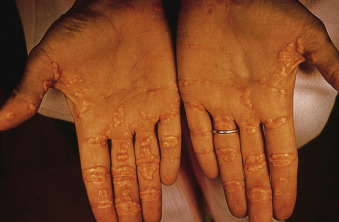
Hình 16.7 U vàng lòng bàn tay (plantar xanthomata) hai bên ở một bệnh nhân PBC.
Chẩn đoán
XÉT NGHIỆM
- Xét nghiệm sinh hóa gan
- Thường có dạng ứ mật (tỷ lệ phosphatase kiềm [ALP] trên aspartate aminotransferase [AST] hoặc alanine aminotransferase [ALT] thường hơn 3 và nồng độ AST hoặc ALT huyết thanh dưới năm lần giới hạn trên của mức bình thường [ULN]).
- Chỉ riêng các xét nghiệm sinh hóa không bao giờ có giá trị chẩn đoán PBC.
- Tăng ALP huyết thanh và gamma-glutamyltranspeptidase là những bất thường sớm nhất; mức độ tăng có thể liên quan đến mức độ nặng của tổn thương ống mật và khả năng đáp ứng điều trị.
- Hoạt độ aminotransferase huyết thanh thường tăng trong suốt quá trình bệnh; sự tăng dai dẳng khi điều trị có liên quan đến các kết cục dài hạn xấu hơn (xem thảo luận sau trong chương).
- Bilirubin huyết thanh thường bình thường ở giai đoạn đầu nhưng sẽ tăng nếu bệnh tiến triển; nó vẫn là yếu tố dự báo kết cục tốt nhất (ngay cả trong giới hạn bình thường), và cùng với các giá trị ALP, là một dấu ấn sinh học được xác thực về kết cục và là một chỉ số thay thế thường được áp dụng cho hiệu quả điều trị.
- AMA có mặt ở 95% bệnh nhân. Ở những người không có AMA, nhiều người có ANA đặc hiệu, bao gồm gp100 và sp210.
- Các phát hiện liên quan khác
- Nồng độ albumin huyết thanh và thời gian prothrombin bình thường ở giai đoạn đầu và bất thường ở giai đoạn cuối.
- Nồng độ IgM huyết thanh tăng đa dòng.
- Nồng độ cholesterol huyết thanh tăng ở ít nhất 50% bệnh nhân, do ứ mật, mà không làm tăng các biến cố tim mạch ở tình trạng chiếm ưu thế ở nữ này; điều trị tăng lipid máu, nếu có các yếu tố nguy cơ đồng thời, là an toàn. Nồng độ lipoprotein mật độ cao (HDL) tăng.
- Nồng độ đồng trong gan và nước tiểu tăng.
- Suy giáp với nồng độ hormone kích thích tuyến giáp (TSH) tăng là thường gặp.
- Có thể tìm thấy bằng chứng về các tình trạng tự miễn đồng thời khác (ví dụ, kháng thể kháng transglutaminase mô trong bệnh celiac).
SINH THIẾT GAN
- Sinh thiết gan không còn được thực hiện thường quy nhưng có thể hỗ trợ xác nhận chẩn đoán PBC và cung cấp ước tính về mức độ nặng của bệnh khi trình diện.
- Ở những bệnh nhân không có AMA (và khi xét nghiệm ANA đặc hiệu không có sẵn) hoặc ở những người có các giải thích thay thế tiềm năng cho các phát hiện xét nghiệm sinh hóa gan, nên xem xét sinh thiết gan. Các trường hợp như vậy bao gồm các hội chứng “chồng lấp” hoặc “giao thoa” trong đó mô học gan là cần thiết để xem xét trong bối cảnh các đặc điểm lâm sàng tổng thể (xem Chương 7).
XÉT NGHIỆM HÌNH ẢNH
Các xét nghiệm hình ảnh hữu ích để loại trừ tắc nghẽn đường mật và sàng lọc sỏi mật nếu có đau bụng.
- Siêu âm: Không xâm lấn và thường đủ để loại trừ tắc nghẽn đường mật.
- Chụp đường mật: Chỉ được chỉ định ở những bệnh nhân âm tính với AMA mà viêm đường mật xơ hóa tiên phát là một chẩn đoán có thể; chụp đường mật cộng hưởng từ là kỹ thuật được ưu tiên.
NGUYÊN TẮC CHẨN ĐOÁN
- Chẩn đoán PBC dựa trên bệnh sử, các phát hiện thực thể, xét nghiệm và mô học, nếu có.
- Sự kết hợp giữa các chỉ số xét nghiệm sinh hóa gan ứ mật và sự hiện diện của AMA có giá trị dự báo dương tính cao cho chẩn đoán mô học của PBC.
- Chẩn đoán PBC hiện nay thường dựa trên các phát hiện xét nghiệm. Tuy nhiên, tỷ lệ béo phì gia tăng có thể đòi hỏi phải khảo sát thêm: 0,5% dân số khỏe mạnh dương tính với AMA, và có tới 30% người khỏe mạnh có thể bị gan nhiễm mỡ, mà về mặt sinh hóa có thể được phản ánh bằng sự gia tăng ALP.
CHẨN ĐOÁN PHÂN BIỆT
- Sỏi mật
- Tắc nghẽn đường mật ngoài gan do cơ học, chẳng hạn như khối u, nang, và hẹp sau phẫu thuật
- Viêm đường mật xơ hóa tiên phát
- Gan nhiễm mỡ không do rượu hoặc do rượu
- Viêm gan siêu vi ứ mật
- Viêm gan u hạt
- Viêm gan tự miễn
- Hội chứng ống mật biến mất
- Ứ mật trong gan tái phát lành tính
- Ứ mật do thuốc
- Bệnh liên quan đến IgG4
Diễn tiến tự nhiên và Tiên lượng
- Thời gian sống trung bình của bệnh nhân có triệu chứng dao động từ 7,5 đến 10 năm và là 7 năm đối với PBC giai đoạn mô học III và IV.
- Thời gian sống trung bình của bệnh nhân không có triệu chứng trong các đoàn hệ lịch sử, không phân tầng đã dao động từ 10 đến 16 năm.
- Hầu hết bệnh nhân không có triệu chứng sẽ phát triển triệu chứng, thường trong vòng 2 đến 4 năm sau khi chẩn đoán.
- Sự hiện diện hoặc hiệu giá của AMA không ảnh hưởng đến sự sống còn.
- Nếu bệnh nhân đạt được đáp ứng sinh hóa với điều trị bằng UDCA (xem phần Phân tầng nguy cơ sau trong chương), thì tỷ lệ sống sót sau 10 năm là rất tốt, >90%.
- Tuổi trình diện trẻ hơn và giới tính nam có liên quan đến tỷ lệ đáp ứng với UDCA giảm.
Điều trị
CÁC TRIỆU CHỨNG CỦA Ứ MẬT MẠN TÍNH
- Ngứa (Bảng 16.1)
a. Thuốc kháng histamine
* Đôi khi hữu ích ở giai đoạn đầu của PBC khi ngứa không nghiêm trọng; tác dụng phụ gây buồn ngủ của thuốc kháng histamine không chọn lọc có thể hữu ích.
b. Cholestyramine
* Nhựa không hấp thu này liên kết với axit mật và làm giảm ngứa ở nhiều bệnh nhân.
* Liệu pháp nên nhằm mục đích giảm triệu chứng, với liều thông thường là 4 g hai lần mỗi ngày, thường được uống pha với nước hoặc nước trái cây trước và sau bữa ăn sáng.
* Tùy thuộc vào mức độ nặng của ứ mật, có thể mất đến 14 ngày trước khi ngứa thuyên giảm.
* Các loại thuốc khác cần được uống trước 1 giờ hoặc sau 2 đến 4 giờ so với cholestyramine, để tránh suy giảm hấp thu ở ruột.
c. Colestipol hydrochloride (nhựa amoni)
* Có thể được xem xét ở những bệnh nhân thấy cholestyramine khó uống; tuy nhiên, một số bệnh nhân thấy colestipol cũng khó uống không kém. Colesevelam cũng là một lựa chọn.
d. Các thuốc chống ngứa khác có thể kiểm soát ngứa ở một số bệnh nhân (theo thứ tự sử dụng được đề xuất)
* Rifampin (150 đến 300 mg hai lần mỗi ngày)
* Sertraline (50 đến 100 mg mỗi ngày một lần)
* Naloxone (chất đối kháng opioid): Dựa trên dữ liệu cho thấy ngứa có thể qua trung gian dẫn truyền thần kinh opioid.
* Nalmefene (chất đối kháng opioid)
* Naltrexone (chất đối kháng opioid)
* Quang trị liệu bằng ánh sáng cực tím B
* Lọc huyết tương (hầu như luôn hữu ích nhưng bất tiện và tốn kém)
* Hệ thống tái tuần hoàn chất hấp phụ phân tử (MARS; hiệu quả ở những nơi có sẵn)
* Ghép gan (LT)
* Các thử nghiệm về thuốc ức chế chất vận chuyển axit mật phụ thuộc natri ở đỉnh tế bào (apical sodium codependent bile acid transporter) đang được tiến hành.
Bảng 16.1 ■ Điều trị ngứa bằng thuốc
| Thuốc | Cơ chế tác dụng | Liều | Tác dụng phụ |
|---|---|---|---|
| Cholestyramine | Nhựa axit mật | 4–16 g uống/ngày | Khó ăn, táo bón, can thiệp hấp thụ thuốc khác |
| Colestipol | Nhựa axit mật | 5 g uống 3 lần/ngày | Táo bón, can thiệp hấp thụ thuốc khác |
| Rifampin | Cạnh tranh với axit mật để hấp thụ gan | 300–600 mg uống/ngày | Độc tính gan đặc hiệu cá thể |
| Sertraline | SSRI | 50–100 mg/ngày | Khô miệng |
| Naloxone | Chất đối kháng opioid | 0,2 μg/kg IV/phút trong 24 giờ | Triệu chứng giống cai thuốc opioid tự giới hạn |
| Nalmefene | Chất đối kháng opioid | 60–120 mg uống/ngày | Triệu chứng giống cai thuốc opioid tự giới hạn |
| Naltrexone | Chất đối kháng opioid | 50 mg uống/ngày | Triệu chứng giống cai thuốc opioid tự giới hạn |
IV, Tĩnh mạch; SSRI, chất ức chế tái hấp thu serotonin chọn lọc.
- Kém hấp thu vitamin tan trong chất béo
a. Tần suất kém hấp thu gần như tỷ lệ thuận với mức độ nặng và thời gian ứ mật và hiện nay hiếm khi là một mối quan tâm lâm sàng.
b. Nồng độ vitamin A, D, E và K nên được đo ở những bệnh nhân PBC bị vàng da; nên kê đơn bổ sung cho những bệnh nhân có nồng độ thấp.
c. Điều trị: Vitamin nên được dùng đường uống cách xa cholestyramine nhất có thể.
* Vitamin K uống: 5 mg/ngày
* Vitamin A: 10.000 đến 25.000 IU/ngày
* 25-OH vitamin D: 20 µg ba lần mỗi tuần; kiểm tra nồng độ 25-OH vitamin D huyết thanh sau vài tuần
* Bổ sung canxi
* Vitamin E: 400 đến 1000 IU/ngày - Tiêu chảy phân mỡ (Steatorrhea)
a. Được điều trị bằng chế độ ăn ít chất béo bổ sung triglyceride chuỗi trung bình (MCT) để duy trì lượng calo hợp lý.
b. Hầu hết bệnh nhân dung nạp 60 mL dầu MCT mỗi ngày.
c. Một số bệnh nhân PBC và hội chứng sicca có thể bị suy tụy đồng thời, có thể được điều trị bằng liệu pháp thay thế enzyme tụy.
d. Bệnh nhân có thể phát triển thiếu máu thiếu sắt, phản ánh sự mất máu đường tiêu hóa không được nhận biết thường là do các biểu hiện ở dạ dày của tăng áp lực tĩnh mạch cửa (bệnh dạ dày hoặc giãn mạch máu hang vị dạ dày). Cần nội soi đại tràng để loại trừ nguyên nhân đường tiêu hóa dưới và loại trừ bệnh celiac đồng thời. - Loãng xương
a. Loãng xương là một biểu hiện của PBC nhưng cũng là một phát hiện thường gặp ở những phụ nữ khỏe mạnh cùng độ tuổi.
b. Mật độ khoáng xương và nguy cơ gãy xương liên quan nên được đánh giá bằng phương pháp đo hấp thụ tia X năng lượng kép (dual x-ray absorptiometry) khi chẩn đoán PBC.
c. Một nghiên cứu hồi cứu đã cho thấy tác dụng có lợi của liệu pháp thay thế hormone ở phụ nữ sau mãn kinh mắc PBC.
d. Ghép gan có hiệu quả trong việc tăng mật độ khoáng xương, với sự cải thiện thường bị trì hoãn cho đến 1 năm sau khi ghép. Mật độ khoáng xương ban đầu giảm trong tối đa 6 tháng sau khi ghép do ức chế miễn dịch bằng glucocorticoid và không hoạt động thể chất.
BỆNH NỀN (Bảng 16.2)
- UDCA
- UDCA là tác nhân ban đầu được sử dụng cho PBC. Nó làm giảm rối loạn chức năng gan và có thể làm chậm sự tiến triển của bệnh. Lợi ích tổng thể lớn nhất là ở những bệnh nhân mắc bệnh giai đoạn sớm, mặc dù lợi ích về sự sống còn chỉ có thể chứng minh được ở những người mắc bệnh tiến triển.
- UDCA an toàn và được dung nạp tốt; tăng cân nhẹ (trung bình 3 kg), đầy hơi và rụng tóc là các tác dụng phụ. Nếu bệnh nhân có đáp ứng sinh hóa với điều trị, nó thường được duy trì; tuy nhiên, nếu liệu pháp UDCA bị gián đoạn, rối loạn chức năng gan sẽ quay trở lại.
- Trong bốn thử nghiệm có đối chứng, UDCA, 13 đến 15 mg/kg trọng lượng cơ thể/ngày đường uống, làm giảm nồng độ bilirubin, ALP, aminotransferase và IgM huyết thanh.
- Các nghiên cứu riêng lẻ cũng chỉ ra UDCA có thể ảnh hưởng thuận lợi đến sự sống còn, làm chậm sự suy giảm mô học, và giảm bớt sự tiến triển của tăng áp lực tĩnh mạch cửa.
- Khi dữ liệu được gộp từ ba nghiên cứu lớn, UDCA kéo dài thời gian đến khi phải ghép gan so với giả dược.
- Trong một nghiên cứu đa trung tâm được thực hiện tại Hoa Kỳ, hiệu quả chỉ giới hạn ở một phân nhóm bệnh nhân giai đoạn I và II có nồng độ bilirubin huyết thanh ban đầu < 2 mg/dL.
- Các phân tích tổng hợp đã cho kết quả mâu thuẫn do thách thức của việc kết hợp các nghiên cứu thời gian ngắn với liều UDCA không đủ với các nghiên cứu thời gian dài hơn với liều UDCA thích hợp.
- Tuy nhiên, nhiều nghiên cứu cho thấy rõ ràng rằng những bệnh nhân có đáp ứng sinh hóa với UDCA có tuổi thọ bình thường; định nghĩa về đáp ứng với liệu pháp khác nhau nhưng thường bao gồm sự cải thiện giá trị ALP huyết thanh.
- Số lượng bệnh nhân PBC cần ghép gan giảm phản ánh việc sử dụng rộng rãi UDCA.
- Axit Obeticholic
- Axit obeticholic (OCA) là một chất chủ vận thụ thể farnesoid-X bán tổng hợp được dùng đường uống. Nó hoạt động để giảm tổng hợp axit mật ở tế bào gan và cũng có tác dụng chống xơ hóa.
- OCA làm giảm hoạt độ phosphatase kiềm huyết thanh khi so sánh với giả dược trong các thử nghiệm có đối chứng trong đó nó được dùng kết hợp với UDCA hoặc dưới dạng đơn trị liệu. Giảm nồng độ phosphatase kiềm huyết thanh tương quan với sự cải thiện sự sống còn trong PBC, nhưng lợi ích trực tiếp về sự sống còn vẫn chưa được chứng minh đối với OCA.
- OCA được cấp phép tại Hoa Kỳ để sử dụng cho những bệnh nhân không có đáp ứng sinh hóa với UDCA hoặc không dung nạp UDCA. Liều ban đầu là 5 mg mỗi ngày đường uống, với việc điều chỉnh liều lên 10 mg mỗi ngày sau 3 tháng, nếu dung nạp.
- Ngứa có thể thấy với OCA; việc quản lý bao gồm điều chỉnh liều cũng như liệu pháp tiêu chuẩn với cholestyramine hoặc rifampin.
- Các tác nhân khác
- Colchicine: Mặc dù dữ liệu ban đầu đáng khích lệ, một tổng quan của Cochrane đã không xác nhận được hiệu quả.
- Methotrexate: Mặc dù dữ liệu ban đầu đáng khích lệ, một tổng quan của Cochrane đã không xác nhận được hiệu quả.
- Những thuốc khác:
- Các tác nhân ứng cử viên đã bao gồm budesonide, fenofibrates, và rituximab; tuy nhiên, không có dữ liệu để hỗ trợ việc sử dụng thường quy ngoài nhãn của các loại thuốc này.
- Các loại thuốc khác tác động lên trục thụ thể farnesoid X (ngoài OCA) có thể sẽ có mặt.
- Đối với những bệnh nhân không có đáp ứng sinh hóa với liệu pháp UDCA, cần có các loại thuốc mới.
- Hút thuốc dường như làm tăng tốc độ tiến triển của PBC và nên được ngưng.
Bảng 16.2 ■ Điều trị thuốc viêm đường mật nguyên phát
| Thuốc | Cơ chế tác dụng | Liều | Lợi ích | Tác dụng phụ | Nhận xét |
|---|---|---|---|---|---|
| Axit ursodeoxycholic | Choleretic | 13–15 mg/kg/ngày uống | Cải thiện sinh hóa gan, làm chậm tiến triển mô học, và có thể cải thiện sự sống còn dài hạn | Tiêu chảy, tăng cân, tóc mỏng, tăng ngứa | Thuốc được sử dụng rộng rãi nhất |
| Obeticholic acid | Chất đồng vận thụ thể Farnesoid-X | 5 mg mỗi ngày, tăng lên 10 mg mỗi ngày sau 3 tháng, nếu dung nạp | Cải thiện sinh hóa gan | Ngứa phụ thuộc liều | Được FDA và EMA phê duyệt cho bệnh nhân có đáp ứng không đủ với UDCA hoặc không dung nạp UDCA |
EMA, Cơ quan Dược phẩm châu Âu; FDA, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ; UDCA, axit ursodeoxycholic.
THEO DÕI CÁC BIẾN CHỨNG CỦA XƠ GAN
- Giãn tĩnh mạch thực quản có thể xảy ra ở bệnh nhân PBC khi không có xơ gan do tăng áp lực tĩnh mạch cửa trước xoang gây ra bởi NRH. Nếu nghi ngờ xơ gan hoặc nếu có giảm số lượng tiểu cầu, chỉ định nội soi để sàng lọc giãn tĩnh mạch thực quản. Bệnh nhân bị mệt mỏi có thể thấy liệu pháp với thuốc chẹn thụ thể beta gây phiền toái, do đó cần phải thắt dự phòng các tĩnh mạch giãn.
- Ung thư biểu mô tế bào gan (HCC) có thể xảy ra ở bệnh nhân xơ gan do PBC; các hướng dẫn khuyến nghị theo dõi bằng siêu âm mỗi 6 tháng ở bệnh nhân xơ gan.
Phân tầng nguy cơ
- Tỷ lệ sống sót không cần ghép có thể được dự đoán bằng đáp ứng sinh hóa với UDCA. Có một loạt các định nghĩa đáp ứng với UDCA được rút ra từ các đoàn hệ lâm sàng bao gồm tiêu chí Paris-1, Barcelona và Toronto.
- Với tiêu chí Paris-1, nếu sau 1 năm điều trị, nồng độ bilirubin huyết thanh < ULN, AST hoặc ALT < 2 lần ULN, và ALP < 3 lần ULN, thì tỷ lệ sống sót không cần ghép sau 10 năm là >90%.
- Trong các bối cảnh thử nghiệm lâm sàng, tiêu chí Toronto đã được sử dụng (ví dụ, mục tiêu sau can thiệp là ALP < 1,67 × ULN, với mức giảm ALP 15%, và nồng độ bilirubin huyết thanh trong giới hạn bình thường).
- Tương tự, thang điểm nguy cơ UK-PBC và GLOBE là các thang điểm nguy cơ tổng hợp dựa trên các biến số ban đầu và sau điều trị UDCA từ các đoàn hệ lâm sàng lớn. Cả hai đều dự đoán chính xác tỷ lệ sống sót không cần ghép tại một số thời điểm. Cả hai thang điểm đều kết hợp các dấu ấn nguy cơ bệnh (ví dụ, tuổi, AST, ALP, bilirubin) và giai đoạn (ví dụ, albumin, tiểu cầu) một cách khác nhau.
- Giãn tĩnh mạch thực quản
- Thời điểm tối ưu để xác định khi nào cần sàng lọc bằng nội soi vẫn còn tranh cãi; nói chung, số lượng tiểu cầu giảm hoặc kích thước lách tăng là các chỉ số.
- Thang điểm Nguy cơ Giãn tĩnh mạch thực quản ở PBC Newcastle (Newcastle Varices in PBC Risk Score) sử dụng một số biến số (albumin, ALP, tiểu cầu, lách to trên siêu âm) để dự đoán nguy cơ tổng hợp của giãn tĩnh mạch thực quản ở bệnh nhân PBC.
- Ung thư biểu mô tế bào gan (HCC)
- Nguy cơ tăng ở những bệnh nhân không đạt được đáp ứng sinh hóa với UDCA.
- Nguy cơ tăng ở giới tính nam, nồng độ aminotransferase huyết thanh tăng, giảm tiểu cầu, và bệnh mất bù.
- Nhìn chung, giới tính nam, trình diện ở tuổi trẻ hơn, và sự hiện diện của các ANA đặc hiệu là các yếu tố dự báo kết cục xấu hơn. Ít hơn 50% phụ nữ trình diện dưới 40 tuổi đạt được đáp ứng sinh hóa.
- Các thang điểm nguy cơ không điều chỉnh cho bệnh đi kèm, có thể đánh giá thấp tác động của xơ gan đã xác định trong một trường hợp trình diện muộn của PBC, và cần một năm điều trị UDCA đủ liều để tính toán.
Ghép gan
- Bệnh nhân bị xơ gan mất bù do PBC là những ứng cử viên xuất sắc cho việc ghép gan; thang điểm MELD (Model for End-stage Liver Disease) nói chung là một cách thích hợp để xác định những bệnh nhân có khả năng được hưởng lợi (xem Chương 33).
- PBC giai đoạn cuối thường được định nghĩa là xơ gan phức tạp bởi ít nhất một trong những điều sau đây: a. Xuất huyết do vỡ giãn tĩnh mạch thực quản-dạ dày b. Cổ trướng khó chữa c. Bệnh não gan d. Albumin huyết thanh < 3.5 g/dL e. Bilirubin huyết thanh > 4 mg/dL
- Tỷ lệ sống sót sau 1 năm sau khi ghép gan ở bệnh nhân PBC là khoảng 90%.
- PBC có thể tái phát trong mảnh ghép, mặc dù tái phát tương đối không thường xuyên và hiếm khi ảnh hưởng đến sự sống còn của mảnh ghép.
- Việc sử dụng ức chế miễn dịch dựa trên cyclosporine, so với tacrolimus, có thể bảo vệ chống lại bệnh tái phát.
TÀI LIỆU THAM KHẢO
- Boonstra K, Beuers U, Ponsioen CY. Epidemiology of primary sclerosing cholangitis and primary biliary cirrhosis: a systematic review. J Hepatol. 2012;56:1181-1188.
- Carbone M, Mells GF, Pells G, et al. Sex and age are determinants of the clinical phenotype of primary biliary cirrhosis and response to ursodeoxycholic acid. Gastroenterology. 2013;144:560-569.
- Carbone M, Sharp SJ, Flack S, et al. The UK-PBC risk scores: derivation and validation of a scoring system for long-term prediction of end-stage liver disease in primary biliary cholangitis. Hepatology. 2016;63:930-950.
- European Association for the Study of the Liver. EASL Clinical Practice Guidelines: the diagnosis and management of patients with primary biliary cholangitis. J Hepatol. 2017 Apr 18. Epub ahead of print.
- Gong Y, Huang ZB, Christensen E, et al. Ursodeoxycholic acid for primary biliary cirrhosis. Cochrane Database Syst Rev. 2008. CD000551.
- Hirschfield GM, Gershwin ME. The immunobiology and pathophysiology of primary biliary cirrhosis. Annu Rev Pathol. 2013;8:303-330.
- Huet PM, Vincent C, Deslaurier J, et al. Portal hypertension and primary biliary cirrhosis: effect of long-term ursodeoxycholic acid treatment. Gastroenterology. 2008;135:1552-1560.
- Lammers WJ, Hirschfield GM, Corpechot C, et al. Development and validation of a scoring system to predict outcomes of patients with primary biliary cirrhosis receiving ursodeoxycholic acid therapy. Gastroenterology. 2015;149:1804-1812.
- Nevens F, Andreone P, Mazzella G, et al. A placebo-controlled trial of obeticholic acid in primary biliary cholangitis. N Engl J Med. 2016;7:631-643.
- Patanwala I, McMeekin P, Walters R, et al. A validated clinical tool for the prediction of varices in PBC: the Newcastle Varices in PBC Score. J Hepatol. 2013;59:327-335.
- Pollheimer MJ, Fickert P. Animal models in primary biliary cirrhosis and primary sclerosing cholangitis. Clin Rev Allergy Immunol. 2015;48:207-217.
- Tang R, Chen H, Miao Q, et al. The cumulative effects of known susceptibility variants to predict primary biliary cirrhosis risk. Genes Immun. 2015;16:193-198.
- Trivedi PJ, Corpechot C, Pares A, et al. Risk stratification in autoimmune cholestatic liver diseases: opportunities for clinicians and trialists. Hepatology. 2016;63:644-659.
- Webb GJ, Siminovitch KA, Hirschfield GM. The immunogenetics of primary biliary cirrhosis: a comprehensive review. J Autoimmun. 2015;64:42-52.
- Yang CY, Ma X, Tsuneyama K, et al. IL-12/Th1 and IL-23/Th17 biliary microenvironment in primary biliary cirrhosis: implications for therapy. Hepatology. 2014;59:1944-1953.
BẢNG CHÚ GIẢI THUẬT NGỮ Y HỌC ANH VIỆT
| STT | Thuật ngữ tiếng Anh | Phiên âm IPA | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Primary Biliary Cholangitis (PBC) | /ˈpraɪmeri ˈbɪliəri ˌkoʊlənˈdʒaɪtɪs/ | Viêm đường mật tiên phát |
| 2 | Primary Biliary Cirrhosis | /ˈpraɪmeri ˈbɪliəri sɪˈroʊsɪs/ | Xơ gan ứ mật tiên phát |
| 3 | Chronic cholestatic liver disease | /ˈkrɒnɪk ˌkoʊlɪˈstætɪk ˈlɪvər dɪˈziːz/ | Bệnh gan ứ mật mạn tính |
| 4 | Pathogenesis | /ˌpæθəˈdʒɛnəsɪs/ | Sinh bệnh học |
| 5 | Environmental factors | /ɪnˌvaɪrənˈmɛntəl ˈfæktərz/ | Yếu tố môi trường |
| 6 | Genetic factors | /dʒəˈnɛtɪk ˈfæktərz/ | Yếu tố di truyền |
| 7 | Human leukocyte antigen (HLA) | /ˈhjuːmən ˈluːkəˌsaɪt ˈæntɪdʒən/ | Kháng nguyên bạch cầu người |
| 8 | Type 1 helper T-cell (Th1) | /taɪp wʌn ˈhɛlpər tiː sɛl/ | Tế bào T hỗ trợ typ 1 |
| 9 | Interleukin-12 (IL-12) | /ˌɪntərˈluːkɪn twɛlv/ | Interleukin-12 |
| 10 | Signaling axis | /ˈsɪɡnəlɪŋ ˈæksɪs/ | Trục tín hiệu |
| 11 | Autoimmune | /ˌɔːtoʊɪˈmjuːn/ | Tự miễn |
| 12 | Lymphocytic cholangitis | /ˌlɪmfoʊˈsɪtɪk ˌkoʊlənˈdʒaɪtɪs/ | Viêm đường mật tế bào lympho |
| 13 | Asymptomatic | /ˌeɪsɪmptəˈmætɪk/ | Không có triệu chứng |
| 14 | Symptom severity | /ˈsɪmptəm sɪˈvɛrəti/ | Mức độ nặng của triệu chứng |
| 15 | Quality of life | /ˈkwɒləti əv laɪf/ | Chất lượng cuộc sống |
| 16 | Liver biochemical test | /ˈlɪvər ˌbaɪoʊˈkɛmɪkəl tɛst/ | Xét nghiệm sinh hóa gan |
| 17 | Biliary imaging | /ˈbɪliəri ˈɪmɪdʒɪŋ/ | Chẩn đoán hình ảnh đường mật |
| 18 | Antimitochondrial antibodies (AMA) | /ˌæntiˌmaɪtəˈkɒndriəl ˈæntɪˌbɒdiz/ | Kháng thể kháng ty thể |
| 19 | Antinuclear antibodies (ANA) | /ˌæntiˈnuːkliər ˈæntɪˌbɒdiz/ | Kháng thể kháng nhân |
| 20 | Liver biopsy | /ˈlɪvər ˈbaɪɒpsi/ | Sinh thiết gan |
| 21 | Consensus guidelines | /kənˈsɛnsəs ˈɡaɪdlaɪnz/ | Hướng dẫn đồng thuận |
| 22 | Ursodeoxycholic acid (UDCA) | /ˌɜːrsoʊdiˌɒksiˈkoʊlɪk ˈæsɪd/ | Axit ursodeoxycholic |
| 23 | Biochemical response | /ˌbaɪoʊˈkɛmɪkəl rɪˈspɒns/ | Đáp ứng sinh hóa |
| 24 | Poorer outcome | /ˈpʊərər ˈaʊtˌkʌm/ | Kết cục xấu hơn |
| 25 | Methotrexate | /ˌmɛθəˈtrɛkseɪt/ | Methotrexate |
| 26 | Colchicine | /ˈkɒltʃɪsiːn/ | Colchicine |
| 27 | Fenofibrate | /ˌfɛnoʊˈfaɪbreɪt/ | Fenofibrate |
| 28 | Bezafibrate | /ˌbɛzəˈfaɪbreɪt/ | Bezafibrate |
| 29 | Farnesoid X-receptor (FXR) | /ˈfɑːrnəˌsɔɪd ɛks rɪˈsɛptər/ | Thụ thể farnesoid X |
| 30 | Obeticholic acid (OCA) | /ˌoʊbɪtɪˈkoʊlɪk ˈæsɪd/ | Axit obeticholic |
| 31 | Nonresponder | /ˌnɒnrɪˈspɒndər/ | Không đáp ứng |
| 32 | Randomized-controlled trials | /ˈrændəmaɪzd kənˈtroʊld ˈtraɪəlz/ | Thử nghiệm ngẫu nhiên có đối chứng |
| 33 | Advanced liver disease | /ədˈvænst ˈlɪvər dɪˈziːz/ | Bệnh gan tiến triển |
| 34 | Liver transplantation (LT) | /ˈlɪvər ˌtrænsplænˈteɪʃən/ | Ghép gan |
| 35 | Transplant indications | /ˈtrænsplænt ˌɪndɪˈkeɪʃənz/ | Chỉ định ghép |
| 36 | Intractable pruritus | /ɪnˈtræktəbəl pruːˈraɪtəs/ | Ngứa khó chữa |
| 37 | Liver failure | /ˈlɪvər ˈfeɪljər/ | Suy gan |
| 38 | Fatigue | /fəˈtiːɡ/ | Mệt mỏi |
| 39 | Nomenclature | /noʊˈmɛnkləˌtʃʊər/ | Danh pháp |
| 40 | Hepatocellular carcinoma (HCC) | /hɪˌpætoʊˈsɛljʊlər ˌkɑːrsɪˈnoʊmə/ | Ung thư biểu mô tế bào gan |
| 41 | Surveillance | /sərˈveɪləns/ | Theo dõi, giám sát |
| 42 | Epidemiology | /ˌɛpɪˌdiːmiˈɒlədʒi/ | Dịch tễ học |
| 43 | Female-predominant | /ˈfiːmeɪl prɪˈdɒmɪnənt/ | Chiếm ưu thế ở nữ |
| 44 | Ethnicity | /ɛθˈnɪsəti/ | Sắc tộc |
| 45 | Incidence | /ˈɪnsɪdəns/ | Tỷ lệ mắc mới |
| 46 | Prevalence | /ˈprɛvələns/ | Tỷ lệ hiện mắc |
| 47 | Age of onset | /eɪdʒ əv ˈɒnˌsɛt/ | Tuổi khởi phát |
| 48 | Menarche | /mɪˈnɑːrki/ | Dậy thì (lần hành kinh đầu) |
| 49 | Decompensation | /ˌdiːˌkɒmpɛnˈseɪʃən/ | Mất bù |
| 50 | Genetic mutation | /dʒəˈnɛtɪk mjuːˈteɪʃən/ | Đột biến di truyền |
| 51 | Celiac disease | /ˈsiːliæk dɪˈziːz/ | Bệnh Celiac |
| 52 | Scleroderma | /ˌsklɪərəˈdɜːrmə/ | Xơ cứng bì |
| 53 | Concordance | /kənˈkɔːrdəns/ | Tương hợp |
| 54 | Identical twins | /aɪˈdɛntɪkəl twɪnz/ | Song sinh cùng trứng |
| 55 | Xenobiotic exposure | /ˌzɛnoʊbaɪˈɒtɪk ɪkˈspoʊʒər/ | Phơi nhiễm với chất lạ |
| 56 | Molecular mimicry | /məˈlɛkjʊlər ˈmɪmɪkri/ | Bắt chước phân tử |
| 57 | Genome-wide association | /dʒiːˈnoʊm waɪd əˌsoʊsiˈeɪʃən/ | Liên kết toàn bộ bộ gen |
| 58 | T-cell activation | /tiː sɛl ˌæktɪˈveɪʃən/ | Hoạt hóa tế bào T |
| 59 | Antigen presentation | /ˈæntɪdʒən ˌprɛzɛnˈteɪʃən/ | Trình diện kháng nguyên |
| 60 | Multiple sclerosis | /ˈmʌltɪpəl sklɪˈroʊsɪs/ | Đa xơ cứng |
| 61 | Ulcerative colitis | /ˈʌlsərətɪv kəˈlaɪtɪs/ | Viêm loét đại tràng |
| 62 | Rheumatoid arthritis | /ˈruːməˌtɔɪd ɑːrˈθraɪtɪs/ | Viêm khớp dạng thấp |
| 63 | Type 1 diabetes mellitus | /taɪp wʌn ˌdaɪəˈbiːtiːz ˈmɛlɪtəs/ | Đái tháo đường typ 1 |
| 64 | X chromosome | /ɛks ˈkroʊməˌsoʊm/ | Nhiễm sắc thể X |
| 65 | Disease susceptibility | /dɪˈziːz səˌsɛptəˈbɪləti/ | Tính nhạy cảm với bệnh |
| 66 | Immunology | /ˌɪmjʊˈnɒlədʒi/ | Miễn dịch học |
| 67 | Immunologic aberrations | /ˌɪmjʊnəˈlɒdʒɪk ˌæbəˈreɪʃənz/ | Bất thường miễn dịch |
| 68 | Acute liver failure | /əˈkjuːt ˈlɪvər ˈfeɪljər/ | Suy gan cấp |
| 69 | Drug injury | /drʌɡ ˈɪndʒəri/ | Tổn thương do thuốc |
| 70 | Autoimmune hepatitis | /ˌɔːtoʊɪˈmjuːn ˌhɛpəˈtaɪtɪs/ | Viêm gan tự miễn |
| 71 | Dihydrolipoamide acyltransferase (E2) | /daɪˌhaɪdroʊˈlɪpəˌmaɪd ˌæsɪlˈtrænsfəˌreɪs/ | Dihydrolipoamide acyltransferase (E2) |
| 72 | Ketoacid dehydrogenase | /ˌkiːtoʊˈæsɪd diːˌhaɪˈdrɒdʒəˌneɪs/ | Ketoacid dehydrogenase |
| 73 | Pyruvate dehydrogenase (PDH) | /paɪˈruːveɪt diːˌhaɪˈdrɒdʒəˌneɪs/ | Pyruvate dehydrogenase |
| 74 | Cloned human mitochondrial proteins | /kloʊnd ˈhjuːmən ˌmaɪtəˈkɒndriəl ˈproʊtiːnz/ | Protein ty thể người được nhân bản |
| 75 | Bile duct injury | /baɪl dʌkt ˈɪndʒəri/ | Tổn thương ống mật |
| 76 | Biliary epithelial cell | /ˈbɪliəri ˌɛpɪˈθiːliəl sɛl/ | Tế bào biểu mô đường mật |
| 77 | Apoptosis | /ˌæpəpˈtoʊsɪs/ | Chết tế bào theo chương trình |
| 78 | Luminal surface | /ˈluːmɪnəl ˈsɜːrfɪs/ | Bề mặt lòng ống |
| 79 | Primary sclerosing cholangitis (PSC) | /ˈpraɪmeri ˈsklɪəroʊsɪŋ ˌkoʊlənˈdʒaɪtɪs/ | Viêm đường mật xơ hóa tiên phát |
| 80 | T-lymphocyte cytotoxicity | /tiː ˈlɪmfoʊˌsaɪt ˌsaɪtoʊtɒkˈsɪsəti/ | Độc tế bào T-lymphocyte |
| 81 | Antibody titer | /ˈæntɪˌbɒdi ˈtaɪtər/ | Hiệu giá kháng thể |
| 82 | Immunization | /ˌɪmjʊnɪˈzeɪʃən/ | Tiêm chủng |
| 83 | 2-octynoic acid | /tuː ˌɒktɪˈnoʊɪk ˈæsɪd/ | Axit 2-octynoic |
| 84 | Escherichia coli (E. coli) | /ˌɛʃəˈrɪkiə ˈkoʊlaɪ/ | Escherichia coli (E. coli) |
| 85 | Autoimmunity-prone mice | /ˌɔːtoʊɪˈmjuːnəti proʊn maɪs/ | Chuột dễ bị tự miễn |
| 86 | T-regulatory pathway | /tiː ˈrɛɡjʊləˌtɔːri ˈpæθweɪ/ | Con đường T-điều hòa |
| 87 | FOXP3 deficiency | /fɒks piː θriː dɪˈfɪʃənsi/ | Thiếu hụt FOXP3 |
| 88 | IL2 receptor alpha dysfunction | /aɪ ɛl tuː rɪˈsɛptər ˈælfə dɪsˈfʌŋkʃən/ | Rối loạn chức năng thụ thể IL2 alpha |
| 89 | Transforming growth factor (TGF) | /trænsˈfɔːrmɪŋ ɡroʊθ ˈfæktər/ | Yếu tố tăng trưởng biến đổi |
| 90 | Anion exchanger | /ˈænaɪən ɪksˈtʃeɪndʒər/ | Chất trao đổi anion |
| 91 | Immunofluorescence | /ˌɪmjʊnoʊflʊəˈrɛsəns/ | Huỳnh quang miễn dịch |
| 92 | Multiple nuclear dot ANA | /ˈmʌltɪpəl ˈnuːkliər dɒt eɪ ɛn eɪ/ | ANA dạng chấm nhân đa dạng |
| 93 | Membrane rim ANA | /ˈmɛmbreɪn rɪm eɪ ɛn eɪ/ | ANA dạng viền màng |
| 94 | Anticentromere antibodies | /ˌæntiˌsɛntrəˈmɪər ˈæntɪˌbɒdiz/ | Kháng thể kháng tâm động |
| 95 | Portal hypertensive phenotype | /ˈpɔːrtl ˌhaɪpərˈtɛnsɪv ˈfiːnoʊˌtaɪp/ | Kiểu hình tăng áp lực tĩnh mạch cửa |
| 96 | Immunoglobulin M (IgM) | /ˌɪmjʊnoʊˈɡlɒbjʊlɪn ɛm/ | Immunoglobulin M (IgM) |
| 97 | Cryoprecipitable | /ˌkraɪoʊprɪˈsɪpɪtəbəl/ | Dễ kết tủa lạnh |
| 98 | Sjögren syndrome | /ˈʃoʊɡrən ˈsɪndroʊm/ | Hội chứng Sjögren |
| 99 | Thyroiditis | /ˌθaɪrɔɪˈdaɪtɪs/ | Viêm tuyến giáp |
| 100 | Hypothyroidism | /ˌhaɪpoʊˈθaɪrɔɪˌdɪzəm/ | Suy giáp |
| 101 | Systemic lupus erythematosus (SLE) | /sɪˈstɛmɪk ˈluːpəs ˌɛrɪθəˈmatoʊsəs/ | Lupus ban đỏ hệ thống |
| 102 | T-regulatory cell | /tiː ˈrɛɡjʊləˌtɔːri sɛl/ | Tế bào T-điều hòa |
| 103 | T follicular helper cells | /tiː fəˈlɪkjʊlər ˈhɛlpər sɛlz/ | Tế bào T hỗ trợ nang lympho |
| 104 | Th17 cells | /tiː eɪtʃ ˌsɛvənˈtiːn sɛlz/ | Tế bào Th17 |
| 105 | Sequestration | /ˌsiːkwɛˈstreɪʃən/ | Tích tụ, biệt lập |
| 106 | Hepatic portal triads | /hɪˈpætɪk ˈpɔːrtl ˈtraɪædz/ | Bộ ba khoảng cửa của gan |
| 107 | Chronic nonsuppurative granulomatous cholangitis | /ˈkrɒnɪk nɒnˈsʌpjʊrətɪv ˌɡrænjʊˈloʊmətəs ˌkoʊlənˈdʒaɪtɪs/ | Viêm đường mật u hạt không sinh mủ mạn tính |
| 108 | Granulomatous destruction | /ˌɡrænjʊˈloʊmətəs dɪˈstrʌkʃən/ | Phá hủy dạng u hạt |
| 109 | Interface hepatitis | /ˈɪntərˌfeɪs ˌhɛpəˈtaɪtɪs/ | Viêm gan vùng chuyển tiếp |
| 110 | Glucocorticoid responsive | /ˌɡluːkoʊˈkɔːrtɪˌkɔɪd rɪˈspɒnsɪv/ | Đáp ứng với glucocorticoid |
| 111 | Graft-versus-host disease | /ɡræft ˈvɜːrsəs hoʊst dɪˈziːz/ | Bệnh mảnh ghép chống chủ |
| 112 | Hepatic allograft rejection | /hɪˈpætɪk ˈæloʊˌɡræft rɪˈdʒɛkʃən/ | Thải ghép gan đồng loại |
| 113 | Bile drainage | /baɪl ˈdreɪnɪdʒ/ | Dẫn lưu mật |
| 114 | Retention of bile acids | /rɪˈtɛnʃən əv baɪl ˈæsɪdz/ | Ứ đọng axit mật |
| 115 | Lipid-soluble substances | /ˈlɪpɪd ˈsɒljʊbəl ˈsʌbstənsɪz/ | Chất tan trong lipid |
| 116 | Portal inflammation | /ˈpɔːrtl ˌɪnfləˈmeɪʃən/ | Viêm khoảng cửa |
| 117 | Gross findings | /ɡroʊs ˈfaɪndɪŋz/ | Tổn thương đại thể |
| 118 | Nodular | /ˈnɒdʒʊlər/ | Dạng nốt |
| 119 | Bile staining | /baɪl ˈsteɪnɪŋ/ | Nhiễm mật |
| 120 | End-stage disease | /ɛnd steɪdʒ dɪˈziːz/ | Bệnh giai đoạn cuối |
| 121 | Gallstones | /ˈɡɔːlˌstoʊnz/ | Sỏi mật |
| 122 | Nodular regenerative hyperplasia (NRH) | /ˈnɒdʒʊlər rɪˈdʒɛnərətɪv ˌhaɪpərˈpleɪʒə/ | Tăng sản nốt tái tạo |
| 123 | Presinusoidal portal hypertension | /ˌpriːˌsaɪnəˈsɔɪdəl ˈpɔːrtl ˌhaɪpərˈtɛnʃən/ | Tăng áp lực tĩnh mạch cửa trước xoang |
| 124 | Lymph nodes | /lɪmf noʊdz/ | Hạch bạch huyết |
| 125 | Benign reactive hyperplasia | /bɪˈnaɪn riˈæktɪv ˌhaɪpərˈpleɪʒə/ | Tăng sản phản ứng lành tính |
| 126 | Porta hepatis | /ˈpɔːrtə hɪˈpætɪs/ | Rốn gan |
| 127 | Lymphoma | /lɪmˈfoʊmə/ | U lympho |
| 128 | Histologic findings | /ˌhɪstəˈlɒdʒɪk ˈfaɪndɪŋz/ | Tổn thương mô học |
| 129 | Histologic staging | /ˌhɪstəˈlɒdʒɪk ˈsteɪdʒɪŋ/ | Phân giai đoạn mô học |
| 130 | Prognostic tool | /prɒɡˈnɒstɪk tuːl/ | Công cụ tiên lượng |
| 131 | Ultrasound elastography | /ˈʌltrəˌsaʊnd ɪˌlæsˈtɒɡrəfi/ | Đo độ đàn hồi gan bằng siêu âm |
| 132 | Sampling variation | /ˈsæmplɪŋ ˌvɛəriˈeɪʃən/ | Biến thiên do lấy mẫu |
| 133 | Florid lesion | /ˈflɔːrɪd ˈliːʒən/ | Tổn thương điển hình |
| 134 | Interlobular bile ducts | /ˌɪntərˈlɒbjʊlər baɪl dʌkts/ | Ống mật gian tiểu thùy |
| 135 | Ductopenia | /ˌdʌktoʊˈpiːniə/ | Giảm ống mật |
| 136 | Fibrous septa | /ˈfaɪbrəs ˈsɛptə/ | Vách xơ |
| 137 | Regenerative nodules | /rɪˈdʒɛnərətɪv ˈnɒdjuːlz/ | Nốt tái tạo |
| 138 | Paucity | /ˈpɔːsəti/ | Sự khan hiếm |
| 139 | Necroinflammatory activity | /ˈnɛkroʊ ɪnˈflæməˌtɔːri ækˈtɪvəti/ | Hoạt động hoại tử-viêm |
| 140 | Osteopenic bone disease | /ˌɒstiəˈpiːnɪk boʊn dɪˈziːz/ | Bệnh xương giảm mật độ |
| 141 | Low bone turnover | /loʊ boʊn ˈtɜːrnˌoʊvər/ | Chu chuyển xương thấp |
| 142 | Osteomalacia | /ˌɒstioʊməˈleɪʃə/ | Nhuyễn xương |
| 143 | Malabsorption | /ˌmæləbˈsɔːrpʃən/ | Kém hấp thu |
| 144 | Critical micellar concentration | /ˈkrɪtɪkəl maɪˈsɛlər ˌkɒnsənˈtreɪʃən/ | Nồng độ micelle tới hạn |
| 145 | Neutral triglycerides | /ˈnuːtrəl traɪˈɡlɪsəˌraɪdz/ | Triglyceride trung tính |
| 146 | Caloric intake | /kəˈlɔːrɪk ˈɪnˌteɪk/ | Lượng calo nạp vào |
| 147 | Night blindness | /naɪt ˈblaɪndnəs/ | Quáng gà |
| 148 | Pancreatic insufficiency | /ˌpænkriˈætɪk ˌɪnsəˈfɪʃənsi/ | Suy tụy |
| 149 | Sicca complex | /ˈsɪkə ˈkɒmplɛks/ | Phức hợp Sicca |
| 150 | Arthralgia | /ɑːrˈθrældʒə/ | Đau khớp |
| 151 | Inflammatory arthritis | /ɪnˈflæməˌtɔːri ɑːrˈθraɪtɪs/ | Viêm khớp viêm |
| 152 | Hepatomegaly | /ˌhɛpətoʊˈmɛɡəli/ | Gan to |
| 153 | Splenomegaly | /ˌspliːnoʊˈmɛɡəli/ | Lách to |
| 154 | Hyperpigmentation | /ˌhaɪpərˌpɪɡmɛnˈteɪʃən/ | Tăng sắc tố da |
| 155 | Melanin | /ˈmɛlənɪn/ | Melanin |
| 156 | Excoriations | /ɪkˌskɔːriˈeɪʃənz/ | Vết trầy xước |
| 157 | Jaundice | /ˈdʒɔːndɪs/ | Vàng da |
| 158 | Xanthelasma | /ˌzænθəˈlæzmə/ | U vàng mí mắt |
| 159 | Xanthomata | /zænˈθoʊmətə/ | U vàng |
| 160 | Hypercholesterolemia | /ˌhaɪpərkəˌlɛstərəˈliːmiə/ | Tăng cholesterol máu |
| 161 | Kayser-Fleischer rings | /ˈkaɪzər ˈflaɪʃər rɪŋz/ | Vòng Kayser-Fleischer |
| 162 | Copper retention | /ˈkɒpər rɪˈtɛnʃən/ | Ứ đọng đồng |
| 163 | Spider telangiectasias | /ˈspaɪdər tɪˌlændʒiɛkˈteɪʒəz/ | Sao mạch |
| 164 | Muscle wasting | /ˈmʌsəl ˈweɪstɪŋ/ | Teo cơ |
| 165 | Ascites | /əˈsaɪtiːz/ | Cổ trướng |
| 166 | Edema | /ɪˈdiːmə/ | Phù |
| 167 | Alkaline phosphatase (ALP) | /ˈælkəˌlaɪn ˈfɒsfəˌteɪs/ | Phosphatase kiềm |
| 168 | Aspartate aminotransferase (AST) | /əˈspɑːrteɪt əˌmiːnoʊˈtrænsfəˌreɪs/ | Aspartate aminotransferase |
| 169 | Alanine aminotransferase (ALT) | /ˈælənɪn əˌmiːnoʊˈtrænsfəˌreɪs/ | Alanine aminotransferase |
| 170 | Gamma-glutamyltranspeptidase (GGT) | /ˈɡæmə ˌɡluːtəˈmɪl trænsˈpɛptɪˌdeɪs/ | Gamma-glutamyltranspeptidase |
| 171 | Polyclonally | /ˌpɒliˈkloʊnəli/ | Đa dòng |
| 172 | High-density lipoprotein (HDL) | /haɪ ˈdɛnsəti ˌlaɪpoʊˈproʊtiːn/ | Lipoprotein mật độ cao |
| 173 | Thyroid-stimulating hormone (TSH) | /ˈθaɪrɔɪd ˈstɪmjʊˌleɪtɪŋ ˈhɔːrmoʊn/ | Hormone kích thích tuyến giáp |
| 174 | Tissue transglutaminase | /ˈtɪʃuː trænsˌɡluːˈtæmɪˌneɪs/ | Transglutaminase mô |
| 175 | Crossover syndrome | /ˈkrɔːsˌoʊvər ˈsɪndroʊm/ | Hội chứng giao thoa |
| 176 | Bile duct obstruction | /baɪl dʌkt əbˈstrʌkʃən/ | Tắc nghẽn đường mật |
| 177 | Cholangiography | /ˌkoʊlænˈdʒiɒɡrəfi/ | Chụp đường mật |
| 178 | Magnetic resonance cholangiography | /mæɡˈnɛtɪk ˈrɛzənəns ˌkoʊlænˈdʒiɒɡrəfi/ | Chụp đường mật cộng hưởng từ |
| 179 | Positive predictive value | /ˈpɒzətɪv prɪˈdɪktɪv ˈvæljuː/ | Giá trị dự báo dương tính |
| 180 | Fatty liver | /ˈfæti ˈlɪvər/ | Gan nhiễm mỡ |
| 181 | Granulomatous hepatitis | /ˌɡrænjʊˈloʊmətəs ˌhɛpəˈtaɪtɪs/ | Viêm gan u hạt |
| 182 | Vanishing bile duct syndrome | /ˈvænɪʃɪŋ baɪl dʌkt ˈsɪndroʊm/ | Hội chứng ống mật biến mất |
| 183 | Benign recurrent intrahepatic cholestasis | /bɪˈnaɪn rɪˈkɜːrənt ˌɪntrəhɪˈpætɪk ˌkoʊlɪˈsteɪsɪs/ | Ứ mật trong gan tái phát lành tính |
| 184 | Drug-induced cholestasis | /drʌɡ ɪnˈdjuːst ˌkoʊlɪˈsteɪsɪs/ | Ứ mật do thuốc |
| 185 | IgG4 disease | /aɪ dʒiː dʒiː fɔːr dɪˈziːz/ | Bệnh liên quan đến IgG4 |
| 186 | Median survival | /ˈmiːdiən sərˈvaɪvəl/ | Thời gian sống trung bình |
| 187 | Transplant-free survival | /ˈtrænsplænt friː sərˈvaɪvəl/ | Tỷ lệ sống sót không cần ghép |
| 188 | Risk stratification | /rɪsk ˌstrætɪfɪˈkeɪʃən/ | Phân tầng nguy cơ |
| 189 | Antihistamines | /ˌæntiˈhɪstəmiːnz/ | Thuốc kháng histamine |
| 190 | Opioid antagonist | /ˈoʊpiˌɔɪd ænˈtæɡənɪst/ | Chất đối kháng opioid |
| 191 | Opioidergic neurotransmission | /ˌoʊpiɔɪˈdɜːrdʒɪk ˌnjʊəroʊtrænsˈmɪʃən/ | Dẫn truyền thần kinh opioid |
| 192 | Plasmapheresis | /ˌplæzməfəˈriːsɪs/ | Lọc huyết tương |
| 193 | Molecular adsorbents recirculation system (MARS) | /məˈlɛkjʊlər ədˈsɔːrbənts ˌriːsɜːrkjʊˈleɪʃən ˈsɪstəm/ | Hệ thống tái tuần hoàn chất hấp phụ phân tử |
| 194 | Medium-chain triglycerides (MCT) | /ˈmiːdiəm tʃeɪn traɪˈɡlɪsəˌraɪdz/ | Triglyceride chuỗi trung bình |
| 195 | Pancreatic enzyme replacement | /ˌpænkriˈætɪk ˈɛnzaɪm rɪˈpleɪsmənt/ | Thay thế enzyme tụy |
| 196 | Dual x-ray absorptiometry (DXA) | /djuːəl ˈɛksˌreɪ əbˌsɔːrpˈtiɒmɪtri/ | Đo hấp thụ tia X năng lượng kép |
| 197 | Hormone replacement therapy (HRT) | /ˈhɔːrmoʊn rɪˈpleɪsmənt ˈθɛrəpi/ | Liệu pháp thay thế hormone |
| 198 | Immunosuppression | /ˌɪmjʊnoʊsəˈprɛʃən/ | Ức chế miễn dịch |
| 199 | Gastroesophageal variceal hemorrhage | /ˌɡæstroʊɪˌsɒfəˈdʒiːəl ˌværɪˈsiːəl ˈhɛmərɪdʒ/ | Xuất huyết do vỡ giãn tĩnh mạch thực quản-dạ dày |
| 200 | Hepatic encephalopathy | /hɪˈpætɪk ɛnˌsɛfəˈlɒpəθi/ | Bệnh não gan |
