[Sách dịch] Sổ tay Bệnh Gan – Handbook of Liver Disease – (C) NXB Elsevier, 2022 – Dịch và chú giải: Ths.Bs. Lê Đình Sáng
CHƯƠNG 3: Viêm gan A và Viêm gan E
Kelvin T. Nguyen, MD & Steven-Huy B. Han, MD, AGAF, FAASLD
ĐIỂM CHÍNH
|
VIRUS VIÊM GAN A
SINH HỌC PHÂN TỬ
- Được phân loại là một picornavirus, phân nhóm là thành viên duy nhất của phân lớp hepatovirus.
- Đường kính từ 27 đến 28 nm với đối xứng hình khối.
- Phân tử RNA mạch đơn, dương, thẳng, dài 7.5 kb trong một khung đọc mở.
- Một serotype ở người; ít nhất 6 genotype.
- Mặc dù được mô tả là một virus không có vỏ bọc, các bằng chứng gần đây cho thấy HAV có thể có cả dạng có vỏ bọc và không có vỏ bọc.
- Chứa một vị trí trung hòa miễn dịch trội duy nhất.
- Chứa bốn polypeptide virion chính trong một capsomere (Hình 3.1).
- Nhân lên trong bào tương của tế bào gan bị nhiễm thông qua một RNA polymerase phụ thuộc RNA; không có bằng chứng xác thực về sự nhân lên kéo dài trong ruột.
- Có khả năng kháng hóa chất và nhiệt độ cao, cho phép HAV tồn tại trong thực phẩm hoặc phân bị ô nhiễm trong nhiều tuần.
- Có thể sống sót khi tiếp xúc với mật và các chất tẩy rửa khác.
- Đã được nuôi cấy trong các dòng tế bào của người và linh trưởng không phải người.
- Không gây ra tình trạng nhiễm virus huyết kéo dài hoặc tình trạng mang virus ở ruột.
- Nhân lên trong gan và gây ra các phản ứng miễn dịch chưa được xác định.
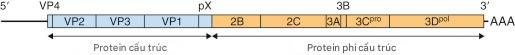
Hình 3.1 Sơ đồ tổ chức bộ gen RNA mạch đơn, dương, dài 7.5-kb của virus viêm gan A. Polyprotein gồm 2227 gốc axit amin được cấu tạo từ cả protein cấu trúc và phi cấu trúc, hai đầu được kẹp bởi các đoạn RNA không được dịch mã 5′ và 3′ chứa các yếu tố điều hòa. VP, Protein virion.
DỊCH TỄ HỌC VÀ CÁC YẾU TỐ NGUY CƠ
- Thời gian ủ bệnh: 15 đến 50 ngày (trung bình, 30 ngày).
- Phân bố trên toàn thế giới; tỷ lệ mắc mới hàng năm trên toàn cầu là 1,5 triệu ca; lưu hành cao ở các nước đang phát triển.
- Ở các nước phát triển với hệ thống nước và vệ sinh được cải thiện, phần lớn dân số đến tuổi trưởng thành mà không bị nhiễm HAV và không có miễn dịch. Ở các nước đang phát triển, những khu vực có sự phát triển kinh tế xã hội và cải thiện vệ sinh đã dẫn đến giảm lây truyền HAV và độ tuổi trung bình khi nhiễm lần đầu cao hơn, lại có sự gia tăng nghịch lý về tỷ lệ mắc HAV có triệu chứng với hậu quả nghiêm trọng hơn, chẳng hạn như viêm gan tối cấp, thời gian nằm viện kéo dài và tử vong, phản ánh mức độ nghiêm trọng gia tăng của nhiễm HAV sau thời thơ ấu (Hình 3.2).
- HAV được bài tiết qua phân của người bị nhiễm trong 1 đến 2 tuần trước và ít nhất 1 tuần sau khi khởi phát bệnh, thường ngay sau khi nồng độ alanine aminotransferase (ALT) trong huyết thanh bắt đầu tăng.
- Nhiễm virus huyết tồn tại trong thời gian ngắn, thường không quá 3 tuần nhưng đôi khi lên đến 90 ngày trong trường hợp nhiễm trùng kéo dài hoặc tái phát.
- Bài tiết qua phân kéo dài (trong nhiều tháng) được báo cáo ở trẻ sơ sinh bị nhiễm; tần suất, nồng độ virus trong phân và tầm quan trọng về mặt dịch tễ học vẫn chưa chắc chắn.
- Viêm gan A tối cấp ngày càng ít phổ biến kể từ khi có vắc-xin HAV.
- Lây truyền qua đường tiêu hóa (phân-miệng) chủ yếu xảy ra do tiếp xúc trực tiếp trong gia đình hoặc qua người chế biến thực phẩm bị nhiễm; các đợt bùng phát không thường xuyên có liên quan đến một nguồn chung:
- Thực phẩm bị ô nhiễm
- Động vật thân mềm hai mảnh vỏ
- Nước
- Các yếu tố nguy cơ nhiễm trùng khác:
- Trung tâm chăm sóc trẻ em ban ngày, trẻ em mặc tã
- Các cơ sở dành cho người khuyết tật về phát triển
- Du lịch đến các nước đang phát triển (yếu tố nguy cơ phổ biến nhất đối với người Mỹ)
- Quan hệ tình dục đường miệng-hậu môn
- Dùng chung dụng cụ hoặc ma túy ở người tiêm chích ma túy
- Không có bằng chứng về lây truyền từ mẹ sang con.
- Tỷ lệ nhiễm HAV có tương quan với tiêu chuẩn vệ sinh và quy mô hộ gia đình lớn hơn.
- Lây truyền qua truyền máu hoặc các sản phẩm từ máu là rất hiếm.
- Không xác định được yếu tố nguy cơ nào trong 30% đến 40% các trường hợp ở Hoa Kỳ.
- Tỷ lệ huyết thanh dương tính chung của nhiễm HAV ở Hoa Kỳ là <30% và đang giảm nhanh chóng với việc sử dụng mở rộng vắc-xin HAV.
- Mức độ nghiêm trọng của bệnh tăng lên ở những người có bệnh gan từ trước hoặc tuổi .
- Thụ thể tế bào HAV 1 (HAVcr1), một biến thể đa hình, có liên quan đến việc tăng nguy cơ viêm gan nặng, có thể là do virus liên kết chặt chẽ hơn với tế bào gan, cũng như tăng cường độc tính tế bào của các tế bào T diệt tự nhiên đối với các tế bào gan bị nhiễm.
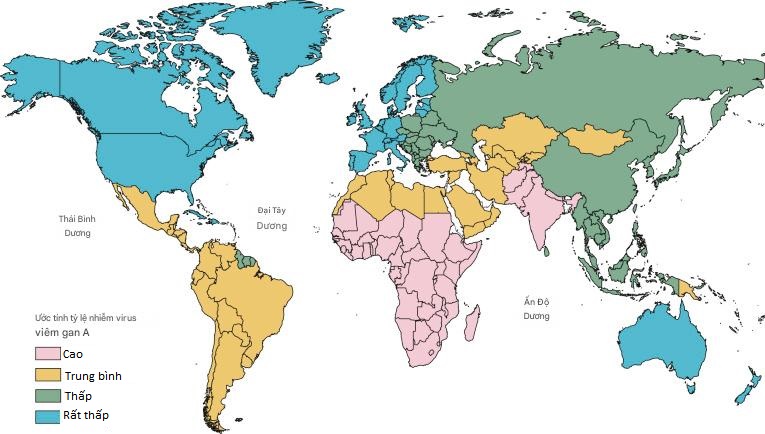
Hình 3.2 Ước tính tỷ lệ lưu hành kháng thể kháng virus viêm gan A (anti-HAV), một dấu ấn của nhiễm HAV trong quá khứ, dựa trên một tổng quan hệ thống các tài liệu từ năm 1990 đến 2005. Ngoài ra, tỷ lệ lưu hành anti-HAV có thể thay đổi trong các quốc gia theo phân nhóm dân số và địa phương. Như được sử dụng trên bản đồ này, các thuật ngữ “cao”, “trung bình”, “thấp” và “rất thấp” về mức độ lưu hành phản ánh bằng chứng có sẵn về mức độ lan rộng của nhiễm HAV trong mỗi quốc gia, thay vì các đánh giá định lượng chính xác.
SINH LÝ BỆNH
Sau khi ăn phải, HAV đi vào tuần hoàn cửa và đến gan sau khi nhân lên trong các tế bào ruột. HAV xâm nhập vào tế bào gan, nơi quá trình nhân lên tiếp theo xảy ra, dẫn đến một lượng lớn virus con được giải phóng vào mật và lòng ruột trước khi được bài tiết qua phân. Tổn thương gan xảy ra thông qua phản ứng miễn dịch của vật chủ.
ĐẶC ĐIỂM LÂM SÀNG
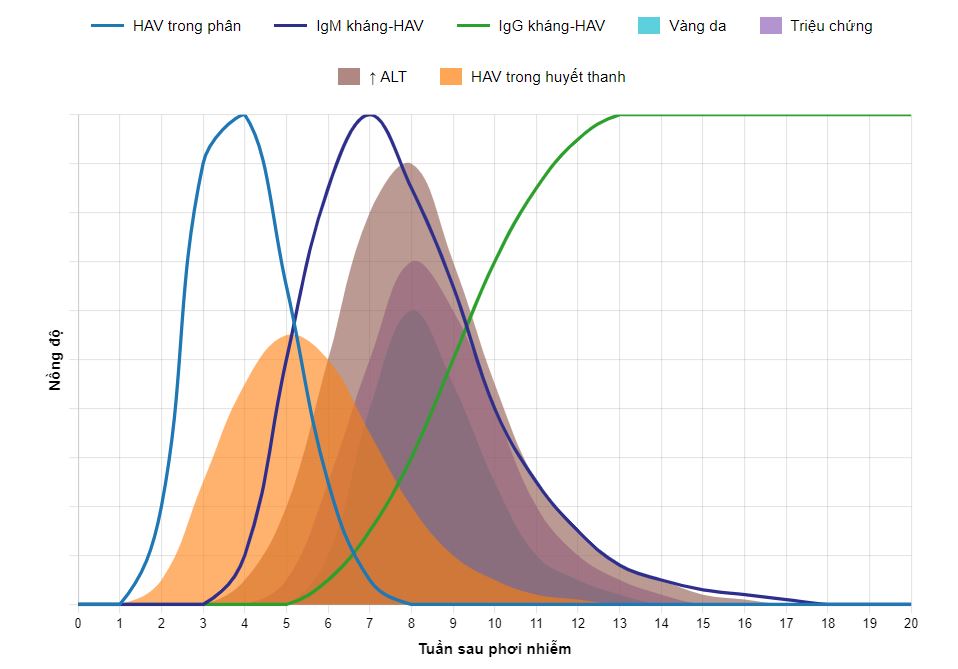
Hình 3.3 Diễn biến huyết thanh học của nhiễm virus viêm gan A.
Bệnh Tự Giới Hạn
- Mức độ nghiêm trọng của bệnh dao động từ nhiễm trùng không triệu chứng đến suy gan cấp gây tử vong; mức độ nghiêm trọng tăng lên ở những người có bệnh gan từ trước hoặc tuổi .
- Khả năng nhiễm trùng có triệu chứng tăng theo tuổi.
- Trẻ em <6 tuổi thường không có triệu chứng.
- Khả năng lây nhiễm đạt đỉnh điểm trong khoảng từ 2 tuần trước đến ít nhất 1 tuần sau khi các triệu chứng bắt đầu.
- Một số người bị nhiễm phát triển một hoặc nhiều đợt tái phát sau khi các triệu chứng ban đầu đã thuyên giảm một phần hoặc hoàn toàn. Trong quá trình tái phát, virus vẫn tiếp tục nhân lên, thường nhẹ hơn so với đợt đầu, mặc dù tình trạng ứ mật kéo dài có thể xảy ra, và cuối cùng sẽ khỏi (xem thảo luận sau trong chương).
- Sốt trong viêm gan virus cấp tính nói chung là không phổ biến, mặc dù nó có thể xảy ra trong viêm gan A cấp.
- Các triệu chứng tiền triệu giảm bớt hoặc biến mất khi bắt đầu vàng da, mặc dù chán ăn, mệt mỏi và yếu có thể kéo dài.
- Vàng da được báo hiệu bằng sự xuất hiện của nước tiểu sẫm màu và phân nhạt màu; ngứa (thường nhẹ và thoáng qua) cũng có thể xảy ra.
- Khám thực thể cho thấy gan to nhẹ và đau khi ấn.
- Lách to nhẹ và hạch bạch huyết cổ sau được ghi nhận ở 15% đến 20% bệnh nhân.
Suy Gan Cấp Xem Chương 2 để biết thông tin về suy gan cấp.
Viêm Gan Ứ Mật
- Ngứa là triệu chứng nổi bật.
- Chán ăn và tiêu chảy kéo dài có ở một vài bệnh nhân.
- Vàng da có thể kéo dài vài tháng trước khi khỏi hẳn.
- Tiên lượng rất tốt, thường khỏi hoàn toàn mà không cần điều trị đặc hiệu.
Viêm Gan Tái Phát
- Các triệu chứng và bất thường trong xét nghiệm sinh hóa gan tái phát sau vài tuần đến vài tháng sau khi hồi phục rõ ràng.
- Kháng thể Immunoglobulin (Ig)M kháng HAV (anti-HAV) có thể vẫn dương tính, và HAV có thể lại được thải ra ngoài qua phân.
- Viêm khớp, viêm mạch và cryoglobulin huyết có thể được quan sát thấy.
- Tiên lượng rất tốt với sự hồi phục hoàn toàn ngay cả sau nhiều lần tái phát (đặc biệt phổ biến ở trẻ em).
BIỂU HIỆN NGOÀI GAN
Xuất huyết nội sọ đã được báo cáo là một biến chứng của nhiễm HAV, chủ yếu do giảm tiểu cầu gây ra bởi thiếu máu bất sản. Các biến chứng khác:
- Tổn thương thận cấp
- Hội chứng thực bào máu
- Bất sản hồng cầu đơn thuần
- Viêm mạch với các biểu hiện ở da
- Viêm khớp
- Thiếu máu tan máu tự miễn
- Hội chứng Guillain-Barré
- Viêm màng ngoài tim
- Cryoglobulin huyết
- Bệnh lý tủy sống
- Viêm đơn dây thần kinh
- Viêm màng não-não
- Viêm tụy cấp
ĐẶC ĐIỂM CẬN LÂM SÀNG
Bệnh Tự Giới Hạn
- Đặc điểm sinh hóa nổi bật nhất: Tăng rõ rệt nồng độ ALT và aspartate aminotransferase (AST) trong huyết thanh.
- Nồng độ aminotransferase (ALT và AST) đỉnh dao động từ 500 đến 5000 U/L; nồng độ ALT thường cao hơn nồng độ AST.
- Nồng độ bilirubin huyết thanh hiếm khi , trừ trường hợp bệnh nặng, suy gan cấp và viêm gan ứ mật.
- Nồng độ phosphatase kiềm trong huyết thanh bình thường hoặc tăng nhẹ.
- Thời gian prothrombin bình thường hoặc tăng từ 1 đến 3 giây.
- Nồng độ albumin huyết thanh bình thường hoặc giảm nhẹ.
- Công thức máu ngoại vi bình thường hoặc có giảm bạch cầu nhẹ, có hoặc không có tăng lympho bào tương đối.
Suy Gan Cấp Xem Chương 2 để biết thông tin về suy gan cấp.
Bệnh Ứ Mật
- Nồng độ bilirubin huyết thanh có thể vượt quá .
- Nồng độ aminotransferase huyết thanh gần như bình thường mặc dù có ứ mật.
- Tăng phosphatase kiềm huyết thanh ở các mức độ khác nhau.
- Albumin huyết thanh bình thường hoặc gần như bình thường.
- Thời gian prothrombin kéo dài, nếu có, thường đáp ứng với việc sử dụng vitamin K.
Viêm Gan Tái Phát
- Sau khi nồng độ aminotransferase và bilirubin huyết thanh trở về bình thường hoặc gần bình thường trong giai đoạn hồi phục, các nồng độ này có thể tăng trở lại.
- Hiếm khi, nồng độ đỉnh có thể vượt quá nồng độ của đợt bệnh ban đầu.
MÔ HỌC
Sinh thiết gan hiếm khi được thực hiện trong nhiễm HAV cấp tính tự giới hạn.
Bệnh Tự Giới Hạn
- Tổn thương tế bào gan chính
- Hoại tử tế bào gan khu trú
- Mất tế bào gan (cell dropout)
- Thoái hóa bóng
- Chết theo chương trình với các thể Councilman (tế bào gan bị hoại tử, hyalin hóa, xác ướp bị đẩy vào xoang gan)
- Viêm nội tĩnh mạch ảnh hưởng đến tĩnh mạch trung tâm.
- Thâm nhiễm tế bào đơn nhân lan tỏa (tế bào CD8+ và tế bào diệt tự nhiên)
- Trong các khoảng cửa mở rộng
- Xói mòn từng đoạn của tấm giới hạn
- Trong nhu mô gan
- Các tế bào Kupffer to ra, tăng sản và chứa sắc tố lipofuscin và mảnh vụn; có thể thấy các tàn dư của tế bào gan bị tổn thương.
Bệnh Ứ Mật
- Thoái hóa và viêm tế bào gan, như trong viêm gan tự giới hạn.
- Nổi bật là các nút mật trong các tiểu quản mật bị giãn và nhuộm bilirubin ở các tế bào gan.
- Các tế bào gan tạo thành nhiều cấu trúc giống ống nằm rải rác (biến đổi giả tuyến).
Viêm Gan Tái Phát Các thay đổi tương tự như trong bệnh tự giới hạn.
CHẨN ĐOÁN
Để chẩn đoán huyết thanh học, xem Bảng 3.1 và Hình 3.3.
- IgM anti-HAV được phát hiện trong giai đoạn cấp tính và trong 3 đến 6 tháng sau đó, và hiếm khi kéo dài đến 24 tháng.
- Sự hiện diện của IgG anti-HAV mà không có IgM anti-HAV cho thấy đã từng nhiễm (đã khỏi) hoặc đã tiêm vắc-xin trước đó.
ĐIỀU TRỊ
Bệnh Tự Giới Hạn
- Chăm sóc hỗ trợ tại cơ sở ngoại trú thường là đủ, trừ khi nôn ói dai dẳng hoặc chán ăn nghiêm trọng dẫn đến mất nước và cần nhập viện.
- Duy trì đủ lượng calo và chất lỏng là rất quan trọng:
- Không có khuyến nghị chế độ ăn uống cụ thể.
- Khuyến khích ăn bữa sáng thịnh soạn, thường là bữa ăn dễ dung nạp nhất ở bệnh nhân viêm gan cấp.
- Cấm sử dụng rượu trong giai đoạn cấp tính.
- Nên tránh hoạt động thể chất mạnh hoặc kéo dài.
- Việc hạn chế các hoạt động hàng ngày và nhu cầu nghỉ ngơi được xác định bởi mức độ mệt mỏi và khó chịu của bệnh nhân.
- Tất cả các loại thuốc không thiết yếu nên được ngưng sử dụng.
Suy Gan Cấp (xem Chương 2)
- N-acetylcysteine đường tĩnh mạch có thể có lợi nếu được dùng sớm sau khi nhập viện; glucocorticoid không có giá trị.
- Các phương pháp điều trị tiềm năng cho nhiễm HAV cần được nghiên cứu thêm. Hai loại là thuốc kháng virus tác động trực tiếp (DAA) và các tác nhân nhắm vào vật chủ (HTA). Có thể có tác dụng hiệp đồng giữa hai nhóm thuốc này. Các mục tiêu thuốc tiềm năng trong bộ gen HAV bao gồm:
- DAA, chẳng hạn như thuốc ức chế protease và thuốc ức chế vị trí xâm nhập ribosome nội tại (IRES).
- HTA, chẳng hạn như alpha interferon, gamma interferon, interferon-lambda 1, ribavirin, amantadine, và các tác nhân chống lại các enzyme chủ chốt hoặc các yếu tố tế bào của vật chủ.
Viêm Gan Ứ Mật
- Diễn biến bệnh có thể được rút ngắn bằng cách điều trị với prednisone hoặc axit ursodeoxycholic, nhưng không có thử nghiệm lâm sàng nào về hiệu quả để hỗ trợ giả định này.
- Ngứa có thể được cải thiện bằng các chất cô lập axit mật như cholestyramine.
Viêm Gan Tái Phát
Việc quản lý giống hệt như nhiễm HAV tự giới hạn.
PHÒNG NGỪA
Dự phòng miễn dịch là nền tảng.
- Dự phòng miễn dịch trước phơi nhiễm
a. Vắc-xin HAV bất hoạt
* Hiệu quả cao (tỷ lệ hiệu quả, 95% đến 100%); đã được chứng minh là có hiệu quả như vắc-xin virus sống giảm độc lực. Một nghiên cứu đã chỉ ra rằng một hoặc hai liều vắc-xin bất hoạt đạt được 93% đến 100% bảo vệ huyết thanh so với 65% với một liều vắc-xin HAV sống giảm độc lực.
* Tính sinh miễn dịch cao (gần 100% ở đối tượng khỏe mạnh).
* Kháng thể bảo vệ được tạo ra sau 15 ngày kể từ liều đầu tiên ở 85% đến 90% người nhận.
* An toàn, dung nạp tốt.
* Thời gian bảo vệ ước tính là 20 đến 50 năm, có thể là suốt đời.
* Anti-HAV tồn tại trong 11 năm sau một liều duy nhất vắc-xin HAV bất hoạt.
* Đau tại chỗ tiêm là tác dụng ngoại ý chính.
b. Liều lượng và lịch tiêm vắc-xin HAV bất hoạt (HAVRIX và VAQTA)
* Người lớn từ 19 tuổi trở lên: Phác đồ hai liều (1440 đơn vị ELISA) của HAVRIX (Glaxo-SmithKline), với liều thứ hai cách liều đầu từ 6 đến 12 tháng; hoặc phác đồ hai liều (50 U) của VAQTA (Merck), với liều thứ hai cách liều đầu từ 6 đến 18 tháng.
* Trẻ em >12 tháng tuổi: Phác đồ hai liều HAVRIX (720 đơn vị ELISA), với liều thứ hai cách liều đầu từ 6 đến 12 tháng; hoặc phác đồ hai liều (25 U) của VAQTA, với liều thứ hai cách liều đầu từ 6 đến 18 tháng.
c. Chỉ định tiêm vắc-xin HAV bất hoạt
* Tất cả trẻ em bắt đầu từ 12 đến 23 tháng tuổi.
* Khách du lịch đến các khu vực có nguy cơ cao (đối với những người khởi hành ngay lập tức, globulin miễn dịch có thể được tiêm đồng thời, tại một vị trí khác, mặc dù chỉ tiêm vắc-xin cũng có thể đủ). Chỉ có 26,6% khách du lịch đến các quốc gia có tỷ lệ lưu hành HAV cao hoặc trung bình hiện đang được tiêm vắc-xin HAV.
* Nam giới đồng tính, song tính và thanh thiếu niên.
* Người tiêm chích ma túy.
* Người bản địa châu Mỹ.
* Trẻ em và thanh niên trong các đợt bùng phát dịch trong cộng đồng.
* Trẻ em ở các vùng, quận và tiểu bang có tỷ lệ tấn công HAV cao hơn mức trung bình toàn quốc.
* Bệnh nhân có bệnh gan mạn tính.
* Bệnh nhân bị rối loạn đông máu.
* Nhân viên phòng thí nghiệm xử lý HAV.
* Người chế biến thực phẩm khi việc tiêm chủng được các quan chức y tế địa phương coi là hiệu quả về chi phí.
* Những người tiếp xúc trong gia đình với trẻ được nhận nuôi từ các vùng lưu hành dịch.
* Nhân viên tại các trung tâm chăm sóc trẻ em ban ngày và công nhân xử lý nước thải. - Dự phòng miễn dịch sau phơi nhiễm
- Vắc-xin HAV trong bối cảnh sau phơi nhiễm có hiệu quả như globulin miễn dịch nếu được tiêm trong vòng 2 tuần kể từ khi bắt đầu phơi nhiễm cho những người từ 2 đến 40 tuổi; có lẽ nó cũng có hiệu quả ở các đối tượng trẻ hơn và lớn tuổi hơn, nhưng nó chưa được nghiên cứu ở các nhóm này.
- Miễn dịch do vắc-xin tạo ra kéo dài hơn; do đó, tiêm vắc-xin được ưu tiên hơn so với việc sử dụng globulin miễn dịch.
- Liều vắc-xin thứ hai nên được tiêm sau 6 đến 18 tháng để cung cấp sự bảo vệ kéo dài.
- Hiệu quả của globulin miễn dịch đã được xác định rõ, nhưng sự sẵn có còn hạn chế và nó chỉ cung cấp sự bảo vệ ngắn hạn.
- Lịch và liều globulin miễn dịch:
- trọng lượng cơ thể, tiêm bắp cơ delta, càng sớm càng tốt sau khi phơi nhiễm.
- Dung nạp tốt; đau tại chỗ tiêm là tác dụng ngoại ý chính.
- Chỉ định: Những người tiếp xúc trong gia đình và thân mật với những người bị nhiễm HAV cấp tính từ chối hoặc không thể tiêm vắc-xin HAV.
- Ngoài việc tiêm vắc-xin, các biện pháp chung khác để bảo vệ chống lại phơi nhiễm với viêm gan virus đường ruột bao gồm đun nóng thực phẩm đến C, sử dụng thuốc tẩy gia dụng để khử trùng, rửa tay, tránh thực phẩm chưa nấu chín hoặc nấu chưa kỹ, xử lý chất thải của con người đúng cách và đảm bảo an toàn nguồn nước.
VIRUS VIÊM GAN E
SINH HỌC PHÂN TỬ
- Được phân loại trong họ Hepeviridae, phân nhóm là một hepevirus. Bệnh do nó gây ra trước đây được gọi là “viêm gan không A, không B lây truyền qua đường ruột”, nay được gọi là viêm gan E theo thứ tự bảng chữ cái của việc phát hiện các loại viêm gan virus; chữ “e” cũng phản ánh bệnh “dịch tễ” (epidemic) và “đặc hữu” (endemic). Hepeviridae, ngoài HEV ở người, còn bao gồm các virus lây nhiễm cho lợn, thỏ, chuột, hươu, nai và cầy mangut và HEV gia cầm xa hơn. Các chủng HEV ở người và lợn có phản ứng chéo huyết thanh học đáng kể.
- Đường kính từ 27 đến 34 nm.
- Phân tử RNA thẳng, dài 7.2 đến 7.4 kb.
- Bộ gen RNA với ba khung đọc mở chồng chéo mã hóa các protein cấu trúc và protein phi cấu trúc liên quan đến sự nhân lên của HEV (Hình 3.4):
- RNA polymerase phụ thuộc RNA (RNA replicase)
- Helicase
- Cysteine protease
- Methyltransferase
- Chỉ có một serotype ở người được xác định; bốn genotype chính.
- Vị trí trung hòa miễn dịch trội trên protein cấu trúc được mã hóa bởi một khung đọc mở thứ hai.
- Có thể được nuôi cấy trong các dòng tế bào ung thư biểu mô tế bào gan người được chuyển nạp và trong các tế bào lưỡng bội phổi của phôi người.
- Có thể sống sót khi tiếp xúc với mật và các chất tẩy rửa khác.
- Được thải ra trong phân và lây truyền qua nước và thực phẩm bị ô nhiễm.
- HEV có thể tiến triển thành bệnh gan mạn tính, mặc dù hiếm.
- Nhân lên trong gan và gây ra các phản ứng miễn dịch chưa được xác định.
- Có thể tồn tại một loại virus viêm gan thứ ba lây truyền qua đường ruột có khả năng lây nhiễm cho tinh tinh.
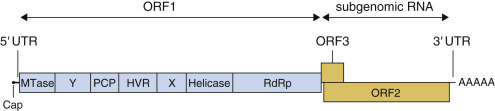
Hình 3.4 Tổ chức bộ gen của virus viêm gan E (HEV). Các protein phi cấu trúc được dịch mã từ ORF1 trong khi các protein cấu trúc ORF2 và ORF3 được dịch mã từ một RNA dưới bộ gen duy nhất. HVR, vùng siêu biến; MTase, methyltransferase; ORF, khung đọc mở; PCP, protease cysteine giống papain; RdRp, polymerase phụ thuộc RNA; UTR, vùng không được dịch mã; X, miền macro; Y, miền Y.
DỊCH TỄ HỌC VÀ CÁC YẾU TỐ NGUY CƠ
- Được mô tả lần đầu tiên vào năm 1978 trong một trận dịch viêm gan ở Thung lũng Kashmir, Ấn Độ. Ước tính có khoảng 52.000 trường hợp viêm gan vàng da đã được báo cáo, dẫn đến 1.700 ca tử vong.
- Thời gian ủ bệnh: Khoảng 40 ngày (dao động, 15 đến 65 ngày).
- Phân bố rộng rãi; dữ liệu huyết thanh học cho thấy một phần ba dân số thế giới đã bị nhiễm HEV, dẫn đến tỷ lệ tử vong hàng năm khoảng 70.000 người; tỷ lệ huyết thanh dương tính trong dân số Hoa Kỳ thấp hơn so với các báo cáo trước đây.
- HEV RNA có mặt trong huyết thanh và phân trong giai đoạn cấp tính. Việc thải virus qua phân xảy ra từ 1 đến 2 tuần trước và 2 đến 4 tuần sau khi khởi phát các triệu chứng.
- Dạng viêm gan lẻ tẻ phổ biến nhất ở thanh niên ở các nước đang phát triển.
- Các đợt bùng phát chủ yếu qua đường nước ở châu Á, châu Phi và Trung Mỹ.
- Các ca bệnh trong gia đình và thứ phát không phổ biến.
- Lây truyền từ mẹ sang con đã được ghi nhận.
- Tại Hoa Kỳ, các trường hợp đã được báo cáo ở những du khách trở về và những người nhập cư gần đây từ các vùng lưu hành dịch; các trường hợp lẻ tẻ, hiếm gặp về lây truyền từ các sản phẩm thịt lợn, gan và các loại nội tạng khác nấu chưa kỹ, động vật có vỏ, và thịt nai hoặc qua truyền máu đã được báo cáo.
- Nhiễm virus huyết hoặc thải qua phân kéo dài là không bình thường; việc thải virus liên tục có thể xảy ra trong những trường hợp hiếm gặp ở những người nhận tạng mà nhiễm HEV mạn tính được công nhận.
- Genotype 1 và 2 đã được phân lập từ các trường hợp lẻ tẻ ở người và các đợt bùng phát qua đường nước; genotype 3 và 4 đã được phân lập từ lợn và các động vật khác, bao gồm lợn rừng và hươu/nai, và rõ ràng lây truyền từ động vật sang người (Hình 3.5).
- Các mô hình dịch tễ học khác biệt được quan sát thấy ở các vùng lưu hành cao như các nước nhiệt đới và cận nhiệt đới ở châu Á, châu Phi và Trung Mỹ và các vùng không lưu hành như Hoa Kỳ, Tây Âu và các nước phát triển của khu vực châu Á-Thái Bình Dương (Bảng 3.2).
- Ở các nước phát triển, các yếu tố nguy cơ nhiễm HEV bao gồm tiêu thụ gan hoặc thịt nhiều hơn một lần một tháng, giới tính nam, dân tộc da trắng không phải gốc Tây Ban Nha, cư trú ở một số khu vực địa lý nhất định và nuôi thú cưng.
- Các yếu tố nguy cơ nhiễm HEV mạn tính là tiêu thụ thịt thú săn và ức chế miễn dịch điều trị ở những người nhận tạng. Giảm liều trong liệu pháp ức chế miễn dịch có thể đẩy nhanh quá trình thanh thải virus.
- Đặc điểm của từng genotype được mô tả trong Bảng 3.3.
- Một trường hợp lây truyền qua người hiến tạng đã được báo cáo.
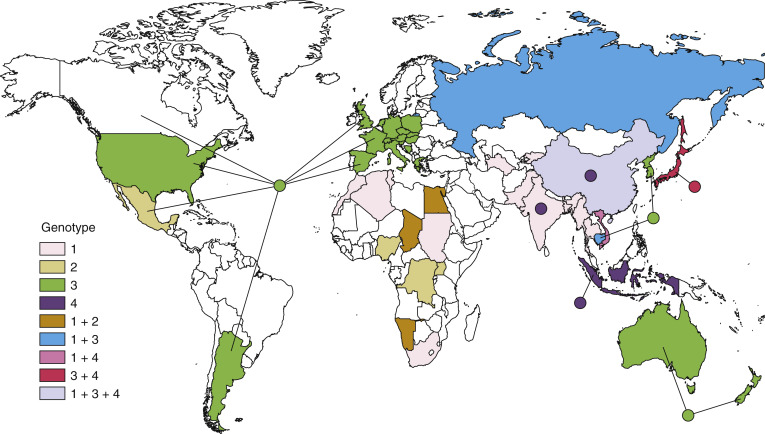
Hình 3.5 Sự phân bố các genotype của virus viêm gan E (HEV) trong các mẫu virus được lấy từ người và động vật (chủ yếu là lợn). Màu sắc được sử dụng cho một quốc gia và vòng tròn liên quan đến nó đại diện cho các genotype HEV chiếm ưu thế của các mẫu phân lập từ người và động vật, tương ứng, từ quốc gia đó.
SINH LÝ BỆNH
- Sau khi ăn phải, HEV đi vào tuần hoàn cửa (tương tự HAV). HEV RNA có thể được phát hiện trong huyết thanh, mật và phân trước khi nồng độ aminotransferase trong huyết thanh tăng. Kháng nguyên HEV có thể được chứng minh trong tế bào gan 7 ngày sau khi nhiễm, với sự lây lan nhanh chóng đến 70% đến 90% tế bào gan.
- Tổn thương tế bào gan là do phản ứng miễn dịch của vật chủ. Tỷ lệ tử vong gia tăng liên quan đến thai kỳ được cho là do phản ứng tế bào T hỗ trợ loại 2 tăng cường.
ĐẶC ĐIỂM LÂM SÀNG
Bệnh Tự Giới Hạn
- Ở các vùng lưu hành cao, nhiều bệnh nhân không nhớ lại cơn viêm gan cấp ban đầu, cho thấy nhiễm HEV phần lớn có thể không có triệu chứng.
- Đáp ứng huyết thanh học là kháng thể IgM ban đầu kháng HEV (anti-HEV), sau đó là đáp ứng IgG anti-HEV. Nồng độ IgM anti-HEV giảm dần sau 4 đến 6 tháng, mặc dù IgG anti-HEV tồn tại trong thời gian dài hơn; hiệu quả bảo vệ lâu dài của huyết thanh dương tính IgG anti-HEV là không rõ ràng (Hình 3.6).
- Các hội chứng lâm sàng do HEV gây ra tương tự như các loại viêm gan virus khác, bắt đầu bằng các triệu chứng toàn thân và tiêu hóa không đặc hiệu:
- Mệt mỏi, chán ăn, buồn nôn và nôn
- Các triệu chứng giống cúm bao gồm viêm họng, ho, sổ mũi, sợ ánh sáng, đau đầu và đau cơ
- Mất ham muốn uống rượu hoặc hút thuốc
- Các triệu chứng có xu hướng khởi phát đột ngột.
- Sốt, mặc dù không phổ biến, có thể xảy ra. Các triệu chứng tiền triệu giảm bớt hoặc biến mất khi bắt đầu vàng da, mặc dù chán ăn, mệt mỏi và yếu có thể kéo dài.
- Vàng da được báo hiệu bằng sự xuất hiện của nước tiểu sẫm màu và phân nhạt màu; ngứa (thường nhẹ và thoáng qua) cũng có thể xảy ra. Khám thực thể cho thấy gan to nhẹ và đau khi ấn.
- Lách to nhẹ và hạch bạch huyết cổ sau được ghi nhận ở 15% đến 20% bệnh nhân.
- Các biểu hiện ngoài gan có thể xảy ra như đối với nhiễm HAV (xem ở trên).
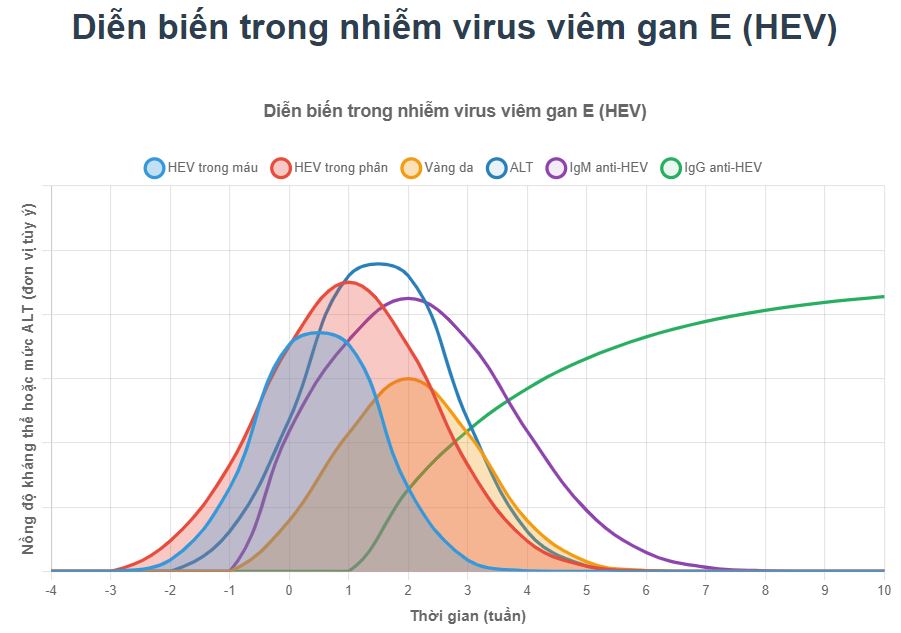
Hình 3.6 Các sự kiện trong quá trình nhiễm virus viêm gan E (HEV). Diễn biến của một ca nhiễm HEV điển hình được thể hiện trước và sau các triệu chứng bao gồm vàng da và tổn thương gan (đo bằng sự gia tăng ALT). Thời gian nhiễm virus huyết (HEV trong máu), thải virus (HEV trong phân) và các đáp ứng anti-HEV được hiển thị.
Suy Gan Cấp (xem Chương 2)
- Một tần suất cao, gần 10% đến 20%, được thấy ở phụ nữ mang thai bị nhiễm HEV, đặc biệt là trong ba tháng cuối của thai kỳ; dẫn đến tỷ lệ tử vong cao ở mẹ và thai nhi (xem thảo luận sắp tới trong chương).
- HEV có thể gây mất bù gan ở những bệnh nhân có bệnh gan mạn tính từ trước.
VIÊM GAN E VÀ THAI KỲ
- Nhiễm HEV trong thai kỳ đặt mẹ và thai nhi vào nguy cơ cao về tử vong và bệnh tật, bao gồm sẩy thai, thai chết lưu, sinh non, và tử vong mẹ hoặc sơ sinh. Các biến chứng có xu hướng xảy ra trong ba tháng giữa và ba tháng cuối của thai kỳ.
- Tử vong ở mẹ là do suy gan cấp do virus gây ra.
- Các thai nhi bị nhiễm HEV có thể phát triển viêm gan vàng da, viêm gan không vàng da, tăng bilirubin máu, sinh non, hạ thân nhiệt và tăng đường huyết, với tỷ lệ tử vong gần 50%.
- Tỷ lệ lây truyền từ mẹ sang thai nhi dao động từ 33% đến 100%.
- Cho con bú được coi là an toàn ở những bệnh nhân không có triệu chứng. Tuy nhiên, nếu người mẹ bị viêm gan E cấp tính với tải lượng virus cao, nên thay thế bằng sữa công thức do có khả năng lây truyền cho em bé từ sữa mẹ bị nhiễm hoặc các tổn thương trên núm vú của mẹ.
VIÊM GAN E MẠN TÍNH
- Được ghi nhận ở những bệnh nhân bị suy giảm miễn dịch nhiễm HEV như người nhận tạng đặc, bệnh nhân mắc bệnh huyết học, người nhiễm virus suy giảm miễn dịch ở người, người nhận hóa trị và bệnh nhân đang điều trị ức chế miễn dịch cho các rối loạn thấp khớp.
- Nhiễm HEV mạn tính không xảy ra với genotype 1 và 2, mà chủ yếu với genotype 3.
- Tác dụng dược lý của thuốc đối với sự nhân lên của HEV là một lĩnh vực đang được tiếp tục nghiên cứu. Các loại thuốc được biết là gây ức chế sự nhân lên của HEV bao gồm ribavirin và pegylated interferon alpha (cả trong ống nghiệm và trong cơ thể sống), sofosbuvir, và axit mycophenolic (chỉ trong ống nghiệm, chưa rõ trong cơ thể sống). Các loại thuốc được biết là gây kích thích sự nhân lên của HEV bao gồm các chất ức chế mTOR (mục tiêu cơ học của rapamycin) như everolimus, rapamycin (cả trong ống nghiệm và trong cơ thể sống), và các chất ức chế calcineurin như cyclosporine và tacrolimus (chỉ trong ống nghiệm, chưa rõ trong cơ thể sống).
Đặc điểm của Viêm gan E mạn tính
- Tăng ALT và AST kéo dài.
- Bằng chứng dai dẳng về HEV RNA trong huyết thanh và/hoặc phân trong ít nhất 6 tháng.
MÔ HỌC
Sinh thiết gan hiếm khi được thực hiện trong viêm gan virus cấp tính tự giới hạn.
Bệnh Tự Giới Hạn
- Tổn thương tế bào gan chính
- Hoại tử tế bào gan khu trú
- Mất tế bào gan (cell dropout)
- Thoái hóa bóng
- Chết theo chương trình với các thể Councilman (tế bào gan bị hoại tử, hyalin hóa, xác ướp bị đẩy vào xoang gan)
- Viêm nội tĩnh mạch ảnh hưởng đến tĩnh mạch trung tâm.
- Thâm nhiễm tế bào đơn nhân lan tỏa (tế bào CD8+ và tế bào diệt tự nhiên)
- Trong các khoảng cửa mở rộng
- Xói mòn từng đoạn của tấm giới hạn
- Trong nhu mô gan
- Các tế bào Kupffer to ra, tăng sản và chứa sắc tố lipofuscin và mảnh vụn; có thể thấy các tàn dư của tế bào gan bị tổn thương.
Viêm Gan E Mạn Tính
- Viêm gan khoảng cửa với thâm nhiễm tế bào lympho dày đặc.
- Hoại tử mối gặm (viêm gan giao diện).
- Xơ hóa với khả năng tiến triển thành xơ gan.
CHẨN ĐOÁN
Để chẩn đoán huyết thanh học, xem Bảng 3.1 và Hình 3.6.
- Các phòng xét nghiệm tham chiếu hiện cung cấp xét nghiệm huyết thanh học cho HEV.
- IgM anti-HEV và IgG anti-HEV được phát hiện sớm trong nhiễm trùng.
- IgA anti-HEV có thể hữu ích cho việc chẩn đoán nhiễm HEV cấp tính ở những bệnh nhân có xét nghiệm âm tính với IgM anti-HEV.
- IgM anti-HEV có thể tồn tại ít nhất 6 tuần sau đỉnh điểm của bệnh.
- IgG anti-HEV có thể vẫn có thể phát hiện được tới 20 tháng trong nhiễm trùng tự giới hạn.
- Sự hiện diện của HEV RNA trong phân hoặc huyết thanh là để xác nhận, nhưng thường không cần thiết trừ khi nghi ngờ HEV mạn tính trong quá trình theo dõi. Vì IgM anti-HEV thiếu độ đặc hiệu, HEV RNA có thể hữu ích để xác nhận nhiễm HEV cấp tính.
- Một xét nghiệm HEV nhanh có thể cho kết quả trong vòng 1 giờ. Hai xét nghiệm nhanh cho thấy độ nhạy tương ứng là 93% đến 96%, với độ đặc hiệu là 100% cho cả hai. Các xét nghiệm này có thể hữu ích trong môi trường lâm sàng, đặc biệt đối với những bệnh nhân mắc bệnh gan mạn tính hoặc bệnh nhân mang thai cần xét nghiệm nhanh để xác định nhu cầu điều trị kháng virus khẩn cấp.
ĐIỀU TRỊ
Bệnh Tự Giới Hạn
- Chăm sóc hỗ trợ tại cơ sở ngoại trú thường là đủ, trừ khi nôn ói dai dẳng hoặc chán ăn nghiêm trọng dẫn đến mất nước và cần nhập viện.
- Duy trì đủ lượng calo và chất lỏng:
- Không có khuyến nghị chế độ ăn uống cụ thể.
- Khuyến khích ăn bữa sáng thịnh soạn, thường là bữa ăn dễ dung nạp nhất ở bệnh nhân viêm gan cấp.
- Cấm sử dụng rượu trong giai đoạn cấp tính.
- Nên tránh hoạt động thể chất mạnh hoặc kéo dài.
- Việc hạn chế các hoạt động hàng ngày và nhu cầu nghỉ ngơi được xác định bởi mức độ mệt mỏi và khó chịu của bệnh nhân.
- Tất cả các loại thuốc không thiết yếu nên được ngưng sử dụng.
Suy Gan Cấp (xem Chương 2)
- Suy gan cấp do HEV là không phổ biến ngoại trừ ở phụ nữ mang thai hoặc bệnh nhân bị xơ gan đã xác định. Tỷ lệ suy gan cấp cao tới 15% đến 25%, với tỷ lệ tử vong cao nhất ở phụ nữ mang thai trong ba tháng cuối của thai kỳ.
- Ribavirin (trong ít nhất 3 tháng) là thuốc được lựa chọn cho những bệnh nhân bị hoặc có nguy cơ cao bị suy gan cấp. Có một tác dụng hiệp đồng trong ống nghiệm giữa ribavirin và pegylated interferon alpha. Một tác dụng phụ đáng kể của ribavirin là thiếu máu nặng, trong khi interferon có thể gây ra các triệu chứng giống cúm, tác dụng phụ tâm thần kinh và thải ghép cấp tính của các tạng đặc. Cả ribavirin và pegylated interferon đều chống chỉ định ở phụ nữ mang thai do tính gây quái thai.
- Tính đến năm 2017, không có phương pháp điều trị nào được phê duyệt cho viêm gan E cấp tính, nhưng ribavirin có thể mang lại lợi ích cho những bệnh nhân có tiên lượng xấu hoặc có nguy cơ cao bị suy gan cấp, chẳng hạn như những người có bệnh gan mạn tính tiềm ẩn.
- Trong nhiễm HEV mạn tính, việc quản lý ban đầu bao gồm giảm thuốc ức chế miễn dịch, nếu có thể; nếu không, có thể sử dụng đơn trị liệu ribavirin hoặc đơn trị liệu pegylated interferon alpha trong ít nhất 3 tháng. Nếu bệnh nhân bị bùng phát, tái phát hoặc tái nhiễm, bệnh nhân có thể được điều trị lại trong một thời gian dài hơn.
- Các loại thuốc kháng HEV tiềm năng khác bao gồm các phân tử hoạt động như chất ức chế sự xâm nhập của HEV, chất ức chế RNA polymerase phụ thuộc RNA, chất ức chế methyltransferase, tham gia vào việc tạo mũ cho bộ gen RNA của virus để có khả năng lây nhiễm, chất ức chế helicase, tham gia vào việc tháo xoắn RNA trong quá trình nhân lên, và các phân tử khác nhắm vào các protein virus hoặc các yếu tố vật chủ khác. Những loại thuốc kháng virus này đang được điều tra.
PHÒNG NGỪA
- Các biện pháp chung để bảo vệ chống lại phơi nhiễm với nhiễm HEV đường ruột bao gồm đun nóng thực phẩm đến C, sử dụng thuốc tẩy gia dụng để khử trùng, rửa tay, tránh thực phẩm chưa nấu chín hoặc nấu chưa kỹ, xử lý chất thải của con người đúng cách và đảm bảo các nguồn nước an toàn.
- IgG anti-HEV có thể có tác dụng bảo vệ, nhưng hiệu quả của globulin miễn dịch chứa anti-HEV là không chắc chắn.
- Hai loại vắc-xin có hiệu quả đã được chứng minh đã được phát triển và đã trải qua thử nghiệm lâm sàng giai đoạn 3 ở Trung Quốc (vắc-xin HEV 239) và Nepal (vắc-xin 56-kD biểu hiện bằng baculovirus). Vắc-xin HEV 239 đã được cấp phép tại Trung Quốc vào năm 2012. Nó dựa trên một kháng nguyên HEV genotype 1 tái tổ hợp và đã cho thấy tỷ lệ hiệu quả từ 94% đến 100% trong việc ngăn ngừa viêm gan E có triệu chứng cấp tính. Sự bảo vệ kéo dài đến 4.5 năm. Vắc-xin này không được cấp phép trên toàn cầu. Vắc-xin có thể hữu ích cho khách du lịch từ các nước phát triển đến các khu vực có tỷ lệ lưu hành viêm gan E cao và có thể được xem xét cho những người có nguy cơ cao, chẳng hạn như phụ nữ mang thai, bệnh nhân mắc bệnh gan mạn tính hoặc bệnh nhân bị suy giảm miễn dịch.
- Vắc-xin DNA đang được điều tra. Tiêm vắc-xin dẫn đến sự tổng hợp protein gây miễn dịch trong các tế bào chủ, bắt chước sự nhiễm trùng tự nhiên và cuối cùng dẫn đến việc gây ra các đáp ứng thể dịch và tế bào.
- Phát triển globulin siêu miễn dịch nồng độ cao là một khả năng khác.
- Truyền các sản phẩm máu chưa được sàng lọc HEV cho một bệnh nhân bị suy giảm miễn dịch có liên quan đến nguy cơ nhiễm HEV mạn tính. Việc sàng lọc hệ thống các sản phẩm máu để tìm HEV nên được xem xét ở các quốc gia mà HEV là bệnh lưu hành.
Bảng 3.1 Các Kiểu Huyết Thanh Học trong Chẩn Đoán Viêm Gan A và E Cấp Tính
| Tác nhân | Giai Đoạn Cấp Tính | Giai Đoạn Hồi Phục |
|---|---|---|
| HAV | Total anti-HAV dương tính IgM anti-HAV dương tính | Xuất hiện IgG anti-HAV Biến mất IgM anti-HAV |
| HEV | IgM anti-HEV dương tính và/hoặc HEV RNA (trong phân hoặc huyết thanh) IgG anti-HEV có thể hiện diện | Mất HEV RNA; xuất hiện IgG anti-HEV Mất IgM anti-HEV |
Chú thích: HAV, Virus viêm gan A; HEV, virus viêm gan E: Ig, immunoglobulin.
Bảng 3.2 Đặc Điểm Của Nhiễm Virus Viêm Gan E ở Các Khu Vực Lưu Hành Cao và Không Lưu Hành
| Đặc điểm | Khu vực lưu hành cao | Khu vực không lưu hành |
|---|---|---|
| Bệnh ở người | Thường xuyên; cả ca bệnh lẻ tẻ và ca bệnh đặc hữu | Ca bệnh lẻ tẻ không thường xuyên |
| Ổ chứa | Chủ yếu là người; có thể là môi trường | Nghi ngờ là từ động vật (lợn, lợn rừng, và hươu/nai) |
| Đường lây truyền chính | Phân-miệng; chủ yếu qua nước bị ô nhiễm | Ăn thịt nấu chưa kỹ, có thể tiếp xúc với động vật |
| Đặc điểm người bệnh | Người trẻ, khỏe mạnh | Chủ yếu là người cao tuổi, có bệnh kèm theo |
| Bệnh ở phụ nữ có thai | Tần suất cao bệnh nặng | Không được báo cáo |
| Genotype phổ biến | 1, 2, (4) | 3, (4) |
| Nhiễm trùng mạn tính | Không được báo cáo | Có thể xảy ra ở người bị suy giảm miễn dịch |
Chú thích: Các số trong ngoặc đơn cho biết tần suất thấp.
Bảng 3.3 Virus Viêm Gan E: Genotype, Phân Bố Địa Lý, và Đặc Điểm Virus và Bệnh
| Genotype | Ổ chứa | Lây từ động vật sang người | Lây qua đường nước | Phân bố địa lý | Mức độ nặng | Mạn tính | Liên quan đến thai kỳ | Dịch |
|---|---|---|---|---|---|---|---|---|
| 1 | Người | Không | Có | Nam Á, Trung Á, Trung Quốc, châu Phi hạ Sahara | Có | Không | Gây bệnh nặng | Có |
| 2 | Người | Không | Có | Mexico, Nigeria | Có | Không | NK | Có |
| 3 | Lợn | Có | NK | Các nước công nghiệp hóa, Hoa Kỳ, Châu Âu, Nhật Bản | Không | Có | NK | Không |
| 4 | Lợn | Có | Có | Đài Loan, Nhật Bản, Trung Quốc | Không | NK | NK | Không |
Chú thích: NK, Không rõ.
Bảng Chú Giải Thuật Ngữ Y Học Anh – Việt. Chương 3. Viêm gan virus A và E
| STT | Thuật ngữ tiếng Anh | Cách phát âm (IPA) | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Hepatitis A | /ˌhɛpəˈtaɪtɪs eɪ/ | Viêm gan A |
| 2 | Hepatitis E | /ˌhɛpəˈtaɪtɪs iː/ | Viêm gan E |
| 3 | Nonenveloped | /nɒnˈɛnvələʊpt/ | Không có vỏ bọc |
| 4 | Enterically transmitted | /ɛnˈtɛrɪkəli trænsˈmɪtɪd/ | Lây truyền qua đường ruột/tiêu hóa |
| 5 | Self-limited infection | /sɛlf-ˈlɪmɪtɪd ɪnˈfɛkʃən/ | Nhiễm trùng tự giới hạn |
| 6 | Severe hepatitis | /sɪˈvɪər ˌhɛpəˈtaɪtɪs/ | Viêm gan nặng |
| 7 | Chronic hepatitis | /ˈkrɒnɪk ˌhɛpəˈtaɪtɪs/ | Viêm gan mạn tính |
| 8 | Immunosuppressed | /ˌɪmjʊnoʊsəˈprɛst/ | Suy giảm miễn dịch |
| 9 | Hepatic fibrosis | /hɪˈpætɪk faɪˈbroʊsɪs/ | Xơ hóa gan |
| 10 | Cirrhosis | /sɪˈroʊsɪs/ | Xơ gan |
| 11 | Genotypes | /ˈdʒiːnəʊtaɪps/ | Genotype, kiểu gen |
| 12 | Acute infection | /əˈkjuːt ɪnˈfɛkʃən/ | Nhiễm trùng cấp tính |
| 13 | Fecal-oral route | /ˈfiːkəl-ˈɔːrəl ruːt/ | Đường phân-miệng |
| 14 | Chronic infection | /ˈkrɒnɪk ɪnˈfɛkʃən/ | Nhiễm trùng mạn tính |
| 15 | Zoonosis | /ˌzoʊəˈnoʊsɪs/ | Bệnh lây truyền từ động vật |
| 16 | Domestic swine | /dəˈmɛstɪk swaɪn/ | Lợn nhà |
| 17 | Wild boar | /waɪld bɔːr/ | Lợn rừng |
| 18 | Wild deer | /waɪld dɪər/ | Hươu/nai hoang dã |
| 19 | Vaccination | /ˌvæksɪˈneɪʃən/ | Tiêm chủng, tiêm vắc-xin |
| 20 | Antiviral therapy | /ˌæntɪˈvaɪərəl ˈθɛrəpi/ | Liệu pháp kháng virus |
| 21 | Ribavirin | /ˌraɪbəˈvaɪərɪn/ | Ribavirin |
| 22 | Picornavirus | /pɪˈkɔːrnəˌvaɪərəs/ | Picornavirus |
| 23 | Hepatovirus | /ˌhɛpətəˈvaɪərəs/ | Hepatovirus |
| 24 | Cubic symmetry | /ˈkjuːbɪk ˈsɪmɪtri/ | Đối xứng hình khối |
| 25 | Single-stranded RNA | /ˈsɪŋɡəl-ˈstrændɪd ɑːr ɛn eɪ/ | RNA mạch đơn |
| 26 | Open reading frame | /ˈoʊpən ˈriːdɪŋ freɪm/ | Khung đọc mở |
| 27 | Serotype | /ˈsɪərəʊtaɪp/ | Serotype, kiểu huyết thanh |
| 28 | Enveloped virus | /ˈɛnvələʊpt ˈvaɪərəs/ | Virus có vỏ bọc |
| 29 | Immunodominant | /ɪˌmjuːnoʊˈdɒmɪnənt/ | Miễn dịch trội |
| 30 | Neutralization site | /ˌnjuːtrəlaɪˈzeɪʃən saɪt/ | Vị trí trung hòa |
| 31 | Virion polypeptides | /ˈvɪriɒn ˌpɒliˈpɛptaɪdz/ | Polypeptide của virion |
| 32 | Capsomere | /ˈkæpsəʊmɪər/ | Capsomere |
| 33 | Replication | /ˌrɛplɪˈkeɪʃən/ | Sự nhân lên |
| 34 | Cytoplasm | /ˈsaɪtəʊˌplæzəm/ | Bào tương |
| 35 | Infected hepatocytes | /ɪnˈfɛktɪd həˈpætəʊsaɪts/ | Tế bào gan bị nhiễm |
| 36 | RNA polymerase | /ɑːr ɛn eɪ pɒˈlɪməreɪz/ | RNA polymerase |
| 37 | Persistent replication | /pərˈsɪstənt ˌrɛplɪˈkeɪʃən/ | Sự nhân lên kéo dài |
| 38 | Intestine | /ɪnˈtɛstɪn/ | Ruột |
| 39 | Thermal resistance | /ˈθɜːrməl rɪˈzɪstəns/ | Khả năng kháng nhiệt |
| 40 | Inactivation | /ɪnˌæktɪˈveɪʃən/ | Sự bất hoạt |
| 41 | Contaminated foods | /kənˈtæmɪneɪtɪd fuːdz/ | Thực phẩm bị ô nhiễm |
| 42 | Fecal matter | /ˈfiːkəl ˈmætər/ | Phân |
| 43 | Bile | /baɪl/ | Mật |
| 44 | Detergents | /dɪˈtɜːrdʒənts/ | Chất tẩy rửa |
| 45 | Propagated | /ˈprɒpəɡeɪtɪd/ | Được nuôi cấy |
| 46 | Nonhuman primate | /nɒnˈhjuːmən ˈpraɪmeɪt/ | Linh trưởng không phải người |
| 47 | Human cell lines | /ˈhjuːmən sɛl laɪnz/ | Dòng tế bào người |
| 48 | Prolonged viremia | /prəˈlɔːŋd vaɪˈriːmiə/ | Nhiễm virus huyết kéo dài |
| 49 | Intestinal carrier state | /ɪnˈtɛstɪnəl ˈkæriər steɪt/ | Tình trạng mang virus ở ruột |
| 50 | Immune responses | /ɪˈmjuːn rɪˈspɒnsɪz/ | Phản ứng miễn dịch |
| 51 | Incubation period | /ˌɪŋkjʊˈbeɪʃən ˈpɪəriəd/ | Thời gian ủ bệnh |
| 52 | Worldwide distribution | /ˈwɜːrldwaɪd ˌdɪstrɪˈbjuːʃən/ | Phân bố trên toàn thế giới |
| 53 | Annual global incidence | /ˈænjuəl ˈɡloʊbəl ˈɪnsɪdəns/ | Tỷ lệ mắc mới hàng năm trên toàn cầu |
| 54 | Hyperendemic | /ˌhaɪpərɛnˈdɛmɪk/ | Lưu hành cao |
| 55 | Developing countries | /dɪˈvɛləpɪŋ ˈkʌntriz/ | Các nước đang phát triển |
| 56 | Sanitation systems | /ˌsænɪˈteɪʃən ˈsɪstəmz/ | Hệ thống vệ sinh |
| 57 | Immunity | /ɪˈmjuːnəti/ | Miễn dịch |
| 58 | Socioeconomic | /ˌsoʊsioʊˌiːkəˈnɒmɪk/ | Kinh tế xã hội |
| 59 | Symptomatic | /ˌsɪmptəˈmætɪk/ | Có triệu chứng |
| 60 | Fulminant hepatitis | /ˈfʊlmɪnənt ˌhɛpəˈtaɪtɪs/ | Viêm gan tối cấp |
| 61 | Alanine aminotransferase | /ˈæləniːn əˌmiːnoʊˈtrænsfəreɪz/ | Alanine aminotransferase (ALT) |
| 62 | Relapsing infection | /rɪˈlæpsɪŋ ɪnˈfɛkʃən/ | Nhiễm trùng tái phát |
| 63 | Fecal excretion | /ˈfiːkəl ɛkˈskriːʃən/ | Bài tiết qua phân |
| 64 | Neonates | /ˈniːəʊneɪts/ | Trẻ sơ sinh |
| 65 | Person-to-person spread | /ˈpɜːrsən-tə-ˈpɜːrsən sprɛd/ | Lây từ người sang người |
| 66 | Food handler | /fuːd ˈhændlər/ | Người chế biến thực phẩm |
| 67 | Bivalve mollusks | /ˈbaɪvælv ˈmɒləsks/ | Động vật thân mềm hai mảnh vỏ |
| 68 | Daycare centers | /ˈdeɪkɛər ˈsɛntərz/ | Trung tâm chăm sóc trẻ ban ngày |
| 69 | Oral-anal contact | /ˈɔːrəl-ˈeɪnəl ˈkɒntækt/ | Quan hệ tình dục đường miệng-hậu môn |
| 70 | Injection drug users | /ɪnˈdʒɛkʃən drʌɡ ˈjuːzərz/ | Người tiêm chích ma túy |
| 71 | Maternal-neonatal transmission | /məˈtɜːrnəl-ˌniːəʊˈneɪtəl trænsˈmɪʃən/ | Lây truyền từ mẹ sang con |
| 72 | Blood transfusion | /blʌd trænsˈfjuːʒən/ | Truyền máu |
| 73 | Seroprevalence | /ˌsɪərəʊˈprɛvələns/ | Tỷ lệ huyết thanh dương tính |
| 74 | Preexisting liver disease | /ˌpriːɪɡˈzɪstɪŋ ˈlɪvər dɪˈziːz/ | Bệnh gan có từ trước |
| 75 | Cellular receptor | /ˈsɛljʊlər rɪˈsɛptər/ | Thụ thể tế bào |
| 76 | Polymorphic variant | /ˌpɒliˈmɔːrfɪk ˈvɛəriənt/ | Biến thể đa hình |
| 77 | Natural killer T cells | /ˈnæʧərəl ˈkɪlər tiː sɛlz/ | Tế bào T diệt tự nhiên |
| 78 | Portal circulation | /ˈpɔːrtəl ˌsɜːrkjʊˈleɪʃən/ | Tuần hoàn cửa |
| 79 | Intestinal cells | /ɪnˈtɛstɪnəl sɛlz/ | Tế bào ruột |
| 80 | Viral progeny | /ˈvaɪərəl ˈprɒdʒəni/ | Virus con |
| 81 | Intestinal lumen | /ɪnˈtɛstɪnəl ˈluːmən/ | Lòng ruột |
| 82 | Host immune response | /hoʊst ɪˈmjuːn rɪˈspɒns/ | Phản ứng miễn dịch của vật chủ |
| 83 | Asymptomatic infection | /ˌeɪsɪmptəˈmætɪk ɪnˈfɛkʃən/ | Nhiễm trùng không triệu chứng |
| 84 | Acute liver failure | /əˈkjuːt ˈlɪvər ˈfeɪljər/ | Suy gan cấp |
| 85 | Infectivity | /ˌɪnfɛkˈtɪvəti/ | Khả năng lây nhiễm |
| 86 | Relapses | /rɪˈlæpsɪz/ | Tái phát |
| 87 | Cholestasis | /ˌkoʊlɪˈsteɪsɪs/ | Ứ mật |
| 88 | Prodromal symptoms | /proʊˈdroʊməl ˈsɪmptəmz/ | Triệu chứng tiền triệu |
| 89 | Jaundice | /ˈdʒɔːndɪs/ | Vàng da |
| 90 | Anorexia | /ˌænəˈrɛksiə/ | Chán ăn |
| 91 | Malaise | /məˈleɪz/ | Mệt mỏi, khó chịu |
| 92 | Dark urine | /dɑːrk ˈjʊərɪn/ | Nước tiểu sẫm màu |
| 93 | Pruritus | /prʊˈraɪtəs/ | Ngứa |
| 94 | Hepatomegaly | /ˌhɛpətəʊˈmɛɡəli/ | Gan to |
| 95 | Splenomegaly | /ˌspliːnoʊˈmɛɡəli/ | Lách to |
| 96 | Lymphadenopathy | /ˌlɪmfædɪˈnɒpəθi/ | Hạch to |
| 97 | Cholestatic hepatitis | /ˌkoʊlɪˈstætɪk ˌhɛpəˈtaɪtɪs/ | Viêm gan ứ mật |
| 98 | Relapsing hepatitis | /rɪˈlæpsɪŋ ˌhɛpəˈtaɪtɪs/ | Viêm gan tái phát |
| 99 | Arthritis | /ɑːrˈθraɪtɪs/ | Viêm khớp |
| 100 | Vasculitis | /ˌvæskjʊˈlaɪtɪs/ | Viêm mạch |
| 101 | Cryoglobulinemia | /ˌkraɪoʊˌɡlɒbjʊlɪˈniːmiə/ | Cryoglobulin huyết |
| 102 | Extrahepatic manifestations | /ˈɛkstrəhɪˈpætɪk ˌmænɪfɛˈsteɪʃənz/ | Biểu hiện ngoài gan |
| 103 | Intracerebral hemorrhage | /ˌɪntrəsəˈriːbrəl ˈhɛmərɪdʒ/ | Xuất huyết nội sọ |
| 104 | Aplastic anemia | /ˌeɪˈplæstɪk əˈniːmiə/ | Thiếu máu bất sản |
| 105 | Thrombocytopenia | /ˌθrɒmboʊˌsaɪtəˈpiːniə/ | Giảm tiểu cầu |
| 106 | Acute kidney injury | /əˈkjuːt ˈkɪdni ˈɪndʒəri/ | Tổn thương thận cấp |
| 107 | Hemolytic anemia | /ˌhiːməˈlɪtɪk əˈniːmiə/ | Thiếu máu tan máu |
| 108 | Guillain-Barré syndrome | /ˌɡiːlæn bɑːˈreɪ ˈsɪndroʊm/ | Hội chứng Guillain-Barré |
| 109 | Pericarditis | /ˌpɛrɪkɑːrˈdaɪtɪs/ | Viêm màng ngoài tim |
| 110 | Pancreatitis | /ˌpæŋkriəˈtaɪtɪs/ | Viêm tụy |
| 111 | Aspartate aminotransferase | /əˈspɑːrteɪt əˌmiːnoʊˈtrænsfəreɪz/ | Aspartate aminotransferase (AST) |
| 112 | Serum bilirubin | /ˈsɪərəm ˌbɪlɪˈruːbɪn/ | Bilirubin huyết thanh |
| 113 | Alkaline phosphatase | /ˈælkəlaɪn ˈfɒsfəteɪz/ | Phosphatase kiềm |
| 114 | Prothrombin time | /proʊˈθrɒmbɪn taɪm/ | Thời gian prothrombin |
| 115 | Serum albumin | /ˈsɪərəm ˈælbjʊmɪn/ | Albumin huyết thanh |
| 116 | Peripheral blood counts | /pəˈrɪfərəl blʌd kaʊnts/ | Công thức máu ngoại vi |
| 117 | Leukopenia | /ˌluːkəˈpiːniə/ | Giảm bạch cầu |
| 118 | Lymphocytosis | /ˌlɪmfoʊsaɪˈtoʊsɪs/ | Tăng lympho bào |
| 119 | Histology | /hɪˈstɒlədʒi/ | Mô học |
| 120 | Liver biopsy | /ˈlɪvər ˈbaɪɒpsi/ | Sinh thiết gan |
| 121 | Hepatocyte necrosis | /həˈpætəʊsaɪt nɛˈkroʊsɪs/ | Hoại tử tế bào gan |
| 122 | Ballooning degeneration | /bəˈluːnɪŋ dɪˌdʒɛnəˈreɪʃən/ | Thoái hóa bóng |
| 123 | Apoptosis | /ˌæpəpˈtoʊsɪs/ | Chết theo chương trình |
| 124 | Councilman-like bodies | /ˈkaʊnsəlmən-laɪk ˈbɒdiz/ | Thể giống Councilman |
| 125 | Mononuclear cell | /ˌmɒnoʊˈnjuːklɪər sɛl/ | Tế bào đơn nhân |
| 126 | Infiltrate | /ˈɪnfɪltreɪt/ | Thâm nhiễm |
| 127 | Portal tracts | /ˈpɔːrtəl trækts/ | Khoảng cửa |
| 128 | Kupffer cells | /ˈkʊpfər sɛlz/ | Tế bào Kupffer |
| 129 | Lipofuscin pigment | /ˌlaɪpəˈfjuːsɪn ˈpɪɡmənt/ | Sắc tố lipofuscin |
| 130 | Bile plugs | /baɪl plʌɡz/ | Nút mật |
| 131 | Biliary canaliculi | /ˈbɪliəri ˌkænəˈlɪkjʊlaɪ/ | Tiểu quản mật |
| 132 | Diagnosis | /ˌdaɪəɡˈnoʊsɪs/ | Chẩn đoán |
| 133 | Serologic diagnosis | /ˌsɪərəˈlɒdʒɪk ˌdaɪəɡˈnoʊsɪs/ | Chẩn đoán huyết thanh học |
| 134 | Immunoglobulin (Ig)M | /ˌɪmjʊnoʊˈɡlɒbjʊlɪn ɛm/ | Immunoglobulin M (IgM) |
| 135 | Immunoglobulin (Ig)G | /ˌɪmjʊnoʊˈɡlɒbjʊlɪn dʒiː/ | Immunoglobulin G (IgG) |
| 136 | Treatment | /ˈtriːtmənt/ | Điều trị |
| 137 | Supportive care | /səˈpɔːrtɪv kɛər/ | Chăm sóc hỗ trợ |
| 138 | Dehydration | /ˌdiːhaɪˈdreɪʃən/ | Mất nước |
| 139 | N-acetylcysteine | /ɛn-əˌsiːtəlˈsɪstiːn/ | N-acetylcysteine |
| 140 | Glucocorticoids | /ˌɡluːkoʊˈkɔːrtɪkɔɪdz/ | Glucocorticoid |
| 141 | Direct-acting antivirals | /dɪˈrɛkt-ˈæktɪŋ ˌæntɪˈvaɪərəlz/ | Thuốc kháng virus tác động trực tiếp (DAA) |
| 142 | Protease inhibitors | /ˈproʊtiːeɪz ɪnˈhɪbɪtərz/ | Thuốc ức chế protease |
| 143 | Interferon | /ˌɪntərˈfɪərɒn/ | Interferon |
| 144 | Prednisone | /ˈprɛdnɪsoʊn/ | Prednisone |
| 145 | Ursodeoxycholic acid | /ˌɜːrsoʊdiˌɒksɪˈkoʊlɪk ˈæsɪd/ | Axit ursodeoxycholic |
| 146 | Cholestyramine | /ˌkoʊlɪˈstaɪərəmiːn/ | Cholestyramine |
| 147 | Prevention | /prɪˈvɛnʃən/ | Phòng ngừa |
| 148 | Immunoprophylaxis | /ˌɪmjʊnoʊˌproʊfɪˈlæksɪs/ | Dự phòng miễn dịch |
| 149 | Preexposure | /ˌpriːɪkˈspoʊʒər/ | Trước phơi nhiễm |
| 150 | Inactivated vaccine | /ɪnˈæktɪveɪtɪd ˌvækˈsiːn/ | Vắc-xin bất hoạt |
| 151 | Efficacy rate | /ˈɛfɪkəsi reɪt/ | Tỷ lệ hiệu quả |
| 152 | Live attenuated virus | /laɪv əˈtɛnjueɪtɪd ˈvaɪərəs/ | Virus sống giảm độc lực |
| 153 | Seroprotection | /ˌsɪərəʊprəˈtɛkʃən/ | Bảo vệ huyết thanh |
| 154 | Immunogenic | /ˌɪmjʊnoʊˈdʒɛnɪk/ | Tính sinh miễn dịch |
| 155 | Protective antibodies | /prəˈtɛktɪv ˈæntɪˌbɒdiz/ | Kháng thể bảo vệ |
| 156 | Adverse event | /ədˈvɜːrs ɪˈvɛnt/ | Tác dụng ngoại ý |
| 157 | Clotting disorders | /ˈklɒtɪŋ dɪsˈɔːrdərz/ | Rối loạn đông máu |
| 158 | Postexposure | /ˌpoʊstɪkˈspoʊʒər/ | Sau phơi nhiễm |
| 159 | Immune globulin | /ɪˈmjuːn ˈɡlɒbjʊlɪn/ | Globulin miễn dịch |
| 160 | Hepeviridae | /ˌhɛpəˈvɪrɪdeɪ/ | Họ Hepeviridae |
| 161 | Serologic cross reactivity | /ˌsɪərəˈlɒdʒɪk krɒs ˌriːækˈtɪvəti/ | Phản ứng chéo huyết thanh học |
| 162 | RNA replicase | /ɑːr ɛn eɪ ˈrɛplɪkeɪz/ | RNA replicase |
| 163 | Helicase | /ˈhiːlɪkeɪz/ | Helicase |
| 164 | Cysteine protease | /ˈsɪstiːn ˈproʊtiːeɪz/ | Cysteine protease |
| 165 | Methyltransferase | /ˌmɛθəlˈtrænsfəreɪz/ | Methyltransferase |
| 166 | Transfected | /trænsˈfɛktɪd/ | Được chuyển nạp |
| 167 | Icteric hepatitis | /ɪkˈtɛrɪk ˌhɛpəˈtaɪtɪs/ | Viêm gan vàng da |
| 168 | Waterborne outbreaks | /ˈwɔːtərbɔːrn ˈaʊtbreɪks/ | Bùng phát qua đường nước |
| 169 | Intrafamilial | /ˌɪntrəfəˈmɪliəl/ | Trong gia đình |
| 170 | Undercooked pork | /ˌʌndərˈkʊkt pɔːrk/ | Thịt lợn nấu chưa kỹ |
| 171 | Organ transplant recipients | /ˈɔːrɡən ˈtrænsplænt rɪˈsɪpiənts/ | Người nhận tạng |
| 172 | T-helper cell | /tiː-ˈhɛlpər sɛl/ | Tế bào T hỗ trợ |
| 173 | Pharyngitis | /ˌfærɪnˈdʒaɪtɪs/ | Viêm họng |
| 174 | Coryza | /kəˈraɪzə/ | Sổ mũi |
| 175 | Photophobia | /ˌfoʊtəˈfoʊbiə/ | Sợ ánh sáng |
| 176 | Myalgias | /maɪˈældʒiəz/ | Đau cơ |
| 177 | Hepatic decompensation | /hɪˈpætɪk ˌdiːkɒmpɛnˈseɪʃən/ | Mất bù gan |
| 178 | Fetal demise | /ˈfiːtəl dɪˈmaɪz/ | Thai chết lưu |
| 179 | Preterm labor | /ˌpriːˈtɜːrm ˈleɪbər/ | Sinh non |
| 180 | Anicteric hepatitis | /ˌænɪkˈtɛrɪk ˌhɛpəˈtaɪtɪs/ | Viêm gan không vàng da |
| 181 | Hyperbilirubinemia | /ˌhaɪpərˌbɪlɪruːbɪˈniːmiə/ | Tăng bilirubin máu |
| 182 | Hypothermia | /ˌhaɪpoʊˈθɜːrmiə/ | Hạ thân nhiệt |
| 183 | Hyperglycemia | /ˌhaɪpərɡlaɪˈsiːmiə/ | Tăng đường huyết |
| 184 | Hematologic diseases | /ˌhiːmətəˈlɒdʒɪk dɪˈziːzɪz/ | Bệnh huyết học |
| 185 | Chemotherapy | /ˌkiːmoʊˈθɛrəpi/ | Hóa trị |
| 186 | Rheumatologic disorders | /ˌruːmətəˈlɒdʒɪk dɪsˈɔːrdərz/ | Rối loạn thấp khớp |
| 187 | Pegylated interferon | /ˌpɛɡɪˈleɪtɪd ˌɪntərˈfɪərɒn/ | Pegylated interferon |
| 188 | Sofosbuvir | /soʊˈfɒsbjuːvɪr/ | Sofosbuvir |
| 189 | Mycophenolic acid | /ˌmaɪkoʊfɪˈnɒlɪk ˈæsɪd/ | Axit mycophenolic |
| 190 | mTOR inhibitors | /ɛmˈtɔːr ɪnˈhɪbɪtərz/ | Thuốc ức chế mTOR |
| 191 | Everolimus | /ˌɛvəˈroʊlɪməs/ | Everolimus |
| 192 | Rapamycin | /ˌræpəˈmaɪsɪn/ | Rapamycin |
| 193 | Calcineurin inhibitors | /ˌkælsɪˈnjʊərɪn ɪnˈhɪbɪtərz/ | Thuốc ức chế calcineurin |
| 194 | Cyclosporine | /ˌsaɪkloʊˈspɔːriːn/ | Cyclosporine |
| 195 | Tacrolimus | /tæˈkroʊlɪməs/ | Tacrolimus |
| 196 | Piecemeal necrosis | /ˈpiːsmiːl nɛˈkroʊsɪs/ | Hoại tử mối gặm |
| 197 | Interface hepatitis | /ˈɪntərfeɪs ˌhɛpəˈtaɪtɪs/ | Viêm gan giao diện |
| 198 | Immunoglobulin (Ig)A | /ˌɪmjʊnoʊˈɡlɒbjʊlɪn eɪ/ | Immunoglobulin A (IgA) |
| 199 | Teratogenicity | /ˌtɛrətoʊdʒəˈnɪsəti/ | Tính gây quái thai |
| 200 | Recombinant | /riːˈkɒmbɪnənt/ | Tái tổ hợp |
TÀI LIỆU THAM KHẢO
Aggarwal R, Jameel S, Hepatitis E. Hepatology. 2011;54:2218–2226.
Blasco-Perrin H, Abravanel F, Blasco-Baque V, et al. Hepatitis E, the neglected one. Liver Int. 2016;36:130–134.
Chionne P, Madonna E, Pisani G, et al. Evaluation of rapid tests for diagnosis of acute hepatitis E. J Clin Virol. 2016;78:4–8.
Debing Y, Neyts J. Antivirals strategies for hepatitis E virus. Antiviral Res. 2014;102:106–118.
FitzSimons D, Hendrickx G, Vorsters A, Van Damme P. Hepatitis A and E: update on prevention and epidemiology. Vaccine. 2010;28:583–588.
Kamar N, Garrouste C, Haagsma E, et al. Factors associated with chronic hepatitis in patients with hepatitis E virus infection who have received solid organ transplants. Gastroenterology. 2011;140:1481–1489.
Kamar N, Izopet J, Tripon S, et al. Ribavirin for chronic hepatitis E virus infection in transplant recipients. N Engl J Med. 2014;370:1111–1120.
Kanda T, Nakamoto S, Wu S, et al. Direct-acting antivirals and host targeting agents against the hepatitis A virus. J Clin Transl Hepatol. 2015;3:205–210.
Lee GY, Poovorawan K, Intharasongkroh, et al. Hepatitis E virus infection: epidemiology and treatment implications. World J Virol. 2015;4:343–355.
Liu X, Chen H, Liao Z, et al. Comparison of immunogenicity between inactivated and live attenuated hepatitis A vaccines among young adults. A 3-year follow-up study. J Infect Dis. 2015;212:1232–1236.
Shalimar S. Hepatitis E and acute liver failure in pregnancy. J Clin Exp Hepatol. 2013;3:213–224.
Vaughan G, Rossi L, Forbi J, et al. Hepatitis A virus: host interactions, molecular epidemiology and evolution. Infect Genet Evol. 2014;21:227–243.
Victor JC, Monto AS, Surdina TY, et al. Hepatitis A vaccine versus immune globulin for post-exposure prophylaxis. N Engl J Med. 2007;357:1685–1694.
Zhang J, Zhang X, Huang S, et al. Long-term efficacy of a hepatitis E vaccine. N Engl J Med. 2015;372:914–922.
Zhu F, Zhang J, Zhang X, et al. Efficacy and safety of a recombinant hepatitis E vaccine in healthy adults: a large-scale, randomized, double-blind placebo-controlled, phase 3 trial. Lancet. 2010;376:895–902.
