Ngoại khoa Căn bản: Vấn đề, Chẩn đoán và Quản lý, ấn bản thứ 7 (2026)
Essential Surgery: Problems, Diagnosis and Management, 7th Edition
Biên tập viên chính: Clive R. G. Quick, Suzanne Biers, Tan Arulampalam, Philip J. Deakin
Dịch & Chú giải: Ths.Bs. Lê Đình Sáng – (C) 2026 Elsevier Limited
CHƯƠNG 2. Quản lý thay đổi sinh lý ở bệnh nhân ngoại khoa
Managing physiological change in the surgical patient
Clive R.G. Quick, MBBS(London), FDS, FRCS(England), MS(London), MA(Cantab); Suzanne M. Biers, BSc, MBBS, MD, FRCS; Tan H.A. Arulampalam, MBBS, MD, FRCS
Essential Surgery: Problems, Diagnosis and Management, 2, 19-33
Các đáp ứng toàn thân
Các yếu tố chịu trách nhiệm cho đáp ứng toàn thân (Hộp 2.1)
Bệnh nhân ngoại khoa phải đối mặt với rất nhiều yếu tố gây stress (stressors), thách thức khả năng duy trì cân bằng sinh lý bình thường và duy trì sự sống của cơ thể. Ví dụ về các yếu tố gây stress này bao gồm:
■ Các cuộc mổ lớn: chấn thương mô; mất máu và dịch; bơm khí phúc mạc trong phẫu thuật nội soi
■ Các biến chứng liên quan đến gây mê: thiếu oxy; tụt huyết áp; tư thế (tư thế Trendelenburg đầu dốc, tư thế ghế bãi biển, tư thế nằm sấp, tư thế chân nâng cao trong giá đỡ); ức chế tim mạch
■ Đa chấn thương: bao gồm gãy xương và bỏng; chấn thương đầu, bụng và ngực
■ Các biến chứng tim mạch lớn: ví dụ, nhồi máu cơ tim, thuyên tắc phổi, đột quỵ
■ Xuất huyết và truyền dịch: bao gồm máu; các bất thường về dịch và điện giải
■ Nhiễm trùng và các đáp ứng viêm toàn thân; nhiễm trùng huyết
■ Thiếu oxy và tụt huyết áp
Khả năng cơ thể đáp ứng với các tác động toàn thân nghiêm trọng phụ thuộc vào nhiều yếu tố: dự trữ sinh lý (physiological reserve) của các hệ cơ quan quan trọng của bệnh nhân (tức là thể trạng cơ bản), loại tác động gặp phải, mức độ nghiêm trọng của rối loạn sinh lý, thời gian trì hoãn trước khi hồi sức và/hoặc độc lực của bất kỳ vi sinh vật nào liên quan và thời gian của rối loạn sinh lý. Nhiều bệnh nhân có khả năng hồi phục tốt đáng kể nếu được chăm sóc cơ bản tốt, nhưng ở một bệnh nhân dễ bị tổn thương hoặc đang xấu đi (deteriorating patient), nhiều hệ thống sinh lý có thể bị rối loạn đồng thời, gây ra một loạt các đáp ứng cân bằng nội môi (homeostatic responses) phức tạp.
HỘP 2.1 Các yếu tố chịu trách nhiệm cho đáp ứng toàn thân đối với chấn thương nặng hoặc phẫu thuật lớn
|
Nhận biết và ngăn ngừa tình trạng sinh lý xấu đi
Mục tiêu luôn là nhận biết tình trạng xấu đi từ rất sớm bằng cách theo dõi lâm sàng (clinical observation) thường xuyên và điều chỉnh sinh lý bất thường một cách nhanh chóng và chính xác để ngăn chặn các cơ chế bù trừ nội tại (intrinsic compensatory mechanisms) bị quá tải. Nếu không được điều chỉnh, sự suy giảm và suy sụp của một hệ cơ quan sẽ dẫn đến mất bù nhanh chóng của các hệ cơ quan khác và suy đa cơ quan (multiorgan failure).
Trong phẫu thuật phiên (elective surgery), nhiều đáp ứng sinh lý được thảo luận trong chương này có thể được ngăn ngừa hoặc giảm nhẹ bằng cách đánh giá và tối ưu hóa trước mổ (preoperative assessment and optimisation) kỹ lưỡng; bằng cách giảm căng thẳng tâm lý và sử dụng các kỹ thuật mổ tối ưu để giảm thiểu chấn thương mô và mất máu; bằng cách đảm bảo cung cấp oxy và quản lý huyết áp trong mổ thích hợp và bằng cách đảm bảo giảm đau sau mổ (postoperative analgesia) tốt. Duy trì oxy hóa bình thường, ngăn ngừa tụt huyết áp hoặc tăng huyết áp và ngăn ngừa nhiễm trùng là tất cả những yếu tố quan trọng trong suốt giai đoạn chu phẫu.
Tầm quan trọng của việc đánh giá lâm sàng thường xuyên bệnh nhân và theo dõi các dấu hiệu sinh tồn đều đặn không thể bị xem nhẹ. Việc sử dụng Thang điểm Cảnh báo Sớm (Early Warning Scores – EWS) của điều dưỡng có thể giúp xác định bệnh nhân đang xấu đi, nhưng trong khi EWS có thể thúc đẩy sự cần thiết phải thảo luận với đội ngũ chăm sóc tích cực, các bác sĩ cũng phải thăm khám và đánh giá bệnh nhân của mình thường xuyên.
Các chương trình phục hồi sớm
Các Chương trình Phục hồi sớm sau phẫu thuật (Enhanced Recovery After Surgery Programmes – ERAS) đã được giới thiệu, trong đó đặc biệt chú ý đến một loạt các yếu tố trước, trong và sau cuộc mổ. Các lợi ích đã được chứng minh là tích lũy được nhờ sự chú ý đến từng chi tiết nhỏ (Bảng 2.1). Danh sách các hướng dẫn của hiệp hội ERAS được cung cấp tại https://erassociety.org/guidelines/. “Phục hồi chức năng trước phẫu thuật” (Prehabilitation), bao gồm tập luyện thể chất để cải thiện dự trữ sinh lý của bệnh nhân trước khi bước vào phẫu thuật phiên lớn, cho thấy nhiều hứa hẹn trong việc cải thiện kết quả điều trị.
Các biến số riêng lẻ chịu trách nhiệm cho các đáp ứng toàn thân có khả năng quá mức đối với chấn thương nặng hoặc phẫu thuật lớn được tóm tắt trong Hộp 2.1.
Bảng 2.1 Các yếu tố trong phác đồ phục hồi sớm
| Thời điểm | Thành phần | Cơ sở/Lý do |
|---|---|---|
| Chuẩn bị từ trước | Thông tin, giáo dục và tư vấn trước mổ có cấu trúc, bao gồm đánh giá tâm lý và điều trị trầm cảm và lo âu | • Tạo kỳ vọng thực tế cho bệnh nhân
• Tạo kỳ vọng thực tế cho thân nhân • Giảm sợ hãi và lo âu |
| Ngừng hút thuốc và uống rượu quá mức | Giảm biến chứng | |
| Ngày phẫu thuật | • Giảm thiểu thời gian nhịn ăn
• Tải dịch và carbohydrate trước mổ |
• Giảm tình trạng thiếu hụt thể tích nội mạch do uống kém
• Giảm kháng insulin và cải thiện phục hồi |
| Không chuẩn bị ruột thường quy | Giảm mất nước và liệt ruột | |
| Dự phòng thuyên tắc huyết khối | Giảm các biến chứng thuyên tắc huyết khối | |
| Kháng sinh dự phòng chống nhiễm trùng trước mổ | Giảm tỷ lệ nhiễm trùng | |
| Không dùng tiền mê | Bệnh nhân tỉnh táo hơn sau mổ | |
| Trong mổ | Các thuốc mê tác dụng ngắn | Hồi phục nhanh hơn |
| Cân nhắc giảm đau vùng | Giảm nhu cầu dùng thuốc giảm đau opioid | |
| Không đặt ống dẫn lưu hoặc rút sớm | Ít khó chịu hơn và vận động tốt hơn | |
| Liệu pháp dịch truyền theo mục tiêu | Tránh quá tải nước và muối | |
| Sau mổ | Tiếp tục vô cảm vùng sau mổ | Ít khó chịu hơn và vận động tốt hơn |
| Tránh sonde dạ dày nếu có thể | Ít khó chịu hơn và vận động tốt hơn | |
| Dự đoán và điều trị buồn nôn và nôn | • Cải thiện sự thoải mái
• Quay lại ăn uống đường miệng sớm hơn và giảm liệt ruột |
|
| Tiếp tục dịch truyền theo mục tiêu | Tránh quá tải | |
| Dinh dưỡng đường miệng sớm để kích thích nhu động ruột | Cải thiện dinh dưỡng và phục hồi chức năng ruột | |
| Rút thông tiểu sớm | Cải thiện sự thoải mái và hỗ trợ vận động sớm | |
| Thuốc giảm đau không opioid (ví dụ: NSAID) | Tránh các biến chứng của opioid | |
| Vận động sớm
Giám sát thường xuyên sự tuân thủ và kết quả |
• Khôi phục sức mạnh; thay đổi áp lực lên các điểm tỳ đè
• Đảm bảo ERAS được duy trì |
|
| ERAS, Chương trình Phục hồi sớm sau phẫu thuật; NSAID, thuốc chống viêm không steroid. |
Các yếu tố gây stress ở bệnh nhân ngoại khoa
Chấn thương mô trực tiếp và gián tiếp
Tổn thương mô (dù là do phẫu thuật hay chấn thương) dẫn đến việc kích hoạt các đáp ứng cytokine tại chỗ ít nhiều tương ứng với quy mô của tổn thương. Các đáp ứng có thể bị phóng đại nếu vết thương bị nhiễm bẩn (ví dụ: với mảnh vụn, dị vật hoặc phân) hoặc nếu có thêm tình trạng thiếu máu mô (tissue ischaemia).
Giảm thể tích nội mạch
Đây là yếu tố then chốt trong việc khởi phát tình trạng sinh lý xấu đi ở nhiều hệ cơ quan. Giảm thể tích máu (Hypovolaemia) là kết quả của:
■ Mất dịch quá mức (Hộp 2.2)
■ Sự cô lập dịch ở mô kẽ dưới dạng phù nề trong các mô bị tổn thương và cũng nói chung là kết quả của các đáp ứng viêm toàn thân. Quá trình này được khuếch đại trong đáp ứng viêm toàn thân và nhiễm trùng huyết
■ Hạn chế ăn uống đường miệng trong giai đoạn chu phẫu
Giảm thể tích nội mạch kích thích hoạt động giao cảm (sympathetic activity) thông qua phản xạ thụ thể áp lực (baroreceptor reflex) nhằm cố gắng duy trì huyết áp bằng cách tăng cung lượng tim và kháng lực ngoại biên (peripheral resistance). Các cơ chế bù trừ này hiệu quả nhất ở những người trẻ, khỏe mạnh, nhưng sự mất bù (decompensation) cuối cùng ở nhóm này có thể xảy ra đột ngột và nhanh chóng. Catecholamine do hệ thần kinh giao cảm tiết ra cũng có tác dụng dị hóa (catabolic effect) sâu sắc, làm tăng chuyển hóa carbohydrate, protein và lipid. Giảm tưới máu thận trong tình trạng tụt huyết áp sẽ kích hoạt hệ renin-angiotensin-aldosterone, làm tăng tái hấp thu natri và nước ở thận nhằm nỗ lực giảm mất dịch thêm. Sự gia tăng tiết hormone chống bài niệu (antidiuretic hormone – ADH) qua trung gian trung ương thúc đẩy việc bảo tồn nước nhiều hơn.
HỘP 2.2 Các nguồn gây mất dịch quá mức ở bệnh nhân ngoại khoa
|
Ảnh hưởng của gây mê toàn thân
Tụt huyết áp khi gây mê toàn thân là phổ biến. Các thuốc mê có thể gây ức chế cơ tim (myocardial depression) trực tiếp và làm giảm cung lượng tim. Nhiều loại thuốc mê gây giãn mạch ngoại biên (peripheral dilatation), làm trầm trọng thêm tình trạng tụt huyết áp đồng thời làm cùn phản xạ thụ thể áp lực bình thường. Thông khí áp lực dương (Positive pressure ventilation) làm cản trở hồi lưu tĩnh mạch (venous return). Tư thế đầu dốc và bơm khí phúc mạc nhân tạo trong phẫu thuật nội soi ảnh hưởng thêm đến hồi lưu tĩnh mạch. Bệnh nhân lớn tuổi và bệnh nhân nặng thường có các đáp ứng đáng kể hơn với gây mê toàn thân. Nhồi máu cơ tim, thuyên tắc phổi hoặc nhiễm trùng huyết trong mổ có khả năng gây ra tình trạng xấu đi thêm của cung lượng tim.
Đau
Đau gây ra sự gia tăng tiết catecholamine và hormone vỏ thượng thận (adrenocorticotrophic hormone – ACTH). Những đáp ứng stress sinh lý này làm tăng nhu cầu oxy (oxygen demand) và khiến bệnh nhân có nguy cơ cao hơn bị các biến chứng sau mổ cùng với việc gây ra căng thẳng cảm xúc. Phong bế chu phẫu để ngăn ngừa đau, ví dụ, bằng vô cảm vùng (regional anaesthesia) như gây tê ngoài màng cứng đoạn ngực và các kỹ thuật khác, làm giảm đáng kể các tác động toàn thân bất lợi và cải thiện kết quả điều trị cho bệnh nhân.
Căng thẳng tâm lý
Căng thẳng tâm lý liên quan đến chấn thương, bệnh nặng hoặc phẫu thuật phiên có ảnh hưởng bất lợi tương tự như đau đối với chức năng giao cảm và hoạt động vùng dưới đồi (hypothalamic activity).
Mất nhiệt quá mức
Mất nhiệt có thể xảy ra trong các cuộc mổ kéo dài và sau khi bị bỏng rộng, đặc biệt là ở trẻ sơ sinh trải qua phẫu thuật. Mất nhiệt đặt ra những yêu cầu rất lớn đối với nguồn năng lượng. Gây mê và bộc lộ cơ thể trong phẫu thuật mở hạn chế khả năng duy trì nhiệt độ trung tâm (core temperature) của cơ thể. Giảm nhiệt độ trung tâm gây ức chế tim mạch, bệnh lý đông máu (coagulopathy) và tăng tỷ lệ nhiễm trùng. Trẻ sơ sinh, người lớn tuổi và những người bị bệnh nặng đặc biệt dễ bị mất nhiệt. Mất nhiệt có thể qua dẫn truyền (conduction), đối lưu (convection) và bức xạ (radiation). Các quá trình này được chống lại trong phòng mổ bằng cách tăng nhiệt độ phòng, cách nhiệt các bộ phận cơ thể bị bộc lộ, sử dụng chăn thổi khí ấm (forced-air warming blankets) và làm ấm dịch truyền tĩnh mạch.
Thay đổi đông máu
Các đáp ứng đối với tổn thương mô bao gồm việc kích hoạt các cơ chế huyết khối (thrombotic mechanisms) và ức chế quá trình tiêu sợi huyết (thrombolysis) bình thường. Do đó, bệnh nhân ở trong tình trạng tăng đông (prothrombotic state) và có nguy cơ bị huyết khối tĩnh mạch và hậu quả là thuyên tắc. Trong trường hợp xuất huyết đáng kể, các yếu tố đông máu có thể bị cạn kiệt. Đáp ứng viêm toàn thân (xem Chương 3) có thể khởi phát huyết khối nội mạch lan rộng, nhanh chóng tiêu thụ các yếu tố đông máu và thúc đẩy đông máu nội mạch lan tỏa (disseminated intravascular coagulation).
Nhịn ăn và dị hóa do stress
Bệnh nhân có bệnh lý ngoại khoa nặng thường bị suy dinh dưỡng (malnourished) trước cuộc mổ (xem phần Quản lý Dinh dưỡng ở Bệnh nhân Ngoại khoa). Bệnh nhân phẫu thuật phiên phải nhịn ăn tối thiểu 6 giờ trước mổ và thường không bắt đầu ăn trong 12 đến 24 giờ sau phẫu thuật. Tình trạng nhịn ăn có thể kéo dài vài ngày sau phẫu thuật đường tiêu hóa (gastrointestinal – GI) lớn và lâu hơn nhiều khi có các biến chứng như bục miệng nối (anastomotic breakdown) hoặc hình thành lỗ rò (fistula formation). Nhịn ăn gây ra dị hóa (catabolism) với tình trạng mất khối lượng cơ (loss of muscle mass), khiến bệnh nhân có nguy cơ cao hơn bị các biến chứng sau mổ.
Về các đáp ứng viêm toàn thân và nhiễm trùng huyết, xem Chương 3.
Các đáp ứng chuyển hóa với stress bệnh lý
Trong giai đoạn chu phẫu, đặc biệt nếu đã có phẫu thuật lớn, đa chấn thương hoặc nhiễm trùng liên quan, yếu tố then chốt trong đáp ứng sinh lý toàn thân là tăng hoạt động giao cảm với tăng catecholamine lưu hành (circulating catecholamines). Các đáp ứng cytokine báo hiệu cho các tế bào khác chuẩn bị hành động (ví dụ: bạch cầu đa nhân (polymorphs) hoặc tế bào T và B).
Sản xuất glucose được tăng lên nhờ quá trình tân tạo đường (gluconeogenesis) dưới ảnh hưởng của catecholamine và tình trạng kháng insulin (insulin resistance) tương đối phát triển, dẫn đến tăng đường huyết (hyperglycaemia). Sự gia tăng tiết ACTH, glucocorticoid (cortisol), glucagon và hormone tăng trưởng (growth hormone) góp phần vào trạng thái dị hóa chung. Những thay đổi chuyển hóa này được thể hiện trong Hình 2.1.
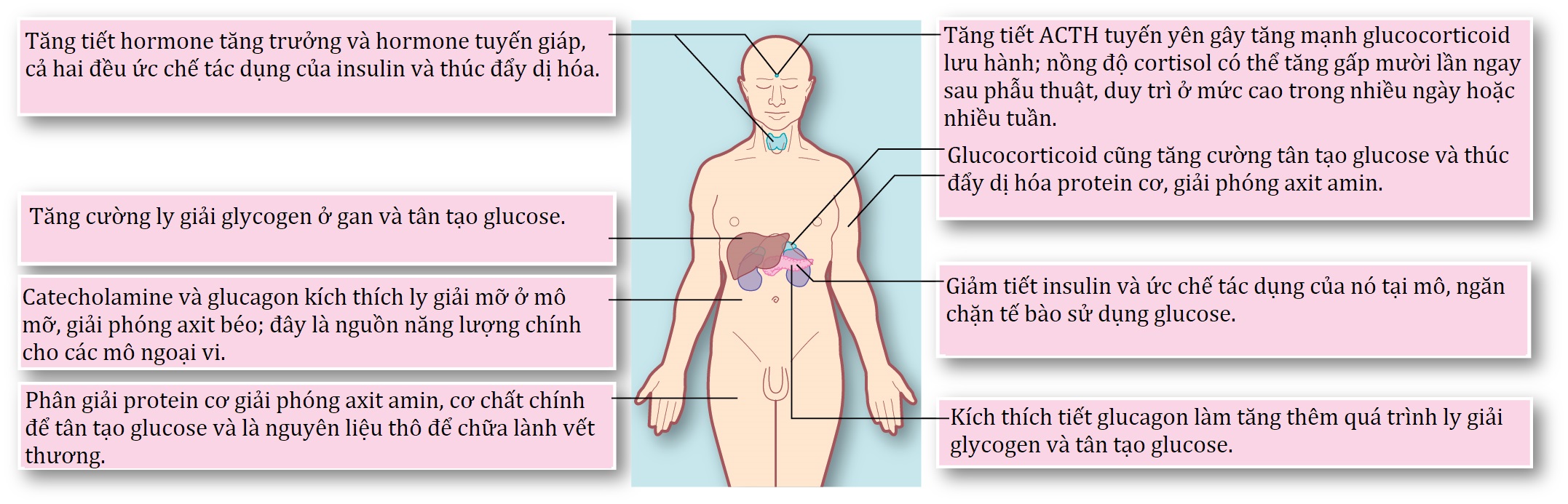
Hình 2.1: Các đáp ứng chuyển hóa với các tác động toàn thân nghiêm trọng.
Ảnh hưởng đến chuyển hóa protein, nitơ và lipid
Cân bằng nitơ (Nitrogen balance) liên tục được duy trì ở người trưởng thành khỏe mạnh bình thường. Chu chuyển protein dẫn đến việc bài tiết 12-20 g nitơ qua nước tiểu hàng ngày, được bù đắp bằng lượng hấp thu qua chế độ ăn. Trong trạng thái dị hóa, lượng nitơ mất đi có thể tăng lên đáng kể. Tình trạng cân bằng nitơ âm (negative nitrogen balance) này góp phần làm mất cơ xương.
Trong quá trình phẫu thuật và bệnh lý nặng, sự hấp thu lipid giảm và cùng với sự gia tăng ly giải mỡ (lipolysis) ở mô mỡ, điều này dẫn đến sự gia tăng các acid béo tự do (free fatty acids).
Ở bệnh nhân bị bệnh nặng, chuyển hóa carbohydrate là tối thiểu, năng lượng chủ yếu đến từ sự dị hóa protein và chất béo. Khi bắt đầu ăn trở lại, có nguy cơ xảy ra hội chứng nuôi ăn lại (refeeding syndrome), điều này cần được lường trước (xem phần Hội chứng nuôi ăn lại sau).
Quản lý dịch, điện giải và thăng bằng kiềm-toan
Giới thiệu
Các rối loạn (derangements) về dịch, điện giải và thăng bằng kiềm-toan có thể được giảm thiểu bằng cách đánh giá trước mổ chi tiết để xác định những bệnh nhân có nguy cơ phát triển rối loạn sinh lý. Theo dõi sau mổ chặt chẽ giúp xác định sớm các bất thường đang phát triển.
Ure và điện giải huyết tương (Plasma urea and electrolytes) cần được kiểm tra ít nhất hàng ngày ở những bệnh nhân trải qua phẫu thuật lớn hoặc những người đang truyền dịch tĩnh mạch.
Nói chung, những bệnh nhân không thể đáp ứng nhu cầu về dịch hoặc điện giải của họ cần liệu pháp thay thế duy trì (maintenance replacement therapy) tương đương với 25-30 mL/kg mỗi ngày nước; 1 mmol/kg mỗi ngày natri, kali và clorid; và 50-100 g/ngày glucose (lưu ý rằng glucose 5% (5% glucose) chỉ chứa 5 g glucose mỗi 100 mL).
Những bệnh nhân bị bệnh nặng có nhiễm trùng ổ bụng, nhiễm trùng huyết và lỗ rò và bệnh nhân bị bỏng nặng có khả năng gặp các vấn đề lớn về cân bằng dịch (và dinh dưỡng, xem phần Quản lý Dinh dưỡng ở Bệnh nhân Ngoại khoa sau). Những trường hợp này được quản lý tốt nhất với sự trợ giúp của các bác sĩ gây mê và hồi sức tích cực có kinh nghiệm tại các đơn vị chăm sóc tăng cường (high-dependency) hoặc điều trị tích cực (intensive care units), nơi việc theo dõi và điều trị có thể được quản lý nghiêm ngặt.
Cân bằng nội môi dịch và điện giải bình thường
Cơ thể của một người trưởng thành trung bình 70 kg chứa 42 L dịch, được phân bố giữa khoang nội bào (intracellular compartment), khoang ngoại bào (extracellular space) và trong lòng mạch (Hình 2.2). Lượng dịch nhập chủ yếu qua đường uống và thức ăn. Lưu ý rằng khoảng 200 mL/ngày nước được tạo ra trong quá trình chuyển hóa. Lượng dịch mất bình thường ở người trưởng thành là từ 2.5 đến 3 L/ngày. Khoảng 1 L bị mất một cách không nhận biết được (insensibly) qua da và phổi, 1300-1800 mL được bài tiết qua nước tiểu (khoảng 60 mL/giờ hoặc 1 mL/kg mỗi giờ) và 100 mL bị mất qua phân. Khoảng 100-150 mmol ion natri và 50-100 mmol ion kali bị mất mỗi ngày qua nước tiểu, và điều này được cân bằng bởi lượng hấp thu qua chế độ ăn bình thường (Bảng 2.2).

Hình 2.2: Phân bố dịch trong các khoang của cơ thể.
Bảng 2.2 Tóm tắt – Lượng dịch và điện giải nhập và xuất hàng ngày bình thường
| Lượng nhập hàng ngày bình thường | Lượng xuất hàng ngày bình thường | |
|---|---|---|
| Nước | Chế độ ăn 2300 mL
Chuyển hóa 200 mL |
Nước tiểu 1400 mL (thể tích bắt buộc tối thiểu 400 mL)
Mất qua da 500 mL (khuếch tán và bay hơi bắt buộc) Lưu ý: đổ mồ hôi khi sốt hoặc nhiệt độ môi trường cao có thể gây mất thêm vài lít mỗi ngày Mất qua phổi 500 mL (bắt buộc) Mất qua phân 100 mL |
| Natri | Chế độ ăn 150 mmol/ngày (khoảng 50-300 mmol) | Phân 5 mmol/ngày
Mồ hôi qua da 5 mmol/ngày (khi không đổ mồ hôi) Nước tiểu 140 mmol/ngày (có thể giảm xuống 15 mmol/ngày nếu cần) |
| Kali | Chế độ ăn 100 mmol/ngày (khoảng 50-200 mmol) | Phân 10 mmol/ngày (bắt buộc)
Da <5 mmol/ngày Nước tiểu 85 mmol/ngày (hiếm khi giảm xuống dưới 60 mmol/ngày) |
Kê toa dịch truyền tĩnh mạch để duy trì nước và natri
Đối với hầu hết bệnh nhân, nhu cầu nước và natri hàng ngày được đáp ứng tốt nhất bằng cách sử dụng số lượng cân bằng thích hợp các dung dịch tinh thể (crystalloid solutions) như nước muối sinh lý (natri clorid 0.9%) (normal saline) và dung dịch dextrose (glucose) 5%. Nước muối sinh lý chứa 154 mmol mỗi loại ion natri và clorid mỗi lít. Do đó, một lít sẽ đáp ứng nhu cầu natri hàng ngày của những bệnh nhân không có biến chứng. Nhu cầu bổ sung về nước được bù bằng 2-2.5 L glucose 5% (Hộp 2.3). Dung dịch Hartmann (Hartmann’s solution) có thể được sử dụng làm dung dịch duy nhất để truyền tĩnh mạch. Dung dịch này sinh lý hơn; nó có độ thẩm thấu tương đương với huyết tương và chứa ít clorid hơn (111 mmol/L) và một ít kali (5 mmol/L).
Nhu cầu dịch duy trì có thể dựa trên các hướng dẫn và công thức đã được công bố, ví dụ: https://www.nice.org.uk/guidance/cg174/ và https://www.mdcalc.com/maintenance-fluids-calculations
Bù kali đường tĩnh mạch
Nhu cầu kali cơ bản được đáp ứng bằng cách truyền 60-80 mmol kali clorid chia làm nhiều lần trong mỗi 24 giờ. Các loại dịch truyền tĩnh mạch pha sẵn thường có sẵn với 20 hoặc 40 mmol kali clorid mỗi 1000 mL túi truyền. Nếu cần nồng độ kali clorid lớn hơn 40 mmol trong 500 mL, chúng nên được truyền qua đường truyền tĩnh mạch trung ương tại một đơn vị chăm sóc tích cực, có theo dõi tim. Tiêm bolus kali clorid không bao giờ được thực hiện vì sự gia tăng nhanh chóng kali huyết tương có thể gây loạn nhịp tim hoặc ngưng tim (cardiac standstill).
HỘP 2.3 Ví dụ về phác đồ truyền dịch tĩnh mạch hàng ngày thay thế cho đường uống trong các trường hợp không biến chứng
Kê toa (1) trong 24 giờ (mỗi túi được truyền trong 8 giờ):
Tổng: 154 mmol natri và 60 mmol kali Kê toa (2) trong 24 giờ (mỗi túi được truyền trong 8 giờ):
Tổng: 90 mmol natri và 60 mmol kali |
Cũng tham khảo Hướng dẫn NICE CG174 về liệu pháp truyền dịch tĩnh mạch ở người lớn trong bệnh viện (https://www.nice.org.uk/guidance/cg174).
Giới hạn của các cơ chế bù trừ
Thận khỏe mạnh bình thường có thể duy trì cân bằng nội môi dịch và điện giải mặc dù có sự thay đổi lớn về lượng dịch uống vào.
Tổng thể tích máu ở nam giới trưởng thành là khoảng 5 L (70 mL/kg), trong đó khoảng 55%-60% là nước (khoảng 3.5 L). Sự giảm thể tích máu diễn ra từ từ có thể được bù đắp bằng sự di chuyển dịch từ khoang ngoại bào, có thể tích khoảng 10 L. Sự thiếu hụt hơn 3 L trong tổng thể tích dịch cơ thể không thể được duy trì, và thể tích nội mạch chắc chắn sẽ bị cạn kiệt. Điều này được phản ánh trong các thay đổi tim mạch bù trừ (xem Chương 4 về sốc giảm thể tích). Khi tổng lượng dịch thiếu hụt đạt khoảng 3 L, nhịp tim tăng lên rõ rệt và tụt huyết áp phát triển. Với sự thiếu hụt dịch ngày càng tăng, giới hạn bù trừ của tim mạch bị đạt đến, và bệnh nhân phát triển sốc giảm thể tích (hypovolaemic shock).
Ở trẻ sơ sinh, trẻ em, người lớn tuổi và bệnh nhân mắc bệnh mạn tính, khả năng bù trừ của tim mạch bị giảm đi rất nhiều, do đó sự mất cân bằng dịch và điện giải tương đối nhỏ cũng có thể gây ra các biến chứng đe dọa tính mạng.
Những thay đổi sinh lý để đáp ứng với phẫu thuật và chấn thương
Các căng thẳng của chấn thương hoặc phẫu thuật gây ra sự gia tăng catecholamine lưu hành. Stress cũng kích thích trục dưới đồi-tuyến yên-thượng thận (hypothalamic-pituitary-adrenal axis), làm tăng tiết cortisol và aldosterone. Các hormone này thúc đẩy thận bảo tồn natri và nước, gây giảm thể tích nước tiểu và nồng độ natri trong nước tiểu.
Ảnh hưởng của giảm tưới máu thận
Bất kỳ sự sụt giảm đáng kể nào về thể tích tuần hoàn hiệu dụng và tụt huyết áp đều gây ra giảm tưới máu thận. Các yếu tố bổ sung như phẫu thuật động mạch chủ liên quan đến kẹp động mạch chủ (aortic clamping), hoặc bơm khí phúc mạc trong phẫu thuật nội soi, làm tăng áp lực trong ổ bụng có thể làm thay đổi động lực học của dòng chảy động mạch thận (xem thêm phần Hội chứng khoang bụng).
Giảm tưới máu thận kích hoạt hệ renin-angiotensin-aldosterone để duy trì huyết áp bình thường. Khi lọc cầu thận giảm, renin được giải phóng từ phức hợp cận tiểu cầu (juxtaglomerular apparatus) của thận và điều này xúc tác cho việc chuyển đổi angiotensin I thành angiotensin II trong phổi. Angiotensin II có tác dụng co mạch (pressor) mạnh mẽ lên mạch máu ngoại biên, chống lại tình trạng tụt huyết áp cũng như kích thích giải phóng aldosterone từ vỏ thượng thận. Aldosterone thúc đẩy tái hấp thu chủ động các ion natri từ các ống lượn xa (distal, convoluted tubules) của thận, đi kèm với tái hấp thu thụ động nước. Tái hấp thu natri được liên kết với sự gia tăng bài tiết các ion kali và hydro.
Tác động thực tế là trong các điều kiện gây giảm tưới máu thận, lượng nước tiểu giảm đáng kể, và nước tiểu được tạo ra có nồng độ natri thấp và nồng độ ion kali và hydro cao. Mất ion hydro góp phần vào sự phát triển của nhiễm kiềm chuyển hóa (metabolic alkalosis).
Các yếu tố khác trong bảo tồn nước
Bảo tồn nước được tăng cường thêm bởi sự tiết ADH (còn được gọi là vasopressin) qua trung gian stress từ tuyến yên sau. Chỉ riêng mất nước làm tăng áp suất thẩm thấu (osmolality) huyết tương, kích thích giải phóng ADH, qua trung gian của các thụ thể thẩm thấu (osmoreceptors) ở vùng dưới đồi. ADH liên kết với các thụ thể ở ống thận xa và thúc đẩy tái hấp thu nước. Việc giải phóng ADH cũng được kích thích bởi sự sụt giảm huyết áp và thể tích, được cảm nhận bởi các thụ thể căng ở tim và các động mạch lớn. Những thay đổi về huyết áp và thể tích là những yếu tố kích thích tiết ADH kém nhạy hơn so với tăng áp suất thẩm thấu nhưng trở nên mạnh mẽ trong các rối loạn tim mạch cực đoan (ví dụ: mất hơn 15% thể tích trong xuất huyết cấp). Stress và đau cũng thúc đẩy giải phóng ADH thông qua các con đường khác của vùng dưới đồi.
Quản lý dịch và kali sau mổ
Tại vị trí chấn thương hoặc phẫu thuật lớn, dịch bị loại bỏ một cách hiệu quả khỏi tuần hoàn dưới dạng phù nề do viêm (inflammatory oedema) (mất dịch vào khoang thứ ba (third space losses) tại chỗ, đẳng trương). Thể tích bị mất này được bù đắp bằng dịch được giữ lại do kết quả của những thay đổi nội tiết tố được mô tả trước đó. Kali được giải phóng từ các tế bào bị tổn thương, và lượng này có thể vượt quá lượng bị mất do trao đổi ở thận. Điều này còn tăng thêm nếu có tình trạng thiếu máu mô tiếp diễn. Máu dự trữ để truyền có chứa nồng độ kali cao. Do đó, vì nhiều lý do, bệnh nhân sau mổ có nguy cơ bị tăng kali máu (hyperkalaemia).
Giai đoạn thiểu niệu tương đối (relative oliguria) và giữ natri bình thường được mô tả ở trên xảy ra trong tối đa 48 giờ sau chấn thương hoặc phẫu thuật lớn, và kiến thức này ảnh hưởng đến các lựa chọn quản lý dịch. Giống như các thay đổi khác trong giai đoạn chu phẫu, những ảnh hưởng này cải thiện cùng với sự phục hồi toàn diện của bệnh nhân.
Hội chứng khoang bụng
Áp lực trong ổ bụng (intra-abdominal pressure) bình thường là khoảng 5 mmHg. Hội chứng khoang bụng (Abdominal compartment syndrome) là không phổ biến, và mô tả các hậu quả sinh lý bệnh của tăng áp lực trong ổ bụng. Áp lực trong ổ bụng phụ thuộc vào dung tích của khoang bụng và độ giãn nở (compliance) của thành bụng. Do đó, bất kỳ sự gia tăng nào của các thành phần trong ổ bụng (phù nề hoặc chướng nội tạng, cổ trướng hoặc xuất huyết trong ổ bụng) hoặc giảm độ giãn nở của thành bụng (phù nề mô, bỏng hoặc đóng thành bụng nguyên phát quá chặt) đều có thể dẫn đến tăng áp lực ổ bụng (intra-abdominal hypertension). Điều này trở nên có ý nghĩa lâm sàng với áp lực >12 mmHg, và hội chứng khoang bụng xảy ra ở mức >20 mmHg. Các ảnh hưởng bất lợi bao gồm:
■ Thiểu niệu (Oliguria) do giảm tưới máu thận và tắc nghẽn đường tiểu
■ Tình trạng hô hấp xấu đi do hạn chế cử động cơ hoành (splinting of the diaphragm) và tăng bất tương xứng thông khí-tưới máu (ventilation-perfusion mismatch). Điều này dẫn đến giảm thể tích khí lưu thông, giảm oxy máu (hypoxemia) và tăng CO2 máu (hypercarbia)
■ Giảm hồi lưu tĩnh mạch và tăng kháng lực mạch máu toàn thân dẫn đến giảm cung lượng tim và tụt huyết áp
■ Giảm lưu lượng máu đến các tạng, động mạch mạc treo, gan và tĩnh mạch cửa gan dẫn đến thiếu máu cục bộ đường ruột và rối loạn chức năng gan
Ở những bệnh nhân bị chướng bụng hoặc được coi là có nguy cơ cao mắc hội chứng khoang bụng, áp lực khoang bụng cần được đo. Điều này có thể đạt được bằng cách sử dụng thông tiểu có gắn bộ chuyển đổi áp lực. Điều trị nhắm mục tiêu vào việc hạ áp lực ổ bụng và hỗ trợ các cơ quan. Điều này có thể bao gồm quản lý bảo tồn hoặc mở bụng (laparotomy) và giải nén phẫu thuật (surgical decompression) tùy thuộc vào nguyên nhân và mức độ nghiêm trọng của tăng áp lực trong ổ bụng. Thậm chí có thể phải để hở bụng cho đến khi áp lực giảm xuống.
Các vấn đề về thiếu hụt dịch và điện giải
Mất máu toàn phần hoặc huyết tương
Xuất huyết nặng (Major haemorrhage) thường được định nghĩa là mất máu vượt quá 150 mL/phút; 20% thể tích tuần hoàn trong 1 giờ; hoặc 50% thể tích tuần hoàn trong 3 giờ. Điều này làm cạn kiệt khoang nội mạch và khả năng bù trừ sinh lý, gây tụt huyết áp và sốc giảm thể tích. Thể tích tuần hoàn cần được phục hồi bằng truyền máu và thay thế các thành phần đông máu.
Nhu cầu truyền máu có thể dựa trên lượng máu mất ước tính hoặc đo được và dựa trên nồng độ hemoglobin đã biết. Mất máu cấp 500-1000 mL ở người trưởng thành có thể được điều trị bằng bù dịch bằng dung dịch tinh thể (crystalloid volume expansion). Mất máu với thể tích lớn hơn nên được thay thế bằng truyền khối hồng cầu (packed red blood cells) hoặc máu toàn phần, bổ sung thêm các thành phần đông máu. Mất máu mạn tính, chậm, ví dụ, từ loét dạ dày tá tràng hoặc nhiễm giun móc (hookworm infestation) không gây ra các vấn đề về cân bằng dịch hoặc cần truyền máu nhưng có thể gây ra các triệu chứng và dấu hiệu của thiếu máu (anaemia).
Trong bỏng nặng (severe burns), lượng huyết tương có khả năng bị mất dễ bị đánh giá thấp và cần được tính toán bằng công thức chuẩn dựa trên diện tích bị bỏng để hướng dẫn bù dịch (xem Chương 17). Bỏng nặng nên được quản lý tại các trung tâm chuyên biệt nếu có thể.
Mất dịch qua đường tiêu hóa
Hàng ngày, có từ 5 L đến 9 L dịch giàu điện giải thường được tiết vào đường tiêu hóa trên dưới dạng nước bọt, dịch vị, mật, dịch tụy và dịch ruột (succus entericus) (dịch tiết ruột non; Bảng 2.3). Hầu hết dịch được tái hấp thu bởi ruột già.
Một lượng lớn nước và điện giải có thể bị mất do Nôn, hút dịch dạ dày qua sonde, tiêu chảy, ứ đọng dịch trong ruột bị tắc hoặc mất động lực (adynamic bowel) hoặc chảy ra bên ngoài qua lỗ rò hoặc mở thông hồi tràng. Trong trường hợp viêm ruột lan rộng gây tiêu chảy như trong viêm dạ dày ruột hoặc viêm loét đại tràng, dịch tiết viêm có thể làm tăng đáng kể tổng lượng dịch bị mất.
Bệnh tả và các bệnh tiêu chảy nhiễm trùng khác có thể gây mất tới 10 L dịch giàu điện giải trong một ngày, và việc mất dịch này cùng với sự cạn kiệt thể tích nội mạch sau đó có thể gây suy đa cơ quan và tử vong, đặc biệt là ở trẻ em.
Lượng dịch mất trong bệnh viện phải được đo lường hoặc ước tính chính xác và ghi lại trên biểu đồ cân bằng dịch. Ngoài ra, cần thường xuyên theo dõi các dấu hiệu mất thể tích bao gồm nhịp tim, huyết áp, lượng nước tiểu định kỳ và, nếu cần, áp lực tĩnh mạch trung ương (CVP). Một test bù dịch (fluid challenge) thích hợp khi nghi ngờ mất thể tích là truyền nhanh (bolus) 250 mL dung dịch tinh thể và đánh giá lại các dấu hiệu đã đề cập ở trên. Doppler thực quản (Oesophageal Doppler), nếu có, có thể được sử dụng để hướng dẫn liệu pháp dịch truyền thông qua các thay đổi đo được về thể tích nhát bóp (stroke volume) để đáp ứng với một liều bolus dịch. Các biện pháp này cho phép bù dịch tĩnh mạch chính xác, và chúng ngăn ngừa các hậu quả bất lợi của việc thiếu hụt dịch và điện giải.
Từ Bảng 2.3, có thể thấy rằng chất nôn, dịch hút từ sonde dạ dày và tiêu chảy có hàm lượng natri và kali phong phú khác nhau. Nói chung, lượng dịch mất qua đường tiêu hóa nên được thay thế bằng một thể tích tương đương dung dịch tinh thể có bổ sung điện giải khi cần thiết. Trong tắc ruột hoặc liệt ruột cơ năng, dịch ứ đọng trong ruột được thay thế theo cách tương tự, mặc dù nhu cầu thể tích phải được ước tính. Đáng chú ý, các lỗ rò đường tiêu hóa và mở thông hồi tràng ra nhiều dịch (high-output ileostomies) gây mất mạn tính dịch có hàm lượng clorid và bicarbonat cao. Có thể cần lời khuyên của chuyên gia trong việc thay thế các tổn thất này.
Tích tụ dịch viêm trong ổ bụng
Viêm nặng trong ổ bụng có thể gây mất vài lít dịch giàu protein huyết tương và điện giải vào khoang phúc mạc. Điều này thường xảy ra trong viêm phúc mạc hoặc viêm tụy cấp trong bối cảnh hội chứng đáp ứng viêm toàn thân (systemic inflammatory response syndrome – SIRS). Tốt nhất nên thay thế bằng các dung dịch tinh thể, và đáp ứng sinh lý với các liều bolus dịch có thể giúp ước tính thể tích cần thiết.
Nhiễm trùng huyết
Nhiễm trùng huyết (Sepsis) liên quan đến tổn thương nội mô (endothelial damage) lan rộng và sự gia tăng lớn tính thấm mao mạch qua trung gian của một loạt các cytokine và các chất trung gian lưu hành khác. Kết quả là mất một lượng lớn dịch giàu protein và điện giải từ tuần hoàn vào khoang ngoại bào (‘mất dịch vào khoang thứ ba’), kết hợp với mất kháng lực ngoại biên, dẫn đến trụy tim mạch (cardiovascular collapse) và sốc (xem phần Nhiễm trùng huyết trong Chương 3).
Thể tích dịch cần thiết rất khó ước tính, và việc thay thế thường được đưa ra với thể tích duy trì sự ổn định tim mạch (nhịp tim và huyết áp) và lượng nước tiểu (ít nhất 0.5 mL/kg trọng lượng cơ thể mỗi giờ) đồng thời tránh quá tải dịch và suy tim. Ở bệnh nhân bị bệnh nặng, người mà nhu cầu thể tích đặc biệt khó đánh giá, nên sử dụng đường truyền CVP để cung cấp phương pháp đánh giá chính xác hơn nhu cầu bù dịch và cho phép sử dụng thuốc vận mạch (vasoactive drug) (xem phần Các chương trình phục hồi sớm; sau trong chương này và Bảng 2.1).
Mất dịch không nhận biết được bất thường
Mất dịch không nhận biết được bất thường có thể làm tăng đáng kể tổng lượng dịch mất, đặc biệt là ở bệnh nhân bị bệnh nặng hoặc bệnh nhân lớn tuổi và phải được bao gồm trong phương trình cân bằng dịch. Sốt (Pyrexia) làm tăng mất dịch không nhận biết được khoảng 20% cho mỗi độ C tăng nhiệt độ cơ thể, chủ yếu dưới dạng hơi nước thở ra và mất nhiệt qua bức xạ. Do đó, sốt 38.5^{\circ}C trong 3 ngày sẽ gây mất thêm một lít dịch. Đổ mồ hôi gây mất dịch giàu natri, điều này có thể dễ dàng bị bỏ qua ở những bệnh nhân bị sốt và khi nhiệt độ môi trường tăng lên.
Ngăn ngừa tổn thương thận cấp
Duy trì cân bằng dịch ở bệnh nhân ngoại khoa phụ thuộc vào việc lường trước các vấn đề trước khi chúng gây ra các tác động bất lợi và nguy cơ tổn thương thận cấp (acute kidney injury – AKI), đây là một biến chứng nghiêm trọng ở bệnh nhân ngoại khoa với tỷ lệ tử vong cao. Phòng ngừa bao gồm các chiến lược tương tự ở tất cả các bệnh nhân có nguy cơ, cụ thể là:
■ Quan sát những thay đổi của các dấu hiệu sinh tồn—nhịp tim, huyết áp và CVP, nếu thích hợp
■ Kiểm tra lượng nước tiểu hàng giờ có đủ không
■ Đo lường lượng dịch mất để hướng dẫn thay thế
■ Tìm kiếm các dấu hiệu lâm sàng của mất cân bằng dịch (mất nước hoặc quá tải)
■ Thường xuyên ước tính ure và điện giải huyết tương
Sự phát triển của AKI thường là do nhiều yếu tố. Trong khi tụt huyết áp với giảm lưu lượng máu đến thận là một yếu tố nguy cơ đáng kể, các nguyên nhân khác có thể xảy ra cần được đánh giá ở bệnh nhân ngoại khoa.
Các yếu tố nguy cơ của AKI có thể được chia thành:
■ Trước thận—cạn kiệt thể tích nội mạch; tắc nghẽn cơ học của dòng máu đến thận
■ Tại thận—tổn thương trực tiếp đến thận do thuốc, tụt huyết áp kéo dài hoặc các quá trình viêm
■ Sau thận—tắc nghẽn dòng chảy của nước tiểu trong đường tiết niệu
Bảng 2.3 Dịch tiết tiêu hóa hàng ngày và thành phần điện giải
| Dịch tiết | Thể tích (L) | Na+ (mmol/L) | K+ (mmol/L) | Cl- (mmol/L) | HCO3- (mmol/L) |
|---|---|---|---|---|---|
| Nước bọt | 1-1.5 | 20-80 | 10-20 | 20-40 | 20-160 |
| Dịch vị | 1-2.5 | 20-100 | 5-10 | 120-160 | Không |
| Mật | Lên đến 1 | 150-250 | 5-10 | 40-60 | 20-60 |
| Dịch tụy | 1-2 | 120 | 5-10 | 10-60 | 80-120 |
| Dịch ruột (succus entericus) | 2-3 | 140 | 5 (tăng lên đến 40 trong tiêu chảy viêm) | Thay đổi | Thay đổi |
Các vấn đề thường gặp khác về dịch và điện giải
Đánh giá trước các cuộc mổ phiên và các cuộc mổ cấp cứu không phức tạp
Hầu hết các cuộc mổ đều thuộc loại này. Bệnh nhân nói chung ở trạng thái cân bằng dịch và điện giải tương đối trước mổ miễn là họ có thể trạng sinh lý bình thường. Đối với những trường hợp này, ure và điện giải huyết tương nên được kiểm tra trước mổ.
Một số loại thuốc thường gặp gây rối loạn điện giải bao gồm thuốc lợi tiểu quai và lợi tiểu thiazide (loop and thiazide diuretics) có thể gây hạ kali máu (hypokalaemia) và thuốc lợi tiểu giữ kali (potassium-sparing diuretics) có thể gây tăng kali máu (hyperkalaemia). Nếu phát hiện thấy các bất thường nghiêm trọng, cuộc mổ nên được hoãn lại cho đến khi vấn đề đã được điều chỉnh. Hạ kali máu thường có thể được điều trị bằng các chất bổ sung kali đường uống.
Rối loạn chức năng thận nhẹ (ure huyết tương lên đến khoảng 12 mmol/L và creatinin lên đến khoảng 170 µmol/L) thường không phải là chống chỉ định phẫu thuật và thường cho thấy tình trạng mất nước nhẹ.
Giới thiệu về quản lý dịch và điện giải
Đối với phẫu thuật phiên, bệnh nhân thường được yêu cầu ‘nhịn ăn uống’ (nil by mouth) ít nhất 6 giờ trước mổ. Tuy nhiên, nên cho phép uống dịch trong (clear fluids) cho đến 2 giờ trước mổ. Do đó, tình trạng thiếu hụt 1000-1500 mL dịch so với lượng hấp thu bình thường là phổ biến. Tình trạng thiếu hụt dịch nhẹ như vậy thường có thể được bù đắp nhanh chóng khi bệnh nhân uống lại bình thường, và hiếm khi cần bù dịch tĩnh mạch sau mổ. Do đó, nên khuyến khích uống dịch sớm. Đối với bệnh nhân suy thận nhẹ, nên bắt đầu truyền dịch tĩnh mạch ngay khi bắt đầu giai đoạn ‘nhịn ăn uống’ để giảm nguy cơ suy thận cấp trên nền mạn (acute-on-chronic kidney failure). Nếu bệnh nhân bị buồn nôn và nôn nhiều sau mổ, điều này nên được điều trị bằng thuốc chống nôn (antiemetic medication), và nên sử dụng dịch truyền tĩnh mạch để ngăn ngừa thời gian dài giảm hấp thu đường miệng.
Trẻ em và đặc biệt là trẻ sơ sinh và trẻ nhỏ dễ bị ảnh hưởng bởi thiếu dịch hơn nhiều do tổng thể tích dịch cơ thể nhỏ và mất dịch không nhận biết được không tương xứng. Ngay cả các cuộc mổ tương đối nhỏ cũng có thể gây mất nước, do đó có thể cần truyền dịch tĩnh mạch, với tốc độ và thể tích được tính toán theo trọng lượng cơ thể và lượng máu mất đo được.
Theo nguyên tắc, cơ thể càng sớm kiểm soát được cân bằng nội môi dịch và điện giải của chính mình thì càng tốt. Nên ngừng truyền dịch tĩnh mạch ngay khi bệnh nhân đã hấp thu đường miệng bình thường trở lại và lượng nước tiểu đạt yêu cầu để ngăn ngừa quá tải dịch và rối loạn điện giải do điều trị (iatrogenic).
Các cuộc mổ lớn
Các cuộc mổ lớn theo kế hoạch hoặc cấp cứu, đặc biệt là những cuộc mổ liên quan đến ruột, đặt ra các vấn đề cụ thể về quản lý dịch. Các lý do chính như sau:
■ Bệnh nhân thường là người lớn tuổi và có khả năng bị giảm dự trữ tim mạch. Họ có thể có các bất thường về dịch và điện giải từ trước
■ Nôn trước mổ và hạn chế hấp thu dịch có thể đã gây mất nước và các bất thường điện giải
■ Mất máu trong và sau mổ có thể đáng kể
■ Các cuộc mổ có thể kéo dài vài giờ với hậu quả là mất dịch không nhận biết được từ vết mổ hở
■ Mất dịch vào khoang thứ ba 500-1000 mL có thể xảy ra do kết quả của các đáp ứng toàn thân với chấn thương sau phẫu thuật lớn hoặc chấn thương
■ Hấp thu đường miệng có thể bị ngăn cản hoặc hạn chế trong giai đoạn sau mổ tùy thuộc vào kết quả phẫu thuật và việc hình thành miệng nối. Hấp thu đường miệng thường là tối thiểu trong trường hợp bệnh nặng, đòi hỏi một thời gian dài an thần và thở máy trong chăm sóc tích cực, ví dụ, sau phẫu thuật ruột phức tạp hoặc viêm phúc mạc do thủng túi thừa hoặc xì rò miệng nối
Đánh giá bệnh nhân trước và sau mổ cẩn thận là điều cần thiết để có thể lường trước các vấn đề. Điều này nên bao gồm khám lâm sàng để đánh giá tình trạng thể tích: mất nước (khô miệng và mất độ đàn hồi da bình thường) hoặc thừa nước (tĩnh mạch cổ nổi hoặc suy tim). Ure và điện giải huyết tương, creatinin và công thức máu toàn bộ nên được đo hàng ngày. Nồng độ ure tăng cao mà creatinin tăng ít là đặc điểm của mất nước. Nồng độ hemoglobin cao bất thường (với điều kiện là không có bệnh đa hồng cầu (polycythaemia) từ trước) với hematocrit (haematocrit) tăng cao cho thấy tình trạng mất nước.
Bất thường của từng chất điện giải
Xem Bảng 2.4 để biết tóm tắt về nguyên nhân và ảnh hưởng của thiếu hụt và dư thừa natri, kali.
Bảng 2.4 Nguyên nhân và ảnh hưởng của thiếu hụt và dư thừa natri, kali
| Bất thường điện giải | Nguyên nhân | Ảnh hưởng bất lợi |
|---|---|---|
| Hạ natri máu | Thuốc lợi tiểu (đặc biệt là thiazide)
Thừa nước (uống hoặc truyền tĩnh mạch) Tiêu chảy Nôn Mất dịch từ lỗ rò ruột Suy thận SIADH (Hội chứng tiết ADH không thích hợp) Bệnh Addison Hội chứng thận hư Suy gan |
Lú lẫn
Co giật Tăng huyết áp Suy tim Yếu cơ Buồn nôn Chán ăn |
| Tăng natri máu | Mất dịch mà không bù nước (ví dụ: tiêu chảy, Nôn hoặc bỏng)
Thừa muối (thường do điều trị) Đái tháo nhạt Nhiễm toan ceton do đái tháo đường Tăng aldosteron nguyên phát (hội chứng Conn) |
Khát
Mất nước Lú lẫn Hôn mê Co giật |
| Tăng kali máu | Lấy mẫu sai (tan máu mẫu hoặc xử lý chậm)
Thuốc (ví dụ: thuốc ức chế men chuyển ACE, spironolactone hoặc suxamethonium) Ngộ độc Digoxin Thừa kali clorid (do điều trị) Truyền máu khối lượng lớn Bỏng Tiêu cơ vân (Rhabdomyolysis) Hội chứng ly giải u (Tumour lysis syndrome) Suy thận Thiếu hụt Aldosterone Bệnh Addison Nhiễm toan chuyển hóa |
Loạn nhịp tim
Đột tử |
| Hạ kali máu | Nôn
Tiêu chảy Mất dịch từ lỗ rò ruột Thuốc lợi tiểu Lạm dụng thuốc nhuận tràng Suy ống thận Bệnh Cushing, steroid ngoại sinh hoặc ACTH Nhiễm kiềm chuyển hóa Tăng aldosteron nguyên phát (hội chứng Conn) Tăng aldosteron thứ phát |
Loạn nhịp tim
Yếu cơ Giảm trương lực cơ Chuột rút Tetany |
| ACE, Angiotensin-converting enzyme (Men chuyển Angiotensin); ACTH, adrenocorticotrophic hormone (hormone vỏ thượng thận); SIADH, syndrome of inappropriate antidiuretic hormone secretion (hội chứng tiết ADH không thích hợp). | ||
Bất thường nồng độ natri huyết tương
Hạ natri máu
Nồng độ natri huyết tương thấp có thể là thật hoặc giả (spurious). Kết quả giả thường phát sinh khi máu được lấy từ cánh tay đang nhận dịch truyền tĩnh mạch; ít phổ biến hơn, kết quả xét nghiệm sai có thể xảy ra nếu có tình trạng tăng lipid máu (lipaemia) (nồng độ lipid/chất béo cao trong máu) do nuôi ăn qua đường tĩnh mạch. Nếu nghi ngờ, xét nghiệm nên được lặp lại với các biện pháp phòng ngừa thích hợp.
Trong hạ natri máu, huyết tương trở nên nhược trương, trong những trường hợp nặng dẫn đến phù não (cerebral oedema). Hạ natri máu có thể được chia thành nhẹ (Na 130-135 mmol/L), trung bình (Na 125-129 mmol/L) và nặng (Na < 125 mmol/L). Hạ natri máu từ trung bình đến nặng có thể dẫn đến lú lẫn. Co giật và hôn mê xảy ra khi nồng độ giảm xuống dưới khoảng 110 mmol/L. Nếu hạ natri máu được xác nhận về mặt sinh hóa, cần gửi các chỉ số độ thẩm thấu của nước tiểu và huyết thanh (urine and serum osmolarity) được lấy đồng thời để xác định độ trương lực của huyết tương và lượng natri bị mất trong nước tiểu. Đánh giá lâm sàng về tình trạng hydrat hóa sẽ hướng dẫn chẩn đoán và điều trị.
Các nguyên nhân có thể bao gồm:
■ Trạng thái pha loãng ưu trương: tăng đường huyết nặng, hấp thu glycine (glycine absorption) trong các thủ thuật tiết niệu hoặc truyền mannitol tĩnh mạch
■ Hạ natri máu giả đẳng trương: tăng lipid máu; nuôi ăn qua đường tĩnh mạch; đa u tủy (multiple myeloma)
■ Trạng thái nhược trương giảm thể tích: trong đó natri và dịch bị mất với khối lượng lớn dẫn đến độ thẩm thấu nước tiểu cao. Các nguyên nhân bao gồm tiêu chảy, Nôn, bỏng, đổ mồ hôi nhiều, viêm tụy và hội chứng mất muối qua não (cerebral salt-wasting syndrome)
■ Trạng thái nhược trương đẳng tích: các nguyên nhân bao gồm hội chứng tiết ADH không thích hợp (SIADH), suy giáp, suy glucocorticoid, truyền dịch nhược trương quá mức, thuốc đặc biệt là thuốc lợi tiểu và thuốc ức chế tái hấp thu serotonin chọn lọc (selective serotonin reuptake inhibitors). Biện pháp điều trị chính là hạn chế dịch
■ Trạng thái nhược trương tăng thể tích: các nguyên nhân bao gồm suy tim, xơ gan (cirrhosis), suy thận và hội chứng thận hư (nephrotic syndrome) Hội chứng sau cắt đốt nội soi qua niệu đạo (Transurethral resection – TUR) là một nguyên nhân phẫu thuật hiếm gặp gây hạ natri máu do điều trị. Đây là một biến chứng tiềm ẩn của các thủ thuật nội soi như cắt đốt nội soi tuyến tiền liệt đơn cực (monopolar TUR) được tưới rửa bằng dung dịch glycine. Nguy cơ có thể được giảm bớt bằng cách hạn chế thời gian mổ và sử dụng kỹ thuật lưỡng cực hoặc laser có sử dụng nước muối sinh lý tưới rửa.
Chẩn đoán chính xác nguyên nhân gây hạ natri máu có thể là một thách thức. Điều trị hạ natri máu trung bình và nặng nên có sự tham gia của các chuyên gia nội tiết và bác sĩ chăm sóc tích cực. Các nguyên tắc điều trị phụ thuộc vào bệnh lý gây ra. Điều chỉnh quá nhanh nồng độ natri có thể dẫn đến hủy myelin cầu não trung tâm (central pontine myelinolysis), gây tổn thương não nghiêm trọng và không thể hồi phục.
Tăng natri máu
Điều này không phổ biến và thường là do điều trị (iatrogenic) ở bệnh nhân ngoại khoa. Nguyên nhân thông thường là do truyền quá nhiều dịch truyền tĩnh mạch chứa natri hoặc bù nước không đủ. Tăng natri máu có nhiều khả năng xảy ra sau một cuộc mổ vì tăng tiết aldosterone làm natri được bảo tồn ở thận. Rất hiếm khi, tăng natri máu là do hội chứng Conn (tăng aldosteron nguyên phát) (Conn’s syndrome (primary hyperaldosteronism)).
Điều trị bao gồm cải thiện tình trạng hydrat hóa bằng cách khuyến khích uống hoặc truyền dịch có hàm lượng natri thấp. Truyền dịch nhược trương có thể gây ra sự dịch chuyển dịch nhanh chóng và cần được thực hiện bởi các chuyên gia.
Bất thường nồng độ kali huyết tương
Nồng độ kali bình thường là từ 3.5 mmol/L đến 5.0 mmol/L
Hạ kali máu
Ở bệnh nhân trước mổ, hạ kali máu (Hypokalaemia) có thể là kết quả của chế độ ăn uống kém, điều trị lợi tiểu, tiêu chảy mạn tính, mất dịch từ mở thông hồi tràng hoạt động không tốt hoặc hiếm hơn là tiết chất nhầy quá mức từ u tuyến nhung mao trực tràng (rectal villous adenoma). Hiếm khi, hạ kali máu có thể do tăng aldosteron nguyên phát (hội chứng Conn).
Hạ kali máu sau mổ thường do bổ sung kali không đủ trong dịch truyền tĩnh mạch. Việc thiếu hấp thu càng trầm trọng hơn do tăng mất kali qua nước tiểu từ tăng aldosteron thứ phát do stress.
Hạ kali máu gây yếu cơ xương và giảm nhu động đường tiêu hóa, với liệt ruột cơ năng (paralytic ileus) trong các trường hợp nghiêm trọng. Khi nặng, có nguy cơ loạn nhịp tim đột ngột hoặc ngừng tim. Hạ kali máu có thể được điều chỉnh bằng các chất bổ sung kali đường uống (viên sủi hoặc viên nén giải phóng chậm). Đối với bệnh nhân truyền dịch tĩnh mạch, các chất bổ sung kali được thêm vào khi thích hợp. Tốc độ truyền thường không nên vượt quá 15-20 mmol K mỗi giờ. Điều trị bằng truyền kali đậm đặc chỉ nên diễn ra qua đường truyền tĩnh mạch trung ương ở một địa điểm được theo dõi đầy đủ như chăm sóc tích cực.
Tăng kali máu
Điều này ít phổ biến hơn hạ kali máu ở bệnh nhân ngoại khoa nhưng cần được điều chỉnh khẩn cấp. Trong giai đoạn trước mổ, tăng kali máu có thể do suy thận mạn, dùng thuốc ức chế men chuyển angiotensin liều cao hoặc thuốc lợi tiểu giữ kali. Tăng kali máu sau mổ có thể là do điều trị, do truyền kali tĩnh mạch quá mức; nó có thể liên quan đến AKI hoặc truyền máu hoặc với tình trạng thiếu máu mô đang diễn ra.
Tăng kali máu nhẹ không có triệu chứng nhưng ở mức độ cao hơn, nó liên quan đến loạn nhịp tim đe dọa tính mạng và ngừng tim. Xử trí cấp cứu tăng kali máu được trình bày trong Hình 2.3.
Tăng kali máu giả (Pseudohyperkalaemia) thường do tăng giả tạo nồng độ đo được do các mẫu máu bị đông hoặc phân tích bị trì hoãn.
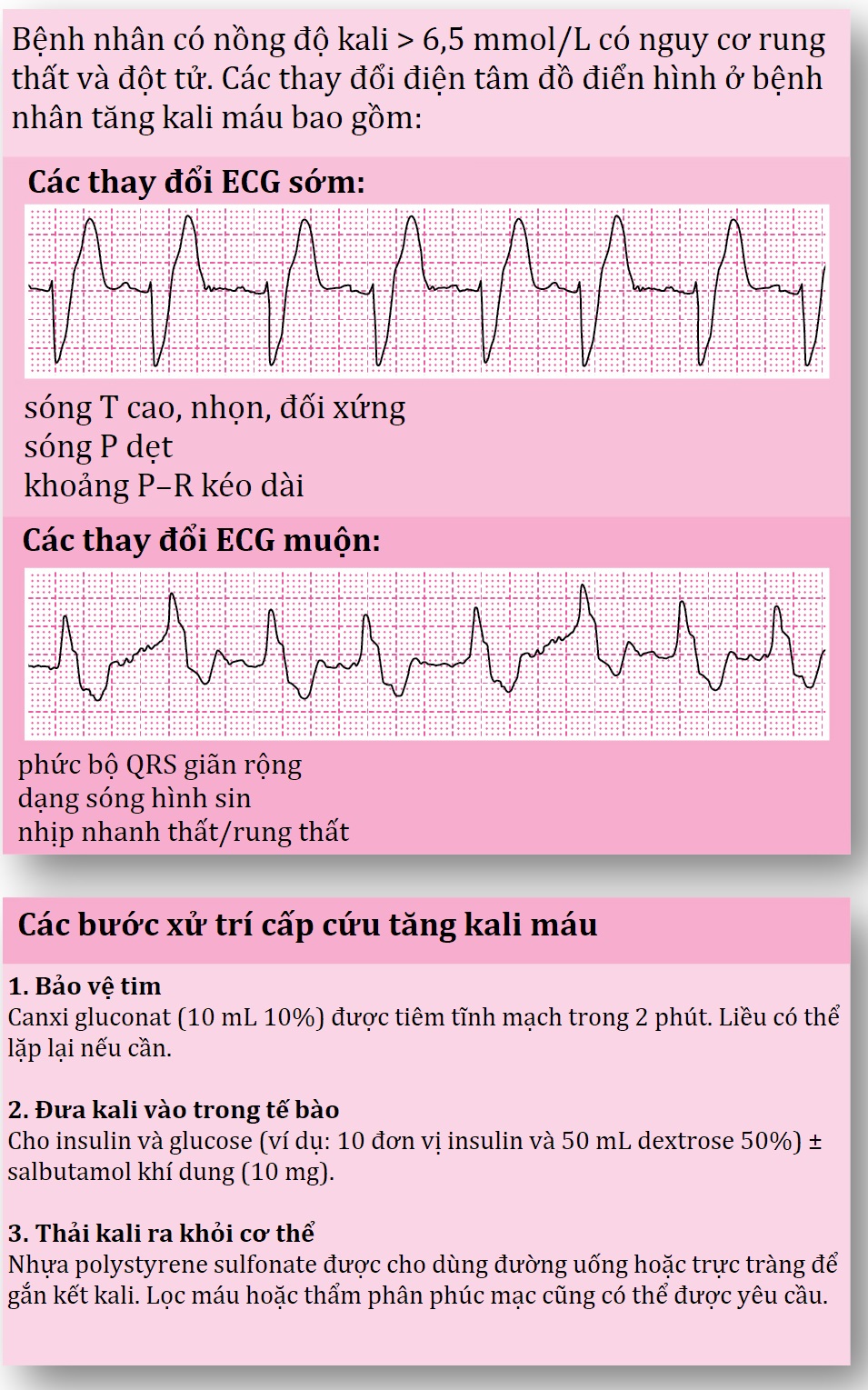
Hình 2.3: Xử trí cấp cứu tăng kali máu.
Rối loạn kiềm-toan
(Hình 2.4 và Bảng 2.5)
Các bất thường kiềm-toan đáng kể rất hiếm gặp trong các cuộc phẫu thuật không biến chứng và thường phát sinh ở những bệnh nhân bị bệnh nặng. Tóm lại, khi thở không đủ, carbon dioxide tích tụ và kết hợp với nước để tạo ra acid carbonic (‘acid hô hấp’) góp phần làm giảm pH. Điều trị là hạ thấp áp suất riêng phần của carbon dioxide (PCO2) bằng cách hỗ trợ thở. Ngoài ra, khi chuyển hóa bình thường bị suy giảm, chuyển hóa oxy hóa (oxidative metabolism) giảm và acid lactic (lactic acid) tích tụ. Các rối loạn có thể có nguyên nhân chuyển hóa hoặc hô hấp, cả hai đều có thể dẫn đến nhiễm toan hoặc nhiễm kiềm.

Hình 2.4: Diễn giải kết quả khí máu động mạch ở bệnh nhân có rối loạn kiềm-toan.
Bảng 2.5 Các rối loạn kiềm-toan
| Kết quả khí máu | |||
|---|---|---|---|
| Tình trạng kiềm-toan | PH | PCO2 | HCO3- |
| Nhiễm toan hô hấp | ↓ hoặc bình thường (nếu được bù) | ↑↑ | ↑ (nếu được bù) |
| Nhiễm kiềm hô hấp | ↑ hoặc bình thường (nếu được bù) | ↓↓ | ↓ (nếu được bù) |
| Nhiễm toan chuyển hóa | ↓ hoặc bình thường (nếu được bù) | ↓ (nếu được bù) | ↓↓ |
| Nhiễm kiềm chuyển hóa | ↑ hoặc bình thường (nếu được bù) | ↑ (nếu được bù) | ↑↑ |
| HCO3 Bicarbonat: PCO2, áp suất riêng phần của carbon dioxide. |
Nhiễm toan chuyển hóa
Nhiễm toan chuyển hóa (Metabolic acidosis) có thể theo sau một giai đoạn thiếu oxy mô nghiêm trọng do một giai đoạn sốc gây ra bởi giảm thể tích máu, nhồi máu cơ tim hoặc nhiễm trùng huyết (xem Chương 4). Thiếu oxy mô không đủ dẫn đến ở cấp độ tế bào là chuyển hóa yếm khí (anaerobic metabolism) và tích tụ acid lactic. Ở bệnh nhân ngoại khoa, sự khởi phát của nhiễm toan chuyển hóa có thể cho thấy sự phát triển của một vấn đề nghiêm trọng trong ổ bụng như tạng bị thiếu máu cục bộ (ischaemic viscus) hoặc xì rò miệng nối (anastomotic leak). Nhiễm toan chuyển hóa cũng được thấy trong AKI và nhiễm toan ceton do đái tháo đường (diabetic ketoacidosis) không kiểm soát được. Bệnh nhân bị nhiễm toan chuyển hóa phát triển kiểu thở Kussmaul (Kussmaul breathing) nhanh, sâu, thở dài trong nỗ lực tăng thông khí và thải carbon dioxide (một cơ chế bù trừ hô hấp). Ước tính khí máu động mạch cho thấy hình ảnh đặc trưng của pH thấp, nồng độ ion hydro tăng và bicarbonat chuẩn (standard bicarbonate) thấp với PaCO2 động mạch thấp hoặc bình thường. Nồng độ kali huyết tương thường tăng cao do sự dịch chuyển từ khoang nội bào sang khoang ngoại bào. Điều trị khẩn cấp nên được hướng vào việc điều trị nguyên nhân cơ bản của tình trạng xấu đi.
Nhiễm toan hô hấp
Điều này là kết quả của sự ứ đọng carbon dioxide (carbon dioxide retention) trong suy hô hấp. Các nguyên nhân thông thường ở bệnh nhân ngoại khoa là bệnh hô hấp mạn tính tiềm ẩn trở nên tồi tệ hơn do các biến chứng ngực sau mổ hoặc ức chế hô hấp kéo dài do thuốc an thần hoặc thuốc opioid. pH huyết tương cao; nồng độ ion hydro và PaCO2 tăng cao, nhưng bicarbonat chuẩn ban đầu bình thường. Một mức độ bù trừ chuyển hóa có thể xảy ra khi thận bài tiết các ion hydro dư thừa và giữ lại bicarbonat. Điều trị được hướng vào nguyên nhân cơ bản và cung cấp thông khí hỗ trợ để giảm PaCO2 cho đến khi nguyên nhân cơ bản được điều chỉnh.
Nhiễm kiềm chuyển hóa
Nhiễm kiềm chuyển hóa (Metabolic alkalosis) có thể do Nôn nghiêm trọng và lặp đi lặp lại hoặc hút dịch dạ dày kéo dài do tắc ruột. Hẹp môn vị (Pyloric stenosis) gây Nôn kéo dài và mất acid dịch vị liên quan. Bệnh nhân trở nên mất nước nghiêm trọng và cạn kiệt các ion natri và clorid; do đó, tình trạng này được gọi là nhiễm kiềm chuyển hóa giảm clorid máu (hypochloraemic metabolic alkalosis). Có những nỗ lực bù trừ của thận thông qua việc bảo tồn các ion hydro, nhưng điều này xảy ra bằng cách hy sinh các ion kali bị mất vào nước tiểu. Bệnh nhân trở nên hạ kali máu do mất quá nhiều qua nước tiểu và cũng do kali dịch chuyển vào tế bào để đáp ứng với tình trạng nhiễm kiềm. Điều trị nhiễm kiềm giảm clorid máu, hạ kali máu bao gồm bù nước bằng truyền nước muối sinh lý có bổ sung kali; thường cần một lượng lớn (lên đến 10 L). Bài tiết các ion bicarbonat qua thận cuối cùng sẽ điều chỉnh tình trạng nhiễm kiềm.
Nhiễm kiềm hô hấp
Điều này là bất thường và xảy ra khi carbon dioxide bị mất qua thông khí phổi quá mức (excessive pulmonary ventilation). Nguyên nhân trong thực hành phẫu thuật là thở máy kéo dài trong quá trình gây mê toàn thân hoặc trong đơn vị chăm sóc tích cực mà không có theo dõi đầy đủ.
Quản lý dinh dưỡng ở bệnh nhân ngoại khoa
Các nguyên tắc thiết yếu
Suy dinh dưỡng (Malnutrition) là một tình trạng suy mòn (wasting condition) do thiếu hụt năng lượng (tức là calo), protein và đôi khi là vitamin và các nguyên tố vi lượng (trace elements). Nhận biết và điều trị suy dinh dưỡng có từ trước và ngăn ngừa tình trạng nhịn ăn sau mổ là những khía cạnh quan trọng của quản lý bệnh nhân tốt nhưng thường bị bỏ qua. Đánh giá cơ bản về suy dinh dưỡng nên là một phần tiêu chuẩn của việc đánh giá bệnh nhân ngoại khoa (Hộp 2.4), vì suy dinh dưỡng không được điều trị dẫn đến một loạt các vấn đề làm chậm quá trình phục hồi đáng kể và góp phần vào tỷ lệ bệnh tật và tử vong (Hộp 2.5).
Nguyên nhân gây suy dinh dưỡng bao gồm giảm hấp thu thức ăn (chán ăn, nhịn ăn, đau khi nuốt hoặc suy giảm thể chất hoặc tinh thần); kém hấp thu (suy giảm tiêu hóa hoặc hấp thu hoặc mất quá nhiều từ ruột); và thay đổi chuyển hóa (chấn thương, bỏng, nhiễm trùng huyết, phẫu thuật, ung thư hoặc suy mòn). Bệnh nhân có bất kỳ yếu tố nguy cơ nào trong số này cần được đánh giá kỹ lưỡng về suy dinh dưỡng. Sự tham gia của chuyên gia dinh dưỡng có thể có giá trị.
Trong thực tế, hầu hết bệnh nhân ngoại khoa không có yêu cầu dinh dưỡng đặc biệt và dễ dàng chịu đựng được thời gian nhịn ăn ngắn liên quan đến bệnh tật và cuộc mổ của họ. Tất cả bệnh nhân nhập viện cần được sàng lọc bằng một công cụ sàng lọc được công nhận và tình trạng dinh dưỡng của họ được ghi lại và tối ưu hóa trước mổ trong phạm vi có thể. Hỗ trợ dinh dưỡng tối ưu nên được cung cấp trong giai đoạn sau mổ.
Hỗ trợ dinh dưỡng trong bệnh viện thường được cung cấp bởi một đội ngũ chuyên gia dinh dưỡng (dietetic team) tận tâm. Các chiến lược bao gồm khuyến khích bệnh nhân ăn uống đều đặn, cung cấp các chất bổ sung giàu protein hoặc giàu năng lượng hoàn chỉnh về mặt dinh dưỡng để uống (ví dụ: Fortisip), bổ sung dinh dưỡng qua đường ruột (enteral nutrition) qua sonde dạ dày (nasogastric tube), và nuôi ăn hoàn toàn qua đường tĩnh mạch (total parenteral nutrition – TPN) dài hạn cho những bệnh nhân không thể hấp thu chất dinh dưỡng từ đường tiêu hóa.
HỘP 2.4 Đánh giá suy dinh dưỡng ở bệnh nhân
Đánh giá lâm sàng
Đánh giá nhân trắc học
Các chỉ số máu
|
HỘP 2.5 Các ảnh hưởng bất lợi của thiếu hụt protein/calo ở bệnh nhân ngoại khoa
|
Nhận biết bệnh nhân có nguy cơ
Suy dinh dưỡng là phổ biến ở bệnh nhân ngoại khoa và thường không được nhận ra. Các nghiên cứu đã chỉ ra rằng có tới 50% bệnh nhân nội trú ngoại khoa bị suy dinh dưỡng nhẹ và 30% bị suy dinh dưỡng nặng. Đánh giá lâm sàng đơn giản là yếu tố quyết định tốt nhất tình trạng dinh dưỡng, mặc dù các chỉ số khác cũng có thể được sử dụng (xem Hộp 2.4). Thời gian nhịn ăn trước và sau mổ nên được giảm thiểu và cung cấp dinh dưỡng thích hợp. Điều này góp phần chữa lành vết thương, cải thiện khả năng chống nhiễm trùng và giảm các biến chứng do yếu cơ (xem Hộp 2.5).
Ảnh hưởng của nhịn ăn
Nhịn ăn đơn thuần
Trong thời gian nhịn ăn đơn thuần (tức là không có bệnh tật hoặc chấn thương), nồng độ glucose máu được duy trì bằng cách giảm tiết insulin và tăng sản xuất glucagon. Dự trữ glycogen ở gan bị cạn kiệt trong vòng 24 giờ nhưng quá trình tân tạo đường ở gan và thận được tăng cường, sử dụng các acid amin từ phân hủy protein và glycerol từ ly giải mỡ làm cơ chất (substrates). Phần lớn glucose được tạo ra theo cách này được não sử dụng, vì hầu hết các mô khác có khả năng chuyển hóa các acid béo và thể ceton (ketones) có nguồn gốc từ mô mỡ. Nhìn chung, nhu cầu năng lượng giảm trong tình trạng nhịn ăn đơn thuần, và năng lượng được lấy chủ yếu từ mỡ cơ thể. Protein được bảo tồn cho đến giai đoạn muộn.
Nhịn ăn trong chấn thương, phẫu thuật hoặc nhiễm trùng huyết
Trong các cuộc phẫu thuật lớn, và đặc biệt là với nhiễm trùng xen kẽ hoặc sau chấn thương lớn, nhu cầu năng lượng tăng lên đến 100%. Giống như trong nhịn ăn đơn thuần, lipid trở thành nguồn nhiên liệu chính; điều này làm giảm sử dụng glucose, nhưng các acid béo khác ngoài glycerol không thể được sử dụng để tổng hợp glucose. Sản xuất glucose ở gan tăng lên, nhưng sử dụng glucose ở ngoại vi bị suy giảm, thường dẫn đến tăng đường huyết.
Ly giải protein (proteolysis) cơ xương và bài tiết nitơ qua nước tiểu tăng lên rất nhiều so với trạng thái nhịn ăn. Protein từ cơ xương bị dị hóa để giải phóng các acid amin (đặc biệt là alanin (alanine)), lactat và pyruvat (pyruvate). Tác nhân kích thích ly giải protein có khả năng là do cytokine gây ra. Cũng có sự giảm tổng hợp albumin ở gan để chuyển sang xây dựng các protein pha cấp (acute-phase proteins) và tân tạo đường. Các acid amin cũng được sử dụng trực tiếp trong quá trình lành vết thương và sản sinh tế bào máu (haemopoiesis).
Trong nhiễm trùng huyết, có sự bất lực ngày càng tăng ở cấp độ ty thể (mitochondrial) trong việc oxy hóa hoàn toàn các cơ chất để tạo năng lượng, dẫn đến giảm tiêu thụ oxy khi nhiễm trùng huyết nặng lên. Các acid béo ngày càng được huy động nhiều hơn từ mô mỡ, biểu hiện bằng tăng triglycerid máu (hypertriglyceridaemia). Sự huy động được điều chỉnh bởi nồng độ catecholamine, cortisol, glucagon và TNF tăng cao. Các acid béo được oxy hóa để sản xuất adenosine triphosphate (ATP) nhằm cung cấp nhiên liệu cho việc tổng hợp glucose và protein mới. Một số acid amin sau đó được chuyển hóa thành các chất vận mạch làm nặng thêm tình trạng giãn mạch và tụt huyết áp thấy trong nhiễm trùng huyết và gây ra bệnh lý não do nhiễm trùng huyết (septic encephalopathy).
Bổ sung dinh dưỡng
Bổ sung dinh dưỡng (ngoài chế độ ăn lỏng và thức uống bổ sung) là một quá trình phức tạp và đôi khi tốn kém với những nguy cơ biến chứng rõ rệt. Không nên thực hiện nếu không có đánh giá đúng đắn. Quyết định xem một bệnh nhân có khả năng được hưởng lợi từ việc bổ sung dinh dưỡng hay không phụ thuộc vào việc xác định những điều sau:
■ Bệnh nhân bị suy dinh dưỡng hoặc sẽ bị thiếu dinh dưỡng trong ít nhất 5 ngày
■ Bệnh nhân có khả năng được hưởng lợi—một số điều kiện nhất định làm cho việc bổ sung dinh dưỡng không hiệu quả (ví dụ: nuôi ăn qua đường ruột trong trường hợp rò tiêu hóa ra da (enterocutaneous fistula) lưu lượng cao)
■ Liệu có đường dùng thích hợp hay không, ví dụ, chức năng ruột đủ
Hỗ trợ dinh dưỡng thường được khuyến nghị ở những bệnh nhân được nuôi dưỡng tốt mà không thể dung nạp thức ăn đường miệng trong hơn 7 ngày hoặc dưới 5 ngày nếu đã bị suy dinh dưỡng.
Phương pháp bổ sung dinh dưỡng
Hộp 2.6 tóm tắt một loạt các chế độ dinh dưỡng và các chỉ định phẫu thuật chính của chúng. Đường tiêu hóa nên được sử dụng bất cứ khi nào có thể vì bất kỳ hình thức nuôi ăn qua đường ruột nào cũng an toàn hơn về bản chất so với nuôi ăn qua đường tĩnh mạch và hiệu quả hơn và rẻ hơn nhiều. Ngoài ra, niêm mạc ruột non có xu hướng teo đi khi không được ‘sử dụng’. Nuôi ăn qua đường ruột hỗ trợ hàng rào miễn dịch liên quan đến đường ruột (gut-associated immunologic shield) và ngăn chặn vi sinh vật chuyển vị vào tuần hoàn, giảm nguy cơ nhiễm trùng đường máu. Chống chỉ định nuôi ăn qua đường ruột bao gồm tắc ruột, rò ruột lưu lượng cao, Nôn hoặc tiêu chảy không kiểm soát được và kém hấp thu (malabsorption) nghiêm trọng.
HỘP 2.6 Các phương pháp dinh dưỡng đặc biệt và chỉ định
|
Chế độ ăn nhấp môi (Sip feeds)
Nếu bệnh nhân có thể ăn, thì chế độ ăn lỏng (toàn bộ hoặc bổ sung) thường có thể được đưa qua đường uống. Các loại thức ăn bổ sung dạng lỏng (sip feed) thương mại chứa calo, protein, khoáng chất và vitamin dễ hấp thu có sẵn ở nhiều công thức và hương vị khác nhau và được dung nạp tốt.
Nuôi ăn qua ống (Tube feeds)
Một số bệnh nhân không phù hợp với chế độ ăn nhấp môi nhưng có thể được nuôi ăn bằng một trong một số đường nuôi ăn qua ống. Chỉ định bao gồm bệnh nhân khó nuốt, chán ăn, thức ăn dạng lỏng không hợp khẩu vị, cần lượng thức ăn nhiều hơn mức bệnh nhân có thể thoải mái xử lý và dự đoán có sự chậm trễ đáng kể trong việc tiếp tục ăn uống đường miệng sau mổ.
Ngay cả khi bệnh nhân không thể nuốt (ví dụ: do liệt hành tủy (bulbar palsy), bất tỉnh hoặc gãy xương mặt), dinh dưỡng qua đường ruột hoàn chỉnh có thể được cung cấp bằng phương tiện sonde mũi-dạ dày hoặc sonde mũi-hỗng tràng lòng nhỏ (fine-bore nasogastric or naso-jejunal tube), loại sau dành cho những người cần nuôi ăn qua đường ruột sau môn vị (post-pyloric enteral feeding) (ví dụ: trong viêm tụy cấp). Một chế độ ăn lỏng riêng biệt được xây dựng và được cung cấp với tốc độ được kiểm soát bằng máy bơm, thường là qua đêm.
Các ống nuôi ăn cũng có thể được đặt qua da (percutaneously) vào dạ dày hoặc hỗng tràng, hoặc tại cuộc mổ (nếu các vấn đề về nuôi ăn được lường trước tại thời điểm phẫu thuật) hoặc với sự trợ giúp của nội soi hoặc nội soi ổ bụng. Mở thông dạ dày có thể được sử dụng ở những bệnh nhân sau đột quỵ hoặc ở những người có miệng nối đường tiêu hóa trên hoặc các tổn thương gây tắc nghẽn. Kỹ thuật thông thường là đặt mở thông dạ dày qua da nội soi (percutaneous endoscopic gastrostomy – PEG), kết hợp nội soi dạ dày và đặt qua da. Ống PEG bị chống chỉ định trong viêm phúc mạc, cổ trướng (ascites) và liệt ruột kéo dài.
Một số bệnh nhân không cần nuôi ăn hoàn toàn qua đường ruột hoặc đường tĩnh mạch có thể được hưởng lợi từ việc bổ sung vitamin, ví dụ, cần bổ sung acid folic và thiamine (thiamine) ở những người nghiện rượu lâu năm, hoặc tiêm vitamin K cho bệnh nhân điều trị kháng sinh kéo dài khi hệ vi khuẩn đường ruột bị xáo trộn có thể làm suy giảm hấp thu vitamin K.
Nuôi ăn hoàn toàn qua đường tĩnh mạch
Nuôi ăn qua đường tĩnh mạch nên được dành riêng cho các trường hợp suy đường ruột (intestinal failure) thích hợp (xem sau). Không nên bắt tay vào thực hiện một cách nhẹ dạ và nên được thực hiện bởi các đội ngũ chuyên gia. Các công thức TPN chủ yếu chứa hỗn hợp glucose, acid amin, lipid, khoáng chất và vitamin. Các nguồn năng lượng không chứa nitơ dưới dạng glucose và lipid có tác dụng tiết kiệm protein và giảm thiểu tiêu thụ các acid amin làm năng lượng. Độ thẩm thấu của hỗn hợp thường cao, vì vậy đường dùng phổ biến nhất là qua đường truyền tĩnh mạch trung tâm chuyên dụng (dedicated central venous line), đường truyền tĩnh mạch trung tâm từ ngoại biên (peripherally inserted central catheter – PICC) hoặc catheter tĩnh mạch trung ương loại Hickman (Hickman-type central venous catheter) để giảm thiểu nguy cơ kích ứng tĩnh mạch và huyết khối. Mục tiêu thông thường của TPN là cung cấp đủ nitơ và năng lượng để bù đắp nhu cầu dị hóa của phẫu thuật và/hoặc chấn thương và các biến chứng của chúng, và nếu có thể, bù đắp cho bất kỳ tình trạng suy dinh dưỡng nào có từ trước.
Khi tính toán nhu cầu, lượng protein hấp thu nên được khớp với lượng nitơ mất đi ước tính có thể được tính bằng công thức chuẩn. Ví dụ, nhu cầu hàng ngày tiêu chuẩn của người trưởng thành là 100 g protein (dưới dạng acid amin), 350 g glucose và 50 g lipid để cung cấp năng lượng.
Các chỉ định có thể bao gồm:
■ Rò tiêu hóa ra da (Enterocutaneous fistula)
■ Hội chứng ruột ngắn (Short bowel syndrome) khi không đủ khả năng hấp thu còn lại sau khi cắt bỏ ruột non hàng loạt ■ Đa chấn thương liên quan đến các tạng
■ Bệnh lý mà đường tiêu hóa không hoạt động hoặc không thể tiếp cận được và có khả năng vẫn như vậy trong một thời gian đáng kể
Phương pháp thực hiện TPN
Nuôi ăn qua đường tĩnh mạch thường được đưa vào tĩnh mạch chủ trên (superior vena cava) qua tĩnh mạch cảnh trong (internal jugular) hoặc tĩnh mạch dưới đòn (subclavian vein) để dòng chảy tĩnh mạch cao nhanh chóng pha loãng dung dịch ưu trương, giảm thiểu nguy cơ huyết khối. Nếu dự đoán thời gian hỗ trợ dinh dưỡng kéo dài, một đường truyền có đường hầm (tunnelled line) được chỉ định thường được sử dụng, với điểm tiếp cận da cách xa điểm vào tĩnh mạch để giảm nguy cơ nhiễm trùng đường truyền.
Nuôi ăn qua đường tĩnh mạch tốn kém về vật liệu và thời gian của nhân viên và dễ bị biến chứng; nên ngừng ngay khi có thể cung cấp dinh dưỡng bằng đường ruột. Bệnh nhân dùng TPN cần được theo dõi chặt chẽ và thường xuyên về một loạt các vấn đề bao gồm các vấn đề về đường truyền, nhiễm trùng tại chỗ và toàn thân, cân bằng dịch và thiếu hụt điện giải (Hộp 2.7). Các biến chứng thường gặp của TPN được trình bày chi tiết trong Hộp 2.8.
HỘP 2.7 Theo dõi nuôi ăn qua đường tĩnh mạch
8 giờ một lần
Hàng ngày
Hai lần mỗi tuần
Hàng tuần
|
HỘP 2.8 Các biến chứng của nuôi ăn qua đường tĩnh mạch
Các vấn đề về catheter (10% các đường truyền trung ương phát triển các biến chứng đáng kể)
Các vấn đề về chuyển hóa (5% phát triển các rối loạn chuyển hóa)
|
Hội chứng nuôi ăn lại
Hội chứng nuôi ăn lại (Refeeding syndrome) được mô tả lần đầu tiên ở các tù nhân ở Viễn Đông sau Chiến tranh Thế giới thứ hai, những người đã phát triển suy tim khi bắt đầu ăn trở lại sau thời gian đói kéo dài. Với việc giảm hấp thu carbohydrate, tiết insulin giảm xuống và chất béo và protein bị dị hóa thay cho carbohydrate. Điều này dẫn đến mất các chất điện giải nội bào, đặc biệt là phosphat, vốn bị cạn kiệt. Phosphat rất cần thiết để tạo ra ATP và cho các phản ứng phosphoryl hóa (phosphorylation reactions) quan trọng khác.
Khi bắt đầu nuôi ăn qua đường ruột hoặc đường tĩnh mạch sau thời gian nhịn ăn, có sự đảo ngược đột ngột từ chuyển hóa chất béo sang chuyển hóa carbohydrate. Tiết insulin tăng lên và sự hấp thu của tế bào đối với glucose, phosphat, kali và nước tăng lên. Điều này có thể dẫn đến hạ phosphat máu (hypophosphataemia) sâu, thường kèm theo hạ kali máu (hypokalaemia) và hạ magnesi máu (hypomagnesaemia). Lưu ý rằng tất cả dịch ngoại bào đều bị ảnh hưởng bởi nồng độ các chất điện giải này giảm xuống. Ở trạng thái nhịn ăn, có sự cạn kiệt toàn bộ các chất điện giải trong cơ thể, nhưng nồng độ trong huyết tương có thể bình thường một cách dễ gây hiểu nhầm do bù trừ của thận.
Hội chứng nuôi ăn lại xảy ra khi phosphat huyết tương giảm xuống dưới 0.50 mmol/L. Các đặc điểm lâm sàng bao gồm suy tim và suy hô hấp, loạn nhịp tim, tiêu cơ vân (rhabdomyolysis), rối loạn chức năng bạch cầu (white cell dysfunction), co giật, hôn mê và đột tử. Các dấu hiệu sớm thường không được nhận ra; phosphat huyết tương có thể không được đo, hoặc ý nghĩa của các kết quả bất thường nghiêm trọng có thể không được đánh giá đúng mức.
Những bệnh nhân suy dinh dưỡng có nguy cơ mắc hội chứng nuôi ăn lại nên bắt đầu nuôi ăn nhân tạo với một phần tư đến một nửa nhu cầu calo dự kiến. Nồng độ phosphat, magnesi, calci, kali, ure và creatinin huyết tương cần được đo hàng ngày, và các thiếu hụt cần được điều chỉnh. Nếu cần, 50 mmol phosphat tĩnh mạch được truyền trong 24 giờ và có thể cần lặp lại. Thiamine cũng phải được thay thế ở những bệnh nhân này. Cần tìm kiếm sự tham gia của chuyên gia dinh dưỡng có kinh nghiệm trong việc quản lý hội chứng nuôi ăn lại bị nghi ngờ.
Các chương trình Phục hồi sớm sau phẫu thuật (ERAS)
Các phác đồ phục hồi sớm (xem Bảng 2.1) nhằm mục đích rút ngắn thời gian nằm viện và giảm tỷ lệ biến chứng sau phẫu thuật lớn bằng cách phát triển các hệ thống có cấu trúc làm giảm đáp ứng stress để tăng cường phục hồi bằng nhiều cách, thường là nhỏ, và cải thiện kết quả. Những điều này liên quan đến sự chú ý đến tất cả các khía cạnh của chăm sóc phẫu thuật, được gọi là tối ưu hóa đa mô thức (multimodal optimisation) hoặc phục hồi nhanh (fast-track recovery). Điều này bao gồm sự chú ý đặc biệt đến quản lý dịch chu phẫu, việc sử dụng các kỹ thuật phẫu thuật xâm lấn tối thiểu (minimal access surgical techniques) và các cơ chế để bảo tồn chức năng cơ quan sau mổ, bao gồm:
■ Đánh giá trước mổ kỹ lưỡng để xác định các vấn đề ở các ứng cử viên cho phẫu thuật
■ Giáo dục bệnh nhân về kế hoạch xuất viện sớm và đảm bảo các sắp xếp tại nhà thích hợp được thực hiện
■ Sử dụng thức uống tải carbohydrate (carbohydrate-loading drinks) trước mổ; chuẩn bị ruột tối thiểu
■ Sử dụng các kỹ thuật phẫu thuật xâm lấn tối thiểu, khi thích hợp
■ Tính toán và bù dịch để đảm bảo bệnh nhân duy trì tình trạng đẳng thể tích máu (normovolaemic), do đó ngăn ngừa giảm thể tích máu trung tâm và quá tải dịch. Viện Quốc gia về Sức khỏe và Chăm sóc Xuất sắc (National Institute for Health and Care Excellence – NICE) của Anh đã khuyến nghị sử dụng theo dõi siêu âm Doppler qua thực quản (transoesophageal Doppler ultrasound) về thể tích nhát bóp thất trái (left ventricular stroke volume) để đánh giá tình trạng dịch trong mổ, cùng với việc cung cấp liệu pháp dịch truyền theo mục tiêu (goal-directed fluid therapy) cá nhân hóa. Các thử nghiệm đã chỉ ra rằng điều này có thể rút ngắn thời gian nằm viện một cách đáng tin cậy và giảm tỷ lệ biến chứng
■ Vận động sớm sau mổ có kế hoạch và có hỗ trợ
■ Rút sớm các ống dẫn lưu và thông tiểu nếu thích hợp
■ Thử thách dinh dưỡng đường ruột sớm
Các phương pháp cho phép chức năng ruột trở lại sớm hơn có thể là nền tảng cho sự phục hồi nhanh chóng. Mô lympho liên quan đến đường ruột (Gut-associated lymphoid tissue) chiếm hơn một nửa khối lượng tế bào miễn dịch của cơ thể và được cho là đóng một vai trò quan trọng trong các đáp ứng stress với phẫu thuật. Duy trì dinh dưỡng của thành ruột non từ bên trong lòng ruột có thể ngăn ngừa sự phá vỡ chức năng hàng rào ruột (intestinal barrier function). Chức năng ruột khỏe mạnh cho phép dung nạp thức ăn sớm hơn, ít liệt ruột sau mổ (postoperative ileus) hơn và ít buồn nôn và nôn sau mổ hơn.
