Sổ tay Phục hồi chức năng Lâm sàng Braddom, Ấn bản thứ hai (2026)
Nhà xuất bản: ELSEVIER, 2026
Tác giả: David Cifu, Henry L. Lew – Dịch và chú giải: Ths.Bs. Lê Đình Sáng
(C) Bản dịch tiếng Việt bởi THƯ VIỆN Y HỌC MEDIPHARM
Chương 42: Các rối loạn bệnh lý cơ
Myopathic disorders
Ziad M. Hawamdeh
Braddom’s Rehabilitation Care: A Clinical Handbook, 42, 415-436.e8
Hướng dẫn nhanh
|
Các rối loạn bệnh lý cơ là một nhóm các bệnh lý thần kinh-cơ di truyền hoặc mắc phải ảnh hưởng đến các sợi cơ xương. Triệu chứng biểu hiện chính là yếu cơ, chủ yếu là ở gốc chi, thường liên quan đến mệt mỏi, chuột rút, trương lực cơ, co thắt cơ và cứng cơ. Sức bền kém và không dung nạp gắng sức cũng là những đặc điểm phổ biến, với trương lực cơ giảm thấy trong các trường hợp khởi phát ở trẻ em. Tăng Creatine phosphokinase (CPK) (tăng CK máu) thường xuất hiện, đặc biệt là trong các bệnh lý cơ loạn dưỡng. Sự liên quan của các sợi cơ tim là một đặc điểm chính của một số bệnh lý dystrophin. Yếu cơ hít vào và thở ra có thể dẫn đến suy hô hấp. Các cơ miệng-hầu có thể trở nên yếu và giảm trương lực, dẫn đến khó nuốt, tăng tiết nước bọt và khó nói. Các bất thường về xương có thể nghiêm trọng, với co rút khớp và vẹo cột sống đồng thời. Chương này nêu bật các rối loạn bệnh lý cơ phổ biến hơn, tập trung vào bệnh lý học, biểu hiện lâm sàng, các phương pháp chẩn đoán và các nguyên tắc phục hồi chức năng.
ĐÁNH GIÁ LÂM SÀNG VÀ CHẨN ĐOÁN TRONG BỆNH LÝ CƠ (HỘP 42.1)
Khai thác bệnh sử chi tiết là điều cần thiết để thiết lập chẩn đoán trong các rối loạn bệnh lý cơ. Các kiểu hình yếu cơ trên lâm sàng, tuổi khởi phát và tiền sử gia đình mắc bệnh thần kinh-cơ là rất quan trọng. Kiểu hình yếu cơ phổ biến nhất là yếu gốc chi tiến triển liên quan đến cơ đai vai và đai chậu, thấy trong các bệnh như loạn dưỡng cơ Duchenne (DMD), loạn dưỡng cơ Becker (BMD) và một số thể loạn dưỡng cơ gốc chi (LGMD), trong khi yếu đối xứng ngọn chi bao gồm các bệnh như loạn dưỡng trương lực cơ (DM1). Bệnh tiến triển chậm phổ biến nhất liên quan đến yếu cơ vai-mác là loạn dưỡng cơ mặt-vai-cánh tay (FSHD), trong khi các kiểu hình yếu không đối xứng ngọn chi bao gồm các bệnh lý dysferlin. Yếu gốc chi với liên quan đến cơ ngoài mắt thường thấy trong loạn dưỡng cơ mắt-hầu (OPMD). Các bệnh lý cơ bẩm sinh được đặc trưng bởi sự tiến triển ổn định sau khi khởi phát ban đầu. Tiền sử sinh và phát triển, bao gồm các cử động thai bất thường trong tử cung, và chậm các mốc phát triển vận động hoặc nhận thức, trương lực cơ giảm và mềm nhũn là phổ biến trong các bệnh lý cơ bẩm sinh và loạn dưỡng cơ trương lực cơ bẩm sinh. Chuột rút, đau cơ và cứng cơ có thể xảy ra khi nghỉ ngơi hoặc khi gắng sức và có thể thấy trong nhiều thể bệnh lý cơ. Điều quan trọng là phải hỏi xem có nước tiểu sẫm màu sau các mức độ gắng sức thể chất khác nhau hay không. Không dung nạp gắng sức hoặc mệt mỏi khi gắng sức là phổ biến với nhiều thể bệnh lý cơ. Trong các bệnh dự trữ glycogen, chẳng hạn như bệnh McArdle, hiện tượng “lấy lại sức” (second-wind phenomenon) là phổ biến sau khi nghỉ ngơi ngắn sau một thời gian gắng sức ngắn. Khó duỗi tay sau khi bắt tay có thể gợi ý loạn dưỡng cơ trương lực cơ hoặc một số bệnh lý kênh ion. Các bất thường cơ xương khớp, loạn sản khớp háng bẩm sinh, co rút, vẹo cột sống, khó nuốt, các vấn đề về hô hấp và các biến chứng tim mạch có thể thấy trong một số thể rối loạn bệnh lý cơ. Những bất thường trong vận động bao gồm khó khăn khi chuyển từ nằm ngửa hoặc ngồi sang đứng, khó khăn khi leo cầu thang, đi nhón gót và tăng tần suất té ngã. Tăng thân nhiệt ác tính (MH) là một mối lo ngại, vì vậy cần khai thác tiền sử phẫu thuật, bao gồm các phản ứng bất lợi với thuốc mê.
Thăm khám lâm sàng
Thực hiện thăm khám thần kinh và cơ xương khớp hoàn chỉnh là rất quan trọng. Việc thăm khám bắt đầu bằng quan sát tư thế và dáng đi. Nên thực hiện thử cơ bằng tay để đánh giá sức mạnh cơ hai bên. Phát hiện ưỡn lưng quá mức, dáng đi lạch bạch, hoặc đi nhón gót có thể thấy trong một số bệnh lý cơ gốc chi, chẳng hạn như DMD và BMD, và các bệnh LGMD. Vai xuôi và xương bả vai nhô (cánh chim) là những đặc điểm phổ biến của FSHD và có thể thấy trong LGMD1B, LGMD2B, bệnh Pompe và các bệnh lý sarcoglycan (LGMD 2C-2F). Điều quan trọng nữa là quan sát bệnh nhân đứng dậy từ tư thế nằm ngửa để đánh giá dấu hiệu Gower. Yếu động tác gập ngón tay đơn độc có thể xuất hiện trong viêm cơ thể vùi (IBM), vì vậy điều quan trọng là phải đánh giá sức mạnh gập và duỗi cổ tay và ngón tay. Yếu động tác gập cổ, được đánh giá ở tư thế nằm ngửa, là phổ biến và có thể xảy ra sớm trong quá trình bệnh do diện tích mặt cắt ngang của các cơ gập cổ tương đối nhỏ. Động tác duỗi cổ có thể được thực hiện ở tư thế nằm sấp cùng với sức mạnh gập gối. Sự liên quan của các cơ ngoài mắt và sụp mi giới hạn chẩn đoán phân biệt với các bệnh như OPMD và FSHD. Có thể có phì đại cơ bắp chân hoặc dấu hiệu lõm nách sau. Lưỡi phì đại (macroglossia) có thể xảy ra trong bệnh lý cơ do suy giáp, bệnh Pompe và bệnh lý cơ do amyloid. Các phản xạ thường mất hoặc giảm. Trương lực cơ dẫn đến thất bại trong việc thư giãn của cơ chế khớp nối actin-myosin. Khám cảm giác thường là bình thường, và nên thực hiện khám thần kinh sọ (bao gồm các cơ ngoài mắt và cơ mặt, lưỡi và vòm miệng). Sụp mi và liệt mắt xuất hiện trong OPMD, các bệnh lý cơ ty thể, DM1, và (ở mức độ thấp hơn) DM2, và thường có liên quan đến cơ mặt trong FSHD. Các quan sát khác khi thăm khám lâm sàng bao gồm đánh giá da để tìm sự hiện diện của ban đỏ hình cánh bướm (heliotropic rash) trên mặt, những thay đổi ở giường mao mạch móng tay như thấy trong viêm da cơ (DM), hoặc dày sừng nang lông như thấy trong bệnh lý cơ collagen. Co rút và vẹo cột sống có thể xảy ra trong nhiều bệnh lý cơ khi bệnh tiến triển.
Đánh giá chẩn đoán
Các xét nghiệm trong phòng thí nghiệm bao gồm CPK, transaminase và aldolase. Tăng alanine transaminase (ALT) và aspartate transaminase (AST) có thể thấy trong cả bệnh lý cơ nguyên phát và bệnh gan. Gamma glutamyl transpeptidase chỉ tăng đặc hiệu trong bệnh gan. Nồng độ CPK thay đổi đáng kể giữa các rối loạn bệnh lý cơ và có thể bình thường trong một số trường hợp. Trong DMD và BMD, giá trị CPK thường tăng cao tới 50 đến 100 lần giới hạn trên của mức bình thường ở trẻ nhũ nhi và trẻ em trong giai đoạn đầu của bệnh và vẫn cao trong suốt thời kỳ nhũ nhi và đầu thời thơ ấu. Khi bệnh tiến triển và yếu cơ xảy ra, các giá trị thường giảm chậm.
Nếu nghi ngờ một bệnh lý cơ viêm nguyên phát, có thể chỉ định các tự kháng thể đặc hiệu. Ví dụ, nếu kiểu hình yếu cơ gợi ý IBM, có thể chỉ định kháng thể NT5C1A và nó có độ đặc hiệu cao cho bệnh này. Nếu chẩn đoán phân biệt bệnh lý cơ viêm rộng, có thể chỉ định các panel lớn hơn bao gồm panel tự kháng thể đặc hiệu cho viêm cơ. Các panel lớn hơn bao gồm các tự kháng thể đặc hiệu thường xuất hiện trong các tình trạng liên quan đến bệnh lý cơ viêm, bao gồm sự hiện diện của kháng thể kháng Jo và bệnh phổi kẽ. Các bệnh lý cơ liên quan đến bệnh lý thần kinh, suy thận và liên quan đến tim bị nghi ngờ là bệnh lý cơ do amyloid, và nên thực hiện điện di miễn dịch cố định các protein đơn dòng trong huyết thanh và nước tiểu.
Các nghiên cứu chẩn đoán điện
Các nghiên cứu dẫn truyền thần kinh (NCS) cảm giác và vận động thường bình thường trong các bệnh lý cơ; tuy nhiên, ở giai đoạn cuối của bệnh, biên độ điện thế hoạt động cơ phức hợp (CMAP) có thể bị giảm do teo cơ. Trên điện cơ đồ (EMG), các đặc điểm bệnh lý cơ của các điện thế hoạt động của đơn vị vận động (MUAP) hữu ý bao gồm kết tập sớm, thời khoảng ngắn, và các đơn vị vận động biên độ nhỏ với đa pha. Các thay đổi thần kinh mạn tính có thể thấy trong các giai đoạn cuối của bệnh do sự chết của các sợi cơ và mất các sợi trục thần kinh ngọn chi liên quan. Trong hoại tử cơ nghiêm trọng, sự kết tập của MUAP cho thấy bằng chứng và bao gồm tái phân bố thần kinh có hoặc không có sự hiện diện của mất phân bố thần kinh đang diễn ra.
Trương lực cơ được thấy trong một số bệnh lý trương lực cơ nhất định như loạn dưỡng cơ trương lực cơ và trương lực cơ bẩm sinh. Các bất thường khớp thần kinh-cơ có thể thấy trong một số bệnh lý cơ, chẳng hạn như bệnh lý cơ trung tâm nhân (CNM), do giảm biểu hiện thụ thể acetylcholine.
Sinh thiết cơ có thể cần thiết. Một cơ yếu thường được chọn với sức mạnh ít nhất là chống lại trọng lực hoặc bậc cơ trên 4 theo thang điểm của Hội đồng Nghiên cứu Y học (MRC); tuy nhiên, tốt nhất nên tránh một cơ quá yếu hoặc teo hoặc bậc cơ MRC dưới 3. Sinh thiết thường được lấy từ các cơ nhị đầu, cơ delta và cơ tứ đầu đùi nếu bệnh lý cơ ở gốc chi và từ cơ bụng chân và cơ chày trước trong các bệnh lý cơ ngọn chi.
| Kinh nghiệm lâm sàng
Tiếp cận lâm sàng đối với bệnh lý cơ nên tập trung vào các triệu chứng biểu hiện chính, tuổi khởi phát, sự hiện diện của các triệu chứng dương tính và âm tính, sự phân bố và kiểu hình yếu cơ và sự tiến triển, thời gian diễn biến, sự liên quan của cơ mặt, sự hiện diện của liên quan ngoài cơ, đáp ứng với điều trị, và sự hiện diện của các yếu tố thúc đẩy và làm nặng thêm. Chẩn đoán điện có thể hữu ích, và sinh thiết cơ và các nghiên cứu di truyền có thể xác nhận chẩn đoán. |
CÁC BỆNH LÝ CƠ ĐẶC HIỆU
Các bệnh lý loạn dưỡng cơ
Các bệnh lý loạn dưỡng cơ là một nhóm các rối loạn thần kinh-cơ di truyền được đặc trưng bởi yếu cơ tiến triển do các khiếm khuyết trong một hoặc nhiều gen liên quan đến cấu trúc và chức năng tế bào cơ bình thường.
LOẠN DƯỠNG CƠ DUCHENNE VÀ BECKER (CÁC BỆNH LÝ DYSTROPHIN) (HỘP 42.2, HÌNH 42.3 VÀ HÌNH 42.4)
DMD và BMD là các rối loạn lặn liên kết nhiễm sắc thể X biểu hiện ở các bé trai do đột biến gen dystrophin nằm trên locus Xp21. Gen dystrophin là một trong những gen mã hóa lớn nhất trong bộ gen của con người. DMD phổ biến và nghiêm trọng hơn BMD. Protein dystrophin là một protein tế bào chất nằm bên trong màng cơ (sarcolemma) và là một mỏ neo thiết yếu kết nối mỗi tế bào cơ với chất nền ngoại bào. Giảm hoặc không có dystrophin ở trẻ em bị ảnh hưởng có thể dẫn đến mất cơ, co rút khớp, vẹo cột sống, suy hô hấp, bệnh lý cơ tim và trong một số trường hợp làm suy giảm nhận thức. Những người nữ mang gen bệnh có thể biểu hiện các triệu chứng yếu cơ; tuy nhiên, bệnh lý cơ tim là đặc điểm thường gặp nhất và cần được theo dõi ở những bệnh nhân này. Ba mươi phần trăm các trường hợp là đột biến mới.
Tiến triển bệnh. Khởi phát của triệu chứng thay đổi, tùy thuộc vào lượng protein dystrophin chức năng có sẵn. Khởi phát lâm sàng của DMD bắt đầu ngay từ khi sinh, với trương lực cơ giảm và tăng CK máu; tuy nhiên, các dấu hiệu và triệu chứng lâm sàng thường không được nhận ra cho đến trung bình từ 2 đến 6 tuổi, mất khả năng đi lại độc lập có thể xảy ra trong độ tuổi từ 7 đến 13 ở những bệnh nhân không được điều trị bằng steroid, và từ 9 đến 16 tuổi ở những bệnh nhân được điều trị bằng steroid. Tử vong xảy ra do suy hô hấp hoặc suy tim thường trước thập niên thứ tư của cuộc đời. BMD nhẹ hơn, và các triệu chứng bắt đầu muộn hơn nhiều; mất khả năng đi lại có thể xảy ra trong thập niên thứ ba đến thứ sáu.
Đánh giá chẩn đoán. Chẩn đoán chính xác là điều cần thiết trong việc giảm tỷ lệ bệnh tật và tử vong. Các xét nghiệm sàng lọc ban đầu nên bao gồm CPK và aldolase. Các bất thường về gen có thể được xác định ở 98% đến 99% tất cả các bệnh nhân, và xét nghiệm di truyền phân tử phần lớn đã thay thế sinh thiết cơ. Định lượng dystrophin được thực hiện bằng Western blot và hóa mô miễn dịch.
Các bệnh lý đi kèm liên quan đến bệnh và quản lý. Bệnh lý cơ tim là một đặc điểm chính của DMD và BMD, với tuổi trung vị khởi phát của các bất thường trên siêu âm tim là từ 14 đến 15 tuổi và thậm chí sớm hơn. Chụp cộng hưởng từ tim nên được bắt đầu từ 6 đến 7 tuổi để phát hiện sớm các bất thường về sức căng (strain) và xơ hóa tim trước khi khởi phát rối loạn chức năng tâm thu. Nếu không có, nên thực hiện siêu âm tim. Bệnh nhân BMD có bệnh lý cơ tim đáng kể, có thể xuất hiện ở độ tuổi muộn hơn DMD, và ghép tim có thể cần thiết trong một số trường hợp. Các thuốc giảm hậu gánh như thuốc ức chế men chuyển angiotensin hoặc thuốc chẹn thụ thể angiotensin nên được bắt đầu dự phòng trước 10 tuổi hoặc sớm hơn nếu có bằng chứng suy giảm chức năng tim qua hình ảnh học. Các thuốc chẹn beta như carvedilol và thuốc ức chế aldosterone như spironolactone hoặc eplerenone cuối cùng được sử dụng ở hầu hết các bệnh nhân.
Suy giảm chức năng phổi hạn chế tiến triển phát triển ở bệnh nhân DMD vào cuối thập niên đầu tiên đến thập niên thứ hai. Đo chức năng hô hấp (PFT) và đa ký giấc ngủ thường quy rất quan trọng trong việc phát hiện sớm sự liên quan đến hô hấp. Áp lực hít vào tối đa và áp lực thở ra tối đa là những thông số phổi đầu tiên cho thấy sự suy giảm trong phần sau của thập niên đầu tiên.
Tỷ lệ giảm thông khí về đêm và tăng CO2 máu tăng lên khi bệnh tiến triển. Dung tích sống gắng sức (FVC) dưới 1 L là dấu hiệu của sự sống còn kém, với ước tính tỷ lệ sống sau 5 năm dưới 8%. Bắt đầu thông khí không xâm lấn (NIV) bằng áp lực đường thở dương hai mức (BiPAP) đã được chứng minh là cải thiện sự sống còn và bảo tồn năng lượng. Các chiến lược làm sạch đường thở có thể bắt đầu trong giai đoạn sớm đến cuối của giai đoạn không đi lại được để ngăn ngừa xẹp phổi, và việc bổ sung thông khí ban ngày có thể được chỉ định trong giai đoạn cuối không đi lại được. Thông khí xâm lấn bằng mở khí quản có thể được chỉ định trong tình trạng cấp tính nếu các phương pháp NIV đã thất bại hoặc trong tình trạng suy hô hấp mạn tính không đáp ứng với NIV 24 giờ bằng BiPAP. Oxy bị chống chỉ định trong bệnh lý đường thở hạn chế do bệnh lý cơ trừ khi có bệnh lý nhu mô phổi tiềm ẩn ảnh hưởng đến vận chuyển oxy qua các mô phổi.
Suy dinh dưỡng có thể liên quan đến tỷ lệ liên quan của bệnh phổi hạn chế tăng lên và can thiệp sớm vì vậy việc đánh giá thường xuyên cân nặng và chỉ số khối cơ thể nên được chuyên gia dinh dưỡng hoàn thành trong mỗi lần khám. Sử dụng steroid và bất động trong giai đoạn đầu của bệnh làm tăng nguy cơ béo phì và hội chứng chuyển hóa, trong khi chậm phát triển và sụt cân có thể xảy ra ở các giai đoạn sau của bệnh do yếu cơ, lượng calo hấp thụ dưới mức tối ưu, trạng thái tăng chuyển hóa và khó nuốt làm ảnh hưởng đến việc hấp thụ đủ qua đường miệng. Có thể cần đặt ống thông dạ dày qua da nội soi để hấp thụ calo và chất lỏng và để thông khí ra khỏi dạ dày trong tình trạng liệt dạ dày và NIV.
Khó nuốt là phổ biến trong DMD và có thể thấy ở 80% bệnh nhân, gần 100% ở giai đoạn cuối của bệnh. Các biến chứng nghiêm trọng có thể xảy ra, bao gồm mất nước, suy dinh dưỡng, viêm phổi hít và chậm phát triển. Đánh giá bởi chuyên gia ngôn ngữ trị liệu (SLP) là cần thiết. Bệnh nhân DMD có thể than phiền về khó nuốt cả chất lỏng và chất rắn. Những điều này được cho là do rối loạn chức năng miệng-hầu và thực quản, tương ứng. Nên xem xét và thảo luận thường xuyên về việc cho ăn bổ sung qua ống thông dạ dày.
Suy giảm tăng trưởng tuyến tính và dậy thì muộn là một đặc điểm phổ biến của DMD và có thể bị làm nặng thêm do sử dụng glucocorticoid. Tăng trưởng tuyến tính nên được đánh giá mỗi 6 tháng sau khi hoàn thành tăng trưởng tuyến tính sau tuổi dậy thì. Sự suy giảm tốc độ tăng trưởng tuyến tính dưới 4 cm mỗi năm phù hợp với suy giảm tăng trưởng và không có sự phát triển dậy thì trước 14 tuổi nên được chuyển đến bác sĩ nội tiết. Sức khỏe xương nên được tầm soát ở những bệnh nhân dùng glucocorticoid bằng X-quang cột sống nghiêng mỗi 2 năm và mỗi 3 năm ở những bệnh nhân không dùng steroid. Sự tham gia sớm của bác sĩ nội tiết để tối ưu hóa sức khỏe xương nên xảy ra khi mất khả năng đi lại hoặc ở dấu hiệu sớm nhất của gãy xương.
Co rút thường thấy đặc biệt là sau khi bất động, và chủ yếu liên quan đến cổ chân, gối và khuỷu tay, với sự bảo tồn tương đối của các khớp ngọn chi. Tầm vận động nên được đánh giá mỗi 6 tháng. Có thể xem xét chuyển đến phẫu thuật chỉnh hình để phẫu thuật kéo dài gân Achilles trong giai đoạn sớm đến cuối của giai đoạn đi lại được và đã được chứng minh là kéo dài thời gian đi lại trong một số trường hợp.
Vẹo cột sống là phổ biến và có thể tiến triển nhanh chóng, từ 16 đến 24 độ mỗi năm, với sự tiến triển nhanh nhất trong giai đoạn tăng vọt tăng trưởng tuổi dậy thì. Đánh giá vẹo cột sống hàng năm nên bắt đầu trong giai đoạn sớm đi lại được và mỗi 6 tháng trong giai đoạn sớm không đi lại được. Suy giảm hô hấp có thể xảy ra dẫn đến suy giảm cơ học của các cơ hô hấp làm nặng thêm bệnh lý đường thở hạn chế. FVC dưới 30% đến 40% giá trị dự đoán là một chỉ số của tăng tỷ lệ bệnh tật chu phẫu; tuy nhiên, nó không loại trừ can thiệp phẫu thuật cho vẹo cột sống. Nẹp thường không hiệu quả, và can thiệp bằng hợp nhất cột sống sau có thể được chỉ định trong các tình huống xác định với các đường cong lớn hơn 40 độ trong giai đoạn sớm đến cuối của giai đoạn không đi lại được.
Suy giảm chức năng nhận thức và trí nhớ có thể ảnh hưởng đến một tập hợp con nhất định các bé trai mắc DMD/BMD với các khiếm khuyết cụ thể trong học tập, bao gồm khiếm khuyết về khả năng ngôn ngữ, trí nhớ ngắn hạn và dài hạn, và chức năng điều hành. Lên đến một phần ba các bé trai mắc DMD, và, ở mức độ thấp hơn là BMD, có suy giảm nhận thức không tiến triển. Đánh giá nhận thức của bệnh nhân nên được thực hiện với trọng tâm là nhu cầu giáo dục và thực hiện các nguồn lực có sẵn, bao gồm các chương trình giáo dục cá nhân (IEP) và các kế hoạch khi cần thiết.
Các điều trị thay đổi bệnh. Sáu loại mục tiêu điều trị chính hiện đang được điều tra. Một loại giải quyết khiếm khuyết di truyền chính, bao gồm thay thế dystrophin hoặc điều hòa tăng utrophin. Phần còn lại giải quyết các khía cạnh hạ nguồn của bệnh sinh, bao gồm rối loạn chức năng ty thể, giảm viêm và xơ hóa, điều chỉnh lưu lượng máu và các rối loạn trong xử lý canxi, và tăng khối lượng cơ. Các mô hình tương lai có thể liên quan đến việc nhắm mục tiêu nhiều con đường để thúc đẩy tác động lớn hơn đến việc thay đổi bệnh.
Điều trị bằng prednisone với liều 0.75 mg/kg/ngày hoặc deflazacort với liều 0.9 mg/kg/ngày đã được chứng minh là cải thiện sức mạnh cơ bắp sau 6 tháng. Deflazacort với liều 0.9 mg/kg/ngày được cho là có hồ sơ tác dụng phụ thuận lợi hơn, đáng chú ý nhất là nguy cơ tăng cân thấp hơn.
LOẠN DƯỠNG CƠ EMERY-DREIFUSS (HỘP 42.5)
Loạn dưỡng cơ Emery-Dreifuss (EDMD) là một bệnh do những bất thường trong các protein màng nhân với sáu loại đã biết. Loại 1 là một rối loạn lặn liên kết nhiễm sắc thể X liên quan đến đột biến gen STA, mã hóa emerin, một protein xuyên màng nằm trên màng nhân trong. EDMD2 là kết quả của các đột biến được tìm thấy trên gen LMNA với các kiểu hình di truyền trội hoặc lặn trên nhiễm sắc thể thường. Đột biến gen LMNA mã hóa các protein màng nhân lamin A và C, các protein giàn giáo chính của màng nhân trong. Mất LMNA dẫn đến mất ổn định hạt nhân và thay đổi chức năng hạt nhân. Cả hai loại bao gồm một nhóm các bệnh lý cơ loạn dưỡng tiến triển được phân biệt bởi co rút khuỷu tay, gân Achilles và cột sống. Giả phì đại cơ thường không có, và sự tiến triển của bệnh chậm hơn nhiều so với DMD. Bệnh lý cơ tim với các bất thường dẫn truyền là phổ biến sau thập niên thứ hai hoặc thứ ba và có thể dẫn đến đột tử do tim; do đó chẩn đoán sớm là rất quan trọng. Mặc dù các yếu tố nguy cơ đối với các bất thường dẫn truyền tim là phổ biến ở cả hai thể EDMD, bệnh lý cơ tim giãn nở phổ biến hơn ở loại 2, có thể dẫn đến ghép tim trong các trường hợp nặng. Can thiệp sớm bằng máy tạo nhịp tim khi nhịp tim dưới 50 có thể cứu sống.
CPK tăng nhẹ. EMG sẽ cho thấy một kiểu hình bệnh lý cơ. Mô bệnh học cơ cho thấy một kiểu hình loạn dưỡng với sự thay đổi kích thước sợi cơ, thay thế cơ bằng mô liên kết và tái tạo sợi cơ. Nhuộm Nicotinamide adenine dinucleotide (NADH) có thể cho thấy hình ảnh nhậy gặm (moth-eaten).
LOẠN DƯỠNG CƠ MẶT-VAI-CÁNH TAY (HỘP 42.6)
FSHD là một bệnh lý cơ di truyền trội trên nhiễm sắc thể thường; nó biểu hiện bằng yếu tiến triển chậm ở các nhóm cơ cụ thể, bao gồm các cơ mặt, cơ vai và cơ cánh tay. Liên quan đến đai vai dẫn đến vai xuôi và yếu cơ bả vai. Khởi phát thay đổi trong độ tuổi từ 3 đến 44 nhưng thường xảy ra vào thập niên thứ hai. Thể bệnh phổ biến nhất là FSHD1, liên quan đến giảm methyl hóa dẫn đến co lại trên gen D4Z4. Bệnh lý di truyền này có liên quan đến 95% các trường hợp. FSHD2, thể ít phổ biến hơn, là kết quả của đột biến được tìm thấy trên gen SMCHD1 và chiếm khoảng 5% các trường hợp FSHD.
Liên quan đến mặt, mặc dù là dấu hiệu đặc trưng, có thể nhẹ và không đáng chú ý và không phải lúc nào cũng xuất hiện. Các cơ mặt phổ biến nhất bị liên quan là cơ vòng miệng và cơ vòng mắt, và cơ liên quan đến việc nâng khóe má, cơ gò má lớn. Thiếu biểu cảm trên khuôn mặt có thể biểu hiện sai cảm xúc và thường có thể dẫn đến khó khăn trong giao tiếp xã hội. Tuổi thọ thường không bị ảnh hưởng; tuy nhiên, trong khoảng 20% các trường hợp, việc phụ thuộc vào xe lăn là không thể tránh khỏi. Mặc dù yếu chi là đặc điểm nổi bật của bệnh, sự liên quan ngoài cơ có thể xảy ra và có thể đe dọa tính mạng. Suy hô hấp và liên quan đến tim có thể phát triển. Bệnh lý mạch máu võng mạc có thể xảy ra ở 75% bệnh nhân, nhưng các triệu chứng rõ ràng không phổ biến. Chuyển đến đo thính lực là cần thiết vì mất thính lực có thể xảy ra.
CPK tăng vừa phải, và phạm vi thay đổi. Chẩn đoán đã tiến bộ đáng kể bằng xét nghiệm di truyền thông qua Southern blot và các xét nghiệm methyl hóa. Sinh thiết cơ thường không được chỉ định và, nếu được thực hiện, sẽ cho thấy các sợi cơ thoái hóa và tái tạo trong giai đoạn đầu và viêm quanh mạch trong giai đoạn cuối cùng với xơ hóa.
LOẠN DƯỠNG CƠ MẮT-HẦU (HỘP 42.7)
OPMD là một bệnh lý cơ khởi phát muộn thường là di truyền trội trên nhiễm sắc thể thường và hiếm khi là lặn trên nhiễm sắc thể thường, biểu hiện vào thập niên thứ năm đến thứ sáu. Cả hai thể đều do sự mở rộng GCG trên gen polyadenylate-binding protein nuclear 1 (PABPN1). Nó được đặc trưng bởi sụp mi đối xứng tiến triển chậm, khó nuốt, thỉnh thoảng nhìn đôi, và yếu nhẹ các cơ mặt, cơ thái dương và cơ cắn, có thể dẫn đến bộ mặt bệnh lý cơ. Yếu cơ có thể xảy ra ở đai chậu và ít hơn ở đai vai và có thể nghiêm trọng hơn ở bệnh khởi phát sớm hơn. Tuổi thọ không giảm.
CPK có thể tăng gấp 2 đến 7 lần so với giá trị bình thường. Sinh thiết cơ sẽ cho thấy các thể vùi trong nhân trên kính hiển vi điện tử và có thể xác nhận chẩn đoán, nhưng chiến lược chẩn đoán này hiện đã được thay thế bằng xét nghiệm di truyền phân tử của gen PABPN1. Sinh thiết cơ có thể được bảo đảm trong các trường hợp gen PABPN1 bình thường. Khó nuốt có thể xuất hiện và có liên quan đến sụt cân nghiêm trọng và viêm phổi hít dẫn đến tăng tỷ lệ bệnh tật và tử vong. Phẫu thuật sụp mi bằng phẫu thuật tạo hình mi mắt hoặc treo mi vào cơ trán được khuyến nghị khi sụp mi cản trở thị lực hoặc gây đau cổ do duỗi cổ quá mức.
LOẠN DƯỠNG CƠ GỐC CHI (HỘP 42.8)
LGMD bao gồm một nhóm lớn các rối loạn bệnh lý cơ và có thể được phân loại là di truyền trội trên nhiễm sắc thể thường (loại 1) hoặc lặn trên nhiễm sắc thể thường (loại II). LGMD2 thường biểu hiện sớm hơn trong cuộc đời và nghiêm trọng hơn. Cho đến nay, hơn 30 phân nhóm khác nhau tồn tại và hơn 50 locus di truyền đã được xác định. Trong hầu hết các trường hợp, yếu cơ chủ yếu là đối xứng và thường ảnh hưởng đến cơ đai chậu và/hoặc đai vai. Các mức độ tiến triển của bệnh và các phát hiện về cơ và ngoài cơ khác nhau, bao gồm liên quan đến tim, hô hấp và nhận thức, có thể thấy tùy thuộc vào kiểu gen cụ thể. CPK có thể rất cao, và chẩn đoán điện cho thấy kiểu hình bệnh lý cơ. Sinh thiết cơ có thể chứng minh những thay đổi bệnh lý cơ. Phân tích DNA để tìm đột biến là phương pháp chẩn đoán chính.
| Kinh nghiệm lâm sàng
Nồng độ CK nên được sàng lọc ở trẻ em biểu hiện chậm phát triển hoặc yếu cơ. Giảm nồng độ CK ở bệnh nhân bệnh lý cơ có nồng độ cao trước đó có thể cho thấy sự tiến triển của bệnh. Liệu pháp steroid đã được chứng minh là làm chậm tốc độ suy giảm và kéo dài thời gian đi lại ở một số loại loạn dưỡng cơ. |
LOẠN DƯỠNG CƠ BẨM SINH
Loạn dưỡng cơ bẩm sinh (CMD) là một nhóm các bệnh không đồng nhất biểu hiện bằng yếu cơ khi sinh hoặc ở tuổi nhũ nhi với chậm các mốc phát triển và thường co rút bẩm sinh. Các khiếm khuyết di truyền có thể dẫn đến những bất thường trong các protein cấu trúc tế bào cơ, quá trình glycosyl hóa, lưới nội chất và các protein màng nhân.
Kiểu hình di truyền chủ yếu là lặn trên nhiễm sắc thể thường ngoại trừ CMD thiếu hụt collagen VI, có thể là lặn hoặc trội trên nhiễm sắc thể thường, và CMD liên quan đến LMNA, là di truyền trội trên nhiễm sắc thể thường. Trương lực cơ giảm và yếu cơ thường ổn định, mặc dù yếu cơ có thể nghiêm trọng với sự tiến triển nhẹ trong suốt cuộc đời. Các biến chứng không thường xuyên bao gồm suy hô hấp, khó nuốt nghiêm trọng, vẹo cột sống, co rút tiến triển và bệnh lý cơ tim. CPK thường bình thường nhưng có thể tăng trong các CMD thiếu hụt merosin. Xét nghiệm di truyền bằng panel CMD có thể chẩn đoán.
Các bệnh lý loạn dưỡng cơ di truyền ngọn chi
Các bệnh lý loạn dưỡng cơ di truyền ngọn chi (DIMD) là các bệnh lý loạn dưỡng cơ ngọn chi hiếm gặp được đặc trưng bởi yếu cơ tiến triển và teo cơ ngọn chi ở cánh tay và cẳng chân.
BỆNH LÝ CƠ NGỌN CHI WELANDER: LOẠI 1 KHỞI PHÁT MUỘN Ở NGƯỜI LỚN
Bệnh lý cơ ngọn chi Welander là một rối loạn di truyền trội trên nhiễm sắc thể thường và được tìm thấy chủ yếu ở Scandinavia. Khởi phát muộn hơn trong cuộc đời (cuối những năm 70). Các đặc điểm lâm sàng bao gồm yếu cơ duỗi cổ tay và ngón tay; yếu cơ duỗi ngón chân và cổ chân có thể xảy ra sau đó. Hiếm khi các cơ gốc chi sẽ bị liên quan. CPK bình thường hoặc tăng nhẹ, và sinh thiết cơ cho thấy các đặc điểm bệnh lý cơ với các không bào.
MARKESBERY-GRIGGS/UDD: LOẠI 2 KHỞI PHÁT MUỘN Ở NGƯỜI LỚN
Markesbery-Griggs/Udd là một bệnh lý cơ ngọn chi khởi phát muộn di truyền trội trên nhiễm sắc thể thường thường sau 40 tuổi với các đặc điểm đặc trưng là yếu ở khoang trước của cẳng chân dẫn đến yếu động tác gập mu và bàn chân rũ tiến triển. Sau đó trong quá trình bệnh, yếu ở các cơ gập cổ tay và ngón tay có thể xảy ra, cũng như liên quan đến cơ gốc chi. CPK bình thường hoặc tăng nhẹ, và sinh thiết cơ cho thấy các không bào rõ rệt. Xét nghiệm di truyền có thể phát hiện đột biến gen TTN.
BỆNH LÝ CƠ NGỌN CHI NONAKA/H-IBM: LOẠI 1 KHỞI PHÁT SỚM Ở NGƯỜI LỚN
Bệnh lý cơ ngọn chi Nonaka/h-IBM là một bệnh lý cơ ngọn chi di truyền lặn trên nhiễm sắc thể thường với khởi phát sớm hơn (trong những năm 20). Yếu cơ bắt đầu ở các cơ gập mu cổ chân và cơ duỗi ngón chân; cơ tứ đầu đùi thường được bảo tồn. Yếu tay ít nghiêm trọng hơn và có thể xảy ra sớm trong bệnh. CPK tăng nhẹ đến vừa phải, và sinh thiết cơ cho thấy một bệnh lý cơ không bào. Những phát hiện này tương tự như IBM; tuy nhiên, Nonaka có thể được phân biệt bằng tuổi khởi phát sớm hơn và các nghiên cứu di truyền dương tính.
BỆNH LÝ CƠ NGỌN CHI LAING: LOẠI 2 KHỞI PHÁT SỚM Ở NGƯỜI LỚN
Bệnh lý cơ ngọn chi Laing là một bệnh di truyền trội trên nhiễm sắc thể thường với yếu tiến triển ở khoang trước của cẳng chân và các cơ gập cổ dẫn đến bàn chân rũ và đầu rũ. Yếu cơ có thể lan đến các cơ gập ngón tay và cuối cùng đến các cơ gốc chi. CPK có thể gấp một đến ba lần giá trị bình thường và sinh thiết cơ cho thấy những thay đổi bệnh lý cơ mà không có không bào.
VIÊM CƠ THỂ VÙI DI TRUYỀN (h-IBM)
Có ba loại IBM di truyền. Loại 1 và 2 h-IBM là di truyền trội trên nhiễm sắc thể thường. Loại lặn là alen với Nonaka. Loại 2 h-IBM có khởi phát thay đổi nhưng phổ biến nhất ở thập niên thứ năm và liên quan đến bệnh Paget, xơ cứng teo cơ một bên và sa sút trí tuệ trán-thái dương. Loại 3 h-IBM được đặc trưng bởi cứng khớp bẩm sinh và yếu ngọn chi. CPK tăng nhẹ đến vừa phải, và sinh thiết cơ cho thấy các không bào có viền và các thể vùi.
Các bệnh lý loạn dưỡng trương lực cơ (Hộp 42.9 và Hộp 42.10)
LOẠN DƯỠNG CƠ TRƯƠNG LỰC CƠ LOẠI I VÀ II
Loạn dưỡng cơ trương lực cơ loại I và II là các rối loạn di truyền trội trên nhiễm sắc thể thường, hiếm gặp, tiến triển, ảnh hưởng đặc biệt đến nhiều hệ thống. DM1 là thể loạn dưỡng cơ người lớn phổ biến nhất do đột biến nhiễm sắc thể 19 và được đặc trưng bởi yếu cơ ngọn chi. DM2 là một kiểu hình nhẹ hơn với yếu cơ gốc chi chiếm ưu thế do đột biến nhiễm sắc thể 3. Cả hai bệnh đều do sự mở rộng lặp lại ba nucleotide.
LOẠN DƯỠNG CƠ TRƯƠNG LỰC CƠ LOẠI 1
Tuổi khởi phát trung bình của DM1 là 29. Trẻ em có thể biểu hiện trẻ hơn nhiều so với cha mẹ. Độ dài của các đoạn lặp lại tương quan nghịch với tuổi khởi phát. Những cá nhân bị ảnh hưởng có thể có từ 50 đến hàng nghìn đoạn lặp lại. Cả sự di truyền từ mẹ và cha đều có thể xảy ra, mặc dù sự di truyền từ cha thường ít nghiêm trọng hơn, vì tinh trùng có hơn 1000 đoạn lặp lại sẽ không có khả năng sống sót. Về mặt lâm sàng, DM1 biểu hiện bằng trương lực cơ nắm tay liên quan đến yếu ngọn chi tiến triển chậm, chủ yếu ảnh hưởng đến các cơ cẳng tay và các cơ mác và chày. Khi bệnh tiến triển, các cơ gốc chi cũng có thể bị ảnh hưởng. Teo cơ và co rút, thường là nhẹ, có thể xảy ra sau đó trong bệnh. Yếu cơ mặt dẫn đến bộ mặt bệnh lý cơ dài, gầy với sụp mi và nụ cười ngang. Trương lực cơ ngoài mắt có thể xuất hiện sau đó trong quá trình bệnh. Hói trán và teo cơ thái dương là những đặc điểm phổ biến và rõ ràng hơn ở nam giới. Khi thăm khám lâm sàng, các phát hiện cụ thể bao gồm trương lực cơ khi gõ, giảm phản xạ, và, trong một số trường hợp, có thể nhận thấy một bệnh lý viêm đa dây thần kinh ngoại biên đối xứng ngọn chi.
Một loạt các hệ cơ quan có thể bị liên quan trong DM1. Suy giảm nhận thức và chỉ số IQ ngôn ngữ và phi ngôn ngữ bất thường là phổ biến. Các bất thường về hành vi bao gồm tăng động, thiếu chú ý và hành vi tự kỷ, có thể dẫn đến hỗ trợ gia đình và xã hội kém, giáo dục kém và không có khả năng tuyển dụng. Liên quan đến tim có thể thấy ở 75% cá nhân. Rối loạn nhịp tim nhanh có thể dẫn đến ngất và đột tử. Suy hô hấp có thể phát triển và là nguyên nhân phổ biến nhất gây bệnh tật và tử vong. Giảm thông khí về đêm xảy ra thường xuyên. Các rối loạn nội tiết là phổ biến, bao gồm tăng nguy cơ kháng insulin và đái tháo đường loại 2. Giảm testosterone và ít tinh trùng ở nam giới dẫn đến các vấn đề về sinh sản. Các bất thường tuyến giáp và ung thư tuyến giáp có thể là di chứng. Đục thủy tinh thể hai bên là phổ biến và thường cần phẫu thuật. Liên quan đến cơ trơn có thể dẫn đến rối loạn vận động tiêu hóa, với cả tiêu chảy và táo bón. Khó nuốt là phổ biến, cũng như bệnh túi mật và viêm túi mật.
LOẠN DƯỠNG CƠ TRƯƠNG LỰC CƠ LOẠI 2
DM2 là một thể nhẹ hơn của loạn dưỡng cơ trương lực cơ ảnh hưởng đến các nhóm cơ gốc chi nhiều hơn ngọn chi. Tuổi khởi phát thay đổi, trong độ tuổi từ 8 đến 80, và mức độ nặng không liên quan đến sự mở rộng lặp lại CCTG. Các cơ mặt thường được bảo tồn, và trương lực cơ không có hoặc nhẹ, cần EMG để phát hiện. Đục thủy tinh thể nổi bật hơn và hầu như luôn thấy. Các bất thường dẫn truyền tim, đái tháo đường và mất thính lực xuất hiện ở 20% cá nhân. Sự liên quan đến cơ quan đa hệ thống bổ sung cũng có thể thấy nhưng thường nhẹ so với DM.
| Kinh nghiệm lâm sàng
Các bệnh lý loạn dưỡng cơ trương lực cơ là các rối loạn bệnh lý cơ hiếm gặp, di truyền trội trên nhiễm sắc thể thường, ảnh hưởng đến nhiều hệ thống. DM1 là thể loạn dưỡng cơ người lớn phổ biến nhất. Trương lực cơ được đặc trưng bởi không có khả năng thư giãn cơ sau khi co cơ hữu ý hoặc khi gõ. EMG cho thấy các điện thế tăng và giảm về biên độ và tần số với âm thanh bổ nhào (dive bomber) điển hình. |
LOẠN DƯỠNG CƠ TRƯƠNG LỰC CƠ BẨM SINH
Loạn dưỡng cơ trương lực cơ bẩm sinh xảy ra ở 25% trẻ nhũ nhi sinh ra từ các bà mẹ bị trương lực cơ và biểu hiện khi sinh với trương lực cơ giảm thường xuyên nghiêm trọng hoặc thậm chí trong tử cung với giảm cử động thai. Sự mở rộng lặp lại CTG lớn, thường lớn hơn 1000, và cha mẹ bị ảnh hưởng thường bị ảnh hưởng nghiêm trọng hơn. Những em bé này thường cần quản lý tại đơn vị chăm sóc tích cực (ICU) do suy hô hấp và khó nuốt nghiêm trọng. Hầu hết trẻ em được cai máy thở và học đi, nhưng các mốc phát triển thường bị chậm. Trẻ em thường có bàn chân khoèo cũng như co rút các khớp thái dương-hàm và các chi trên và dưới.
Chẩn đoán có thể được thực hiện bằng khám lâm sàng, và tiền sử gia đình và xét nghiệm di truyền phân tử là xác nhận. EMG cho thấy trương lực cơ nổi bật và các đặc điểm bệnh lý cơ. CPK bình thường hoặc tăng nhẹ, và sinh thiết cơ thường không còn được sử dụng nhưng các đặc điểm phổ biến bao gồm các nhân ở trung tâm, thay thế bằng mỡ và các cụm nhân đông đặc.
Các bệnh lý cơ bẩm sinh (Hộp 42.11 và Hình 42.12)
Các bệnh lý cơ bẩm sinh là các bệnh lý cơ hiếm gặp biểu hiện khi sinh hoặc ở tuổi nhũ nhi với trương lực cơ giảm và yếu cơ. Ở các thể nặng, những bệnh lý cơ này thường có thể tử vong nhanh chóng. Phân loại chủ yếu dựa trên các đặc điểm mô học sinh thiết cơ; tuy nhiên, xét nghiệm di truyền phân tử gần đây đã đóng một vai trò trong việc nhóm các đặc điểm kiểu hình và mô học cụ thể. Nồng độ CPK thường bình thường hoặc tăng nhẹ.
BỆNH LÝ CƠ NEMALINE
Bệnh lý cơ Nemaline có thể nhẹ, trung bình hoặc nặng. Kiểu hình di truyền là lặn hoặc trội trên nhiễm sắc thể thường. Có hơn 10 gen liên quan đến bệnh lý cơ nemaline. Phổ biến nhất là các đột biến lặn gen NEB; mã hóa protein nebulin chiếm 50% các trường hợp. Thể phổ biến nhất được đặc trưng bởi yếu động tác gập mu cổ chân và yếu cổ. Các dị dạng khuôn mặt độc đáo, vòm miệng cao và môi trên hình lều có thể dẫn đến khó nuốt và khó nói. Thể khởi phát sơ sinh nặng xảy ra ở khoảng 16% các trường hợp và liên quan đến trương lực cơ giảm nghiêm trọng, khó nuốt, cứng khớp và bệnh lý cơ tim. Liên quan đến cơ hoành là phổ biến và có thể dẫn đến suy hô hấp và viêm phổi hít. Sự tiến triển của bệnh thường tĩnh hoặc tiến triển rất chậm với sự bảo tồn IQ và các cơ mắt. Sinh thiết cơ cho thấy các thể vùi giống que nhỏ.
Các bệnh lý cơ lõi
Các bệnh lý cơ lõi đại diện cho một nhóm các bệnh lý cơ được đặc trưng bởi các đặc điểm sinh thiết cơ của chúng là giảm hoạt động oxy hóa trên nhuộm NADH, đại diện cho giảm hoạt động của ty thể. Các lõi trung tâm kéo dài toàn bộ sợi cơ của các sợi cơ loại 1 và trông giống như các mục tiêu ở trung tâm của sợi cơ. Các tiểu lõi ngắn hơn ở mặt cắt dọc và có thể ảnh hưởng đến cả hai loại sợi.
BỆNH LÝ CƠ LÕI TRUNG TÂM
Bệnh lý cơ lõi trung tâm liên quan đến đột biến RYR1, và các cá nhân có nguy cơ mắc MH. Các đặc điểm lâm sàng bao gồm trương lực cơ giảm khi sinh với yếu chi dưới gốc chi; không có dị dạng khuôn mặt phân biệt bệnh lý cơ này với các bệnh lý cơ bẩm sinh khác.
BỆNH LÝ CƠ ĐA LÕI (TIỂU LÕI)
Bệnh lý cơ đa lõi được đặc trưng bởi yếu cơ trục với kiểm soát đầu kém và cứng cột sống. Vẹo cột sống phát triển vào thập niên đầu tiên của cuộc đời. Các biến chứng bao gồm liên quan đến hô hấp và tim và vận nhãn.
BỆNH LÝ CƠ TRUNG TÂM NHÂN (HÌNH ỐNG)
Trên sinh thiết cơ, CNM cho thấy các nhân ở trung tâm, và trên mặt cắt dọc, các nhân ở trung tâm giống như các ống thần kinh của thai nhi, do đó tên bệnh lý cơ hình ống có thể liên kết nhiễm sắc thể X hoặc trội trên nhiễm sắc thể thường. Thể liên kết nhiễm sắc thể X phổ biến hơn với yếu cơ nghiêm trọng biểu hiện trong giai đoạn sơ sinh và liên quan đến suy hô hấp cần thông khí xâm lấn. Yếu cơ vận nhãn và cơ mặt là phổ biến, trong khi cơ tim và nhận thức thường được bảo tồn. Các đột biến trội trên nhiễm sắc thể thường liên quan đến bệnh khởi phát từ trung bình đến muộn với các đặc điểm cổ điển là yếu cơ, các biến dạng mặt bao gồm vòm miệng cao và liên quan đến vận nhãn.
BỆNH LÝ CƠ BẨM SINH MẤT CÂN ĐỐI LOẠI SỢI
Bệnh lý cơ bẩm sinh mất cân đối loại sợi (CFTD) là một chẩn đoán loại trừ, vì các phát hiện trên sinh thiết cơ của sợi loại I chiếm ưu thế với teo cơ là không đặc hiệu. Biểu hiện di truyền và kiểu hình là rộng, làm phức tạp thêm chẩn đoán.
| Kinh nghiệm lâm sàng
Các bệnh lý cơ bẩm sinh có triệu chứng khi sinh hoặc trong giai đoạn chu sinh với trương lực cơ giảm và yếu cơ, và một số loại có thể tử vong nhanh chóng. Sự hiện diện của liên quan đến mặt nổi bật có hoặc không có sụp mi, cùng với yếu và rối loạn chức năng của các cơ hô hấp và cơ hành não có thể giúp chẩn đoán phân biệt. CK bình thường hoặc tăng nhẹ. Cảm giác còn nguyên vẹn, và trí thông minh thường bình thường. |
Các bệnh lý trương lực cơ không loạn dưỡng (Hộp 42.13)
Các bệnh lý trương lực cơ không loạn dưỡng (NDM) là một nhóm các bệnh lý cơ di truyền hiếm gặp liên quan đến các rối loạn của các kênh ion màng cơ. Các đột biến liên quan tạo ra giảm hoặc tăng kích thích và có thể biểu hiện bằng trương lực cơ hoặc liệt chu kỳ và ở mức độ thấp hơn là yếu tiến triển.
Rối loạn kênh clorua (trương lực cơ bẩm sinh) là thể phổ biến nhất với di truyền trội hoặc lặn trên nhiễm sắc thể thường. Nó được đặc trưng về mặt lâm sàng bởi khó mở mắt sau khi nhắm mắt mạnh, méo mặt sau cơn khóc, và cứng chân với vài bước đầu tiên.
Rối loạn kênh natri có di truyền trội trên nhiễm sắc thể thường. Kiểu hình thay đổi và có thể biểu hiện bằng liệt chu kỳ tăng kali máu, trương lực cơ cận nghịch, trương lực cơ nặng thêm do kali, hoặc liệt chu kỳ hạ kali máu loại 2.
Rối loạn kênh kali (hội chứng Andersen-Tawil) là một hội chứng bộ ba hiếm gặp di truyền trội trên nhiễm sắc thể thường của liệt chu kỳ, rối loạn nhịp thất và các bất thường về xương. Bệnh nhân có thể biểu hiện rối loạn nhịp thất, có thể đe dọa tính mạng; hội chứng QT dài là phát hiện phổ biến nhất.
Chẩn đoán NDM dựa trên bệnh sử, thăm khám và đo nồng độ điện giải. CPK bình thường đến tăng nhẹ. Quản lý bao gồm quản lý triệu chứng của trương lực cơ, quản lý rối loạn nhịp tim nếu có, và dùng thuốc khi được chỉ định.
Các bệnh lý cơ chuyển hóa (Hộp 42.14)
Các bệnh lý cơ chuyển hóa là một nhóm các rối loạn di truyền không đồng nhất ảnh hưởng đến chuyển hóa carbohydrate và lipid. Trong các đợt gắng sức ngắn (<45 phút), nguồn năng lượng sinh học chính của cơ là từ phân hủy glycogen và đường phân. Tổn thương con đường này dẫn đến không dung nạp gắng sức, đau cơ, chuột rút, tăng CK máu và myoglobin niệu. Các bệnh lý cơ chuyển hóa có thể là tĩnh với yếu cơ cố định hoặc tiến triển hoặc động dẫn đến không dung nạp gắng sức.
CÁC RỐI LOẠN CHUYỂN HÓA GLYCOGEN
Bệnh McArdle
Bệnh McArdle (bệnh dự trữ glycogen loại V [GSD V]) là một rối loạn di truyền lặn trên nhiễm sắc thể thường. Đây là bệnh lý cơ chuyển hóa phổ biến nhất của chuyển hóa carbohydrate và là do đột biến gen PYGM mã hóa myophosphorylase. Các triệu chứng thường biểu hiện ở trẻ em hoặc thanh niên và biểu hiện là không dung nạp gắng sức do đau và chuột rút sau khi gắng sức ngắn hoặc rất dữ dội thường được thuyên giảm bằng nghỉ ngơi. Hiện tượng “lấy lại sức” là đặc trưng. GSD V liên quan đến myoglobin niệu và tiêu cơ vân, có thể bị biến chứng bởi suy thận ở khoảng một phần ba các trường hợp. Co rút không có điện thế hoạt động có thể phát triển giữa các cơn. Một số bệnh nhân có thể phát triển yếu gốc chi tiến triển theo thời gian, tiến triển thành yếu cố định, nhưng hầu hết bệnh nhân có thăm khám bình thường giữa các cơn.
Nồng độ CPK có thể tăng ở các mức độ khác nhau tùy thuộc vào mức độ hoạt động. Nghiên cứu chẩn đoán điện thường bình thường. Thử nghiệm gắng sức cẳng tay cho thấy sự gia tăng bình thường của amoniac huyết thanh nhưng không có sự gia tăng đáng kể của axit lactic. Trên sinh thiết cơ, nhuộm myophosphorylase không có hoặc giảm, và ghi nhận sự tích tụ glycogen dưới sarcolemma và giữa các sợi cơ trong các không bào. Xét nghiệm di truyền cho thấy đột biến PYGM. Quản lý tập trung vào việc tránh các bài tập gắng sức mạnh để giảm nguy cơ tiêu cơ vân. Các triệu chứng có thể giảm bằng một bài tập cường độ thấp được giám sát trong 5 đến 10 phút trước khi tập thể dục vừa phải hơn. Uống sucrose trước khi gắng sức đã được chứng minh là cải thiện khả năng dung nạp gắng sức, nhưng điều này có thể dẫn đến tăng cân và có khả năng ức chế việc sử dụng axit béo với các bài tập aerobic kéo dài hơn.
Bệnh Pompe/Thiếu hụt Acid Maltase (Bệnh Glycogenosis loại II)
Bệnh Pompe cũng là bệnh di truyền lặn trên nhiễm sắc thể thường và dẫn đến tích tụ glycogen trong cơ xương, cơ tim và cơ trơn có thể dẫn đến chết tế bào. Phổ lâm sàng rộng, bao gồm các thể ở trẻ nhũ nhi, trẻ em và người lớn, và mức độ nặng của bệnh tương quan nghịch với lượng enzyme có sẵn trong tế bào cơ. Ở thể trẻ nhũ nhi, không có mức enzyme đo được. Người lớn thường có kiểu hình nhẹ hơn với hoạt động enzyme đo được khoảng 20%. Thể trẻ nhũ nhi được đặc trưng bởi trương lực cơ giảm khi sinh, tim to và lưỡi to. Yếu tiến triển, khó nuốt và suy hô hấp thường dẫn đến tử vong trước 2 tuổi. Khởi phát ở trẻ em biểu hiện trước thập niên đầu tiên của cuộc đời với chậm các mốc phát triển vận động và yếu tiến triển chậm liên quan đến các cơ gốc chi ở chân và tay. Những trẻ này có kiểu hình BMD/DMD. Tim to và phì đại lưỡi ít phổ biến hơn thể trẻ nhũ nhi; tuy nhiên, yếu cơ và suy hô hấp là tiến triển, dẫn đến tử vong vào thập niên thứ hai hoặc thứ ba.
Bệnh khởi phát ở người lớn thường biểu hiện trong khoảng thập niên thứ ba và thứ tư với yếu gốc chi và thân mình cố định và khi gắng sức. Sụp mi, teo cơ cạnh sống và xương bả vai cánh chim cũng phổ biến. Yếu cơ hô hấp là phổ biến ở 80% các trường hợp, với các triệu chứng ảnh hưởng đến cả cơ hít vào và thở ra. Yếu cơ hoành có thể thấy, và PFT cho thấy giảm FVC hơn 25% từ tư thế ngồi sang nằm ngửa. Bệnh lý cơ tim phì đại là một đặc điểm phổ biến, và một số có thể có các bất thường dẫn truyền. Hội chứng Wolf-Parkinson-White đã được báo cáo ở cả thể người lớn và trẻ nhũ nhi. Bệnh lý giãn mạch cũng có thể xảy ra, làm tăng nguy cơ xuất huyết dưới nhện.
ĐÁNH GIÁ CHẨN ĐOÁN.
Xét nghiệm enzyme trên giọt máu khô được thực hiện như công cụ sàng lọc hàng đầu để thiết lập hoạt động của enzyme acid maltase và nhạy hơn sinh thiết cơ. Xác nhận chẩn đoán được thực hiện bằng xét nghiệm di truyền phân tử của gen GAA. CPK huyết thanh có thể rất cao, lên đến 10 lần giới hạn bình thường. NCS bình thường, và EMG cho thấy các phát hiện mất phân bố thần kinh mạn tính. Các phóng điện trương lực cơ cũng có thể thấy.
QUẢN LÝ.
Alglucosidase alpha (GAA người) đã được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ phê duyệt vào năm 2006 cho bệnh Pompe. Bắt đầu sớm alglucosidase ở người lớn liên quan đến cải thiện đáp ứng cơ xương khớp và ổn định chức năng phổi. Bệnh nhân nên được sàng lọc thường xuyên bệnh lý cơ tim, ngoài PFT thường quy để đánh giá suy hô hấp.
CÁC RỐI LOẠN CHUYỂN HÓA LIPID
Thiếu hụt Carnitine Palmitoyltransferase II
Thiếu hụt Carnitine palmitoyltransferase II (CPTII) là một rối loạn di truyền trội trên nhiễm sắc thể thường và là khiếm khuyết oxy hóa axit béo phổ biến nhất ở người lớn. Tăng canxi tự do trong bào tương và ty thể do cạn kiệt adenosine triphosphate xảy ra gây tổn thương tế bào cơ. Các triệu chứng thường bắt đầu trong thập niên thứ hai và thứ ba của cuộc đời và được kích hoạt bởi gắng sức dữ dội hoặc kéo dài và bệnh có sốt. Các triệu chứng bao gồm yếu cơ, đau cơ, chuột rút và myoglobin niệu tái phát. Yếu cơ thường không kéo dài ngoài các cơn. Thể khởi phát ở trẻ em ít phổ biến hơn và liên quan đến suy gan và bệnh lý cơ tim. Tổn thương thận cấp tính có thể là kết quả của tiêu cơ vân nghiêm trọng. Nồng độ CPK thường bình thường giữa các cơn. Tuy nhiên, chúng có thể cao tới 400 lần giá trị bình thường sau một cơn. Quản lý bao gồm tránh tập thể dục kéo dài, và khuyến nghị nhịn ăn kéo dài cũng như chế độ ăn bổ sung axit béo chuỗi trung bình và carbohydrate.
Thiếu hụt Carnitine
Thiếu hụt carnitine nguyên phát toàn thân (CDSP) là một rối loạn di truyền lặn trên nhiễm sắc thể thường của vận chuyển carnitine. Carnitine là một cơ chất quan trọng trong chuyển hóa axit béo. CDSP là một rối loạn không đồng nhất về mặt lâm sàng liên quan đến khởi phát, liên quan đến cơ quan và mức độ nặng thay đổi. Biểu hiện phổ biến nhất ở trẻ nhỏ hoặc trẻ nhũ nhi bao gồm bệnh lý cơ tim, hội chứng Reye và hạ đường huyết không tăng ceton theo đợt. Người lớn có thể chỉ có yếu cơ gốc chi tiến triển nhẹ. Thiếu hụt carnitine thứ phát có thể là kết quả của các bệnh lý mắc phải khác nhau như suy dinh dưỡng, các bệnh lý nội tiết, tác dụng độc của thuốc, suy thận hoặc gan, hoặc từ các bệnh lý loạn dưỡng cơ di truyền.
CHẨN ĐOÁN
Nồng độ carnitine tự do trong huyết tương cực kỳ thấp (<5 μΜ [bình thường 25-50 μΜ]). Nồng độ carnitine trong cơ có thể giảm đáng kể. Nồng độ CPK có thể bình thường hoặc tăng, và có thể thấy hạ đường huyết và tăng men gan. Trong thiếu hụt carnitine thứ phát, nồng độ carnitine có thể giảm vừa phải.
QUẢN LÝ
L-carnitine đường uống có thể cung cấp một số lợi ích. Nồng độ carnitine nên được đo thường xuyên để đảm bảo bổ sung đầy đủ. Sàng lọc tim mạch thường quy, bao gồm siêu âm tim và điện tâm đồ, nên được thực hiện.
CÁC BỆNH LÝ CƠ TY THỂ (HỘP 42.15)
Các bệnh lý cơ ty thể là một nhóm các rối loạn di truyền từ mẹ hiếm gặp với kiểu hình rất đa dạng do các khiếm khuyết hoặc đột biến của bộ gen ty thể (mtDNA) ảnh hưởng đến nhiều hệ cơ quan và dẫn đến yếu cơ tiến triển do suy giảm quá trình phosphoryl hóa oxy hóa và chuyển hóa năng lượng.
Động kinh giật cơ với sợi đỏ rách rưới
Động kinh giật cơ với sợi đỏ rách rưới biểu hiện ở cuối tuổi vị thành niên đến đầu tuổi trưởng thành. Các đặc điểm lâm sàng bao gồm bệnh lý cơ gốc chi và các cơn co giật giật cơ toàn thể có thể nhạy cảm với ánh sáng. Thất điều tiểu não (70%), teo dây thần kinh thị giác (20%) và đau nửa đầu migraine (50%) là các đặc điểm lâm sàng phổ biến khác. Rối loạn chức năng hô hấp có thể xảy ra ở 65% bệnh nhân, và liên quan đến hành não với khó nuốt và khó nói ở 40%. Cũng có thể thấy một bệnh lý thần kinh ngoại biên cảm giác vận động ngọn chi nhẹ.
Bệnh não cơ ty thể, nhiễm toan lactic, và các cơn giống đột quỵ
Bệnh não cơ ty thể, nhiễm toan lactic, và các cơn giống đột quỵ (MELAS) thường biểu hiện ở trẻ em, với yếu cơ gốc chi tiến triển (50%) và tầm vóc thấp. Đau đầu từng đợt mạn tính, co giật, bệnh não và các cơn giống đột quỵ không liên tục lan tỏa có thể phát triển do tăng kích thích thần kinh. Bệnh lý cơ tim có thể xảy ra ở 40% bệnh nhân với sự gia tăng liên quan đến tỷ lệ bệnh tật và tử vong. Các mốc phát triển vận động và nhận thức sớm thường đạt được, theo sau là sự suy giảm tiến triển về chức năng vận động và nhận thức, với sa sút trí tuệ ở 60% bệnh nhân.
Liệt mắt ngoài tiến triển
Liệt mắt ngoài tiến triển (PEO) thường là rời rạc, với tần suất tăng nhẹ ở dân số Phần Lan. Các phân nhóm PEO bao gồm hội chứng Kearns-Sayre (KSS) và phổ bệnh lý thần kinh thất điều. KSS được đặc trưng bởi bộ ba triệu chứng, bao gồm khởi phát sớm, thường dưới 20 tuổi, và PEO và viêm võng mạc sắc tố. Các triệu chứng bổ sung có thể xảy ra, bao gồm khó nuốt và yếu cơ gốc chi nhiều hơn ngọn chi, và nó thường rõ rệt hơn khi gắng sức hoặc mệt mỏi. Một tình trạng tương tự được gọi là CPEO-plus tương tự như KSS với các phát hiện bổ sung về thất điều tiểu não, các dấu hiệu bó tháp, thường là các bất thường dẫn truyền tim, tầm vóc thấp và sa sút trí tuệ.
Bệnh não-cơ-thần kinh-tiêu hóa ty thể
Bệnh não-cơ-thần kinh-tiêu hóa ty thể thường bắt đầu trước 20 tuổi, với các đặc điểm nổi bật là rối loạn vận động tiêu hóa có và không có bệnh não. Suy giảm nhận thức có thể xảy ra ở 10% bệnh nhân. Yếu cơ có thể ở gốc chi và ngọn chi. Các biểu hiện hệ thống khác có thể bao gồm tầm vóc thấp, sụp mi, liệt mắt, mất thính lực và viêm đa dây thần kinh.
CHẨN ĐOÁN
Nồng độ CPK bình thường hoặc tăng nhẹ. Lactate cao thường thấy nhưng có thể bình thường. Tỷ lệ lactate/pyruvate cao (> 50:1) gợi ý block chuyển hóa trong chuỗi hô hấp; tuy nhiên, tỷ lệ bình thường có thể gợi ý một block chuyển hóa cao hơn trong chuỗi hô hấp. Yếu tố tăng trưởng nguyên bào sợi 21 thường cao nhưng không đặc hiệu. Các sợi đỏ rách rưới xuất hiện trên nhuộm Gomori trichrome sửa đổi. Các panel di truyền bệnh lý cơ ty thể có sẵn.
QUẢN LÝ
Tránh các loại thuốc độc hại cho ty thể là rất quan trọng. Bổ sung các thành phần chuỗi hô hấp và các hỗn hợp ty thể, bao gồm coenzyme Q10, có thể hữu ích. Các cơn giống đột quỵ trong MELAS có thể được điều trị bằng taurine để giảm tần suất của chúng. Xét nghiệm tim mạch và PFT thường quy là rất quan trọng. Khám mắt và xét nghiệm thính lực thường xuyên là rất quan trọng. Phẫu thuật tạo hình mi mắt có thể cải thiện thị lực trong các trường hợp sụp mi và liệt mắt nghiêm trọng hơn. Khó nuốt nên được theo dõi, và có thể cần nghiên cứu nuốt bằng X-quang tăng sáng truyền hình (videofluoroscopic swallow study). Tập thể dục trị liệu rất quan trọng để duy trì sức mạnh và sự linh hoạt.
| Kinh nghiệm lâm sàng
Các bệnh lý cơ chuyển hóa là các rối loạn ảnh hưởng đến chuyển hóa carbohydrate và lipid, và các bệnh lý cơ ty thể là do các khiếm khuyết hoặc đột biến của bộ gen ty thể (mtDNA); cả hai thường liên quan đến yếu cơ và không dung nạp gắng sức. Tiêu cơ vân và myoglobin niệu liên quan đến các bệnh lý cơ chuyển hóa, trong khi liên quan đến hệ thống (ví dụ, mất thính lực hoặc thị lực, sụp mi, hoặc liệt mắt) liên quan đến các bệnh lý cơ ty thể. |
CÁC BỆNH LÝ CƠ MẮC PHẢI ĐẶC HIỆU (HỘP 42.16)
Các bệnh lý cơ viêm tự phát
Các bệnh lý cơ viêm tự phát (IIMs), được gọi chung là viêm cơ, bao gồm một nhóm các bệnh lý mắc phải của cơ xương với sự liên quan đa hệ thống thay đổi; bệnh sinh của chúng phần lớn là tự miễn. Yếu cơ gốc chi đối xứng là kiểu hình yếu cơ phổ biến nhất; tuy nhiên, yếu ngọn chi phổ biến hơn trong IBM. Nó ảnh hưởng đến người lớn nhiều hơn trẻ em, ngoại trừ DM khởi phát ở trẻ em. Phụ nữ thường bị ảnh hưởng nhiều hơn nam giới, ngoại trừ trường hợp IBM, ảnh hưởng đến nam giới nhiều hơn phụ nữ. Tất cả các IIM, ngoại trừ IBM, đã được chứng minh là có liên quan đến tần suất ung thư cao hơn; tuy nhiên, DM ở người lớn có liên quan cao nhất đến ung thư.
Viêm da cơ
DM có thể biểu hiện ở cả trẻ em và người lớn với yếu cơ đối xứng gốc chi âm thầm hoặc bán cấp, đau khớp, và có thể liên quan đến các biểu hiện da đặc trưng, bao gồm dấu hiệu khăn choàng hoặc chữ V, sẩn Gottron, và ban đỏ hình cánh bướm. Các lắng đọng canxi được gọi là vôi hóa có thể phân bố dọc theo các điểm tỳ đè, bao gồm gối, khuỷu tay và mông. Khó nuốt có thể xảy ra ở 30% các trường hợp. Nguy cơ ung thư cao nhất với DM và thường được chẩn đoán trong vòng 3 đến 5 năm kể từ khi khởi phát bệnh và liên quan đến khoảng 15% các trường hợp người lớn, với ung thư đại trực tràng, buồng trứng và phổi là các khối u ác tính liên quan nhiều nhất. CPK có thể bình thường hoặc tăng lên đến 50 lần giới hạn trên của mức bình thường.
Hội chứng kháng Synthetase
Hội chứng kháng synthetase là một phân nhóm mới hơn của IIM và biểu hiện bằng yếu cơ gốc chi đối xứng, được phân biệt độc đáo bởi sự liên quan cao với các kháng thể kháng Jo-1 có liên quan cao đến sự phát triển của bệnh phổi kẽ. Các phát hiện chính khác bao gồm viêm khớp, hội chứng Raynaud và bàn tay thợ cơ khí. CPK có thể bình thường hoặc tăng vừa phải.
Viêm đa cơ
Viêm đa cơ (PM) là một loại IIM hiếm gặp, chiếm dưới 5% tất cả các trường hợp, và được coi là một chẩn đoán loại trừ. Chẩn đoán thường bị trì hoãn. Một phần ba các trường hợp biểu hiện bằng yếu cơ gốc chi đối xứng bán cấp hoặc âm thầm có hoặc không có yếu gập cổ và khó nuốt. Đau cơ có thể xảy ra sau đó trong quá trình tiến triển của bệnh. Tuổi khởi phát thường trên 20 tuổi. CPK luôn tăng và thường rất cao (50 lần giới hạn trên của mức bình thường). Aldolase, AST, ALT và lactate cũng tăng. Nguy cơ ung thư cũng tăng, nhưng mối liên quan không mạnh bằng DM.
Viêm cơ hoại tử tự miễn
Viêm cơ hoại tử tự miễn (NAM) chiếm khoảng 20% tất cả các IIM và thường bị chẩn đoán nhầm là viêm đa cơ. Nồng độ CPK tăng trong tất cả các trường hợp và có thể cao tới 10 lần giới hạn trên của mức bình thường. Anti-HMGCR đặc hiệu cho NAM và có thể liên quan đến việc sử dụng statin hoặc từ các nguồn khác, bao gồm cả các nguồn nội sinh. Tuy nhiên, nếu có sử dụng statin, yếu cơ có thể tiến triển quá 2 tháng sau khi ngừng statin. Các kháng thể khác liên quan đến NAM bao gồm anti-SRP.
Viêm cơ thể vùi
IBM là một bệnh lý cơ viêm âm thầm ảnh hưởng đến nam giới nhiều hơn nữ giới. Nó có thể được phân biệt về mặt lâm sàng với tất cả các IIM khác bởi kiểu hình yếu không đối xứng ảnh hưởng chủ yếu đến cẳng tay, các cơ gập ngón tay, cơ tứ đầu đùi và cơ chày trước. Khó nuốt là phổ biến và có thể là triệu chứng biểu hiện ban đầu. Tăng CPK nhẹ hơn, với phạm vi từ bình thường đến tăng nhẹ (10-15 lần giới hạn trên của mức bình thường). Kháng thể liên quan nhiều nhất là NT5C1A và có thể thấy ở 60% các trường hợp. Dữ liệu gần đây cho thấy mức độ nặng của bệnh và tỷ lệ tử vong cao hơn.
CHẨN ĐOÁN
Kiểu hình yếu cơ trên lâm sàng và các phát hiện da đặc trưng là rất quan trọng, và nồng độ CPK tăng có thể gợi ý IIM; tuy nhiên, CPK bình thường không loại trừ chẩn đoán, ngoại trừ NAM vì với bệnh này CPK luôn tăng. Sinh thiết cơ có thể chẩn đoán trong hầu hết các trường hợp IIM. Các đặc điểm mô học của IBM bao gồm viêm nội cơ, các không bào có viền, và sự xâm nhập của các tế bào T CD8+ gây độc tế bào. DM bao gồm viêm quanh bó cơ và teo quanh bó cơ và tăng phức hợp tương hợp mô chính loại 1. PM có thể được phân biệt với DM bởi viêm nội cơ. Sự xâm nhập của các sợi cơ bởi các tế bào T CD8+ cũng có thể thấy trong PM; tuy nhiên, không nên có các không bào có viền. NCS bình thường ngoại trừ các trường hợp yếu cơ đáng kể, và EMG có thể cho thấy các đặc điểm bệnh lý cơ. Các panel tự kháng thể viêm cơ toàn diện có sẵn.
QUẢN LÝ
Hầu hết bệnh nhân đáp ứng hợp lý với điều trị ức chế miễn dịch, ngoại trừ những người mắc IBM. Glucocorticosteroid là điều trị hàng đầu ban đầu trong IIM và đã được chứng minh là cải thiện các triệu chứng bệnh ở hầu hết các bệnh nhân. Điều trị ban đầu bao gồm liệu pháp liều cao với prednisolone 60 mg/ngày được giảm dần khi bệnh ổn định. Thường cần một liều duy trì 5 mg/ngày. Các thuốc ức chế miễn dịch bổ sung có thể được sử dụng để điều trị duy trì bao gồm methotrexate, azathioprine và mycophenolate mofetil. Các phương pháp điều trị đã được thiết lập tốt khác bao gồm globulin miễn dịch đường tĩnh mạch, đặc biệt là trong DM và NAM (Viêm cơ hoại tử tự miễn). Trong một số trường hợp kháng trị, nên xem xét điều trị bằng rituximab và cyclophosphamide. Sàng lọc bệnh ác tính nên được thực hiện, tại thời điểm chẩn đoán, và sau đó đều đặn. Glucocorticosteroid tại chỗ có thể được sử dụng nếu có phát ban. Bệnh phổi kẽ cho thấy mức độ nặng và có thể cần một chế độ ức chế miễn dịch tiên tiến hơn. Các chương trình phục hồi chức năng đa ngành bao gồm các bài tập nhẹ đến vừa phải, cung cấp dụng cụ chỉnh hình và các dụng cụ trợ giúp có thể cải thiện khả năng đi lại và chức năng. Quản lý khó nuốt và các rối loạn nuốt là vô cùng quan trọng.
| Kinh nghiệm lâm sàng
Các bệnh lý cơ viêm là một nhóm các rối loạn bệnh lý cơ mắc phải hiếm gặp. Bệnh sinh của chúng phần lớn là tự miễn. Tất cả ngoại trừ IBM biểu hiện bằng yếu gốc chi đối xứng bán cấp, đáp ứng tốt với liệu pháp miễn dịch, ảnh hưởng đến nữ giới nhiều hơn nam giới, và liên quan đến tần suất ung thư cao. PM được coi là một chẩn đoán loại trừ. |
CÁC BỆNH LÝ CƠ CHUYỂN HÓA MẮC PHẢI
Các bệnh lý cơ nội tiết
CÁC BỆNH LÝ CƠ DO NHIỄM ĐỘC GIÁP
Bệnh lý cơ do tuyến giáp có thể thấy ở khoảng ba phần tư bệnh nhân suy giáp. Các than phiền phổ biến bao gồm yếu cơ gốc chi, không dung nạp gắng sức, đau cơ và mệt mỏi. Các phản xạ có vẻ nhanh nhạy do giai đoạn thư giãn chậm. Nồng độ CPK có thể bình thường hoặc tăng nhẹ. Bệnh lý cơ cũng thấy với nhiễm độc giáp, nhưng với điều trị, sức mạnh cơ bắp có thể trở lại sau vài tháng.
BỆNH LÝ CƠ DO CORTICOSTEROID
Bệnh lý cơ do corticosteroid có thể do cả nguyên nhân ngoại sinh và nội sinh. Tiếp xúc mạn tính với liều cao corticosteroid uống tổng hợp (> 30 mg/ngày) có nguy cơ teo cơ ảnh hưởng chủ yếu đến các sợi cơ giật nhanh loại IIb đường phân. Tuy nhiên, bệnh lý cơ do steroid cũng có thể xảy ra sau một thời gian ngắn tiếp xúc với corticosteroid uống. Bệnh lý cơ toàn thể nặng cấp tính có thể thấy ở liều cao corticosteroid IV. Phụ nữ có nguy cơ cao hơn nam giới (2:1). Các biểu hiện lâm sàng bao gồm yếu cơ gốc chi và diện mạo Cushing. Các phản xạ bình thường. CPK bình thường hoặc tăng nhẹ; tuy nhiên, kali huyết thanh có thể thấp do dư thừa glucocorticoid dẫn đến yếu cơ thêm. NCS bình thường. Điện cơ kim bình thường hoặc có thể cho thấy những thay đổi bệnh lý cơ nhẹ và các điện thế rung giật. Sinh thiết cơ cho thấy teo sợi cơ loại 2. Quản lý bao gồm giảm liều steroid dung nạp được.
Các bệnh lý cơ do độc chất
Nhiều chất, cả kê đơn và giải trí, có thể độc hại đối với mô cơ. Rượu, cũng như nhiều loại thuốc kê đơn như thuốc hạ cholesterol, gây ra bệnh lý cơ. Biểu hiện lâm sàng rộng và từ đau cơ nhẹ đến yếu cơ nghiêm trọng, suy cơ quan và tử vong. Quản lý bao gồm loại bỏ tác nhân gây bệnh, có thể làm giảm đáng kể hoặc loại bỏ tỷ lệ bệnh tật và tử vong.
BỆNH LÝ CƠ LIÊN QUAN ĐẾN RƯỢU
Sử dụng rượu nhiều hàng ngày có thể gây ra bệnh lý cơ hoại tử hoặc bệnh lý cơ hạ kali máu và thường liên quan đến các bệnh lý đi kèm phổ biến khác liên quan đến rượu, bao gồm bệnh lý cơ tim giãn nở và bệnh lý thần kinh ngoại biên. Bệnh sinh được cho là do chất chuyển hóa độc hại và sự tích tụ gốc tự do ảnh hưởng đến màng lipid, hoặc suy dinh dưỡng liên quan đến nghiện rượu. Bệnh lý cơ hoại tử độc tính cấp tính có thể biểu hiện sau khi uống nhiều rượu, với đau cơ, khó chịu, yếu cơ gốc chi và suy thận cấp. Myoglobin niệu và tăng CK máu hầu như luôn xuất hiện. EMG có thể cho thấy một bệnh lý cơ kích thích, và sinh thiết cơ có thể phát hiện hoại tử cơ lan tỏa và các không bào. Bệnh lý cơ hạ kali máu tiếp theo có thể phát triển. Với việc ngừng rượu, yếu cơ có thể cải thiện trong vài tuần, và nồng độ CPK có thể trở lại bình thường.
BỆNH LÝ CƠ DO THUỐC
Các thuốc hạ cholesterol là nguyên nhân phổ biến nhất của bệnh lý cơ hoại tử; chúng có thể biểu hiện bằng đau cơ, yếu cơ gốc chi và tăng CK máu. Nó sẽ giải quyết trong vòng vài tháng sau khi ngừng statin nếu không liên quan đến bệnh lý cơ tự miễn do statin. Các trường hợp nặng có thể bị biến chứng bởi myoglobin niệu và suy thận. Các thuốc hạ cholesterol khác, bao gồm niacin, ezetimibe và các dẫn xuất axit fibric (fenofibrate và gemfibrozil), đã có liên quan đến bệnh lý cơ, nhưng statin có liên quan cao nhất. Nhiều loại thuốc và độc chất khác có thể gây ra bệnh lý cơ và nằm ngoài phạm vi của chương này. Tuy nhiên, một số trong số này là các immunophilin (cyclosporine và tacrolimus), thuốc chống tăng huyết áp (labetolol), propofol và nọc rắn liên quan đến các bệnh lý cơ hoại tử. Các thuốc kháng virus như azidothymidine (AZT) có thể gây ra bệnh lý cơ ty thể. Bệnh lý cơ do thuốc lưỡng phần bao gồm tiếp xúc với chloroquine và amiodarone, liên quan đến một bệnh lý thần kinh-cơ với các triệu chứng của bệnh lý thần kinh và yếu cơ gốc chi không đau ảnh hưởng đến cánh tay nhiều hơn cẳng chân. Amiodarone cũng có thể gây run và thất điều. Nồng độ CPK tăng, và NCS cho thấy một bệnh lý thần kinh cảm giác vận động sợi trục nhẹ. Trên sinh thiết cơ, thấy các không bào tự thực ngoài teo cơ do thần kinh. Các thuốc chống vi ống, bao gồm các loại thuốc thường được sử dụng cho bệnh gút, và vincristine phá vỡ sự hình thành của tubulin thành các vi ống. Những loại thuốc này liên quan đến các bệnh lý thần kinh-cơ độc hại. Nồng độ CPK tăng nghiêm trọng trong bệnh lý cơ do colchicine.
Bệnh lý cơ do nhiễm trùng
Bệnh lý cơ do nhiễm trùng thường liên quan đến AIDS. Nó không đồng nhất và có thể dẫn đến bệnh lý cơ viêm, bệnh lý cơ ty thể, viêm vi mạch, bệnh lý cơ hoại tử, hoặc teo sợi cơ loại 2. Di chứng của nhiễm virus HIV ngoài tác dụng độc của AZT lên cơ có thể là một yếu tố góp phần phát triển bệnh lý cơ. CPK thường tăng, và sinh thiết cơ có thể trông giống như PM với viêm nội cơ hoặc IBM với các thể vùi.
Bệnh lý cơ do bệnh lý nặng
Bệnh lý cơ do bệnh lý nặng (CIM) được thấy ở những bệnh nhân nhập ICU với bệnh nặng và có thể có hoặc không có bệnh lý thần kinh. Các yếu tố nguy cơ bao gồm suy đa cơ quan, bao gồm suy thận, nhiễm trùng huyết và tiếp xúc với steroid. CIM biểu hiện là yếu liệt mềm lan tỏa với những khó khăn đáng kể trong việc cai máy thở thường kéo dài thời gian nằm ICU, làm tăng tỷ lệ bệnh tật và tử vong. Các ảnh hưởng lâu dài có thể kéo dài hàng tháng đến hàng năm, với giảm khả năng dung nạp gắng sức và giảm chất lượng cuộc sống.
Các tiêu chí chẩn đoán bao gồm một bệnh nhân bị bệnh nặng với yếu chi và khó cai máy thở và biên độ CMAP dưới 80% bình thường với các điện thế hoạt động thần kinh cảm giác bình thường. Điện cơ kim cho thấy các phát hiện bệnh lý cơ có hoặc không có sự hiện diện của các điện thế rung giật và sinh thiết cơ với các phát hiện bệnh lý cơ nguyên phát.
Quản lý là hỗ trợ và bao gồm điều trị tích cực tác nhân gây bệnh, bao gồm quản lý nhiễm trùng huyết, giảm steroid và loại bỏ các thuốc phong bế thần kinh-cơ. Phục hồi chức năng sớm, kích thích điện và huy động là rất quan trọng.
CÁC NGUYÊN TẮC PHỤC HỒI CHỨC NĂNG CHUNG TRONG CÁC RỐI LOẠN BỆNH LÝ CƠ (HỘP 42.17, BẢNG 42.18 VÀ HÌNH 42.19)
Tổng quan
Mục tiêu của quản lý phục hồi chức năng trong bệnh lý cơ và loạn dưỡng cơ là cung cấp chăm sóc hỗ trợ để cải thiện chất lượng cuộc sống và sự sống còn và giảm tỷ lệ bệnh tật và tác động của khuyết tật lên các chức năng hàng ngày. Các đội ngũ đa ngành bao gồm các bác sĩ cả về thần kinh và y học phục hồi, các nhà trị liệu (vật lý, hoạt động, ngôn ngữ và hô hấp), các nhà tâm lý học, các kỹ thuật viên chỉnh hình và nhân viên xã hội nên phối hợp các nỗ lực của họ để đạt được những mục tiêu đó. Các chuyên khoa y tế liên quan, bao gồm tim mạch, phổi, tiêu hóa, nội tiết, phẫu thuật chỉnh hình và phẫu thuật thần kinh, tham gia vào việc chăm sóc mỗi bệnh nhân và là một phần quan trọng trong chăm sóc đa ngành của mỗi bệnh nhân.
Chăm sóc răng miệng
Quản lý tiết dịch là quan trọng vì cả tăng tiết nước bọt và khô miệng đều có thể thấy. Tăng tiết nước bọt có thể được quản lý bằng cách sử dụng một thiết bị hút hoặc bằng các kỹ thuật hành vi, bao gồm sử dụng khăn tay và hiếm khi tiêm botulinum toxin. Chất bôi trơn miệng hoặc kẹo chua có thể được sử dụng cho khô miệng nhưng phải thận trọng ở những bệnh nhân bị khó nuốt.
Nuốt
Các rối loạn nuốt là phổ biến và có thể góp phần đáng kể vào tỷ lệ bệnh tật và tử vong, bao gồm viêm phổi hít, suy dinh dưỡng và chậm phát triển. Các chiến lược quản lý bao gồm theo dõi cân nặng thường xuyên và sàng lọc khó nuốt một cách đều đặn. Nên thực hiện chuyển đến đánh giá nuốt bởi một SLP. Các chiến lược hành vi bao gồm điều chỉnh độ đặc của thực phẩm, chẳng hạn như làm đặc chất lỏng, nghiền thuốc, xay nhuyễn thức ăn đặc và tránh thức ăn khô. Nếu chức năng tay bị suy giảm hoặc khả năng đưa thức ăn hoặc đồ uống lên miệng bị giảm, điều quan trọng là cung cấp các dụng cụ trợ giúp và điều chỉnh các dụng cụ ăn uống để cải thiện việc ăn uống. Người chăm sóc nên được dạy thủ thuật Heimlich trong trường hợp bị hít sặc. Nếu khó nuốt nghiêm trọng, nên xem xét bắt đầu cho ăn qua đường ruột bằng cách sử dụng ống thông dạ dày. Nếu xem xét cho ăn bằng ống thông dạ dày, thủ thuật nên được thực hiện sớm trong quá trình bệnh và trước khi mất FVC.
Dinh dưỡng
Đánh giá quản lý dinh dưỡng về cân nặng, chế độ ăn, hydrat hóa, sức khỏe răng miệng, rối loạn chức năng nuốt và chức năng chi để hỗ trợ ăn uống độc lập nên được thực hiện thường xuyên. Bổ sung calo protein dinh dưỡng y tế và/hoặc bổ sung thực phẩm có thể cần thiết để đáp ứng nhu cầu calo và protein hàng ngày trong một số trường hợp.
Theo dõi sức khỏe xương sớm là rất quan trọng để đánh giá tình trạng dễ gãy xương vì các cá nhân thường có thể tương đối không có triệu chứng. Gãy xương đốt sống và gãy xương dài thường xuyên xảy ra với việc sử dụng steroid. Điều trị bằng bisphosphonate được chỉ định trong các trường hợp gãy xương đốt sống hoặc gãy xương dài do chấn thương nhẹ. Điều trị bằng liệu pháp bisphosphonate đường tĩnh mạch đã được chứng minh là có tác dụng bảo vệ cột sống trong DMD và BMD.
Nhận thức
Suy giảm nhận thức và chậm phát triển có thể thấy trong một số loại bệnh lý cơ và nên được sàng lọc vì chúng có thể cản trở việc quản lý chăm sóc sức khỏe, bao gồm cả việc theo dõi chăm sóc, và có thể có ảnh hưởng đến tỷ lệ bệnh tật, tử vong và khả năng tuyển dụng.
Các tình trạng hành vi thần kinh hoặc tâm thần kinh xuất hiện trong các kiểu hình nhất định của DMD và DM1. Xét nghiệm tâm lý thần kinh có thể xác định điểm mạnh và điểm yếu và hỗ trợ lập kế hoạch học tập hoặc hướng nghiệp. Điều quan trọng là đánh giá tâm trạng và sự thích ứng với khuyết tật tại mỗi lần khám đa ngành. Dịch vụ công tác xã hội và tư vấn có thể cung cấp hỗ trợ tâm lý, ngoài hỗ trợ gia đình, xã hội và tôn giáo. Các loại thuốc như thuốc chống trầm cảm có thể có lợi. Cần thận trọng khi sử dụng benzodiazepine cho lo âu trong các rối loạn bệnh lý cơ có suy hô hấp vì điều này có thể làm giảm ổ hô hấp và dẫn đến suy hô hấp.
Mệt mỏi
Mệt mỏi và buồn ngủ ban ngày quá mức là những than phiền phổ biến liên quan đến teo cơ, các biến chứng hô hấp và các rối loạn giấc ngủ. Nên xem xét các chiến lược để cải thiện giấc ngủ và tâm trạng cũng như các kỹ thuật bảo tồn năng lượng. Thử dùng một loại thuốc kích thích thần kinh, chẳng hạn như modafinil, có thể cải thiện các triệu chứng mệt mỏi.
Đau
Đau là một than phiền phổ biến, đặc biệt là ở các giai đoạn cuối của bệnh. Cần đặc biệt cẩn thận để tránh sử dụng thuốc giãn cơ và ma túy vì điều này có thể làm tăng yếu cơ trong bệnh lý cơ. Có thể xem xét mexiletine liều thấp cho chứng trương lực cơ khó chịu; tuy nhiên, nên thực hiện điện tâm đồ khi bắt đầu điều trị, vì đã có một số trường hợp báo cáo về kéo dài QT. Các phương pháp điều trị khác đã được thử là magiê, axit axetic và nước tonic (chứa quinine). Có thể thử vật lý trị liệu, tắm nước ấm hoặc đệm sưởi ấm theo sau là kéo giãn nhẹ nhàng, các kỹ thuật bảo tồn năng lượng và đánh giá thiết bị để đảm bảo an toàn.
Co rút
Đánh giá thường xuyên tầm vận động khớp để theo dõi sự phát triển của co rút là rất quan trọng. Với động tác gập mu thụ động dưới 10 độ, chỉ định sử dụng nẹp ban đêm được đúc tùy chỉnh. Chuyển đến phẫu thuật chỉnh hình cho co rút gân Achilles có thể kéo dài thời gian đi lại. Trong giai đoạn sớm không đi lại được, các bài tập khung đứng rất quan trọng để quản lý co rút. Phẫu thuật bàn chân có thể được xem xét trong các giai đoạn sau để cải thiện vị trí bàn chân trên xe lăn và tạo thuận lợi cho việc mang giày.
Chăm sóc cột sống
Vẹo cột sống nghiêm trọng thường phát triển sau khi mất khả năng đi lại. Chụp X-quang vẹo cột sống thường quy được chỉ định ít nhất hàng năm một khi được phát hiện trên lâm sàng, với việc xem xét sàng lọc thường xuyên hơn sau khi mất khả năng đi lại. Mặc dù có thể thử nẹp, các biện pháp tích cực hơn thường được yêu cầu. Nên xem xét chuyển đến phẫu thuật hợp nhất và cố định cột sống một khi đường cong cột sống đạt 20 đến 30 độ và trước khi FVC suy giảm xuống dưới 30% đến 40%. Yếu cột sống, yếu gập và duỗi cổ, và gãy lún đốt sống ngực-thắt lưng có thể là một nguồn đau lưng đáng kể và có thể cản trở việc ăn uống, giao tiếp và tư thế. Nhiều loại nẹp hỗ trợ, bao gồm nẹp cổ mềm, nẹp cổ Philadelphia, và áo nịt ngực-thắt lưng, và đai, đã được sử dụng.
Các can thiệp
Vật lý trị liệu rất quan trọng và cần thiết cho các vấn đề liên quan đến yếu cơ, di chuyển, co rút và đau. Hoạt động trị liệu có thể hữu ích để duy trì và tối đa hóa khả năng tự chăm sóc. Các bài tập aerobic và kháng trở nhẹ đến vừa phải là an toàn trong hầu hết các trường hợp và có thể cải thiện sức khỏe tim mạch. Bệnh nhân nên được cảnh báo không tập thể dục với cường độ quá mức. Các bài tập nên có tác động thấp, chẳng hạn như thủy trị liệu, đạp xe trong nhà với kháng trở thấp hoặc không có, hoặc bài tập trên ghế. Tập thể dục lệch tâm có thể dẫn đến phá vỡ cơ và nên tránh. Một khung đứng có thể được sử dụng ở những bệnh nhân không đi lại được để phòng ngừa co rút.
Nẹp cổ-bàn chân bằng sợi carbon nhẹ với hỗ trợ gập mu được bắt đầu sớm trong quá trình bệnh có thể kéo dài thời gian đi lại và bảo tồn năng lượng, đặc biệt là ở những người bị yếu động tác gập mu cổ chân. Nẹp PHAT thường được sử dụng để cung cấp sự ổn định cho gối và một số hỗ trợ động. Nẹp gối-cổ-bàn chân có thể được sử dụng trong một số trường hợp nhất định với các chương trình kéo giãn tại nhà và/hoặc sau phẫu thuật cắt gân. Phẫu thuật cắt gân để kéo dài gân gót và/hoặc gân kheo có thể cần thiết để tối ưu hóa sự vừa vặn của nẹp.
Các dụng cụ trợ giúp di chuyển rất quan trọng để phòng ngừa té ngã và bảo tồn năng lượng. Bệnh nhân có thể tiến từ dụng cụ hỗ trợ ít nhất, gậy một điểm, đến khung tập đi và cuối cùng là xe lăn. Một chiếc xe lăn tay có thể đủ; tuy nhiên, nếu có liên quan đến chi trên đáng kể, việc đẩy xe lăn tay có thể không thực tế, và do đó xe lăn điện có thể phù hợp hơn. Trẻ em thường có thể được dạy vận hành xe lăn điện một cách an toàn trước 2 tuổi, tùy thuộc vào các bệnh lý đi kèm liên quan đến nhận thức và/hoặc hành vi.
Yếu cơ nội tại bàn tay, cẳng tay và cổ tay có thể ảnh hưởng đến cả kỹ năng vận động tinh và thô của bàn tay. Nẹp, bao gồm vòng bít đa năng và nẹp tay, có thể thúc đẩy sự độc lập với các hoạt động sinh hoạt hàng ngày và hoạt động như một kỹ thuật bảo tồn năng lượng để bảo tồn chức năng tay và ngăn ngừa chấn thương trong các bệnh lý cơ ảnh hưởng đến các cơ nội tại bàn tay và cơ cẳng tay. Trong các bệnh lý cơ chủ yếu ảnh hưởng đến gốc chi trên, ảnh hưởng gián tiếp đến chức năng tay, một thiết bị dụng cụ chỉnh hình cẳng tay cân bằng có thể thúc đẩy sự độc lập, cho phép chức năng chi trên bao gồm chải chuốt và ăn uống.
Bệnh nhân mắc bệnh phổi hạn chế thần kinh-cơ cần theo dõi phổi thường xuyên. Các chiến lược làm sạch đường thở cơ học như thiết bị hỗ trợ ho hoặc hệ thống làm sạch đường thở bằng áo rung có thể cần thiết. Nên xem xét thông khí hai mức không xâm lấn về đêm khi FVC đạt 50%. Thông khí qua ống ngậm hoặc thông khí hai mức ban ngày và ban đêm thường cần thiết khi FVC đạt 30%. Đôi khi thông khí xâm lấn bằng mở khí quản được xem xét nếu thông khí hai mức liên tục 24 giờ cản trở giao tiếp hoặc không đủ để đáp ứng nhu cầu thông khí.
KẾT LUẬN VÀ CÁC ĐỊNH HƯỚNG TƯƠNG LAI
Những tiến bộ lớn trong sự hiểu biết về cơ sở phân tử và di truyền của nhiều bệnh lý cơ và bệnh sinh của chúng đã tăng cường đáng kể độ chính xác chẩn đoán và cung cấp cơ sở cho sự phát triển của các can thiệp điều trị mới cho những rối loạn này. Các phương pháp phục hồi chức năng truyền thống sẽ cần được tích hợp với các can thiệp dược lý mới hơn, các liệu pháp dựa trên di truyền phân tử, các liệu pháp tế bào gốc và liệu pháp gen, đang ngày càng trở thành hiện thực trong việc quản lý những tình trạng này. Với quản lý đa ngành được cải thiện và áp dụng các tiêu chuẩn chăm sóc và phục hồi chức năng được cải thiện, những bệnh nhân mắc bệnh lý cơ mà trước đây được coi là bệnh của trẻ em hiện đang sống tốt đến tuổi trưởng thành với sự sống còn được cải thiện và chất lượng cuộc sống tốt hơn.
| Kinh nghiệm lâm sàng
Phục hồi chức năng các rối loạn bệnh lý cơ nên bao gồm các bài tập linh hoạt, kéo giãn và kháng trở cường độ nhẹ đến vừa phải, tránh các bài tập lệch tâm. Nên tránh mệt mỏi. Nẹp có thể cần thiết để kéo dài thời gian đi lại, điều chỉnh các biến dạng và ngăn ngừa co rút. Các dụng cụ trợ giúp di chuyển có thể cần thiết. Đánh giá tim-phổi và chẩn đoán và quản lý sớm các biến chứng liên quan là bắt buộc. Quản lý khó nuốt, hỗ trợ dinh dưỡng và hỗ trợ tâm lý xã hội là vô cùng quan trọng. |
Hộp 42.1 Các rối loạn bệnh lý cơ
|
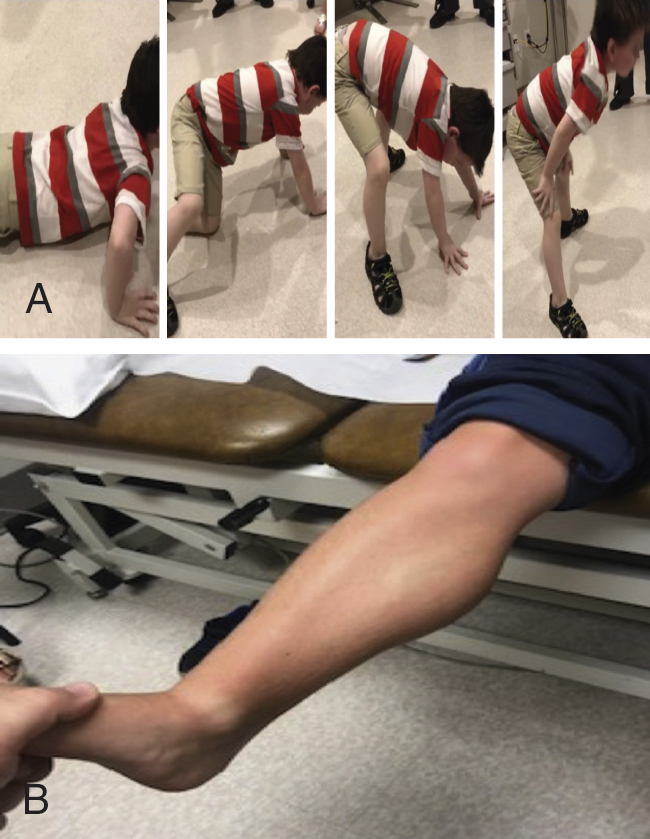
Hộp 42.2 Các bệnh lý Dystrophin
(a) Dấu hiệu Gower (b) Giả phì đại bắp chân |
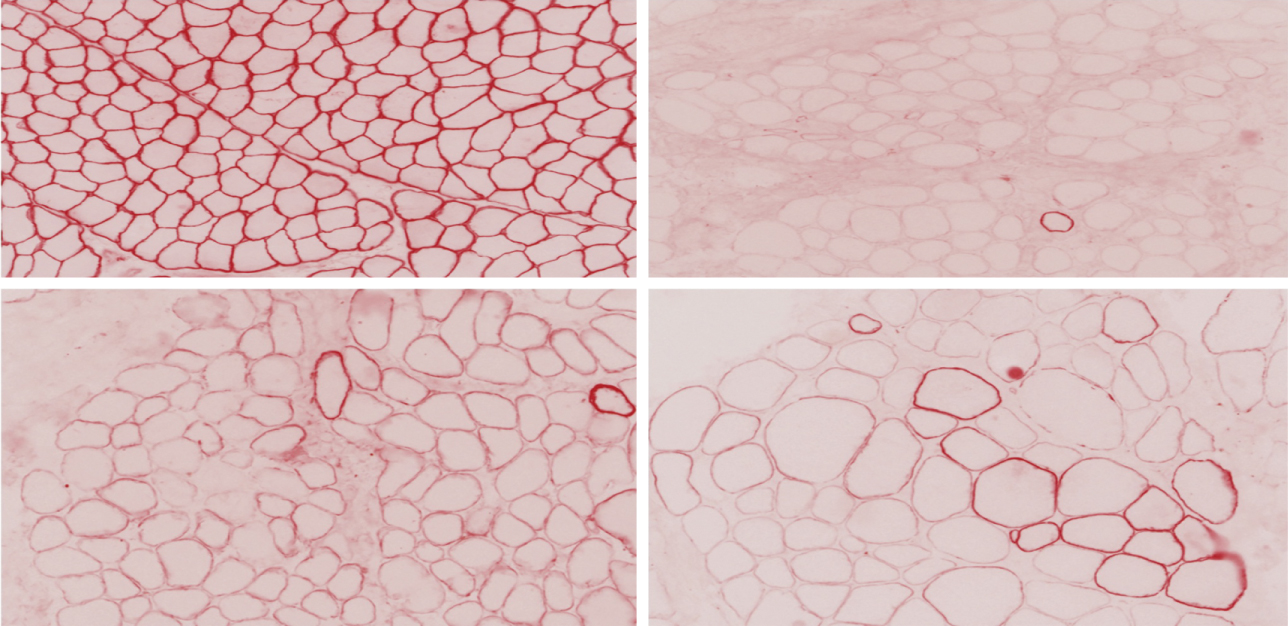
Hình 42.3 Sinh thiết cơ trong bệnh lý Dystrophin
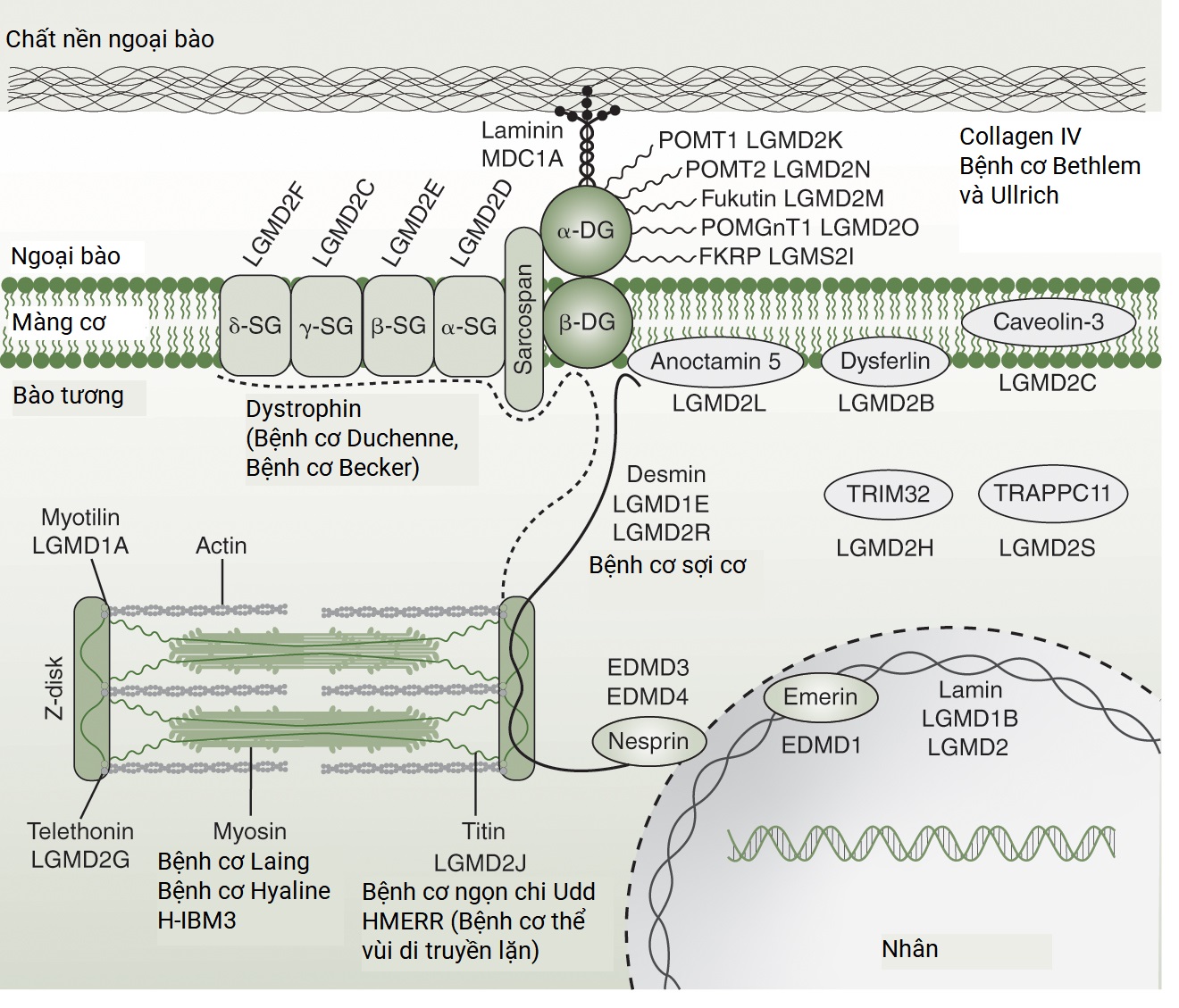
Hình 42.4 Các protein và gen của tế bào cơ liên quan đến các rối loạn bệnh lý cơ chọn lọc. Sơ đồ này minh họa các protein cấu trúc khác nhau trong tế bào cơ (màng sarcolemma, tế bào chất, đĩa Z, nhân) và các gen tương ứng liên quan đến các loại loạn dưỡng cơ khác nhau (DMD, BMD, LGMD, EDMD, v.v.).
Hộp 42.5 Loạn dưỡng cơ Emery-Dreifuss
|
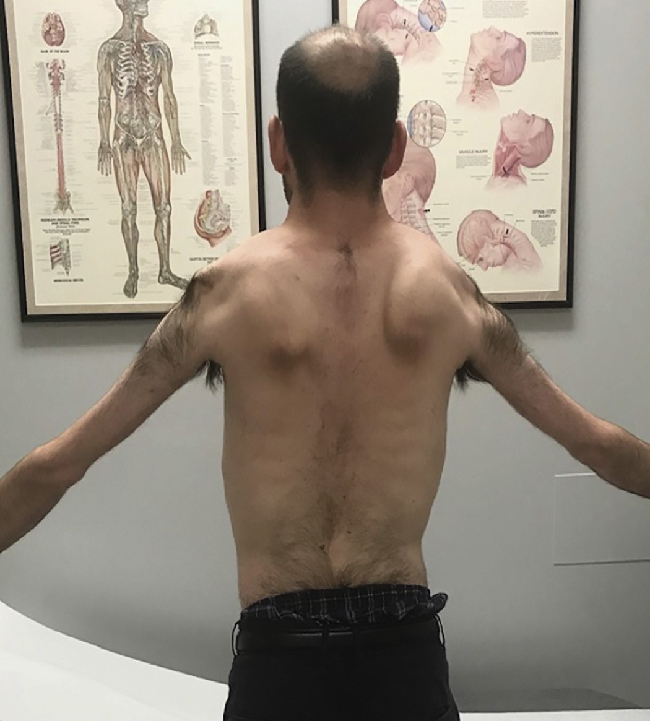
Hộp 42.6 Loạn dưỡng cơ mặt-vai-cánh tay
Xương bả vai nhô ở bệnh nhân loạn dưỡng cơ mặt-vai-cánh tay |
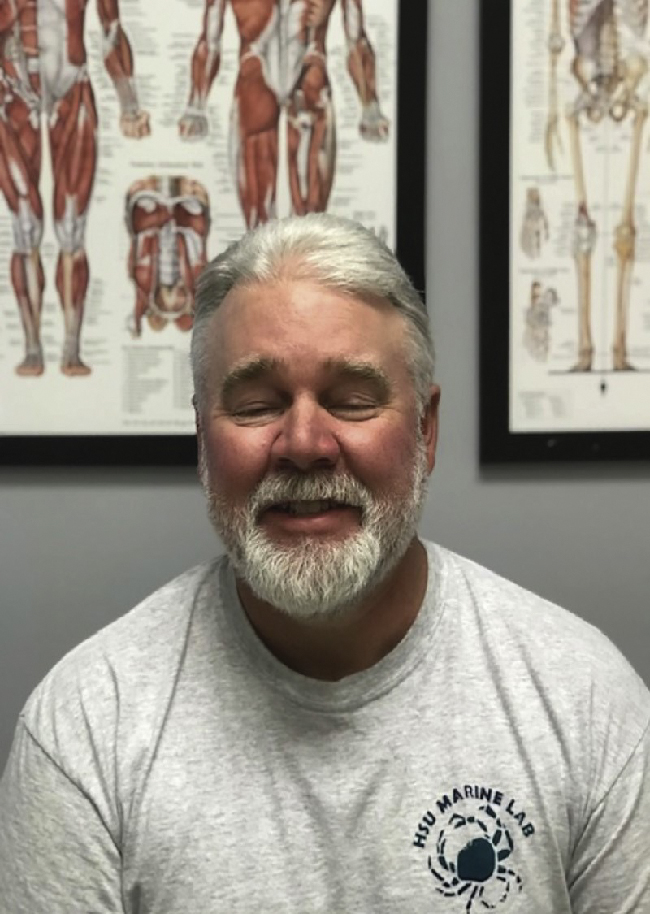
Hộp 42.7 Loạn dưỡng cơ mắt-hầu
Sụp mi ở bệnh nhân loạn dưỡng cơ mắt-hầu |
Hộp 42.8 Loạn dưỡng cơ gốc chi
|
Hộp 42.9 Loạn dưỡng trương lực cơ
Hiện tượng trội hơn ở mẹ và con gái bị loạn dưỡng cơ trương lực cơ |
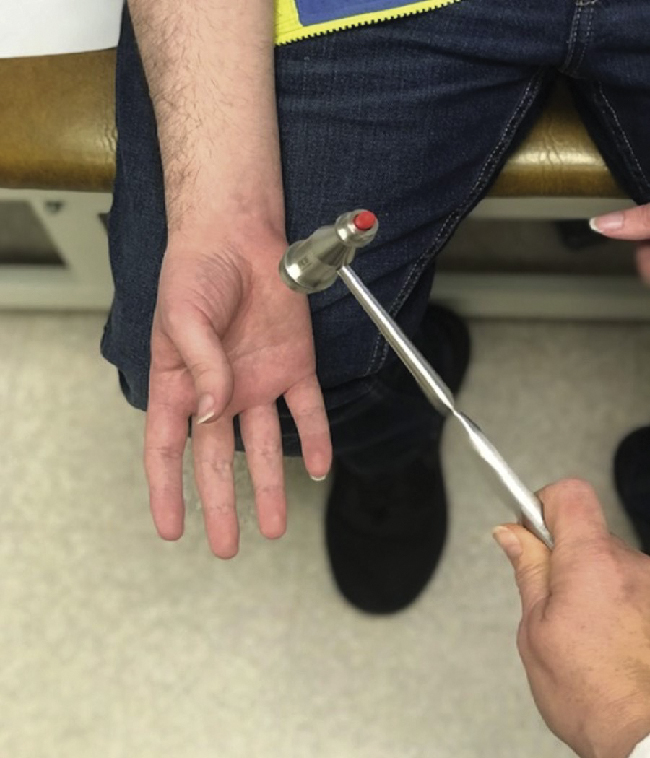
Hộp 42.10 Trương lực cơ (Trương lực cơ khi gõ)
|
Hộp 42.11 Các bệnh lý cơ bẩm sinh
|
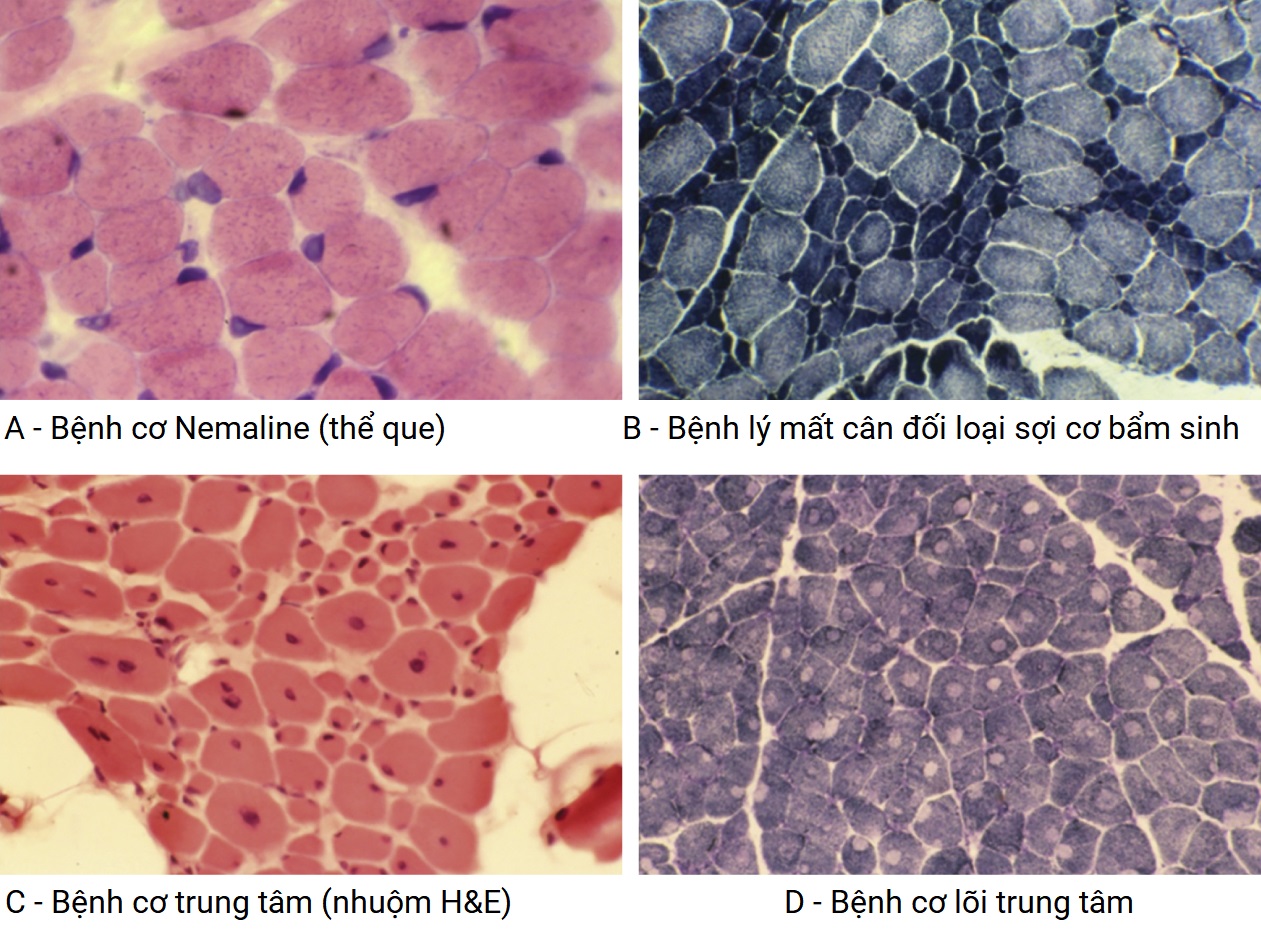
Hình 42.12 Mô học của các bệnh lý cơ bẩm sinh. (a) Bệnh lý cơ Nemaline (que) (b) Bệnh lý cơ bẩm sinh mất cân đối loại sợi (c) Bệnh lý cơ trung tâm nhân (d) Bệnh lý cơ lõi trung tâm
Hộp 42.13 Các bệnh lý trương lực cơ không loạn dưỡng
|
Hộp 42.14 Các bệnh lý cơ chuyển hóa
|
Hộp 42.15 Các bệnh lý cơ ty thể
|
Hộp 42.16 Các bệnh lý cơ viêm tự phát
|
Hộp 42.17 Phục hồi chức năng các bệnh lý cơ
|
Bảng 42.18 Các xem xét về tim và phổi
| Phục hồi chức năng phổi | Phục hồi chức năng tim |
|---|---|
| Theo dõi phổi thường xuyên là cần thiết ở bệnh nhân mắc bệnh phổi hạn chế. | Theo dõi thường xuyên cơ tim |
| Các chiến lược làm sạch đường thở cơ học có thể cần thiết. | Quản lý các bất thường dẫn truyền tim |
| Nên xem xét thông khí hai mức không xâm lấn về đêm khi dung tích sống gắng sức (FVC)%p dự đoán đạt 50%. | Quản lý suy tim |
| Thông khí qua ống ngậm hoặc thông khí hai mức ban ngày và ban đêm thường cần thiết khi FVC%p đạt 30%. | Có thể ghép tim cho bệnh nhân suy tim giai đoạn cuối |
| Thông khí xâm lấn bằng mở khí quản được xem xét nếu thông khí hai mức liên tục 24 giờ không hiệu quả. |
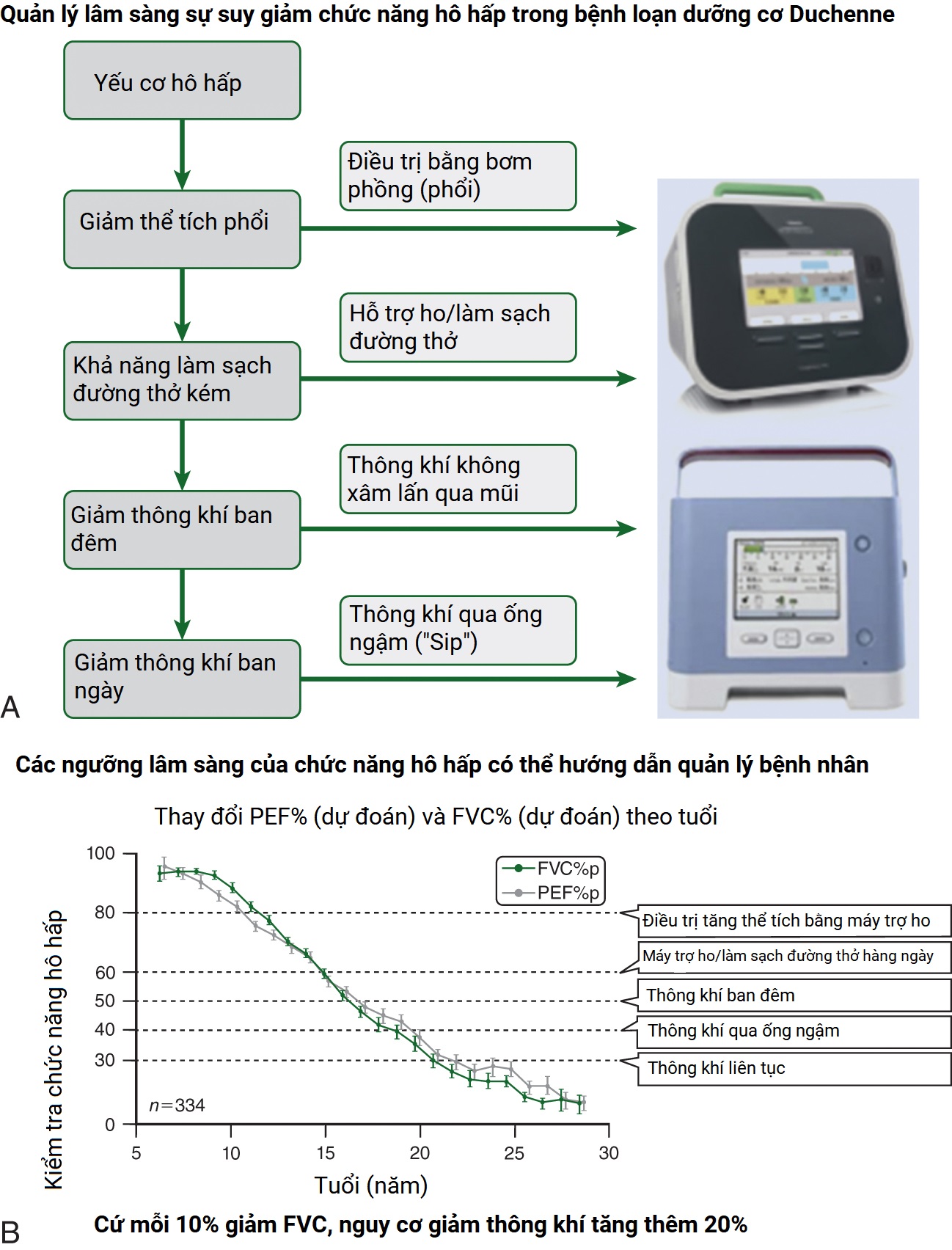
Hình 42.19 Chức năng hô hấp trong các rối loạn bệnh lý cơ
(A) Quản lý lâm sàng sự suy giảm chức năng hô hấp trong các bệnh lý cơ. (B) Các ngưỡng lâm sàng của chức năng hô hấp có thể hướng dẫn quản lý bệnh nhân.
(A) Quản lý lâm sàng sự suy giảm chức năng hô hấp trong loạn dưỡng cơ Duchenne (Biểu đồ cho thấy: Yếu cơ hô hấp -> Thể tích phổi thấp -> Điều trị tăng phồng phổi; Thể tích phổi thấp -> Làm sạch đường thở kém -> Hỗ trợ ho/làm sạch đường thở; Làm sạch đường thở kém -> Giảm thông khí về đêm -> Thông khí không xâm lấn qua mũi; Giảm thông khí về đêm -> Giảm thông khí ban ngày -> Thông khí qua ống ngậm “Hít”)
(B) Các ngưỡng lâm sàng của chức năng hô hấp có thể hướng dẫn quản lý bệnh nhân (Biểu đồ cho thấy sự thay đổi của PEF%p và FVC%p theo tuổi, với các ngưỡng can thiệp như: Điều trị tăng phồng phổi bằng máy thổi vào-thở ra, Hỗ trợ ho/làm sạch đường thở hàng ngày, Thông khí ban đêm, Thông khí qua ống ngậm, Thông khí liên tục) Cứ mỗi 10% giảm FVC, tỷ lệ giảm thông khí tăng 20%
Bảng chú giải thuật ngữ Y học Anh – Việt (Chương 42)
| STT | Thuật ngữ tiếng Anh | Phiên âm IPA | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Myopathic disorders | /ˌmaɪoʊˈpæθɪk dɪsˈɔːrdərz/ | Các rối loạn bệnh lý cơ |
| 2 | Duchenne (DMD) | /duːˈʃɛn/ | Bệnh Duchenne |
| 3 | Becker (BMD) | /ˈbɛkər/ | Bệnh Becker |
| 4 | Dystrophinopathies | /ˌdɪstrəfɪˈnɒpəθiz/ | Các bệnh lý Dystrophin |
| 5 | X-linked recessive | /ˌɛksˌlɪŋkt rɪˈsɛsɪv/ | Lặn liên kết nhiễm sắc thể X |
| 6 | Dystrophin gene | /ˈdɪstrəfɪn dʒiːn/ | Gen Dystrophin |
| 7 | Respiratory failure | /ˈrɛspərətɔːri ˈfeɪljər/ | Suy hô hấp |
| 8 | Cardiac failure | /ˈkɑːrdiæk ˈfeɪljər/ | Suy tim |
| 9 | Loss of ambulation | /lɒs əv ˌæmbjʊˈleɪʃən/ | Mất khả năng đi lại |
| 10 | Emery-Dreifuss muscular dystrophy (EDMD) | /ˈɛməri ˈdraɪfəs ˈmʌskjələr ˈdɪstrəfi/ | Loạn dưỡng cơ Emery-Dreifuss |
| 11 | Nuclear envelope proteins | /ˈnjuːkliər ˈɛnvəloʊp ˈproʊtiːnz/ | Protein màng nhân |
| 12 | Contractures | /kənˈtrækʃərz/ | Co rút |
| 13 | Cardiomyopathy | /ˌkɑːrdioʊmaɪˈɒpəθi/ | Bệnh lý cơ tim |
| 14 | Pseudohypertrophy | /ˌsuːdoʊhaɪˈpɜːrtrəfi/ | Giả phì đại |
| 15 | Facioscapulohumeral muscular dystrophy (FSH) | /ˌfeɪʃioʊˌskæpjəloʊˈhjuːmərəl ˈmʌskjələr ˈdɪstrəfi/ | Loạn dưỡng cơ mặt-vai-cánh tay |
| 16 | Oculopharyngeal muscular dystrophy (OPMD) | /ˌɒkjəloʊfəˈrɪndʒiəl ˈmʌskjələr ˈdɪstrəfi/ | Loạn dưỡng cơ mắt-hầu |
| 17 | Autosomal dominant (AD) | /ˌɔːtəˈsoʊməl ˈdɒmɪnənt/ | Di truyền trội trên nhiễm sắc thể thường |
| 18 | Ptosis | /ˈtoʊsɪs/ | Sụp mi |
| 19 | Dysphagia | /dɪsˈfeɪdʒiə/ | Khó nuốt |
| 20 | Limb girdle muscular dystrophy (LGMD) | /lɪm ˈɡɜːrdl ˈmʌskjələr ˈdɪstrəfi/ | Loạn dưỡng cơ gốc chi |
| 21 | Autosomal recessive | /ˌɔːtəˈsoʊməl rɪˈsɛsɪv/ | Di truyền lặn trên nhiễm sắc thể thường |
| 22 | Pelvic girdle | /ˈpɛlvɪk ˈɡɜːrdl/ | Đai chậu |
| 23 | Shoulder girdle | /ˈʃoʊldər ˈɡɜːrdl/ | Đai vai |
| 24 | Cognitive involvement | /ˈkɒɡnɪtɪv ɪnˈvɒlvmənt/ | Liên quan đến nhận thức |
| 25 | Dystrophic myotonia (DM) | /dɪsˈtroʊfɪk ˌmaɪəˈtoʊniə/ | Loạn dưỡng trương lực cơ |
| 26 | Congenital myopathies | /kənˈdʒɛnɪtl maɪˈɒpəθiz/ | Các bệnh lý cơ bẩm sinh |
| 27 | Hypotonia | /ˌhaɪpoʊˈtoʊniə/ | Trương lực cơ giảm |
| 28 | Creatine phosphokinase (CPK) | /ˈkriːətiːn ˌfɒsfoʊˈkaɪneɪs/ | Creatine phosphokinase |
| 29 | Congenital muscular dystrophy (CMD) | /kənˈdʒɛnɪtl ˈmʌskjələr ˈdɪstrəfi/ | Loạn dưỡng cơ bẩm sinh |
| 30 | Metabolic myopathies | /ˌmɛtəˈbɒlɪk maɪˈɒpəθiz/ | Các bệnh lý cơ chuyển hóa |
| 31 | Carbohydrate metabolism | /ˌkɑːrboʊˈhaɪdreɪt məˈtæbəlɪzəm/ | Chuyển hóa carbohydrate |
| 32 | Lipid metabolism | /ˈlɪpɪd məˈtæbəlɪzəm/ | Chuyển hóa lipid |
| 33 | Exercise intolerance | /ˈɛksərsaɪz ɪnˈtɒlərəns/ | Không dung nạp gắng sức |
| 34 | Mitochondrial myopathies | /ˌmaɪtəˈkɒndriəl maɪˈɒpəθiz/ | Các bệnh lý cơ ty thể |
| 35 | Maternally inherited | /məˈtɜːrnəli ɪnˈhɛrɪtɪd/ | Di truyền từ mẹ |
| 36 | Oxidative phosphorylation | /ˈɒksɪdeɪtɪv ˌfɒsfɔːrɪˈleɪʃən/ | Quá trình phosphoryl hóa oxy hóa |
| 37 | Idiopathic inflammatory myopathies (IIMs) | /ˌɪdioʊˈpæθɪk ɪnˈflæmətɔːri maɪˈɒpəθiz/ | Các bệnh lý cơ viêm tự phát |
| 38 | Acquired diseases | /əˈkwaɪərd dɪˈziːzɪz/ | Các bệnh lý mắc phải |
| 39 | Skeletal muscle | /ˈskɛlɪtl ˈmʌsəl/ | Cơ xương |
| 40 | Inclusion body myositis (IBM) | /ɪnˈkluːʒən ˈbɒdi ˌmaɪəˈsaɪtɪs/ | Viêm cơ thể vùi |
| 41 | Asymmetric pattern | /ˌeɪsɪˈmɛtrɪk ˈpætərn/ | Kiểu hình không đối xứng |
| 42 | Autoimmune pathogenesis | /ˌɔːtoʊɪˈmjuːn ˌpæθəˈdʒɛnəsɪs/ | Bệnh sinh tự miễn |
| 43 | Neuromuscular diseases | /ˌnjʊəroʊˈmʌskjələr dɪˈziːzɪz/ | Bệnh lý thần kinh-cơ |
| 44 | Muscle cramps | /ˈmʌsəl kræmps/ | Chuột rút (vọp bẻ) |
| 45 | Muscle spasms | /ˈmʌsəl ˈspæzəmz/ | Co thắt cơ |
| 46 | Muscle stiffness | /ˈmʌsəl ˈstɪfnəs/ | Cứng cơ |
| 47 | HyperCKemia | /ˌhaɪpərˌsiːkeɪˈiːmiə/ | Tăng CK máu |
| 48 | Dystrophic myopathies | /dɪsˈtroʊfɪk maɪˈɒpəθiz/ | Các bệnh lý cơ loạn dưỡng |
| 49 | Myocardial fibers | /ˌmaɪəˈkɑːrdiəl ˈfaɪbərz/ | Sợi cơ tim |
| 50 | Respiratory insufficiency | /ˈrɛspərətɔːri ˌɪnsəˈfɪʃənsi/ | Suy hô hấp |
| 51 | Oropharyngeal muscles | /ˌɔːroʊfəˈrɪndʒiəl ˈmʌsəlz/ | Các cơ miệng-hầu |
| 52 | Sialorrhea | /ˌsaɪəloʊˈriə/ | Tăng tiết nước bọt |
| 53 | Dysarthria | /dɪsˈɑːrθriə/ | Khó nói |
| 54 | Scoliosis | /ˌskoʊliˈoʊsɪs/ | Vẹo cột sống |
| 55 | Neuromuscular disease | /ˌnjʊəroʊˈmʌskjələr dɪˈziːz/ | Bệnh thần kinh-cơ |
| 56 | Proximal weakness | /ˈprɒksɪməl ˈwiːknəs/ | Yếu gốc chi |
| 57 | Distal symmetric weakness | /ˈdɪstl sɪˈmɛtrɪk ˈwiːknəs/ | Yếu đối xứng ngọn chi |
| 58 | Myotonic dystrophy (DM1) | /ˌmaɪəˈtɒnɪk ˈdɪstrəfi/ | Loạn dưỡng trương lực cơ (loại 1) |
| 59 | Scapuloperoneal weakness | /ˌskæpjəloʊˌpɛrəˈniːəl ˈwiːknəs/ | Yếu cơ vai-mác |
| 60 | Distal asymmetric weakness | /ˈdɪstl ˌeɪsɪˈmɛtrɪk ˈwiːknəs/ | Yếu không đối xứng ngọn chi |
| 61 | Dysferlinopathies | /ˌdɪsfɜːrlɪˈnɒpəθiz/ | Các bệnh lý Dysferlin |
| 62 | Extraocular muscle | /ˌɛkstrəˈɒkjələr ˈmʌsəl/ | Cơ ngoài mắt |
| 63 | Fetal movements | /ˈfiːtl ˈmuːvmənts/ | Cử động thai |
| 64 | Myalgias | /maɪˈældʒiəz/ | Đau cơ |
| 65 | Dark-colored urine | /dɑːrk ˈkʌlərd ˈjʊərɪn/ | Nước tiểu sẫm màu |
| 66 | Glycogen storage diseases | /ˈɡlaɪkədʒən ˈstɔːrɪdʒ dɪˈziːzɪz/ | Các bệnh dự trữ glycogen |
| 67 | McArdle disease | /məkˈɑːrdl dɪˈziːz/ | Bệnh McArdle |
| 68 | Second-wind phenomenon | /ˈsɛkənd wɪnd fəˈnɒmɪnɒn/ | Hiện tượng “lấy lại sức” |
| 69 | Channelopathies | /ˌtʃænlˈɒpəθiz/ | Các bệnh lý kênh ion |
| 70 | Congenital hip dysplasia | /kənˈdʒɛnɪtl hɪp dɪsˈpleɪziə/ | Loạn sản khớp háng bẩm sinh |
| 71 | Malignant hyperthermia (MH) | /məˈlɪɡnənt ˌhaɪpərˈθɜːrmiə/ | Tăng thân nhiệt ác tính |
| 72 | Neurologic examination | /ˌnjʊərəˈlɒdʒɪk ɪɡˌzæmɪˈneɪʃən/ | Thăm khám thần kinh |
| 73 | Musculoskeletal examination | /ˌmʌskjəloʊˈskɛlɪtl ɪɡˌzæmɪˈneɪʃən/ | Thăm khám cơ xương khớp |
| 74 | Lordosis | /lɔːrˈdoʊsɪs/ | Chứng ưỡn lưng |
| 75 | Waddling gait | /ˈwɒdlɪŋ ɡeɪt/ | Dáng đi lạch bạch |
| 76 | Toe walking | /toʊ ˈwɔːkɪŋ/ | Đi nhón gót |
| 77 | Winging of the scapulae | /ˈwɪŋɪŋ əv ðə ˈskæpjəliː/ | Xương bả vai nhô (cánh chim) |
| 78 | Pompe disease | /ˈpɒmpeɪ dɪˈziːz/ | Bệnh Pompe |
| 79 | Sarcoglycanopathies | /ˌsɑːrkoʊɡlaɪkəˈnɒpəθiz/ | Các bệnh lý Sarcoglycan |
| 80 | Gower sign | /ˈɡaʊər saɪn/ | Dấu hiệu Gower |
| 81 | Neck flexion weakness | /nɛk ˈflɛkʃən ˈwiːknəs/ | Yếu động tác gập cổ |
| 82 | Hypertrophy | /haɪˈpɜːrtrəfi/ | Phì đại |
| 83 | Macroglossia | /ˌmækroʊˈɡlɒsiə/ | Lưỡi to (chứng lưỡi to) |
| 84 | Hypothyroid myopathy | /ˌhaɪpoʊˈθaɪrɔɪd maɪˈɒpəθi/ | Bệnh lý cơ do suy giáp |
| 85 | Amyloid myopathy | /ˈæməlɔɪd maɪˈɒpəθi/ | Bệnh lý cơ do amyloid |
| 86 | Myotonia | /ˌmaɪəˈtoʊniə/ | Trương lực cơ |
| 87 | Actin-myosin coupling | /ˈæktɪn ˈmaɪəsɪn ˈkʌplɪŋ/ | Khớp nối Actin-myosin |
| 88 | Heliotropic rash | /ˌhiːliəˈtroʊpɪk ræʃ/ | Ban đỏ hình cánh bướm |
| 89 | Dermatomyositis (DM) | /ˌdɜːrmətoʊˌmaɪəˈsaɪtɪs/ | Viêm da cơ |
| 90 | Hyperkeratosis pilaris | /ˌhaɪpərˌkɛrəˈtoʊsɪs paɪˈlɛərɪs/ | Dày sừng nang lông |
| 91 | Transaminases | /trænsˈæmɪneɪsɪz/ | Các men Transaminase (men gan) |
| 92 | Aldolase | /ˈældəleɪs/ | Men Aldolase |
| 93 | Alanine transaminase (ALT) | /ˈæləniːn trænsˈæmɪneɪs/ | Alanine transaminase (ALT) |
| 94 | Aspartate transaminase (AST) | /əˈspɑːrteɪt trænsˈæmɪneɪs/ | Aspartate transaminase (AST) |
| 95 | Gamma glutamyl transpeptidase | /ˈɡæmə ˈɡluːtəmɪl trænsˈpɛptɪdeɪs/ | Gamma glutamyl transpeptidase (GGT) |
| 96 | Autoantibodies | /ˌɔːtoʊˈæntibɒdiz/ | Tự kháng thể |
| 97 | NT5C1A antibody | /ɛn tiː faɪv siː wʌn eɪ ˈæntibɒdi/ | Kháng thể NT5C1A |
| 98 | Myositis-specific autoantibody | /ˌmaɪəˈsaɪtɪs spəˈsɪfɪk ˌɔːtoʊˈæntibɒdi/ | Tự kháng thể đặc hiệu cho viêm cơ |
| 99 | Anti-Jo antibodies | /ˌæntiˈdʒoʊ ˈæntibɒdiz/ | Kháng thể kháng Jo |
| 100 | Interstitial lung disease | /ˌɪntərˈstɪʃəl lʌŋ dɪˈziːz/ | Bệnh phổi kẽ |
| 101 | Immunofixation electrophoresis | /ˌɪmjənoʊfɪkˈseɪʃən ɪˌlɛktroʊfəˈriːsɪs/ | Điện di miễn dịch cố định |
| 102 | Nerve conduction studies (NCS) | /nɜːrv kənˈdʌkʃən ˈstʌdiz/ | Các nghiên cứu dẫn truyền thần kinh |
| 103 | Compound muscle action potential (CMAP) | /ˈkɒmpaʊnd ˈmʌsəl ˈækʃən pəˈtɛnʃəl/ | Điện thế hoạt động cơ phức hợp |
| 104 | Electromyography (EMG) | /ɪˌlɛktroʊmaɪˈɒɡrəfi/ | Điện cơ đồ |
| 105 | Volitional motor unit action potentials (MUAPs) | /voʊˈlɪʃənl ˈmoʊtər ˈjuːnɪt ˈækʃən pəˈtɛnʃəlz/ | Điện thế hoạt động của đơn vị vận động hữu ý |
| 106 | Early recruitment | /ˈɜːrli rɪˈkruːtmənt/ | Kết tập sớm |
| 107 | Polyphasicity | /ˌpɒliˈfeɪzɪsɪti/ | Tính đa pha |
| 108 | Neurogenic changes | /ˌnjʊəroʊˈdʒɛnɪk ˈtʃeɪndʒɪz/ | Các thay đổi do thần kinh |
| 109 | Muscle necrosis | /ˈmʌsəl nəˈkroʊsɪs/ | Hoại tử cơ |
| 110 | Denervation | /ˌdiːnɜːrˈveɪʃən/ | Mất phân bố thần kinh |
| 111 | Neuromuscular junction | /ˌnjʊəroʊˈmʌskjələr ˈdʒʌŋkʃən/ | Khớp thần kinh-cơ |
| 112 | Centronuclear myopathy (CNM) | /ˌsɛntroʊˈnjuːkliər maɪˈɒpəθi/ | Bệnh lý cơ trung tâm nhân |
| 113 | Acetylcholine receptor | /əˌsiːtlˈkoʊliːn rɪˈsɛptər/ | Thụ thể Acetylcholine |
| 114 | Muscle biopsy | /ˈmʌsəl ˈbaɪɒpsi/ | Sinh thiết cơ |
| 115 | Medical Research Council (MRC) grade | /ˈmɛdɪkl rɪˈsɜːrtʃ ˈkaʊnsəl ɡreɪd/ | Bậc cơ (theo thang điểm MRC) |
| 116 | Tibialis anterior | /ˌtɪbiˈeɪlɪs ænˈtɪəriər/ | Cơ chày trước |
| 117 | Muscular dystrophies | /ˈmʌskjələr ˈdɪstrəfiz/ | Các bệnh lý loạn dưỡng cơ |
| 118 | Sarcolemma | /ˌsɑːrkoʊˈlɛmə/ | Màng cơ (Sarcolemma) |
| 119 | Extracellular matrix | /ˌɛkstrəˈsɛljələr ˈmeɪtrɪks/ | Chất nền ngoại bào |
| 120 | Echocardiography | /ˌɛkoʊˌkɑːrdioʊˈɡræfi/ | Siêu âm tim |
| 121 | Cardiac magnetic resonance imaging | /ˈkɑːrdiæk mæɡˈnɛtɪk ˈrɛzənəns ˈɪmɪdʒɪŋ/ | Chụp cộng hưởng từ tim |
| 122 | Cardiac fibrosis | /ˈkɑːrdiæk faɪˈbroʊsɪs/ | Xơ hóa tim |
| 123 | Systolic dysfunction | /sɪsˈtɒlɪk dɪsˈfʌŋkʃən/ | Rối loạn chức năng tâm thu |
| 124 | Afterload reducing agents | /ˈɑːftərloʊd rɪˈdjuːsɪŋ ˈeɪdʒənts/ | Các thuốc giảm hậu gánh |
| 125 | Angiotensin-converting enzyme inhibitors | /ˌændʒioʊˈtɛnsɪn kənˈvɜːrtɪŋ ˈɛnzaɪm ɪnˈhɪbɪtərz/ | Thuốc ức chế men chuyển Angiotensin |
| 126 | Angiotensin receptor blockers | /ˌændʒioʊˈtɛnsɪn rɪˈsɛptər ˈblɒkərz/ | Thuốc chẹn thụ thể Angiotensin |
| 127 | Beta blockers | /ˈbeɪtə ˈblɒkərz/ | Thuốc chẹn beta |
| 128 | Aldosterone inhibitors | /ælˈdɒstəroʊn ɪnˈhɪbɪtərz/ | Thuốc ức chế Aldosterone |
| 129 | Restrictive pulmonary impairment | /rɪˈstrɪktɪv ˈpʊlmənəri ɪmˈpɛərmənt/ | Suy giảm chức năng phổi hạn chế |
| 130 | Pulmonary function test (PFT) | /ˈpʊlmənəri ˈfʌŋkʃən tɛst/ | Đo chức năng hô hấp |
| 131 | Polysomnography | /ˌpɒlisoʊmˈnɒɡrəfi/ | Đa ký giấc ngủ |
| 132 | Nocturnal hypoventilation | /nɒkˈtɜːrnl ˌhaɪpoʊˌvɛntɪˈleɪʃən/ | Giảm thông khí về đêm |
| 133 | Hypercapnia | /ˌhaɪpərˈkæpniə/ | Tăng CO2 máu |
| 134 | Forced vital capacity (FVC) | /fɔːrst ˈvaɪtl kəˈpæsɪti/ | Dung tích sống gắng sức |
| 135 | Noninvasive ventilation (NIV) | /ˌnɒnɪnˈveɪsɪv ˌvɛntɪˈleɪʃən/ | Thông khí không xâm lấn |
| 136 | Bilevel positive airway pressure (BiPAP) | /ˈbaɪlɛvl ˈpɒzətɪv ˈɛərweɪ ˈprɛʃər/ | Áp lực đường thở dương hai mức (BiPAP) |
| 137 | Airway clearance | /ˈɛərweɪ ˈklɪərəns/ | Làm sạch đường thở |
| 138 | Atelectasis | /ˌætɪˈlɛktəsɪs/ | Xẹp phổi |
| 139 | Tracheostomy | /ˌtreɪkiˈɒstəmi/ | Mở khí quản |
| 140 | Intraparenchymal lung disease | /ˌɪntrəpəˈrɛŋkɪməl lʌŋ dɪˈziːz/ | Bệnh lý nhu mô phổi |
| 141 | Malnutrition | /ˌmælnjuːˈtrɪʃən/ | Suy dinh dưỡng |
| 142 | Metabolic syndrome | /ˌmɛtəˈbɒlɪk ˈsɪndroʊm/ | Hội chứng chuyển hóa |
| 143 | Hypermetabolic state | /ˌhaɪpərˌmɛtəˈbɒlɪk steɪt/ | Trạng thái tăng chuyển hóa |
| 144 | Percutaneous endoscopic gastrostomy (PEG) | /ˌpɜːrkjuːˈteɪniəs ˌɛndoʊˈskɒpɪk ɡæsˈtrɒstəmi/ | Mở thông dạ dày qua da nội soi (PEG) |
| 145 | Gastroparesis | /ˌɡæstroʊpəˈriːsɪs/ | Liệt dạ dày |
| 146 | Aspiration pneumonia | /ˌæspəˈreɪʃən njuːˈmoʊniə/ | Viêm phổi hít |
| 147 | Speech language pathologist (SLP) | /spiːtʃ ˈlæŋɡwɪdʒ pəˈθɒlədʒɪst/ | Chuyên gia ngôn ngữ trị liệu |
| 148 | Oropharyngeal dysfunction | /ˌɔːroʊfəˈrɪndʒiəl dɪsˈfʌŋkʃən/ | Rối loạn chức năng miệng-hầu |
| 149 | Esophageal dysfunction | /ɪˌsɒfəˈdʒiːəl dɪsˈfʌŋkʃən/ | Rối loạn chức năng thực quản |
| 150 | Glucocorticoid | /ˌɡluːkoʊˈkɔːrtɪkɔɪd/ | Glucocorticoid |