Ngoại khoa Căn bản: Vấn đề, Chẩn đoán và Quản lý, ấn bản thứ 7 (2026)
Essential Surgery: Problems, Diagnosis and Management, 7th Edition
Biên tập viên chính: Clive R. G. Quick, Suzanne Biers, Tan Arulampalam, Philip J. Deakin
Dịch & Chú giải: Ths.Bs. Lê Đình Sáng – (C) 2026 Elsevier Limited
Chương 5. Chẩn đoán Hình ảnh và Kỹ thuật Can thiệp trong X-Quang và Ngoại khoa
Imaging and interventional techniques in radiology and surgery
Clive R.G. Quick, MBBS(London), FDS, FRCS(England), MS(London), MA(Cantab); Suzanne M. Biers, BSc, MBBS, MD, FRCS; Tan H.A. Arulampalam, MBBS, MD, FRCS
Essential Surgery: Problems, Diagnosis and Management, 5, 62-86
Dẫn Nhập (Introduction)
Chương này cung cấp cái nhìn tổng quan về các quy trình chẩn đoán hình ảnh (imaging), nội soi (endoscopic), can thiệp (interventional) và sinh thiết (biopsy) được sử dụng để đưa ra chẩn đoán và điều trị bệnh nhân. X-Quang can thiệp (Interventional radiology) mô tả các thủ thuật xâm lấn tối thiểu (minimal access procedures) sử dụng hướng dẫn hình ảnh để điều trị các tình trạng bệnh lý với mức độ tổn thương thấp nhất. Kỹ thuật này thường được thực hiện bởi các bác sĩ X-Quang (radiologists) hoặc các bác sĩ lâm sàng chuyên khoa (specialist clinicians). Các ví dụ bao gồm nong mạch (angioplasty), mở thận ra da (nephrostomy) và đặt stent đường mật (biliary stents) qua nội soi.
X-Quang Thường Quy (Plain radiology)
Các mô cơ thể hấp thụ tia X theo tỷ lệ mật độ điện tử (electron density) của chúng, được xác định bởi số nguyên tử (atomic number) của các nguyên tố và mật độ vật lý (physical density) của chúng. Một phim chụp X-Quang thường quy là một “bóng” (shadow) của tổng hợp mật độ dọc theo đường đi của chùm tia X, trong khi chụp cắt lớp vi tính (computed tomography – CT) là một bản đồ về mật độ điện tử trong một lát cắt của cơ thể. Canxi (Calcium), một nguyên tử lớn có trong xương, có nhiều điện tử, do đó xương hấp thụ tia X tương đối dễ dàng. Theo quy ước lịch sử, xương được hiển thị màu trắng trên X-Quang và do đó cũng được hiển thị màu trắng trên CT. Thuốc cản quang (Contrast media) hấp thụ tia X tốt vì chúng chứa I-ốt (iodine) hoặc Bari (barium)—các nguyên tử lớn có nhiều điện tử.
Mặt khác, các mô mật độ thấp được tạo thành từ các nguyên tử có số nguyên tử thấp, chẳng hạn như không khí (air) trong phổi, hấp thụ ít tia X và được hiển thị màu đen. Các mô mật độ trung gian như cơ (muscle), chủ yếu được cấu tạo từ nước (water), được hiển thị màu xám. Mật độ điện tử của chất béo (fat) thấp hơn nước vì các phân tử của nó được sắp xếp kém đặc hơn; do đó, chất béo không hấp thụ nhiều tia X như nước. Để dễ hiểu hơn, hãy nhớ rằng chất béo nổi trên mặt nước vì mật độ vật lý của nó thấp hơn nước. Đây là lý do tại sao chất béo xung quanh các cơ quan trong ổ bụng xuất hiện tối hơn nước, ví dụ, trong túi mật (gall bladder) trên phim CT.
Một số dị vật (foreign bodies) có tính cản quang (radiopaque), bao gồm kim loại (metal) và hầu hết các mảnh thủy tinh (glass fragments) và có thể được nhìn thấy trên X-Quang thường quy và CT. Gỗ (wood) và nhựa (plastic) có tính thấu quang (radiolucent) và thường không được hiển thị trên X-Quang thường quy. Gỗ có thể hiện ra dưới dạng vùng thấu quang mật độ thấp trên CT, và nhựa có hình ảnh thay đổi tùy thuộc vào thành phần cụ thể của nó. Các miếng gạc phẫu thuật (Gauze swabs) được sử dụng trong phòng mổ là thấu quang nhưng có một sợi cản quang, cho phép chúng được định vị bằng X-Quang nếu bị bỏ quên trong cơ thể (Hình 5.1). Siêu âm (Ultrasound) có thể được sử dụng để định vị dị vật ở các vị trí nông, chẳng hạn như da (skin) và mô dưới da (subcutaneous tissues).
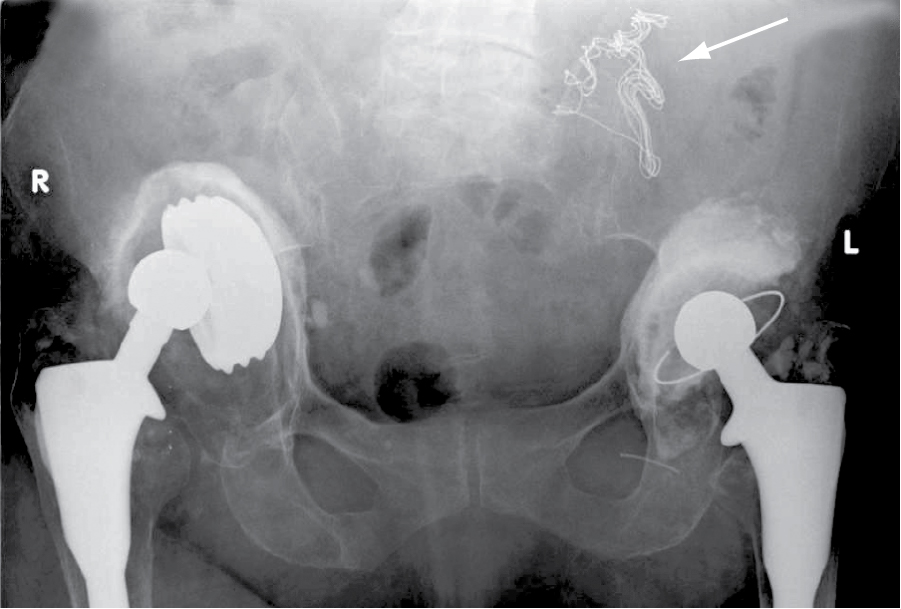
[Hình 5.1] X-Quang bụng thường quy cho thấy gạc phẫu thuật bị bỏ quên. Bệnh nhân nữ 83 tuổi này bị đau dai dẳng ở hố chậu trái sau khi thay khớp háng trái. Phim X-Quang khung chậu này được chụp để kiểm tra khớp mới. Tuy nhiên, một dấu cản quang (mũi tên) đã được phát hiện, chỉ ra một miếng gạc phẫu thuật đã bị bỏ quên trong ổ bụng sau một cuộc mở bụng (laparotomy) để xử lý thủng ổ loét tá tràng (perforated duodenal ulcer) 8 năm trước đó. Miếng gạc đã được lấy ra suôn sẻ trong lần mở bụng thứ hai.
An toàn trong Khoa Chẩn đoán Hình Ảnh Y học (Safety in departments of medical imaging)
An toàn bức xạ (Radiation safety)
Bức xạ ion hóa (Ionising radiation) vừa gây đột biến (mutagenic) vừa gây ung thư (carcinogenic), và việc chiếu xạ bệnh nhân và người quan sát phải được giảm thiểu. Điều này được thực hiện theo các cách sau:
- Cung cấp đào tạo về bảo vệ bức xạ (radiation protection) cho tất cả nhân viên sử dụng và làm việc gần thiết bị X-Quang.
- Đảm bảo mọi xét nghiệm đều có khả năng giúp ích cho việc quản lý và không được thực hiện một cách ‘thường quy’.
- Liên tục cải tiến thiết kế thiết bị X-Quang để giảm thiểu liều bức xạ (radiation dose) và bức xạ tán xạ (scatter) từ thiết bị, đồng thời duy trì chi tiết chẩn đoán.
- Bức xạ năng lượng thấp, có thể bị hấp thụ bởi cơ thể, được loại bỏ bằng các bộ lọc mỏng bằng đồng (copper) hoặc nhôm (aluminium) đặt phía trước chùm tia X. Bức xạ năng lượng thấp có thể gây hại tiềm tàng và không đóng góp vào việc hình thành hình ảnh.
- Các rào cản vật lý được xây dựng trong các phòng X-Quang (radiology suites) hoặc được cung cấp để bảo vệ nhân viên. Chúng bao gồm thạch cao bari (barium plaster) trong tường, cửa sổ kính chì (lead-glass windows) và tạp dề cao su chì (lead-rubber aprons).
- Người làm việc liên quan đến tia X nên tránh xa đường đi của chùm tia trực tiếp và duy trì khoảng cách an toàn với nguồn tia X trong suốt quá trình chiếu. Sự giảm bức xạ theo khoảng cách được xác định bởi định luật nghịch đảo bình phương (inverse square law). Do đó, di chuyển cách xa chùm tia X vài feet (khoảng 1-2 mét) có thể giảm đáng kể liều lượng cho người vận hành.
- Tất cả những người tham gia chụp X-Quang nên được theo dõi và đeo huy hiệu phim nhạy cảm với tia X (x-ray-sensitive film badges), cần được đánh giá thường xuyên để phát hiện việc tiếp xúc quá mức với bức xạ.
An toàn thuốc cản quang (Contrast media safety)
1. Thuốc cản quang chứa I-ốt (Iodinated contrast): Thuốc cản quang chứa I-ốt tiêm tĩnh mạch (intravenous iodinated contrast) đôi khi có thể gây ra phản ứng quá mẫn (hypersensitivity reactions) và hiếm khi gây sốc phản vệ (anaphylaxis). Nó cũng có khả năng gây độc cho thận (nephrotoxic) ở những bệnh nhân bị suy giảm chức năng thận (impaired renal function). Các yếu tố nguy cơ (risk factors) cần được chỉ rõ trong yêu cầu xét nghiệm để giúp bác sĩ X-Quang lập kế hoạch thăm khám an toàn nhất. Các xét nghiệm thay thế, chẳng hạn như siêu âm, CT không tiêm thuốc (unenhanced CT) hoặc cộng hưởng từ (magnetic resonance – MR) có thể được xem xét.
Các yếu tố nguy cơ quan trọng đối với phản ứng quá mẫn bao gồm:
- Tiền sử phản ứng đã biết với thuốc cản quang chứa I-ốt.
- Tiền sử hen suyễn (asthma).
- Tiền sử dị ứng đáng kể hoặc chàm (eczema).
Các yếu tố nguy cơ đối với độc tính trên thận bao gồm:
- Đái tháo đường (Diabetes mellitus).
- Suy thận (Renal insufficiency) (luôn bao gồm kết quả xét nghiệm chức năng thận trong các yêu cầu chụp CT). Bệnh nhân có tốc độ lọc cầu thận ước tính (estimated glomerular filtration rates – EGFR) lớn hơn 45 mL/phút/1,73 m² không cần bất kỳ biện pháp phòng ngừa nào. Ở những người có EGFR từ 30 – 45 mL/phút/1,73 m², hãy cân nhắc bù nước trước khi tiêm thuốc cản quang bằng dung dịch muối sinh lý (normal saline) tiêm tĩnh mạch. Nếu EGFR nhỏ hơn 30 mL/phút/1,73 m², phải bù nước trước khi tiêm thuốc cản quang. Thuốc cản quang có thể được sử dụng nếu bệnh nhân đang chạy thận nhân tạo (dialysis) hoặc được lên kế hoạch chạy thận nhân tạo.
- Đa u tủy (Multiple myeloma).
- Suy tim (Heart failure).
2. Gadolinium chelates: Các hợp chất Gadolinium (Gadolinium compounds) được sử dụng để tăng cường tương phản (contrast enhancement) tiêm tĩnh mạch trong chụp cộng hưởng từ (MRI) có thể gây ra phản ứng dị ứng, mặc dù nguy cơ thấp hơn so với thuốc cản quang chứa I-ốt. Nguy cơ chính là gây xơ hóa hệ thống sinh do thận (nephrogenic systemic sclerosis) (một rối loạn xơ hóa da và các cơ quan) ở những bệnh nhân bị suy giảm chức năng thận. Một số hợp chất ít rủi ro hơn và nên được sử dụng nếu việc tăng cường tương phản là cần thiết ở bệnh nhân suy thận.
An toàn cộng hưởng từ (Magnetic resonance imaging safety)
MRI an toàn hơn so với bức xạ ion hóa. Nó thường được coi là an toàn trong thai kỳ (pregnancy) nhưng không nên được thực hiện mà không cân nhắc kỹ lưỡng. Một số bệnh nhân không thích ở trong ‘đường hầm’ (tunnel) và/hoặc tiếng kêu lách cách của máy. Các vấn đề an toàn chính của MR liên quan đến tác động của nam châm mạnh (powerful magnets) lên các vật thể sắt từ (ferromagnetic objects), cả bên ngoài và bên trong cơ thể bệnh nhân.
- Các vật thể sắt từ phải được loại trừ khỏi phòng chụp vì từ trường mạnh có thể đẩy chúng với tốc độ lớn đến mức chúng trở thành vật phóng (missiles) có khả năng gây thương tích về thể chất.
- Từ trường tác động lên các vật liệu kim loại cấy ghép (implanted metal) bao gồm dị vật cấy sâu (embedded foreign bodies) và kẹp phẫu thuật (surgical clips). Dị vật kim loại trong mắt có thể bị dịch chuyển và dẫn đến mù lòa. Hầu hết các kẹp phình mạch (aneurysm clips) hiện đại đều không nhiễm sắt từ (nonferromagnetic) và không bị ảnh hưởng bởi MRI nhưng vẫn cần được ghi chép đầy đủ trong hồ sơ bệnh án của bệnh nhân. Khoa chẩn đoán hình ảnh cần được thông báo về sự hiện diện của bất kỳ kẹp kim loại, vật cấy ghép (implants) hoặc thiết bị cố định nào để chúng có thể được kiểm tra về khả năng tương thích với MRI (MRI compatibility).
- Trong những năm gần đây, người ta đã chứng minh rằng bệnh nhân có hầu hết các loại máy tạo nhịp tim (cardiac pacemakers) có thể được chụp MRI an toàn. Tuy nhiên, khoa chẩn đoán hình ảnh vẫn phải được thông báo về sự hiện diện của máy tạo nhịp tim.
- Các bộ phận giả (prostheses) được cấy ghép chắc chắn, chẳng hạn như thay khớp háng (hip replacements) được làm bằng vật liệu ‘thân thiện với MRI’ (MRI-friendly), nhìn chung là an toàn.
Các Nguyên lý Chung của X-Quang (General principles of radiology)
Các yếu tố sau đây liên quan đến việc tạo ra một hình ảnh X-Quang hữu ích:
- Công suất và thời gian phơi sáng của tia X được chọn để cung cấp liều chiếu xạ (exposure) hữu ích cho chẩn đoán mà không quá liều. Hình ảnh chất lượng cao có một phạm vi mật độ phù hợp với vùng giải phẫu. Ví dụ, chụp cột sống ngực cần liều lớn hơn phổi.
- Các góc chiếu (projections) khác nhau tạo ra các góc nhìn khác nhau của cùng một đối tượng. Ống tia X thực chất là một nguồn điểm tạo ra một chùm tia phân kỳ (diverging beam) (Hình 5.2), do đó đối tượng bị phóng đại (magnified). Sự biến dạng ít ảnh hưởng nhất đến bộ phận cơ thể gần phim nhất, do đó bộ phận đó được hiển thị rõ ràng nhất. Hướng chùm tia nên được ghi lại trên phim vì nó có ý nghĩa đối với việc giải thích, ví dụ, phim ngực thẳng (frontal chest film) có thể là sau-trước (posteroanterior – PA) hoặc trước-sau (anteroposterior – AP). Với các lần chiếu nghiêng (lateral exposures), mặt gần phim nhất được chỉ định, ví dụ, phim X-Quang ngực nghiêng ‘Rt’ (Right lateral chest x-ray – CXR) có mặt phải gần phim nhất.
- Tư thế bệnh nhân (Patient position) trong khi chiếu (ví dụ: nằm ngửa (supine), nằm sấp (prone), nghiêng (oblique) hoặc đứng thẳng (erect)) ảnh hưởng đến hình ảnh vì trọng lực tác động lên các cơ quan, khí (gas) hoặc dịch (fluid). Hầu hết các phim X-Quang bụng được chụp khi bệnh nhân nằm ngửa với chùm tia X hướng thẳng đứng xuống. Một chùm tia ngang (horizontal beam) (tư thế đứng thẳng hoặc nằm nghiêng – lateral decubitus) có thể thể hiện mức dịch (fluid levels) trong khoang hoặc ruột, hoặc khí tự do (free gas) dưới cơ hoành (diaphragm).
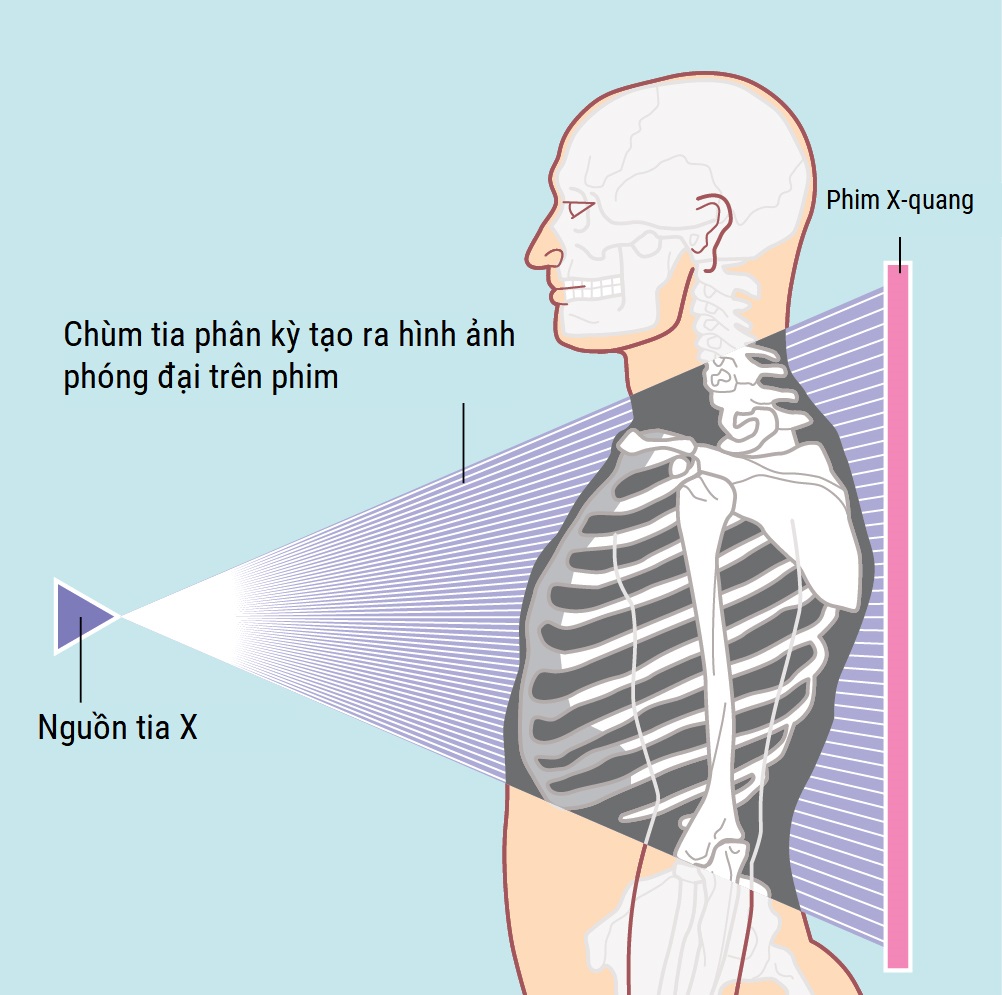
[Hình 5.2] Góc chiếu X-Quang.
Lưu trữ và Truyền Tải Hình Ảnh (Image storage and transfer)
Hầu như tất cả các hình ảnh hiện được lưu trữ điện tử dưới dạng kỹ thuật số (digital format) và được xem và giải thích từ màn hình máy tính. Các hệ thống lưu trữ dữ liệu điện tử cần được duy trì và bảo vệ khỏi vi-rút, phần mềm độc hại (malware intrusion) và tin tặc (hackers). Điều này đòi hỏi sự hỗ trợ của Công nghệ Thông tin (IT). Việc cập nhật phần cứng (hardware) và phần mềm (software) là cần thiết để bắt kịp với những thay đổi công nghệ và các mối đe dọa đối với tính toàn vẹn của dữ liệu (data integrity).
Hình ảnh điện tử có ưu điểm lớn là chúng có thể được xem từ nhiều địa điểm trong cùng một cơ sở cùng một lúc. Chúng cũng có thể dễ dàng được chuyển qua mạng đến các cơ sở khác, nhà của bác sĩ lâm sàng hoặc thậm chí đến các nơi khác trên thế giới để giải thích.
X-Quang Thường Quy (Plain radiology)
Phim X-Quang thường quy ngực và bụng hiện nay ít được sử dụng trong thực hành ngoại khoa hơn. Những hạn chế của chúng được nhận ra rõ hơn, và sự sẵn có của CT ngày càng tăng. Các nghiên cứu đã chỉ ra rằng CT chính xác hơn nhiều trong việc chẩn đoán nhiều loại bệnh lý bụng cấp tính (acute abdominal conditions), vì vậy nó được sử dụng thường xuyên hơn và sớm hơn trong quy trình chẩn đoán so với trước đây. Trong các trường hợp nghi ngờ thủng tạng (suspected perforation) hoặc tắc ruột (bowel obstruction), X-Quang thường quy ngực và bụng vẫn thường được sử dụng làm xét nghiệm hình ảnh đầu tiên. X-Quang bụng thường quy cũng hữu ích để theo dõi sự giãn đại tràng (colonic dilatation) ở bệnh nhân viêm đại tràng (colitis). Trong các tình huống không khẩn cấp, chúng cũng hữu ích để theo dõi sỏi đường tiết niệu (renal tract calculi) về kích thước, số lượng và vị trí.
X-Quang Ngực (Chest radiograph)
Việc giải thích X-Quang ngực thường quy (CXR) đòi hỏi một phương pháp tiếp cận có hệ thống. (tham khảo thêm liên kết geekymedics.com).
X-Quang Bụng (Abdominal radiograph)
Việc giải thích X-Quang bụng đòi hỏi một phương pháp tiếp cận có hệ thống. Sẽ hữu ích nếu xem xét các cơ quan trong và xung quanh khoang bụng một cách có phương pháp, cả trong phúc mạc (intraperitoneal) và sau phúc mạc (retroperitoneal), đáy phổi, xương và các lỗ thoát vị (hernial orifices). (tham khảo thêm liên kết geekymedics.com).
Khi kiểm tra X-Quang bụng, các đặc điểm quan trọng cần tìm kiếm là:
- Vôi hóa (Calcification) ở các khu vực dễ hình thành sỏi (ví dụ: thận (kidney), niệu quản (ureters), bàng quang (bladder) hoặc đường mật (biliary tree)).
- Ống tiêu hóa (gastrointestinal – GI) giãn (dạ dày (stomach) hoặc ruột non (small bowel) hoặc ruột già/đại tràng (large bowel)).
- Khí tự do trong phúc mạc (Free intraperitoneal gas) cho thấy thủng ruột (bowel perforation).
- Khí ở những vị trí bất thường (ví dụ: đường mật hoặc đường tiết niệu—gợi ý rò với ruột (fistula with the bowel)).
- Các vật thể phi sinh học (Non-biological objects) (ví dụ: dị vật, ống phẫu thuật (surgical tubes) hoặc mảnh kim loại).
- Vôi hóa bệnh lý (Pathological calcification) (ví dụ: phình động mạch chủ (aortic aneurysm), tụy (pancreas), tuyến thượng thận (adrenals) hoặc u xơ tử cung (uterine fibroids)).
Hầu hết các phim bụng được chụp khi bệnh nhân nằm ngửa. Ruột có thể nhìn thấy khi nó chứa khí (Hình 5.3 và 5.4); ruột non bình thường rộng dưới 3 cm và có xu hướng nằm ở trung tâm ổ bụng. Khi giãn, nó cho thấy các nếp gấp ngang (nếp vòng – plicae circulares) cắt ngang hoàn toàn lòng ruột. Đại tràng thường nằm ở ngoại vi và có các ngấn (haustrations); các nếp gấp này chỉ cắt ngang lòng ruột một phần (xem Hình 5.3). Đại tràng bình thường rộng dưới 6 cm và thường chứa các khối phân với hình ảnh lốm đốm.
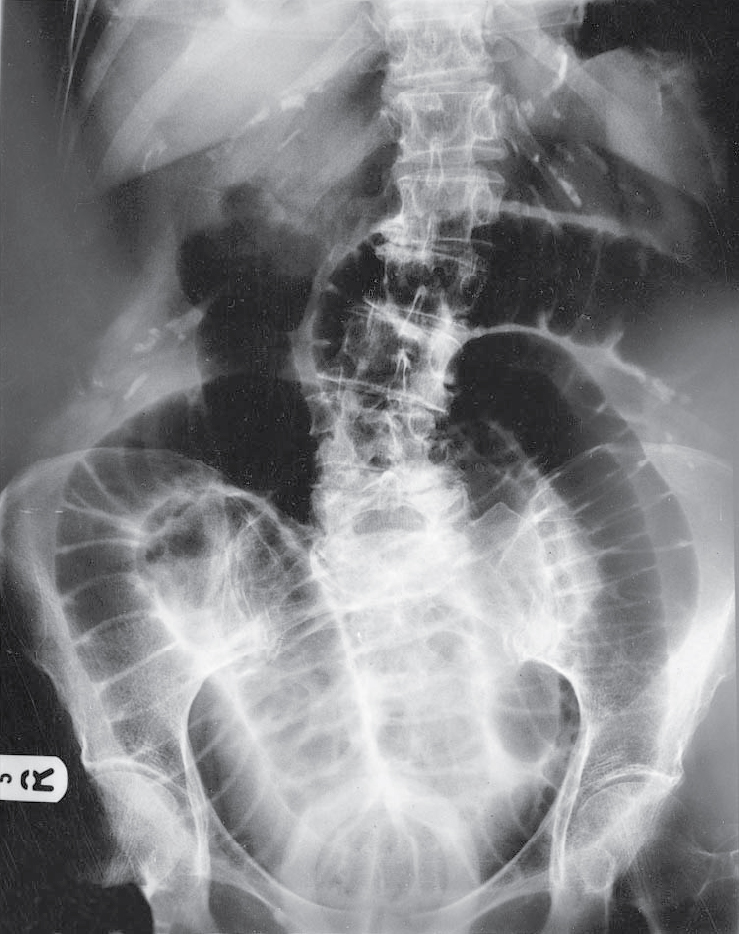
[Hình 5.3] X-Quang bụng. Một phim X-Quang bụng thường quy tư thế nằm ngửa cho thấy ruột non giãn to rõ rệt. Khi mở bụng, nguyên nhân được xác định là ung thư biểu mô tắc nghẽn ở manh tràng (carcinoma of the caecum).
Các hạn chế của X-Quang bụng thường quy được tóm tắt trong Hộp 5.1.
HỘP 5.1 Hạn chế của X-Quang bụng thường quy
|
Khí tự do trong phúc mạc (Free intraperitoneal gas)
Khí tự do là dấu hiệu chẩn đoán thủng ruột (bowel perforation), ngoại trừ sau khi mở bụng (laparotomy) gần đây. Khí tự do thường tồn tại trong 3 đến 6 ngày sau khi mở bụng, mặc dù nó có thể kéo dài hơn. Điều này có thể gây khó khăn trong việc chẩn đoán rò miệng nối (anastomotic leak) có thể xảy ra. Khí carbon dioxide được sử dụng trong phẫu thuật nội soi (laparoscopic surgery) thường được hấp thụ nhanh hơn không khí.
X-Quang ngực tư thế đứng thẳng là kỹ thuật X-Quang thường quy tốt nhất (CT còn tốt hơn) để chứng minh khí tự do từ một chỗ thủng. Thủng cũng có thể được chẩn đoán khi cả mặt trong và mặt ngoài của thành ruột được bao bọc bởi các bóng mờ thấu quang (radiolucent shadows). Đây được gọi là dấu hiệu Rigler (Rigler’s sign). Nên yêu cầu chụp CT khi chẩn đoán lâm sàng không rõ ràng hoặc X-Quang thường quy không chắc chắn, bệnh nhân quá yếu để ngồi hoặc đứng, hoặc nếu lâm sàng nghi ngờ thủng nhưng X-Quang thường quy không thấy khí tự do (xem Hình 5.4).
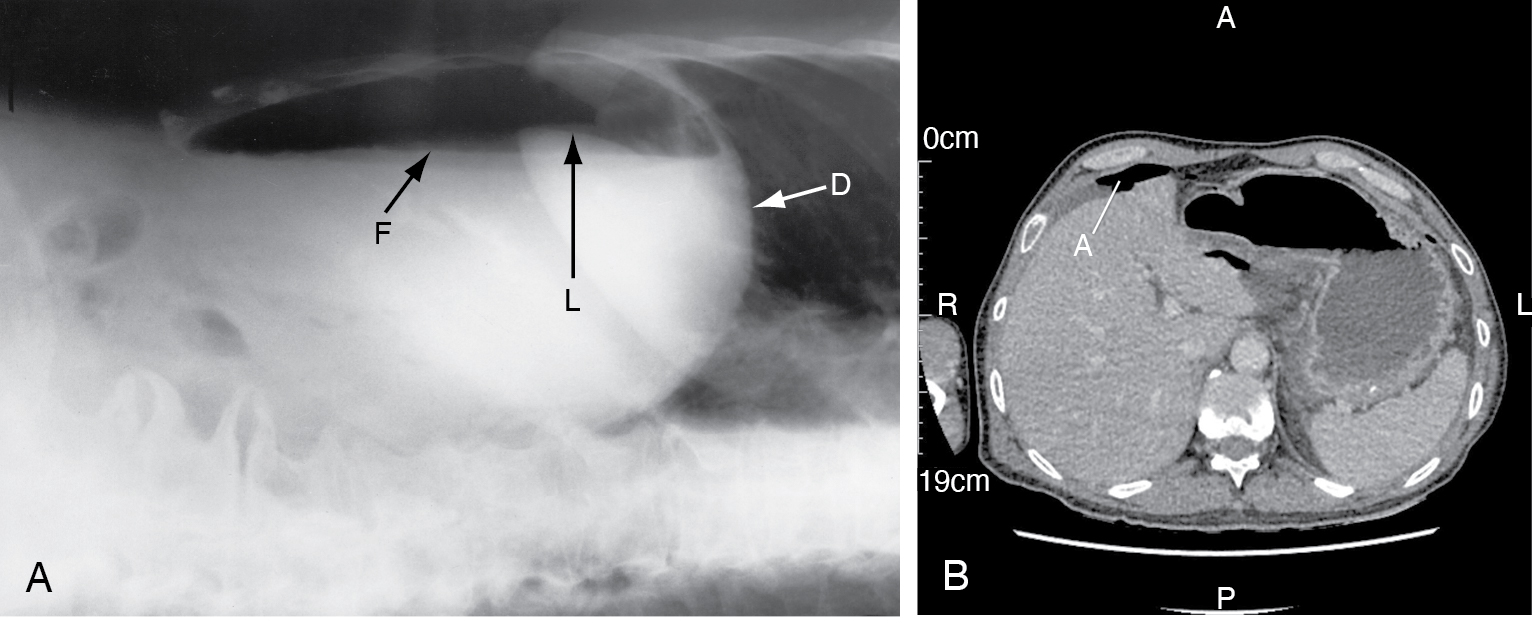
[Hình 5.4] Khí tự do trong ổ bụng. Bệnh nhân nữ 78 tuổi này nhập viện với cơn đau bụng đột ngột, dữ dội. X-Quang ngực đứng thẳng (A) không thấy khí tự do trong ổ bụng, nhưng lâm sàng nghi ngờ thủng, nên đã thực hiện X-Quang nằm nghiêng (lateral decubitus). Phía bên phải được nâng lên, và đầu hướng về bên phải của hình ảnh; chùm tia X là ngang. Khí tự do trong phúc mạc được nhìn thấy phía trên mức dịch (F) bên dưới cơ hoành (D) và ‘nổi’ trên gan (L). Khi mở bụng, nguyên nhân được xác định là thủng ổ loét tá tràng. CT cắt ngang (B) cho thấy khí ngoài lòng ruột (extraluminal air) tự do từ một ổ loét tá tràng bị thủng (A).
X-Quang Xương (Bone radiographs)
X-Quang xương thông thường vẫn giữ vai trò quan trọng trong chẩn đoán các bệnh lý xương: gãy xương (fractures), nhiễm trùng (infection), tân sinh (neoplasia) và các bệnh lý thoái hóa (degenerative conditions). Các xét nghiệm khác bao gồm xạ hình xương (bone scintigraphy), CT, MRI và siêu âm được sử dụng khi X-Quang bình thường hoặc để đánh giá thêm các bất thường được chứng minh bằng X-Quang. Nếu nghi ngờ, hãy thảo luận với bác sĩ X-Quang.
X-Quang Cản Quang (Contrast radiology)
Nhiều nghiên cứu cản quang đã được sử dụng trước đây đã được thay thế bằng các xét nghiệm khác, tốt hơn:
- Chụp niệu đồ tĩnh mạch (Intravenous urogram – IVU) → Chụp niệu đồ CT (CT urogram), CT hệ tiết niệu không chuẩn bị (CT KUB – kidneys, ureters and bladder). Đôi khi là Chụp niệu đồ MR (MR urogram).
- Chụp khung đại tràng bằng Bari (Barium enema) → Chụp cắt lớp vi tính đại tràng (CT colonography).
- Chụp ruột non theo dõi bằng Bari (Barium follow-through) → Chụp ruột non bằng MR (MR enterography) hoặc CT (CT enterography).
- Chụp động mạch bằng ống thông (Catheter angiography) → Chụp mạch MR (MR angiography – MRA), Chụp mạch CT (CT angiography – CTA) hoặc Siêu âm Doppler (Doppler ultrasound).
- Chụp tĩnh mạch (Venography) → Siêu âm Doppler, Chụp tĩnh mạch CT hoặc MR (CT or MR venography).
Các nghiên cứu cản quang vẫn hữu ích trong các tình huống sau:
- Thực quản (Oesophagus): cho phép quan sát cơ chế nuốt (swallowing mechanism) và nhu động thực quản (oesophageal peristalsis) trong thời gian thực.
- Lỗ rò ruột-da (Enterocutaneous fistulae): để đánh giá các kết nối sâu của các lỗ rò tiềm ẩn bằng cách tiêm thuốc cản quang trực tiếp qua lỗ ngoài da.
- Đánh giá tính toàn vẹn của miệng nối (anastomosis): ví dụ, sau phẫu thuật ung thư trực tràng trước khi đóng hồi tràng hoặc đại tràng tạo hậu môn nhân tạo (defunctioning ileostomy or colostomy).
- Khi xét nghiệm CT hoặc MR thay thế bị chống chỉ định (contraindicated) hoặc không có sẵn.
Các Chất Cản Quang (Contrast materials)
Bari sulfat (Barium sulphate) có mật độ rất cao và hữu ích cho việc phác thảo trực tiếp đường tiêu hóa (GI tract) trừ khi nghi ngờ rò rỉ (leak) hoặc thủng (perforation) hoặc có nguy cơ hít vào phổi (aspirating into the lungs). Trong những trường hợp này, nên sử dụng hợp chất chứa I-ốt tan trong nước (water-soluble iodinated compound) (xem Hộp 5.2).
HỘP 5.2 Hạn chế của nghiên cứu cản quang Bari
|
Các dẫn xuất axit benzoic có chứa I-ốt (Iodinated benzoic acid derivatives) là các hợp chất tan trong nước có thể được tiêm vào động mạch (arteries) hoặc tĩnh mạch (veins) để làm chúng cản quang. Tăng cường tương phản của phim CT cung cấp thêm thông tin hữu ích; ví dụ, hình ảnh hẹp động mạch (arterial stenoses) hoặc huyết khối tĩnh mạch (venous thromboses) hiệu quả hơn bằng cách sử dụng liều thuốc cản quang thấp hơn và do đó thay thế các nghiên cứu trực tiếp. CT tăng cường tương phản (Enhanced CT) làm tăng khả năng hiển thị của di căn gan (liver metastases) so với CT không tăng cường.
Gadolinium chelates là các hợp chất sắt từ được tiêm để tăng cường tương phản các mô trong quá trình chụp MRI. Chúng tương tự như các chất cản quang chứa I-ốt được sử dụng với CT và có thể làm tăng khả năng hiển thị của các tổn thương và cung cấp thông tin về động mạch và tĩnh mạch.
Chất cản quang siêu âm (Ultrasound contrast agents) bao gồm một bong bóng khí siêu nhỏ (micro air bubble) bên trong một vỏ bọc. Bong bóng khí phản xạ sóng âm và do đó chất cản quang hiển thị sáng trên hình ảnh. Siêu âm tăng cường tương phản (Contrast-enhanced ultrasound) chủ yếu được sử dụng trong việc đánh giá các tổn thương gan, để phân biệt các tổn thương lành tính (benign lesions) với các tổn thương ác tính (malignant lesions) nhờ các đặc điểm mạch máu khác nhau của chúng. Các chất này cũng hữu ích để tăng độ rõ nét của mạch máu hoặc buồng tim (cardiac chambers) và xác định sự hiện diện hay vắng mặt của cục máu đông (clots) hoặc tắc nghẽn (occlusions).
Ví dụ về X-Quang Cản Quang
Đại tràng (Large bowel) Với công nghệ được cải thiện, CT đã gần như thay thế hoàn toàn chụp khung đại tràng bằng Bari (barium enema). CT có thể được thực hiện mà không cần chuẩn bị thuốc nhuận tràng (laxative preparation) trong những trường hợp chấp nhận bỏ sót các polyp nhỏ và có thể đặc biệt hữu ích ở người lớn tuổi ốm yếu khi nghi ngờ ung thư đại tràng bên phải (right-sided colonic cancer) do thiếu máu (anaemia) hoặc một khối sờ thấy được (palpable mass).
Ở những bệnh nhân cần phát hiện polyp cũng như ung thư lớn hơn, Chụp cắt lớp vi tính đại tràng (CT colonography – CTC) được ưu tiên. CTC bao gồm việc làm sạch ruột để loại bỏ các chất phân. Không khí hoặc, tốt hơn là, carbon dioxide được bơm vào trực tràng để làm căng ruột. Kỹ thuật này đủ nhạy để phát hiện các tổn thương từ 1 cm (hoặc 10 mm) hoặc thậm chí nhỏ hơn. Với một kỹ thuật tốt, độ chính xác của CTC tương đương với nội soi đại tràng quang học (optical colonoscopy) trong việc phát hiện polyp và ung thư (Hình 5.5).
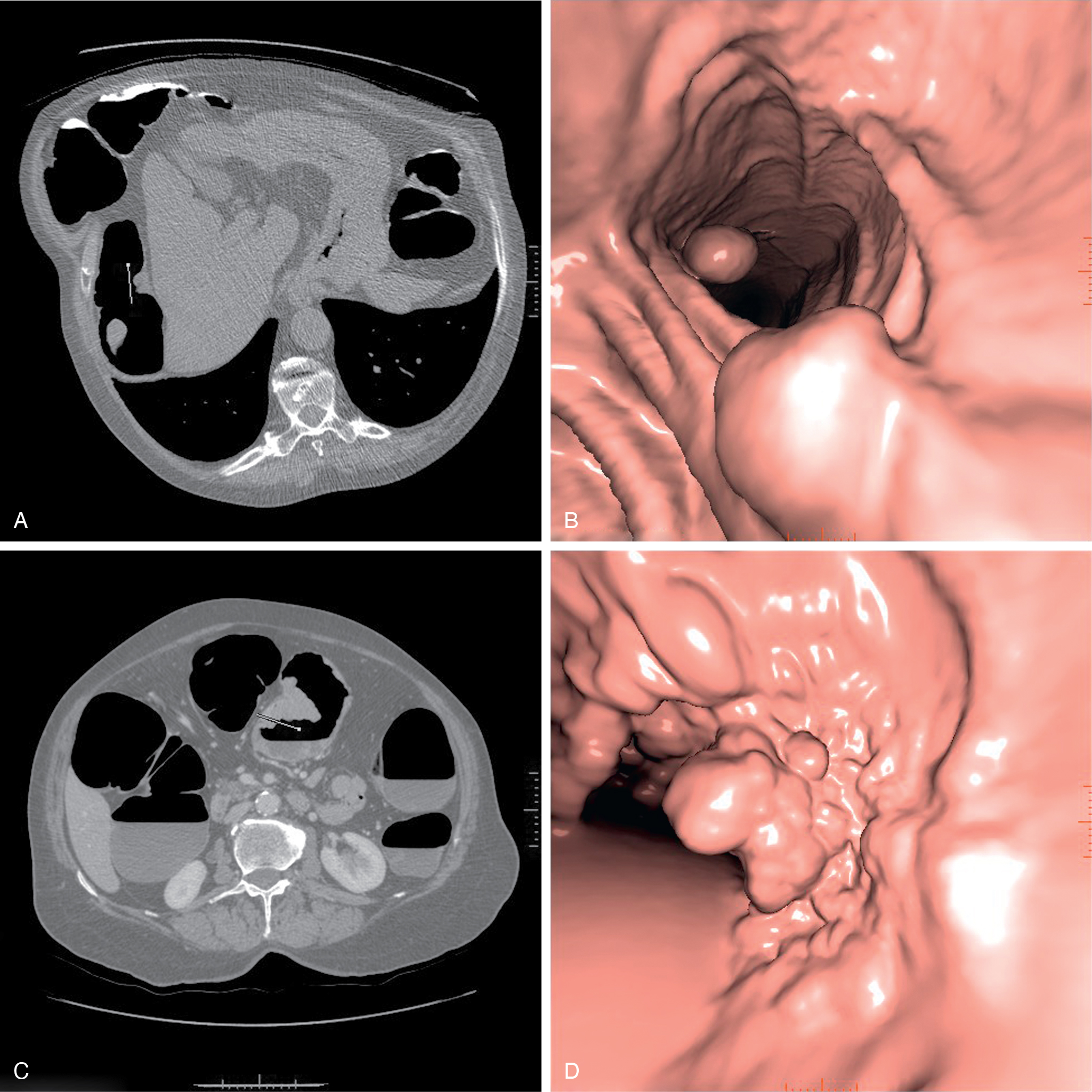
[Hình 5.5] Ví dụ về Chụp cắt lớp vi tính đại tràng (CT colonography). (A) Tư thế nằm sấp. Một trong các hình ảnh CT cắt ngang được sử dụng để tái tạo hình ảnh ba chiều (3D) cho thấy một polyp tuyến (adenomatous polyp) trong (B). (C) Một trong các hình ảnh CT cắt ngang được sử dụng để tái tạo hình ảnh 3D cho thấy một ung thư biểu mô đại tràng ngang (transverse colon carcinoma) trong (D).
Ruột non (Small bowel) Việc sử dụng các nghiên cứu Bari để kiểm tra ruột non đang giảm dần và được thay thế bằng Chụp ruột non bằng CT hoặc MR (CT or MR enterography). Những kỹ thuật này cũng cho phép kiểm tra mạc treo (mesentery) gắn vào ruột để tìm các biến chứng như áp xe (abscesses) hoặc lỗ rò. Nội soi viên nang (Capsule endoscopy) có thể được sử dụng để tìm kiếm các tổn thương nhỏ mà các xét nghiệm khác không phát hiện được (xem phần sau).
X-Quang Đường Mật (Biliary radiology)
Chụp Cộng Hưởng Từ Đường Mật Tụy (Magnetic resonance cholangio-pancreatography – MRCP)
MRCP (Hình 5.6c và d) là một phương thức chẩn đoán ít xâm lấn hơn so với Chụp Mật Tụy Ngược Dòng Qua Nội Soi (Endoscopic retrograde cholangio-pancreatography – ERCP). MRCP là một chuỗi xung MRI đặc biệt mô tả nước có cường độ tín hiệu cao (nước sáng) trong khi triệt tiêu tín hiệu nền (background signal) từ các cơ quan khác (= tối). Vì mật (bile) và dịch tụy (pancreatic juice) chủ yếu là nước, MRCP cung cấp hình ảnh rõ ràng về mật trong túi mật và các ống dẫn (ducts) và phác thảo ống tụy (pancreatic duct). Nó cho thấy các khiếm khuyết lấp đầy (filling defects) gây ra bởi sỏi (stones) hoặc khối u (tumours). MRCP có thể xác định rò rỉ mật (bile leaks), sỏi mật trong ống mật (gallstones in bile ducts) và tắc nghẽn ống dẫn (duct obstruction) do bất kỳ nguyên nhân nào. Không có nguy cơ nào được biết đến. MRCP ngày càng được sử dụng trước ERCP để thăm dò tụy-mật nhằm giảm số lượng các thăm dò xâm lấn hơn (và có khả năng rủi ro) hơn.
Các chỉ định cho MRCP bao gồm:
|
Chụp Mật Tụy Ngược Dòng Qua Nội Soi (Endoscopic retrograde cholangio-pancreatography – ERCP)
Kỹ thuật này được mô tả sau trong chương này—xem phần Nội soi tá tràng chẩn đoán và điều trị (Diagnostic and Therapeutic Duodenoscopy); việc sử dụng nó trong vàng da tắc mật (obstructive jaundice) được mô tả chi tiết trong Chương 18. Kỹ thuật cơ bản được minh họa trong Hình 5.6A và B.
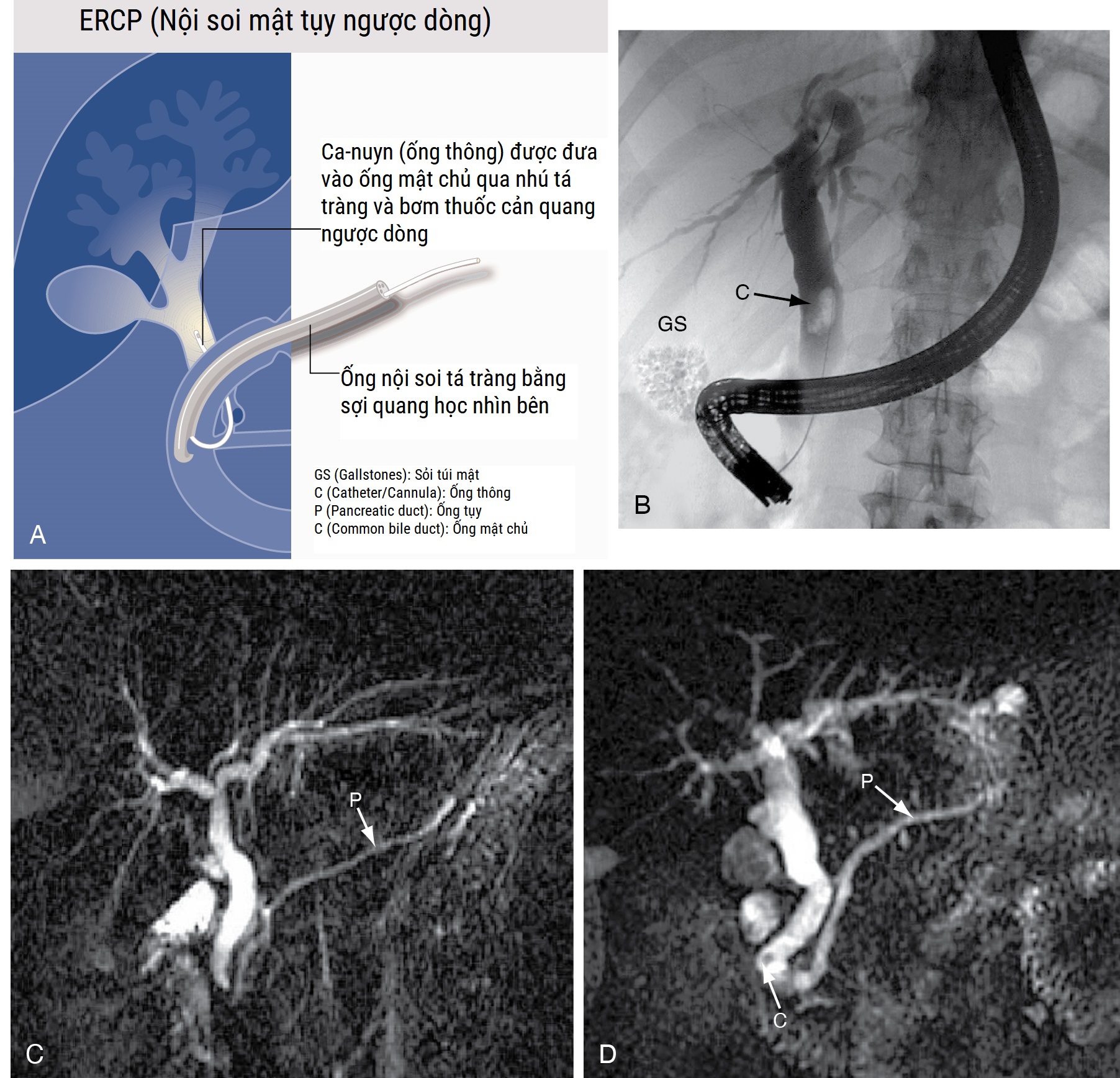
[Hình 5.6] Một số kỹ thuật để hiển thị hệ thống đường mật. (A và B) Chụp mật tụy ngược dòng qua nội soi. Bệnh nhân được an thần, và một ống nội soi tá tràng nhìn ngang (side-viewing gastroscope) được đưa xuống sao cho đầu ống đến phần thứ hai của tá tràng. Bóng Vater (ampulla of Vater) được đặt ống thông (cannulated) dưới sự quan sát trực tiếp và chất cản quang được tiêm ngược dòng (retrogradely) để phác thảo các ống mật. (B) Một viên sỏi mật lớn (C) được nhìn thấy bên trong ống mật chủ bị giãn (dilated common bile duct) và một tập hợp các viên sỏi mật cản quang (GS) được nhìn thấy trong túi mật. (C và D) Chụp Cộng Hưởng Từ Đường Mật Tụy (MRCP). Kỹ thuật này tạo ra hình ảnh chất lỏng tĩnh; do đó, hình ảnh là các chất bài tiết mật và tụy tự nhiên. Mỗi hình ảnh được thu được trong một giây bằng phương pháp chiếu lát dày (thick slab projection method) tạo ra hình ảnh rất giống với ERCP. Ống tụy trong mỗi hình ảnh được dán nhãn (P). (C) Một ví dụ về hệ thống ống mật và ống tụy bình thường. (D) Một viên sỏi nhỏ, (C), ở phần xa ống mật chủ. Cũng có sự giãn nhẹ của ống tụy với một số nhánh bên có thể nhìn thấy.
Chụp đường mật trong mổ và nội soi ống mật chủ (Operative cholangiography and choledochoscopy)
Việc thực hiện chụp đường mật trong mổ (operative cholangiography) là thông thường trong quá trình cắt túi mật mở (open cholecystectomy). Đối với cắt túi mật nội soi (laparoscopic cholecystectomy), một số bác sĩ phẫu thuật thực hiện chụp đường mật trong mổ một cách thường quy trong khi những người khác thích không chụp hình ảnh nào cả đối với các trường hợp được chọn lọc hoặc đánh giá trước mổ bằng MRCP đối với những trường hợp được cho là có khả năng có sỏi ống mật.
Chụp đường mật trong mổ cho phép hiển thị giải phẫu đường mật; nó chứng minh sỏi trong ống mật và cho thấy liệu thuốc cản quang có chảy tự do vào tá tràng (duodenum) hay không. Một ống thông nhựa mịn được đưa vào một vết mổ nhỏ trên ống túi mật (cystic duct) và đi vào ống mật chủ (common bile duct). Chất cản quang tan trong nước được tiêm để phác thảo hệ thống ống dẫn và hình ảnh X-Quang tăng sáng truyền hình (fluoroscopic images) hoặc phim X-Quang được chụp. Nếu sỏi ống dẫn được chứng minh, chúng thường được lấy ra bằng phẫu thuật trong cùng một cuộc mổ. Trong cắt túi mật mở, việc này được thực hiện thông qua một vết mổ dọc trong ống mật chủ (thăm dò ống mật chủ – exploration of the common bile duct).
Trong phẫu thuật nội soi, một kỹ thuật tương tự được sử dụng thông qua đường túi mật hoặc thông qua một vết cắt ngang hoặc dọc nhỏ trên ống mật chủ (choledochotomy), tùy thuộc vào kích thước ống dẫn và kích thước của viên sỏi cần được lấy ra. Một ống nội soi 5 mm (hoặc 3 mm) linh hoạt được gọi là ống nội soi ống mật chủ (choledochoscope) có thể được đưa vào ống mật và sỏi có thể được lấy ra bằng một loạt các kỹ thuật bao gồm thòng lọng (snares), rọ (baskets) và bóng (balloons) hoặc chúng thậm chí có thể được tán nhỏ bằng các đầu dò tán sỏi (lithotripsy probes). Ống nội soi ống mật chủ cho phép kiểm tra mật và các ống dẫn trong gan (intrahepatic ducts) sau đó để xác nhận rằng tất cả sỏi đã được loại bỏ. Một phim chụp đường mật tiếp theo thường được thực hiện sau đó để đảm bảo ống dẫn thông suốt. Việc loại bỏ sỏi ống dẫn có thể được hoãn lại và thực hiện sau đó tại ERCP, mặc dù điều này mang theo nguy cơ biến chứng, bao gồm rò rỉ mật (biliary leakage), viêm tụy cấp (acute pancreatitis) và thậm chí tử vong trong những trường hợp hiếm.
Chụp đường mật qua ống T (T-tube cholangiography)
Sau khi thăm dò ống mật để tìm sỏi, một ống chữ T (T-tube) thường được để lại tại chỗ để dẫn lưu ống mật. Nhánh ngang ngắn nằm bên trong ống dẫn và nhánh dài dẫn lưu ra bề mặt. Điều này cho phép tiêm thuốc cản quang sau mổ dưới hướng dẫn X-Quang tăng sáng truyền hình để phác thảo cây đường mật và cho thấy bất kỳ sỏi sót nào, rò rỉ mật hoặc hẹp ống dẫn (duct stenosis), cũng như xác nhận dẫn lưu mật tự do vào tá tràng. Nếu có sỏi sót lại, chúng có thể được lấy ra tại ERCP hoặc đôi khi bởi bác sĩ X-Quang thông qua ống chữ T. Việc sử dụng thường xuyên ống chữ T hiện đang giảm.
X-Quang Mạch Máu và Can Thiệp (Vascular and interventional radiology)
Các nguyên tắc chung và nguy cơ của chụp động mạch và tĩnh mạch
Thông tin chi tiết hơn về các ứng dụng của X-Quang mạch máu được đưa ra trong Chương 40.
Các tĩnh mạch (veins) hoặc động mạch (arteries) của một vùng giải phẫu có thể được làm cản quang bằng cách tiêm thuốc cản quang vào tĩnh mạch hoặc vào động mạch. Đây là chụp mạch (angiography) và bao gồm chụp động mạch (arteriography) và chụp tĩnh mạch (venography). Trong chụp động mạch, chọc kim vào động mạch tiếp cận (access artery) được tiếp nối bằng việc đưa dây dẫn (guidewire) vào, rút kim ra và đưa một ống bọc (sheath) qua dây dẫn. Các ống thông (catheters) và dây dẫn có hình dạng khác nhau được đưa qua ống bọc để đẩy đầu ống thông đến một vị trí thích hợp cho chụp động mạch. Các ống thông siêu nhỏ (Microcatheters) và dây dẫn siêu nhỏ (microwires) có sẵn để cho phép đặt ống thông siêu chọn lọc (super-selective catheterisation) vào các mạch nhỏ hơn.
Các nghiên cứu đông máu (Clotting studies) nên được thực hiện trước đó để dự đoán các biến chứng xuất huyết (haemorrhagic complications) tiềm tàng từ vị trí chọc mạch, đặc biệt nếu bệnh nhân đang dùng thuốc chống đông máu (anticoagulants) hoặc nếu có nghi ngờ về rối loạn đông máu tiềm ẩn.
Thuốc cản quang giống như loại được sử dụng cho CT và mang các nguy cơ tương tự, đó là phản ứng dị ứng và độc tính trên thận (xem phần trước).
Các biến chứng từ vị trí tiếp cận mạch máu bao gồm chảy máu (bleeding) hoặc huyết khối (thrombosis) trong tĩnh mạch và bóc tách (dissection), rò động tĩnh mạch (arteriovenous fistula) hoặc hình thành giả phình mạch (pseudoaneurysm) trong động mạch.
Chụp động mạch (Arteriography)
Chụp mạch xóa nền kỹ thuật số (Digital subtraction angiography – DSA) là tiêu chuẩn vàng (gold standard) để chụp ảnh mạch máu. Độ cản quang không đổi của hình ảnh X-Quang thường quy (đặc biệt là xương và khí ruột) được xóa bỏ kỹ thuật số (digitally subtracted) khỏi hình ảnh sau khi tiêm thuốc cản quang. Tuy nhiên, do những tiến bộ trong hình ảnh cắt ngang (CT và MRI), các phương thức này hiện tạo ra hình ảnh chẩn đoán thỏa đáng để giúp xác định mô hình bệnh lý và hỗ trợ lập kế hoạch điều trị, đồng thời ít xâm lấn hơn DSA.
Lưu ý rằng chụp mạch chẩn đoán trực tiếp đánh giá tốt hơn tình trạng hẹp (stenoses) hoặc tắc nghẽn (occlusions), đặc biệt ở các mạch máu bị vôi hóa nặng, vì CT thường đánh giá quá mức mức độ nghiêm trọng của hẹp do vôi hóa.
Các kỹ thuật nội mạch (Endovascular techniques)
Nong mạch qua da nội lòng mạch (Percutaneous transluminal angioplasty) hoặc Nong mạch bằng bóng (balloon angioplasty)
Nong mạch dưới gây tê tại chỗ là một lựa chọn ít xâm lấn hơn so với phẫu thuật để điều trị nhiều trường hợp hẹp động mạch ngoại vi (peripheral) và động mạch vành (coronary). Nói chung, hẹp ngắn ở các mạch lớn là phù hợp nhất. Các biến chứng lớn của nong mạch là hiếm gặp nhưng có một nguy cơ nhỏ gây thiếu máu cục bộ cấp tính (acute ischaemia) do thuyên tắc xa (distal embolisation) hoặc bóc tách. Do đó, cần phải có sẵn phương pháp cứu chữa bằng phẫu thuật (surgical salvage) nếu biến chứng phát triển. Tỷ lệ hẹp lại (restenosis) hoặc tắc nghẽn của các tổn thương đã được nong mạch trong vòng 1 năm là 25%-40%, nhưng quá trình này thường có thể được lặp lại. Khi hẹp không thể giữ thông suốt bằng nong bóng thường, stent có thể được đặt qua tổn thương đã điều trị để duy trì độ thông suốt. Những tiến bộ bao gồm việc tích hợp thuốc chống tăng sinh (antiproliferative properties) vào bóng và stent để giảm tỷ lệ hẹp lại. Stent ngày càng được sử dụng nhiều trong hẹp và tắc nghẽn động mạch chậu (iliac), động mạch đùi nông (superficial femoral artery) và động mạch khoeo (popliteal).
Các kỹ thuật nong mạch qua da
Nong mạch thường được thực hiện dưới gây tê tại chỗ (Hình 5.7). Kỹ thuật này bao gồm việc đưa kim vào động mạch, đưa dây dẫn, đưa ống bọc (sheath), đưa ống thông, thay dây dẫn dài, và cuối cùng là đưa ống thông nong mạch với bóng (angioplasty catheter) qua chỗ hẹp. Bóng được bơm hơi đến áp suất điển hình từ 6 đến 15 atm (608 kPa đến 1520 kPa) để nong chỗ hẹp. Có thể đo gradient áp suất trước và sau khi nong mạch để đánh giá khách quan đáp ứng sinh lý với điều trị.
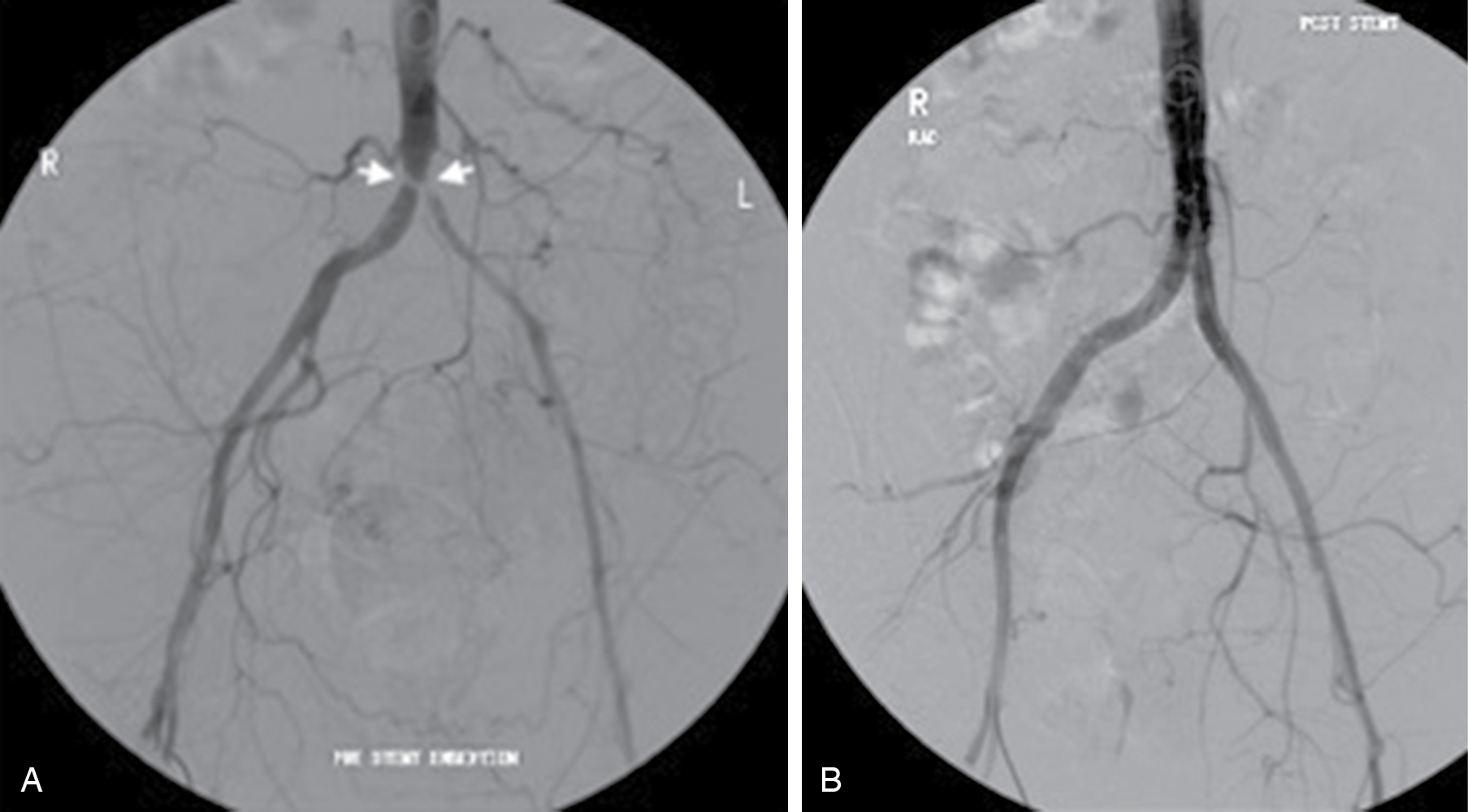
[Hình 5.7] Nong mạch qua da nội lòng mạch. Người đàn ông 55 tuổi này nhập viện với chứng đau cách hồi (claudication) ở bắp chân và đùi hai bên. (A) Hẹp nặng cục bộ ở động mạch chủ bụng đoạn xa (đầu mũi tên). (B) Kỹ thuật ‘bóng hôn’ (kissing balloon) được sử dụng để nong chỗ hẹp. Hai bóng được sử dụng để ngăn ngừa nong không đối xứng; sau đó, các stent ‘hôn’ được triển khai để duy trì độ thông suốt.
Liệu pháp tiêu sợi huyết động mạch tại chỗ (Local arterial thrombolytic therapy)
Một động mạch mới bị tắc nghẽn do huyết khối (thrombus) và gây thiếu máu cục bộ (ischaemia) có thể được tái thông (recanalised) bằng cách truyền các chất tiêu sợi huyết (thrombolytic agents) vào động mạch tại chỗ. Chất thường được sử dụng là chất hoạt hóa plasminogen mô tái tổ hợp (R-tPa). Mặc dù mục đích là nồng độ tại chỗ cao và hạn chế tràn hệ thống, nguy cơ xuất huyết lớn vẫn tồn tại. Các biến chứng nghiêm trọng bao gồm đột quỵ xuất huyết nội sọ (intracerebral haemorrhagic strokes). Lấy huyết khối nội mạch (endovascular thrombectomy) có thể là một thay thế cho phẫu thuật khi cục máu đông dẫn đến một tình trạng cấp tính như nhồi máu cơ tim, thuyên tắc phổi và đột quỵ thiếu máu cục bộ.
Thuyên tắc trị liệu (Therapeutic embolisation)
Các tổn thương có nhiều mạch máu (highly vascular lesions) hoặc mạch máu đang chảy máu tích cực có thể được giảm hoặc tắc nghẽn nguồn cung cấp động mạch bằng cách gây thuyên tắc (embolisation). Động mạch cung cấp chính được xác định bằng chụp động mạch chọn lọc (selective arteriography). Vật liệu gây thuyên tắc có thể là tạm thời (như bọt gelatin – gelatine foam) hoặc vĩnh viễn (như cuộn dây thép nhỏ, keo cyanoacrylate). Thuyên tắc đặc biệt hữu ích trong điều trị: xuất huyết tiêu hóa, một số giả phình mạch, u xơ tử cung (uterine fibroids), dị dạng động tĩnh mạch (arteriovenous malformations) và trước khi sửa chữa phình động mạch nội mạch (endovascular aneurysm repair – EVAR).
Đặt mảnh ghép xâm lấn tối thiểu (Minimal access graft placement) Sửa chữa phình động mạch nội mạch (EVAR) hiện được sử dụng rộng rãi để điều trị cả phình động mạch chủ bụng và ngực bằng stent graft (stent kim loại và vật liệu ghép polyester). Một thiết bị được đưa vào qua động mạch đùi và được triển khai dưới hướng dẫn X-Quang tăng sáng truyền hình. Một nhược điểm của EVAR là rò nội mạch (endoleakage), tức là tiếp tục chảy máu chậm vào túi phình do vòng đệm không đủ. Mặc dù tỷ lệ can thiệp lại cao hơn so với phẫu thuật mở, EVAR cho phép điều trị cho nhiều bệnh nhân không đủ sức khỏe để phẫu thuật mở.
Các kỹ thuật tĩnh mạch (Venous techniques)
Chụp tĩnh mạch (Venography) Siêu âm Doppler Duplex màu (Colour duplex Doppler ultrasound scanning) đã thay thế chụp tĩnh mạch cản quang để chẩn đoán huyết khối tĩnh mạch sâu (deep vein thrombosis – DVT), cũng như để chứng minh trào ngược (reflux) trong giãn tĩnh mạch (varicose veins).
Đặt bộ lọc tĩnh mạch chủ (Placement of vena caval filters)
Ở một số bệnh nhân bị thuyên tắc phổi tái phát (recurrent pulmonary embolism) mặc dù đã chống đông máu hoặc những người bị chống chỉ định chống đông máu, nguy cơ thuyên tắc phổi lớn có thể được giảm bằng cách đặt một bộ lọc (filter) trong tĩnh mạch chủ dưới (inferior vena cava). Hầu hết các bộ lọc có thể được lấy ra sau đó bằng các kỹ thuật qua da nếu cần thiết.
Điều trị giãn tĩnh mạch xâm lấn tối thiểu (Minimally invasive treatment of varicose veins)
Một số phương pháp triệt tiêu tĩnh mạch hiển lớn hoặc hiển bé đã xuất hiện trong những năm gần đây, bao gồm liệu pháp xơ hóa bằng bọt (foam sclerotherapy) và triệt tiêu bằng laser (laser) hoặc tần số vô tuyến (radiofrequency ablation – RFA). (Được mô tả trong Chương 43).
Can thiệp Đường Mật (Biliary intervention)
Chụp đường mật qua da xuyên gan (Percutaneous transhepatic cholangiography – PTC)
Kỹ thuật này bao gồm chọc dò đường mật qua da, thường dưới hướng dẫn siêu âm và X-Quang tăng sáng truyền hình. Có ba lựa chọn điển hình cho các can thiệp PTC:
- Dẫn lưu mật ngoài (External biliary drainage).
- Dẫn lưu mật trong-ngoài (Internal external biliary drain).
- Đặt stent đường mật (Biliary stent insertion): thường là stent kim loại trần (bare metal stent) qua một tổn thương ác tính.
Các can thiệp gan-mật qua da khác (Other percutaneous hepatobiliary interventions)
Bệnh nhân cần sinh thiết gan không mục tiêu có thể được sinh thiết gan qua tĩnh mạch cảnh (transjugular liver biopsy). Có thể điều trị các khối u gan bằng cách gây thuyên tắc—hóa trị thuyên tắc động mạch xuyên gan (transarterial chemoembolisation) và xạ trị thuyên tắc (radioembolisation). Các kỹ thuật nhiệt hủy (Thermoablative techniques) như RFA hoặc triệt tiêu bằng vi sóng cũng có thể được sử dụng. Thuyên tắc tĩnh mạch cửa (Portal vein embolisation) có thể được sử dụng trước khi cắt gan để tăng kích thước các phân đoạn gan còn lại, giảm tỷ lệ mắc bệnh sau mổ.
Chẩn đoán Hình ảnh Đường Tiết Niệu Trên (Upper urinary tract imaging)
Cơn đau quặn niệu quản cấp tính (Acute ureteric colic)
Chụp CT không tiêm thuốc, liều bức xạ thấp đã gần như thay thế hoàn toàn Chụp niệu đồ tĩnh mạch (IVU) để chẩn đoán cơn đau quặn niệu quản. Nó thường được gọi là CT KUB (thận, niệu quản và bàng quang) và nhạy hơn trong việc phát hiện sỏi so với IVU.
Tiểu máu (Haematuria)
Tiểu máu đại thể (visible) hoặc tiểu máu vi thể (microscopic – nonvisible) dai dẳng ban đầu được đánh giá bằng nội soi bàng quang (cystoscopy) và chẩn đoán hình ảnh. Siêu âm thường được dùng cho tiểu máu không nhìn thấy, và CT được dành riêng cho tiểu máu nhìn thấy (CT niệu đồ – CT urogram).
Đánh giá khối u thận (Evaluation of renal masses)
Khi một khối u thận được phát hiện, hình ảnh CT chuỗi không tiêm thuốc và có tiêm thuốc cản quang (CT thận ba thì – triple-phase renal CT) được sử dụng để mô tả đặc điểm khối u chính xác hơn. MRI thận cũng có thể được sử dụng để đánh giá thêm các tổn thương thận dạng nang phức tạp (complex cystic renal lesions).
Các kỹ thuật điều trị thận qua da (Percutaneous therapeutic renal techniques)
Bể thận (renal pelvis) có thể được chọc dò qua da bằng kim dưới hướng dẫn siêu âm. Đường vào này có thể được sử dụng để loại bỏ sỏi hoặc để giảm thận ứ nước (hydronephrosis) thông qua việc đặt ống thông mở thận ra da (nephrostomy) qua da. Đường vào này cũng có thể được sử dụng để đặt stent niệu quản đuôi lợn kép (double pigtail – JJ stent) ngược dòng (antegrade) trong các trường hợp đặt stent niệu quản ngược dòng qua nội soi bàng quang thất bại.
Các Kỹ thuật Chẩn đoán Hình Ảnh (Imaging techniques)
Siêu âm (Ultrasound)
Các nguyên lý chung của siêu âm y tế (General principles of medical ultrasound)
Siêu âm là không xâm lấn, không đau và an toàn mà không có rủi ro bức xạ. Một đầu dò siêu âm (ultrasound probe) chứa một bộ chuyển đổi áp điện (piezo-electric transducer) vừa truyền vừa nhận siêu âm; phản xạ hiển thị dưới dạng các đốm sáng trên màn hình tối trong thời gian thực (real time) (chế độ B – B-mode).
Siêu âm Duplex (Duplex scanning) kết hợp hình ảnh từ hình ảnh hai chiều (2D) và siêu âm Doppler. Duplex màu (colour duplex) bổ sung màu giả để hiển thị hướng và thể tích lưu lượng.
Đầu dò đặc biệt (Special transducers)
Các đầu dò đã được phát triển để sử dụng qua các lỗ tự nhiên (trực tràng, âm đạo) và cả các khoang cơ thể (nội soi thực quản, nội soi ổ bụng). Những đầu dò này cho phép sử dụng sóng âm tần số cao hơn, mang lại độ phân giải không gian (spatial resolution) lớn hơn. Theo dõi Doppler thực quản (Oesophageal Doppler monitoring) đo vận tốc dòng máu trong động mạch chủ ngực xuống và có thể cung cấp ước tính liên tục về cung lượng tim (cardiac output) trong các cuộc mổ.
Các ứng dụng của siêu âm trong ngoại khoa tổng quát (Applications of ultrasound in general surgery)
Siêu âm thường được sử dụng làm xét nghiệm hình ảnh đầu tiên, đặc biệt là ở trẻ em và phụ nữ trong độ tuổi sinh đẻ (tránh bức xạ ion hóa).
- FAST (Focused Assessment with Sonography for Trauma) là công cụ tuyệt vời trong việc đánh giá chấn thương bụng để phát hiện dịch (máu) tự do.
- Phân biệt đáng tin cậy các tổn thương đặc (solid) với tổn thương nang (cystic).
- Phát hiện tổn thương các cơ quan đặc sau chấn thương (ví dụ: vỡ lách, gan).
- Đánh giá hệ thống đường mật để tìm sỏi mật, thành túi mật dày, ống dẫn giãn, khối u.
- Hướng dẫn các thủ thuật qua da: hút dịch cổ trướng, sinh thiết tổn thương gan, đặt ống dẫn lưu.
HỘP 5.3 Hạn chế của siêu âm chẩn đoán
|
Siêu âm Doppler thay đổi tần số (Doppler-shifted ultrasound)
Thiết bị cầm tay đơn giản (Hình 5.8) phát hiện dòng máu bằng nguyên lý Doppler, tạo ra tín hiệu âm thanh có độ cao liên quan đến vận tốc máu.
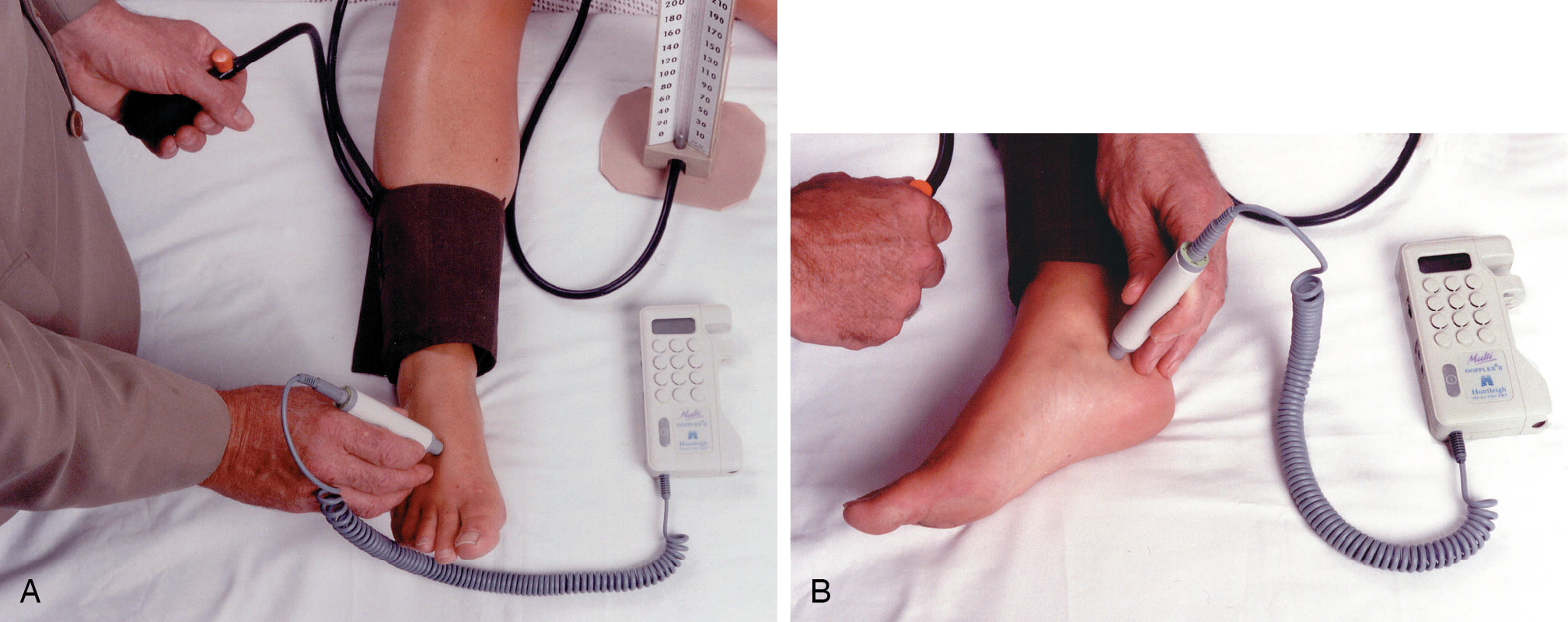
[Hình 5.8] Đo huyết áp tâm thu mắt cá chân bằng máy đo Doppler cầm tay. (A) Đo tại mạch mu chân. (B) Đo tại mạch chày sau.
Các ứng dụng chính của siêu âm Doppler cầm tay là:
- Đo huyết áp tâm thu khi nó thấp, bao gồm huyết áp tâm thu mắt cá chân (ankle systolic pressures) trong thiếu máu cục bộ chi dưới.
- Phát hiện nhịp tim thai nhi.
- Phát hiện đơn giản trào ngược máu tĩnh mạch trong giãn tĩnh mạch.
Siêu âm Doppler Duplex (Duplex Doppler ultrasound scanning)
Quét Doppler Duplex bổ sung phân tích phổ tần số (frequency spectral analysis) của dòng máu vào hình ảnh B-mode 2D của mạch máu, và Doppler dòng chảy màu (Colour flow Doppler) hiển thị hướng và thể tích lưu lượng.
Các ứng dụng của Doppler Duplex:
- Huyết khối tĩnh mạch sâu (DVT): Đây là phương pháp được lựa chọn để phát hiện DVT.
- Suy tĩnh mạch sâu chi dưới mãn tính, Giãn tĩnh mạch: Đánh giá độ thông suốt và khả năng hoạt động của van.
- Bệnh động mạch cảnh (Carotid artery disease): Trở thành xét nghiệm tiêu chuẩn để thăm dò bệnh mạch máu ngoài sọ, cho phép tính toán phần trăm hẹp.
- Cầu nối động mạch đùi-khoeo (Femoro-popliteal bypass grafts): Được sử dụng để theo dõi mảnh ghép sau phẫu thuật.
- Bệnh tắc nghẽn động mạch chủ-chậu và đùi-khoeo.
- Bệnh tim (Siêu âm tim – Echocardiography): Đánh giá cấu trúc và chức năng tim, rối loạn chức năng thất, bất thường van, và các khiếm khuyết tim bẩm sinh.
Chẩn đoán Hình ảnh: Chụp cắt lớp vi tính (CT scanning)
Chụp cắt lớp vi tính (Computed tomography – CT) đã trở thành một kỹ thuật chẩn đoán không thể thiếu trong ngoại khoa tổng quát (general surgery). Nguyên lý của CT là sử dụng một bó tia X mỏng được quay quanh bệnh nhân; các máy dò (detectors) đo lượng tia X đi qua. Dữ liệu từ hàng ngàn phép đo được sử dụng để tạo ra một bản đồ chi tiết về mật độ mô của cơ thể trong một lát cắt (slice).
CT đa lát cắt (Multislice CT)
Những tiến bộ gần đây trong công nghệ CT, đặc biệt là sự ra đời của CT đa lát cắt (multislice CT) (còn gọi là CT đa đầu dò), đã rút ngắn đáng kể thời gian quét và cải thiện độ phân giải. Công nghệ này sử dụng nhiều hàng đầu dò, cho phép thu thập dữ liệu nhanh hơn, do đó, có thể quét các khu vực giải phẫu lớn hơn mà không cần nín thở (breath-holding) và giảm thiểu các cử động (motion artefacts).
Ưu điểm của CT:
|
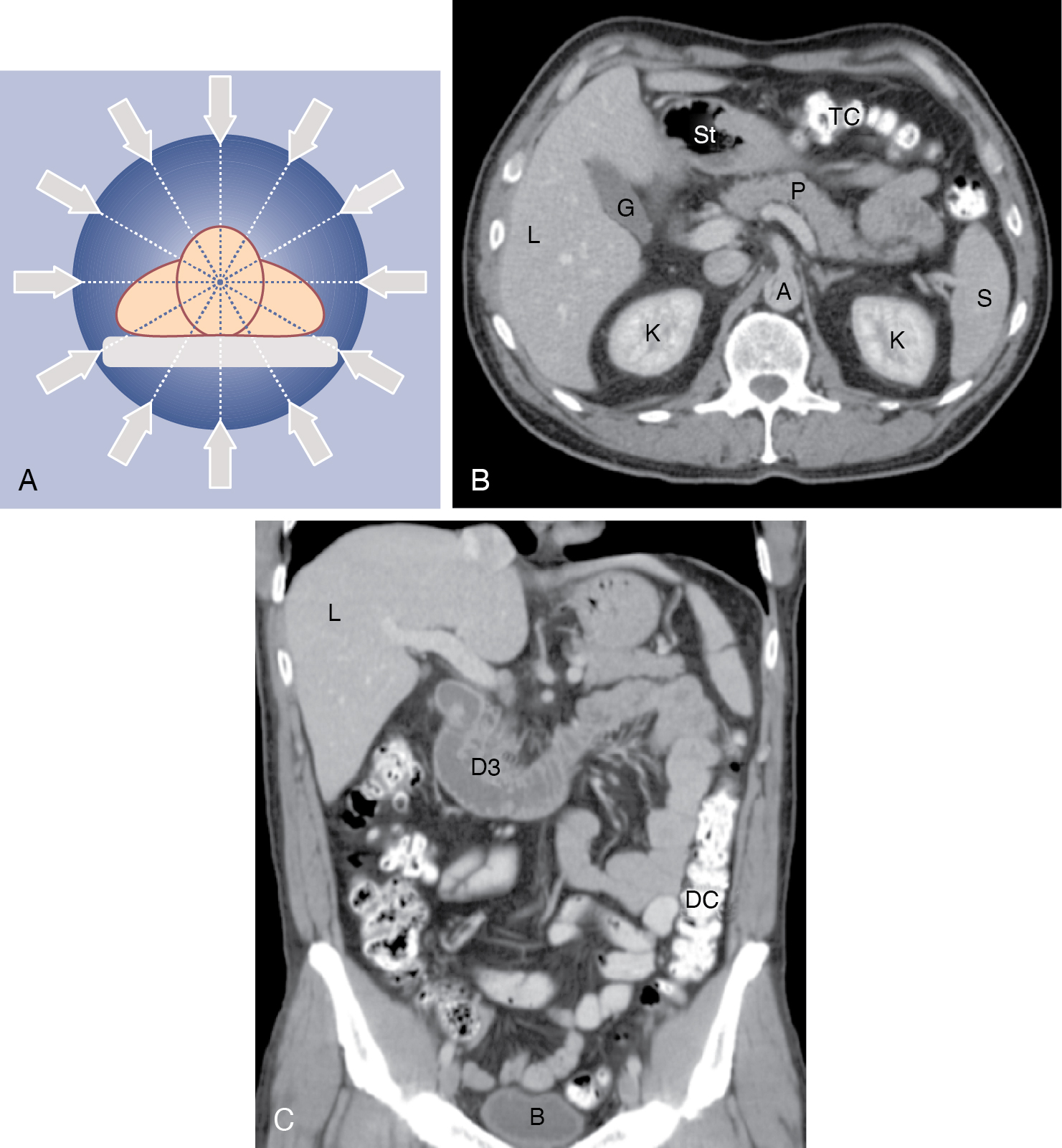
[Hình 5.9]. Sơ đồ Nguyên lý CT và Hình ảnh CT. (A) Nguyên lý quét CT. (B) Hình ảnh CT cắt ngang bụng bình thường. (C) Tái tạo hình ảnh CT trong mặt phẳng trán.
CT: Hướng dẫn đặt ống thông dẫn lưu áp xe. Hình ảnh CT bụng với kim sinh thiết được đặt trong một áp xe màng phổi (subphrenic abscess).
Các ứng dụng ngoại khoa của CT:
- Bụng cấp tính (Acute abdomen): CT ngày càng được sử dụng sớm hơn trong quá trình chẩn đoán (ví dụ: đối với viêm ruột thừa, viêm túi thừa, tắc ruột).
- Đánh giá chấn thương (Trauma evaluation): CT toàn thân (Pan-CT) đã trở thành tiêu chuẩn để đánh giá đa chấn thương (polytrauma), đặc biệt là chấn thương bụng kín.
- Ung thư học (Oncology): CT là phương thức chính để xác định giai đoạn (staging) và theo dõi (follow-up) bệnh nhân ung thư đường tiêu hóa và tiết niệu-sinh dục.
- Phẫu thuật mạch máu (Vascular surgery): Chụp mạch CT (CT angiography – CTA) được sử dụng để đánh giá phình động mạch (aneurysms) và bệnh tắc nghẽn (occlusive disease).
Nhược điểm của CT:
|
Chẩn đoán Hình ảnh: Cộng hưởng từ (Magnetic resonance imaging – MRI)
MRI sử dụng từ trường mạnh (powerful magnetic fields) và sóng vô tuyến (radiofrequency waves) để tạo ra hình ảnh chi tiết của các cơ quan và mô. Nguyên lý dựa trên sự định hướng lại các proton (hạt nhân hydro) trong cơ thể khi chịu tác dụng của từ trường và sóng vô tuyến.
Ưu điểm của MRI:
|
Các ứng dụng ngoại khoa của MRI:
- Trực tràng và Hậu môn (Rectum and Anus): Đánh giá giai đoạn ung thư trực tràng, áp xe (abscesses) và lỗ rò quanh hậu môn (perianal fistulae).
- Gan-Mật-Tụy (Hepatobiliary-Pancreatic): MRI và Chụp Cộng Hưởng Từ Đường Mật Tụy (MRCP) để đánh giá các khối u, nang (cysts) và sỏi ống mật chủ.
- Các tổn thương mô mềm khác: Đánh giá các khối u mô mềm (soft-tissue tumours) và bệnh lý tủy xương (bone marrow pathology).
Nhược điểm của MRI:
|
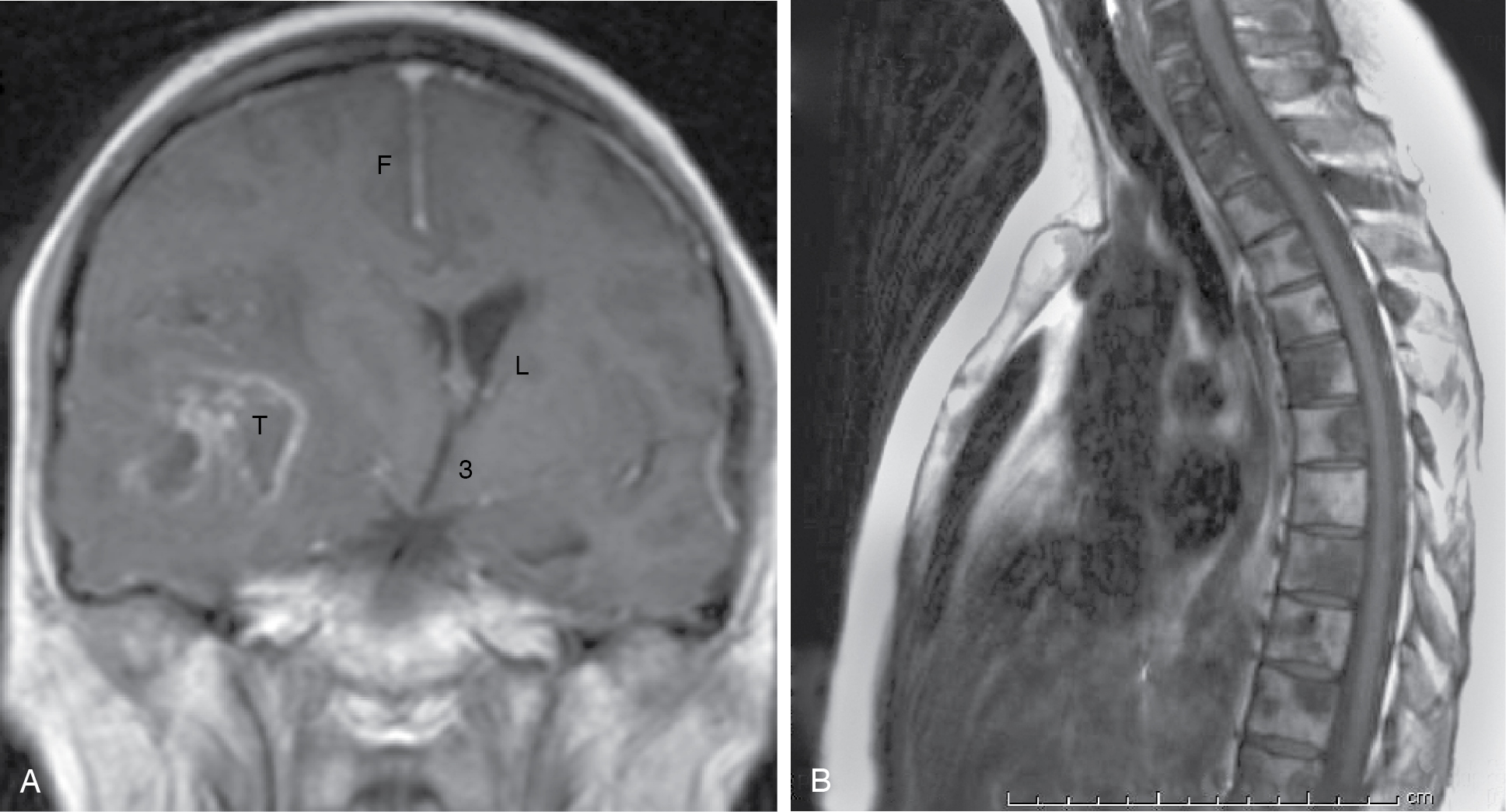
[Hình 5.10]. Hình ảnh Cộng hưởng từ (MRI). (A) MRI não T1 có tăng cường Gadolinium cho thấy khối u và sự dịch chuyển đường giữa. (B) MRI cột sống ngực T1 cho thấy di căn xương ở bệnh nhân ung thư tiền liệt tuyến.
X-Quang Can Thiệp (Interventional radiology)
X-Quang can thiệp (IR) là một chuyên ngành phụ (sub-speciality) của X-Quang sử dụng hướng dẫn hình ảnh để thực hiện các thủ thuật xâm lấn tối thiểu. IR là một chuyên ngành đang phát triển, với các thủ thuật ngày càng thay thế các cuộc mổ truyền thống.
Lấy Mẫu Mô (Tissue sampling)
Sinh thiết (biopsy) thường được thực hiện để chẩn đoán các khối u. Lấy mẫu mô có thể được hướng dẫn bằng siêu âm, CT hoặc X-Quang tăng sáng truyền hình (fluoroscopy).
Sinh thiết bằng kim nhỏ (Fine-needle aspiration – FNA)
FNA sử dụng kim gauge nhỏ (22–25G) để lấy mẫu các tế bào riêng lẻ, thường được hướng dẫn bằng siêu âm hoặc sờ nắn. Nó chủ yếu hữu ích để lấy mẫu các hạch bạch huyết (lymph nodes), các khối ở tuyến giáp (thyroid) hoặc vú (breast), và để xác nhận các tổn thương di căn.
Sinh thiết lõi (Core biopsy)
Sinh thiết lõi sử dụng kim gauge lớn hơn (14–20G) với một thiết bị cắt lò xo để lấy một lõi mô lớn hơn, cung cấp thông tin về cấu trúc mô học (histology) và cho phép đánh giá các dấu hiệu miễn dịch hóa học (immunohistochemistry) hữu ích cho việc xác định các phương pháp điều trị đích (targeted therapies).
Sinh thiết phẫu thuật (Surgical biopsy)
Sinh thiết phẫu thuật, lấy toàn bộ hoặc một phần tổn thương, được dành riêng cho các trường hợp:
- Không thể tiếp cận tổn thương bằng sinh thiết kim.
- Lấy mẫu bằng kim không đủ để chẩn đoán (ví dụ: u lympho – lymphoma).
- Cần can thiệp phẫu thuật để giảm đau hoặc giải áp.
Vị trí chọc dò (Approach)
Tiếp cận phổ biến nhất là xuyên da (percutaneous) (qua da), nhưng các tiếp cận khác bao gồm xuyên phế quản (transbronchial), xuyên hậu môn/trực tràng (transanal/rectal) và xuyên nội soi (transendoscopic). Các nguy cơ liên quan đến sinh thiết tùy thuộc vào cơ quan được chọc dò (ví dụ: tràn khí màng phổi (pneumothorax) sau sinh thiết phổi, chảy máu sau sinh thiết gan) và phải được thảo luận trước với bệnh nhân.
Dẫn Lưu Áp Xe và Tụ Dịch (Drainage of abscesses and fluid collections)
Các áp xe (abscesses) ở bụng, sau phúc mạc (retroperitoneal) và ngực (thoracic) thường có thể được dẫn lưu qua da dưới hướng dẫn CT hoặc siêu âm. Việc sử dụng ống dẫn lưu qua da (percutaneous drain) được ưu tiên hơn so với phẫu thuật mở ở những bệnh nhân không đáp ứng với kháng sinh, vì nó ít xâm lấn hơn và ít gây bệnh hơn.
Kỹ thuật Seldinger (Seldinger technique)
Các ống thông dẫn lưu thường được đặt bằng kỹ thuật Seldinger:
- Chọc kim vào khoang dịch dưới hướng dẫn hình ảnh.
- Đưa dây dẫn (guidewire) qua kim vào trong khoang.
- Rút kim ra, để lại dây dẫn.
- Đưa ống thông dẫn lưu qua dây dẫn vào khoang.
- Rút dây dẫn và kết nối ống thông với một túi dẫn lưu.
Một mẫu dịch (fluid sample) phải được gửi đi cấy (culture) và phân tích. Thất bại trong việc dẫn lưu áp xe có thể do dịch quá đặc hoặc áp xe có nhiều khoang (multiloculated).
Xạ Hình Hạt Nhân (Radionuclide scanning)
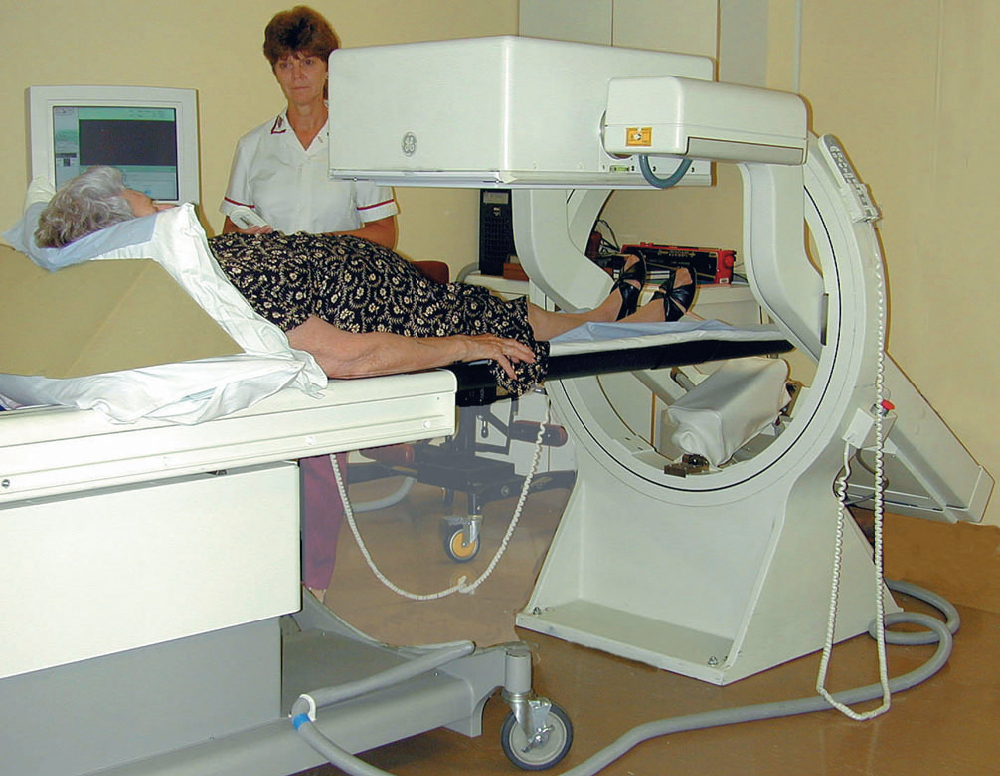
[Hình 5.11]. Xạ hình Isotope sử dụng camera gamma. Bệnh nhân đã được tiêm tĩnh mạch chất đánh dấu phóng xạ. Mô hình hấp thụ được chụp ảnh bởi mảng đầu dò và truyền điện tử để hiển thị trên màn hình.
Các Nguyên lý của Xạ Hình Hạt Nhân (Principles of radionuclide scanning)
Xạ hình hạt nhân (Radionuclide scanning) là một kỹ thuật hình ảnh chức năng (functional imaging) sử dụng các đồng vị phóng xạ (radioactive isotopes) để tạo ra hình ảnh. Đồng vị phóng xạ (radionuclide) được gắn vào một dược chất phóng xạ (radiopharmaceutical), là một phân tử mà cơ thể chuyển hóa hoặc xử lý. Sự phân bố của dược chất phóng xạ trong cơ thể được phát hiện bởi một camera gamma (gamma camera), tạo ra một hình ảnh cho thấy hoạt động sinh lý (physiological activity) hoặc chuyển hóa (metabolic activity) của một cơ quan.
Kỹ thuật SPECT (Single-photon emission CT – SPECT)
Kỹ thuật này sử dụng nhiều đầu dò camera gamma quay quanh bệnh nhân để tạo ra hình ảnh 3D, cung cấp độ phân giải không gian tốt hơn so với xạ hình 2D phẳng truyền thống.
Các Ứng dụng của Xạ Hình Hạt Nhân (Applications of radionuclide scanning)
- Xạ hình xương (Bone scintigraphy): Sử dụng technetium-99m methylene diphosphonate (Tc-99m MDP). Nó hấp thụ vào các vùng có hoạt động nguyên bào xương (osteoblastic activity) cao, cho thấy các khu vực tái tạo xương (bone turnover). Ứng dụng chính là phát hiện di căn xương (bone metastases) và các quá trình viêm (ví dụ: viêm tủy xương – osteomyelitis). (Hình 5.12 và 5.13)
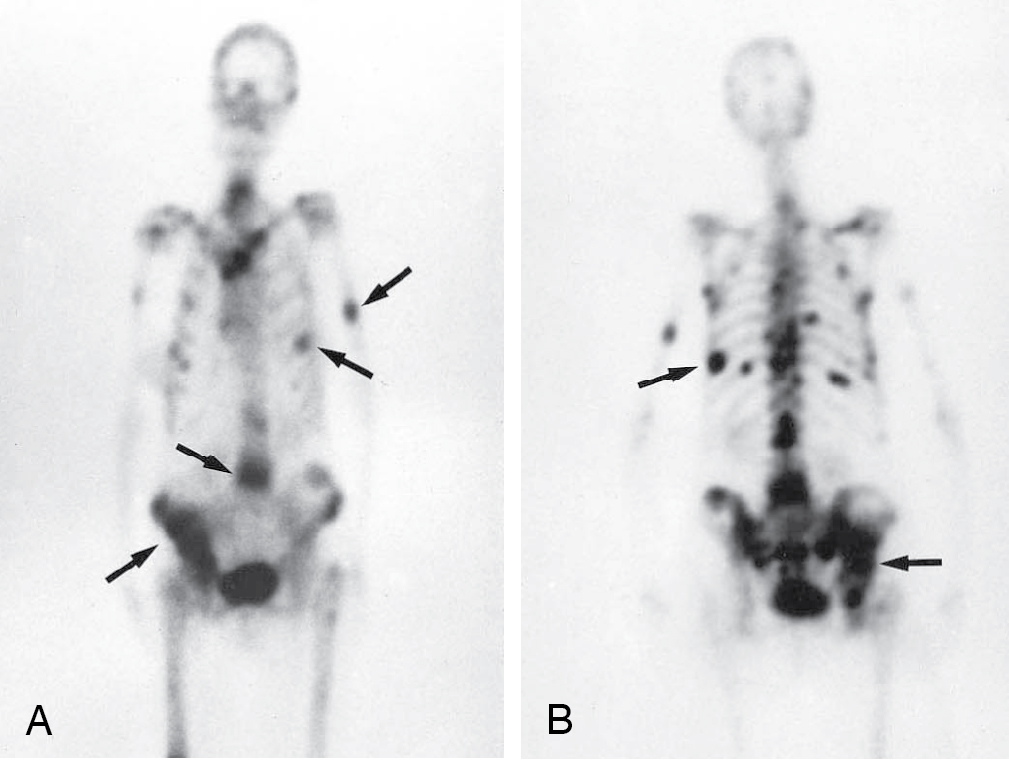
[Hình 5.12] Xạ hình xương bằng đồng vị phóng xạ. (A) Hình ảnh trước của xạ hình xương ở bệnh nhân di căn xương đa ổ (mũi tên) từ ung thư vú. (B) Hình ảnh sau của xạ hình xương ở cùng bệnh nhân.
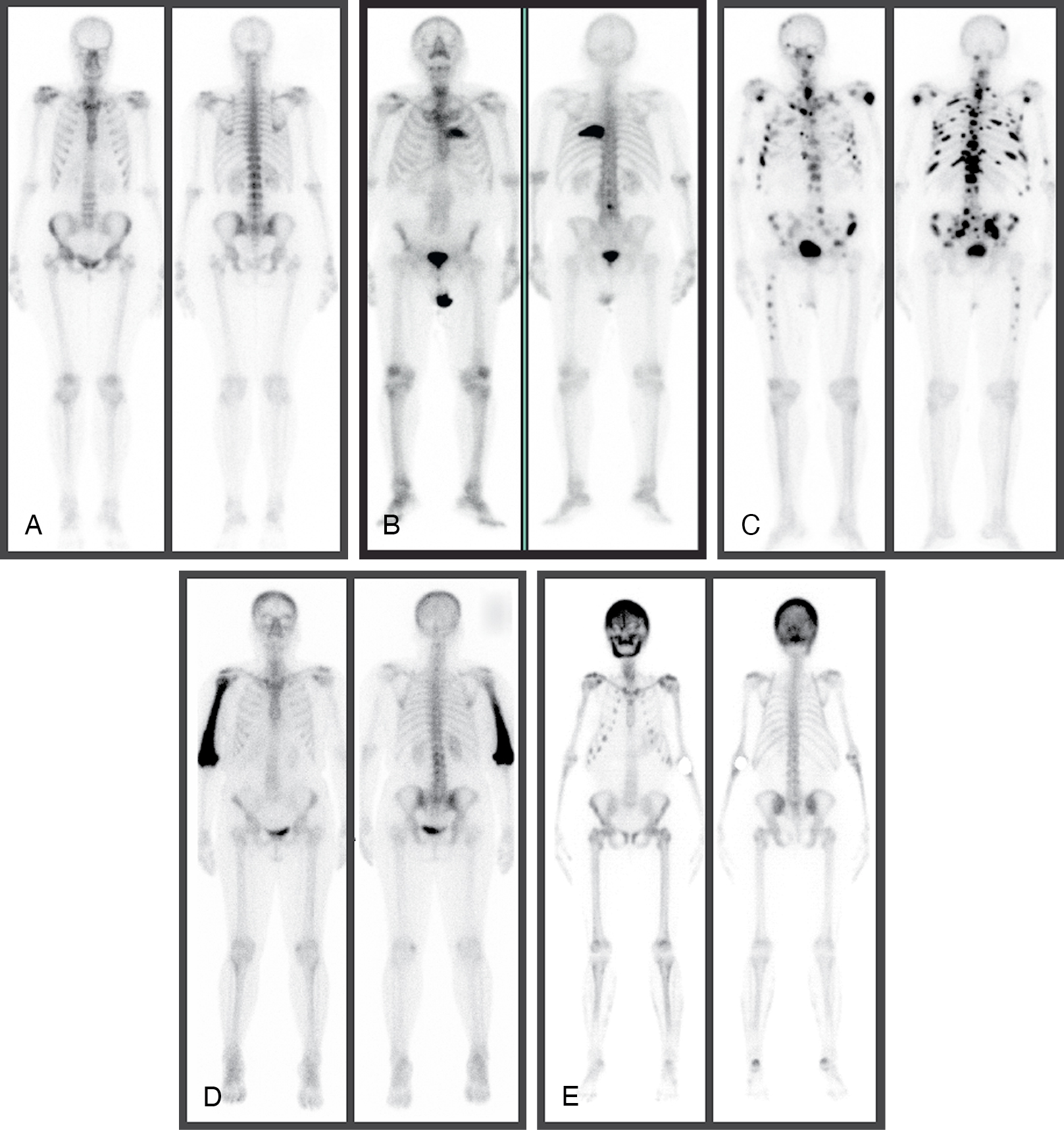
[Hình 5.13] Xạ hình xương ở người lớn. (A) Xạ hình bình thường với hấp thụ đối xứng trong bộ xương. (B) Di căn xương đơn ổ trên xương sườn trái. (C) Di căn xương lan rộng với nhiều vị trí hấp thụ trên hộp sọ, cột sống, xương chậu và xương đùi phải. (D) Bệnh Paget đơn cốt trên xương cánh tay phải. (E) Cường tuyến cận giáp với hoạt động nguyên bào xương mạnh trên hộp sọ và hấp thụ khu trú ở xương sườn.
- Xạ hình tuyến giáp (Thyroid scanning): Sử dụng I-ốt-123 (I-123) hoặc Tc-99m pertechnetate để đánh giá chức năng và hình thái tuyến giáp.
- Xạ hình thận (Renal scanning): Sử dụng Tc-99m MAG3 hoặc Tc-99m DTPA để đánh giá chức năng lọc (filtration) và bài tiết (excretion) của thận. Hữu ích trong việc đánh giá sự tắc nghẽn đường tiết niệu (urinary tract obstruction) và chức năng thận tương đối. (Hình 5.14)
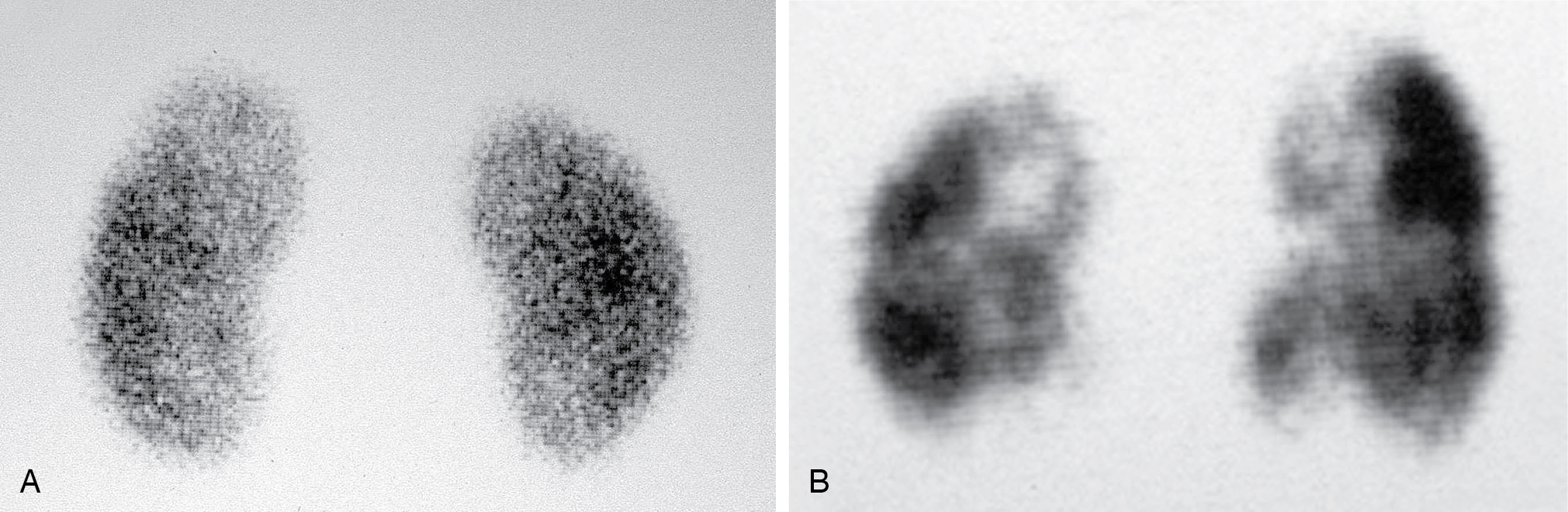
[Hình 5.14] Xạ hình thận Dimercapto-Succinic Acid (DMSA) bằng đồng vị phóng xạ. (A) Bình thường và (B) bất thường cho thấy sẹo loang lổ do các đợt viêm đài bể thận (pyelonephritis).
- Xạ hình tuyến nước bọt (Salivary gland imaging): Đánh giá chức năng và bài tiết của tuyến nước bọt. (Hình 5.15)
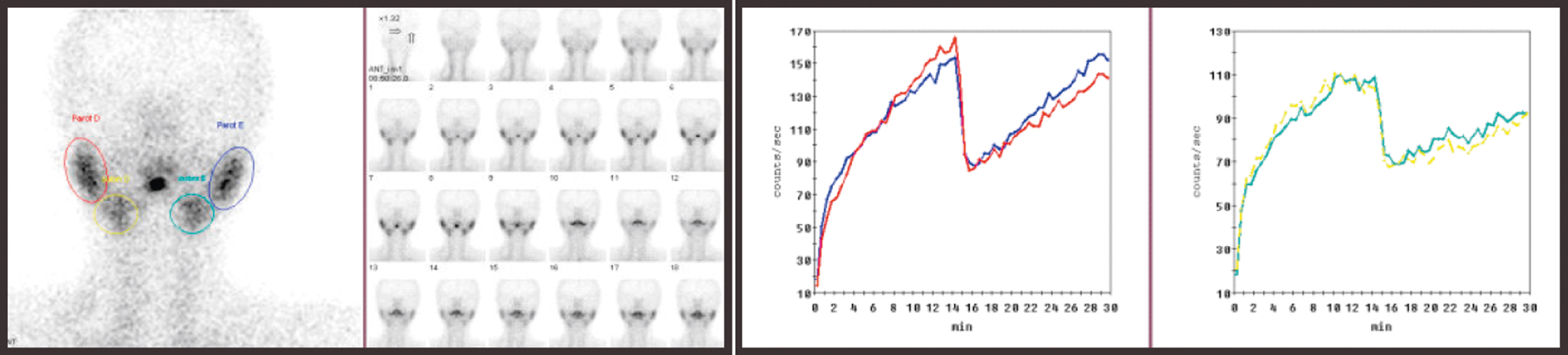
[Hình 5.15] Xạ hình tuyến nước bọt bình thường. Hình ảnh động được thực hiện trong 30 phút và kích thích bằng axit citric được đưa ra sau 15 phút.
Xạ hình thực quản và dạ dày (Oesophageal and gastric imaging):
- Thăm dò trào ngược dạ dày-thực quản (Investigation of a gastro-oesophageal reflux): Xạ hình là phương pháp nhạy nhất, không xâm lấn để phát hiện trào ngược dạ dày-thực quản, đặc biệt ở trẻ em. (Hình 5.16)
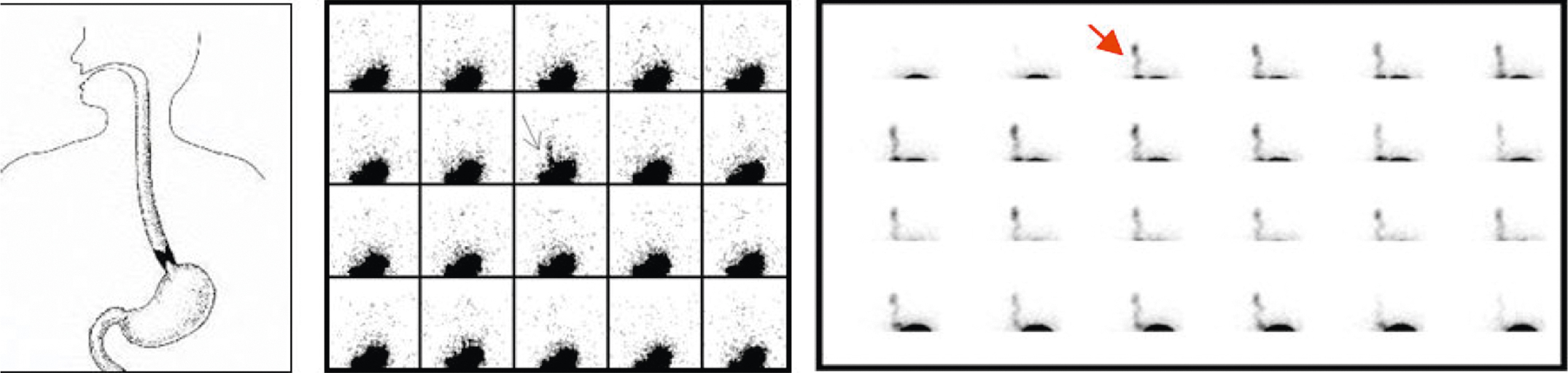
[Hình 5.16] Xạ hình trào ngược dạ dày-thực quản. Một đợt trào ngược ngắn, đơn lẻ (mũi tên đen) và một đợt trào ngược kéo dài (mũi tên đỏ) trong quá trình quét động.
-
- Thời gian làm rỗng dạ dày (Gastric emptying): Xác định thời gian bán hủy làm rỗng và/hoặc phần trăm làm rỗng để chẩn đoán các tình trạng như liệt dạ dày do đái tháo đường (diabetic gastroparesis).
- Xạ hình túi mật (Hepatobiliary iminodiacetic acid – HIDA scanning): Sử dụng Tc-99m gắn với một axit iminodiacetic (IDA) để đánh giá sự bài tiết mật từ gan vào túi mật và ruột. Nó hữu ích trong việc chẩn đoán viêm túi mật cấp (acute cholecystitis) (túi mật không thấy) và rò rỉ mật (bile leaks).
Xạ Hình Hạch Gác (Sentinel node imaging) cho các khối u ác tính khác nhau
Xạ hình hạch gác (Sentinel node imaging) được sử dụng để xác định hạch bạch huyết (lymph node) đầu tiên nhận được dẫn lưu bạch huyết từ một khối u. Nếu hạch gác (sentinel node) không chứa tế bào ung thư, thì rất khó có khả năng các hạch khác cũng chứa.
Ứng dụng:
- U hắc tố (Melanoma)
- Ung thư vú (Breast cancer)
- Một số trường hợp ung thư đại trực tràng (colorectal cancer)
Kỹ thuật: Một dược chất phóng xạ (ví dụ: Tc-99m sulphur colloid) được tiêm vào khu vực xung quanh khối u. Dược chất này đi đến hạch gác, nơi nó được phát hiện bằng camera gamma. Hạch được đánh dấu bằng chất nhuộm màu xanh lam (blue dye) hoặc phát hiện bằng máy dò gamma trong mổ (intraoperative gamma detector) và được sinh thiết. (Hình 5.17)
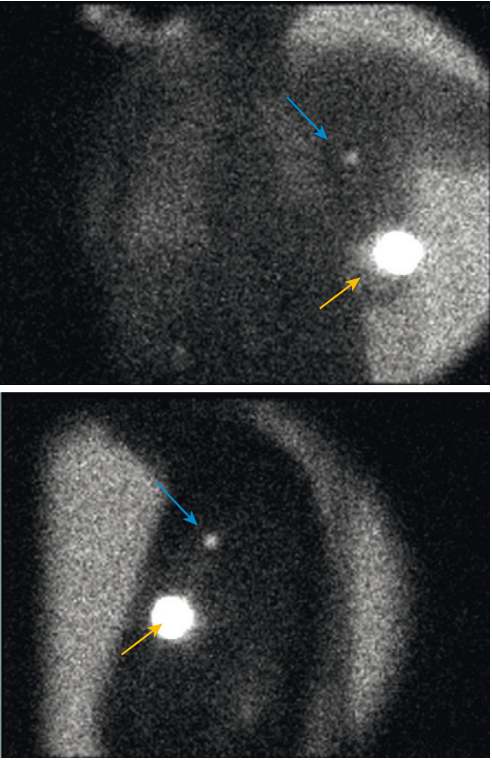
[Hình 5.17] Xạ hình hạch gác ung thư vú. Hình ảnh trước và bên trái của ngực bệnh nhân. Sau khi tiêm dược chất phóng xạ vào vú trái (mũi tên vàng), hạch gác được xác định trong chuỗi bạch huyết nách trái (mũi tên xanh).
Chẩn đoán Hình ảnh: Chụp cắt lớp phát xạ Positron (Positron emission tomography – PET) cho khối u
PET/CT và PET/MR
PET sử dụng một dược chất phóng xạ phát ra positron (ví dụ: fluorodeoxyglucose – FDG) để tạo ra hình ảnh chuyển hóa. Vì các tế bào ung thư (cancer cells) thường có tốc độ chuyển hóa glucose (glucose metabolism) cao hơn các tế bào bình thường, chúng tích lũy FDG nhiều hơn và hiển thị dưới dạng các vùng ‘nóng’ (hot spots) trên hình ảnh PET.
PET hiện được sử dụng kết hợp với CT hoặc MRI (PET/CT hoặc PET/MR) để kết hợp hình ảnh chuyển hóa chức năng với hình ảnh giải phẫu chi tiết. (Hình 5.18 và 5.19)
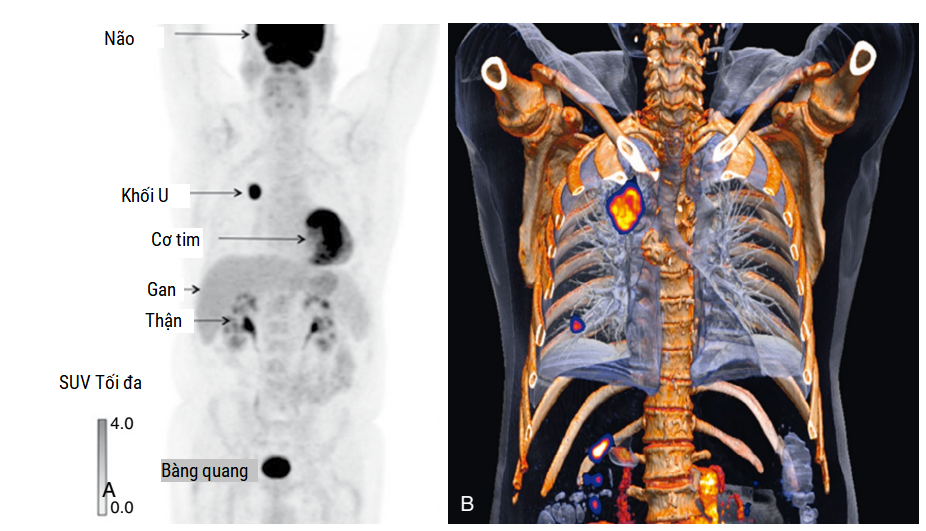
[Hình 5.18] Xạ hình Positron phát xạ Fluorine-18 (18F-FDG PET-CT). (A) Hình ảnh chiếu cường độ tối đa của bệnh nhân nghi ngờ ung thư phổi. Có sự hấp thụ cao bình thường của dược chất phóng xạ FDG trong não, cơ tim, gan, thận và bàng quang. Ngoài ra còn có sự hấp thụ khu trú mạnh ở phổi phải. (B) Hình ảnh PET chuyển hóa được hợp nhất với hình ảnh CT giải phẫu tạo ra hình ảnh lai.
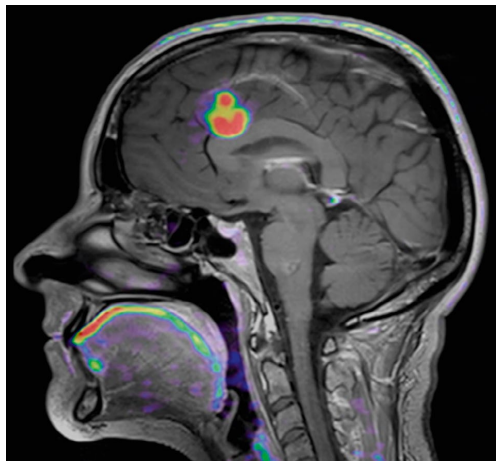
[Hình 5.19] Xạ hình Positron phát xạ Axit amin 18F-Tyrosine (PET-MRI). Hình ảnh PET-MRI lai cho thấy sự hấp thụ dược chất phóng xạ cao ở thùy trán, cho thấy sự hiện diện của khối u não.
Các ứng dụng ngoại khoa của PET:
- Xác định giai đoạn ung thư (Cancer staging): Phát hiện các di căn (metastases) mà các phương thức hình ảnh khác có thể bỏ sót.
- Đánh giá phản ứng điều trị (Therapy response): Đánh giá sớm phản ứng của khối u với hóa trị (chemotherapy) hoặc xạ trị (radiotherapy).
- Tìm kiếm ung thư tái phát (Recurrence): Phát hiện ung thư tái phát khó định vị.
- U thực quản, đại trực tràng, phổi và đầu cổ.
Nội Soi Ống Mềm (Flexible endoscopy)
Các Nguyên lý của Nội Soi Ống Mềm (Principles of flexible endoscopy)
Nội soi (Endoscopy) là kỹ thuật quan sát bên trong các cơ quan rỗng (hollow organs) hoặc khoang cơ thể. Nó cho phép chẩn đoán trực tiếp các tổn thương (lesions) và cho phép các thủ thuật điều trị được thực hiện dưới tầm nhìn trực tiếp.
Nội soi sợi quang (Fibreoptic illumination)
Ánh sáng được đưa vào qua các sợi quang (fibreoptic bundles) từ một nguồn sáng bên ngoài, cung cấp ánh sáng lạnh và sáng. Điều này cho phép quan sát rõ ràng bên trong các khoang cơ thể rỗng.
Truyền hình ảnh (Image transmission)
Các ống nội soi hiện đại sử dụng một con chip video nhỏ (charge-coupled device – CCD) ở đầu ống để thu hình ảnh kỹ thuật số (digital image). Hình ảnh được xử lý bởi máy tính (processor) và hiển thị trên màn hình.
Cấu trúc của ống nội soi mềm (Structure of flexible endoscopes)
Một ống nội soi mềm có bốn kênh chính: (Hình 5.20)
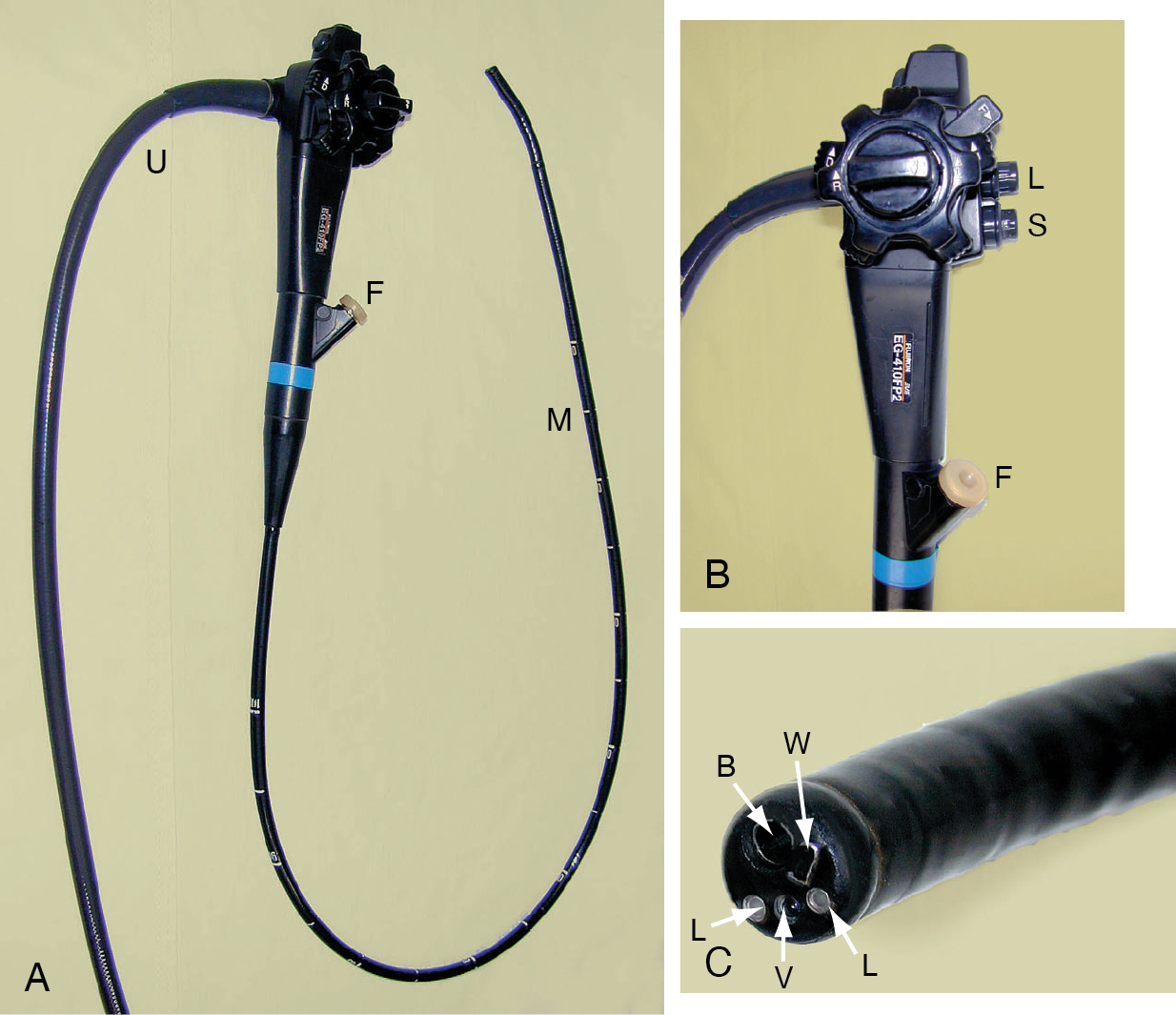
[Hình 5.20] Ống nội soi dạ dày sợi quang mềm. (A) Ống nội soi dạ dày nhìn thẳng gồm trục chính mềm (M) dài 1 m; đầu xa 10 cm có thể uốn cong theo bốn hướng. Có dây rốn (U) cắm vào hộp điều khiển, mang khí, nước rửa ống kính và hút. Có ống rửa (F). (B) Các điều khiển lái gồm hai bánh xe đồng tâm. (C) Đầu ống nội soi chi tiết, với hai ống dẫn ánh sáng (L), ống kính chụp ảnh (V), lỗ thoát khí/nước (W) và kênh dụng cụ/hút (B).
- Truyền hình ảnh: Cung cấp hình ảnh trực quan.
- Hút: Để hút dịch (fluid) hoặc khí (gas).
- Thổi khí/Rửa: Để làm căng và làm sạch tầm nhìn.
- Kênh làm việc: Để đưa các dụng cụ điều trị và chẩn đoán như kẹp sinh thiết, thòng lọng (snares) hoặc đầu dò.
Các ứng dụng của nội soi mềm:
- Nội soi tiêu hóa trên (Upper GI endoscopy/gastroscopy): Thực quản (oesophagus), dạ dày (stomach) và tá tràng (duodenum).
- Nội soi đại tràng (Colonoscopy): Trực tràng, đại tràng và đôi khi là đoạn cuối hồi tràng (terminal ileum).
- Nội soi phế quản (Bronchoscopy): Khí quản và cây phế quản.
- Nội soi mật-tụy ngược dòng qua nội soi (ERCP – Endoscopic retrograde cholangio-pancreatography) (xem phần sau).
- Nội soi viên nang (Capsule endoscopy): Một viên nang có gắn camera (video capsule) được nuốt vào, chụp ảnh khi nó đi qua ruột non. Rất hữu ích trong việc chẩn đoán chảy máu đường tiêu hóa không rõ nguyên nhân (obscure gastrointestinal bleeding) và bệnh Crohn.
Các kỹ thuật nội soi điều trị:
- Polypectomy: Cắt bỏ polyp.
- Cầm máu (Haemostasis): Dùng kẹp, tiêm epinephrine (Adrenalin) hoặc liệu pháp nhiệt (thermal therapy) để điều trị chảy máu loét.
- Thắt tĩnh mạch thực quản (Oesophageal variceal banding): Điều trị giãn tĩnh mạch thực quản.
- Đặt stent: Thực quản, dạ dày, tá tràng hoặc đại tràng.
- Nong (Dilatation): Đối với hẹp thực quản hoặc đại tràng.
- Nội soi tá tràng chẩn đoán và điều trị (Diagnostic and therapeutic duodenoscopy) (ERCP) (xem phần sau).
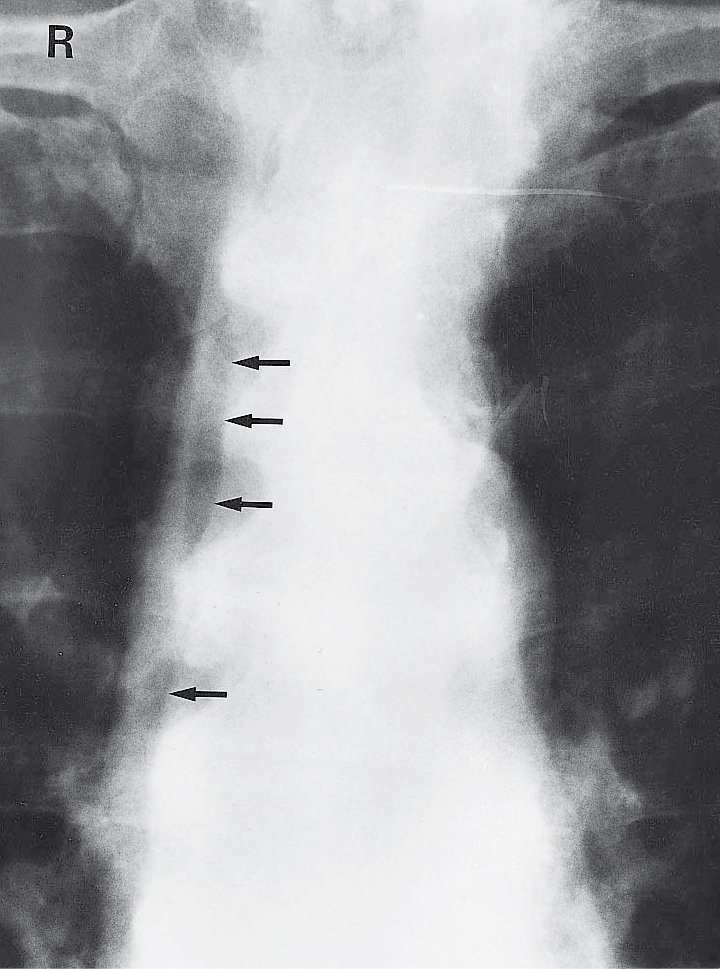
[Hình 5.21] Tràn khí trung thất sau thủng khối u thực quản trong nội soi. Bệnh nhân nam 56 tuổi bị đau ngực sau khi kiểm tra khó nuốt.
Nội Soi Tá Tràng Chẩn đoán và Điều trị (Diagnostic and Therapeutic Duodenoscopy)
ERCP (Endoscopic retrograde cholangio-pancreatography)
ERCP là một thủ thuật nội soi kết hợp với X-Quang tăng sáng truyền hình (fluoroscopy) để hình dung và can thiệp vào cây đường mật và ống tụy.
Quy trình:
- Một ống nội soi tá tràng nhìn ngang (side-viewing duodenoscope) được đưa vào tá tràng để định vị nhú tá tràng lớn (major duodenal papilla) (Bóng Vater).
- Một ống thông nhỏ (catheter) được đưa vào nhú và chất cản quang được tiêm ngược dòng vào ống mật chủ (common bile duct) và/hoặc ống tụy (pancreatic duct) dưới hướng dẫn X-Quang tăng sáng truyền hình.
ERCP Điều trị (Therapeutic ERCP):
- Cắt cơ vòng (Sphincterotomy): Rạch cơ vòng Oddi (sphincter of Oddi) để tiếp cận ống dẫn.
- Lấy sỏi (Stone removal): Sử dụng rọ (baskets) hoặc bóng (balloons) để lấy sỏi ống mật chủ.
- Nong và đặt stent (Stent placement): Đặt stent nhựa hoặc kim loại để giải quyết tắc nghẽn đường mật do hẹp (strictures) (lành tính hoặc ác tính). (Hình 5.22)
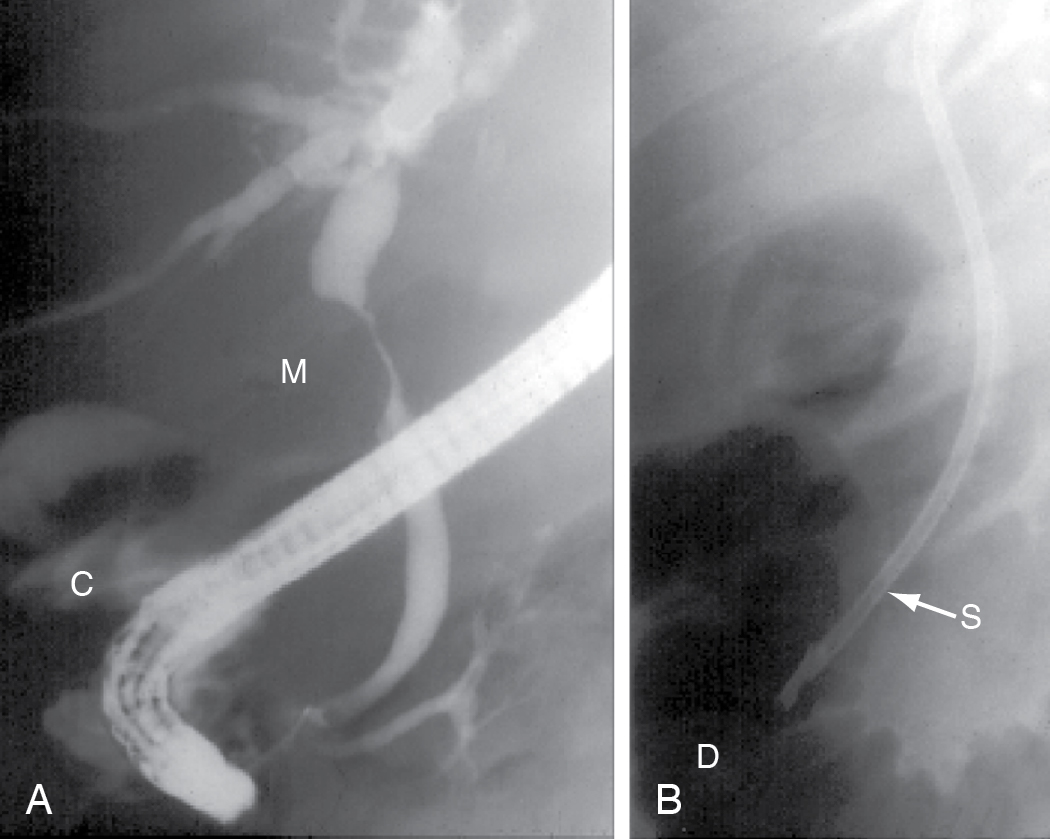
[Hình 5.22] Đặt stent cho hẹp đường mật. (A) Chụp ERCP cho thấy hẹp ác tính ống mật chủ do ung thư đường mật. (B) Đặt stent (S) qua nội soi qua chỗ hẹp.
- Dẫn lưu tụy (Pancreatic drainage): Đặt stent vào ống tụy để điều trị hẹp ống tụy hoặc rò tụy.
Các biến chứng của ERCP:
- Viêm tụy cấp (Acute pancreatitis): Biến chứng phổ biến nhất (khoảng 5%).
- Thủng (Perforation): Ở tá tràng hoặc ống dẫn mật.
- Chảy máu (Bleeding): Từ vị trí cắt cơ vòng.
- Nhiễm trùng (Infection): Viêm đường mật cấp (acute cholangitis) hoặc nhiễm trùng nang giả tụy (pancreatic pseudocyst).
Các phương pháp Nội Soi Khác
Nội soi ruột non với bóng (Balloon enteroscopy)
Nội soi ruột non là một phương tiện để tiếp cận sâu hơn vào ruột non, ngoài tầm với của nội soi tiêu hóa trên (gastroscopy) hoặc nội soi đại tràng (colonoscopy) tiêu chuẩn. Nó sử dụng một hoặc hai bóng gắn vào đầu ống nội soi để cố định vị trí, cho phép bác sĩ nội soi (endoscopist) có thể thu ngắn (pleat) và đẩy sâu hơn ống nội soi vào ruột.
Ứng dụng:
- Chảy máu đường tiêu hóa không rõ nguyên nhân (Obscure GI bleeding): Để điều trị các tổn thương như dị dạng mạch máu (angiodysplasias).
- Lấy dị vật (Foreign body retrieval).
- Đặt ống dẫn lưu hoặc điều trị hẹp (strictures).
Nội soi tá tràng bằng kim (Needlescopic duodenoscopy)
Đây là một ống nội soi mỏng được sử dụng để can thiệp ERCP ở trẻ em hoặc trong những trường hợp khó đặt ống thông (cannulation) nhú tá tràng.
Phẫu thuật Nội soi (Endoscopic Surgery) Cắt bỏ niêm mạc qua nội soi (Endoscopic mucosal resection – EMR) và Phân tách dưới niêm mạc qua nội soi (Endoscopic submucosal dissection – ESD)
Các kỹ thuật này được phát triển để loại bỏ ung thư sớm (early cancer) ở thực quản, dạ dày và đại tràng.
- EMR: Cắt bỏ tổn thương trên niêm mạc bằng cách tiêm dịch xuống dưới tổn thương để nâng nó lên, sau đó dùng thòng lọng để cắt bỏ.
- ESD: Cho phép cắt bỏ các tổn thương lớn hơn (lên đến 5 cm) bằng cách rạch niêm mạc xung quanh tổn thương và sau đó cắt bỏ tổn thương một cách nguyên khối (en bloc) khỏi lớp dưới niêm mạc bằng dao điện (electrocautery knife). Kỹ thuật này khó hơn nhưng cho phép cắt bỏ toàn bộ (complete resection) với nguy cơ tái phát tại chỗ thấp hơn.
Nội soi trực tràng qua ngả hậu môn (Transanal rectal endoscopy) Cắt bỏ vi phẫu nội soi trực tràng qua ngả hậu môn (Transanal Endoscopic Microsurgery – TEM) và Cắt bỏ nội soi qua ngả hậu môn (Transanal Endoscopic Operation – TEO)
Đây là các kỹ thuật phẫu thuật xâm lấn tối thiểu sử dụng nội soi đặc biệt để cắt bỏ ung thư trực tràng giai đoạn sớm và các polyp trực tràng lớn. Các dụng cụ và khí bơm được sử dụng tương tự như phẫu thuật nội soi ổ bụng (laparoscopy).
Can thiệp Nội soi qua Da (Percutaneous Endoscopic Intervention) Mở dạ dày qua da bằng nội soi (Percutaneous Endoscopic Gastrostomy – PEG)
Đặt ống thông dạ dày qua da dưới hướng dẫn nội soi.
- Kỹ thuật kéo (Pull technique): Ống nội soi dạ dày được đưa vào, định vị thành bụng. Một kim được chọc qua da vào dạ dày, sau đó một dây dẫn (guidewire) được kéo ra qua miệng. Ống PEG được gắn vào dây dẫn và được kéo qua miệng và ra khỏi thành bụng.
- Kỹ thuật đẩy (Push technique): Tương tự, nhưng ống PEG được đẩy qua đường hầm xuyên da.
Dụng cụ: Thường là ống thông mỏng bằng silicone với một đầu đĩa/mũ (mushroom tip) bên trong và một đĩa cố định (external bolster) bên ngoài để giữ nó cố định tại chỗ. Biến chứng: Nhiễm trùng vết thương, viêm cân mạc hoại tử (necrotising fasciitis – hiếm), rò dạ dày-đại tràng (gastrocolic fistula – hiếm), chảy máu và thủng.
Lấy Sỏi qua Da (Percutaneous Stone Removal)
Các phương pháp nội soi để lấy sỏi qua da từ bể thận (renal pelvis) ngày càng phổ biến (Tán sỏi thận qua da – percutaneous nephrolithotomy). Kỹ thuật này bao gồm việc tạo ra một kênh từ da vào bể thận và làm giãn nó cho đến khi có thể đưa ống nội soi vào. Khi nhìn thấy sỏi, các dụng cụ khác nhau có thể được sử dụng để làm vỡ và lấy chúng ra.
Phẫu thuật Có Hướng Dẫn Hình Ảnh (Image-guided surgery)
Các kỹ thuật hướng dẫn hình ảnh đang ở giai đoạn sơ khai, nhưng khả năng tăng cường tầm nhìn và nhận thức của bác sĩ phẫu thuật về trường mổ là một bước phát triển thú vị. Hiện tại, phẫu thuật có hướng dẫn Indocyanine Green (ICG) đã trở lại phổ biến. ICG là một chất huỳnh quang (fluorescent ligand) được tiêm tĩnh mạch và được kích thích bởi nguồn sáng đặc biệt ở bước sóng 850 nm. Các ống nội soi ổ bụng (laparoscopes) được điều chỉnh đặc biệt có thể phát hiện huỳnh quang, giúp xác định và định lượng tưới máu mô (tissue perfusion) (ví dụ: trước khi nối đại trực tràng) và đánh giá giải phẫu đường mật (biliary anatomy) và rò rỉ mật (bile leaks). Đây là một lĩnh vực hình ảnh quan trọng được kỳ vọng sẽ nâng cao hiệu suất phẫu thuật trong thời gian thực (real time).
Nội Soi Ổ Bụng Chẩn đoán và Điều trị (Diagnostic and therapeutic laparoscopy) Phần này đã được trình bày chi tiết trong Chương 10.
Nội soi Đại tràng (colonoscopy)
Ống nội soi mềm với độ dài khác nhau có sẵn để kiểm tra đại tràng (Hình 5.23). Ống nội soi sigma sợi quang (fibreoptic sigmoidoscope) là ngắn nhất, khoảng 60 cm (600 mm). Nó đơn giản để sử dụng và cho phép kiểm tra trực tràng, đại tràng sigma và đại tràng xuống với sự chuẩn bị ruột tối thiểu. Các ống nội soi đại tràng dài hơn cho phép kiểm tra toàn bộ đại tràng. Thân ống chính có các bộ phận thay đổi độ cứng để hỗ trợ đặt ống vào đến manh tràng (caecum). Các kỹ thuật khác giúp tiếp cận manh tràng bao gồm thổi khí carbon dioxide thay vì không khí và giải phóng dầu hạt (seed oil) từ đầu ống để bôi trơn dụng cụ.
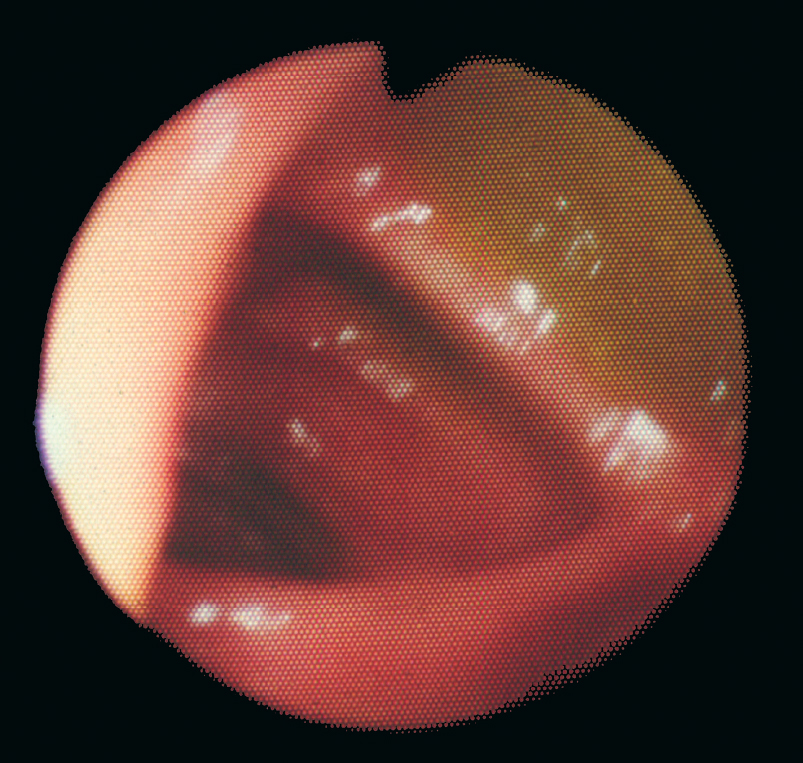
[Hình 5.23] Hình ảnh nội soi đại tràng ngang bình thường. Khi được nhìn thấy bằng nội soi đại tràng, đại tràng ngang thường có mặt cắt ngang hình tam giác; các dải cơ dọc (taenia coli) tạo thành các đỉnh.
Nội soi đại tràng cho phép kiểm tra các tổn thương bệnh lý, sinh thiết các tổn thương nghi ngờ và cắt bỏ các tổn thương như polyp. Nội soi đại tràng cũng được sử dụng để giám sát (surveillance) và theo dõi bệnh nhân đã điều trị ung thư đại trực tràng hoặc polyp. Các khối u hoặc polyp mới (tổn thương dị kỳ – metachronous lesions) được tìm kiếm, và vị trí phẫu thuật ban đầu có thể được kiểm tra. Các thăm khám tương tự cũng được sử dụng để giám sát bệnh nhân viêm đại tràng mãn tính (longstanding ulcerative colitis): nhiều mẫu sinh thiết được lấy để kiểm tra chứng loạn sản (dysplasia), và toàn bộ đại tràng được kiểm tra để tìm u tuyến (adenomas) hoặc ung thư biểu mô. Các tổn thương dị dạng mạch máu (angiodysplastic lesions) đang chảy máu cấp tính trong đại tràng có thể được điều trị bằng dao điện (diathermy).
Nội soi đại tràng là phương pháp đáng tin cậy nhất để sàng lọc (screening) ung thư biểu mô đại trực tràng ở những người không có triệu chứng. Tuy nhiên, ứng dụng của nó bị hạn chế bởi sự thiếu hụt các bác sĩ nội soi được đào tạo, bởi chi phí và bởi sự tuân thủ (compliance) của bệnh nhân.
Nội soi Tiết niệu (Urological endoscopy)
Nội soi tiết niệu (Endoscopic urology) là một phần ngày càng lớn của phẫu thuật tiết niệu với các dụng cụ mềm được sử dụng để nội soi bàng quang (cystoscopy) chẩn đoán và nội soi niệu quản (ureteroscopy).
Nội soi niệu đạo-bàng quang (Cysto-urethroscopy) sử dụng dụng cụ cứng là công cụ chẩn đoán và điều trị chính cho bệnh lý niệu đạo (urethra), tuyến tiền liệt (prostate) và bàng quang, cho phép sinh thiết và đốt điện (diathermy) mô. Một máy cắt đốt nội soi rửa (irrigating resectoscope) được sử dụng để loại bỏ mô tuyến tiền liệt trong phẫu thuật cửa ra bàng quang (cắt đốt tuyến tiền liệt qua niệu đạo – transurethral resection of the prostate – TURP) đã gần như loại bỏ nhu cầu phẫu thuật mở tuyến tiền liệt sau xương mu (retropubic prostatectomy). Hầu hết các khối u bàng quang sớm có thể được điều trị bằng cách cắt bỏ qua nội soi niệu đạo. Một dụng cụ tương tự như ống nội soi bàng quang (nhưng dài hơn), ống nội soi niệu quản cứng (rigid ureteroscope), có thể được sử dụng để hướng dẫn điều trị bằng laser cho sỏi hoặc khối u trong niệu quản, trong khi ống nội soi niệu quản mềm (flexible ureteroscope) dài hơn, mỏng hơn có thể tiếp cận niệu quản trên và hệ thống đài bể thận của thận để điều trị (xem Hình 37.6 trong Chương 37).
Các phương pháp nội soi để lấy sỏi qua da từ bể thận (renal pelvis) ngày càng phổ biến (Tán sỏi thận qua da – percutaneous nephrolithotomy). Kỹ thuật này bao gồm việc tạo ra một kênh từ da vào bể thận và làm giãn nó cho đến khi có thể đưa ống nội soi vào. Khi nhìn thấy sỏi, các dụng cụ khác nhau có thể được sử dụng để làm vỡ và lấy chúng ra (xem Hình 37.7B trong Chương 37).
Phẫu thuật Có Hướng Dẫn Hình Ảnh (Image-guided surgery)
Các kỹ thuật hướng dẫn hình ảnh đang ở giai đoạn sơ khai, nhưng khả năng tăng cường tầm nhìn và nhận thức của bác sĩ phẫu thuật về trường mổ là một bước phát triển thú vị. Hiện tại, phẫu thuật có hướng dẫn Indocyanine Green (ICG) đã trở lại phổ biến. ICG là một chất huỳnh quang (fluorescent ligand) được tiêm tĩnh mạch và được kích thích bởi nguồn sáng đặc biệt ở bước sóng 850 nm. Các ống nội soi ổ bụng (laparoscopes) được điều chỉnh đặc biệt có thể phát hiện huỳnh quang, giúp xác định và định lượng tưới máu mô (tissue perfusion) (ví dụ: trước khi nối đại trực tràng) và đánh giá giải phẫu đường mật (biliary anatomy) và rò rỉ mật (bile leaks). Đây là một lĩnh vực hình ảnh quan trọng được kỳ vọng sẽ nâng cao hiệu suất phẫu thuật trong thời gian thực (real time).
Nội Soi Ổ Bụng Chẩn đoán và Điều trị (Diagnostic and therapeutic laparoscopy)
Phần này đã được trình bày chi tiết trong Chương 10.
