Sách dịch: CÁC NGUYÊN LÝ Y HỌC HÔ HẤP, ẤN BẢN THỨ 8
Dịch và chú giải: Ts.Bs. Lê Nhật Huy, Ths.Bs. Lê Đình Sáng
Chương 22. Các Cơ chế Phòng vệ của Phổi
Lung defense mechanisms
Steven E. Weinberger MD, MACP, FRCP, Barbara A. Cockrill MD and Jess Mandel MD, MACP, FRCP
Principles of Pulmonary Medicine, 22, 265-274
MỤC LỤC CHƯƠNG
| Các Yếu tố Vật lý hay Giải phẫu Peptide Kháng khuẩn Các tế bào Thực bào và Tế bào Viêm Đại thực bào Phế nang Phổi Tế bào Tua Bạch cầu đa nhân Trung tính Tế bào Diệt Tự nhiên Đáp ứng Miễn dịch Thích ứng Cơ chế Miễn dịch Dịch thể Cơ chế Miễn dịch Tế bào Sự Suy yếu của Các Cơ chế Phòng vệ Đường hô hấp Suy giảm Thanh thải Vật lý Suy giảm chức năng của Peptide Kháng khuẩn Suy giảm chức năng của các Tế bào Thực bào và Tế bào Viêm Khiếm khuyết trong Hệ thống Miễn dịch Thích ứng Tăng cường Các Cơ chế Phòng vệ Đường hô hấp |
Trong quá trình trao đổi hàng nghìn lít không khí mỗi ngày để hấp thu và thải trừ , phổi phải tiếp xúc với vô số vi sinh vật và các chất lạ theo không khí hít vào. Một số trong đó có khả năng gây hại; một số khác tương đối vô hại. Không khí hít vào không phải là nguồn vật chất lạ duy nhất. Dịch tiết từ miệng và hầu họng thường bị hít sặc vào cây khí phế quản, đặc biệt là trong khi ngủ, ngay cả ở những người khỏe mạnh. Vô số những “kẻ xâm nhập” lạ đối với phổi này có lẽ được phân loại tốt nhất thành ba nhóm chính: các hạt nhỏ, các khí độc, và vi sinh vật. Bởi vì vùng hầu họng có rất nhiều vi khuẩn, dịch tiết bị hít sặc là một nguồn vi khuẩn không mong muốn xâm nhập vào đường thở đặc biệt quan trọng.
Để tự bảo vệ khỏi các vật chất hít vào có khả năng gây độc, hệ hô hấp đã phát triển các cơ chế bảo vệ phức tạp có thể được hình dung như các nhóm thành phần khác nhau. Mỗi thành phần dường như có một vai trò riêng biệt, nhưng có một mức độ dư thừa và tương tác rất lớn giữa các thành phần khác nhau. Việc nhu mô phổi ở đoạn xa thường không bị nhiễm trùng là một minh chứng cho hiệu quả của hệ thống phòng vệ. Tuy nhiên, các cơ chế bảo vệ có thể bị phá vỡ, dẫn đến nhiễm trùng đường hô hấp. Sự phá vỡ hệ thống phòng vệ như vậy có thể xảy ra do một số bệnh lý nhất định, một lượng lớn vi sinh vật xâm nhập áp đảo một ký chủ bình thường, một sinh vật có độc lực đặc biệt mạnh, hoặc thường là hậu quả của các phương pháp điều trị y tế làm suy yếu hệ miễn dịch.
Trước khi thảo luận về các rối loạn nhiễm trùng của hệ hô hấp trong Chương 23 đến 27, điều thích hợp là trước tiên xem xét cách phổi tự bảo vệ khỏi các tác nhân nhiễm trùng mà nó tiếp xúc. Mặc dù chương này tập trung vào các cơ chế bảo vệ chống lại nhiễm trùng, các cơ chế phòng vệ chống lại các chất không nhiễm trùng, đặc biệt là các hạt hít vào, cũng được đề cập. Các loại cơ chế phòng vệ chính sẽ được thảo luận bao gồm (1) các yếu tố vật lý hoặc giải phẫu liên quan đến sự lắng đọng và thanh thải các vật chất hít vào, (2) các peptide kháng khuẩn, (3) các tế bào thực bào và tế bào viêm tương tác với vật chất hít vào, và (4) các đáp ứng miễn dịch thích ứng, phụ thuộc vào sự tiếp xúc trước đó và nhận diện vật chất lạ. Chương này tập trung vào các khía cạnh của hệ thống phòng vệ của ký chủ đặc hiệu cho phổi và sau đó tiếp tục với một cuộc thảo luận về một số cách hệ thống này bị phá vỡ, dẫn đến việc không thể xử lý vi sinh vật và tăng nguy cơ mắc một số loại nhiễm trùng đường hô hấp. Chương này kết thúc bằng cách xem xét ngắn gọn cách chúng ta có thể kích hoạt hoặc tăng cường các đáp ứng miễn dịch đặc hiệu thông qua tiêm chủng, từ đó nâng cao khả năng phòng vệ chống lại các mầm bệnh hô hấp được chọn lọc.
CÁC YẾU TỐ VẬT LÝ HAY GIẢI PHẪU
Con đường từ miệng hoặc mũi xuống đến các phế nang đòi hỏi không khí hít vào phải đi qua một loạt các đường thở phân nhánh liên tiếp. Dòng chảy tầng của không khí qua đường thở trở nên hỗn loạn hơn tại các điểm phân nhánh (dưới cựa khí quản – subcarinae), do đó tăng cường sự lắng đọng của các hạt trên bề mặt niêm mạc phế quản tại các vị trí này. Do đó, các hạt hít vào thường lắng đọng tại nhiều điểm khác nhau dọc theo đường thở, không bao giờ đến được vùng xa nhất của phổi là các khoang phế nang. Kích thước của tiểu phân là một yếu tố quyết định quan trọng đến sự lắng đọng dọc theo đường thở và do đó ảnh hưởng đến khả năng một tiểu phân đến được nhu mô xa. Khi một tiểu phân hít vào có đường kính lớn hơn 10μm, sự lắng đọng có xu hướng xảy ra ở vị trí thấp hơn, trong khí quản hoặc các đường dẫn khí, nhưng không xuống đến mức của các đường thở nhỏ và phế nang. các hạt có khả năng đến nhu mô phổi xa nhất có kích thước từ 0,5 đến $5μm. Nhiều vi khuẩn nằm trong phạm vi kích thước này, vì vậy sự lắng đọng dọc theo đường thở không hiệu quả lắm trong việc loại trừ vi khuẩn khỏi đường hô hấp dưới. Tuy nhiên, các hạt bụi lớn và các vật chất hít vào khác được ngăn chặn hiệu quả không cho đến nhu mô phổi xa nhờ vào kích thước của chúng. Đáng chú ý, kích thước mục tiêu cho các hạt của thuốc hít, chẳng hạn như thuốc giãn phế quản, là dưới 5 µm để thuốc có thể đi qua các đường dẫn khí và đến được vùng phổi xa hơn.
Khi các hạt lắng đọng trong khí quản hoặc phế quản, hai quá trình chính, ho và vận chuyển nhầy-lông chuyển, chịu trách nhiệm cho việc loại bỏ vật lý các hạt này khỏi đường thở. Ho là một cơ chế bảo vệ quan trọng, thường được kích hoạt bởi sự kích thích của các thụ thể kích thích đường thở, vốn nổi bật nhất ở các đường thở gần và được kích hoạt bởi các vật chất lạ hít vào hoặc hít sặc. Sự tăng tốc nhanh và tốc độ dòng khí cao đạt được nhờ một cơn ho thường có hiệu quả trong việc làm sạch các vật chất lạ gây kích ứng khỏi đường thở.
|
Các yếu tố ảnh hưởng đến sự lắng đọng và thanh thải vật lý của các hạt: 1. Kích thước tiểu phân 2. Ho 3. Vận chuyển nhầy-lông chuyển |
Thuật ngữ vận chuyển nhầy-lông chuyển hay thanh thải nhầy-lông chuyển đề cập đến một quá trình trong đó các sóng phối hợp của các lông chuyển đập di chuyển một lớp chất nhầy (và bất kỳ vật chất nào bị giữ lại trong chất nhầy) lên dần dọc theo cây khí phế quản. Từ khí quản xuống đến các tiểu phế quản hô hấp, lớp tế bào biểu mô bề mặt nhất lót đường thở có các lông chuyển nhô ra lòng đường thở. Các lông chuyển này có cấu trúc giống hệt với các lông chuyển được tìm thấy ở những nơi khác trong cơ thể, bao gồm các vi ống dọc với một cấu trúc đặc trưng. Cụ thể, mặt cắt ngang của lông chuyển cho thấy hai vi ống trung tâm được bao quanh bởi chín cặp vi ống được sắp xếp xung quanh ngoại vi (Hình 22.1). Các tay đòn nhỏ nhô ra từ mỗi cặp vi ống, được gọi là tay đòn dynein, rất quan trọng đối với chức năng co của các vi ống và do đó đối với sự chuyển động của lông chuyển.
Sự chuyển động của các lông chuyển trên một tế bào cụ thể và sự chuyển động giữa các tế bào được phối hợp một cách đáng kinh ngạc, tạo ra các “sóng” chuyển động của lông chuyển thực sự. Cách chính xác một mô hình chuyển động của lông chuyển như vậy được phối hợp từ tế bào này sang tế bào khác hoặc thậm chí trong cùng một tế bào vẫn chưa được biết đầy đủ. Chuyển động dạng sóng này thực hiện việc di chuyển lớp chất nhầy phủ bên trên theo hướng về phía đầu (tức là, từ các phần xa đến các phần gần hơn của cây khí phế quản) với tốc độ đáng kinh ngạc ước tính từ 6 đến trong khí quản. các hạt hít vào bị giữ lại trong lớp chất nhầy cũng được vận chuyển lên trên và cuối cùng được khạc ra hoặc nuốt vào.
Hai lớp tạo nên lớp màng nhầy bao bọc các tế bào biểu mô. Ngay sát các tế bào là lớp sol, nơi các lông chuyển định vị. Lớp sol dạng nước này chứa một số phân tử trong dung dịch là một phần của hệ miễn dịch bẩm sinh và được thảo luận trong phần “Peptide kháng khuẩn”. Phía trên lớp sol là lớp gel nhớt hơn, được sản xuất bởi cả các tuyến nhầy dưới niêm mạc và các tế bào hình đài. Lớp gel nhớt nổi trên lớp sol và được đẩy theo hướng về phía đầu khi các lông chuyển đập tự do hơn trong lớp sol ít nhớt hơn.
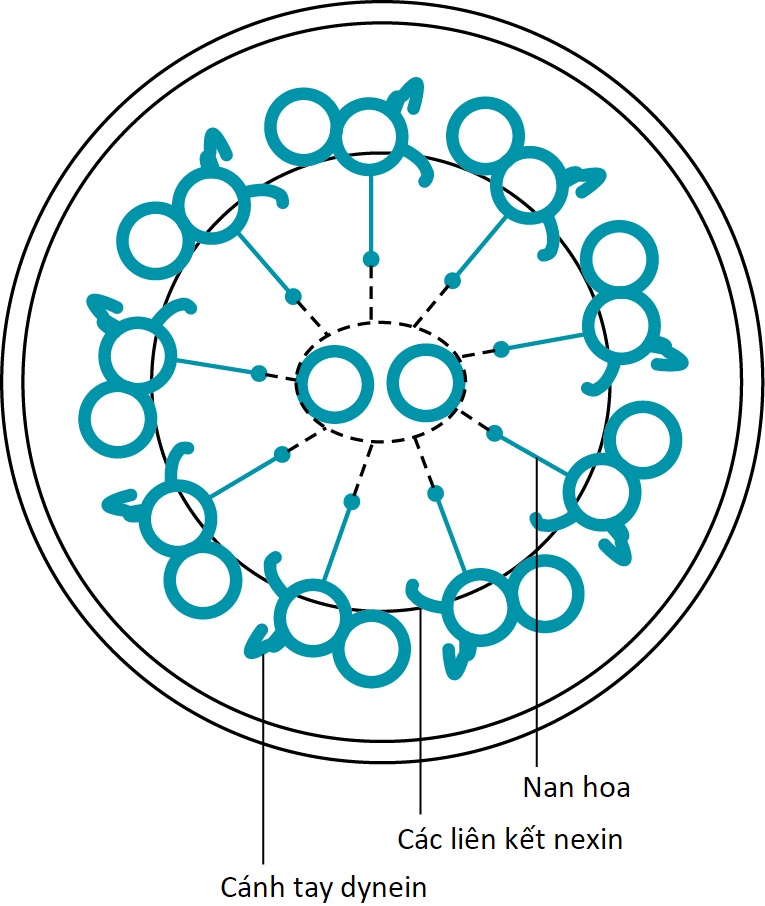
Hình 22.1 *Sơ đồ mặt cắt ngang của lông chuyển. Cho thấy hai vi ống trung tâm và chín cặp vi ống ngoại vi. Một tay đòn dynein nhô ra từ mỗi cặp đôi ngoại vi, và các liên kết nexin cùng các nan hoa hướng tâm tạo ra các kết nối bên trong cấu trúc vi ống. *
PEPTIDE KHÁNG KHUẨN
Lớp sol chứa một số chất quan trọng trong miễn dịch bẩm sinh. Hệ miễn dịch bẩm sinh có thể được coi là một hệ thống tác động nhanh, sẵn sàng bảo vệ phổi một cách nhanh chóng mà không cần sự mẫn cảm trước đó và lý tưởng nhất là tránh kích hoạt hệ miễn dịch thích ứng (thảo luận trong phần “Các Đáp ứng Miễn dịch Thích ứng”). Ngoài việc thanh thải nhầy-lông chuyển, hệ miễn dịch bẩm sinh bao gồm các phân tử nhỏ, protein, và các tế bào có khả năng đáp ứng với các hạt hít vào mà không cần bất kỳ sự tiếp xúc trước đó với tiểu phân. Các phân tử này thường được bảo tồn cao trong quá trình tiến hóa và có mặt ở nhiều loài không xương sống cũng như ở người. Chúng có thể tương tác ngay lập tức với vi sinh vật thông qua các thụ thể nhận dạng mẫu được kích thích bởi các cấu trúc được bảo tồn trên vi khuẩn, và chúng có thể tác động trực tiếp để tiêu diệt kẻ xâm nhập và khởi đầu một đáp ứng miễn dịch bổ sung của ký chủ. Đáp ứng miễn dịch bẩm sinh cung cấp một tuyến phòng thủ đầu tiên nhanh chóng, hiệu quả về năng lượng, với sự chồng chéo rộng rãi trong các hoạt động. Có nhiều thành phần của miễn dịch bẩm sinh trong phổi và hơn 2000 peptide kháng khuẩn tự nhiên. Một mô tả đầy đủ nằm ngoài phạm vi của chương này; tuy nhiên, độc giả quan tâm được giới thiệu đến các bài tổng quan sâu sắc được liệt kê trong phần Đọc thêm. Chương này tập trung vào một vài trong số các phân tử được mô tả rõ nhất: lysozyme, lactoferrin, defensin, collectin (protein surfactant A [SP-A] và protein surfactant D [SP-D]), và immunoglobulin (Ig)A.
|
Các chất miễn dịch bẩm sinh trong đường thở bao gồm: 1. Lysozyme 2. Lactoferrin 3. Defensin 4. Collectin (protein surfactant A và D) 5. IgA |
Lysozyme có mặt trên toàn bộ đường hô hấp nhưng nổi bật nhất ở các đường thở gần. Nó được tổng hợp bởi các tế bào biểu mô đường hô hấp, các tế bào tuyến thanh dịch, và các đại thực bào. Như tên gọi của nó, lysozyme gây chết tế bào vi khuẩn bằng cách gây ly giải. Nó hoạt động mạnh nhất chống lại các sinh vật Gram dương. Mức độ lysozyme giảm có tương quan với sự nhạy cảm tăng lên đối với viêm phế quản cấp tính.
Lactoferrin có mặt trong dịch đường thở. Nó được sản xuất bởi các tế bào thanh dịch và bạch cầu đa nhân trung tính. Lactoferrin có tác dụng ngưng kết và tiêu diệt vi khuẩn, tăng cường sự bám dính của bạch cầu đa nhân trung tính, và mồi cho quá trình sản xuất superoxide của bạch cầu đa nhân trung tính. Tên của nó bắt nguồn từ thực tế là lactoferrin cũng có chức năng ngăn chặn sắt hỗ trợ quá trình chuyển hóa của vi khuẩn. Lactoferrin liên kết với vi khuẩn thông qua việc nhận dạng các nhóm carbohydrate được bảo tồn cao trên bề mặt tế bào vi sinh vật.
Defensin là một họ các protein nhỏ có hoạt tính kháng khuẩn nội tại được tìm thấy trong phổi và trên các bề mặt niêm mạc khác, bao gồm đường tiêu hóa và đường sinh sản. Hai loại defensin quan trọng trong phổi là α-defensin và β-defensin. α-Defensin được tổng hợp bởi các bạch cầu đa nhân trung tính thường trú; β-defensin được tạo ra bởi các tế bào biểu mô đường hô hấp. Defensin có hoạt tính kháng khuẩn rộng chống lại cả sinh vật Gram dương và Gram âm. Chúng hoạt động bằng cách làm cho thành tế bào vi sinh vật thấm qua, do đó gây ra sự giải phóng các thành phần tế bào vi sinh vật và phá hủy điện thế màng. Hoạt động của defensin rất nhạy cảm với nồng độ ion và chúng bị bất hoạt trong môi trường bất thường ở phổi của bệnh nhân bị xơ nang.
SP-A và SP-D là các thành viên của họ protein collectin. Chức năng kháng khuẩn của chúng là kết quả của việc liên kết và kết tụ vi khuẩn và tạo điều kiện cho sự tương tác với các tế bào thực bào. Chúng cũng dường như quan trọng trong việc điều hòa hoạt động của đại thực bào phổi và sản xuất cytokine. Các mô hình động vật chỉ ra rằng khiếm khuyết ở một trong hai protein này làm tăng tính nhạy cảm với nhiễm trùng đường hô hấp.
IgA đường hô hấp có thể được coi là một phần của hệ miễn dịch bẩm sinh vì nó cũng được sản xuất liên tục bởi biểu mô đường hô hấp và không cần tiếp xúc trước đó. IgA được thảo luận thêm trong phần “Các Cơ chế Miễn dịch Dịch thể”.
CÁC TẾ BÀO THỰC BÀO VÀ TẾ BÀO VIÊM
Đại thực bào Phế nang
Trong đường thở và ở cấp độ phế nang, các hạt và vi khuẩn có thể bị dọn dẹp bởi các tế bào thực bào đơn nhân được gọi là đại thực bào phế nang. Các tế bào này cấu thành một hình thức phòng vệ chính chống lại các vật chất đã thoát khỏi sự lắng đọng ở đường hô hấp trên và đã đến được đường thở trong lồng ngực hoặc các cấu trúc phế nang. Đại thực bào phế nang là các tế bào di động lớn có đường kính khoảng 15 đến 50 µm. Chúng là hậu duệ của các bạch cầu đơn nhân lưu hành có nguồn gốc từ tủy xương. Các tế bào này bám vào biểu mô phế nang. Bào tương của chúng chứa nhiều loại hạt có hình dạng và kích thước khác nhau, nhiều trong số đó là các gói enzyme tiêu hóa có thể xử lý các vật chất lạ đã được nuốt vào.
Đại thực bào phế nang có vai trò chính trong việc tiêu diệt các vi sinh vật đã đến đường hô hấp dưới. Chúng cũng giải phóng các cytokine hóa hướng động (chemokine) để chiêu mộ các tế bào viêm khác. Khi một đại thực bào phế nang tiếp xúc với các hạt hoặc vi khuẩn hít vào, sự gắn kết của vật chất lạ vào bề mặt đại thực bào là bước đầu tiên trong chuỗi xử lý. các hạt hoặc vi khuẩn được bao bọc trong màng plasma, màng này lõm vào và tách ra bên trong tế bào để tạo thành một thể thực bào (phagosome) trong bào tương chứa vật chất lạ hiện đã được cô lập. Trong một số trường hợp, chuỗi gắn kết và thực bào này được tạo điều kiện bởi các opsonin, vốn bao bọc vật chất lạ. Opsonin là các protein liên kết với các vật chất ngoại bào và làm cho chúng dính hơn vào các tế bào thực bào và dễ bị nuốt hoặc tiêu hóa hơn. Opsonin có thể đặc hiệu cho chất lạ cụ thể, chẳng hạn như các kháng thể chống lại vật liệu kháng nguyên, hoặc chúng có thể thể hiện sự liên kết không đặc hiệu với nhiều chất khác nhau. Các opsonin đặc hiệu đặc biệt quan trọng là các kháng thể thuộc lớp IgG chống lại vật liệu kháng nguyên lạ, có thể là vi khuẩn hoặc các hạt kháng nguyên khác. Các opsonin không đặc hiệu trong phổi bao gồm IgA tiết, bổ thể, và fibronectin. Tất cả các opsonin này thúc đẩy mạnh mẽ sự gắn kết và tiêu hóa bởi các đại thực bào.
Sau khi vi khuẩn hoặc vật chất lạ khác được cô lập trong các thể thực bào, một quá trình tiêu hóa nội bào xảy ra bên trong đại thực bào. Thường thì các thể thực bào kết hợp với các lysosome để tạo thành các thể thực bào-lysosome (phagolysosome), trong đó các enzyme phân giải protein do lysosome cung cấp sẽ tiêu hóa, giải độc, hoặc phá hủy các thành phần trong thể thực bào. Ngoài các enzyme lysosome, một loạt các sản phẩm oxy hóa, chẳng hạn như hydrogen peroxide và các sản phẩm trung gian khác của quá trình chuyển hóa oxy hóa, có độc tính đối với vi khuẩn và đóng một vai trò trong khả năng của đại thực bào để tiêu diệt các vi sinh vật đã được nuốt vào.
Sau khi được kích hoạt, các đại thực bào phổi thường trú tham gia vào việc điều phối các đáp ứng miễn dịch tiếp theo. Các đại thực bào giải phóng các chất trung gian gây viêm như yếu tố hoại tử khối u-α và interleukin-1β, cũng như các cytokine và chemokine khác có hoạt tính trong việc chiêu mộ thêm các tế bào viêm.
Đại thực bào không phải lúc nào cũng tiêu diệt hoặc loại bỏ hoàn toàn vật chất lạ hít vào mà nó tiếp xúc. Trong một số trường hợp, chẳng hạn như với các hạt silica hít vào, vật chất được nuốt vào có độc tính đối với đại thực bào và cuối cùng có thể giết chết tế bào thực bào. Trong các trường hợp khác, vật chất được nuốt vào là trơ nhưng về cơ bản không thể tiêu hóa được và có thể tồn tại vô thời hạn dưới dạng cặn không thể bị phân hủy thêm hoặc bị thanh thải. Một số sinh vật có khả năng đặc biệt trong việc gây nhiễm trùng dai dẳng ở các đại thực bào mà không bị tiêu diệt hoặc bất hoạt, bao gồm Mycobacterium tuberculosis và virus gây suy giảm miễn dịch ở người (HIV).
Đại thực bào phế nang cũng quan trọng trong việc ức chế viêm trong phổi. Phổi là duy nhất ở chỗ nó liên tục tiếp xúc với các chất lạ hít vào nhưng đồng thời phải duy trì một bộ máy trao đổi khí cực kỳ tinh vi. Ngay cả một lượng nhỏ viêm trong thành phế nang cũng sẽ có tác động tiêu cực đến trao đổi khí, và một sự cân bằng tinh tế giữ cho các đường thở xa không bị nhiễm trùng nhưng không ở trong tình trạng viêm có hại liên tục. Đại thực bào phế nang có thể xử lý một lượng lớn các chất hít vào mà không gây ra đáp ứng miễn dịch bên ngoài bản thân đại thực bào. Người ta ước tính rằng quần thể đại thực bào phế nang bình thường có thể xử lý tới vi khuẩn hít vào trước khi vi khuẩn áp đảo các đại thực bào và gây nhiễm trùng trong phế nang. Ngoài ra, đại thực bào phế nang, thông qua các cơ chế tín hiệu phức tạp, có chức năng kiểm soát sự kích hoạt của tế bào tua và tế bào T. Hoạt động chi tiết của sự cân bằng tinh tế này giữa viêm và trạng thái tĩnh trong phổi là một lĩnh vực nghiên cứu tích cực.
|
Các tế bào thực bào và tế bào viêm thường trú chính: 1. Đại thực bào phế nang 2. Tế bào tua (đường thở và nhu mô) 3. Bạch cầu đa nhân trung tính 4. Tế bào diệt tự nhiên |
Tế bào Tua
Tế bào tua có mặt trên khắp cơ thể dưới nhiều hình thức khác nhau. Chúng là các tế bào có nguồn gốc từ tủy xương, trong phổi, chúng nằm trong biểu mô đường thở cũng như trong thành phế nang và mô liên kết quanh phế quản. Các tế bào này có các phần mở rộng bào tương dài và không đều tạo thành một mạng lưới liên tục. Chức năng chính của tế bào tua là lấy mẫu vi môi trường đường thở, nuốt và xử lý kháng nguyên, sau đó di chuyển đến các hạch bạch huyết khu vực. Trong các hạch bạch huyết, tế bào tua trình diện kháng nguyên cho các tế bào T, một bước quan trọng cho sự phòng vệ miễn dịch sau này do các tế bào lympho cung cấp. Tế bào Langerhans, một loại tế bào tua có hình dạng siêu cấu trúc đặc biệt, là các tế bào có sự tăng sinh bất thường dường như chịu trách nhiệm cho bệnh mô bào Langerhans của phổi (còn được gọi là u hạt ái toan; xem Chương 11).
Bạch cầu đa nhân trung tính
Một tế bào quan trọng khác liên quan đến phòng vệ phổi là bạch cầu đa nhân trung tính (PMN). PMN là một thành phần đặc biệt quan trọng của cơ chế phòng vệ đối với một nhiễm trùng vi khuẩn đã hình thành ở đường hô hấp dưới. Thông thường, có rất ít PMN cư trú trong các đường thở nhỏ và phế nang. Khi vi khuẩn áp đảo các cơ chế phòng vệ ban đầu đã được thảo luận, chúng có thể nhân lên trong các khoang phế nang, gây ra viêm phổi do vi khuẩn. Việc kiểm tra các đặc điểm mô học của một bệnh viêm phổi do vi khuẩn cho thấy một thành phần nổi bật của đáp ứng viêm là sự tràn ra của các PMN vào các khoang phế nang. Các tế bào này có lẽ bị thu hút đến phổi bởi nhiều kích thích khác nhau, đặc biệt là các sản phẩm của quá trình hoạt hóa bổ thể và các yếu tố hóa hướng động do các đại thực bào phế nang giải phóng. Sự di chuyển cuối cùng của PMN ra khỏi mạch máu và vào nhu mô phổi phụ thuộc vào sự bám dính ban đầu của PMN vào nội mô mạch máu. Một loạt các yếu tố làm trung gian cho quá trình bám dính này, bao gồm các integrin (trên bề mặt PMN) và các phân tử kết dính (trên bề mặt tế bào nội mô mạch máu). Khi PMN tham gia, chúng đóng một vai trò quan trọng trong việc thực bào và tiêu diệt quần thể vi khuẩn xâm nhập và tăng sinh. Các hạt của bạch cầu đa nhân trung tính chứa một số chất kháng khuẩn, bao gồm defensin, lysozyme, protein làm tăng tính thấm của vi khuẩn, và lactoferrin. Ngoài ra, bạch cầu đa nhân trung tính có thể tạo ra các sản phẩm của quá trình chuyển hóa oxy hóa có độc tính đối với vi khuẩn.
Tế bào Diệt Tự nhiên
Tế bào diệt tự nhiên (NK) là một phần của đáp ứng ban đầu nhanh chóng và có khả năng, không cần mẫn cảm trước, tiêu diệt các tế bào bị nhiễm vi sinh vật, đặc biệt là virus. Tế bào NK thiếu các dấu ấn bề mặt đặc trưng của cả tế bào lympho T hoặc B (thảo luận trong phần “Các Cơ chế Miễn dịch Tế bào”). Chúng hoạt động bằng cách nhận dạng và tiêu diệt các tế bào bị nhiễm virus đã bị biến đổi và biểu hiện các dấu ấn khác nhau về sức khỏe tế bào trên bề mặt tế bào. Tế bào NK cũng quan trọng trong việc giám sát các khối u tân sinh, và chúng sử dụng các phương pháp tương tự để phát hiện và tiêu diệt các tế bào bị biến đổi ác tính.
CÁC ĐÁP ỨNG MIỄN DỊCH THÍCH ỨNG
Loại cơ chế phòng vệ cuối cùng cho hệ hô hấp là đáp ứng miễn dịch thích ứng, bao gồm việc nhận dạng và đáp ứng với vật liệu kháng nguyên cụ thể sau khi đã có sự mẫn cảm trước đó. Vi khuẩn, virus, và các vi sinh vật khác có lẽ là những kháng nguyên quan trọng nhất mà đường hô hấp tiếp xúc lặp đi lặp lại. Có lẽ, các cơ chế phòng vệ miễn dịch đặc biệt quan trọng trong việc bảo vệ cá nhân chống lại các tác nhân này. Các quá trình của đáp ứng miễn dịch thích ứng không phải là duy nhất đối với phổi, và chỉ một cuộc thảo luận sơ lược về các nguyên tắc chung được cung cấp ở đây làm cơ sở để hiểu các đáp ứng miễn dịch thích ứng trong phổi. Để biết thêm thông tin chi tiết, độc giả được giới thiệu đến các văn bản chuyên ngành và các bài báo tổng quan về miễn dịch học.
Hai thành phần chính của hệ miễn dịch thích ứng là dịch thể (liên quan đến tế bào lympho B) và tế bào (liên quan đến tế bào lympho T). Miễn dịch dịch thể liên quan đến việc kích hoạt các tế bào lympho B (không cần tuyến ức để biệt hóa) và sản xuất kháng thể bởi các tương bào (có nguồn gốc từ tế bào lympho B). Miễn dịch tế bào đề cập đến việc kích hoạt các tế bào lympho T (phụ thuộc vào tuyến ức để biệt hóa) và thực hiện các chức năng cụ thể của tế bào lympho T, bao gồm sản xuất các chất trung gian hòa tan hoặc cytokine. Hai hệ thống tế bào lympho không độc lập với nhau. Cụ thể, các tế bào lympho T dường như có một vai trò quan trọng trong việc điều hòa tổng hợp immunoglobulin hoặc kháng thể bởi hệ miễn dịch dịch thể.
Cả miễn dịch dịch thể và miễn dịch tế bào đều quan trọng trong việc bảo vệ hệ hô hấp chống lại vi sinh vật. Đối với một số tác nhân nhiễm trùng nhất định, miễn dịch dịch thể là phương thức bảo vệ chính. Đối với các tác nhân khác, miễn dịch tế bào dường như là tối quan trọng. Trong phổi và trong máu, các tế bào lympho T nhiều hơn các tế bào lympho B, nhưng cả hai hệ thống đều cần thiết cho việc phòng vệ hiệu quả chống lại phổ vi sinh vật có khả năng gây hại.
Các tế bào lympho có thể được tìm thấy ở nhiều vị trí trong đường hô hấp, kéo dài từ vòm mũi họng xuống đến các vùng xa của nhu mô phổi. Các hạch bạch huyết thực sự có mặt xung quanh khí quản và cựa khí quản, và tại rốn mỗi phổi trong khu vực của các phế quản gốc. Các hạch bạch huyết này nhận dẫn lưu bạch huyết từ hầu hết các đường thở và nhu mô phổi. Mô bạch huyết có mặt trong vòm mũi họng, và các tập hợp tế bào lympho được sắp xếp thành các nốt được tìm thấy dọc theo các phế quản từ trung bình đến lớn. Các tập hợp sau này được gọi là mô bạch huyết liên quan đến phế quản và có thể chịu trách nhiệm chặn và xử lý các kháng nguyên lắng đọng dọc theo các đường dẫn khí. Các tập hợp tế bào lympho nhỏ hơn có thể được tìm thấy trong các đường thở xa hơn và thậm chí nằm rải rác khắp nhu mô phổi.
|
Các thành phần chính của hệ miễn dịch thích ứng hoạt động trong đường hô hấp: 1. Tế bào lympho T 2. Tế bào lympho B 3. IgG |
Các Cơ chế Miễn dịch Dịch thể
Miễn dịch dịch thể trong đường hô hấp xuất hiện dưới dạng hai lớp immunoglobulin chính: IgA và IgG. Các kháng thể thuộc lớp IgA đặc biệt quan trọng ở vòm mũi họng và đường hô hấp trên, nơi chúng cấu thành loại kháng thể chính. Dạng IgA có mặt ở những khu vực này là IgA tiết, bao gồm một dimer các phân tử IgA (được nối với nhau bằng một polypeptide) cộng với một thành phần glycoprotein bổ sung được gọi là thành phần tiết. IgA tiết dường như được tổng hợp tại chỗ, và lượng IgA lớn hơn nhiều ở đường hô hấp trên so với trong huyết thanh.
Bằng chứng cho thấy IgA tiết đóng một vai trò quan trọng trong hệ thống phòng vệ đường hô hấp. Nhờ khả năng liên kết với kháng nguyên, IgA có thể liên kết với virus và vi khuẩn, ngăn chặn sự bám dính của chúng vào các tế bào biểu mô. Ngoài ra, IgA có hiệu quả trong việc ngưng kết các vi sinh vật; các vi khuẩn bị ngưng kết dễ dàng được thanh thải hơn bởi hệ thống vận chuyển nhầy-lông chuyển. Cuối cùng, IgA dường như có khả năng trung hòa một loạt các virus đường hô hấp cũng như một số vi khuẩn. Tuy nhiên, nhiều chức năng của IgA là dư thừa so với các phần khác của hệ miễn dịch, vì phần lớn các cá nhân bị thiếu hụt IgA chọn lọc không có triệu chứng, trong khi ít hơn 10% phát triển các bệnh nhiễm trùng xoang-phổi tái phát.
Trái ngược với IgA, IgG đặc biệt phong phú ở đường hô hấp dưới. Nó được tổng hợp tại chỗ ở một mức độ lớn, mặc dù một phần cũng có nguồn gốc từ IgG huyết thanh. Nó có một số đặc tính sinh học, chẳng hạn như ngưng kết các hạt, trung hòa virus và độc tố vi khuẩn, đóng vai trò là opsonin cho quá trình thực bào vi khuẩn của đại thực bào, hoạt hóa bổ thể, và gây ly giải vi khuẩn Gram âm khi có sự hiện diện của bổ thể. Vai trò tổng thể của hệ miễn dịch dịch thể trong phòng vệ đường hô hấp bao gồm bảo vệ phổi chống lại một loạt các bệnh nhiễm trùng do vi khuẩn và, ở một mức độ nào đó, là virus. Các ý nghĩa lâm sàng của vai trò này và hậu quả của sự suy giảm trong hệ miễn dịch dịch thể được thảo luận trong phần “Khiếm khuyết trong Hệ Miễn dịch Thích ứng”.
Các Cơ chế Miễn dịch Tế bào
Các cơ chế miễn dịch tế bào, những cơ chế được trung gian bởi các tế bào lympho phụ thuộc tuyến ức (T), cũng hoạt động như một phần của hệ thống phòng vệ tổng thể của phổi. Các tế bào lympho T đã được mẫn cảm tạo ra một loạt các chất trung gian hòa tan, có hoạt tính sinh học được gọi là cytokine, một số trong đó (ví dụ, interferon [IFN]-y) có chức năng thu hút hoặc kích hoạt các loại tế bào bảo vệ khác, đặc biệt là các đại thực bào. Các tế bào lympho T cũng có thể tương tác với hệ miễn dịch dịch thể và điều chỉnh sản xuất kháng thể.
Hai loại tế bào lympho T quan trọng đã được đặc trưng rõ ràng dựa trên các dấu ấn bề mặt tế bào cụ thể và các đặc điểm chức năng. Một loại bao gồm các tế bào dương tính với dấu ấn bề mặt CD4, thường được gọi là tế bào T hoặc tế bào T hỗ trợ. Tế bào , lần lượt, được chia thành các phân nhóm và , lần lượt làm trung gian cho phòng vệ miễn dịch tế bào và viêm dị ứng. Loại tế bào lympho T chính khác bao gồm các tế bào dương tính với dấu ấn bề mặt CD8. Các tế bào này bao gồm các tế bào T ức chế và tế bào T gây độc. Khi tiếp xúc với các kháng nguyên cụ thể, cả tế bào và đều tạo ra nhiều loại cytokine tương tác với các thành phần khác của hệ miễn dịch, đặc biệt là các tế bào lympho B và đại thực bào.
Một vai trò quan trọng của hệ miễn dịch tế bào là bảo vệ chống lại các vi khuẩn có mô hình phát triển nội bào, đặc biệt là M. tuberculosis (xem thảo luận về bệnh lao trong Chương 25). Ngoài ra, hệ miễn dịch tế bào có một vai trò quan trọng trong việc xử lý nhiều loại virus, nấm, và động vật đơn bào.
Mặc dù việc phân chia sự bảo vệ miễn dịch của phổi thành các loại khác nhau là quan trọng cho mục đích thảo luận, các chức năng này lại đan xen sâu sắc, và rối loạn chức năng ở một khía cạnh có khả năng gây ra vấn đề ở các phần khác của hệ thống. Sự phát triển của một bệnh nhiễm trùng đường hô hấp thường chỉ ra rằng một số cơ chế phòng vệ đã bị sinh vật gây bệnh vượt qua.
SỰ SUY YẾU CỦA CÁC CƠ CHẾ PHÒNG VỆ ĐƯỜNG HÔ HẤP
Các khiếm khuyết quan trọng về mặt lâm sàng đã được ghi nhận cho mỗi loại cơ chế phòng vệ đường hô hấp chính. Kết quả là, các bệnh nhiễm trùng đường hô hấp có thể xảy ra, và việc phân tích các loại nhiễm trùng cụ thể liên quan đến từng loại khiếm khuyết là hữu ích về mặt lâm sàng.
Suy giảm Thanh thải Vật lý
Sự suy giảm thanh thải vật lý đơn giản nhất để hiểu là không có khả năng ho hiệu quả. Ba yếu tố được yêu cầu để tạo ra vận tốc cao của một cơn ho hiệu quả: (1) một nhịp hít vào sâu, (2) sự gia tăng áp lực trong lồng ngực khi thanh môn đóng, và (3) một luồng thở ra phối hợp trong đó thanh môn mở ra. Xem xét từng bước này, sẽ dễ dàng hiểu tại sao một số bệnh nhân gặp khó khăn trong việc làm sạch các hạt hít vào và dịch tiết đường hô hấp. Bệnh nhân có cơ hoành yếu hoặc bị liệt sẽ không thể hít một hơi thật sâu. Bệnh nhân có cơ thở ra yếu, chẳng hạn như người bị liệt tứ chi, sẽ không thể tạo ra sự gia tăng lớn áp lực trong lồng ngực. Bệnh nhân có mở khí quản mãn tính hoặc liệt dây thanh âm sẽ không thể đóng thanh môn hiệu quả để tăng áp lực trong lồng ngực. Tất cả những bệnh nhân này đều dễ bị nhiễm trùng đường hô hấp, ngay cả khi hệ thống miễn dịch cơ bản của họ là bình thường.
Các yếu tố vật lý hoặc giải phẫu khác ảnh hưởng đến sự lắng đọng và thanh thải các hạt bao gồm các bất thường di truyền và các yếu tố môi trường ảnh hưởng đến hệ thống vận chuyển nhầy-lông chuyển. Thông tin đặc biệt thú vị đã được cung cấp bởi một bất thường di truyền được gọi là rối loạn vận động lông chuyển nguyên phát, đôi khi còn được gọi là hội chứng lông chuyển rối loạn vận động hoặc hội chứng lông chuyển bất động. Trong rối loạn này, một khiếm khuyết trong cấu trúc và chức năng của lông chuyển dẫn đến sự vận động của lông chuyển bị mất hoặc suy giảm và do đó dẫn đến việc thanh thải nhầy-lông chuyển không hiệu quả. Hơn 20 loại khiếm khuyết được ghi nhận, nhưng phổ biến nhất là sự thiếu vắng các tay đòn dynein trên các vi ống (Hình 22.1). Về mặt lâm sàng, sự suy giảm thanh thải nhầy-lông chuyển có liên quan đến viêm xoang mãn tính, viêm phế quản mãn tính, và giãn phế quản. Ở nam giới, đuôi của tinh trùng, có cấu trúc tương tự như lông chuyển, bị bất thường, dẫn đến khả năng vận động của tinh trùng kém và vô sinh. Rối loạn được gọi là hội chứng Kartagener, bao gồm bộ ba viêm xoang mãn tính, giãn phế quản, và đảo ngược phủ tạng (situs inversus), là một biến thể của rối loạn vận động lông chuyển nguyên phát (xem Chương 7). Chuyển động bình thường của lông chuyển theo một hướng cụ thể được cho là chịu trách nhiệm cho sự xoay bình thường của tim và định vị của các cơ quan trong ổ bụng trong quá trình phát triển phôi thai. Khi chức năng của lông chuyển bị rối loạn đáng kể, việc định vị của tim và các cơ quan trong ổ bụng trở nên ngẫu nhiên, do đó giải thích cho tình trạng đảo ngược phủ tạng được tìm thấy ở khoảng 50% bệnh nhân bị rối loạn vận động lông chuyển nguyên phát.
|
Các nguyên nhân gây suy giảm thanh thải nhầy-lông chuyển: 1. Rối loạn vận động lông chuyển nguyên phát 2. Nhiễm trùng đường hô hấp do virus 3. Hút thuốc lá 4. Nồng độ cao trong thời gian dài 5. Gây mê toàn thân |
Nhiễm trùng đường hô hấp do virus thường gây tổn thương cấu trúc tạm thời cho niêm mạc khí phế quản. Niêm mạc bị tổn thương có liên quan đến việc suy giảm thanh thải nhầy-lông chuyển, điều này có thể làm chậm quá trình vận chuyển vi khuẩn xâm nhập ra khỏi cây khí phế quản. Đây là một trong những cơ chế mà nhiễm trùng đường hô hấp do virus khiến cá nhân dễ bị bội nhiễm vi khuẩn.
Các yếu tố môi trường cũng có thể gây suy giảm thanh thải nhầy-lông chuyển. Tiếp xúc với khói thuốc lá là quan trọng nhất về mặt lâm sàng và có lẽ góp phần vào xu hướng của những người hút thuốc nặng bị nhiễm trùng đường hô hấp tái phát. Một số chất gây ô nhiễm không khí, chẳng hạn như sulfur dioxide , nitrogen dioxide , và ozone , dường như làm suy giảm thanh thải nhầy-lông chuyển, nhưng hậu quả lâm sàng không hoàn toàn rõ ràng. Nồng độ cao, chẳng hạn như 90% đến 100% hít vào trong hơn vài giờ, dường như có liên quan đến chức năng nhầy-lông chuyển bị suy giảm. Ở đây, hậu quả có thể liên quan đến các bệnh nhân bị suy hô hấp cần những nồng độ cực cao này. Ngoài ra, gây mê toàn thân với các loại thuốc hít được sử dụng trong phẫu thuật có liên quan đến rối loạn chức năng lông chuyển ngắn hạn và góp phần làm tăng nguy cơ viêm phổi ở bệnh nhân trong giai đoạn hậu phẫu.
Việc quản lý bệnh nhân bị suy hô hấp thường liên quan đến việc đặt một ống vào khí quản (ống nội khí quản) và hỗ trợ trao đổi khí bằng máy thở cơ học (xem Chương 30). Ống nội khí quản gây ra một nguy cơ đáng kể về nhiễm trùng vi khuẩn đường hô hấp dưới, thường được gọi là viêm phổi liên quan đến máy thở, một phần là do ngăn cản sự đóng của thanh môn, một thành phần quan trọng của chuỗi các sự kiện dẫn đến một cơn ho hiệu quả. Ngoài ra, ống nội khí quản cung cấp một đường dẫn trực tiếp vào khí quản cho các vi khuẩn đã xâm chiếm hoặc làm ô nhiễm ống máy thở hoặc chính ống nội khí quản.
Suy giảm Chức năng của Peptide Kháng khuẩn
Có sự chồng chéo đáng kể trong chức năng của các chất kháng khuẩn có trong lớp sol. Do đó, một khiếm khuyết riêng lẻ ở bất kỳ thành phần nào cũng không có khả năng gây ra hậu quả thảm khốc. Sự thiếu hụt lysozyme có liên quan đến việc tăng nguy cơ viêm phế quản cấp do vi khuẩn. Ở những bệnh nhân bị xơ nang, hàm lượng natri và clorua cao trong dịch tiết đường hô hấp của họ dường như làm bất hoạt các defensin và góp phần vào các bệnh nhiễm trùng đường hô hấp nặng thường xảy ra. Ở động vật, các khiếm khuyết trong SP-A hoặc SP-D có liên quan đến sự gia tăng các bệnh nhiễm trùng đường hô hấp, nhưng các vấn đề tương tự ở người chưa được xác định.
Suy giảm Chức năng của Các Tế bào Thực bào và Tế bào Viêm
Các vấn đề lâm sàng phát sinh từ sự thiếu hụt về số lượng hoặc chức năng của hai loại tế bào thực bào và tế bào viêm chính: đại thực bào phế nang và PMN. Một trong những cách quan trọng hơn mà chức năng của đại thực bào có thể bị suy giảm là do nhiễm trùng đường hô hấp do virus. Những bệnh nhiễm trùng này có thể làm tê liệt khả năng của đại thực bào trong việc tiêu diệt vi khuẩn, một lý do khác tại sao bệnh nhân bị nhiễm virus dễ bị viêm phế quản hoặc viêm phổi do vi khuẩn bội nhiễm hơn. Hút thuốc lá làm suy giảm khả năng của đại thực bào phế nang trong việc hấp thu và tiêu diệt vi khuẩn. Thiếu oxy, nhiễm HIV, đói, nghiện rượu, và tiếp xúc với lạnh tương tự dường như là những tình trạng mà việc tiêu diệt vi khuẩn bị suy giảm ít nhất một phần là do chức năng của đại thực bào bị suy giảm. Điều trị bằng corticosteroid, được sử dụng cho vô số bệnh, dường như làm suy giảm sự di chuyển và chức năng của đại thực bào, và điều này có thể làm tăng thêm các tác dụng phụ của steroid đối với các tế bào lympho và hệ miễn dịch. HIV có thể lây nhiễm cho các đại thực bào phế nang, vừa đóng vai trò là ổ chứa cho các hạt virus vừa dẫn đến suy giảm chức năng của đại thực bào ở bệnh nhân AIDS, có khả năng làm phức tạp thêm các khiếm khuyết phòng vệ khác của ký chủ được ghi nhận trong bệnh (xem Chương 27).
|
Các tình huống lâm sàng có khả năng làm suy giảm chức năng đại thực bào bao gồm: 1. Nhiễm trùng đường hô hấp do virus 2. Hút thuốc lá 3. Nghiện rượu 4. Tình trạng đói 5. Tiếp xúc với lạnh 6. Thiếu oxy 7. Liệu pháp corticosteroid 8. HIV/AIDS |
PMN bị giảm số lượng trong một số trường hợp lâm sàng, thường là do bệnh tủy xương tiềm ẩn (ví dụ, bệnh bạch cầu) hoặc do phương pháp điều trị được áp dụng. Các tác nhân hóa trị liệu được sử dụng để điều trị bệnh ác tính thường phá hủy các tế bào tăng sinh nhanh của tủy xương, dẫn đến mất tạm thời các tiền chất của PMN và suy giảm rõ rệt số lượng PMN lưu hành. Khi PMN có mặt ở nồng độ thấp bất thường, nguy cơ nhiễm trùng vi khuẩn bắt đầu tăng lên, trở nên đặc biệt rõ rệt khi số lượng giảm xuống dưới . Mặc dù các bệnh nhiễm nấm cơ hội thường liên quan đến sự suy giảm miễn dịch tế bào hơn là với giảm bạch cầu trung tính, nấm Aspergillus là một tác nhân gây bệnh đường hô hấp quan trọng ở bệnh nhân giảm bạch cầu trung tính.
|
Các nguyên nhân làm giảm số lượng PMN: 1. Tủy xương bị thay thế bởi khối u 2. Các tác nhân hóa trị liệu ung thư |
Khiếm khuyết trong Hệ Miễn dịch Thích ứng
Hệ miễn dịch thích ứng có thể bị khiếm khuyết về chức năng ảnh hưởng đến các thành phần dịch thể và tế bào của nó. So với miễn dịch bẩm sinh, có ít sự dư thừa hơn nhiều trong hệ miễn dịch thích ứng, và theo nguyên tắc chung, các khiếm khuyết trong miễn dịch thích ứng dẫn đến nguy cơ nhiễm trùng lớn hơn nhiều. Sự thiếu hụt trong hệ miễn dịch dịch thể, chẳng hạn như giảm hoặc không sản xuất immunoglobulin (tức là, giảm gammaglobulin máu hoặc không có gammaglobulin máu), có liên quan đến các bệnh nhiễm trùng đường hô hấp do vi khuẩn và virus tái phát, thường dẫn đến giãn phế quản. Nguy cơ nhiễm trùng được xác định rõ nhất đối với những người bị thiếu hụt IgG hoặc immunoglobulin toàn phần. Mặc dù một số cá nhân bị thiếu hụt IgA chọn lọc dường như có nguy cơ nhiễm trùng đường hô hấp tăng lên, dù là do virus hay vi khuẩn, nguy cơ này có thể ít nhất một phần liên quan đến sự thiếu hụt đồng thời của một trong bốn phân lớp IgG được công nhận. Phần lớn bệnh nhân bị thiếu hụt IgA chọn lọc không phát triển các bệnh nhiễm trùng xoang-phổi tái phát, có lẽ là do sự dư thừa trong hệ miễn dịch.
|
Các nguyên nhân gây suy giảm miễn dịch thích ứng: 1. Dịch thể: giảm hoặc không có immunoglobulin 2. Tế bào: corticosteroid, thuốc gây độc tế bào, bệnh Hodgkin và các loại u lympho khác, HIV/AIDS |
Miễn dịch tế bào bị rối loạn thường xuyên nhất do điều trị bằng corticosteroid, các tác nhân gây độc tế bào, hoặc các loại thuốc ức chế miễn dịch khác và trong một số tình trạng bệnh được xác định rõ, chẳng hạn như u lympho Hodgkin và AIDS. Một số hội chứng suy giảm miễn dịch bẩm sinh cũng được đặc trưng bởi sự suy giảm sâu sắc trong miễn dịch tế bào. Không giống như hầu hết các thiếu hụt khác trong phòng vệ đường hô hấp, các vấn đề với miễn dịch qua trung gian tế bào có thể dẫn đến nhiễm trùng với một nhóm vi sinh vật cụ thể, bao gồm các vi khuẩn nội bào (đặc biệt là mycobacteria), nấm, Pneumocystis, và một số loại virus nhất định, đặc biệt là cytomegalovirus. Một số trong những sinh vật này, chẳng hạn như Pneumocystis và một số loại nấm, hiếm khi ảnh hưởng đến những người có miễn dịch tế bào bình thường, trong khi các sinh vật khác, chẳng hạn như M. tuberculosis, có thể ảnh hưởng đến những người không có khiếm khuyết xác định nào trong miễn dịch tế bào.
Tóm lại, các cơ chế phòng vệ có sẵn để bảo vệ đường hô hấp khỏi các vi sinh vật xâm nhập rất đa dạng và phức tạp. Các cơ chế phòng vệ này có thể bị cản trở bởi việc tiếp xúc với các ảnh hưởng gây hại, chẳng hạn như khói thuốc lá và ethanol. Điều quan trọng không kém, các phương pháp điều trị dược lý và các hình thức điều trị khác do các bác sĩ cung cấp có thể phá vỡ các cơ chế phòng vệ của ký chủ, làm cho việc các bác sĩ nhận thức được các biến chứng nhiễm trùng tiềm ẩn của liệu pháp trở nên cần thiết.
Trong bối cảnh lâm sàng, sự thiếu hụt immunoglobulin và PMN có liên quan chặt chẽ đến nguy cơ nhiễm trùng vi khuẩn tăng lên. Mặc dù các vấn đề với thanh thải nhầy-lông chuyển và chức năng đại thực bào ít được xác định rõ hơn về nguy cơ nhiễm trùng cụ thể, các bệnh nhiễm trùng vi khuẩn cũng dường như nổi bật trong những bối cảnh này. Ngược lại, các rối loạn trong miễn dịch tế bào được đặc trưng bởi nguy cơ tăng lên của một tập hợp con các bệnh nhiễm trùng khác, đặc biệt là những bệnh do mycobacteria, Pneumocystis, nấm, và một số loại virus nhất định gây ra.
TĂNG CƯỜNG CÁC CƠ CHẾ PHÒNG VỆ ĐƯỜNG HÔ HẤP
Quan trọng là, có những cơ hội đáng kể để tăng cường các cơ chế phòng vệ và bảo vệ chống lại một số hình thức nhiễm trùng đường hô hấp. Tiêm chủng chống lại một số tác nhân gây bệnh đường hô hấp đã tạo ra việc sản xuất kháng thể chống lại các sinh vật và đã mang lại sự bảo vệ tương đối hoặc hoàn toàn chống lại sự lây nhiễm của các vi khuẩn này.
Có lẽ những ví dụ đáng chú ý nhất là tiêm chủng chống lại SARS-CoV-2 (gây ra bệnh COVID-19), virus cúm, và nhiều phân nhóm của vi khuẩn phổ biến Streptococcus pneumoniae (phế cầu khuẩn) cũng như độc tố của Bordetella pertussis (gây ra bệnh ho gà). Tiêm chủng thích hợp là rất quan trọng đối với bất kỳ bệnh nhân nào có tình trạng bệnh nền làm tăng nguy cơ mắc bệnh nặng. Tại thời điểm xuất bản, việc tiêm vắc-xin SARS-CoV-2 được khuyến nghị cho tất cả các cá nhân từ 5 tuổi trở lên. Tiêm chủng toàn dân chống ho gà được khuyến nghị trong thời thơ ấu và một liều nhắc lại được khuyến nghị cho tất cả người lớn. Tiêm vắc-xin cúm hàng năm được chỉ định cho tất cả các cá nhân từ 6 tháng tuổi trở lên. Tiêm vắc-xin phế cầu khuẩn hiện được khuyến nghị rộng rãi cho cả trẻ nhỏ và người lớn trên 65 tuổi. Tiêm vắc-xin phế cầu khuẩn cũng được khuyến nghị cho những người ngoài các nhóm tuổi đó có nguy cơ cao mắc bệnh phế cầu khuẩn xâm lấn.
TÀI LIỆU THAM KHẢO ĐỀ XUẤT
Phòng thủ Vật chủ Phổi
Burgoyne, R. A., Fisher, A. J., & Borthwick, L. A. (2021). The role of epithelial damage in the pulmonary immune response. Cells, 10, 2763.
Byrne, A. J., Mathie, S. A., Gregory, L. G., & Lloyd, C. M. (2015). Pulmonary macrophages: Key players in the innate defence of the airways. Thorax, 70, 1189–1196.
Carlier, F. M., de Fays, C., & Pilette, C. (2021). Epithelial barrier dysfunction in chronic respiratory diseases. Frontiers in Physiology, 12, 691227.
Horani, A., & Ferkol, T. W. (2021). Understanding primary ciliary dyskinesia and other ciliopathies. Journal of Pediatric, 230, 15–22.e1.
Janssen, W. J., Stefanski, A. L., Bochner, B. S., & Evans, C. M. (2016). Control of lung defence by mucins and macrophages: Ancient defence mechanisms with modern functions. European Respiratory Journal, 48, 1201–1214.
Johnston, S. L., Goldblatt, D. L., Evans, S. E., Tuvim, M. J., & Dickey, B. F. (2021). Airway epithelial innate immunity. Frontiers in Physiology, 12, 749077.
Lugg, S. T., Scott, A., Parekh, D., Naidu, B., & Thickett, D. R. (2022). Cigarette smoke exposure and alveolar macrophages: Mechanisms for lung disease. Thorax, 77, 94–101.
Quinton, L. J., Walkey, A. J., & Mizgerd, J. P. (2018). Integrative physiology of pneumonia. Physiological Reviews, 98, 1417–1464.
Shotland, A. M., Fontenot, A. P., & McKee, A. S. (2021). Pulmonary macrophage cell death in lung health and disease. American Journal of Respiratory Cell and Molecular Biology, 64, 547–556.
Wallmeier, J., Nielsen, K. G., Kuehni, C. E., Lucas, J. S., Leigh, M. W., Zariwala, M. A., et al. (2020). Motile ciliopathies. Nature Reviews Disease Primers, 6, 77.
Watson, A., Madsen, J., & Clark, H. W. (2021). SP-A and SP-D: Dual functioning immune molecules with antiviral and immunomodulatory properties. Frontiers in Immunology, 11, 622598.
Upham, J. W., & Xi, Y. (2017). Dendritic cells in human lung disease: Recent advances. Chest, 151, 668–673.
Zhang, H., He, F., Li, P., Hardwidge, P. R., Li, N., & Peng, Y. (2021). The role of innate immunity in pulmonary infections. BioMed Research International, 2021, 6646071.
Tăng cường Cơ chế Bảo vệ Hô hấp
Centers for Disease Control and Prevention (CDC). (2021). Prevention and control of seasonal influenza with vaccines: Recommendations of the Advisory Committee on Immunization Practices — United States, 2021-22 influenza season. MMWR, 70(RR-5), 1–28.
Castells, M. C., & Phillips, E. J. (2021). Maintaining safety with SARS-CoV-2 vaccines. New England Journal of Medicine, 384, 643–649.
Murthy, N., Wodi, A. P., Bernstein, H., Ault K. A., Advisory Committee on Immunization Practices, & Advisory Committee on Immunization Practices. (2022). Advisory Committee on Immunization Practices. Recommended adult immunization schedule, United States, 2022. Annals of Internal Medicine, 175, 432–443.
Scelfo, C., Menzella, F., Fontana, M., Ghidoni, G., Galeone, C., & Facciolongo, N. C. (2021). Pneumonia and invasive pneumococcal diseases: The role of pneumococcal conjugate vaccine in the era of multi-drug resistance. Vaccines (Basel), 9, 420.
Treanor, J. J. (2016). Influenza vaccination. New England Journal of Medicine, 375, 1261–1268.
BẢNG CHÚ GIẢI THUẬT NGỮ Y HỌC ANH – VIỆT
CHƯƠNG 22. Các Cơ chế Phòng vệ của Phổi
| STT | Thuật ngữ tiếng Anh | Phiên âm | Nghĩa tiếng Việt |
|---|---|---|---|
| 1 | Lung Defense Mechanisms | /lʌŋ dɪˈfens ˈmekəˌnɪzəmz/ | Cơ chế bảo vệ phổi |
| 2 | Physical clearance | /ˈfɪzɪkəl ˈklɪrəns/ | Thanh thải vật lý |
| 3 | Antimicrobial peptides | /ˌæntɪmaɪˈkroʊbiəl ˈpeptaɪdz/ | Peptide kháng khuẩn |
| 4 | Phagocytic cells | /ˌfæɡəˈsɪtɪk selz/ | Tế bào thực bào |
| 5 | Inflammatory cells | /ɪnˈflæməˌtɔri selz/ | Tế bào viêm |
| 6 | Pulmonary alveolar macrophages | /ˈpʌlməˌneri ælˈviələr ˈmækrəˌfeɪdʒəz/ | Đại thực bào phế nang |
| 7 | Dendritic cells | /denˈdrɪtɪk selz/ | Tế bào cây |
| 8 | Polymorphonuclear leukocytes | /ˌpɑliˌmɔrfoʊˈnukliər ˈlukəˌsaɪts/ | Bạch cầu đa nhân |
| 9 | Natural killer cells | /ˈnætʃərəl ˈkɪlər selz/ | Tế bào diệt tự nhiên |
| 10 | Adaptive immune responses | /əˈdæptɪv ɪˈmjun rɪˈspɑnsəz/ | Đáp ứng miễn dịch thích ứng |
| 11 | Humoral immune mechanisms | /ˈhjuməral ɪˈmjun ˈmekəˌnɪzəmz/ | Cơ chế miễn dịch thể dịch |
| 12 | Cellular immune mechanisms | /ˈseljələr ɪˈmjun ˈmekəˌnɪzəmz/ | Cơ chế miễn dịch tế bào |
| 13 | Respiratory tract | /ˈrespərəˌtɔri trækt/ | Đường hô hấp |
| 14 | Tracheobronchial tree | /ˌtreɪkioʊˈbrɑŋkiəl tri/ | Cây khí phế quản |
| 15 | Alveolar spaces | /ælˈviələr ˈspeɪsəz/ | Khoang phế nang |
| 16 | Microorganisms | /ˌmaɪkroʊˈɔrɡəˌnɪzəmz/ | Vi sinh vật |
| 17 | Particulate material | /pərˈtɪkjələt məˈtɪriəl/ | Vật chất hạt |
| 18 | Noxious gases | /ˈnɑkʃəs ˈɡæsəz/ | Khí độc hại |
| 19 | Oropharynx | /ˌɔroʊˈfærɪŋks/ | Hầu họng |
| 20 | Aspirated secretions | /ˈæspəˌreɪtəd sɪˈkriʃənz/ | Chất tiết hít phải |
| 21 | Airways | /ˈerˌweɪz/ | Đường thở |
| 22 | Lung parenchyma | /lʌŋ pəˈreŋkəmə/ | Nhu mô phổi |
| 23 | Host defense system | /hoʊst dɪˈfens ˈsɪstəm/ | Hệ thống phòng thủ vật chủ |
| 24 | Infectious agents | /ɪnˈfekʃəs ˈeɪdʒənts/ | Tác nhân nhiễm trùng |
| 25 | Virulent organism | /ˈvɪrjələnt ˈɔrɡəˌnɪzəm/ | Sinh vật độc lực |
| 26 | Immune system | /ɪˈmjun ˈsɪstəm/ | Hệ miễn dịch |
| 27 | Respiratory infection | /ˈrespərəˌtɔri ɪnˈfekʃən/ | Nhiễm trùng hô hấp |
| 28 | Respiratory pathogens | /ˈrespərəˌtɔri ˈpæθədʒənz/ | Tác nhân gây bệnh hô hấp |
| 29 | Particle size | /ˈpɑrtɪkəl saɪz/ | Kích thước hạt |
| 30 | Deposition | /ˌdepəˈzɪʃən/ | Lắng đọng |
| 31 | Laminar flow | /ˈlæmənər floʊ/ | Dòng chảy tầng |
| 32 | Turbulent flow | /ˈtɜrbjələnt floʊ/ | Dòng chảy rối |
| 33 | Branch points | /bræntʃ pɔɪnts/ | Điểm phân nhánh |
| 34 | Subcarinae | /sʌbkəˈraɪni/ | Dưới chỗ chia |
| 35 | Bronchial mucosal surfaces | /ˈbrɑŋkiəl mjuˈkoʊsəl ˈsɜrfəsəz/ | Bề mặt niêm mạc phế quản |
| 36 | Upper airway | /ˈʌpər ˈerˌweɪ/ | Đường thở trên |
| 37 | Trachea | /ˈtreɪkiə/ | Khí quản |
| 38 | Conducting airways | /kənˈdʌktɪŋ ˈerˌweɪz/ | Đường thở dẫn truyền |
| 39 | Small airways | /smɔl ˈerˌweɪz/ | Đường thở nhỏ |
| 40 | Alveoli | /ælˈviəˌlaɪ/ | Phế nang |
| 41 | Bacteria | /bækˈtɪriə/ | Vi khuẩn |
| 42 | Lower respiratory tract | /ˈloʊər ˈrespərəˌtɔri trækt/ | Đường hô hấp dưới |
| 43 | Bronchodilators | /ˌbrɑŋkoʊˈdaɪleɪtərz/ | Thuốc giãn phế quản |
| 44 | Cough | /kɔf/ | Ho |
| 45 | Mucociliary transport | /ˌmjukoʊˈsɪliˌeri ˈtrænspɔrt/ | Vận chuyển niêm mao |
| 46 | Irritant receptors | /ˈɪrətənt rɪˈseptərz/ | Thụ thể kích thích |
| 47 | Proximal airways | /ˈprɑksəməl ˈerˌweɪz/ | Đường thở gần |
| 48 | Foreign material | /ˈfɔrən məˈtɪriəl/ | Vật chất lạ |
| 49 | Flow rates | /floʊ reɪts/ | Tốc độ dòng chảy |
| 50 | Mucociliary clearance | /ˌmjukoʊˈsɪliˌeri ˈklɪrəns/ | Thanh thải niêm mao |
| 51 | Cilia | /ˈsɪliə/ | Lông mao |
| 52 | Respiratory bronchioles | /ˈrespərəˌtɔri ˈbrɑŋkiˌoʊlz/ | Tiểu phế quản hô hấp |
| 53 | Epithelial cells | /ˌepəˈθiliəl selz/ | Tế bào biểu mô |
| 54 | Airway lumen | /ˈerˌweɪ ˈlumən/ | Lòng đường thở |
| 55 | Microtubules | /ˈmaɪkroʊˌtjubz/ | Vi ống |
| 56 | Cross-sectional view | /krɔs ˈsekʃənəl vju/ | Cái nhìn cắt ngang |
| 57 | Central microtubules | /ˈsentrəl ˈmaɪkroʊˌtjubz/ | Vi ống trung tâm |
| 58 | Peripheral microtubules | /pəˈrɪfərəl ˈmaɪkroʊˌtjubz/ | Vi ống chu vi |
| 59 | Dynein arms | /ˈdaɪniɪn ɑrmz/ | Cánh tay dynein |
| 60 | Contractile function | /kənˈtræktaɪl ˈfʌŋkʃən/ | Chức năng co bóp |
| 61 | Ciliary motion | /ˈsɪliˌeri ˈmoʊʃən/ | Chuyển động lông mao |
| 62 | Coordinated movement | /koʊˈɔrdəˌneɪtəd ˈmuvmənt/ | Chuyển động phối hợp |
| 63 | Wavelike motion | /ˈweɪvˌlaɪk ˈmoʊʃən/ | Chuyển động giống sóng |
| 64 | Mucous layer | /ˈmjukəs ˈleɪər/ | Lớp niêm |
| 65 | Cephalad direction | /ˈsefələd dəˈrekʃən/ | Hướng đầu |
| 66 | Inhaled particles | /ɪnˈheɪld ˈpɑrtɪkəlz/ | Hạt hít vào |
| 67 | Expectorated | /ɪkˈspektəˌreɪtəd/ | Khạc ra |
| 68 | Swallowed | /ˈswɑloʊd/ | Nuốt |
| 69 | Mucous blanket | /ˈmjukəs ˈblæŋkət/ | Tấm niêm |
| 70 | Sol layer | /sɔl ˈleɪər/ | Lớp sol |
| 71 | Aqueous sol layer | /ˈeɪkwiəs sɔl ˈleɪər/ | Lớp sol nước |
| 72 | Innate immune system | /ɪˈneɪt ɪˈmjun ˈsɪstəm/ | Hệ miễn dịch bẩm sinh |
| 73 | Gel layer | /dʒel ˈleɪər/ | Lớp gel |
| 74 | Viscous gel layer | /ˈvɪskəs dʒel ˈleɪər/ | Lớp gel nhớt |
| 75 | Submucosal mucous glands | /sʌbmjuˈkoʊsəl ˈmjukəs ɡlændz/ | Tuyến niêm dưới niêm mạc |
| 76 | Goblet cells | /ˈɡɑblət selz/ | Tế bào chén |
| 77 | Fast-acting system | /fæst ˈæktɪŋ ˈsɪstəm/ | Hệ thống tác động nhanh |
| 78 | Prior sensitization | /ˈpraɪər ˌsensətəˈzeɪʃən/ | Nhạy hóa trước |
| 79 | Small molecules | /smɔl ˈmɑləˌkjulz/ | Phân tử nhỏ |
| 80 | Proteins | /ˈproʊˌtinz/ | Protein |
| 81 | Pattern recognition receptors | /ˈpætərn ˌrekəɡˈnɪʃən rɪˈseptərz/ | Thụ thể nhận biết mẫu |
| 82 | Conserved structures | /kənˈsɜrvd ˈstrʌktʃərz/ | Cấu trúc được bảo tồn |
| 83 | Microbes | /ˈmaɪkroʊbz/ | Vi khuẩn |
| 84 | Host immune response | /hoʊst ɪˈmjun rɪˈspɑns/ | Đáp ứng miễn dịch vật chủ |
| 85 | Energy-efficient | /ˈenərdʒi ɪˈfɪʃənt/ | Hiệu quả năng lượng |
| 86 | Frontline defense | /ˈfrʌntˌlaɪn dɪˈfens/ | Phòng thủ tuyến đầu |
| 87 | Broad overlap | /brɔd ˈoʊvərˌlæp/ | Chồng chéo rộng |
| 88 | Components | /kəmˈpoʊnənts/ | Thành phần |
| 89 | Naturally occurring | /ˈnætʃərəli əˈkɜrɪŋ/ | Xuất hiện tự nhiên |
| 90 | Lysozyme | /ˈlaɪsəˌzaɪm/ | Lysozyme |
| 91 | Lactoferrin | /ˌlæktoʊˈferɪn/ | Lactoferrin |
| 92 | Defensins | /dɪˈfensɪnz/ | Defensin |
| 93 | Collectins | /kəˈlektɪnz/ | Collectin |
| 94 | Surfactant protein A | /ˈsɜrfəktənt ˈproʊˌtin eɪ/ | Protein surfactant A |
| 95 | Surfactant protein D | /ˈsɜrfəktənt ˈproʊˌtin di/ | Protein surfactant D |
| 96 | Immunoglobulin A | /ˌɪmjənoʊˈɡlɑbjələn eɪ/ | Immunoglobulin A |
| 97 | Respiratory epithelial cells | /ˈrespərəˌtɔri ˌepəˈθiliəl selz/ | Tế bào biểu mô hô hấp |
| 98 | Serous glandular cells | /ˈsɪriəs ˈɡlændjələr selz/ | Tế bào tuyến huyết thanh |
| 99 | Macrophages | /ˈmækrəˌfeɪdʒəz/ | Đại thực bào |
| 100 | Bacterial cell death | /bækˈtɪriəl sel deθ/ | Chết tế bào vi khuẩn |
| 101 | Lysis | /ˈlaɪsəs/ | Ly giải |
| 102 | Gram-positive organisms | /ɡræm ˈpɑzətɪv ˈɔrɡəˌnɪzəmz/ | Sinh vật Gram dương |
| 103 | Acute bronchitis | /əˈkjut brɑŋˈkaɪtəs/ | Viêm phế quản cấp tính |
| 104 | Airway fluid | /ˈerˌweɪ ˈfluəd/ | Dịch đường thở |
| 105 | Serous cells | /ˈsɪriəs selz/ | Tế bào huyết thanh |
| 106 | Neutrophils | /ˈnutrəˌfɪlz/ | Bạch cầu trung tính |
| 107 | Agglutinate | /əˈɡlutəˌneɪt/ | Kết tụ |
| 108 | Neutrophil adherence | /ˈnutrəˌfɪl ædˈhɪrəns/ | Sự bám dính bạch cầu trung tính |
| 109 | Superoxide production | /ˈsupərˌɑksaɪd prəˈdʌkʃən/ | Sản xuất superoxide |
| 110 | Bacterial metabolism | /bækˈtɪriəl məˈtæbəˌlɪzəm/ | Quá trình trao đổi chất vi khuẩn |
| 111 | Carbohydrate moieties | /ˌkɑrboʊˈhaɪdreɪt ˈmɔɪətiz/ | Nhóm carbohydrate |
| 112 | Microbial cell surface | /maɪˈkroʊbiəl sel ˈsɜrfəs/ | Bề mặt tế bào vi khuẩn |
| 113 | Family of small proteins | /ˈfæməli ʌv smɔl ˈproʊˌtinz/ | Họ protein nhỏ |
| 114 | Intrinsic antimicrobial activity | /ɪnˈtrɪnzɪk ˌæntɪmaɪˈkroʊbiəl ækˈtɪvəti/ | Hoạt tính kháng khuẩn nội tại |
| 115 | Mucosal surfaces | /mjuˈkoʊsəl ˈsɜrfəsəz/ | Bề mặt niêm mạc |
| 116 | Gastrointestinal tract | /ˌɡæstroʊɪnˈtestənəl trækt/ | Đường tiêu hóa |
| 117 | Reproductive tracts | /ˌriprəˈdʌktɪv trækts/ | Đường sinh sản |
| 118 | Alpha-defensins | /ˈælfə dɪˈfensɪnz/ | Alpha-defensin |
| 119 | Beta-defensins | /ˈbeɪtə dɪˈfensɪnz/ | Beta-defensin |
| 120 | Resident neutrophils | /ˈrezədənt ˈnutrəˌfɪlz/ | Bạch cầu trung tính thường trú |
| 121 | Gram-negative organisms | /ɡræm ˈneɡətɪv ˈɔrɡəˌnɪzəmz/ | Sinh vật Gram âm |
| 122 | Microbial cell wall | /maɪˈkroʊbiəl sel wɔl/ | Thành tế bào vi khuẩn |
| 123 | Permeable | /ˈpɜrmiəbəl/ | Thấm được |
| 124 | Cell contents | /sel ˈkɑntents/ | Nội dung tế bào |
| 125 | Membrane potential | /ˈmemˌbreɪn pəˈtenʃəl/ | Điện thế màng |
| 126 | Ionic concentrations | /aɪˈɑnɪk ˌkɑnsənˈtreɪʃənz/ | Nồng độ ion |
| 127 | Abnormal milieu | /æbˈnɔrməl mɪˈlju/ | Môi trường bất thường |
| 128 | Cystic fibrosis | /ˈsɪstɪk faɪˈbroʊsəs/ | Xơ nang |
| 129 | Collectin family | /kəˈlektɪn ˈfæməli/ | Họ collectin |
| 130 | Antimicrobial function | /ˌæntɪmaɪˈkroʊbiəl ˈfʌŋkʃən/ | Chức năng kháng khuẩn |
| 131 | Binding and aggregating | /ˈbaɪndɪŋ ænd ˈæɡrəˌɡeɪtɪŋ/ | Liên kết và kết tụ |
| 132 | Phagocytic cells | /ˌfæɡəˈsɪtɪk selz/ | Tế bào thực bào |
| 133 | Pulmonary macrophage activity | /ˈpʌlməˌneri ˈmækrəˌfeɪdʒ ækˈtɪvəti/ | Hoạt động đại thực bào phổi |
| 134 | Cytokine production | /ˈsaɪtoʊˌkaɪn prəˈdʌkʃən/ | Sản xuất cytokine |
| 135 | Animal models | /ˈænəməl ˈmɑdəlz/ | Mô hình động vật |
| 136 | Susceptibility | /səˌseptəˈbɪləti/ | Tính nhạy cảm |
| 137 | Respiratory IgA | /ˈrespərəˌtɔri aɪ dʒi eɪ/ | IgA hô hấp |
| 138 | Constitutively produced | /ˈkɑnstəˌtutɪvli prəˈdust/ | Sản xuất liên tục |
| 139 | Respiratory epithelium | /ˈrespərəˌtɔri ˌepəˈθiliəm/ | Biểu mô hô hấp |
| 140 | Prior exposure | /ˈpraɪər ɪkˈspoʊʒər/ | Tiếp xúc trước |
| 141 | Mononuclear phagocytic cells | /ˌmɑnoʊˈnukliər ˌfæɡəˈsɪtɪk selz/ | Tế bào thực bào đơn nhân |
| 142 | Scavenged | /ˈskævəndʒd/ | Thu gom |
| 143 | Intrathoracic airways | /ˌɪntrəθəˈræsɪk ˈerˌweɪz/ | Đường thở trong lồng ngực |
| 144 | Alveolar structures | /ælˈviələr ˈstrʌktʃərz/ | Cấu trúc phế nang |
| 145 | Large mobile cells | /lɑrdʒ ˈmoʊbəl selz/ | Tế bào di động lớn |
| 146 | Diameter | /daɪˈæmətər/ | Đường kính |
| 147 | Circulating monocytes | /ˈsɜrkjəˌleɪtɪŋ ˈmɑnoʊˌsaɪts/ | Tế bào đơn nhân tuần hoàn |
| 148 | Bone marrow | /boʊn ˈmæroʊ/ | Tủy xương |
| 149 | Alveolar epithelium | /ælˈviələr ˌepəˈθiliəm/ | Biểu mô phế nang |
| 150 | Cytoplasm | /ˈsaɪtəˌplæzəm/ | Tế bào chất |
| 151 | Granules | /ˈɡrænjulz/ | Hạt |
| 152 | Digestive enzymes | /daɪˈdʒestɪv ˈenzaɪmz/ | Enzyme tiêu hóa |
| 153 | Ingested foreign material | /ɪnˈdʒestəd ˈfɔrən məˈtɪriəl/ | Vật chất lạ đã ăn vào |
| 154 | Chemoattractant cytokines | /ˌkimoʊəˈtræktənt ˈsaɪtoʊˌkaɪnz/ | Cytokine hóa hướng động |
| 155 | Chemokines | /ˈkimoʊˌkaɪnz/ | Chemokine |
| 156 | Recruit | /rɪˈkrut/ | Tuyển mộ, huy động |
| 157 | Attachment | /əˈtætʃmənt/ | Gắn kết |
| 158 | Processing sequence | /ˈprɑsesɪŋ ˈsikwəns/ | Chuỗi xử lý |
| 159 | Engulfed | /ɪnˈɡʌlft/ | Nuốt chửng |
| 160 | Plasma membrane | /ˈplæzmə ˈmemˌbreɪn/ | Màng tế bào chất |
| 161 | Invaginates | /ɪnˈvædʒəˌneɪts/ | Lõm vào |
| 162 | Pinches off | /ˈpɪntʃəz ɔf/ | Tách ra |
| 163 | Cytoplasmic phagosome | /ˌsaɪtəˈplæzmɪk ˈfæɡəˌsoʊm/ | Phagosome tế bào chất |
| 164 | Isolated foreign material | /ˈaɪsəˌleɪtəd ˈfɔrən məˈtɪriəl/ | Vật chất lạ bị cô lập |
| 165 | Phagocytosis | /ˌfæɡoʊsaɪˈtoʊsəs/ | Thực bào |
| 166 | Opsonins | /ˈɑpsəˌnɪnz/ | Opsonin |
| 167 | Coat | /koʊt/ | Bao phủ |
| 168 | Extracellular materials | /ˌekstrəˈseljələr məˈtɪriəlz/ | Vật chất ngoại bào |
| 169 | Adherent | /ædˈhɪrənt/ | Bám dính |
| 170 | Amenable to engulfment | /əˈminəbəl tu ɪnˈɡʌlfmənt/ | Dễ nuốt chửng |
| 171 | Ingestion | /ɪnˈdʒestʃən/ | Ăn vào |
| 172 | Specific opsonins | /spəˈsɪfɪk ˈɑpsəˌnɪnz/ | Opsonin đặc hiệu |
| 173 | Antibodies | /ˈæntɪˌbɑdiz/ | Kháng thể |
| 174 | Antigenic material | /ˌæntəˈdʒenɪk məˈtɪriəl/ | Vật chất kháng nguyên |
| 175 | Nonspecific binding | /ˌnɑnspəˈsɪfɪk ˈbaɪndɪŋ/ | Liên kết không đặc hiệu |
| 176 | IgG class | /aɪ dʒi dʒi klæs/ | Lớp IgG |
| 177 | Antigenic foreign material | /ˌæntəˈdʒenɪk ˈfɔrən məˈtɪriəl/ | Vật chất lạ kháng nguyên |
| 178 | Antigenic particles | /ˌæntəˈdʒenɪk ˈpɑrtɪkəlz/ | Hạt kháng nguyên |
| 179 | Nonspecific opsonins | /ˌnɑnspəˈsɪfɪk ˈɑpsəˌnɪnz/ | Opsonin không đặc hiệu |
| 180 | Secretory IgA | /sɪˈkritəri aɪ dʒi eɪ/ | IgA tiết |
| 181 | Complement | /ˈkɑmpləmənt/ | Complement |
| 182 | Fibronectin | /ˌfaɪbroʊˈnektɪn/ | Fibronectin |
| 183 | Promote attachment | /prəˈmoʊt əˈtætʃmənt/ | Thúc đẩy gắn kết |
