SÁCH DỊCH “Y HỌC CHU PHẪU: QUẢN LÝ HƯỚNG ĐẾN KẾT QUẢ, ẤN BẢN THỨ 2”
Được dịch và chuyển thể sang tiếng Việt từ sách gốc “Perioperative Medicine: Managing for Outcome, 2nd Edition”
Dịch và chú giải: Ths.Bs. Lê Đình Sáng – Hiệu đính: Ts.Bs.Lê Nhật Huy
Chương 7. Đánh giá Nguy cơ Hệ Thần kinh Trung ương: Phòng ngừa Tổn thương Não sau Phẫu thuật
Central Nervous System Risk Assessment: Preventing Postoperative Brain Injury
MEGAN MAXWELL, MEGHAN MICHAEL, and DAVID L. MCDONAGH
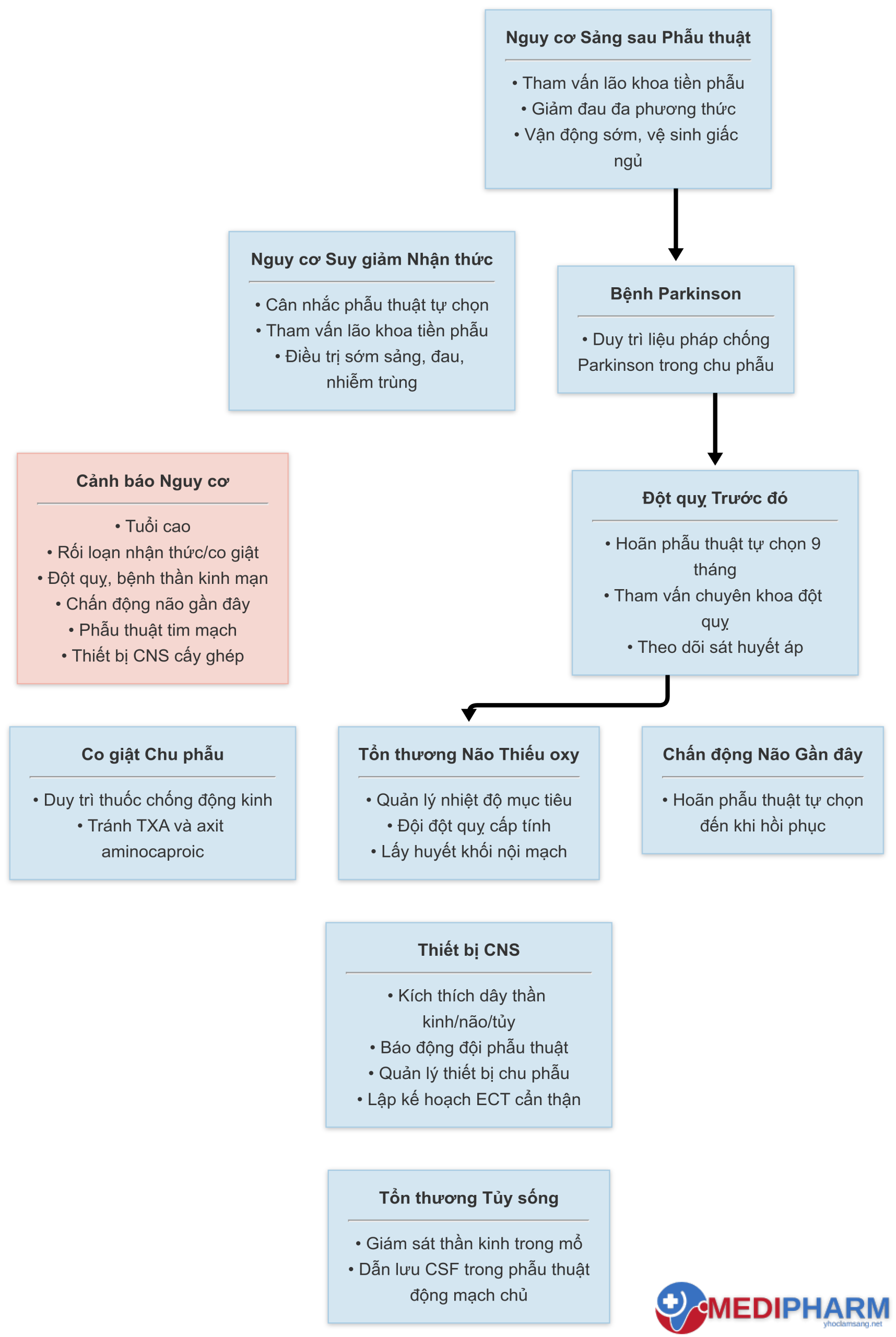
Các biến chứng chu phẫu liên quan đến hệ thần kinh trung ương (CNS) là phổ biến. Tuy nhiên, những vấn đề này thường ít được chú ý trong quá trình đánh giá tiền phẫu. Dữ liệu mới cho phép chúng ta hướng dẫn tốt hơn cho bác sĩ và người bệnh về nguy cơ CNS chu phẫu và các cách để giảm thiểu nguy cơ đó (Hình 7.1).

Hình 7.1: Khuyến nghị quản lý các tình trạng hệ thần kinh trung ương có nguy cơ.
Sảng sau Phẫu thuật
ĐỊNH NGHĨA
Sảng sau phẫu thuật (POD) là một hội chứng lú lẫn cấp tính thường gặp trong môi trường hậu phẫu. Thực tế, đây là biến chứng phẫu thuật phổ biến nhất ở người cao tuổi, với tỷ lệ mắc từ 15% đến 50% ở dân số này, tùy thuộc vào thủ thuật. Sảng có thể được định nghĩa là một rối loạn cấp tính, dao động, đa yếu tố đặc trưng bởi sự suy giảm chú ý, nhận thức và ý thức, và nó là một rối loạn riêng biệt tách biệt với sa sút trí tuệ hoặc suy giảm nhận thức mạn tính. Có ba phân nhóm sảng: tăng động, giảm động và hỗn hợp.
Mặc dù sảng giảm động là phân nhóm phổ biến nhất, những người bệnh bị sảng giảm động ít được chẩn đoán hơn và có tiên lượng kém hơn so với những người bị sảng tăng động. Đáng tiếc, chẩn đoán sảng mang đến nhiều hệ quả cho người bệnh vì những người được chẩn đoán sảng có tăng tỷ lệ bệnh tật, tử vong, mất độc lập, khả năng phải vào viện sau đó và chi phí chăm sóc sức khỏe tăng.
Việc thiết lập chẩn đoán sảng đòi hỏi phải xác định trạng thái tâm thần nền của người bệnh bằng sàng lọc tiền phẫu hoặc thông qua một người cung cấp thông tin có hiểu biết. Sau khi xác định điều này, có thể sử dụng xét nghiệm sàng lọc nhận thức để xác định sự thay đổi, nếu có, so với trạng thái nền của người bệnh. Có nhiều công cụ chẩn đoán và thang đo mức độ nghiêm trọng khác nhau cho sảng, với hai công cụ phổ biến nhất là Phương pháp Đánh giá Lú lẫn (CAM) và CAM-ICU, một dẫn xuất của CAM dành cho người bệnh thở máy trong đơn vị chăm sóc tích cực (ICU) (Hình 7.2).
Hình 7.2: Phương pháp đánh giá lú lẫn để chẩn đoán sảng trong đơn vị chăm sóc tích cực (CAM-ICU).
YẾU TỐ NGUY CƠ
Cơ chế bệnh sinh cơ bản của sảng chưa được hiểu rõ và có thể bao gồm mất cân bằng chất dẫn truyền thần kinh và/hoặc viêm thần kinh. Mặc dù thiếu nguyên nhân xác định của sảng, nhiều yếu tố tiên phát và thúc đẩy gây sảng đã được làm sáng tỏ (Bảng 7.1). Tổng hợp các yếu tố tiên phát và thúc đẩy sẽ xác định khả năng phát triển sảng của người bệnh; gánh nặng cao của các yếu tố tiên phát sẽ cần ít yếu tố thúc đẩy hơn. Nhiều loại thuốc đã được chứng minh làm tăng khả năng sảng ở người cao tuổi và nên tránh trong giai đoạn chu phẫu nếu có thể. Những thuốc này bao gồm benzodiazepine, thuốc kháng cholinergic, diphenhydramine, hydroxyzine, meperidine, thuốc đối kháng histamine-2 và thuốc an thần gây ngủ.
QUẢN LÝ TRONG KHI MỔ
Hiện tại, quản lý tối ưu trong khi mổ cho người bệnh có nguy cơ sảng vẫn chưa được xác định rõ. Các biện pháp can thiệp giảm sảng trong khi mổ duy nhất có khuyến nghị mạnh là tránh sử dụng các thuốc tiên phát và kiểm soát đau đầy đủ, với thuốc không opioid và gây tê vùng là một lựa chọn khi có thể hoặc phù hợp. Tuy nhiên, một số biện pháp can thiệp hiện đang được nghiên cứu. Một số nghiên cứu đã chỉ ra rằng mức độ gây mê sâu hơn có liên quan đến tăng tỷ lệ POD và gây mê có hướng dẫn bằng chỉ số bispectral (BIS) có liên quan đến tỷ lệ POD thấp hơn. Người ta đã đưa ra giả thuyết rằng gây mê có hướng dẫn BIS có thể có ít thời kỳ ức chế đột phát điện não đồ (EEG). Tuy nhiên, gánh nặng tăng của ức chế đột phát và các mẫu EEG khác được xác định ở người bệnh có POD có thể chỉ đơn giản là một dấu hiệu của sự mong manh chứ không phải là một yếu tố nguyên nhân. Thử nghiệm ngẫu nhiên lớn nhất cho đến nay, thử nghiệm ENGAGES [Hướng dẫn gây mê bằng điện não đồ], đã ngẫu nhiên hóa hơn 1200 người bệnh để gây mê có hướng dẫn EEG hoặc đối chứng và không tìm thấy sự khác biệt về tỷ lệ POD. Các nghiên cứu khác đang tiếp tục.
Một biện pháp can thiệp khác đã được nghiên cứu trong những năm gần đây là sử dụng dexmedetomidine. Các nghiên cứu gần đây đã chỉ ra rằng dexmedetomidine được sử dụng trong chu phẫu như một liệu pháp truyền liều thấp dự phòng có thể làm giảm không chỉ POD mà còn tỷ lệ đột quỵ và cả tỷ lệ tử vong trong và sau phẫu thuật. Những phát hiện này có thể được giải thích một phần bởi bằng chứng cho thấy dexmedetomidine hoạt động thông qua con đường JAK2/STAT3 để làm giảm thiểu thiếu hụt thần kinh nhận thức do isoflurane gây ra ở chuột già. Tuy nhiên, các nghiên cứu khác không thể lặp lại những phát hiện này và thấy rằng dexmedetomidine không làm giảm POD. Một báo cáo gần đây cho thấy dexmedetomidine liều thấp ban đêm làm giảm POD trong ICU, nhưng điều này cần được xác nhận trong các thử nghiệm lớn hơn. Vì dữ liệu còn mâu thuẫn vào thời điểm này, sẽ hợp lý nếu bác sĩ gây mê xem xét việc sử dụng dexmedetomidine trong chu phẫu ở người bệnh có nguy cơ nếu được xem là khả thi/phù hợp về mặt lâm sàng. Vẫn chưa rõ liệu liều lượng trong khi mổ, sau mổ, hay kết hợp là hiệu quả nhất.
Giống như dexmedetomidine, ketamine đã cho thấy triển vọng ban đầu như một biện pháp can thiệp trong khi mổ để ngăn ngừa POD. Tuy nhiên, một nghiên cứu gần đây không thể lặp lại kết quả này, và người bệnh nhận ketamine đã trải qua tỷ lệ ảo giác và ác mộng cao hơn (nhưng không phải sảng). Mặc dù ketamine có lợi ích trong việc giảm sảng ở trẻ em, vẫn còn tương đối ít nghiên cứu xem xét ketamine trong phòng ngừa sảng ở người lớn. Ketamine có thể cho phép sử dụng liều opioid chu phẫu thấp hơn, và bác sĩ gây mê vẫn có thể xem xét sử dụng ketamine ở người bệnh có nguy cơ như một phần của gây mê đa phương thức.
Cuối cùng, cả thuốc ức chế cholinesterase như rivastigmine và thuốc chống loạn thần như haloperidol được sử dụng trong chu phẫu với khả năng phòng ngừa đã được nghiên cứu. Thuốc ức chế cholinesterase không làm giảm tỷ lệ sảng và hơn nữa có thể liên quan đến tăng tác dụng phụ, bao gồm tử vong. Không khuyến nghị người bệnh không dùng thuốc ức chế cholinesterase tiền phẫu bắt đầu dùng một loại trong môi trường chu phẫu. Dữ liệu về sử dụng thuốc chống loạn thần dự phòng chu phẫu ít kết luận hơn nhưng nói chung không ủng hộ việc sử dụng chúng, do kết quả hỗn hợp về phòng ngừa sảng, không giảm tỷ lệ tử vong và tỷ lệ tác dụng phụ cao.
Sảng Tỉnh
Sảng tỉnh là một hiện tượng cấp tính, ngắn hạn xảy ra trong giai đoạn hậu phẫu sớm/ngay lập tức sau khi người bệnh tỉnh dậy. Những người bệnh này trải qua sự suy giảm ý thức ngắn hạn có thể biểu hiện là mất định hướng, ảo giác, lú lẫn, bồn chồn và hành vi tăng động có thể bạo lực hoặc gây hại cho người bệnh hoặc nhân viên bệnh viện. Tỷ lệ mắc được báo cáo từ 3% đến 21%, và những người bệnh này trải qua thời gian hồi phục dài hơn, sử dụng nhiều tài nguyên hơn và có nguy cơ gây hại cho bản thân và nhân viên bệnh viện cao hơn.
Sảng tỉnh không được nghiên cứu kỹ ở dân số người lớn như ở dân số trẻ em. Tuy nhiên, một số yếu tố nguy cơ đã được xác định ở người lớn bao gồm sử dụng benzodiazepine tiền phẫu, rối loạn căng thẳng sau chấn thương, phẫu thuật vú, phẫu thuật bụng, thời gian phẫu thuật kéo dài, tuổi trẻ, có ống nội khí quản và/hoặc ống thông tiểu, gây mê bằng sevoflurane, hút thuốc gần đây và đau sau phẫu thuật mức 5 trên thang đánh giá số.
Điều trị sảng tỉnh cũng chưa được nghiên cứu kỹ, nhưng có một số báo cáo ca bệnh và loạt ca mô tả việc sử dụng dexmedetomidine hiệu quả, cả dưới dạng truyền trong khi mổ ở người bệnh có tiền sử sảng tỉnh và thông qua liều bolus tĩnh mạch như liệu pháp cứu hộ cho người bệnh sau khi rút ống. Do đó, hợp lý khi xem xét sử dụng dexmedetomidine ở người bệnh có tiền sử sảng tỉnh, những người có yếu tố nguy cơ sảng tỉnh, hoặc những người trải qua sảng đáng kể khi tỉnh dậy sau gây mê.
Điều trị Sảng sau Phẫu thuật sau Giai đoạn Hồi phục Ngay lập tức
Vì đã chứng minh được rằng đến 40% trường hợp sảng có thể phòng ngừa được, phương pháp điều trị tốt nhất cho sảng là ngăn ngừa sự xuất hiện của nó ngay từ đầu. Các chiến lược phòng ngừa hiện được khuyến nghị bao gồm định hướng nhận thức, tăng cường giấc ngủ với các quy trình và vệ sinh giấc ngủ không dùng thuốc, thích ứng cho suy giảm thị giác và thính giác, vận động sớm, bổ sung dinh dưỡng và dịch, tránh thuốc gây bệnh, cung cấp oxy đầy đủ, phòng ngừa táo bón, kiểm soát đau, giáo dục cho chuyên gia chăm sóc sức khỏe và sử dụng đội ngũ đa chuyên ngành.
Nếu người bệnh phát triển sảng, các liệu pháp không dùng thuốc nêu trên nên được áp dụng như biện pháp điều trị đầu tiên nếu chưa thực hiện. Ngoài ra, người bệnh nên được đánh giá về sự hiện diện của bất kỳ yếu tố gây bệnh nào (như nhiễm trùng đường tiết niệu hoặc đau không kiểm soát tốt) cần can thiệp. Trong trường hợp các biện pháp can thiệp trên không hiệu quả và người bệnh đang trải qua sảng tăng động đe dọa đến bản thân và/hoặc nhân viên bệnh viện, có thể sử dụng thuốc chống loạn thần. Khuyến nghị sử dụng liều thấp nhất có thể trong thời gian ngắn nhất có thể. Không khuyến nghị sử dụng benzodiazepine trừ khi có chỉ định y tế, như trong trường hợp cai rượu hoặc benzodiazepine.
Kế hoạch Hành động:
|
Rối loạn Nhận thức sau Phẫu thuật
ĐỊNH NGHĨA
Rối loạn nhận thức sau phẫu thuật (POCD) mô tả một hội chứng suy giảm kéo dài hoặc suy thoái chức năng nhận thức với sự khởi phát thường xảy ra vài tuần đến vài tháng sau phẫu thuật. Đánh giá sự suy giảm được thực hiện bằng xét nghiệm trước và sau phẫu thuật. Đặc điểm bao gồm hạn chế về trí nhớ, khả năng trí tuệ và chức năng điều hành.
Một cách tiếp cận chuẩn hóa để xác định và nghiên cứu POCD đã bị hạn chế do thiếu các tiêu chí chẩn đoán đồng thuận. Nhìn chung, chẩn đoán liên quan đến việc xác định sự xấu đi trong xét nghiệm thần kinh nhận thức hậu phẫu chính thức so với mức độ tiền phẫu và do đó khó khăn ngoài một quy trình nghiên cứu. Nghiên cứu Quốc tế về Rối loạn Nhận thức sau Phẫu thuật (ISPOCD) đã đưa ra chẩn đoán POCD dựa trên điểm Z kết hợp >2 (tức là, 2 độ lệch chuẩn so với giá trị trung bình) qua nhiều xét nghiệm nhận thức riêng lẻ hoặc ít nhất hai điểm Z >2 cho các tham số xét nghiệm đơn lẻ. Các nhà nghiên cứu khác đã xem xét những thay đổi trong các lĩnh vực nhận thức như trí nhớ và chức năng điều hành, dựa trên các xét nghiệm thần kinh nhận thức riêng lẻ tương tự, so với mức nền của người bệnh hoặc so với nhóm đối chứng.
Mặc dù một định nghĩa đồng thuận vẫn còn khó nắm bắt, hầu hết các nhà nghiên cứu đồng ý rằng bệnh tật của suy giảm nhận thức là đáng kể. POCD có liên quan đến thời gian nằm viện và chi phí kéo dài hơn, rút lui sớm khỏi lực lượng lao động, và tăng tỷ lệ tử vong sau 1 năm, và có thể gây ra sự thay đổi trong quỹ đạo hướng tới sa sút trí tuệ.
Sự chú ý đến việc nhận biết tiền phẫu ở người bệnh có nguy cơ POCD đã tăng lên trong những năm gần đây với hy vọng rằng việc xác định, tư vấn tiền phẫu, điều chỉnh yếu tố nguy cơ và các chiến lược can thiệp có thể có thể giúp giảm thiểu tác động không mong muốn của POCD đối với từng người bệnh và hệ thống chăm sóc sức khỏe nói chung.
TỶ LỆ MẮC
Kể từ năm 1955, với việc xuất bản “Tác động Bất lợi của Gây mê lên Não ở Người già” trên tạp chí The Lancet, các bác sĩ lâm sàng đã quan sát thấy sự suy giảm nhận thức sau phẫu thuật có thể kéo dài trong nhiều tháng hoặc thậm chí nhiều năm. Những quan sát ban đầu này đã truyền cảm hứng cho nghiên cứu về hiện tượng suy giảm nhận thức và tần suất xảy ra. Các nghiên cứu hiện tại báo cáo tỷ lệ mắc từ 10% đến 80% do các quần thể người bệnh và cách tiếp cận đo lường POCD khác nhau.
Các nghiên cứu ban đầu tập trung vào suy giảm nhận thức sau phẫu thuật tim. Tỷ lệ POCD cao hơn ban đầu được mô tả sau phẫu thuật bắc cầu động mạch vành so với phẫu thuật không phải tim, với tỷ lệ cao đến 24% sau 6 tháng và 42% sau 5 năm. Công trình gần đây hơn cho thấy bệnh động mạch vành cơ bản và các yếu tố nguy cơ liên quan có thể góp phần vào suy giảm nhận thức nhiều hơn so với phẫu thuật tim và gây mê; nghiên cứu đang tiếp tục là cần thiết để phân tích đóng góp của từng yếu tố nguy cơ này.
Ngay sau đó đã rõ ràng rằng POCD xuất hiện sau phẫu thuật không phải tim cũng như sau phẫu thuật tim. ISPOCD là một loạt các nghiên cứu đa trung tâm, tiền cứu, có đối chứng về POCD trong phẫu thuật không phải tim. Nghiên cứu ISPOCD1 (tuổi trung bình 68) tìm thấy POCD ở 25% người bệnh sau 1 tuần, ở 10% sau 3 tháng và ở 1% sau 1 năm. Công trình tiếp theo xem xét các nhóm tuổi trẻ, trung niên và cao tuổi tìm thấy tỷ lệ POCD tăng (12,7%) ở nhóm tuổi cao hơn (tuổi trung bình 70) sau 3 tháng, so với 5,7% ở nhóm trẻ và 5,6% ở nhóm trung niên. Thực tế, những người có POCD cả khi xuất viện và sau 3 tháng có khả năng tử vong trong năm đầu tiên sau phẫu thuật cao gấp năm lần so với những người không có POCD.
YẾU TỐ NGUY CƠ
Các yếu tố nguy cơ cho POCD bao gồm cả yếu tố có thể điều chỉnh (ngoại sinh) và không thể điều chỉnh (nội sinh) (Bảng 7.2). Việc sàng lọc các yếu tố nguy cơ nội sinh rất quan trọng, mặc dù các biến số này khó hoặc không thể điều chỉnh, vì điều này có thể ảnh hưởng đến quyết định về phẫu thuật tự chọn hoàn toàn. Các yếu tố nguy cơ nội sinh bao gồm tuổi tăng, suy giảm nhận thức sẵn có, trình độ học vấn thấp hơn và các bệnh đồng mắc. Các yếu tố ngoại sinh, như mất ổn định huyết động, rối loạn chuyển hóa hoặc kiểm soát đau, có thể dễ dàng được giải quyết và tối ưu hóa trong giai đoạn chu phẫu trong nỗ lực giảm tỷ lệ POCD.
Liên quan rõ ràng hơn đến POD, đóng góp của hạ huyết áp và thiếu oxy trong khi mổ đối với POCD ít rõ ràng hơn. Các nghiên cứu sớm như nghiên cứu ISPOCD1 thấy rằng thiếu oxy máu và hạ huyết áp nhẹ, ngắn là các yếu tố nguy cơ độc lập cho sự phát triển của POCD. Bằng chứng mới hơn chỉ ra rằng huyết áp thấp có thể đẩy nhanh sự suy giảm nhận thức ở người bệnh cao tuổi. Cần thêm nghiên cứu trong lĩnh vực chu phẫu.
CÔNG CỤ SÀNG LỌC
Mặc dù có sự đồng thuận rằng nên thực hiện xét nghiệm rối loạn nhận thức tiền phẫu, không có sự đồng thuận về cách chúng ta nên kiểm tra hoặc công cụ nào chúng ta nên sử dụng. Một công cụ tiêu chuẩn, được xác nhận vừa kỹ lưỡng vừa thực tế vẫn chưa được phát triển. Tuy nhiên, POCD khó chẩn đoán và định lượng nếu không có tài liệu về trạng thái nền.
Hướng dẫn Thực hành Tốt nhất năm 2012 của Chương trình Cải thiện Chất lượng Phẫu thuật Quốc gia của Trường Cao đẳng Phẫu thuật Hoa Kỳ/Hiệp hội Lão khoa Hoa Kỳ để Đánh giá Tối ưu Tiền phẫu ở Người bệnh Phẫu thuật Lão khoa khuyến nghị kiểm tra nhận thức sớm ở bất kỳ người bệnh nào trên 65 tuổi, nên bao gồm phỏng vấn với vợ/chồng hoặc thành viên gia đình để bổ sung đánh giá.
Cũng khuyến nghị giới thiệu đến bác sĩ lão khoa để quản lý chu phẫu, nếu có rối loạn nhận thức hiện diện. Những hướng dẫn này khuyến nghị sử dụng công cụ Mini-Cog (bao gồm một bài kiểm tra nhớ lại ba mục và bài tập vẽ đồng hồ); tuy nhiên, các công cụ khác tồn tại trong tài liệu POCD (Bảng 7.3).
BỆNH SINH VÀ MỐI LIÊN QUAN VỚI GÂY MÊ
Sinh bệnh học cơ bản của POCD vẫn chưa rõ ràng. Hầu hết các nguồn đồng ý rằng suy giảm nhận thức có thể đa yếu tố về nguyên nhân, với những yếu tố nghi ngờ đóng góp bao gồm viêm toàn thân, căng thẳng phẫu thuật, rối loạn giấc ngủ, đau không kiểm soát, giảm tưới máu và có thể tác động độc thần kinh trực tiếp từ các thuốc gây mê.
Bằng chứng tồn tại cho thấy rằng nguy cơ sa sút trí tuệ tăng lên với phẫu thuật lặp lại cùng với gây mê toàn thân. Tuy nhiên, câu hỏi vẫn còn đó là mức độ mà các loại thuốc và kỹ thuật gây mê khác nhau phải chịu trách nhiệm. Mặc dù thiếu bằng chứng rõ ràng về tác động của gây mê lên não người lớn, các nghiên cứu trên động vật đã chứng minh độc tính thần kinh của gây mê. Vì độc tính thần kinh được đề xuất này, nhiều người hy vọng tránh gây mê toàn thân có thể dẫn đến tác động bảo vệ thần kinh. Đáng tiếc, các nghiên cứu hiện có không chứng minh được kết quả nhận thức được cải thiện với kỹ thuật gây tê vùng hoặc thần kinh. Wu và cộng sự đã cung cấp một đánh giá toàn diện năm 2004 kết luận rằng lựa chọn gây mê không ảnh hưởng đến tỷ lệ POCD. Điều này được xác nhận bởi một phân tích tổng hợp năm 2011 so sánh gây mê toàn thân và vùng và không thấy rằng gây mê toàn thân độc lập liên quan đến POCD. POCD ngắn hạn, được chẩn đoán khoảng 1 tuần sau phẫu thuật, có thể phổ biến hơn sau gây mê toàn thân, điều này có thể hiểu được một cách trực quan do gần với thời điểm phẫu thuật. Cần thêm nghiên cứu để xác định rõ bất kỳ mối liên kết nào giữa thuốc gây mê và POCD.
CAN THIỆP
Nhận biết tiền phẫu ở người bệnh có vẻ có nguy cơ cao phát triển POCD và giới thiệu đến chuyên gia lão khoa có thể tối ưu hóa các yếu tố nguy cơ có thể điều chỉnh nên được xem xét. Tư vấn người bệnh và gia đình về nguy cơ suy giảm nhận thức cũng nên được bao gồm trong phỏng vấn tiền phẫu. Quyết định tiến hành phẫu thuật tự chọn hoàn toàn chỉ nên xảy ra sau đánh giá đa chuyên khoa ở người bệnh có nguy cơ cao.
Mặc dù mối liên kết không được xác định rõ ràng, việc giảm thiểu xâm lấn phẫu thuật; thời gian phẫu thuật; và, do đó, thời gian dưới gây mê có thể giảm nhẹ nguy cơ POCD. Nên xem xét giám sát độ sâu gây mê và oxy hóa não ở người bệnh có nguy cơ cao. Tránh mất ổn định huyết động cũng quan trọng.
Sau phẫu thuật, vì đã biết rằng sảng có thể là một yếu tố nguy cơ cho sự phát triển của POCD, việc xác định và điều trị sảng nhanh chóng là quan trọng. Điều trị cẩn thận đau và biến chứng y tế có thể giúp cải thiện quỹ đạo nhận thức.
Kế hoạch Hành động:
|
Rối loạn Co giật và Động kinh
Người bệnh có rối loạn co giật/động kinh sẵn có có nguy cơ cao bị co giật trong thời kỳ chu phẫu chủ yếu do những lý do sau:
- Ngừng liệu pháp thuốc chống động kinh (AED): Giảm nồng độ huyết thanh cho phép tái phát các cơn co giật đã được kiểm soát trước đó.
- Co giật do một số loại thuốc gây ra, phổ biến nhất là các chất tương tự lysine, axit epsilon-aminocaproic và tranexamic. Người bệnh có rối loạn co giật không nên nhận những thuốc này, nếu có thể, hoặc họ nên được cho liều điều trị thấp nhất.
Kế hoạch Hành động:
|
Chấn động Não Gần đây
Chấn động não là sự xuất hiện của rối loạn chức năng thần kinh thoáng qua (thường là nhận thức) sau chấn thương đầu; các nghiên cứu chẩn đoán hình ảnh thần kinh thông thường là bình thường. Có ít bằng chứng để hướng dẫn thực hành gây mê ở những người bệnh này. Mối quan tâm lý thuyết là não bị chấn động có thể dễ bị tổn thương thứ phát hơn trong môi trường gây mê và phẫu thuật.
Kế hoạch Hành động:
|
Nguy cơ Đột quỵ
Có các yếu tố thủ thuật và yếu tố người bệnh trong đánh giá nguy cơ đột quỵ. Một số thủ thuật phẫu thuật (mở và nội mạch), bao gồm phẫu thuật tim mạch, động mạch chủ và thần kinh mạch máu, mang nguy cơ đáng kể gây đột quỵ. Các trung tâm y tế thực hiện những thủ thuật này phải có một lộ trình cho chăm sóc đột quỵ chu phẫu cấp tính, thường liên quan đến một đội ngũ đột quỵ đa chuyên ngành. Thrombolysis và lấy huyết khối nội mạch nên được sẵn sàng. Mặt khác, trong phẫu thuật không phải tim mạch, đột quỵ thiếu máu cục bộ chu phẫu không phổ biến. Một phân tích gần đây về 150.198 ca từ Bệnh viện Đa khoa Massachusetts và hai bệnh viện liên kết thấy tỷ lệ đột quỵ thiếu máu cục bộ trong vòng 30 ngày sau phẫu thuật là 0,5%. Đáng chú ý, người bệnh được chẩn đoán tiền phẫu có lỗ bầu dục thông (PFO; n=1540), có nguy cơ cao hơn, với 3,2% bị đột quỵ chu phẫu. Trong phân tích điều chỉnh, nguy cơ đột quỵ ước tính là 5,9 trên 1000 người bệnh có PFO so với 2,2 trên 1000 người bệnh không có PFO.
Các yếu tố người bệnh bao gồm đột quỵ trước đó (thảo luận dưới đây), rung nhĩ, tình trạng tăng đông máu, PFO và van tim nhân tạo. Sàng lọc thường quy tất cả người bệnh về PFO hiện không được khuyến nghị, nhưng cần thêm nghiên cứu. Quản lý cẩn thận thuốc chống đông máu, được sử dụng để dự phòng đột quỵ ở người bệnh rung nhĩ hoặc van nhân tạo, và thuốc chống kết tập tiểu cầu, được sử dụng để dự phòng đột quỵ ở người bệnh có bệnh mạch máu não, đòi hỏi đầu vào từ tim mạch học và/hoặc thần kinh học về thời gian ngừng và bắt đầu lại trong chu phẫu.
Kế hoạch Hành động cho Thủ thuật hoặc Người bệnh có Nguy cơ Đột quỵ Cao:
|
Đột quỵ Trước đó
Người bệnh có đột quỵ trước đó có nguy cơ rất cao bị đột quỵ sau phẫu thuật, cũng như các hội chứng nhận thức sau phẫu thuật đã thảo luận ở trên. Hiện tại, bằng chứng tốt nhất về nguy cơ đột quỵ tái phát chu phẫu đến từ phân tích hồi cứu của Sổ đăng ký Quốc gia Đan Mạch. Christiansen và cộng sự đã phân tích 146.694 ca phẫu thuật cấp cứu ở người bệnh Đan Mạch từ năm 2005 đến 2011, 7496 người (5%) trong số đó có đột quỵ trước đó. Biến cố tim mạch bất lợi lớn trong 30 ngày (MACE; nhồi máu cơ tim cấp, đột quỵ thiếu máu cục bộ và tử vong do tim mạch) xảy ra ở 2,3% người bệnh không có đột quỵ trước đó, 20,7% người bệnh bị đột quỵ trong 3 tháng trước đó, 10,3% người bệnh bị đột quỵ trong 3-9 tháng trước đó, và 8,8% người bệnh bị đột quỵ hơn 9 tháng trước khi phẫu thuật cấp cứu.
Jorgensen và đồng nghiệp đã thực hiện một phân tích tương tự về Sổ đăng ký Quốc gia Đan Mạch cho người bệnh phẫu thuật tự chọn. Tổng cộng 474.046 người bệnh không có đột quỵ trước đó được so sánh với 7137 người bệnh có đột quỵ trước đó. MACE trong 30 ngày xảy ra ở 0,4% người bệnh không có đột quỵ trước đó. Những người có đột quỵ trước đó <3 tháng trước phẫu thuật tự chọn có tỷ lệ MACE 30 ngày là 17,7%; tỷ lệ là 7,2% đối với những người bị đột quỵ 3-6 tháng trước đó, 4,1% đối với những người bị đột quỵ 6-12 tháng trước đó, và 3,4% đối với người bệnh bị đột quỵ 12 tháng trước khi phẫu thuật. Các tác giả kết luận, dựa trên các đường cong hồi quy lập phương cho người bệnh có đột quỵ trước đó, rằng tỷ lệ cơ hội cho MACE, tử vong do mọi nguyên nhân và đột quỵ thiếu máu cục bộ đã giảm xuống ở khoảng 9 tháng. Do đó, bằng chứng tốt nhất hiện tại cho thấy các thủ thuật tự chọn hoàn toàn nên được trì hoãn 9 tháng sau một đột quỵ thiếu máu cục bộ.
Ở người bệnh có đột quỵ không nghiêm trọng gần đây hoặc cơn thiếu máu não thoáng qua (TIA) do bệnh động mạch cảnh có triệu chứng, phẫu thuật điều chỉnh (stent động mạch cảnh hoặc nội mạc cắt bỏ) nên được thực hiện sớm, thường là dưới 2 tuần sau đột quỵ hoặc TIA. Bằng chứng có sẵn cho thấy rằng nội mạc cắt bỏ cấp tính an toàn hơn đặt stent động mạch cảnh trong 7 ngày đầu sau khi khởi phát triệu chứng.
Theo các khuyến nghị từ Hiệp hội Thần kinh học trong Gây mê và Chăm sóc Tích cực, huyết áp trong và sau khi mổ nên nhắm đến việc duy trì mức huyết áp nền và tránh hạ huyết áp. Beta-blockade, bắt đầu trước phẫu thuật, có thể làm tăng nguy cơ đột quỵ trong phẫu thuật không phải tim.
Cần nhấn mạnh rằng “đột quỵ” là một thuật ngữ rộng bao gồm đột quỵ thiếu máu cục bộ mạch lớn và nhỏ, đột quỵ xuất huyết và xuất huyết dưới màng nhện. Hiểu biết về nguyên nhân là cần thiết để phân tầng nguy cơ cho người bệnh một cách thích hợp. Ví dụ, người bệnh có bệnh mạch máu não tắc nghẽn có thể rất phụ thuộc vào áp lực tưới máu và cần huyết áp tương đối cao trong suốt thời kỳ chu phẫu, trong khi những người có đột quỵ xuất huyết trước đó hoặc xuất huyết dưới màng nhện (và có khả năng phình mạch không được bảo vệ) có thể cần tránh tăng huyết áp cẩn thận.
Kế hoạch Hành động:
|
Nguy cơ Tổn thương Thiếu máu-Thiếu oxy
Các thủ thuật có nguy cơ cao bao gồm phẫu thuật tim, phẫu thuật động mạch chủ, can thiệp động mạch vành qua da và có thể các thủ thuật điện sinh lý can thiệp. Tổn thương não thiếu oxy trong bối cảnh ngừng tim quanh thủ thuật nên được điều trị bằng quản lý nhiệt độ mục tiêu. Cảm ứng nhanh hạ thân nhiệt điều trị hoặc kiểm soát thân nhiệt bình thường chặt chẽ là tiêu chuẩn chăm sóc.
Kế hoạch Hành động:
|
Thiết bị Kích thích Thần kinh Cấy ghép và Thiết bị Khác
Những thiết bị này bao gồm kích thích não sâu cho rối loạn vận động hoặc chỉ định khác, kích thích tủy sống cho đau mạn tính, kích thích dây thần kinh phế vị cho động kinh và bơm trong màng cứng cho đau hoặc co cứng (opioid hoặc baclofen). Phẫu thuật với đốt điện, kích thích điện (như điện thế gợi ra trong phẫu thuật cột sống) hoặc kích thích từ đòi hỏi lập kế hoạch cẩn thận để tránh truyền năng lượng quá mức đến não, tủy sống hoặc mô thần kinh hoặc làm hỏng thiết bị.
Kế hoạch Hành động:
|
Xem Bảng 7.4 để biết tóm tắt các kế hoạch hành động cho đánh giá rủi ro CNS chu phẫu và điều chỉnh.
HẾT CHƯƠNG 7.
Bảng chú giải thuật ngữ Y học Anh-Việt – Chương 7
| STT | Thuật ngữ tiếng Anh | Cách phát âm | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Central Nervous System (CNS) | /ˈsen.trəl ˈnɜː.vəs ˈsɪs.təm/ | Hệ thần kinh trung ương |
| 2 | Perioperative | /ˌper.i.ˈɒp.ər.ə.tɪv/ | Quanh phẫu thuật (giai đoạn trước, trong và sau phẫu thuật) |
| 3 | Postoperative delirium (POD) | /ˌpəʊst.ˈɒp.ər.ə.tɪv dɪˈlɪr.i.əm/ | Sảng sau phẫu thuật |
| 4 | Acute confusional syndrome | /əˈkjuːt kənˈfjuː.ʒən.əl ˈsɪn.drəʊm/ | Hội chứng lú lẫn cấp tính |
| 5 | Fluctuating | /ˈflʌk.tʃu.eɪ.tɪŋ/ | Dao động, biến thiên |
| 6 | Multifactorial | /ˌmʌl.ti.fækˈtɔː.ri.əl/ | Đa yếu tố |
| 7 | Hyperactive | /ˌhaɪ.pəˈræk.tɪv/ | Tăng hoạt động |
| 8 | Hypoactive | /ˌhaɪ.pəʊˈæk.tɪv/ | Giảm hoạt động |
| 9 | Mixed | /mɪkst/ | Hỗn hợp |
| 10 | Morbidity | /mɔːˈbɪd.ə.ti/ | Tỷ lệ mắc bệnh |
| 11 | Mortality | /mɔːˈtæl.ə.ti/ | Tỷ lệ tử vong |
| 12 | Institutionalization | /ˌɪn.stɪ.tjuː.ʃən.əl.aɪˈzeɪ.ʃən/ | Việc đưa vào cơ sở chăm sóc |
| 13 | Confusion Assessment Method (CAM) | /kənˈfjuː.ʒən əˈses.mənt ˈmeθ.əd/ | Phương pháp đánh giá lú lẫn |
| 14 | CAM-ICU | /kæm-aɪ.siː.juː/ | CAM cho đơn vị hồi sức tích cực |
| 15 | Pathophysiologic | /ˌpæθ.əʊ.fɪz.i.əˈlɒdʒ.ɪk/ | Sinh lý bệnh |
| 16 | Neurotransmitter | /ˌnjʊə.rəʊ.trænzˈmɪt.ər/ | Chất dẫn truyền thần kinh |
| 17 | Neuroinflammation | /ˌnjʊə.rəʊ.ɪn.fləˈmeɪ.ʃən/ | Viêm thần kinh |
| 18 | Predisposing | /ˌpriː.dɪˈspəʊ.zɪŋ/ | Yếu tố tiền định, yếu tố thuận lợi |
| 19 | Precipitating | /prɪˈsɪp.ɪ.teɪ.tɪŋ/ | Yếu tố khởi phát |
| 20 | Benzodiazepines | /ˌben.zəʊ.daɪˈæz.ə.piːnz/ | Benzodiazepine (nhóm thuốc an thần) |
| 21 | Anticholinergics | /ˌæn.ti.kəʊ.lɪˈnɜː.dʒɪks/ | Thuốc kháng cholinergic |
| 22 | Diphenhydramine | /ˌdaɪ.fɛn.ˈhaɪ.drə.miːn/ | Diphenhydramine (thuốc kháng histamine) |
| 23 | Hydroxyzine | /haɪˈdrɒk.sɪ.ziːn/ | Hydroxyzine (thuốc kháng histamine) |
| 24 | Meperidine | /məˈper.ɪ.diːn/ | Meperidine (thuốc giảm đau opioid) |
| 25 | Histamine-2 antagonists | /ˈhɪs.tə.miːn tuː ænˈtæɡ.ə.nɪsts/ | Thuốc đối kháng histamine-2 |
| 26 | Sedative hypnotics | /ˈsed.ə.tɪv hɪpˈnɒt.ɪks/ | Thuốc an thần gây ngủ |
| 27 | Intraoperative | /ˌɪn.trə.ˈɒp.ər.ə.tɪv/ | Trong phẫu thuật |
| 28 | Regional anesthesia | /ˈriː.dʒən.əl ˌæn.əsˈθiː.zi.ə/ | Gây tê vùng |
| 29 | Bispectral index (BIS) | /baɪˈspek.trəl ˈɪn.deks/ | Chỉ số phổ hai thành phần (theo dõi độ sâu gây mê) |
| 30 | Electroencephalogram (EEG) | /ɪˌlek.trəʊ.ɛnˈsɛf.ə.lə.ɡræm/ | Điện não đồ |
| 31 | Burst suppression | /bɜːst səˈpreʃ.ən/ | Ức chế đột biến (trên điện não đồ) |
| 32 | Dexmedetomidine | /deks.me.dəˈtɒm.ɪ.diːn/ | Dexmedetomidine (thuốc an thần) |
| 33 | Prophylactic | /ˌprɒf.əˈlæk.tɪk/ | Dự phòng |
| 34 | JAK2/STAT3 pathway | /dʒeɪ-eɪ-keɪ tuː / stæt θriː ˈpɑːθ.weɪ/ | Đường dẫn JAK2/STAT3 (con đường tín hiệu tế bào) |
| 35 | Isoflurane | /ˌaɪ.səʊˈflʊə.reɪn/ | Isoflurane (thuốc gây mê đường hô hấp) |
| 36 | Neurocognitive | /ˌnjʊə.rəʊˈkɒɡ.nɪ.tɪv/ | Thần kinh nhận thức |
| 37 | Ketamine | /ˈket.ə.miːn/ | Ketamine (thuốc gây mê) |
| 38 | Multimodal | /ˌmʌl.ti.ˈməʊd.əl/ | Đa phương thức |
| 39 | Cognitive reorientation | /ˈkɒɡ.nɪ.tɪv riː.ˌɔːr.i.ənˈteɪ.ʃən/ | Định hướng nhận thức |
| 40 | Adaptations | /ˌæd.æpˈteɪ.ʃənz/ | Thích nghi |
| 41 | Interdisciplinary | /ˌɪn.tə.dɪsˈɪ.plɪ.nər.i/ | Liên ngành |
| 42 | Antipsychotics | /ˌæn.ti.saɪˈkɒt.ɪks/ | Thuốc chống loạn thần |
| 43 | Haloperidol | /ˌhæl.əˈper.ɪ.dɒl/ | Haloperidol (thuốc chống loạn thần) |
| 44 | Postoperative Cognitive Dysfunction (POCD) | /ˌpəʊst.ˈɒp.ər.ə.tɪv ˈkɒɡ.nɪ.tɪv dɪsˈfʌŋk.ʃən/ | Rối loạn nhận thức sau phẫu thuật |
| 45 | Executive function | /ɪɡˈzek.jʊ.tɪv ˈfʌŋk.ʃən/ | Chức năng điều hành |
| 46 | Neurocognitive testing | /ˌnjʊə.rəʊˈkɒɡ.nɪ.tɪv ˈtes.tɪŋ/ | Kiểm tra thần kinh nhận thức |
| 47 | Z-score | /ziː skɔːr/ | Điểm Z (đơn vị đo lường thống kê) |
| 48 | Standard deviation | /ˈstæn.dəd ˌdiː.vi.ˈeɪ.ʃən/ | Độ lệch chuẩn |
| 49 | Cognitive domains | /ˈkɒɡ.nɪ.tɪv dəʊˈmeɪnz/ | Lĩnh vực nhận thức |
| 50 | Coronary artery bypass grafting | /ˈkɒr.ən.ər.i ˈɑː.tər.i ˈbaɪ.pɑːs ˈɡrɑːf.tɪŋ/ | Phẫu thuật bắc cầu động mạch vành |
| 51 | Comorbid | /ˌkəʊ.mɔːˈbɪd/ | Bệnh đồng mắc |
| 52 | Hemodynamic | /ˌhiː.məʊ.daɪˈnæm.ɪk/ | Huyết động học |
| 53 | Metabolic derangements | /ˌmet.əˈbɒl.ɪk dɪˈreɪndʒ.mənts/ | Rối loạn chuyển hóa |
| 54 | Mini-Cog | /ˈmɪn.i kɒɡ/ | Mini-Cog (công cụ đánh giá nhận thức tối thiểu) |
| 55 | Clock drawing exercise | /klɒk ˈdrɔː.ɪŋ ˈek.sə.saɪz/ | Bài tập vẽ đồng hồ |
| 56 | Systemic inflammation | /sɪˈstem.ɪk ɪnˌflæ.məˈeɪ.ʃən/ | Viêm toàn thân |
| 57 | Surgical stress | /ˈsɜː.dʒɪ.kəl stres/ | Stress phẫu thuật |
| 58 | Hypoperfusion | /ˌhaɪ.pəʊ.pəˈfjuː.ʒən/ | Giảm tưới máu |
| 59 | Neurotoxic | /ˌnjʊə.rəʊˈtɒk.sɪk/ | Độc thần kinh |
| 60 | Neuraxial | /njʊəˈræk.si.əl/ | Liên quan đến trục thần kinh |
| 61 | Seizure disorders | /ˈsiː.ʒər dɪˈsɔː.dəz/ | Rối loạn co giật |
| 62 | Epilepsy | /ˈep.ɪ.lep.si/ | Động kinh |
| 63 | Antiepileptic drug (AED) | /ˌæn.ti.ep.ɪˈlep.tɪk drʌɡ/ | Thuốc chống động kinh |
| 64 | Epsilon-aminocaproic acid | /ˈep.sɪ.lɒn æm.ɪ.nəʊ.kəˈprəʊ.ɪk ˈæs.ɪd/ | Acid epsilon-aminocaproic |
| 65 | Tranexamic acid | /trænˌeks.æm.ɪk ˈæs.ɪd/ | Acid tranexamic |
| 66 | γ-aminobutyric acid type A | /ɡæm.ə æm.ɪ.nəʊ.bjuːˈtɪr.ɪk ˈæs.ɪd taɪp eɪ/ | Acid γ-aminobutyric loại A (chất dẫn truyền thần kinh ức chế) |
| 67 | Concussion | /kənˈkʌʃ.ən/ | Chấn động não |
| 68 | Transient neurologic dysfunction | /ˈtrænz.i.ənt ˌnjʊə.rəˈlɒdʒ.ɪk dɪsˈfʌŋk.ʃən/ | Rối loạn chức năng thần kinh tạm thời |
| 69 | Neuroimaging | /ˌnjʊə.rəʊˈɪm.ɪ.dʒɪŋ/ | Chẩn đoán hình ảnh thần kinh |
| 70 | Endovascular | /ˌen.dəʊˈvæs.kjʊ.lər/ | Nội mạch |
| 71 | Neurovascular | /ˌnjʊə.rəʊˈvæs.kjʊ.lər/ | Thần kinh mạch máu |
| 72 | Thrombectomy | /θrɒmˈbek.tə.mi/ | Lấy huyết khối |
| 73 | Patent foramen ovale (PFO) | /ˈpeɪ.tənt fəˈreɪ.mən əʊˈvɑː.li/ | Lỗ bầu dục còn thông |
| 74 | Atrial fibrillation | /ˈeɪ.tri.əl ˌfɪb.rɪˈleɪ.ʃən/ | Rung nhĩ |
| 75 | Hypercoagulable | /ˌhaɪ.pər.kəʊˈæɡ.jʊ.lə.bəl/ | Tăng đông máu |
| 76 | Prosthetic heart valves | /prɒsˈθet.ɪk hɑːt vælvz/ | Van tim nhân tạo |
| 77 | Anticoagulation | /ˌæn.ti.kəʊ.æɡ.jʊˈleɪ.ʃən/ | Chống đông máu |
| 78 | Antiplatelet | /ˌæn.tɪˈpleɪt.lɪt/ | Chống kết tập tiểu cầu |
| 79 | Major adverse cardiovascular events (MACE) | /ˈmeɪ.dʒər ˈæd.vɜːs ˌkɑː.di.əʊˈvæs.kjʊ.lər ɪˈvents/ | Biến cố tim mạch bất lợi chính |
| 80 | Ischemic stroke | /ɪsˈkiː.mɪk strəʊk/ | Đột quỵ thiếu máu cục bộ |
| 81 | Cardiovascular death | /ˌkɑː.di.əʊˈvæs.kjʊ.lər deθ/ | Tử vong do tim mạch |
| 82 | Cubic regression splines | /ˈkjuː.bɪk rɪˈɡreʃ.ən splaɪnz/ | Đường cong hồi quy bậc ba |
| 83 | Odds ratio | /ɒdz ˈreɪ.ʃi.əʊ/ | Tỷ số chênh |
| 84 | Transient ischemic attack (TIA) | /ˈtrænz.i.ənt ɪsˈkiː.mɪk əˈtæk/ | Cơn thiếu máu não thoáng qua |
| 85 | Carotid | /kəˈrɒt.ɪd/ | Động mạch cảnh |
| 86 | Endarterectomy | /ˌend.ɑː.təˈrek.tə.mi/ | Phẫu thuật lấy nội mạc |
| 87 | Carotid artery stenting | /kəˈrɒt.ɪd ˈɑː.tər.i ˈsten.tɪŋ/ | Đặt stent động mạch cảnh |
| 88 | Beta-blockade | /ˈbeɪ.tə ˈblɒk.eɪd/ | Ức chế beta |
| 89 | Subarachnoid hemorrhage | /ˌsʌb.əˈræk.nɔɪd ˈhem.ər.ɪdʒ/ | Xuất huyết dưới nhện |
| 90 | Perfusion pressure | /pəˈfjuː.ʒən ˈpreʃ.ər/ | Áp lực tưới máu |
| 91 | Aneurysms | /ˈæn.jʊ.rɪz.əmz/ | Phình mạch |
| 92 | Hypoxic-ischemic injury | /haɪˈpɒk.sɪk-ɪsˈkiː.mɪk ˈɪn.dʒər.i/ | Tổn thương thiếu oxy-thiếu máu cục bộ |
| 93 | Percutaneous coronary interventions | /pəˌkjuː.teɪ.ni.əs ˈkɒr.ən.ər.i ˌɪn.təˈven.ʃənz/ | Can thiệp động mạch vành qua da |
| 94 | Electrophysiologic | /ɪˌlek.trəʊ.fɪz.i.əˈlɒdʒ.ɪk/ | Điện sinh lý |
| 95 | Anoxic | /əˈnɒk.sɪk/ | Thiếu oxy |
| 96 | Targeted temperature management | /ˈtɑː.ɡɪ.tɪd ˈtem.prə.tʃər ˈmæn.ɪdʒ.mənt/ | Kiểm soát thân nhiệt có mục tiêu |
| 97 | Therapeutic hypothermia | /ˌθer.əˈpjuː.tɪk ˌhaɪ.pəʊˈθɜː.mi.ə/ | Hạ thân nhiệt điều trị |
| 98 | Normothermia | /ˌnɔː.məʊˈθɜː.mi.ə/ | Thân nhiệt bình thường |
| 99 | Computed tomography | /kəmˈpjuː.tɪd təˈmɒɡ.rə.fi/ | Chụp cắt lớp vi tính |
| 100 | Computed tomographic angiography | /kəmˈpjuː.tɪd ˌtəm.əˈɡræf.ɪk ˌæn.dʒi.ˈɒɡ.rə.fi/ | Chụp mạch máu bằng cắt lớp vi tính |
| 101 | Alteplase | /ˈæl.tə.pleɪz/ | Alteplase (thuốc tiêu sợi huyết) |
| 102 | Implanted neurostimulator | /ɪmˈplɑːn.tɪd ˌnjʊə.rəʊˈstɪm.jʊ.leɪ.tər/ | Thiết bị kích thích thần kinh cấy ghép |
| 103 | Deep brain stimulators | /diːp breɪn ˈstɪm.jʊ.leɪ.tərz/ | Máy kích thích não sâu |
| 104 | Spinal cord stimulators | /ˈspaɪ.nəl kɔːd ˈstɪm.jʊ.leɪ.tərz/ | Máy kích thích tủy sống |
| 105 | Vagal nerve stimulators | /ˈveɪ.ɡəl nɜːv ˈstɪm.jʊ.leɪ.tərz/ | Máy kích thích dây thần kinh phế vị |
| 106 | Intrathecal pumps | /ˌɪn.trəˈθiː.kəl pʌmps/ | Bơm nội tủy |
| 107 | Baclofen | /ˈbæk.ləʊ.fen/ | Baclofen (thuốc giãn cơ) |
| 108 | Electrocautery | /ɪˌlek.trəʊˈkɔː.tər.i/ | Đốt điện |
| 109 | Evoked potentials | /ɪˈvəʊkt pəˈten.ʃəlz/ | Điện thế gợi ra |
| 110 | Magnetic stimulation | /mæɡˈnet.ɪk ˌstɪm.jʊˈleɪ.ʃən/ | Kích thích từ tính |
| 111 | Electroconvulsive therapy | /ɪˌlek.trəʊ.kənˈvʌl.sɪv ˈθer.ə.pi/ | Liệu pháp sốc điện |
| 112 | Motor evoked potential | /ˈməʊ.tər ɪˈvəʊkt pəˈten.ʃəl/ | Điện thế vận động gợi ra |
| 113 | Emergence delirium | /ɪˈmɜː.dʒəns dɪˈlɪr.i.əm/ | Sảng khi tỉnh dậy sau gây mê |
| 114 | Hallucinations | /həˌluː.sɪˈneɪ.ʃənz/ | Ảo giác |
| 115 | Disorentation | /dɪsˌɔːr.i.ənˈteɪ.ʃən/ | Mất định hướng |
| 116 | Restlessness | /ˈrest.ləs.nəs/ | Bồn chồn |
| 117 | Post-traumatic stress disorder | /pəʊst trɔːˈmæt.ɪk stres dɪˈsɔː.dər/ | Rối loạn stress sau sang chấn |
| 118 | Endotracheal tube | /ˌen.dəʊˈtreɪ.ki.əl tjuːb/ | Ống nội khí quản |
| 119 | Urinary catheter | /ˈjʊə.rɪn.ər.i ˈkæθ.ɪ.tər/ | Ống thông tiểu |
| 120 | Sevoflurane | /ˌsev.əʊˈflʊə.reɪn/ | Sevoflurane (thuốc gây mê đường hô hấp) |
| 121 | Extubation | /ˌeks.tjuːˈbeɪ.ʃən/ | Rút ống nội khí quản |
| 122 | Cognitive reorientation | /ˈkɒɡ.nɪ.tɪv riː.ˌɔːr.i.ənˈteɪ.ʃən/ | Tái định hướng nhận thức |
| 123 | Sleep enhancement | /sliːp ɪnˈhɑːns.mənt/ | Tăng cường giấc ngủ |
| 124 | Sleep hygiene | /sliːp ˈhaɪ.dʒiːn/ | Vệ sinh giấc ngủ |
| 125 | Early mobility | /ˈɜː.li məʊˈbɪl.ə.ti/ | Vận động sớm |
| 126 | Oxygenation | /ˌɒk.sɪ.dʒəˈneɪ.ʃən/ | Cung cấp oxy |
| 127 | Constipation | /ˌkɒn.stɪˈpeɪ.ʃən/ | Táo bón |
| 128 | Urinary tract infection | /ˈjʊə.rɪn.ər.i trækt ɪnˈfek.ʃən/ | Nhiễm trùng đường tiết niệu |
| 129 | Montreal Cognitive Assessment (MoCA) | /mɒn.triˈɔːl ˈkɒɡ.nɪ.tɪv əˈses.mənt/ | Đánh giá nhận thức Montreal |
| 130 | Mini Mental State Examination (MMSE) | /ˈmɪn.i ˈmen.təl steɪt ɪɡˌzæm.ɪˈneɪ.ʃən/ | Kiểm tra trạng thái tâm thần tối thiểu |
| 131 | Saint Louis University Mental Status Exam (SLUMS) | /seɪnt ˈluː.ɪs ˌjuː.nɪˈvɜː.sə.ti ˈmen.təl ˈsteɪ.təs ɪɡˈzæm/ | Kiểm tra trạng thái tâm thần đại học Saint Louis |
| 132 | Specificity | /ˌspes.ɪˈfɪs.ɪ.ti/ | Độ đặc hiệu |
| 133 | Sensitivity | /ˌsen.sɪˈtɪv.ə.ti/ | Độ nhạy |
| 134 | Rivastigmine | /rɪˈvæs.tɪɡ.miːn/ | Rivastigmine (thuốc ức chế cholinesterase) |
| 135 | Cholinesterase inhibitors | /ˌkəʊ.lɪˈnes.tər.eɪz ɪnˈhɪb.ɪ.tərz/ | Thuốc ức chế cholinesterase |
| 136 | Geriatrics | /ˌdʒer.iˈæt.rɪks/ | Lão khoa |
| 137 | American College of Surgeons | /əˈmer.ɪ.kən ˈkɒl.ɪdʒ əv ˈsɜː.dʒənz/ | Hiệp hội Phẫu thuật viên Hoa Kỳ |
| 138 | Geriatric Surgical Patient | /ˌdʒer.iˈæt.rɪk ˈsɜː.dʒɪ.kəl ˈpeɪ.ʃənt/ | Bệnh nhân phẫu thuật lão khoa |
| 139 | Operating room | /ˈɒp.ər.eɪ.tɪŋ ruːm/ | Phòng phẫu thuật |
| 140 | Comprehensive stroke center | /ˌkɒm.prɪˈhen.sɪv strəʊk ˈsen.tər/ | Trung tâm đột quỵ toàn diện |
| 141 | Cerebral perfusion pressure | /ˈser.ə.brəl pəˈfjuː.ʒən ˈpreʃ.ər/ | Áp lực tưới máu não |
| 142 | Hemorrhagic stroke | /ˌhem.əˈrædʒ.ɪk strəʊk/ | Đột quỵ xuất huyết |
| 143 | Cerebral oximetry | /ˈser.ə.brəl ɒkˈsɪm.ɪ.tri/ | Đo oxy não |
| 144 | American Heart Association | /əˈmer.ɪ.kən hɑːt əˌsəʊ.siˈeɪ.ʃən/ | Hiệp hội Tim mạch Hoa Kỳ |
| 145 | Geriatric medicine | /ˌdʒer.iˈæt.rɪk ˈmed.ɪ.sɪn/ | Y học lão khoa |
| 146 | Acute stroke team | /əˈkjuːt strəʊk tiːm/ | Đội đột quỵ cấp tính |
| 147 | Cerebrospinal fluid | /ˌser.ə.brəʊˈspaɪ.nəl ˈfluː.ɪd/ | Dịch não tủy |
| 148 | CSF drainage | /siː es ef ˈdreɪn.ɪdʒ/ | Dẫn lưu dịch não tủy |
| 149 | Aortic surgery | /eɪˈɔː.tɪk ˈsɜː.dʒər.i/ | Phẫu thuật động mạch chủ |
| 150 | Intraoperative neuromonitoring | /ˌɪn.trə.ˈɒp.ər.ə.tɪv ˌnjʊə.rəʊˈmɒn.ɪ.tər.ɪŋ/ | Theo dõi thần kinh trong phẫu thuật |
TÀI LIỆU THAM KHẢO
- Marcantonio E.R.: Postoperative delirium: a 76-year-old woman with delirium following surgery. JAMA 2012; 308: pp. 73-81.
- Inouye S.K., Westendorp R.G., Saczynski J.S.: Delirium in elderly people. Lancet 2014; 383: pp. 911-922.
- American Psychiatric Association : DSM-5 Task Force: Diagnostic and Statistical Manual of Mental Disorders: DSM-5.ed 52013.American Psychiatric AssociationWashington, DC
- Mohanty S., Rosenthal R.A., Russell M.M., Neuman M.D., Ko C.Y., Esnaola N.F.: Optimal perioperative management of the geriatric patient: a best practices guideline from the American College of Surgeons NSQIP and the American Geriatrics Society. J Am Coll Surg 2016; 222: pp. 930-947.
- Marcantonio E.R.: In the clinic. Delirium. Ann Intern Med. 2011; 154: pp. ITC6-ITC16.
- Oh E.S., Fong T.G., Hshieh T.T., Inouye S.K.: Delirium in older persons: advances in diagnosis and treatment. JAMA 2017; 318: pp. 1161-1174.
- Inouye S.K., van Dyck C.H., Alessi C.A., Balkin S., Siegal A.P., Horwitz R.I.: Clarifying confusion: the confusion assessment method. A new method for detection of delirium. Ann Intern Med 1990; 113: pp. 941-948.
- Ely E.W., Inouye S.K., Bernard G.R., et. al.: Delirium in mechanically ventilated patients: Validity and reliability of the confusion assessment method for the intensive care unit (CAM-ICU). JAMA 2001; 286: pp. 2703-2710.
- Inouye S.K.: Delirium in older persons. N Engl J Med 2006; 354: pp. 1157-1165.
- Marcantonio E.R.: Delirium in hospitalized older adults. N Engl J Med 2017; 377: pp. 1456-1466.
- Inouye S.K., Charpentier P.A.: Precipitating factors for delirium in hospitalized elderly persons. Predictive model and interrelationship with baseline vulnerability. JAMA 1996; 275: pp. 852-857.
- American Geriatrics Society Expert Panel on Postoperative Delirium in Older Adults : American Geriatrics Society abstracted clinical practice guideline for postoperative delirium in older adults. J Am Geriatr Soc 2015; 63: pp. 142-150.
- Smith P.J., Attix D.K., Weldon B.C., Monk T.G.: Depressive symptoms and risk of postoperative delirium. Am J Geriatr Psychiatry 2016; 24: pp. 232-238.
- Chan M.T., Cheng B.C., Lee T.M., Gin T.: BIS-guided anesthesia decreases postoperative delirium and cognitive decline. J Neurosurg Anesthesiol 2013; 25: pp. 33-42.
- Sieber F.E., Zakriya K.J., Gottschalk A., et. al.: Sedation depth during spinal anesthesia and the development of postoperative delirium in elderly patients undergoing hip fracture repair. Mayo Clin Proc 2010; 85: pp. 18-26.
- Hesse S., Kreuzer M., Hight D., et. al.: Association of electroencephalogram trajectories during emergence from anaesthesia with delirium in the postanaesthesia care unit: an early sign of postoperative complications. Br J Anaesth 2019; 122: pp. 622-634.
- Wildes T.S., Mickle A.M., Ben Abdallah A., et. al.: Effect of electroencephalography-guided anesthetic administration on postoperative delirium among older adults undergoing major surgery: the ENGAGES Randomized Clinical Trial. JAMA 2019; 321: pp. 473-483.
- Cheng H., Li Z., Young N., et. al.: The effect of dexmedetomidine on outcomes of cardiac surgery in elderly patients. J Cardiothorac Vasc Anesth 2016; 30: pp. 1502-1508.
- Su X., Meng Z.T., Wu X.H., et. al.: Dexmedetomidine for prevention of delirium in elderly patients after non-cardiac surgery: a randomised, double-blind, placebo-controlled trial. Lancet 2016; 388: pp. 1893-1902.
- Geng J., Qian J., Cheng H., Ji F., Liu H.: The influence of perioperative dexmedetomidine on patients undergoing cardiac surgery: a meta-analysis. PLoS One 2016; 11:
- Si Y., Zhang Y., Han L., et. al.: Dexmedetomidine acts via the JAK2/STAT3 pathway to attenuate isoflurane-induced neurocognitive deficits in senile mice. PLoS One 2016; 11:
- Deiner S., Luo X., Lin H.M., et. al.: Intraoperative infusion of dexmedetomidine for prevention of postoperative delirium and cognitive dysfunction in elderly patients undergoing major elective noncardiac surgery: a randomized clinical trial. JAMA Surg 2017; 152:
- Li X., Yang J., Nie X.L., et. al.: Impact of dexmedetomidine on the incidence of delirium in elderly patients after cardiac surgery: a randomized controlled trial. PLoS One 2017; 12:
- Skrobik Y., Duprey M.S., Hill N.S., Devlin J.W.: Low-dose nocturnal dexmedetomidine prevents ICU delirium. A randomized, placebo-controlled trial. Am J Respir Crit Care Med 2018; 197: pp. 1147-1156.
- Hudetz J.A., Patterson K.M., Iqbal Z., et. al.: Ketamine attenuates delirium after cardiac surgery with cardiopulmonary bypass. J Cardiothorac Vasc Anesth 2009; 23: pp. 651-657.
- Avidan M.S., Maybrier H.R., Abdallah A.B., et. al.: Intraoperative ketamine for prevention of postoperative delirium or pain after major surgery in older adults: an international, multicentre, double-blind, randomised clinical trial. Lancet 2017; 390: pp. 267-275.
- Chen J.Y., Jia J.E., Liu T.J., Qin M.J., Li W.X.: Comparison of the effects of dexmedetomidine, ketamine, and placebo on emergence agitation after strabismus surgery in children. Can J Anaesth 2013; 60: pp. 385-392.
- Dahmani S., Delivet H., Hilly J.: Emergence delirium in children: an update. Curr Opin Anaesthesiol 2014; 27: pp. 309-315.
- van den Boogaard M., Slooter A.J.C., Brüggemann R.J.M., et. al.: Effect of haloperidol on survival among critically ill adults with a high risk of delirium: the REDUCE randomized clinical trial. JAMA 2018; 319: pp. 680-690.
- Munk L., Andersen G., Møller A.M.: Post-anaesthetic emergence delirium in adults: Incidence, predictors and consequences. Acta Anaesthesiol Scand 2016; 60: pp. 1059-1066.
- Yu D., Chai W., Sun X., Yao L.: Emergence agitation in adults: risk factors in 2,000 patients. Can J Anaesth 2010; 57: pp. 843-848.
- Lepousé C., Lautner C.A., Liu L., Gomis P., Leon A.: Emergence delirium in adults in the post-anaesthesia care unit. Br J Anaesth 2006; 96: pp. 747-753.
- Kim H.J., Kim D.K., Kim H.Y., Kim J.K., Choi S.W.: Risk factors of emergence agitation in adults undergoing general anesthesia for nasal surgery. Clin Exp Otorhinolaryngol 2015; 8: pp. 46-51.
- Umholtz M., Cilnyk J., Wang C.K., Porhomayon J., Pourafkari L., Nader N.D.: Postanesthesia emergence in patients with post-traumatic stress disorder. J Clin Anesth 2016; 34: pp. 3-10.
- Fujisawa T., Komasawa N., Fujiwara A., Kido H., Minami T.: Effective dexmedetomidine administration for the prevention of emergence agitation and postoperative delirium in patients with a history of postoperative delirium. in Japanese Masui 2016; 65: pp. 395-397.
- Read M.D., Maani C.V., Blackwell S.: Dexmedetomidine as a rescue therapy for emergence delirium in adults: A case series. A Case Rep 2017; 9: pp. 20-23.
- Inouye S.K., Bogardus S.T., Charpentier P.A., et. al.: A multicomponent intervention to prevent delirium in hospitalized older patients. N Engl J Med 1999; 340: pp. 669-676.
- Marcantonio E.R., Flacker J.M., Wright R.J., Resnick N.M., et. al.: Reducing delirium after hip fracture: A randomized trial. J Am Geriatr Soc 2001; 49: pp. 516-522.
- Strøm C., Rasmussen L.S., Sieber F.E.: Should general anaesthesia be avoided in the elderly?. Anaesthesia 2014; 69: pp. 35-44.
- O’Brien H., Mohan H., Hare C.O., Reynolds J.V., Kenny R.A.: Mind over matter? The hidden epidemic of cognitive dysfunction in the older surgical patient. Ann Surg 2017; 265: pp. 677-691.
- Petersen R.C., Parisi J.E., Dickson D.W., et. al.: Neuropathologic features of amnestic mild cognitive impairment. Arch Neurol 2006; 63: pp. 665-672.
- Winblad B., Palmer K., Kivipelto M., et. al.: Mild cognitive impairment—beyond controversies, towards a consensus: report of the International Working Group on Mild Cognitive Impairment. J Intern Med 2004; 256: pp. 240-246.
- Greene N.H., Attix D.K., Weldon B.C., Smith P.J., McDonagh D.L., Monk T.G.: Measures of executive function and depression identify patients at risk for postoperative delirium. Anesthesiology 2009; 110: pp. 788-795.
- Crosby G., Culley D.J., Hyman B.T.: Preoperative cognitive assessment of the elderly surgical patient: a call for action. Anesthesiology 2011; 114: pp. 1265-1268.
- Monk T.G., Weldon B.C., Garvan C.W., et. al.: Predictors of cognitive dysfunction after major noncardiac surgery. Anesthesiology 2008; 108: pp. 18-30.
- Chen C.W., Lin C.C., Chen K.B., Kuo Y.C., Li C.Y., Chung C.J.: Increased risk of dementia in people with previous exposure to general anesthesia: a nationwide population-based case-control study. Alzheimers Dement 2014; 10: pp. 196-204.
- Bedford P.D.: Adverse cerebral effects of anaesthesia on old people. Lancet 1955; 269: pp. 259-263.
- Rudolph J.L., Schreiber K.A., Culley D.J., et. al.: Measurement of post-operative cognitive dysfunction after cardiac surgery: a systematic review. Acta Anaesthesiol Scand 2010; 54: pp. 663-677.
- Newman M.F., Kirchner J.L., Phillips-Bute B., et. al.: Longitudinal assessment of neurocognitive function after coronary-artery bypass surgery. N Engl J Med 2001; 344: pp. 395-402.
- Selnes O.A., Grega M.A., Bailey M.M., et. al.: Do management strategies for coronary artery disease influence 6-year cognitive outcomes?. Ann Thorac Surg 2009; 88: pp. 445-454.
- Moller J.T., Cluitmans P., Rasmussen L.S., et. al.: Long-term postoperative cognitive dysfunction in the elderly ISPOCD1 study. ISPOCD investigators. International Study of Post-Operative Cognitive Dysfunction Lancet 1998; 351: pp. 857-861.
- Abildstrom H., Rasmussen L.S., Rentowl P., et. al.: Cognitive dysfunction 1-2 years after non-cardiac surgery in the elderly. ISPOCD group. International Study of Post-Operative Cognitive Dysfunction. Acta Anaesthesiol Scand 2000; 44: pp. 1246-1251.
- Johnson T., Monk T., Rasmussen L.S., et. al.: Postoperative cognitive dysfunction in middle-aged patients. Anesthesiology 2002; 96: pp. 1351-1357.
- Rasmussen L.S., Johnson T., Kuipers H.M., et. al.: Does anaesthesia cause postoperative cognitive dysfunction? A randomised study of regional versus general anaesthesia in 438 elderly patients. Acta Anaesthesiol Scand 2003; 47: pp. 260-266.
- Silverstein J.H., Steinmetz J., Reichenberg A., Harvey P.D., Rasmussen L.S.: Postoperative cognitive dysfunction in patients with preoperative cognitive impairment: which domains are most vulnerable?. Anesthesiology 2007; 106: pp. 431-435.
- Steinmetz J., Christensen K.B., Lund T., Lohse N., Rasmussen L.S.: Long-term consequences of postoperative cognitive dysfunction. Anesthesiology 2009; 110: pp. 548-555.
- Steinmetz J., Siersma V., Kessing L.V., Rasmussen L.S.: Is postoperative cognitive dysfunction a risk factor for dementia? A cohort follow-up study. Br J Anaesth 2013; 110: pp. i92-i97.
- Fu H., Fan L., Wang T.: Perioperative neurocognition in elderly patients. Curr Opin Anaesthesiol 2018; 31: pp. 24-29.
- Jiang X., Chen D., Lou Y., Li Z.: Risk factors for postoperative delirium after spine surgery in middle- and old-aged patients. Aging Clin Exp Res 2017; 29: pp. 1039-1044.
- Mossello E., Pieraccioli M., Nesti N., et. al.: Effects of low blood pressure in cognitively impaired elderly patients treated with antihypertensive drugs. JAMA Intern Med 2015; 175: pp. 578-585.
- Chow W.B., Rosenthal R.A., Merkow R.P., et. al.: Optimal preoperative assessment of the geriatric surgical patient: a best practices guideline from the American College of Surgeons National Surgical Quality Improvement Program and the American Geriatrics Society. J Am Coll Surg 2012; 215: pp. 453-466.
- Zietlow K., McDonald S.R., Sloane R., Browndyke J., Lagoo-Deenadayalan S., Heflin M.T.: Preoperative cognitive impairment as a predictor of postoperative outcomes in a collaborative care model. J Am Geriatr Soc 2018; 66: pp. 584-589.
- Vichitvejpaisal P., Preechakoon B., Supaprom W., et. al.: The Montreal Cognitive Assessment as a screening tool for preoperative cognitive impairment in geriatric patients. J Med Assoc Thai 2015; 98: pp. 782-789.
- Long L.S., Shapiro W.A., Leung J.M.: A brief review of practical preoperative cognitive screening tools. Can J Anaesth 2012; 59: pp. 798-804.
- Krenk L., Rasmussen L.S., Kehlet H.: New insights into the pathophysiology of postoperative cognitive dysfunction. Acta Anaesthesiol Scand 2010; 54: pp. 951-956.
- Chen P.L., Yang C.W., Tseng Y.K., et. al.: Risk of dementia after anaesthesia and surgery. Br J Psychiatry 2014; 204: pp. 188-193.
- Ballard C., Jones E., Gauge N., et. al.: Optimised anaesthesia to reduce post operative cognitive decline (POCD) in older patients undergoing elective surgery, a randomised controlled trial. PLoS One 2012; 7:
- Rasmussen L.S., O’Brien J.T., Silverstein J.H., et. al.: Is peri-operative cortisol secretion related to post-operative cognitive dysfunction?. Acta Anaesthesiol Scand 2005; 49: pp. 1225-1231.
- Hudson A.E., Hemmings H.C.: Are anaesthetics toxic to the brain?. Br J Anaesth 2011; 107: pp. 30-37.
- Jevtovic-Todorovic V., Beals J., Benshoff N., Olney J.W.: Prolonged exposure to inhalational anesthetic nitrous oxide kills neurons in adult rat brain. Neuroscience 2003; 122: pp. 609-616.
- Wu C.L., Hsu W., Richman J.M., Raja S.N.: Postoperative cognitive function as an outcome of regional anesthesia and analgesia. Reg Anesth Pain Med 2004; 29: pp. 257-268.
- Guay J.: General anaesthesia does not contribute to long-term post-operative cognitive dysfunction in adults: a meta-analysis. Indian J Anaesth 2011; 55: pp. 358-363.
- Steinmetz J., Rasmussen L.S.: Cognitive deterioration after surgery. in Danish Ugeskr Laeger 2008; 170: pp. 4032-4034.
- Mashour G.A., Moore L.E., Lele A.V., Robicsek S.A., Gelb A.W.: Perioperative care of patients at high risk for stroke during or after non-cardiac, non-neurologic surgery: consensus statement from the Society for Neuroscience in Anesthesiology and Critical Care. J Neurosurg Anesthesiol 2014; 26: pp. 273-285.
- Zorrilla-Vaca A., Healy R., Grant M.C., et. al.: Intraoperative cerebral oximetry-based management for optimizing perioperative outcomes: a meta-analysis of randomized controlled trials. Can J Anaesth 2018; 65: pp. 529-542.
- Sprung J., Roberts R.O., Weingarten T.N., et. al.: Postoperative delirium in elderly patients is associated with subsequent cognitive impairment. Br J Anaesth 2017; 119: pp. 316-323.
- Lecker I., Wang D.S., Whissell P.D., Avramescu S., Mazer C.D., Orser B.A.: Tranexamic acid-associated seizures: causes and treatment. Ann Neurol 2016; 79: pp. 18-26.
- Vavilala M.S., Ferrari L.R., Herring S.A.: Perioperative care of the concussed patient: making the case for defining best anesthesia care. Anesth Analg 2017; 125: pp. 1053-1055.
- Powers W.J., Rabinstein A.A., Ackerson T., et. al.: 2018 Guidelines for the early management of patients with acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2018; 49: pp. e46-e110.
- Ng P.Y., Ng A.K., Subramaniam B., et. al.: Association of preoperatively diagnosed patent foramen ovale with perioperative ischemic stroke. JAMA 2018; 319: pp. 452-462.
- Christiansen M.N., Andersson C., Gislason G.H., et. al.: Risks of cardiovascular adverse events and death in patients with previous stroke undergoing emergency noncardiac, nonintracranial surgery: the importance of operative timing. Anesthesiology 2017; 127: pp. 9-19.
- Jørgensen M.E., Torp-Pedersen C., Gislason G.H., et. al.: Time elapsed after ischemic stroke and risk of adverse cardiovascular events and mortality following elective noncardiac surgery. JAMA 2014; 312: pp. 269-277.
- Rantner B., Kollerits B., Roubin G.S., et. al.: Early endarterectomy carries a lower procedural risk than early stenting in patients with symptomatic stenosis of the internal carotid artery: results from 4 randomized controlled trials. Stroke 2017; 48: pp. 1580-1587.
- Neumar R.W., Shuster M., Callaway C.W., et. al.: Part 1: executive summary: 2015 American Heart Association guidelines update for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation 2015; 132: pp. S315-S367.
- Srejic U., Larson P., Bickler P.E.: Little black boxes: noncardiac implantable electronic medical devices and their anesthetic and surgical implications. Anesth Analg 2017; 125: pp. 124-138.

BÌNH LUẬN