SÁCH DỊCH “Y HỌC CHU PHẪU: QUẢN LÝ HƯỚNG ĐẾN KẾT QUẢ, ẤN BẢN THỨ 2”
Được dịch và chuyển thể sang tiếng Việt từ sách gốc “Perioperative Medicine: Managing for Outcome, 2nd Edition”
Dịch và chú giải: Ths.Bs. Lê Đình Sáng – Hiệu đính: Ts.Bs.Lê Nhật Huy
CHƯƠNG 9. ĐÁNH GIÁ NGUY CƠ PHỔI
Pulmonary Risk Assessment – Ramesh Swamiappan and Maurizio Cereda
Perioperative Medicine, 9, 83-100
Giới thiệu
Biến chứng phổi hậu phẫu (PPCs) có tầm quan trọng lâm sàng không thể phủ nhận vì chúng thường xảy ra và gây ra gánh nặng đáng kể về bệnh tật và tử vong trong giai đoạn chu phẫu. Tỷ lệ PPCs được báo cáo khác nhau đáng kể giữa các nghiên cứu, từ 2% đến 40%, với một số yếu tố nguy cơ đã được xác định (Bảng 9.1). Những điểm không rõ ràng trong định nghĩa của PPCs và thiếu các nghiên cứu có hệ thống đã tạo ra nhiều thách thức hơn cho việc đánh giá nguy cơ phổi trong giai đoạn chu phẫu. Tuy nhiên, trong thập kỷ qua, các định nghĩa đã được cải thiện và các yếu tố nguy cơ đã được phân tích toàn diện và đưa vào các mô hình dự đoán kết quả đã được xác thực.
Bảng 9.1 Các yếu tố nguy cơ cho biến chứng phổi hậu phẫu.
| Bằng chứng mạnh | Bằng chứng khá | Không xác định |
|---|---|---|
| Yếu tố liên quan đến người bệnh | ||
| Tuổi cao | Tiền sử hút thuốc | Nhiễm trùng hô hấp trong tháng qua |
| ASA lớp >2 | Suy giảm cảm giác | GERD |
| Suy tim sung huyết | Sử dụng rượu | Sử dụng rượu |
| Phụ thuộc chức năng | Giảm cân | Tiểu đường |
| COPD | Béo phì | |
| Ngưng thở khi ngủ tắc nghẽn mức độ trung bình/nặng | ||
| Tăng huyết áp | ||
| Bệnh gan | ||
| Ung thư | ||
| Nhiễm trùng huyết | ||
| Hen suyễn | ||
| Suy thận | ||
| Cổ trướng | ||
| Sốc trước phẫu thuật | ||
| Yếu tố liên quan đến thủ thuật | ||
| Phình động mạch chủ | Truyền máu | Thủ thuật có nguy cơ cao cho ALI/ARDS |
| Ngực | Thủ thuật có nguy cơ cho UEPI | |
| Bụng | Ống thông mũi-dạ dày chu phẫu | |
| Bụng trên | Sử dụng thuốc phong bế thần kinh cơ tác dụng kéo dài | |
| Phẫu thuật thần kinh | Chiến lược thông khí cơ học | |
| Phẫu thuật kéo dài (>3 giờ) | Phẫu thuật bụng mở (so với nội soi) | |
| Đầu và cổ | Neostigmine | |
| Phẫu thuật khẩn cấp | Không sử dụng máy kích thích thần kinh ngoại vi | |
| Mạch máu | ||
| Gây mê toàn thân | ||
| Truyền máu | ||
| Xét nghiệm/kiểm tra trước phẫu thuật | ||
| Albumin huyết thanh thấp | X-quang ngực | Test ho dương tính |
| Urê máu | Độ bão hòa oxy trước phẫu thuật thấp | Biến thể di truyền |
| Thiếu máu | Tăng creatinine | |
| Kết quả xét nghiệm chức năng gan bất thường | ||
| Tiêu thụ oxy tối đa dự đoán | ||
| FEV1/FVC <0,7 và FEV1 <80% dự đoán |
Dịch tễ học
Khoảng 1 triệu người bệnh phẫu thuật có PPCs mỗi năm tại Hoa Kỳ. Các nghiên cứu đã chỉ ra rằng PPCs xảy ra ở 2%-12% các phẫu thuật không thuộc lồng ngực và lên đến 38% các phẫu thuật lồng ngực. Ở người bệnh sau phẫu thuật bụng lớn, tỷ lệ PPCs khoảng 6%.
Trong một nghiên cứu đa trung tâm, tỷ lệ tử vong trong 30 ngày được ước tính là 19,5% ở những người có PPC so với 0,5% ở những người không có PPC. Một nghiên cứu đoàn hệ tiến cứu trên người bệnh trải qua phẫu thuật không thuộc lồng ngực cho thấy rằng người bệnh phát triển PPC có thời gian nằm viện trung bình là 27,9 ngày so với giá trị trung bình là 4,5 ngày ở người bệnh không có PPC.
Một nghiên cứu trên những người thụ hưởng Medicare của Hoa Kỳ cho thấy rằng viêm phổi và suy hô hấp lần lượt chiếm 2,8% và 1,4% nguyên nhân tái nhập viện sau phẫu thuật. Chương trình Cải thiện Chất lượng Phẫu thuật Quốc gia của Trường Môn Phẫu thuật Hoa Kỳ (ACS-NSQIP) đã phân tích các yêu cầu của người bệnh nội trú Medicare và phát hiện rằng việc ngăn ngừa biến chứng hậu phẫu sẽ tránh được 41.846 trường hợp tái nhập viện và tiết kiệm 620 triệu đô la chi phí y tế công cộng mỗi năm.
Định nghĩa
Các nghiên cứu trước đây đã gộp các sự kiện có ý nghĩa lâm sàng đáng nghi ngờ, chẳng hạn như co thắt phế quản trong khi phẫu thuật hoặc sốt nhẹ, cùng với các biến chứng nghiêm trọng hơn, chẳng hạn như viêm phổi và suy hô hấp. Một cách tiếp cận có hệ thống hơn chỉ nên đánh giá những biến chứng có khả năng ảnh hưởng đến tỷ lệ tử vong, kéo dài thời gian nằm viện, hoặc yêu cầu điều trị cụ thể. Những thực thể lâm sàng này nên được xác định bởi các tiêu chí càng nghiêm ngặt và rõ ràng càng tốt, chẳng hạn như các tiêu chí đối với viêm phổi bệnh viện. Tuy nhiên, tỷ lệ biến chứng phổi được báo cáo là thay đổi ngay cả khi các tiêu chí nghiêm ngặt hơn được sử dụng để chẩn đoán PPCs, có lẽ do sự không đồng nhất của các quần thể được nghiên cứu và các thủ thuật phẫu thuật được thực hiện (Bảng 9.2). Sự khác biệt lớn giữa các nghiên cứu cũng là do khó khăn trong việc phân biệt từng biến chứng vì chúng có các con đường phụ thuộc lẫn nhau.
Bảng 9.2 Tỷ lệ biến chứng phổi hậu phẫu được báo cáo với các yếu tố nguy cơ liên quan đến thủ thuật khác nhau.
| Yếu tố nguy cơ liên quan đến thủ thuật | OR điều chỉnh cho PPCs (95% CI) | Tỷ lệ PPC (%) |
|---|---|---|
| Vị trí phẫu thuật | ||
| Động mạch chủ | 6,90 (2,74-17,36) | – |
| Mạch máu (động mạch chủ) | 2,10 (0,81-5,42) | 25,5 |
| Đầu và cổ | 2,21 (1,82-2,68) | 10,3 |
| Ngực | 4,24 (2,89-6,23) | – |
| Cắt thực quản | – | 18,9 |
| Bụng trên | – | 19,7 |
| Hông | – | 5,1 |
| Bụng dưới | – | 7,7 |
| Phẫu thuật thần kinh | 2,53 (1,84-3,47) | – |
| Phụ khoa và tiết niệu | – | 1,8 |
| Phẫu thuật kéo dài | 2,26 (1,47-3,47) | – |
| Phẫu thuật khẩn cấp | 2,52 (1,69-3,75) | – |
| Gây mê toàn thân | 2,35 (1,77-3,12) | – |
Viêm phổi có lẽ là PPC đơn lẻ quan trọng nhất vì nó có tác động xác định đến kết quả. Viêm phổi hậu phẫu đã được phát hiện ở 18,6% trong số 140 người bệnh trải qua phẫu thuật lớn và có liên quan đến tỷ lệ tử vong cao tới 21%. Co thắt phế quản trong chu phẫu dường như xảy ra ở một phần đáng ngạc nhiên nhỏ của dân số, ngay cả khi người bệnh hen suyễn được xem xét. Tuy nhiên, co thắt phế quản là biến chứng thường xuyên nhất ở những người hút thuốc có bằng chứng tắc nghẽn đường thở qua đo hô hấp ký. Gần đây, các định nghĩa Kết quả Lâm sàng Chu phẫu Châu Âu đã bao gồm một định nghĩa phổ quát về PPCs với danh sách toàn diện các thành phần (Bảng 9.3).
Bảng 9.3 Định nghĩa của biến chứng phổi hậu phẫu.
| Đo lường | Định nghĩa theo Canet và cộng sự 2010 | Định nghĩa khác |
|---|---|---|
| Suy hô hấp | PaO2 hậu phẫu <60 mmHg trên không khí phòng, tỷ lệ PaO2/FiO2 <300, hoặc độ bão hòa oxyhemoglobin động mạch đo bằng máy đo oxy xung <90% và yêu cầu liệu pháp oxy | Yêu cầu thông khí cơ học xâm lấn hoặc không xâm lấn |
| Nghi ngờ nhiễm trùng phổi | Điều trị bằng kháng sinh cho nhiễm trùng đường hô hấp, cộng với ít nhất một trong các tiêu chí sau: Đờm mới hoặc thay đổi, Tổn thương phổi mới hoặc thay đổi trên X-quang ngực được chỉ định về mặt lâm sàng, Nhiệt độ >38,3°C, Số lượng bạch cầu >12.000/mm3 | Các tiêu chí chẩn đoán lâm sàng cho viêm phổi bệnh viện |
| Xẹp phổi | Được gợi ý bởi đặc hóa phổi với sự chuyển dịch của trung thất, rốn, hoặc cơ hoành về phía vùng bị ảnh hưởng và giãn nở bù trừ ở phổi không xẹp liền kề | Yêu cầu can thiệp (soi phế quản, liệu pháp tư thế) |
| Viêm phổi do hít | Suy hô hấp sau khi hít phải nội dung dạ dày trào ngược | |
| Tràn khí màng phổi | Không khí trong khoang màng phổi không có giường mạch máu bao quanh màng phổi tạng | Yêu cầu dẫn lưu |
| Tràn dịch màng phổi | X-quang ngực thể hiện làm mờ góc sườn hoành, mất rõ nét đường viền của cơ hoành đồng bên | Yêu cầu dẫn lưu |
| Co thắt phế quản | Tiếng thở khò khè thở ra mới phát hiện được điều trị bằng thuốc giãn phế quản | Yêu cầu liệu pháp thuốc giãn phế quản |
| ARDS | Khởi phát cấp tính <1 tuần, thâm nhiễm hai bên trên CXR, thiếu oxy máu thể hiện bởi PaO2/FiO2 <300, bằng chứng tối thiểu của quá tải dịch nhĩ trái, PCWP <18 cm H2O | |
| Viêm phế quản | Đờm mủ với X-quang ngực bình thường, không kháng sinh đường tĩnh mạch | |
| Phù phổi | Sung huyết phổi/ứ đọng, phù phổi cấp, suy tim sung huyết | |
| Đợt cấp của bệnh phổi đã tồn tại | Không được định nghĩa thêm | |
| Thuyên tắc phổi | Không được định nghĩa thêm |
Căn nguyên và Sinh lý bệnh
Các cơ chế dẫn đến PPCs là phức tạp và chỉ được hiểu một phần. Các yếu tố liên quan đến bệnh lý đã tồn tại trước đó, chấn thương phẫu thuật, và gây mê tương tác trong việc chuẩn bị cho người bệnh phát triển PPC (Hình 9.1).

Hình 9.1. Cơ chế dẫn đến biến chứng phổi ở người bệnh phẫu thuật. FRC, Dung tích cặn chức năng.
Mất thể tích phổi trong chu phẫu với hậu quả là hình thành xẹp phổi được chấp nhận rộng rãi là một trong những cơ chế quan trọng nhất dẫn đến PPC. Xẹp phổi bắt đầu trong giai đoạn gây mê và thông khí cơ học và làm giảm trao đổi khí trong quá trình phẫu thuật và trong giai đoạn hậu phẫu sớm. Sử dụng chụp cắt lớp vi tính của ngực, Hedenstierna và cộng sự đã quan sát thấy các vùng nhỏ xẹp phế nang ngay sau khi gây mê toàn thân ở các đối tượng khỏe mạnh nhưng không thể chứng minh được hiện tượng tương tự ở người bệnh nhận gây mê ngoài màng cứng. Nguyên nhân hình thành xẹp phổi trong khi gây mê toàn thân là nhiều. Mô phổi có xu hướng tự nhiên hiển thị sự xẹp phế nang phụ thuộc vào trọng lực trong quá trình thông khí cơ học, như được gợi ý bởi thực tế là xẹp phổi nằm ở các phần nằm của phổi (Hình 9.2). Thông khí cơ học và giãn cơ gây ra sự di chuyển theo hướng đầu và giảm sự di chuyển hô hấp của phần sau của cơ hoành, một phát hiện giải thích sự phân bố chủ yếu theo hướng đuôi của các vùng xẹp phổi (Hình 9.3). Phần oxy được hít vào cao và áp lực căng phổi thấp hơn dẫn đến việc đóng đường thở phụ thuộc và xẹp phổi hấp thu sau đó. Ba cơ chế được giả thuyết cho xẹp phổi trong khi gây mê toàn thân là nén mô phổi, xẹp phổi hấp thu, và mất surfactant.

Hình 9.2. Tái tạo ba chiều của hình ảnh chụp cắt lớp vi tính ngực ở người được gây mê và liệt cơ. (Với sự cho phép từ Hedenstierna G. Sự xẹp phế nang và đóng đường thở: tác động thường xuyên của gây mê. Clin Physiol Funct Imaging 2003;23(3):123-129.)

Hình 9.3. Các góc nhìn bên của cơ hoành ở cuối hít vào (đường chấm chấm) và ở cuối thở ra (đường đậm) ở một đối tượng khỏe mạnh trong khi thở tự nhiên (A và B) và trong khi thông khí cơ học (C và D). Vùng giữa hai đường biểu thị sự di chuyển của cơ hoành. Hình ảnh với thể tích khí lưu thông cơ bản (A và C) và với thể tích khí lưu thông lớn (B và D) được hiển thị. Sự di chuyển tổng thể của cơ hoành bị giảm trong khi thông khí cơ học ở cả hai thể tích khí lưu thông. Phần sau (phần dưới của hình ảnh) của cơ hoành có sự giảm lớn nhất trong sự di chuyển theo nhịp thở. (Với sự cho phép từ Kleinman BS, Frey K, VanDrunen M, và cộng sự. Chuyển động của cơ hoành ở người bệnh mắc bệnh phổi tắc nghẽn mạn tính trong khi thở tự nhiên so với trong khi thở áp lực dương sau khi gây mê và giãn cơ thần kinh. Anesthesiology, 2002;97(2):298-305.)
Dung tích cặn chức năng giảm sau phẫu thuật, và những thay đổi được quan sát là lớn hơn khi vị trí vết mổ gần cơ hoành hơn. Đau và chấn thương phẫu thuật dẫn đến hạn chế sự mở rộng hít vào và là những yếu tố đóng góp quan trọng vào mất thể tích phổi hậu phẫu. Đau trong giai đoạn hậu phẫu ngay lập tức gây ra ức chế phản xạ tủy sống của dây thần kinh hoành do đầu vào cảm nhận đau đến sừng bụng và bụng bên của tủy sống, điều này ảnh hưởng đến chức năng cơ hoành. Có bằng chứng cho thấy sự thao tác phẫu thuật ở các tạng bụng trên dẫn đến rối loạn chức năng phản xạ của cơ hoành không liên quan đến đau, như được chỉ ra ở người bệnh sau phẫu thuật cắt túi mật nội soi. Xẹp phổi được coi là một biến chứng có liên quan trong chính nó, vì nó có thể gây ra thiếu oxy máu và suy hô hấp và cũng vì nó có thể dẫn đến viêm phổi. Tuy nhiên, mối liên kết nhân quả giữa xẹp phổi và viêm phổi vẫn chưa được chứng minh. Dữ liệu thực nghiệm cho thấy sự phát triển vi khuẩn hạn chế sau khi phục hồi phế nang trong một mô hình động vật bị viêm phổi, cho thấy rằng phổi xẹp cung cấp một môi trường thuận lợi cho nhiễm trùng.
Ngoài mất thể tích, các yếu tố khác đóng vai trò trong việc hình thành PPC và viêm phổi hậu phẫu. Một yếu tố quan trọng có lẽ là giữ lại chất nhầy do giảm ho do đau và thuốc và do rối loạn chức năng vận chuyển chất nhầy-lông chuyển trong niêm mạc đường thở. Vận chuyển chất nhầy-lông chuyển là một cơ chế quan trọng của phòng vệ phổi, và vận tốc của nó bị giảm bởi gây mê và bởi đặt nội khí quản với một ống có bóng chèn. Những người hút thuốc có tốc độ vận chuyển chất nhầy-lông chuyển giảm trong khi gây mê so với những người không hút thuốc, một phát hiện có thể giúp giải thích tỷ lệ cao của PPC ở những người bệnh này. Không rõ sự suy giảm chức năng này của vận chuyển chất nhầy kéo dài bao lâu sau khi kết thúc gây mê và rút ống.
Hít phải chất tiết hầu họng bị nhiễm khuẩn được cho là một cơ chế nổi bật dẫn đến viêm phổi bệnh viện và hậu phẫu. Giãn cơ tiềm ẩn dưới lâm sàng đã được phát hiện ở người bệnh đã nhận các thuốc giãn cơ tác dụng kéo dài, và nó có liên quan đến tỷ lệ biến chứng phổi tăng. Các tác dụng còn sót lại của thuốc phong bế thần kinh cơ gây ra xẹp phổi trong phòng hồi sức hậu phẫu. Khối phong bế còn sót lại được định nghĩa là tỷ lệ Kích thích Chuỗi 4 <0,9, có liên quan đến giá trị thấp hơn của dung tích sống gắng sức và của lưu lượng thở ra đỉnh được đo bằng kiểm tra chức năng phổi (PFT). Bảo vệ đường thở kém và hít phải chất tiết có lẽ thậm chí còn phổ biến hơn sau một số thủ thuật nhất định, chẳng hạn như cắt thực quản qua khe hoành, giải thích tỷ lệ 28,5% của PPCs được quan sát sau phẫu thuật này.
Cuối cùng, bệnh phổi tắc nghẽn mạn tính (COPD) gây ra các bất thường trao đổi khí và cơ học hô hấp làm giảm khả năng của người bệnh để chịu đựng bệnh phổi cấp tính chồng chất và làm cho họ dễ bị suy hô hấp. Ngoài ra, người bệnh COPD có rối loạn chức năng của cơ hô hấp do biến dạng thành ngực và do bệnh cơ. Những người bệnh này có thể không có khả năng chịu đựng nhu cầu thông khí tăng và công hô hấp cao hơn cần thiết trong thời kỳ hậu phẫu và có thể cần hỗ trợ thông khí sớm hơn so với người bệnh có chức năng cơ bình thường.
Đánh giá Phổi Trước Phẫu thuật cho Phẫu thuật Không thuộc Lồng ngực
Đánh giá phổi trước phẫu thuật là một phần không thể tách rời của đánh giá nguy cơ chung trước phẫu thuật. Đánh giá nên bắt đầu bằng việc thu thập thông tin về tình trạng sức khỏe tổng thể của người bệnh, sau đó tập trung vào hệ hô hấp và bao gồm một cuộc kiểm tra cẩn thận.
Phần lớn người bệnh trải qua các thủ thuật không thuộc lồng ngực ít có khả năng được hưởng lợi từ kiểm tra bằng dụng cụ. Họ nên tiến hành phẫu thuật, hoãn phẫu thuật, hoặc từ chối phẫu thuật mà không cần đánh giá thêm. Cách tiếp cận này nên giống nhau, bất kể loại phẫu thuật dự kiến, và khác với đánh giá của người bệnh ứng viên cho cắt bỏ phổi, được thảo luận sau trong chương này.
Để hiểu rõ hơn, các yếu tố nguy cơ cho PPC được nhóm thành các yếu tố người bệnh và các yếu tố phẫu thuật. Các yếu tố người bệnh bao gồm các yếu tố phổi và ngoài phổi, trong khi các yếu tố phẫu thuật bao gồm các yếu tố gây mê và phẫu thuật, được thảo luận riêng.
Các Yếu tố Người bệnh
CÁC YẾU TỐ PHỔI
Sau khi đánh giá tình trạng sức khỏe tổng thể, việc lấy tiền sử nên thu thập các yếu tố nguy cơ phổi cụ thể, chẳng hạn như bệnh phổi mạn tính hoặc cấp tính, tiền sử hút thuốc, và rối loạn thở liên quan đến giấc ngủ.
Sự hiện diện của COPD có liên quan đến tăng nguy cơ PPCs trong nhiều nghiên cứu. Trong quần thể NSQIP, chẩn đoán COPD trước đây là một yếu tố nguy cơ độc lập cho viêm phổi hậu phẫu (tỷ số chênh [OR], 1,71), đặt lại nội khí quản (OR 1,54), và thất bại trong việc cai thở máy (OR, 1,45). Ngay cả khi tiền sử COPD không được ghi nhận, sự hiện diện của nó nên được nghi ngờ dựa trên các yếu tố của tiền sử, chẳng hạn như tăng sản xuất đờm. Trong một nghiên cứu tiến cứu trên 148 cựu chiến binh trải qua phẫu thuật không thuộc lồng ngực, sự hiện diện của tăng sản xuất đờm trước phẫu thuật là một yếu tố dự đoán độc lập của PPC bằng phân tích đa biến. Một đánh giá có hệ thống của Smetana và cộng sự ở người bệnh COPD trải qua phẫu thuật không thuộc lồng ngực cho thấy rằng OR cho PPCs do COPD là 2,36.
Không rõ liệu tiền sử hen suyễn có liên quan đến tăng tỷ lệ PPCs có ý nghĩa lâm sàng hay không. Trong một đánh giá hồ sơ của 706 người bệnh hen suyễn trải qua phẫu thuật, Warner và cộng sự đã báo cáo một tỷ lệ nhỏ (1,7%) co thắt phế quản trong hoặc sau phẫu thuật. Tỷ lệ sự kiện này cao hơn ở người bệnh có đợt cấp hen suyễn gần đây. Tuy nhiên, tỷ lệ của các biến chứng nghiêm trọng hơn và suy hô hấp hậu phẫu (PRF) là không đáng kể trong nghiên cứu này. Trong cả hai nghiên cứu tiến cứu của McAlister và cộng sự, tiền sử hen suyễn không liên quan đến nguy cơ cao hơn của PPCs.
Tiền sử của quá trình phổi cấp tính gần đây hoặc đợt cấp của bệnh phổi đã tồn tại trước đó là một phát hiện có giá trị cao vì những người bệnh này dễ bị tăng phản ứng đường thở và thay đổi đáp ứng miễn dịch, thường liên quan đến việc sử dụng kháng sinh hoặc chính nhiễm trùng. Tiền sử như vậy được coi là một yếu tố nguy cơ phát triển PPCs và được cho là một lý do đầy đủ để hoãn phẫu thuật chọn lọc. Trong
nghiên cứu NSQIP, sự hiện diện của viêm phổi đã tồn tại trước đó có OR là 1,7 để phát triển PRF. Đối với người bệnh đã có gần đây hoặc đang có nhiễm trùng đường hô hấp trên, việc hoãn phẫu thuật có lẽ là thích hợp trong bối cảnh phẫu thuật chọn lọc, nhưng bằng chứng hỗ trợ quyết định này tương đối yếu. Các nghiên cứu đã báo cáo các giai đoạn giảm bão hòa oxy thường xuyên hơn nhưng không có biến chứng phổi lớn hoặc bệnh tật. Ví dụ, nhiễm trùng đường hô hấp trên gần đây đã làm phức tạp đáng kể quá trình hậu phẫu ở trẻ em sau phẫu thuật tim, nhưng có ít bằng chứng cho thấy vấn đề này cũng xảy ra ở người lớn. Trong nghiên cứu của Warner và cộng sự, người bệnh hen suyễn với nhiễm trùng đường hô hấp trên gần đây không có nguy cơ PPC tăng so với phần còn lại của quần thể. Trong một nghiên cứu tiến cứu, tiền sử nhiễm trùng đường hô hấp trên hoặc dưới không liên quan đến nguy cơ cao hơn của PPC. Tương tự, nhiễm trùng đường hô hấp trên gần đây không liên quan đến PPCs trong cả hai nghiên cứu của McAlister và cộng sự. Tuy nhiên, gần đây, Canet và cộng sự đã đưa vào nghiên cứu của họ những người bệnh đã có nhiễm trùng đường hô hấp trên và dưới gần đây với tiền sử sốt và sử dụng kháng sinh gần đây. Họ phát hiện rằng 17,2% quần thể nghiên cứu (n = 2464) phát triển một hoặc nhiều PPCs, và nhiễm trùng đường hô hấp gần đây là một yếu tố nguy cơ độc lập.
Sự hiện diện của khó thở và không dung nạp tập thể dục nên được điều tra trong quá trình đánh giá trước phẫu thuật vì những triệu chứng này đã được liên quan đến nguy cơ PPCs. Mối liên hệ giữa khó thở và PPCs không được xác nhận trong các nghiên cứu trước đây. Thực tế, đây không phải là một tiêu chí trong chỉ số nguy cơ được đề xuất bởi Arozullah. Tuy nhiên, khó thở đã được đưa vào mô hình điểm nguy cơ Đánh giá Nguy cơ Hô hấp ở Người bệnh Phẫu thuật ở Catalonia (ARISCAT) được đề xuất bởi Canet và cộng sự, đã được xác thực trong một nghiên cứu đoàn hệ quan sát đa trung tâm tiến cứu.
Có tiền sử sử dụng thuốc lá có lẽ là yếu tố nguy cơ vững chắc nhất cho PPC, vì hút thuốc đã được xác định là một yếu tố dự đoán độc lập của PPC bởi một số nghiên cứu. Ở những người bệnh không phải là người hút thuốc hiện tại, nguy cơ mắc PPC giảm theo thời gian kể từ khi ngừng hút thuốc, nhưng không rõ cần bao nhiêu thời gian để nguy cơ này giảm tối ưu. Warner và cộng sự báo cáo rằng người bệnh bỏ hút thuốc dưới 8 tuần trước phẫu thuật có tỷ lệ PPC cao hơn so với người bệnh bỏ sớm hơn. Tuy nhiên, một thời gian không hút thuốc dài hơn dường như cần thiết để giảm nguy cơ PPCs xuống mức của quần thể không hút thuốc, như được gợi ý bởi nghiên cứu của Arozullah và cộng sự, cho thấy rằng đã hút thuốc trong vòng 1 năm trước phẫu thuật làm tăng nguy cơ viêm phổi so với các người bệnh còn lại. Trên cơ sở kết quả nghiên cứu, người ta đã đề xuất rằng những người hút thuốc không bỏ hoàn toàn hoặc bỏ dưới 8 tuần trước phẫu thuật có thể có nguy cơ PPC tăng không chỉ so với quần thể không hút thuốc mà còn so với người bệnh đã tiếp tục hút thuốc. Kết quả của các nghiên cứu của McAlister và cộng sự gợi ý rằng mức độ tiêu thụ thuốc lá trước đó có thể là một yếu tố nguy cơ quan trọng hơn cho PPCs so với thời điểm bỏ hút thuốc. Canet và cộng sự quan sát thấy rằng PPC có liên quan đến số gói-năm đã hút và tiền sử hút thuốc hơn 40 gói-năm có liên quan đến PPCs trong phân tích hai biến. Trong một phân tích tổng hợp gần đây, hút thuốc trước phẫu thuật được phát hiện có liên quan đến PPCs (nguy cơ tương đối [RR]=1,73; khoảng tin cậy 95% [CI], 1,35-2,23) nhưng không liên quan đến tỷ lệ tử vong sau phẫu thuật.
Sự hiện diện của ngưng thở khi ngủ có thể liên quan đến tỷ lệ biến chứng chu phẫu tăng. Thực tế, OSA đi kèm với một nhóm các bệnh đồng mắc có thể ảnh hưởng đến kết quả phẫu thuật. Các bệnh này bao gồm tăng huyết áp hệ thống và tăng áp phổi (PH), suy tim phải, tiểu đường, béo phì và đột quỵ. Tuy nhiên, cũng là một nhận thức phổ biến rằng bản thân OSA có thể độc lập làm tăng nguy cơ biến chứng của phẫu thuật và gây mê. Người bệnh mắc rối loạn thở liên quan đến giấc ngủ có giảm khả năng kiểm soát trương lực cơ đường thở và thông khí trong khi ngủ, điều này bị trầm trọng hơn bởi các thuốc giảm đau opioid tác dụng kéo dài và bởi tác dụng còn sót lại của thuốc gây mê trong giai đoạn hậu phẫu. Các vấn đề về đường thở, thiếu oxy máu hậu phẫu, và suy hô hấp xảy ra theo cách phụ thuộc vào mức độ nghiêm trọng ở người bệnh OSA trải qua phẫu thuật đường thở trên. Tuy nhiên, có bằng chứng hạn chế cho thấy OSA có liên quan đến bệnh tật trong các loại phẫu thuật khác. Memtsoudis và cộng sự đã phân tích một cơ sở dữ liệu quốc gia để đánh giá ảnh hưởng của rối loạn thở khi ngủ đối với kết quả phổi trong các quần thể phẫu thuật chỉnh hình và phẫu thuật tổng quát và phát hiện ra tăng nguy cơ kết quả phổi xấu hơn, bao gồm viêm phổi hít, hội chứng suy hô hấp cấp tính (ARDS), và đặt nội khí quản khẩn cấp, nhưng không phải tắc mạch phổi.
BẢN CÂU HỎI STOP-BANG
Trong một nghiên cứu của Canada về người bệnh phẫu thuật, điểm STOP-Bang từ 5-8 xác định người bệnh có xác suất cao mắc OSA mức độ trung bình/nặng với độ đặc hiệu cao (Bảng 9.4). Các khuyến nghị của Lực lượng đặc nhiệm Hiệp hội Gây mê Hoa Kỳ (ASA) như sau: ▪ Áp lực đường thở dương liên tục nên được bắt đầu ở người bệnh bị OSA nặng trước phẫu thuật. ▪ Có tài liệu không đủ để đưa ra hướng dẫn về việc người bệnh nào mắc OSA có thể được quản lý an toàn trên cơ sở nội trú so với ngoại trú. Đó nên là quyết định kết hợp giữa bác sĩ phẫu thuật và bác sĩ gây mê, được cá nhân hóa cho người bệnh. ▪ Không khuyến nghị nghiên cứu giấc ngủ thường quy cho tất cả người bệnh mắc OSA. ▪ Ở người bệnh đã có phẫu thuật chỉnh sửa đường thở, chẳng hạn như uvulopalatopharyngoplasty hoặc phẫu thuật đẩy xương hàm dưới về phía trước, nên giả định rằng họ vẫn có nguy cơ biến chứng OSA trừ khi được chứng minh là không còn bởi một nghiên cứu giấc ngủ bình thường hoặc đảo ngược các triệu chứng.
Bảng 9.4 Điểm STOP-BANG
| Câu hỏi | Nội dung |
|---|---|
| 1. Ngáy (Snoring) | Bạn có ngáy to (to hơn nói chuyện hoặc đủ to để nghe được qua cửa đóng)? |
| 2. Mệt mỏi (Tired) | Bạn có thường cảm thấy mệt mỏi, kiệt sức, hoặc buồn ngủ vào ban ngày? |
| 3. Quan sát thấy ngưng thở (Observed apnea) | Có ai đã quan sát thấy bạn ngừng thở trong khi ngủ không? |
| 4. Huyết áp (Blood pressure) | Bạn có hoặc đang được điều trị tăng huyết áp không? |
| 5. BMI | Có lớn hơn 35 kg/m² không? |
| 6. Tuổi (Age) | Tuổi trên 50? |
| 7. Chu vi cổ (Neck circumference) | Chu vi cổ lớn hơn 40 cm? |
| 8. Giới tính (Gender) | Giới tính nam? |
Tính 1 điểm cho mỗi kết quả dương tính. Diễn giải: 0-2 = nguy cơ thấp; 3-4 = nguy cơ trung bình; 5-8 = nguy cơ cao cho OSA
Khám Thể chất
Khám thể chất là một công cụ thiết yếu khác trong đánh giá trước phẫu thuật về tình trạng phổi của người bệnh vì nó cho phép phát hiện bệnh phổi không được nhận ra. Mặc dù chẩn đoán bệnh phổi mạn tính thường được thực hiện bằng kiểm tra bằng dụng cụ, sự kết hợp của dữ liệu từ tiền sử người bệnh và từ khám thể chất có độ chính xác hợp lý trong dự đoán sự hiện diện của COPD. Lawrence và cộng sự đã ghi nhận rằng có kết quả khám thể chất ngực bất thường là một yếu tố dự đoán độc lập của PPCs. Tuy nhiên, các bất thường chính xác được phát hiện không được chỉ định, do đó làm giảm khả năng áp dụng kết quả của họ. Các nghiên cứu của McAlister và cộng sự có thông tin hơn vì họ đã đánh giá nghiêm ngặt các phát hiện thể chất cụ thể và phát hiện mối tương quan đáng kể giữa các phát hiện này và nguy cơ PPCs (Bảng 9.5). Trong các nghiên cứu này, nhiều phát hiện thể chất có tương quan với tỷ lệ PPCs, và hai trong số đó là các yếu tố dự đoán độc lập của biến chứng: giảm chiều cao thanh quản và test ho dương tính. Sự hiện diện của tiếng thở khò khè trên nghe thính phổi tiêu chuẩn thường được coi là một dấu hiệu thể chất quan trọng, nhưng nó không liên quan đáng kể với nguy cơ cao hơn của PPCs trong các nghiên cứu này. Kết quả này phù hợp với một nghiên cứu trước đó trong đó giảm chiều cao thanh quản là một yếu tố dự đoán độc lập của sự hiện diện của COPD được chẩn đoán bằng đo hô hấp ký, trong khi tiếng thở khò khè thì không. Những nghiên cứu này gợi ý rằng các phát hiện đơn giản thu được thông qua một cuộc khám thể chất có phương pháp có thể giúp trong việc dự đoán xác suất của PPCs. Tuy nhiên, không có thông số khám thể chất nào đã được thêm vào trong các mô hình dự đoán nguy cơ hiện tại, chủ yếu được lấy từ dữ liệu hồ sơ y tế.
Bảng 9.5 Các phát hiện thể chất liên quan đến tăng nguy cơ biến chứng phổi hậu phẫu.
| Phát hiện | Kỹ thuật | Tỷ số chênh (95% CI) | Giá trị p |
|---|---|---|---|
| Test ho dương tính | Ho một lần sau khi hít sâu gây ra ho tái phát | 4,3 (1,5-12,3)ᵃ
3,84 (1,51-9,80)ᵇ |
0,01
0,01 |
| Test thở khò khè dương tính | Thở khò khè sau năm lần hít vào/thở ra sâu | 3,4 (1,2-9,4)ᵃ
0,94 (0,12-7,08)ᵇ |
0,04
1,00 |
| Thời gian thở ra gắng sức ≥9 giây | Thời gian thở ra gắng sức sau một lần hít sâu | 5,7 (2,3-14,2)ᵃ
4,28 (1,22-15,02)ᵇ |
0,0002
0,04 |
| Chiều cao thanh quản tối đa ≤4 cm | Khoảng cách giữa hõm ức và đỉnh của sụn giáp ở cuối thở ra | 6,9 (2,7-17,4)ᵃ
1,17 (0,44-3,12)ᵇ |
<0,0001
0,79 |
| Thở khò khè trong nghe thính phổi tiêu chuẩn | Sự hiện diện hoặc vắng mặt của thở khò khè trong kiểm tra ngực tiêu chuẩn | 3,1 (0,9-10,0)ᵃ
2,39 (0,54-10,51)ᵇ |
0,13
0,23 |
CÁC YẾU TỐ NGOÀI PHỔI
Việc đánh giá tiền sử chung của người bệnh là quan trọng để tăng độ chính xác của đánh giá phổi trước phẫu thuật vì một số yếu tố ngoài phổi có tương quan với xác suất của PPCs. Tuổi cao có lẽ là một yếu tố nguy cơ quan trọng. Các nghiên cứu ban đầu không bao gồm phân tích đa biến để tính đến sự hiện diện của các bệnh đồng thời ở người bệnh lớn tuổi và có lẽ đã bị sai sót. Các nghiên cứu sau đó đã tính đến các điều kiện khác xác nhận rằng có một mối liên hệ giữa tuổi và PPC tồn tại. Li và cộng sự tìm thấy mối liên hệ của tuổi như một yếu tố nguy cơ độc lập cho biến chứng hậu phẫu ở người bệnh trải qua sửa chữa phình động mạch chủ bụng (AAA). Kết quả tương tự được thể hiện trong hai nghiên cứu ở người bệnh trải qua phẫu thuật không thuộc lồng ngực. Arozullah và cộng sự phát hiện một mối liên hệ độc lập của tuổi cao với cả suy thông khí hậu phẫu và viêm phổi hậu phẫu. Người bệnh lớn hơn 80 tuổi có khả năng có PPCs cao hơn 5,1 lần so với người bệnh trẻ hơn 50 tuổi. Những nghiên cứu này sử dụng phân tích đa biến và đáp ứng các tiêu chí của một thiết kế chất lượng cao cho việc đánh giá các biến tiên lượng. Khía cạnh này là có liên quan ở đây trong bối cảnh tỷ lệ phẫu thuật ở người bệnh cao tuổi ngày càng tăng.
Các yếu tố không phổi khác có liên quan đến nguy cơ PPCs. Arozullah và cộng sự báo cáo rằng các chỉ số về tình trạng dinh dưỡng kém, chẳng hạn như nồng độ albumin huyết thanh thấp và tiền sử giảm cân, và các chỉ số về tình trạng thể tích máu thay đổi, chẳng hạn như nồng độ nitơ urê máu bất thường, tất cả đều liên quan đến PRF và viêm phổi. Trong cùng các nghiên cứu này, một xác suất PPCs tăng cũng được quan sát thấy ở người bệnh có tiền sử tình trạng chức năng phụ thuộc, sử dụng rượu gần đây, tiểu đường, suy tim sung huyết, và suy thận. Suy giảm thần kinh trước phẫu thuật và tiền sử đột quỵ cũng đã được báo cáo là các yếu tố dự đoán độc lập của PPCs trong hơn một nghiên cứu, có lẽ do tăng xảy ra hít phải chất tiết dạ dày hoặc hầu họng. Bằng chứng cho thấy suy tim sung huyết là một trong những yếu tố nguy cơ đáng kể cho PPCs (OR, 2,93; CI, 1,02-8,43).
Phân loại ASA là một công cụ hợp lý để đánh giá tình trạng thể chất tổng thể của người bệnh, và điểm số của nó có liên quan đến tỷ lệ biến chứng hậu phẫu. Nhiều nghiên cứu đã phát hiện một mối tương quan của điểm ASA với PPCs. Điểm ASA cao hơn 2 có giá trị dự đoán của PPCs sau phẫu thuật bụng. Trong một nghiên cứu dọc tiến cứu, sự đồng thời của tuổi cao và điểm ASA >2 xác định phần lớn (88%) người bệnh phát triển bất kỳ PPC nào. Gupta và cộng sự đã phân tích dữ liệu NSQIP và nghiên cứu các biến trước phẫu thuật liên quan đến PPCs. Sau phân tích đa biến, người bệnh trong ASA lớp IV có OR là 1,28 (CI, 1,04-1,57) cho PPCs. Gần đây, ASA đã được đưa vào như một thành phần của chỉ số nguy cơ PRF được đề xuất bởi Gupta và cộng sự.
Các hệ thống phân loại sức khỏe khác không tập trung cụ thể vào hệ hô hấp có thể hữu ích trong đánh giá phổi. Cả chỉ số nguy cơ tim mạch Goldman và chỉ số bệnh đồng mắc Charlson đều đã được báo cáo là có liên quan đến tỷ lệ PPCs. Sự phụ thuộc chức năng trước phẫu thuật và trạng thái cảm giác thay đổi đã được chứng minh là các yếu tố nguy cơ. Thiếu máu trước phẫu thuật được định nghĩa bằng hemoglobin <10g% đã được chứng minh là liên quan đến nguy cơ phát triển PPC cao gấp ba lần. Đồng thời, không có bằng chứng rõ ràng cho thấy truyền máu trước phẫu thuật loại bỏ nguy cơ.
Các yếu tố nguy cơ khác được hỗ trợ bởi bằng chứng không đồng nhất, bao gồm trào ngược dạ dày thực quản, lạm dụng rượu, giảm cân, chẩn đoán ung thư hoặc nhiễm trùng huyết, và test ho dương tính. Không có bằng chứng mạnh mẽ để nói rằng khả năng tập thể dục, tiểu đường, và nhiễm virút suy giảm miễn dịch ở người có phải là yếu tố nguy cơ độc lập cho PPCs hay không.
Thường giả định rằng người bệnh béo phì có nguy cơ cao mắc PPCs, nhưng niềm tin này đã bị nghi ngờ dựa trên các nghiên cứu không phát hiện tương quan giữa béo phì và PPCs. Ví dụ, một nghiên cứu trên người bệnh trải qua mở ngực không tìm thấy nguy cơ PPCs cao hơn ở người bệnh béo phì. Tuy nhiên, các yếu tố liên quan đến loại phẫu thuật và lựa chọn người bệnh trong các nghiên cứu này có thể giải thích kết quả này, vì các nghiên cứu khác đã phát hiện một mối tương quan giữa béo phì và PPCs. Thực tế, chỉ số khối cơ thể (BMI) cao là một yếu tố dự đoán độc lập của PPCs bằng phân tích đa biến trong ít nhất hai nghiên cứu. Trong nghiên cứu mù tiến cứu của McAlister và cộng sự, BMI >30 kg/m2 có liên quan đến tăng nguy cơ PPCs bằng phân tích một biến, mặc dù mối tương quan không đáng kể bằng phân tích đa biến. Hướng dẫn của Trường Trường Môn Bác sĩ Hoa Kỳ (ACP) nêu rằng béo phì không phải là một yếu tố nguy cơ đáng kể cho PPCs và không nên ảnh hưởng đến việc lựa chọn người bệnh cho các thủ thuật nguy cơ cao khác. Tuyên bố này đúng ngay cả với người bệnh béo phì bệnh lý.
Các Yếu tố Phẫu thuật
Nhiều nghiên cứu đã báo cáo tương quan giữa các yếu tố phẫu thuật và tỷ lệ PPCs (Bảng 9.6), cả loại phẫu thuật và vị trí của vết mổ đều là những yếu tố đóng góp chính vào nguy cơ phổi này. Trong các nghiên cứu của Arozullah và cộng sự, phẫu thuật động mạch chủ bụng, ngực, và bụng trên là những yếu tố dự đoán độc lập mạnh nhất của PPC vì chúng có OR cao nhất cho suy hô hấp và viêm phổi. Các nghiên cứu khác đã báo cáo tăng nguy cơ PPCs trong phẫu thuật bụng và đặc biệt là sau các vết mổ bụng trên. Trên thực tế, nguy cơ PPCs cao hơn khi vết mổ gần cơ hoành hơn. McAlister và cộng sự phát hiện một mối tương quan giữa tỷ lệ PPCs và phẫu thuật bụng, mặc dù điều này không được xác nhận bằng phân tích một biến. Sự khác biệt này với các nghiên cứu trước đó có thể được giải thích bởi thực tế là chỉ một thiểu số người bệnh nghiên cứu đã trải qua phẫu thuật bụng trên trong nghiên cứu của McAlister. Phẫu thuật khẩn cấp có liên quan đến nguy cơ PPC cao hơn. Trong các nghiên cứu NSQIP, cả phẫu thuật thần kinh và phẫu thuật cổ đều có liên quan đến tăng nguy cơ suy hô hấp và viêm phổi, gợi ý một vai trò của việc bảo vệ đường thở kém trong việc hình thành PPC, mặc dù OR không cao như đối với phẫu thuật ngực bụng.
Bảng 9.6 Các yếu tố dự đoán độc lập của biến chứng phổi hậu phẫu thu được từ dữ liệu trong phẫu thuật.
| Yếu tố nguy cơ trong phẫu thuật | Ý nghĩa |
| Thời gian gây mê hoặc phẫu thuật | OR (CI), 4,9 (2,4-10,1) với >2 giờ và 9,7 (4,7-19,9) khi >3 giờ |
| Loại gây mê | Gây mê vùng giảm tỷ lệ tử vong trong 30 ngày, tỷ lệ nguy cơ (CI), 0,71 (0,53-0,94) |
| Loại phẫu thuật | Nội soi so với phẫu thuật mở được báo cáo có ít biến chứng hơn (ảnh hưởng của tăng IAP trên xẹp phổi)
Phẫu thuật khẩn cấp: biến chứng cao hơn so với theo kế hoạch |
| Vị trí phẫu thuật | Thuốc phong bế thần kinh cơ tác dụng kéo dài trong GA: yếu tố nguy cơ
Phẫu thuật cổ, ngực, bụng trên, phẫu thuật thần kinh và phẫu thuật phình động mạch chủ bụng Khoảng cách từ vết mổ đến cơ hoành tỷ lệ nghịch với tỷ lệ biến chứng Biến chứng phẫu thuật bụng trên tăng lên một hệ số 1,5 |
| Truyền máu | Hơn 4 đơn vị |
| Thông khí cơ học >48 giờ | Yếu tố dự đoán của VALI |
| NGT | Sự hiện diện liên quan đến VAP và PP, khuyến nghị đặt NGT có chọn lọc hơn là thường quy |
Sự lựa chọn cách tiếp cận phẫu thuật có thể ảnh hưởng đáng kể đến nguy cơ PPCs. Có một số bằng chứng cho thấy việc thực hiện phẫu thuật nội soi có liên quan đến giảm PPCs, như được chỉ ra bởi Hall và cộng sự. Trong một nghiên cứu ngẫu nhiên, người bệnh trải qua nẹp đáy dạ dày nội soi có chức năng hô hấp tốt hơn và thời gian nằm viện ngắn hơn so với người bệnh được thực hiện thủ thuật mở. Nhưng không rõ liệu rối loạn chức năng phổi giảm có chuyển thành sự khác biệt có ý nghĩa lâm sàng trong tỷ lệ PPC hay không. Sự ra đời của sửa chữa phình động mạch nội mạch có khả năng sẽ ảnh hưởng đến tỷ lệ PPCs. Trên thực tế, một nghiên cứu gần đây của Châu Âu đã phân tích một sổ đăng ký mạch máu toàn quốc của người bệnh trải qua sửa chữa mở so với sửa chữa phình động mạch chủ bụng nội mạch, phát hiện một nguy cơ PPCs nặng nhỏ hơn đáng kể ở những người bệnh nhận sửa chữa nội mạch (1,0% so với 6,9%). Cắt túi mật nội soi có liên quan đến thời gian hồi phục ngắn hơn, giảm thể tích phổi hậu phẫu ít hơn, và ít đau hậu phẫu hơn so với cắt túi mật mở, với tỷ lệ PPCs khoảng 2,7% và 17,2%, tương ứng (P < 0,05).
Trong số các yếu tố trong khi phẫu thuật, thời gian gây mê và phẫu thuật có lẽ là một trong những yếu tố dự đoán PPCs đáng tin cậy nhất, và mối liên hệ này đã được phát hiện bởi hơn một nghiên cứu. McAlister và cộng sự báo cáo rằng thời gian gây mê dài hơn 2,5 giờ là một yếu tố dự đoán độc lập của PPCs, với OR là 3,3. Thời gian gây mê là một yếu tố nguy cơ độc lập cho PPCs cũng trong một nghiên cứu tiến cứu của Mitchell và cộng sự. Tuy nhiên, không rõ liệu thời gian của thủ thuật có ảnh hưởng đến PPCs độc lập với độ phức tạp và loại thủ thuật hay không. Trong một nghiên cứu đoàn hệ dựa trên quần thể, thời gian phẫu thuật hơn 3 giờ có liên quan đến tỷ lệ PPC là 21% so với 2,5% nếu thời gian ngắn hơn 2 giờ. Mối tương quan này được duy trì trong phân tích đa biến.
Liên quan đến kỹ thuật gây mê, bằng chứng về tầm quan trọng của loại gây mê là không rõ ràng. Trong các nghiên cứu NSQIP, gây mê toàn thân có liên quan đến nguy cơ suy thông khí và viêm phổi cao hơn, với OR lần lượt là 1,91 và 1,56. Tuy nhiên, trong cả hai nghiên cứu của McAlister và cộng sự, gây mê toàn thân không có tương quan với nguy cơ PPCs. Việc đánh giá loại gây mê như một yếu tố nguy cơ cho PPCs thông qua các nghiên cứu quan sát bị phức tạp bởi thực tế là tác dụng của gây mê không dễ dàng phân biệt với tác dụng của vị trí phẫu thuật. Trên thực tế, gây mê toàn thân thường xuyên hơn trong các phẫu thuật có nguy cơ cao của PPCs, chẳng hạn như phẫu thuật ngực bụng, và tương đối ít thường xuyên được lựa chọn trong phẫu thuật ngoại vi. Trong một đánh giá dữ liệu trên người bệnh COPD từ cơ sở dữ liệu NSQIP (2005-2010), người bệnh nhận gây mê vùng so với người bệnh nhận gây mê toàn thân có tỷ lệ viêm phổi hậu phẫu thấp hơn (0,3% so với 1,3%; P = 0,03) với giảm nguy cơ tuyệt đối là 1,0%. Trong phân tích này, phụ thuộc máy thở kéo dài (2,1% so với 0,9%; P = 0,0008) và đặt nội khí quản hậu phẫu không theo kế hoạch (2,6% so với 1,8%; P = 0,04) thường xuyên hơn trong gây mê toàn thân so với gây mê vùng. Việc đánh giá lựa chọn gây mê như một chiến lược để giảm nguy cơ PPCs sẽ được thảo luận trong Chương 20.
Việc sử dụng ống dạ dày trong chu phẫu có lẽ là một yếu tố nguy cơ cho sự phát triển của PPCs. Ít nhất hai nghiên cứu tiến cứu đã báo cáo rằng việc sử dụng ống mũi-dạ dày chu phẫu là một yếu tố dự đoán độc lập của PPCs. Mối tương quan này được xác nhận bằng phân tích đa biến, điều này gợi ý rằng chính việc hút dạ dày, chứ không phải việc sử dụng nó trong các thủ thuật có nguy cơ cao, gây ra PPCs. Cơ chế gây ra PPCs bởi ống mũi-dạ dày có lẽ là do các phản xạ đường thở giảm và hít phải chất tiết hầu họng.
Xét nghiệm Trước Phẫu thuật
Xét nghiệm trước phẫu thuật chỉ có giá trị nếu nó cung cấp dữ liệu không thể thu được từ tiền sử và khám thể chất và nếu nó giúp xác định xác suất của một biến chứng ở người bệnh đã biết có yếu tố nguy cơ. Các xét nghiệm trước phẫu thuật thường được yêu cầu để đánh giá nguy cơ phổi bao gồm các PFT, khí máu động mạch, X-quang ngực, và ít phổ biến hơn, kiểm tra tập thể dục và siêu âm tim.
PFT đã được sử dụng để sàng lọc bệnh phổi không rõ và để phân tầng nguy cơ cho người bệnh, giả định một mối quan hệ giữa mức độ nghiêm trọng của bất thường PFT và xác suất của PPCs. Dựa trên bằng chứng hiện có, PFT không có khả năng đáp ứng cả hai mục đích này. PFT có lẽ không phải là không thể thiếu cho việc xác định người bệnh có bệnh phổi, như được gợi ý bởi các nghiên cứu trong đó việc lấy tiền sử và khám thể chất có độ chính xác hợp lý trong chẩn đoán COPD.
Các nghiên cứu nghiêm ngặt hơn hoặc không thể chứng minh mối tương quan giữa PFT và tỷ lệ PPCs hoặc không thể xác nhận bằng phân tích đa biến rằng dữ liệu PFT là các yếu tố dự đoán độc lập của PPCs. Trong một nghiên cứu đối chứng trường hợp của Lawrence và cộng sự, các chỉ số bệnh đồng mắc và khám ngực bất thường có liên quan độc lập với PPCs, trong khi kết quả PFT thì không. Mitchell và cộng sự đã chỉ ra rằng, ở người bệnh trải qua phẫu thuật chọn lọc tổng quát, kết quả PFT không có tương quan đáng kể với PPCs, không giống như sản xuất đờm trước phẫu thuật, thời gian của thủ thuật, và sử dụng ống mũi-dạ dày.
Một lời giải thích có thể cho những kết quả này là các yếu tố khác, chẳng hạn như tình trạng thể chất tổng thể và các bệnh đồng mắc không phổi, có thể quan trọng hơn mức độ tắc nghẽn đường thở trong việc tạo điều kiện cho PPCs. Các nghiên cứu khác cũng gợi ý rằng dữ liệu phổi và không phổi thu thập thông qua đánh giá lâm sàng chứa phần lớn thông tin cần thiết để đưa ra dự đoán nguy cơ, làm cho thông tin thu được từ PFT trở nên thừa.
Trong các nghiên cứu của McAlister và cộng sự, dữ liệu PFT có liên quan đáng kể với tỷ lệ PPCs. Tuy nhiên, không có biến PFT nào được tìm thấy là yếu tố dự đoán độc lập của PPCs bằng phân tích đa biến, trong khi các biến như tiền sử hút thuốc, thời gian gây mê, và các phát hiện khám thể chất được chọn có liên quan độc lập với PPCs. Những kết quả này ngụ ý rằng không có thông tin nào được thêm vào bằng cách thường quy thực hiện PFT trong đánh giá lâm sàng của người bệnh trải qua phẫu thuật không thuộc lồng ngực.
Do đó PFT chỉ nên được sử dụng trong bối cảnh của quá trình chẩn đoán để xác nhận chẩn đoán bệnh phổi ở người bệnh có các phát hiện gợi ý sự hiện diện của nó hoặc ở người bệnh có bệnh phổi mạn tính đã biết có triệu chứng gợi ý một đợt cấp chồng chất. Tuyên bố đồng thuận năm 1990 của ACP hạn chế việc sử dụng PFT trong phẫu thuật không thuộc lồng ngực cho người bệnh trải qua phẫu thuật bụng trên có tiền sử hút thuốc hoặc khó thở và cho người bệnh trải qua các phẫu thuật ngoại vi hơn có triệu chứng phổi không giải thích được.
Năm 1995, ước tính rằng 39% PFT trước phẫu thuật được thực hiện không đáp ứng các khuyến nghị của ACP. Dựa trên ước tính này, một phân tích chi phí được thực hiện năm 1997 mô tả một chi phí dư thừa hàng năm là hàng triệu đô la do PFT không cần thiết. Có thể việc tuân thủ hướng dẫn ACP đã cải thiện trong những năm gần đây, với tiết kiệm tài chính đáng kể. Tuy nhiên, có thể lập luận rằng việc sử dụng PFT nên thậm chí bị hạn chế hơn so với đề xuất của ACP.
Không có bằng chứng mạnh mẽ có sẵn hỗ trợ việc sử dụng thường quy PFT trước phẫu thuật cho các phẫu thuật không thuộc lồng ngực có nguy cơ cao và ở người bệnh có nguy cơ cao. Trong một nghiên cứu của Warner và cộng sự, 135 người bệnh có giới hạn dòng trung bình đến nặng bởi PFT được so sánh với một nhóm người bệnh có đặc điểm tương tự nhưng không có bệnh tắc nghẽn. Nhóm có bệnh tắc nghẽn có tần suất co thắt phế quản tăng, nhưng tỷ lệ các biến chứng đáng kể hơn là tương tự giữa hai nhóm. Đặc biệt, không có sự khác biệt về tỷ lệ đặt nội khí quản kéo dài.
Trong một nghiên cứu của Wong và cộng sự, người bệnh có COPD nặng có nguy cơ cao (37%) phát triển bất kỳ PPCs nào. Bằng phân tích đa biến, có thể xác định rằng, mặc dù thể tích thở ra gắng sức trong 1 giây (FEV1) thấp hơn có liên quan đến PPCs, các yếu tố không phổi như thời gian gây mê và các hệ thống chấm điểm như ASA là các yếu tố dự đoán tốt hơn.
Tương tự như PFT, khí máu động mạch đã được sử dụng trong quá khứ cho đánh giá trước phẫu thuật của người bệnh phẫu thuật không thuộc lồng ngực mà không có bằng chứng mạnh mẽ gợi ý giá trị của nó. Tăng carbon dioxide máu với áp suất riêng phần của carbon dioxide cao hơn 45 mmHg đã được coi là một yếu tố nguy cơ quan trọng cho PPCs và tử vong. Tương tự, thiếu oxy máu động mạch đã được coi là một yếu tố nguy cơ quan trọng cho PPCs và một chống chỉ định cho phẫu thuật. Những thay đổi khí máu này có thể giúp trong đánh giá lợi ích so với nguy cơ của một thủ thuật nhất định vì sự hiện diện của chúng có liên quan đến tuổi thọ ngắn hơn đáng kể ở người bệnh COPD. Tuy nhiên, cả tăng carbon dioxide máu và thiếu oxy máu đều không được chứng minh là yếu tố dự đoán độc lập của nguy cơ PPCs. Gần đây hơn, độ bão hòa oxy thấp trước phẫu thuật trên không khí phòng đã được đưa vào như một thành phần trong điểm ARISCAT, và bằng chứng gần đây đã xác thực bên ngoài điểm này trong quần thể phẫu thuật.
X-quang ngực vẫn thường được thực hiện thường quy trước phẫu thuật ở người bệnh lớn tuổi, ở người bệnh có bệnh phổi đã biết, và ở người bệnh hút thuốc. Mặc dù thực hành này ăn sâu vào gốc rễ, có ít hoặc không có bằng chứng rằng x-quang ngực thường quy ảnh hưởng đến quản lý chu phẫu hoặc kết quả theo bất kỳ cách nào. Ở người bệnh không có triệu chứng hoặc không có yếu tố nguy cơ cho bệnh phổi, x-quang ngực không có khả năng tiết lộ thông tin mới, và chúng có khả năng dẫn đến xét nghiệm thêm không cần thiết trong trường hợp kết quả dương tính giả. Người bệnh có yếu tố nguy cơ cho bệnh phổi có nhiều khả năng có các phát hiện bất thường hơn. Tuy nhiên, không rõ liệu x-quang ngực có thêm bất kỳ thông tin nào vào phân tầng nguy cơ phổi ở người bệnh có triệu chứng ổn định hoặc không có triệu chứng gì cả hay không. Việc sử dụng X-quang ngực duy nhất thích hợp có thể là trong trường hợp người bệnh có triệu chứng phổi mới hoặc không giải thích được, trong đó X-quang có thể phát hiện bệnh phổi không rõ yêu cầu kiểm tra thêm hoặc một quá trình cấp tính, chẳng hạn như viêm phổi, do đó có thể là thận trọng để hoãn phẫu thuật chọn lọc.
Bằng chứng hạn chế hỗ trợ kiểm tra tập thể dục như một công cụ hữu ích để xác định người bệnh có nguy cơ PPCs trong phẫu thuật không thuộc lồng ngực. Girish và cộng sự đã thực hiện kiểm tra tập thể dục trước các phẫu thuật có nguy cơ cao, bao gồm cả mở ngực, bằng cách đơn giản đo số tầng cầu thang mà người bệnh có khả năng leo. Một hiệu suất kém trên bài kiểm tra đơn giản này là một yếu tố nguy cơ độc lập cho các biến chứng tim phổi kết hợp, trong khi kết quả PFT, tuổi, cân nặng, và bệnh phổi đã tồn tại trước đó thì không. Không có khả năng leo hơn hai tầng cầu thang có giá trị dự đoán dương tính là 0,8 và giá trị dự đoán âm tính là 0,82 cho các biến chứng tim phổi hậu phẫu. Nghiên cứu này gợi ý rằng bài kiểm tra dung nạp tập thể dục đơn giản này có thể được áp dụng trong đánh giá lâm sàng của người bệnh dự kiến trải qua các phẫu thuật có nguy cơ cao. Tuy nhiên, có bằng chứng không đầy đủ để khuyến nghị kiểm tra tập thể dục thường quy cho đánh giá trước phẫu thuật của người bệnh phẫu thuật không thuộc lồng ngực.
Một hình thức kiểm tra tập thể dục có thể dễ dàng kiểm tra trong môi trường văn phòng là bài kiểm tra đi bộ 6 phút. Ở người bệnh phẫu thuật ngực hoặc bụng trên, khoảng cách đi bộ 6 phút được chứng minh có tương quan âm với tỷ lệ và mức độ nghiêm trọng của các biến chứng hậu phẫu nói chung nhưng không giới hạn ở PPCs.
Tăng áp phổi (PH) tương đối phổ biến ở người bệnh COPD hoặc với các loại bệnh phổi mạn tính khác. PH được định nghĩa bởi áp suất động mạch phổi trung bình lớn hơn hoặc bằng 25 mmHg khi nghỉ ngơi. Theo hướng dẫn của Trường Trường Môn Tim mạch Hoa Kỳ/Hiệp hội Tim Hoa Kỳ, PH hiện không được liệt kê là một yếu tố nguy cơ độc lập cho người bệnh trải qua phẫu thuật không tim, mặc dù có các báo cáo về tử vong không lường trước được trong giai đoạn chu phẫu. Tỷ lệ phổ biến của PH ở người bệnh COPD nặng nằm giữa 5% và 10%. Việc phát hiện nó trong các quần thể như vậy có giá trị tiên lượng quan trọng và có thể giúp trong việc lựa chọn người bệnh, vì tình trạng này có liên quan đến tuổi thọ ngắn hơn đáng kể ở COPD. Trong phẫu thuật ngực, PH được sử dụng như một tiêu chí để từ chối một số thủ thuật nhất định, chẳng hạn như phẫu thuật giảm thể tích phổi. PH và suy thất phải có thể làm phức tạp đáng kể quản lý trong và sau phẫu thuật của người bệnh trải qua các phẫu thuật có nguy cơ cao, và có thể giả thuyết rằng người bệnh chịu đựng được tăng áp lực vừa phải khi nghỉ ngơi có thể trở nên mất bù cấp tính trong giai đoạn chu phẫu. Ít nhất nên có nhận thức về sự hiện diện có thể của những tình trạng này khi đánh giá người bệnh có bệnh phổi mạn tính và cần trải qua phẫu thuật lớn. Sự tồn tại của chúng có thể bị nghi ngờ trên cơ sở đánh giá lâm sàng, nhưng độ chính xác của tiền sử và khám thể chất trong chẩn đoán PH có lẽ là thấp. Siêu âm tim thường được sử dụng trong đánh giá người bệnh nghi ngờ có tổn thương thất phải hoặc PH. Theo hướng dẫn của Hiệp hội Siêu âm tim Hoa Kỳ, áp suất động mạch phổi tâm thu có thể được ước tính một cách hợp lý bằng cách đo vận tốc hở van ba lá và sử dụng phương trình Bernoulli đơn giản hóa. Áp suất tâm trương có thể được ước tính từ vận tốc hở động mạch phổi cuối tâm trương. Áp suất trung bình có thể được ước tính bằng thời gian tăng tốc động mạch phổi hoặc bắt nguồn từ áp suất tâm thu và tâm trương. Mặc dù có bằng chứng hỗ trợ hạn chế cho siêu âm tim thường quy, việc thu được nghiên cứu ở những người bệnh có bệnh phổi nặng có dấu hiệu tương thích với rối loạn chức năng tim phải hoặc những người có không dung nạp tập thể dục đáng kể là hợp lý. Lai và cộng sự đã nghiên cứu 62 người bệnh có PH nặng trải qua phẫu thuật không tim và báo cáo bệnh tật và tử vong hậu phẫu lần lượt là 24% và 9,7%. Các bệnh tật lớn là rút ống nội khí quản trễ (21%), suy tim (9,7%), và loạn nhịp tim lớn (3,2%). Một lần nữa, không có phân tích riêng biệt giữa nguyên nhân tim và phổi trong nghiên cứu này. Kiểm tra tập thể dục tim phổi (CPET) là một trong những xét nghiệm thường được thực hiện trước phẫu thuật, trong một số quốc gia Châu Âu. Nó có thể được sử dụng như một công cụ phân tầng nguy cơ để dự đoán PPC. Ở Hoa Kỳ, CPET không được thực hiện thường quy. Người bệnh có PFT biên giới được đánh giá thêm với CPET. Có các công cụ mới như bảng câu hỏi Chỉ số Trạng thái Hoạt động Duke (DASI), đã được đánh giá để xác định người bệnh có khả năng chức năng kém nhưng chưa được xác thực trong quần thể phẫu thuật rộng hơn.
Điểm Dự đoán Nguy cơ
Điểm nguy cơ có thể là các công cụ lâm sàng hữu ích nếu chúng cung cấp một ước tính hợp lý về xác suất của biến chứng và nếu thông tin có thể được sử dụng để hướng dẫn lựa chọn điều trị. Ngoài ra, điểm nguy cơ có thể cung cấp một số hiểu biết về các yếu tố quan trọng nhất đóng góp vào nguồn gốc của một kết quả nhất định. Mặc dù các điểm nguy cơ tim mạch như chỉ số Goldman đã được sử dụng trong nhiều năm, đánh giá phổi đã thiếu một chỉ số nguy cơ hợp lệ.
Trong hai nghiên cứu đoàn hệ đồng hành, Arozullah và cộng sự đã xây dựng và xác thực các hệ thống điểm nguy cơ đa yếu tố để dự đoán viêm phổi hậu phẫu và suy hô hấp. Các nghiên cứu sử dụng dữ liệu người bệnh từ NSQIP của Bộ Cựu chiến binh. Người bệnh nghiên cứu trải qua nhiều thủ thuật không tim khác nhau, bao gồm cắt bỏ phổi.
Chỉ số suy hô hấp Arozullah (Bảng 9.7) dự đoán tỷ lệ PRF (thông khí cơ học trong 48 giờ) dựa trên một số yếu tố, bao gồm loại phẫu thuật, kết quả xét nghiệm, tình trạng chức năng, tiền sử COPD, và tuổi. Loại phẫu thuật là yếu tố dự đoán mạnh nhất cũng trong chỉ số viêm phổi (Bảng 9.8), cùng với tuổi và tình trạng chức năng. Dựa trên điểm nguy cơ cuối cùng, người bệnh được phân vào năm nhóm nguy cơ, và đối với mỗi nhóm, độ chính xác của dự đoán nguy cơ được xác thực trong các đoàn hệ độc lập của người bệnh, xác nhận rằng các mô hình có hiệu suất đầy đủ (Bảng 9.9). Do số lượng thông số cần thiết cho dự đoán, những hệ thống chấm điểm này phức tạp để sử dụng trong thực hành lâm sàng, mặc dù chúng đã được sử dụng trong bối cảnh nghiên cứu. Một hạn chế khác của các nghiên cứu này là cơ sở dữ liệu NSQIP được sử dụng để lấy mô hình chủ yếu bao gồm các đối tượng nam. Thực tế là cả khí máu và PFT đều không được đưa vào trong các mô hình do khó khăn trong việc thu thập những dữ liệu này có thể được coi là một điểm yếu khác của nghiên cứu.
Bảng 9.7 Chỉ số nguy cơ suy hô hấp.
| Yếu tố dự đoán trước phẫu thuật | Giá trị điểm |
|---|---|
| Loại phẫu thuật | |
| Bụng | 27 |
| Ngực | 21 |
| Phẫu thuật thần kinh, bụng trên, mạch máu ngoại vi | 14 |
| Cổ | 11 |
| Phẫu thuật khẩn cấp | 11 |
| Albumin <3 g/dL | 9 |
| Urê nitơ máu >30 mg/dL | 8 |
| Tình trạng chức năng phụ thuộc một phần hoặc hoàn toàn | 7 |
| Tiền sử bệnh phổi tắc nghẽn mạn tính | 6 |
| Tuổi (năm) | |
| >70 | 6 |
| 60-69 | 4 |
Bảng 9.8 Chỉ số nguy cơ viêm phổi hậu phẫu.
| Yếu tố nguy cơ trước phẫu thuật | Giá trị điểm |
|---|---|
| Loại phẫu thuật | |
| Động mạch chủ bụng | 15 |
| Ngực | 14 |
| Bụng trên | 10 |
| Cổ | 8 |
| Phẫu thuật thần kinh | 8 |
| Mạch máu | 3 |
| Tuổi (năm) | |
| >80 | 17 |
| 70-79 | 13 |
| 60-69 | 9 |
| 50-59 | 4 |
| Tình trạng chức năng | |
| Phụ thuộc hoàn toàn | 10 |
| Phụ thuộc một phần | 6 |
| Giảm cân >10% trong 6 tháng qua | 7 |
| Tiền sử COPD | 5 |
| Gây mê toàn thân | 4 |
| Suy giảm cảm giác | 4 |
| Tiền sử tai biến mạch máu não | 4 |
| Mức urê nitơ máu | |
| <8 mg/dL | 4 |
| 22-30 mg/dL | 2 |
| >30 mg/dL | 3 |
| Truyền máu >4 đơn vị | 3 |
| Phẫu thuật khẩn cấp | 3 |
| Sử dụng steroid cho tình trạng mạn tính | 3 |
| Hiện đang hút thuốc trong vòng 1 năm | 3 |
| Tiêu thụ rượu >2 ly/ngày trong 2 tuần qua | 2 |
Bảng 9.9 Các nhóm nguy cơ cho suy hô hấp và viêm phổi.
| Nhóm | Chỉ số nguy cơ suy hô hấp hậu phẫu (tổng điểm) | Xác suất suy hô hấp (%) | Chỉ số nguy cơ viêm phổi hậu phẫu (tổng điểm) | Xác suất viêm phổi (%) |
|---|---|---|---|---|
| 1 | 0-10 | 0,5 | 0-15 | 0,2 |
| 2 | 11-19 | 2,2 | 16-25 | 1,2 |
| 3 | 20-27 | 5,0 | 26-40 | 4,0 |
| 4 | 28-40 | 11,6 | 41-55 | 9,4 |
| 5 | >40 | 30,5 | >55 | 15,3 |
Canet và cộng sự tránh sai lệch lấy mẫu bằng cách nghiên cứu tiến cứu một nhóm người bệnh không đồng nhất và lấy một mô hình dự đoán mới gọi là “điểm ARISCAT” (Bảng 9.10a và 9.10b). Điều này bao gồm các thành phần sau:
- Tuổi cao
- Phẫu thuật bụng trên hoặc ngực
- Phẫu thuật kéo dài hơn 2 giờ
- Phẫu thuật khẩn cấp
- Độ bão hòa oxy trước phẫu thuật thấp
- Nhiễm trùng đường hô hấp trong tháng qua
- Thiếu máu trước phẫu thuật
Bảng 9.10a Các yếu tố dự đoán độc lập về nguy cơ PPCs được xác định trong mô hình hồi quy logistic.
| Phân tích đa biến OR (95% CI) n = 1.624* | Hệ số β | Điểm nguy cơ† |
|---|---|---|
| Tuổi, năm | ||
| ≤50 | 1 | 1 |
| 51-80 | 1,4 (0,6-3,3) | 0,331 |
| >80 | 5,1 (1,9-13,3) | 1,619 |
| SpO₂ trước phẫu thuật, % | ||
| ≥96 | 1 | 1 |
| 91-95 | 2,2 (1,2-4,2) | 0,802 |
| ≤90 | 10,7 (4,1-28,1) | 2,375 |
| Nhiễm trùng hô hấp trong tháng qua | 5,5 (2,6-11,5) | 1,698 |
| Thiếu máu trước phẫu thuật (≤10 g/dl) | 3,0 (1,4-6,5) | 1,105 |
| Vết mổ phẫu thuật | ||
| Ngoại vi | 1 | 1 |
| Bụng trên | 4,4 (2,3-8,5) | 1,480 |
| Trong lồng ngực | 11,4 (4,9-26,0) | 2,431 |
| Thời gian phẫu thuật, giờ | ||
| ≤2 | 1 | 1 |
| >2 đến 3 | 4,9 (2,4-10,1) | 1,593 |
| >3 | 9,7 (4,7-19,9) | 2,268 |
| Thủ thuật khẩn cấp | 2,2 (1,0-4,5) | 0,768 |
*Do thiếu giá trị cho một số biến, ba người bệnh đã bị loại trừ. Mô hình hồi quy logistic được xây dựng với mẫu phát triển phụ, chỉ số c = 0,90; Kiểm định chi-bình phương Hosmer-Lemeshow = 7,862; P = 0,447. †Điểm nguy cơ đơn giản hóa là tổng của mỗi hệ số β hồi quy logistic nhân với 10, sau khi làm tròn giá trị của nó.
Bảng 9.10b Điểm nguy cơ PPC: phân bố người bệnh và tỷ lệ theo khoảng.
| Khoảng điểm nguy cơ* | Nguy cơ thấp <26 điểm | Nguy cơ trung bình 26-44 điểm | Nguy cơ cao ≥45 điểm |
|---|---|---|---|
| Mẫu phụ phát triển, Số (%) người bệnh† | 1.238 (76,2) | 288 (17,7) | 98 (6,0) |
| Mẫu phụ xác thực, Số (%) người bệnh | 645 (77,1) | 135 (16,1) | 57 (6,8) |
| Tỷ lệ PPC, mẫu phát triển, % (95% CI) | 0,7 (0,2-1,2) | 6,3 (3,5-9,1) | 44,9 (35,1-54,7) |
| Tỷ lệ PPC, mẫu xác thực, % (95% CI) | 1,6 (0,6-2,6) | 13,3 (7,6-19,0) | 42,1 (29,3-54,9) |
*Khoảng nguy cơ dựa trên việc phân chia mẫu phụ phát triển thành các khoảng nguy cơ tối ưu, theo điểm nguy cơ đơn giản hóa và áp dụng nguyên tắc mô tả độ dài tối thiểu. †Ba người bệnh bị loại trừ do thiếu giá trị trong một số biến.
Ba biến cuối cùng không được đưa vào trong các hệ thống dự đoán trước đó hoặc hướng dẫn ACP. Tỷ lệ PPCs ở người bệnh có điểm được phân loại là nguy cơ nhẹ, trung bình, và nặng được ước tính lần lượt là 1,6%, 13,3%, và 42,2%. Gần đây, điểm ARISCAT đã được xác thực bên ngoài trong một đoàn hệ quần thể Châu Âu gọi là PERISCOPE (Đánh giá Tiến cứu của Điểm Nguy cơ cho các biến chứng phổi hậu phẫu ở Châu Âu) với sự phân biệt tốt và thống kê C 0,80 (CI, 0,78-0,82).
Chỉ số PRF (Bảng 9.11) của Gupta và cộng sự sử dụng nhiều yếu tố trước phẫu thuật để dự đoán nguy cơ thất bại trong việc cai khỏi thông khí cơ học trong vòng 48 giờ sau phẫu thuật và đặt nội khí quản và đặt lại nội khí quản hậu phẫu không theo kế hoạch. Máy tính nguy cơ bao gồm các biến như nhiễm trùng huyết và sốc nhiễm trùng ngoài chỉ số Arozullah đã đề cập trước đó. Nó được lấy từ bộ dữ liệu NSQIP sử dụng các kỹ thuật hồi quy logistic. Một lần nữa, điểm này đã được xác thực sử dụng quần thể đoàn hệ PERISCOPE ở Châu Âu.
Bảng 9.11 Bảng tính nguy cơ viêm phổi hậu phẫu.
| Đo lường | Điểm |
|---|---|
| Thủ thuật | |
| Hậu môn trực tràng | 1 |
| Động mạch chủ | 2 |
| Béo phì | 3 |
| Não | 4 |
| Vú | 5 |
| Tim | 6 |
| Tai mũi họng (trừ tuyến giáp/cận giáp) | 7 |
| Dạ dày/gan tụy mật | 8 |
| Túi mật, ruột thừa, tuyến thượng thận, và lách | 9 |
| Thoát vị (thành bụng, bẹn, đùi) | 10 |
| Ruột | 11 |
| Cổ (tuyến giáp và cận giáp) | 12 |
| Sản/phụ khoa | 13 |
| Chỉnh hình và chi không mạch máu | 14 |
| Bụng khác | 15 |
| Mạch máu ngoại vi | 16 |
| Da | 17 |
| Cột sống | 18 |
| Ngực không phải thực quản | 19 |
| Tĩnh mạch | 20 |
| Tiết niệu | 21 |
| Lớp ASA | I-V |
| Tuổi | Tuổi tính bằng năm |
| COPD | |
| COPD giai đoạn GOLD 2-4 | 1 |
| Không có GOLD | 0 |
| Tình trạng chức năng | |
| Người bệnh có tình trạng chức năng phụ thuộc hoàn toàn | 2 |
| Người bệnh có tình trạng chức năng phụ thuộc một phần | 1 |
| Người bệnh hoàn toàn độc lập | 0 |
| Nhiễm trùng huyết | |
| Người bệnh có viêm hệ thống trước phẫu thuật | 3 |
| Người bệnh có sốc nhiễm trùng trước phẫu thuật | 2 |
| Người bệnh có nhiễm trùng huyết trước phẫu thuật | 1 |
| Không có | 0 |
| Hút thuốc | |
| Hút thuốc trong năm trước phẫu thuật | 1 |
| Không hút thuốc | 0 |
Kor và cộng sự đã lấy một mô hình dự đoán tổn thương phổi do phẫu thuật (Bảng 9.12a và 9.12b) ở người bệnh đã trải qua phẫu thuật lớn và nhận thông khí cơ học >3 giờ và phát hiện rằng phẫu thuật tim/ngực/mạch máu, COPD, nghiện rượu, tiểu đường, và bệnh trào ngược dạ dày thực quản là các yếu tố dự đoán của PPC. Mô hình này được phát triển để phân biệt người bệnh có nguy cơ cao phát triển tổn thương phổi cấp/ARDS với một diện tích dưới đường cong đặc trưng hoạt động của người nhận (95% CI) là 0,82 (0,78-0,86). Tuy nhiên, mô hình này chưa được xác thực bên ngoài.
Bảng 9.12a Ước tính tham số cho các yếu tố dự đoán nguy cơ ALI trong phân tích hồi quy logistic đa biến (n = 4.280).
| Yếu tố dự đoán nguy cơ | Ước tính tham số | Tỷ số chênh (95% CI) | Giá trị P |
|---|---|---|---|
| Nhân khẩu học | |||
| Tuổi* | 0,010 | 1,01 (0,99-1,03) | 0,25 |
| Giới tính, nam | -0,071 | 0,93 (0,61-1,45) | 0,75 |
| Yếu tố thủ thuật | |||
| Tim nguy cơ cao | 1,854 | 6,39 (3,87-10,87) | <0,01 |
| Mạch máu nguy cơ cao | 3,276 | 26,46 (8,52-73,63) | <0,01 |
| Mạch máu nguy cơ thấp | 0,542 | 1,72 (0,39-5,23) | 0,39 |
| Ngực nguy cơ cao | 1,486 | 4,42 (1,86-9,67) | <0,01 |
| Bệnh đồng mắc | |||
| Đái tháo đường | 0,588 | 1,80 (1,13-2,80) | 0,01 |
| COPD | 0,761 | 2,14 (1,22-3,63) | <0,01 |
| Bệnh phổi hạn chế | 0,510 | 1,66 (0,73-3,40) | 0,19 |
| GERD | 0,619 | 1,86 (1,23-2,82) | <0,01 |
| Điều kiện thay đổi | |||
| Sử dụng thuốc lá | |||
| Trước đây | 0,063 | 1,07 (0,66-1,73) | 0,79 |
| Hiện tại | 0,473 | 1,60 (0,86-2,95) | 0,13 |
| Lạm dụng rượu | 1,050 | 2,86 (1,85-4,38) | <0,01 |
| Hóa trị gần đây† | 0,667 | 1,95 (0,55-6,25) | 0,27 |
| Amiodarone | 0,312 | 1,37 (0,73-2,44) | 0,31 |
| Statin | 0,154 | 1,17 (0,77-1,78) | 0,47 |
*Tuổi, cho mỗi năm bổ sung. †Trong vòng 6 tháng của thủ thuật phẫu thuật; chỉ ở người bệnh trải qua cắt thực quản hoặc cắt bỏ phổi vì ung thư.
Bảng 9.12b Tiêu chí chấm điểm SLIP (n = 4.328).
| Biến dự đoán | Ước tính tham số | Điểm SLIP |
|---|---|---|
| Thủ thuật phẫu thuật nguy cơ cao | ||
| Tim | 1,88 | 19 |
| Mạch máu | 3,21 | 32 |
| Ngực | 1,60 | 16 |
| Bệnh đồng mắc | ||
| Đái tháo đường | 0,62 | 6 |
| COPD | 0,95 | 10 |
| GERD | 0,72 | 7 |
| Điều kiện thay đổi | ||
| Lạm dụng rượu | 1,13 | 11 |
Mô hình Đánh giá cho Phẫu thuật Không thuộc Lồng ngực
Một tiền sử kỹ lưỡng và khám thể chất nên được thu thập, với sự chú ý đặc biệt đến các yếu tố phổi và không phổi như đã mô tả trước đây (Hình 9.4). Ở người bệnh có nhiễm trùng đường hô hấp gần đây hoặc đang diễn ra, việc trì hoãn phẫu thuật 2-3 tuần nên được xem xét nếu chấp nhận được từ quan điểm phẫu thuật. Người bệnh có bệnh phổi mạn tính đã biết và có triệu chứng xấu đi hoặc người bệnh không có bệnh đường hô hấp đã biết nhưng có triệu chứng khởi phát mới nên nhận đánh giá thêm, và sự tham gia của chuyên gia phổi có thể được xem xét. X-quang ngực và PFT cũng có thể được xem xét. Ở người bệnh có triệu chứng phổi ổn định nhưng đang trải qua một thủ thuật có nguy cơ cao (phẫu thuật bụng trên, mạch máu lớn, thời gian có thể kéo dài hơn 2,5 giờ, có khả năng sử dụng hút dạ dày), một nỗ lực phân tầng nguy cơ thêm sử dụng điểm ARISCAT (xem Bảng 9.10) hoặc Gupta (xem Bảng 9.11) có thể được thực hiện. Ở người bệnh có điểm cao và có xác suất cao của PPCs, các chiến lược giảm nguy cơ, cách tiếp cận phẫu thuật thay thế, hoặc quản lý không phẫu thuật có thể được xem xét, tùy thuộc vào chỉ định phẫu thuật và sở thích của người bệnh.
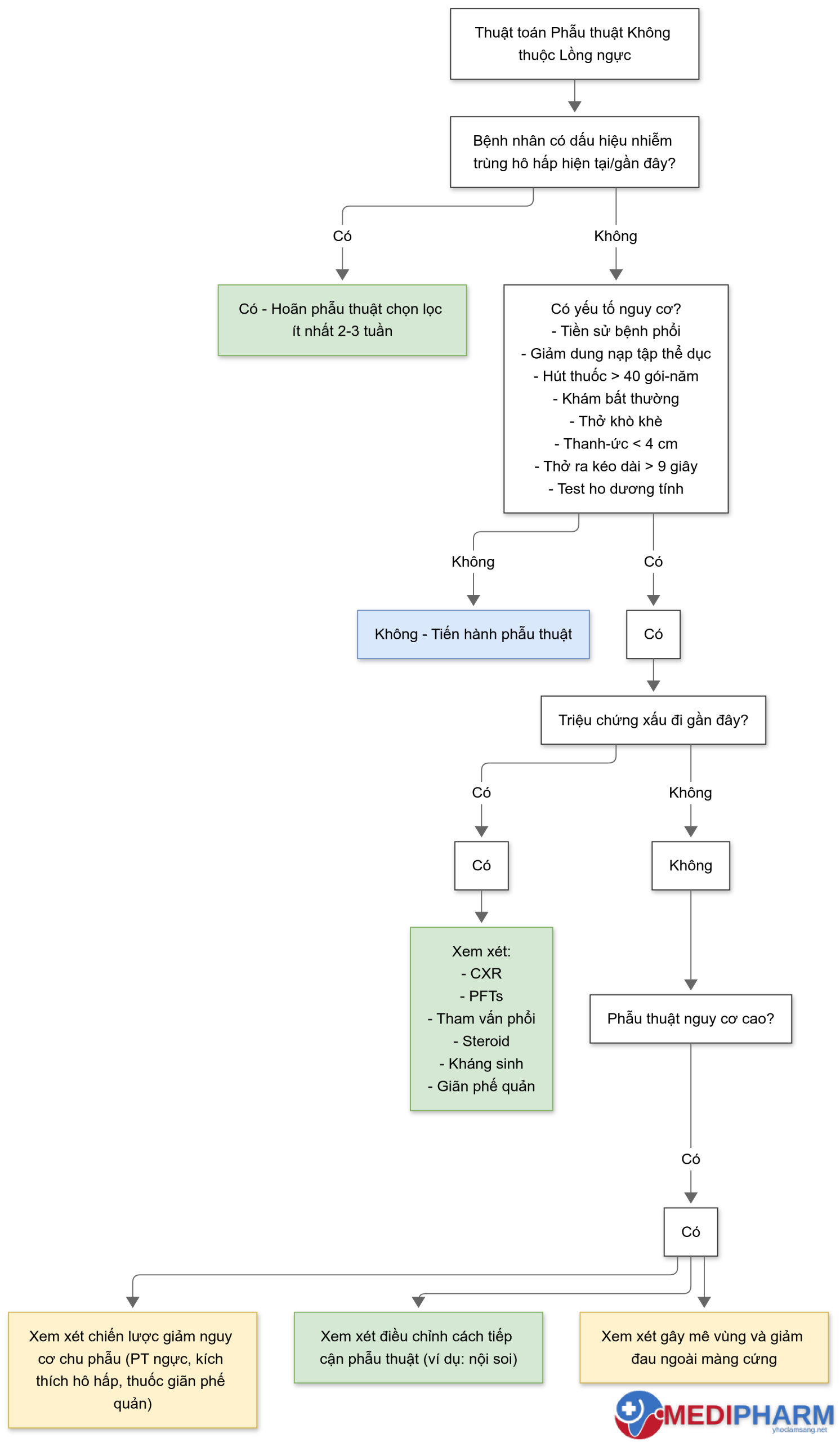
Hình 9.4 Cách tiếp cận phẫu thuật không thuộc lồng ngực cho người bệnh có bệnh phổi. CXR, X-quang ngực; DOE, khó thở khi gắng sức; Hx, tiền sử; PFTs, xét nghiệm chức năng phổi; PT, vật lý trị liệu; py, gói-năm.
Đánh giá Ứng viên Cắt bỏ Phổi
Mục tiêu của đánh giá trước phẫu thuật không chỉ là để đánh giá nguy cơ của PPCs mà còn để xác định liệu một người bệnh có phải là ứng viên cho phẫu thuật hay không và để thiết lập lượng mô phổi có thể được cắt bỏ mà không gây ra sự suy giảm chức năng không thể chịu đựng được. Không giống như phẫu thuật không thuộc lồng ngực, đánh giá trước phẫu thuật của ứng viên cắt bỏ phổi dựa vào kiểm tra bằng dụng cụ. Các mô hình đánh giá cho phẫu thuật ngực bao gồm các xét nghiệm được hỗ trợ bởi bằng chứng lâm sàng đầy đủ và đặc biệt nhấn mạnh vào dự đoán chức năng phổi hậu phẫu và sử dụng kiểm tra tập thể dục.
Tỷ lệ tử vong được báo cáo trong cơ sở dữ liệu phẫu thuật ngực tổng quát là 1,6%-2,3% sau cắt thùy phổi và 3,7%-6,7% sau cắt bỏ phổi. Những kết quả này đã cải thiện qua các năm, mặc dù chúng vẫn đáng kể. Do đó, các tiêu chí lựa chọn được coi là hợp lệ trong quá khứ hiện đang bị nghi ngờ. Ví dụ, tuổi cao được coi là một chống chỉ định chính cho cắt bỏ phổi mở rộng. Tuy nhiên, hướng dẫn gần đây chỉ ra rằng người bệnh ung thư phổi là ứng viên tiềm năng cho cắt bỏ phổi chữa bệnh nên được đánh giá bất kể tuổi tác.
Đánh giá trước phẫu thuật cho cắt bỏ phổi nên bắt đầu với việc xác định các yếu tố nguy cơ phổi và không phổi cho PPCs bằng khám thể chất và lấy tiền sử, như đã thảo luận cho phẫu thuật không thuộc lồng ngực. Các yếu tố đã được chứng minh là có liên quan đến PPCs ở người bệnh phẫu thuật ngực bao gồm bệnh tim mạch, tiền sử hút thuốc, và tình trạng ASA. Các yếu tố trong khi phẫu thuật đã được chứng minh ảnh hưởng đến tỷ lệ PPCs ở người bệnh cắt bỏ phổi là thời gian của thủ thuật, mất máu, và lượng dịch truyền tĩnh mạch.
Tất cả ứng viên cắt bỏ phổi nên nhận đo hô hấp ký trong đánh giá ban đầu của họ. Trước đây, nó được khuyến nghị rằng phẫu thuật nên được thực hiện mà không cần đánh giá thêm ở người bệnh cắt bỏ phổi có FEV1 >2 L hoặc >80% dự đoán và ở người bệnh cắt thùy phổi có FEV1 >1,5 L. Bản cập nhật gần đây nhất được cung cấp bởi Trường Môn Bác sĩ Ngực Hoa Kỳ (ACCP).
Ở người bệnh bị ung thư phổi đang được xem xét cho phẫu thuật, khuyến nghị rằng giá trị dự đoán hậu phẫu (PPO) của cả FEV1 và khả năng khuếch tán của phổi đối với carbon monoxide (DLCO) nên được tính toán. Những giá trị này được ước tính từ giá trị trước phẫu thuật và phạm vi dự kiến của cắt bỏ phổi. Phạm vi sau có thể được xác định bằng cách sử dụng chụp xạ hình phổi bằng đồng vị phóng xạ hoặc đơn giản bằng cách thêm các phân đoạn sẽ bị loại bỏ. Việc sử dụng chụp xạ hình phổi để dự đoán chức năng phổi hậu phẫu được khuyến nghị cho cắt bỏ phổi, trong khi đối với cắt thùy phổi, sử dụng phương pháp đếm phân đoạn có lẽ đủ chính xác. Tuy nhiên, tỷ lệ tử vong và bệnh tật chấp nhận được đã được báo cáo ngay cả ở người bệnh có chức năng phổi PPO thấp. Ngoài ra, đã được đề xuất rằng PFT trước phẫu thuật ước tính quá mức mất khả năng tập thể dục hậu phẫu, đặc biệt là sau cắt thùy phổi. Do đó, đánh giá thêm thông qua kiểm tra tập thể dục ở người bệnh có chức năng phổi PPO kém là cần thiết. Kiểm tra tập thể dục có giá trị cho mục đích này vì nó cung cấp một đánh giá hợp lý chính xác về tình trạng chức năng tim phổi của người bệnh và khả năng chịu đựng của họ đối với căng thẳng chu phẫu.
Ở Hoa Kỳ, có sự khác biệt rộng rãi giữa các bác sĩ phẫu thuật về việc tuân thủ CPET như một phương thức đánh giá trước phẫu thuật ngực. Các biến chính được sử dụng trong CPET là ngưỡng kỵ khí (AT) và lượng oxy tiêu thụ đỉnh (VO2peak) và tương đương thông khí của carbon dioxide (VE/VCO2).
AT là một thước đo của khả năng tập thể dục tối đa hay bền vững và được định nghĩa là lượng oxy tiêu thụ mà trên đó sản xuất lactate vượt quá mức nghỉ ngơi liên tục. Nó liên quan đến toan chuyển hóa. Giá trị nhỏ hơn 10 mL/kg/phút dự đoán nguy cơ. VO2 đỉnh khác với VO2 tối đa, và nó được định nghĩa là lượng oxy tiêu thụ đỉnh trong khi thực hiện kiểm tra tập thể dục tăng dần.
(VE/VCO2) là một thước đo để đánh giá hiệu quả trao đổi khí. Nếu điều này được đo tại AT, thì nó đã được chứng minh là dự đoán tỷ lệ bệnh tật và tử vong trong nhiều loại người bệnh phẫu thuật.
Đáng chú ý, một bố cục đồ thị được sắp xếp cụ thể gồm ba-theo-ba gọi là biểu đồ 9 bảng thường được sử dụng.
Khả năng tập thể dục có thể được đánh giá bằng cách tính toán lượng tiêu thụ oxy tối đa (VO2max). Kiểm tra tập thể dục có thể được kết hợp với chụp xạ hình phổi bằng đồng vị phóng xạ để có được VO2max PPO.
ACCP đã khuyến nghị hướng dẫn đánh giá sinh lý của người bệnh bị ung thư phổi được xem xét cho phẫu thuật mở ngực với phẫu thuật cắt bỏ phổi (cắt thùy phổi hoặc nhiều hơn). Thuật toán được hiển thị trong Hình 9.5.

Hình 9.5 Đánh giá sinh lý của người bệnh được xem xét cho phẫu thuật mở ngực với phẫu thuật cắt bỏ phổi nhiều hơn cắt thùy phổi. CPET, Kiểm tra tập thể dục tim phổi; DLCO, khả năng khuếch tán carbon monoxide; FEV1, thể tích thở ra gắng sức trong 1 giây; PPO, giá trị hậu phẫu dự đoán; SCT, test leo cầu thang; SWT, test đi bộ xen kẽ; VO2max, tiêu thụ oxy tối đa.
▪ Nếu PPO FEV1 và PPO DLCO lớn hơn 60% giá trị dự đoán, người bệnh được coi là có nguy cơ thấp cho thủ thuật phẫu thuật.
▪ Nếu PPO FEV1 hoặc PPO DLCO nhỏ hơn 60% nhưng lớn hơn 30% giá trị dự đoán, thì người bệnh nên trải qua bài kiểm tra leo cầu thang hoặc đi bộ xen kẽ. Đây được coi là kiểm tra tập thể dục công nghệ thấp, trái ngược với CPET tiêu chuẩn.
▪ Nếu PPO FEV1 nhỏ hơn 30% dự đoán hoặc PPO DLCO nhỏ hơn 30% dự đoán, thì người bệnh nên được đưa vào CPET với tính toán VO2max. ▪ Khi trải qua các bài kiểm tra công nghệ thấp, người bệnh thực hiện <25 lần di chuyển (hoặc <400 m) trong bài kiểm tra đi bộ xen kẽ hoặc leo <22 m trong bài kiểm tra leo cầu thang giới hạn theo triệu chứng nên được đưa vào CPET một lần nữa với đo lường VO2max.
▪ Trong CPET, giá trị VO2max nên được diễn giải cẩn thận. Nếu giá trị dự đoán nhỏ hơn 10 mL/kg/phút hoặc <35% dự đoán, người bệnh được coi là trong nhóm nguy cơ cao, và họ nên được tư vấn về phẫu thuật xâm lấn tối thiểu, cắt bỏ dưới thùy, hoặc các lựa chọn điều trị không phẫu thuật.
▪ Người bệnh có VO2max là 10-20 mL/kg/phút hoặc 35%-75% giá trị dự đoán từ kiểm tra CPET được coi là trong nhóm nguy cơ trung bình.
▪ Giá trị VO2max 10-15 mL/kg/phút vẫn được coi là ngụ ý tăng nguy cơ tử vong, có tính đến các yếu tố khác, chẳng hạn như PPO FEV1 và DLCO cũng như bệnh đồng mắc của người bệnh.
Người bệnh không nên bị loại trừ khỏi phẫu thuật chỉ dựa trên một tiêu chí, chẳng hạn như giá trị PPO FEV1 thấp hoặc giá trị DLCO thấp.
Một nghiên cứu gần đây đã đặt câu hỏi về việc sử dụng VO2max như một yếu tố dự đoán ở người bệnh COPD. Các tác giả đã phân tích một đoàn hệ người bệnh được xem xét cho cắt bỏ phổi sau một đánh giá chức năng trước phẫu thuật đầy đủ, bao gồm CPET. Người bệnh có độ dốc phút thông khí đến sản lượng carbon dioxide >35 có liên quan đến nhiều biến chứng hô hấp hậu phẫu và tử vong hơn (tỷ lệ nguy cơ, 5,1).
Kết luận
Các mô hình mới để dự đoán PPCs tương đối đơn giản và dễ tính toán tại giường bệnh. Dữ liệu gần đây hỗ trợ xác thực của chúng trong một phạm vi rộng các quần thể người bệnh. Những mô hình dự đoán nguy cơ này có thể được đưa vào thực hành lâm sàng và được sử dụng để đánh giá người bệnh trải qua phẫu thuật ngực và không thuộc lồng ngực lớn. PFT nên được dành riêng cho các phẫu thuật cắt bỏ phổi. Kiến thức kỹ lưỡng về đánh giá nguy cơ phổi nên giúp bác sĩ lâm sàng xác định nhóm phụ của người bệnh dễ bị tổn thương và thực hiện các biện pháp thích hợp nhằm ngăn ngừa biến chứng hậu phẫu.
HẾT CHƯƠNG 9.
Bảng chú giải thuật ngữ Y học Anh-Việt – Chương 9 (Người dịch)
| STT | Thuật ngữ tiếng Anh | Cách phát âm | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Postoperative pulmonary complications (PPCs) | pəʊst-ˈɒp(ə)rətɪv ˈpʌlmən(ə)ri ˌkɒmplɪˈkeɪʃ(ə)nz | Biến chứng phổi hậu phẫu |
| 2 | Perioperative morbidity | ˌpɛrɪˈɒp(ə)rətɪv mɔːˈbɪdɪti | Bệnh suất chu phẫu |
| 3 | Pulmonary risk evaluation | ˈpʌlmən(ə)ri rɪsk ɪˌvæljʊˈeɪʃ(ə)n | Đánh giá nguy cơ phổi |
| 4 | Outcome prediction models | ˈaʊtkʌm prɪˈdɪkʃ(ə)n ˈmɒd(ə)lz | Mô hình dự đoán kết quả |
| 5 | Respiratory failure | ˈrɛsp(ə)rət(ə)ri ˈfeɪljə | Suy hô hấp |
| 6 | Rehospitalization | ˌriːhɒspɪtəlaɪˈzeɪʃən | Tái nhập viện |
| 7 | Medicare beneficiaries | ˈmɛdɪkɛə ˌbɛnɪˈfɪʃ(ə)riz | Người thụ hưởng Medicare (chương trình bảo hiểm y tế Mỹ) |
| 8 | Inpatient claims | ˈɪnpeɪʃ(ə)nt kleɪmz | Yêu cầu thanh toán nội trú |
| 9 | Public health expense | ˈpʌblɪk hɛlθ ɪkˈspɛns | Chi phí y tế công |
| 10 | Nosocomial pneumonia | ˌnɒsəˈkəʊmɪəl njuːˈməʊnɪə | Viêm phổi bệnh viện |
| 11 | Perioperative bronchospasm | ˌpɛrɪˈɒp(ə)rətɪv ˈbrɒŋkəʊspæz(ə)m | Co thắt phế quản chu phẫu |
| 12 | Atelectasis | ˌætɪˈlɛktəsɪs | Xẹp phổi |
| 13 | European Perioperative Clinical Outcome | ˌjʊərəˈpiːən ˌpɛrɪˈɒp(ə)rətɪv ˈklɪnɪk(ə)l ˈaʊtkʌm | Kết quả lâm sàng chu phẫu Châu Âu |
| 14 | Surgical trauma | ˈsɜːdʒɪk(ə)l ˈtrɔːmə | Chấn thương phẫu thuật |
| 15 | Computed tomographic scans | kəmˈpjuːtɪd təˈmɒɡrəfɪk skænz | Chụp cắt lớp vi tính |
| 16 | Induction of general anesthesia | ɪnˈdʌkʃ(ə)n ɒv ˈdʒɛn(ə)r(ə)l ˌænɪsˈθiːzɪə | Khởi mê gây mê toàn thân |
| 17 | Epidural anesthesia | ˌɛpɪˈdjʊər(ə)l ˌænɪsˈθiːzɪə | Gây tê ngoài màng cứng |
| 18 | Gravity-dependent alveolar collapse | ˈɡrævɪti dɪˈpɛnd(ə)nt ælˈviːələ kəˈlæps | Xẹp phế nang theo trọng lực |
| 19 | Mechanical ventilation | mɪˈkænɪk(ə)l ˌvɛntɪˈleɪʃ(ə)n | Thông khí nhân tạo |
| 20 | Muscle relaxation | ˈmʌs(ə)l ˌriːlækˈseɪʃ(ə)n | Giãn cơ |
| 21 | Cephalad displacement | sɛˈfæləd dɪsˈpleɪsmənt | Di chuyển lên phía đầu |
| 22 | Diaphragm | ˈdaɪəfræm | Cơ hoành |
| 23 | Absorption atelectasis | əbˈzɔːpʃ(ə)n ˌætɪˈlɛktəsɪs | Xẹp phổi do hấp thu |
| 24 | Surfactant | səˈfækt(ə)nt | Chất hoạt động bề mặt (chất làm giảm sức căng bề mặt phế nang) |
| 25 | Functional residual capacity | ˈfʌŋ(k)ʃ(ə)n(ə)l rɪˈzɪdjʊəl kəˈpæsɪti | Dung tích cặn chức năng |
| 26 | Spinal reflex inhibition | ˈspaɪn(ə)l ˈriːflɛks ɪnhɪˈbɪʃ(ə)n | Ức chế phản xạ tủy sống |
| 27 | Phrenic nerve | ˈfrɛnɪk nɜːv | Thần kinh hoành |
| 28 | Nociceptive inputs | nəʊsɪˈsɛptɪv ˈɪnpʊts | Tín hiệu cảm nhận đau |
| 29 | Ventral horns | ˈvɛntr(ə)l hɔːnz | Sừng trước (của tủy sống) |
| 30 | Ventrolateral horns | ˌvɛntrəʊˈlæt(ə)r(ə)l hɔːnz | Sừng bên trước (của tủy sống) |
| 31 | Laparoscopic cholecystectomy | ˌlæp(ə)rəˈskɒpɪk ˌkɒlɪsɪsˈtɛktəmi | Cắt túi mật nội soi |
| 32 | Alveolar recruitment | ælˈviːələ rɪˈkruːtmənt | Mở phế nang |
| 33 | Mucociliary transport | ˌmjuːkəʊˈsɪlɪəri ˈtrænspɔːt | Vận chuyển nhầy-lông chuyển |
| 34 | Airway mucosa | ˈɛəweɪ mjuːˈkəʊsə | Niêm mạc đường thở |
| 35 | Cuffed tube | kʌft tjuːb | Ống có bóng chèn |
| 36 | Aspiration | ˌæspɪˈreɪʃ(ə)n | Hít sặc |
| 37 | Oropharyngeal secretions | ˌɔːrəʊfəˈrɪndʒɪəl sɪˈkriːʃ(ə)nz | Dịch tiết miệng-hầu |
| 38 | Residual muscle relaxation | rɪˈzɪdjʊəl ˈmʌs(ə)l ˌriːlækˈseɪʃ(ə)n | Tồn dư giãn cơ |
| 39 | Train-of-four ratio | treɪn ɒv fɔː ˈreɪʃɪəʊ | Tỷ lệ bộ bốn kích thích (đo mức độ giãn cơ) |
| 40 | Forced vital capacity | fɔːst ˈvaɪt(ə)l kəˈpæsɪti | Dung tích sống gắng sức |
| 41 | Peak expiratory flow rate | piːk ɪkˈspaɪrət(ə)ri fləʊ reɪt | Lưu lượng thở ra đỉnh |
| 42 | Pulmonary function testing (PFT) | ˈpʌlmən(ə)ri ˈfʌŋ(k)ʃ(ə)n ˈtɛstɪŋ | Đo chức năng hô hấp |
| 43 | Transhiatal esophagectomy | trænzˈhaɪət(ə)l ɪˌsɒfəˈdʒɛktəmi | Cắt thực quản qua khe hoành |
| 44 | Gas exchange | ɡæs ɪksˈtʃeɪndʒ | Trao đổi khí |
| 45 | Respiratory mechanics | ˈrɛsp(ə)rət(ə)ri mɪˈkænɪks | Cơ học hô hấp |
| 46 | Chest wall deformation | tʃɛst wɔːl ˌdiːfɔːˈmeɪʃ(ə)n | Biến dạng thành ngực |
| 47 | Myopathy | maɪˈɒpəθi | Bệnh cơ |
| 48 | Ventilatory demand | ˈvɛntɪlət(ə)ri dɪˈmɑːnd | Nhu cầu thông khí |
| 49 | Work of breathing | wɜːk ɒv ˈbriːðɪŋ | Công hô hấp |
| 50 | Ventilatory support | ˈvɛntɪlət(ə)ri səˈpɔːt | Hỗ trợ thông khí |
| 51 | Respiratory system | ˈrɛsp(ə)rət(ə)ri ˈsɪstəm | Hệ hô hấp |
| 52 | Instrumental testing | ˌɪnstrʊˈmɛnt(ə)l ˈtɛstɪŋ | Kiểm tra bằng dụng cụ |
| 53 | Smoking history | ˈsməʊkɪŋ ˈhɪst(ə)ri | Tiền sử hút thuốc |
| 54 | Sleep-related breathing disorders | sliːp rɪˈleɪtɪd ˈbriːðɪŋ dɪsˈɔːdəz | Rối loạn hô hấp liên quan đến giấc ngủ |
| 55 | Chronic obstructive pulmonary disease (COPD) | ˈkrɒnɪk əbˈstrʌktɪv ˈpʌlmən(ə)ri dɪˈziːz | Bệnh phổi tắc nghẽn mạn tính |
| 56 | Sputum production | ˈspjuːtəm prəˈdʌkʃ(ə)n | Tiết đờm |
| 57 | Acute pulmonary process | əˈkjuːt ˈpʌlmən(ə)ri ˈprəʊsɛs | Quá trình phổi cấp tính |
| 58 | Postoperative respiratory failure (PRF) | pəʊst-ˈɒp(ə)rətɪv ˈrɛsp(ə)rət(ə)ri ˈfeɪljə | Suy hô hấp hậu phẫu |
| 59 | Upper respiratory infection | ˈʌpə ˈrɛsp(ə)rət(ə)ri ɪnˈfɛkʃ(ə)n | Nhiễm trùng hô hấp trên |
| 60 | Dyspnea | ˈdɪspniə | Khó thở |
| 61 | Exercise intolerance | ˈɛksəsaɪz ɪnˈtɒlər(ə)ns | Không dung nạp gắng sức |
| 62 | Assess Respiratory Risk in Surgical Patients in Catalonia (ARISCAT) | əˈsɛs ˈrɛsp(ə)rət(ə)ri rɪsk ɪn ˈsɜːdʒɪk(ə)l ˈpeɪʃ(ə)nts ɪn ˌkætəˈləʊnɪə | Đánh giá nguy cơ hô hấp ở người bệnh phẫu thuật tại Catalonia |
| 63 | Pack-years | pæk jɪəz | Bao-năm (đơn vị đo lượng thuốc lá đã hút) |
| 64 | Smoking cessation | ˈsməʊkɪŋ sɛˈseɪʃ(ə)n | Cai thuốc lá |
| 65 | Obstructive sleep apnea (OSA) | əbˈstrʌktɪv sliːp ˈæpnɪə | Ngưng thở khi ngủ do tắc nghẽn |
| 66 | Apnea–hypopnea index | ˈæpnɪə-ˌhaɪpəpˈnɪə ˈɪndɛks | Chỉ số ngưng thở-giảm thở |
| 67 | Polysomnography | ˌpɒlɪsɒmˈnɒɡrəfi | Đa ký giấc ngủ |
| 68 | Pulmonary hypertension (PH) | ˈpʌlmən(ə)ri haɪpəˈtɛnʃ(ə)n | Tăng áp phổi |
| 69 | STOP-BANG questionnaire | stɒp bæŋ ˌkwɛstʃəˈnɛə | Bảng câu hỏi STOP-BANG (sàng lọc ngưng thở khi ngủ) |
| 70 | Decreased laryngeal height | dɪˈkriːst ləˈrɪndʒɪəl haɪt | Giảm chiều cao thanh quản |
| 71 | Positive cough test | ˈpɒzɪtɪv kɒf tɛst | Nghiệm pháp ho dương tính |
| 72 | Functional dependence | ˈfʌŋ(k)ʃ(ə)n(ə)l dɪˈpɛndəns | Phụ thuộc chức năng |
| 73 | American Society of Anesthesiologists (ASA) | əˈmɛrɪkən səˈsaɪəti ɒv ˌænɪsˈθiːzɪɒlədʒɪsts | Hiệp hội Gây mê Hoa Kỳ |
| 74 | Serum albumin | ˈsɪərəm ˈælbjʊmɪn | Albumin huyết thanh |
| 75 | Weight loss | weɪt lɒs | Sụt cân |
| 76 | Blood urea nitrogen | blʌd jʊˈrɪə ˈnaɪtrədʒən | Nitơ urê máu |
| 77 | Neurologic impairment | ˌnjʊərəˈlɒdʒɪk ɪmˈpɛəmənt | Suy giảm thần kinh |
| 78 | Congestive heart failure | kənˈdʒɛstɪv hɑːt ˈfeɪljə | Suy tim sung huyết |
| 79 | Body mass index (BMI) | ˈbɒdi mæs ˈɪndɛks | Chỉ số khối cơ thể |
| 80 | American College of Physicians (ACP) | əˈmɛrɪkən ˈkɒlɪdʒ ɒv fɪˈzɪʃ(ə)nz | Trường Cao đẳng Bác sĩ Hoa Kỳ |
| 81 | Abdominal aortic aneurysm (AAA) | æbˈdɒmɪn(ə)l eɪˈɔːtɪk ˈænjʊrɪz(ə)m | Phình động mạch chủ bụng |
| 82 | Upper abdominal incisions | ˈʌpər æbˈdɒmɪn(ə)l ɪnˈsɪʒ(ə)nz | Vết mổ bụng trên |
| 83 | Emergent surgery | ɪˈmɜːdʒ(ə)nt ˈsɜːdʒ(ə)ri | Phẫu thuật cấp cứu |
| 84 | Laparoscopic surgery | ˌlæp(ə)rəˈskɒpɪk ˈsɜːdʒ(ə)ri | Phẫu thuật nội soi |
| 85 | Endovascular aneurysm repair | ˌɛndəʊˈvæskjʊlər ˈænjʊrɪz(ə)m rɪˈpɛə | Sửa chữa phình mạch nội mạch |
| 86 | Duration of anesthesia | djʊˈreɪʃ(ə)n ɒv ˌænɪsˈθiːzɪə | Thời gian gây mê |
| 87 | Regional anesthesia | ˈriːdʒ(ə)n(ə)l ˌænɪsˈθiːzɪə | Gây tê vùng |
| 88 | Perioperative gastric tube | ˌpɛrɪˈɒp(ə)rətɪv ˈɡæstrɪk tjuːb | Ống thông dạ dày chu phẫu |
| 89 | Nasogastric tubes | ˌneɪzəʊˈɡæstrɪk tjuːbz | Ống thông mũi-dạ dày |
| 90 | Forced expiratory volume in 1 second (FEV1) | fɔːst ɪkˈspaɪrət(ə)ri ˈvɒljuːm ɪn wʌn ˈsɛk(ə)nd | Thể tích thở ra gắng sức trong 1 giây |
| 91 | Arterial blood gases | ɑːˈtɪərɪəl blʌd ˈɡæsɪz | Khí máu động mạch |
| 92 | Hypercapnia | ˌhaɪpəˈkæpnɪə | Tăng CO2 máu |
| 93 | Arterial hypoxemia | ɑːˈtɪərɪəl ˌhaɪpɒkˈsiːmɪə | Giảm oxy máu động mạch |
| 94 | Chest radiographs | tʃɛst ˈreɪdɪəʊɡrɑːfs | Phim X-quang ngực |
| 95 | Exercise testing | ˈɛksəsaɪz ˈtɛstɪŋ | Kiểm tra gắng sức |
| 96 | Six-minute walk test | sɪks ˈmɪnɪt wɔːk tɛst | Nghiệm pháp đi bộ 6 phút |
| 97 | Mean pulmonary artery pressure | miːn ˈpʌlmən(ə)ri ˈɑːt(ə)ri ˈprɛʃə | Áp lực động mạch phổi trung bình |
| 98 | Tricuspid regurgitation | traɪˈkʌspɪd rɪˌɡɜːdʒɪˈteɪʃ(ə)n | Hở van ba lá |
| 99 | Simplified Bernoulli equation | ˈsɪmplɪfaɪd bɜːˈnuːi ɪˈkweɪʒ(ə)n | Phương trình Bernoulli đơn giản hóa |
| 100 | Pulmonary regurgitation | ˈpʌlmən(ə)ri rɪˌɡɜːdʒɪˈteɪʃ(ə)n | Hở van động mạch phổi |
| 101 | Pulmonary acceleration time | ˈpʌlmən(ə)ri əkˌsɛləˈreɪʃ(ə)n taɪm | Thời gian tăng tốc phổi |
| 102 | Risk prediction scores | rɪsk prɪˈdɪkʃ(ə)n skɔːz | Điểm dự đoán nguy cơ |
| 103 | Arozullah respiratory failure index | ɑːˈrəzʊlə ˈrɛsp(ə)rət(ə)ri ˈfeɪljə ˈɪndɛks | Chỉ số suy hô hấp Arozullah |
| 104 | Postoperative pneumonia risk index | pəʊst-ˈɒp(ə)rətɪv njuːˈməʊnɪə rɪsk ˈɪndɛks | Chỉ số nguy cơ viêm phổi hậu phẫu |
| 105 | Surgical lung injury prediction model | ˈsɜːdʒɪk(ə)l lʌŋ ˈɪndʒəri prɪˈdɪkʃ(ə)n ˈmɒd(ə)l | Mô hình dự đoán tổn thương phổi phẫu thuật |
| 106 | Cardiopulmonary exercise testing (CPET) | ˌkɑːdɪəʊˈpʌlmən(ə)ri ˈɛksəsaɪz ˈtɛstɪŋ | Kiểm tra gắng sức tim phổi |
| 107 | Anaerobic threshold (AT) | ænəˈrəʊbɪk ˈθrɛʃəʊld | Ngưỡng yếm khí |
| 108 | Peak oxygen uptake (VO2peak) | piːk ˈɒksɪdʒən ˈʌpteɪk | Lượng oxy tiêu thụ đỉnh |
| 109 | Ventilatory equivalent of carbon dioxide (VE/VCO2) | ˈvɛntɪlət(ə)ri ɪˈkwɪvələnt ɒv ˈkɑːbən daɪˈɒksaɪd | Đương lượng thông khí của carbon dioxide |
| 110 | Maximal oxygen consumption (VO2max) | ˈmæksɪm(ə)l ˈɒksɪdʒən kənˈsʌm(p)ʃən | Lượng oxy tiêu thụ tối đa |
| 111 | Diffusing capacity of the lung for carbon monoxide (DLCO) | dɪˈfjuːzɪŋ kəˈpæsɪti ɒv ðə lʌŋ fɔː ˈkɑːbən mɒˈnɒksaɪd | Khả năng khuếch tán carbon monoxide của phổi |
| 112 | Predicted postoperative (PPO) | prɪˈdɪktɪd pəʊst-ˈɒp(ə)rətɪv | Dự đoán hậu phẫu |
| 113 | Radionuclide lung perfusion scans | ˌreɪdɪəʊˈnjuːklaɪd lʌŋ pəˈfjuːʒən skænz | Xạ hình tưới máu phổi |
| 114 | Shuttle walk test | ˈʃʌt(ə)l wɔːk tɛst | Nghiệm pháp đi bộ con thoi |
| 115 | Symptom-limited stair-climbing test | ˈsɪmptəm ˈlɪmɪtɪd stɛə ˈklaɪmɪŋ tɛst | Nghiệm pháp leo cầu thang giới hạn bởi triệu chứng |
| 116 | Minute ventilation to carbon dioxide output slope | ˈmɪnɪt ˌvɛntɪˈleɪʃ(ə)n tuː ˈkɑːbən daɪˈɒksaɪd ˈaʊtpʊt sləʊp | Độ dốc tỷ lệ thông khí phút với lượng carbon dioxide thải ra |
| 117 | Asthma | ˈæsmə | Hen suyễn |
| 118 | Acute respiratory distress syndrome (ARDS) | əˈkjuːt ˈrɛsp(ə)rət(ə)ri dɪˈstrɛs ˈsɪndrəʊm | Hội chứng suy hô hấp cấp |
| 119 | Pulmonary edema | ˈpʌlmən(ə)ri ɪˈdiːmə | Phù phổi |
| 120 | Pulmonary embolism | ˈpʌlmən(ə)ri ˈɛmbəlɪz(ə)m | Thuyên tắc phổi |
| 121 | American College of Chest Physicians (ACCP) | əˈmɛrɪkən ˈkɒlɪdʒ ɒv tʃɛst fɪˈzɪʃ(ə)nz | Trường Cao đẳng Bác sĩ Lồng ngực Hoa Kỳ |
| 122 | Duke Activity Status Index (DASI) | djuːk ækˈtɪvɪti ˈsteɪtəs ˈɪndɛks | Chỉ số trạng thái hoạt động Duke |
| 123 | Borderline PFT | ˈbɔːdəlaɪn piː-ɛf-tiː | Đo chức năng hô hấp ngưỡng |
| 124 | Hazard ratio | ˈhæzəd ˈreɪʃɪəʊ | Tỷ suất nguy cơ |
| 125 | Cardiopulmonary complications | ˌkɑːdɪəʊˈpʌlmən(ə)ri ˌkɒmplɪˈkeɪʃ(ə)nz | Biến chứng tim phổi |
| 126 | Lobectomy | ləʊˈbɛktəmi | Cắt thùy phổi |
| 127 | Pneumonectomy | ˌnjuːməˈnɛktəmi | Cắt phổi |
| 128 | Lung cancer | lʌŋ ˈkænsə | Ung thư phổi |
| 129 | Spirometry | spaɪˈrɒmɪtri | Đo hô hấp ký |
| 130 | Segment count method | ˈsɛɡmənt kaʊnt ˈmɛθəd | Phương pháp đếm phân đoạn |
| 131 | Lung reduction surgery | lʌŋ rɪˈdʌkʃ(ə)n ˈsɜːdʒ(ə)ri | Phẫu thuật giảm thể tích phổi |
| 132 | Neurosurgery | ˌnjʊərəʊˈsɜːdʒəri | Phẫu thuật thần kinh |
| 133 | Vascular surgery | ˈvæskjʊlə ˈsɜːdʒəri | Phẫu thuật mạch máu |
| 134 | Esophagectomy | ɪˌsɒfəˈdʒɛktəmi | Cắt thực quản |
| 135 | Pleural effusion | ˈplʊər(ə)l ɪˈfjuːʒ(ə)n | Tràn dịch màng phổi |
| 136 | Pneumothorax | ˌnjuːməʊˈθɔːræks | Tràn khí màng phổi |
| 137 | Tracheobronchitis | ˌtreɪkɪəʊbrɒŋˈkaɪtɪs | Viêm khí phế quản |
| 138 | Pulmonary congestion | ˈpʌlmən(ə)ri kənˈdʒɛstʃən | Sung huyết phổi |
| 139 | Preoperative shock | ˌpriːˈɒp(ə)rətɪv ʃɒk | Sốc trước phẫu thuật |
| 140 | Airway obstruction | ˈɛəweɪ əbˈstrʌkʃ(ə)n | Tắc nghẽn đường thở |
| 141 | Hypertension | ˌhaɪpəˈtɛnʃ(ə)n | Tăng huyết áp |
| 142 | Liver disease | ˈlɪvə dɪˈziːz | Bệnh gan |
| 143 | Renal failure | ˈriːn(ə)l ˈfeɪljə | Suy thận |
| 144 | Ascites | əˈsaɪtiːz | Cổ trướng |
| 145 | Transfusion | trænsˈfjuːʒ(ə)n | Truyền máu |
| 146 | Prolonged hospitalization | prəˈlɒŋd hɒˌspɪt(ə)laɪˈzeɪʃən | Nằm viện kéo dài |
| 147 | Acute lung injury (ALI) | əˈkjuːt lʌŋ ˈɪndʒəri | Tổn thương phổi cấp |
| 148 | Neuromuscular blockers | ˌnjʊərəʊˈmʌskjʊlə ˈblɒkəz | Thuốc ức chế thần kinh-cơ |
| 149 | Gastroesophageal reflux disease (GERD) | ˌɡæstrəʊɪˌsɒfəˈdʒiːəl ˈriːflʌks dɪˈziːz | Bệnh trào ngược dạ dày-thực quản |
| 150 | Sepsis | ˈsɛpsɪs | Nhiễm trùng huyết |
| 151 | Anemia | əˈniːmɪə | Thiếu máu |
| 152 | Impaired sensorium | ɪmˈpɛəd sɛnˈsɔːrɪəm | Suy giảm cảm giác |
| 153 | Thoracic surgery | θəˈræsɪk ˈsɜːdʒəri | Phẫu thuật lồng ngực |
| 154 | Abdominal surgery | æbˈdɒmɪn(ə)l ˈsɜːdʒəri | Phẫu thuật bụng |
| 155 | Peripheral vascular | pəˈrɪf(ə)rəl ˈvæskjʊlə | Mạch máu ngoại vi |
| 156 | Functional status | ˈfʌŋ(k)ʃ(ə)n(ə)l ˈsteɪtəs | Tình trạng chức năng |
| 157 | Blood urea | blʌd jʊˈrɪə | Urê máu |
| 158 | Hip surgery | hɪp ˈsɜːdʒəri | Phẫu thuật khớp háng |
| 159 | Lower abdomen | ˈləʊər ˈæbdəmən | Bụng dưới |
| 160 | Gynecologic surgery | ˌɡaɪnəˈkɒlədʒɪk ˈsɜːdʒəri | Phẫu thuật phụ khoa |
| 161 | Urologic surgery | ˌjʊərəˈlɒdʒɪk ˈsɜːdʒəri | Phẫu thuật tiết niệu |
| 162 | Lung opacification | lʌŋ əˌpæsɪfɪˈkeɪʃ(ə)n | Mờ đục phổi |
| 163 | Mediastinum | ˌmiːdɪəˈstaɪnəm | Trung thất |
| 164 | Hilum | ˈhaɪləm | Rốn phổi |
| 165 | Hemidiaphragm | ˌhɛmɪˈdaɪəfræm | Nửa cơ hoành |
| 166 | Nonatelectatic lung | nɒnˌætɪˈlɛktætɪk lʌŋ | Phổi không xẹp |
| 167 | Inhalation | ˌɪnhəˈleɪʃən | Hít vào |
| 168 | Regurgitated gastric contents | rɪˈɡɜːdʒɪteɪtɪd ˈɡæstrɪk ˈkɒntɛnts | Dịch dạ dày trào ngược |
| 169 | Costophrenic angle | ˌkɒstəʊˈfrɛnɪk ˈæŋɡ(ə)l | Góc sườn hoành |
| 170 | Ipsilateral hemidiaphragm | ˌɪpsɪˈlæt(ə)rəl ˌhɛmɪˈdaɪəfræm | Nửa cơ hoành cùng bên |
| 171 | Expiratory wheezing | ɪkˈspaɪrət(ə)ri ˈwiːzɪŋ | Tiếng khò khè khi thở ra |
| 172 | Bronchodilators | ˌbrɒŋkəʊdaɪˈleɪtəz | Thuốc giãn phế quản |
| 173 | Bilateral infiltrates | baɪˈlæt(ə)rəl ˈɪnfɪltreɪts | Thâm nhiễm hai bên |
| 174 | Pulmonary capillary wedge pressure (PCWP) | ˈpʌlmən(ə)ri ˈkæpɪl(ə)ri wɛdʒ ˈprɛʃə | Áp lực mao mạch phổi bít |
| 175 | Purulent sputum | ˈpjʊərʊl(ə)nt ˈspjuːtəm | Đờm mủ |
| 176 | Pulmonary congestion | ˈpʌlmən(ə)ri kənˈdʒɛstʃən | Sung huyết phổi |
| 177 | Acute edema of lung | əˈkjuːt ɪˈdiːmə ɒv lʌŋ | Phù phổi cấp |
| 178 | Congestive heart failure | kənˈdʒɛstɪv hɑːt ˈfeɪljə | Suy tim sung huyết |
| 179 | Aorta | eɪˈɔːtə | Động mạch chủ |
| 180 | Head and neck surgery | hɛd ænd nɛk ˈsɜːdʒəri | Phẫu thuật đầu cổ |
| 181 | General anesthesia | ˈdʒɛn(ə)r(ə)l ˌænɪsˈθiːzɪə | Gây mê toàn thân |
| 182 | Intra-abdominal pressure | ˌɪntrə æbˈdɒmɪn(ə)l ˈprɛʃə | Áp lực trong ổ bụng |
| 183 | Nasogastric tube (NGT) | ˌneɪzəʊˈɡæstrɪk tjuːb | Ống thông mũi-dạ dày |
| 184 | Ventilator-associated pneumonia (VAP) | ˈvɛntɪleɪtər əˈsəʊʃɪeɪtɪd njuːˈməʊnɪə | Viêm phổi liên quan đến máy thở |
| 185 | Ventilator-associated lung injury (VALI) | ˈvɛntɪleɪtər əˈsəʊʃɪeɪtɪd lʌŋ ˈɪndʒəri | Tổn thương phổi liên quan đến máy thở |
| 186 | Postoperative pneumonia (PP) | pəʊst-ˈɒp(ə)rətɪv njuːˈməʊnɪə | Viêm phổi hậu phẫu |
| 187 | Open repair | ˈəʊp(ə)n rɪˈpɛə | Sửa chữa mổ mở |
| 188 | Active processing | ˈæktɪv ˈprəʊsɛsɪŋ | Xử lý tích cực |
| 189 | Peripheral surgery | pəˈrɪf(ə)rəl ˈsɜːdʒəri | Phẫu thuật ngoại vi |
| 190 | General elective surgery | ˈdʒɛn(ə)r(ə)l ɪˈlɛktɪv ˈsɜːdʒəri | Phẫu thuật tự chọn tổng quát |
| 191 | Right ventricular failure | raɪt vɛnˈtrɪkjʊlə ˈfeɪljə | Suy thất phải |
| 192 | Right ventricular compromise | raɪt vɛnˈtrɪkjʊlə ˈkɒmprəmaɪz | Tổn hại thất phải |
| 193 | Cardiac risk index | ˈkɑːdɪæk rɪsk ˈɪndɛks | Chỉ số nguy cơ tim mạch |
| 194 | Charlson comorbidity index | ˈtʃɑːlsən kəʊmɔːˈbɪdɪti ˈɪndɛks | Chỉ số bệnh đồng mắc Charlson |
| 195 | Preoperative anemia | ˌpriːˈɒp(ə)rətɪv əˈniːmɪə | Thiếu máu trước phẫu thuật |
| 196 | Preoperative transfusion | ˌpriːˈɒp(ə)rətɪv trænsˈfjuːʒ(ə)n | Truyền máu trước phẫu thuật |
| 197 | Human immunodeficiency virus | ˈhjuːmən ˌɪmjʊnəʊdɪˈfɪʃ(ə)nsi ˈvaɪrəs | Vi rút suy giảm miễn dịch ở người |
| 198 | Thoracotomy | ˌθɔːrəˈkɒtəmi | Mở ngực |
| 199 | Goldman cardiac risk index | ˈɡəʊldmən ˈkɑːdɪæk rɪsk ˈɪndɛks | Chỉ số nguy cơ tim mạch Goldman |
| 200 | Preoperative sputum production | ˌpriːˈɒp(ə)rətɪv ˈspjuːtəm prəˈdʌkʃ(ə)n | Tiết đờm trước phẫu thuật |
| 201 | Anorectal surgery | ˌeɪnəʊˈrɛkt(ə)l ˈsɜːdʒəri | Phẫu thuật hậu môn-trực tràng |
| 202 | Bariatric surgery | ˌbærɪˈætrɪk ˈsɜːdʒəri | Phẫu thuật béo phì |
| 203 | Ear, nose, and throat (ENT) | ɪə, nəʊz, ænd θrəʊt | Tai, mũi, họng |
| 204 | Foregut | ˈfɔːɡʌt | Đường tiêu hóa trên |
| 205 | Hepatopancreatobiliary | ˌhɛpətəʊˌpæŋkrɪətəʊˈbɪlɪəri | Gan-tụy-mật |
| 206 | Gallbladder | ˈɡɔːlˌblædə | Túi mật |
| 207 | Appendix | əˈpɛndɪks | Ruột thừa |
| 208 | Adrenal gland | əˈdriːn(ə)l ɡlænd | Tuyến thượng thận |
| 209 | Spleen | spliːn | Lách |
| 210 | Hernia | ˈhɜːnɪə | Thoát vị |
| 211 | Ventral hernia | ˈvɛntr(ə)l ˈhɜːnɪə | Thoát vị thành bụng |
| 212 | Inguinal hernia | ˈɪŋɡwɪn(ə)l ˈhɜːnɪə | Thoát vị bẹn |
| 213 | Femoral hernia | ˈfɛm(ə)r(ə)l ˈhɜːnɪə | Thoát vị đùi |
| 214 | Intestinal surgery | ɪnˈtɛstɪn(ə)l ˈsɜːdʒəri | Phẫu thuật ruột |
| 215 | Thyroid | ˈθaɪrɔɪd | Tuyến giáp |
| 216 | Parathyroid | ˌpærəˈθaɪrɔɪd | Tuyến cận giáp |
| 217 | Obstetric | əbˈstɛtrɪk | Sản khoa |
| 218 | Gynecologic | ˌɡaɪnəˈkɒlədʒɪk | Phụ khoa |
| 219 | Orthopedic | ˌɔːθəˈpiːdɪk | Chỉnh hình |
| 220 | Nonvascular extremity | nɒnˈvæskjʊlə ɪkˈstrɛmɪti | Chi không mạch máu |
| 221 | Skin surgery | skɪn ˈsɜːdʒəri | Phẫu thuật da |
| 222 | Spine surgery | spaɪn ˈsɜːdʒəri | Phẫu thuật cột sống |
| 223 | Nonesophageal thoracic | nɒnɪˌsɒfəˈdʒiːəl θəˈræsɪk | Lồng ngực không phải thực quản |
| 224 | Vein surgery | veɪn ˈsɜːdʒəri | Phẫu thuật tĩnh mạch |
| 225 | Urology | jʊˈrɒlədʒi | Tiết niệu học |
| 226 | Global Initiative for Chronic Obstructive Lung Disease (GOLD) | ˈɡləʊb(ə)l ɪˈnɪʃɪətɪv fɔː ˈkrɒnɪk əbˈstrʌktɪv lʌŋ dɪˈziːz | Sáng kiến toàn cầu về bệnh phổi tắc nghẽn mạn tính |
| 227 | Partially dependent | ˈpɑːʃ(ə)li dɪˈpɛndənt | Phụ thuộc một phần |
| 228 | Totally dependent | ˈtəʊt(ə)li dɪˈpɛndənt | Phụ thuộc hoàn toàn |
| 229 | Totally independent | ˈtəʊt(ə)li ˌɪndɪˈpɛndənt | Độc lập hoàn toàn |
| 230 | Systemic inflammatory response syndrome | sɪˈstɛmɪk ɪnˈflæmət(ə)ri rɪˈspɒns ˈsɪndrəʊm | Hội chứng đáp ứng viêm hệ thống |
| 231 | Septic shock | ˈsɛptɪk ʃɒk | Sốc nhiễm trùng |
| 232 | Alcoholism | ˈælkəhɒlɪz(ə)m | Nghiện rượu |
| 233 | Low-risk cardiac | ləʊ rɪsk ˈkɑːdɪæk | Tim mạch nguy cơ thấp |
| 234 | High-risk cardiac | haɪ rɪsk ˈkɑːdɪæk | Tim mạch nguy cơ cao |
| 235 | Low-risk vascular | ləʊ rɪsk ˈvæskjʊlə | Mạch máu nguy cơ thấp |
| 236 | High-risk vascular | haɪ rɪsk ˈvæskjʊlə | Mạch máu nguy cơ cao |
| 237 | High-risk thoracic | haɪ rɪsk θəˈræsɪk | Lồng ngực nguy cơ cao |
| 238 | Restrictive lung disease | rɪˈstrɪktɪv lʌŋ dɪˈziːz | Bệnh phổi hạn chế |
| 239 | Modifying conditions | ˈmɒdɪfaɪɪŋ kənˈdɪʃ(ə)nz | Điều kiện biến đổi |
| 240 | Tobacco use | təˈbækəʊ juːs | Sử dụng thuốc lá |
| 241 | Alcohol abuse | ˈælkəhɒl əˈbjuːs | Lạm dụng rượu |
| 242 | Chemotherapy | ˌkiːməʊˈθɛrəpi | Hóa trị |
| 243 | Amiodarone | əˈmɪədərəʊn | Amiodarone (thuốc chống loạn nhịp tim) |
| 244 | Statins | ˈstætɪnz | Statin (thuốc hạ mỡ máu) |
| 245 | Risk stratification | rɪsk ˌstrætɪfɪˈkeɪʃ(ə)n | Phân tầng nguy cơ |
| 246 | Nine-panel plot | naɪn ˈpæn(ə)l plɒt | Biểu đồ 9 ô |
| 247 | Preoperative shock | ˌpriːˈɒp(ə)rətɪv ʃɒk | Sốc trước phẫu thuật |
| 248 | Ventilatory failure | ˈvɛntɪlət(ə)ri ˈfeɪljə | Suy thông khí |
| 249 | Postoperative outcomes | pəʊst-ˈɒp(ə)rətɪv ˈaʊtkʌmz | Kết quả hậu phẫu |
| 250 | Quality improvement | ˈkwɒlɪti ɪmˈpruːvmənt | Cải thiện chất lượng |
| 251 | Mortality rates | mɔːˈtælɪti reɪts | Tỷ lệ tử vong |
| 252 | Lung volume loss | lʌŋ ˈvɒljuːm lɒs | Mất thể tích phổi |
| 253 | Airway reflexes | ˈɛəweɪ ˈriːflɛksɪz | Phản xạ đường thở |
| 254 | Intraoperative factors | ˌɪntrəˈɒp(ə)rətɪv ˈfæktəz | Yếu tố trong mổ |
| 255 | Blood loss | blʌd lɒs | Mất máu |
| 256 | Intravenous fluids | ˌɪntrəˈviːnəs ˈfluːɪdz | Dịch truyền tĩnh mạch |
| 257 | Airway protection | ˈɛəweɪ prəˈtɛkʃ(ə)n | Bảo vệ đường thở |
| 258 | Cephalad distribution | sɛˈfæləd ˌdɪstrɪˈbjuːʃ(ə)n | Phân bố về phía đầu |
| 259 | Diaphragm excursion | ˈdaɪəfræm ɪkˈskɜːʃ(ə)n | Di động cơ hoành |
| 260 | Recumbent parts | rɪˈkʌmbənt pɑːts | Phần nằm nghỉ |
| 261 | Compensatory overinflation | ˌkɒmp(ə)nˈseɪt(ə)ri ˌəʊvərɪnˈfleɪʃ(ə)n | Quá căng đền bù |
| 262 | Pulmonary distending pressures | ˈpʌlmən(ə)ri dɪˈstɛndɪŋ ˈprɛʃəz | Áp lực giãn nở phổi |
| 263 | Dependent airway closure | dɪˈpɛndənt ˈɛəweɪ ˈkləʊʒə | Đóng đường thở phụ thuộc |
| 264 | Chest examination | tʃɛst ɪɡˌzæmɪˈneɪʃ(ə)n | Khám ngực |
| 265 | Preoperative pulmonary function | ˌpriːˈɒp(ə)rətɪv ˈpʌlmən(ə)ri ˈfʌŋkʃ(ə)n | Chức năng phổi trước phẫu thuật |
| 266 | American Society of Echocardiography | əˈmɛrɪkən səˈsaɪəti ɒv ˌɛkəʊkɑːdɪˈɒɡrəfi | Hiệp hội Siêu âm tim Hoa Kỳ |
| 267 | Diastolic pressure | daɪəˈstɒlɪk ˈprɛʃə | Áp lực tâm trương |
| 268 | Risk reduction strategies | rɪsk rɪˈdʌkʃ(ə)n ˈstrætɪdʒiz | Chiến lược giảm nguy cơ |
| 269 | Dyspnea on exertion (DOE) | ˈdɪspniə ɒn ɪɡˈzɜːʃ(ə)n | Khó thở khi gắng sức |
| 270 | Chest physiotherapy (PT) | tʃɛst ˌfɪzɪəʊˈθɛrəpi | Vật lý trị liệu ngực |
| 271 | Incentive spirometry | ɪnˈsɛntɪv spaɪˈrɒmɪtri | Đo hô hấp ký khuyến khích |
| 272 | Sublobar resection | sʌbˈləʊbə rɪˈsɛkʃən | Cắt dưới thùy phổi |
| 273 | Nonoperative treatment | nɒnˈɒp(ə)rətɪv ˈtriːtmənt | Điều trị không mổ |
| 274 | Minimally invasive surgery | ˈmɪnɪm(ə)li ɪnˈveɪsɪv ˈsɜːdʒəri | Phẫu thuật xâm lấn tối thiểu |
| 275 | Lung resection candidates | lʌŋ rɪˈsɛkʃən ˈkændɪdeɪts | Ứng viên cắt phổi |
| 276 | Coexisting diseases | ˌkəʊɪɡˈzɪstɪŋ dɪˈziːzɪz | Bệnh đồng mắc |
TÀI LIỆU THAM KHẢO
- Canet J., Sabaté S., Mazo V., et. al.: Development and validation of a score to predict postoperative respiratory failure in a multicentre European cohort: a prospective, observational study. Eur J Anaesthesiol 2015; 32: pp. 458-470.
- Yang C.K., Teng A., Lee D.Y., et. al.: Pulmonary complications after major abdominal surgery: National Surgical Quality Improvement Program analysis. J Surg Res 2015; 198: pp. 441-449.
- Kor D.J., Lingineni R.K., Gajic O., et. al.: Predicting risk of postoperative lung injury in high-risk surgical patients: a multicenter cohort study. Anesthesiology 2014; 120: pp. 1168-1181.
- Mazo V., Sabaté S., Canet J., et. al.: Prospective external validation of a predictive score for postoperative pulmonary complications. Anesthesiology 2014; 121: pp. 219-231.
- Gupta H., Gupta P.K., Fang X., et. al.: Development and validation of a risk calculator predicting postoperative respiratory failure. Chest 2011; 140: pp. 1207-1215.
- Canet J., Gallart L., Gomar C., et. al.: Prediction of postoperative pulmonary complications in a population-based surgical cohort. Anesthesiology 2010; 113: pp. 1338-1350.
- Kor D.J., Warner D.O., Alsara A., et. al.: Derivation and diagnostic accuracy of the surgical lung injury prediction model. Anesthesiology 2011; 115: pp. 117-128.
- Ramachandran S.K., Nafiu O.O., Ghaferi A., et. al.: Independent predictors and outcomes of unanticipated early postoperative tracheal intubation after nonemergent, noncardiac surgery. Anesthesiology 2011; 115: pp. 44-53.
- Kaw R., Chung F., Pasupuleti V., et. al.: Meta-analysis of the association between obstructive sleep apnoea and postoperative outcome. Br J Anaesth 2012; 109: pp. 897-906.
- McAlister F.A., Bertsch K., Man J., et. al.: Incidence of and risk factors for pulmonary complications after nonthoracic surgery. Am J Respir Crit Care Med 2005; 171: pp. 514-517.
- Blum J.M., Stentz M.J., Dechert R., et. al.: Preoperative and intraoperative predictors of postoperative acute respiratory distress syndrome in a general surgical population. Anesthesiology 2013; 118: pp. 19-29.
- Arozullah A.M., Khuri S.F., Henderson W.G., et. al.: Participants in the National Veterans Affairs Surgical Quality Improvement Program. Development and validation of a multifactorial risk index for predicting postoperative pneumonia after major noncardiac surgery. Ann Intern Med 2001; 135: pp. 847-857.
- Li C., Yang W.H., Zhou J., et. al.: Risk factors for predicting postoperative complications after open infrarenal abdominal aortic aneurysm repair: results from a single vascular center in China. J Clin Anesth 2013; 25: pp. 371-378.
- Berg H., Roed J., Viby-Mogensen J., et. al.: Residual neuromuscular block is a risk factor for postoperative pulmonary complications: a prospective, randomised, and blinded study of postoperative pulmonary complications after atracurium, vecuronium and pancuronium. Acta Anaesthesiol Scand 1997; 41: pp. 1095-1103.
- Jeong B.H., Shin B., Eom J.S., et. al.: Development of a prediction rule for estimating postoperative pulmonary complications. PLoS One 2014; 9:
- Sasaki N., Meyer M.J., Malviya S.A., et. al.: Effects of neostigmine reversal of nondepolarizing neuromuscular blocking agents on postoperative respiratory outcomes: a prospective study. Anesthesiology 2014; 121: pp. 959-968.
- Kim J.Y., Hildebrandt M.A.T., Pu X., et. al.: Variations in the vascular endothelial growth factor pathway predict pulmonary complications. Ann Thorac Surg 2012; 94: pp. 1079-1084. discussion 1084
- Johnson R.G., Arozullah A.M., Neumayer L., et. al.: Multivariable predictors of postoperative respiratory failure after general and vascular surgery: results from the patient safety in surgery study. J Am Coll Surg 2007; 204: pp. 1188-1198.
- Scholes R.L., Browning L., Sztendur E.M., et. al.: Duration of anaesthesia, type of surgery, respiratory co-morbidity, predicted VO 2 max and smoking predict postoperative pulmonary complications after upper abdominal surgery: an observational study. Aust J Physiother 2009; 55: pp. 191-198.
- Smetana G.W., Lawrence V.A., Cornell J.E.: American College of Physicians: Preoperative pulmonary risk stratification for noncardiothoracic surgery: systematic review for the American College of Physicians. Ann Intern Med 2006; 144: pp. 581-595.
- Kassin M.T., Owen R.M., Perez S.D., et. al.: Risk factors for 30-day hospital readmission among general surgery patients. J Am Coll Surg 2012; 215: pp. 322-330.
- Lawson E.H., Hall B.L., Louie R., et. al.: Association between occurrence of a postoperative complication and readmission: implications for quality improvement and cost savings. Ann Surg 2013; 258: pp. 10-18.
- Smetana G.W.: Preoperative pulmonary evaluation. N Engl J Med 1999; 340: pp. 937-944.
- American Thoracic Society; Infectious Diseases Society of America : Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia. Am J Respir Crit Care Med 2005; 171: pp. 388-416.
- Ephgrave K.S., Kleiman-Wexler R., Pfaller M., et. al.: Postoperative pneumonia: A prospective study of risk factors and morbidity. Surgery 1993; 114: pp. 815-819. discussion 819
- Warner D.O., Warner M.A., Barnes R.D., et. al.: Perioperative respiratory complications in patients with asthma. Anesthesiology 1996; 85: pp. 460-467.
- Warner D.O., Warner M.A., Offord K.P., et. al.: Airway obstruction and perioperative complications in smokers undergoing abdominal surgery. Anesthesiology 1999; 90: pp. 372-379.
- Jammer I., Wickboldt N., Sander M., et. al.: Standards for definitions and use of outcome measures for clinical effectiveness research in perioperative medicine: European Perioperative Clinical Outcome (EPCO) definitions. 2015; 32: pp. 88-105.
- Miskovic A., Lumb A.B.: Postoperative pulmonary complications. Br J Anaesth 2017; 118: pp. 317-334.
- Strandberg A., Tokics L., Brismar B., et. al.: Atelectasis during anaesthesia and in the postoperative period. Acta Anaesthesiol Scand 1986; 30: pp. 154-158.
- Hedenstierna G., Tokics L., Strandberg A., et. al.: Correlation of gas exchange impairment to development of atelectasis during anaesthesia and muscle paralysis. Acta Anaesthesiol Scand 1986; 30: pp. 183-191.
- Reber A., Bein T., Högman M., et. al.: Lung aeration and pulmonary gas exchange during lumbar epidural anaesthesia and in the lithotomy position in elderly patients. Anaesthesia 1998; 53: pp. 854-861.
- Hedenstierna G.: Alveolar collapse and closure of airways: regular effects of anaesthesia. Clin Physiol Funct Imaging 2003; 23: pp. 123-129.
- Reber A., Nylund U., Hedenstierna G.: Position and shape of the diaphragm: implications for atelectasis formation. Anaesthesia 1998; 53: pp. 1054-1061.
- Kleinman B.S., Frey K., VanDrunen M., et. al.: Motion of the diaphragm in patients with chronic obstructive pulmonary disease while spontaneously breathing versus during positive pressure breathing after anesthesia and neuromuscular blockade. Anesthesiology 2002; 97: pp. 298-305.
- Magnusson L., Spahn D.R.: New concepts of atelectasis during general anaesthesia. Br J Anaesth 2003; 91: pp. 61-72.
- Kleinman B.S., Frey K., VanDrunen M., et. al.: Motion of the diaphragm in patients with chronic obstructive pulmonary disease while spontaneously breathing versus during positive pressure breathing after anesthesia and neuromuscular blockade. Anesthesiology. 2002; 97: pp. 298-305.
- Latimer R.G., Dickman M., Day W.C., et. al.: Ventilatory patterns and pulmonary complications after upper abdominal surgery determined by preoperative and postoperative computerized spirometry and blood gas analysis. Am J Surg 1971; 122: pp. 622-632.
- Kelkar K.V.: Post-operative pulmonary complications after non-cardiothoracic surgery. Indian J Anaesth 2015; 59: pp. 599-605.
- Sharma R.R., Axelsson H., Oberg A., et. al.: Diaphragmatic activity after laparoscopic cholecystectomy. Anesthesiology 1999; 91: pp. 406-413.
- van Kaam A.H., Lachmann R.A., Herting E., et. al.: Reducing atelectasis attenuates bacterial growth and translocation in experimental pneumonia. Am J Respir Crit Care Med 2004; 169: pp. 1046-1053.
- Trawöger R., Kolobow T., Cereda M., et. al.: Tracheal mucus velocity remains normal in healthy sheep intubated with a new endotracheal tube with a novel laryngeal seal. Anesthesiology 1997; 86: pp. 1140-1144.
- Sackner M.A., Hirsch J., Epstein S.: Effect of cuffed endotracheal tubes on tracheal mucous velocity. Chest 1975; 68: pp. 774-777.
- Kumar G.V., Nair A.P., Murthy H.S., et. al.: Residual neuromuscular blockade affects postoperative pulmonary function. Anesthesiology 2012; 117: pp. 1234-1244.
- Atkins B.Z., Shah A.S., Hutcheson K.A., et. al.: Reducing hospital morbidity and mortality following esophagectomy. Ann Thorac Surg 2004; 78: pp. 1170-1176. discussion 1170
- Skeletal muscle dysfunction in chronic obstructive pulmonary disease: a statement of the American Thoracic Society and European Respiratory Society : Am J Respir Crit Care Med 1999; 159: pp. S1-S40. (4 Pt 2)
- McAlister F.A., Khan N.A., Straus S.E., et. al.: Accuracy of the preoperative assessment in predicting pulmonary risk after nonthoracic surgery. Am J Respir Crit Care Med 2003; 167: pp. 741-744.
- Hall J.C., Tarala R.A., Hall J.L., et. al.: A multivariate analysis of the risk of pulmonary complications after laparotomy. Chest 1991; 99: pp. 923-927.
- Gupta H., Ramanan B., Gupta P.K., et. al.: Impact of COPD on postoperative outcomes: results from a national database. Chest 2013; 143: pp. 1599-1606.
- Mitchell C.K., Smoger S.H., Pfeifer M.P., et. al.: Multivariate analysis of factors associated with postoperative pulmonary complications following general elective surgery. Arch Surg 1998; 133: pp. 194-198.
- Arozullah A.M., Daley J., Henderson W.G., et. al.: National Veterans Administration Surgical Quality Improvement Program. Multifactorial risk index for predicting postoperative respiratory failure in men after major noncardiac surgery. Ann Surg 2000; 232: pp. 242-253.
- Khongphatthanayothin A., Wong P.C., Samara Y., et. al.: Impact of respiratory syncytial virus infection on surgery for congenital heart disease: postoperative course and outcome. Crit Care Med 1999; 27: pp. 1974-1981.
- Brooks-Brunn J.A.: Predictors of postoperative pulmonary complications following abdominal surgery. Chest 1997; 111: pp. 564-571.
- Warner M.A., Offord K.P., Warner M.E., et. al.: Role of preoperative cessation of smoking and other factors in postoperative pulmonary complications: a blinded prospective study of coronary artery bypass patients. Mayo Clin Proc 1989; 64: pp. 609-616.
- Grønkjær M., Eliasen M., Skov-Ettrup L.S., et. al.: Preoperative smoking status and postoperative complications: a systematic review and meta-analysis. Ann Surg 2014; 259: pp. 52-71.
- Young T., Peppard P.E., Gottlieb D.J.: Epidemiology of obstructive sleep apnea. Am J Respir Crit Care Med 2002; 165: pp. 1217-1239.
- Finkel K.J., Searleman A.C., Tymkew H., et. al.: Prevalence of undiagnosed obstructive sleep apnea among adult surgical patients in an academic medical center. Sleep Med 2009; 10: pp. 753-758.
- Yaggi H.K., Concato J., Kernan W.N., et. al.: Obstructive sleep apnea as a risk factor for stroke and death. N Engl J Med 2005; 353: pp. 2034-2041.
- Loadsman J.A.: Anaesthesia and sleep apnoea. Br J Anaesth 2001; 86: pp. 254-266.
- Memtsoudis S., Liu S.S., Ma Y., et. al.: Perioperative pulmonary outcomes in patients with sleep apnea after noncardiac surgery. Anesth Analg 2011; 112: pp. 113-121.
- Chung F., Subramanyam R., Liao P., et. al.: High STOP-Bang score indicates a high probability of obstructive sleep apnoea. Br J Anaesth 2012; 108: pp. 768-775.
- American Society of Anesthesiologists Task Force on Perioperative Management of Patients with Obstructive Sleep Apnea : Practice guidelines for the perioperative management of patients with obstructive sleep apnea: an updated report by the American Society of Anesthesiologists Task Force on Perioperative Management of Patients with Obstructive Sleep Apnea. Anesthesiology 2014; 120: pp. 268-286.
- Straus S.E., McAlister F.A., Sackett D.L., Deeks J.J.: CARE-COAD1 Group. The accuracy of patient history, wheezing, and laryngeal measurements in diagnosing obstructive airway disease. [published correction appears in JAMA 2000;284(2):181]. JAMA. 2000; 283: pp. 1853-1857.
- Lawrence V.A., Dhanda R., Hilsenbeck S.G., et. al.: Risk of pulmonary complications after elective abdominal surgery. Chest 1996; 110: pp. 744-750.
- Qaseem A., Snow V., Fitterman N., et. al.: Risk assessment for and strategies to reduce perioperative pulmonary complications for patients undergoing noncardiothoracic surgery: a guideline from the American College of Physicians. Ann Intern Med 2006; 144: pp. 575-580.
- Lawrence V.A., Cornell J.E., Smetana G.W.: American College of Physicians. Strategies to reduce postoperative pulmonary complications after noncardiothoracic surgery: systematic review for the American College of Physicians. Ann Intern Med 2006; 144: pp. 596-608.
- Dales R.E., Dionne G., Leech J.A., et. al.: Preoperative prediction of pulmonary complications following thoracic surgery. Chest 1993; 104: pp. 155-159.
- Wong D.H., Weber E.C., Schell M.J., et. al.: Factors associated with postoperative pulmonary complications in patients with severe chronic obstructive pulmonary disease. Anesth Analg 1995; 80: pp. 276-284.
- Guay J., Choi P., Suresh S., et. al.: Neuraxial blockade for the prevention of postoperative mortality and major morbidity: an overview of Cochrane systematic reviews. Cochrane Database Syst Rev 2014; 1: CD010108
- Nelson R., Edwards S., Tse B.: Prophylactic nasogastric decompression after abdominal surgery. Cochrane Database Syst Rev 2007; 3: CD004929
- Hall J.C., Tarala R.A., Hall J.L.: A case-control study of postoperative pulmonary complications after laparoscopic and open cholecystectomy. J Laparoendosc Surg 1996; 6: pp. 87-92.
- Nilsson G., Larsson S., Johnsson F.: Randomized clinical trial of laparoscopic versus open fundoplication: blind evaluation of recovery and discharge period. Br J Surg 2000; 87: pp. 873-878.
- Wahlgren C.M., Malmstedt J.: Swedish Vascular Registry. Outcomes of endovascular abdominal aortic aneurysm repair compared with open surgical repair in high-risk patients: results from the Swedish Vascular Registry. J Vasc Surg 2008; 48: pp. 1382-1388. discussion 1388
- Hausman M.S., Jewell E.S., Engoren M.: Regional versus general anesthesia in surgical patients with chronic obstructive pulmonary disease: does avoiding general anesthesia reduce the risk of postoperative complications?. Anesth Analg 2015; 120: pp. 1405-1412.
- Bullock T.K., Waltrip T.J., Price S.A., et. al.: A retrospective study of nosocomial pneumonia in postoperative patients shows a higher mortality rate in patients receiving nasogastric tube feeding. Am Surg 2004; 70: pp. 822-826.
- De Nino L.A., Lawrence V.A., Averyt E.C., et. al.: Preoperative spirometry and laparotomy: blowing away dollars. Chest 1997; 111: pp. 1536-1541.
- Tisi G.M.: Preoperative evaluation of pulmonary function: validity, indications, and benefits. Am Rev Respir Dis 1979; 119: pp. 293-310.
- Joo H.S., Wong J., Naik V.N., et. al.: The value of screening preoperative chest x-rays: a systematic review. Can J Anaesth 2005; 52: pp. 568-574.
- Rucker L., Frye E.B., Staten M.A.: Usefulness of screening chest roentgenograms in preoperative patients. JAMA 1983; 250: pp. 3209-3211.
- Girish M., Trayner E., Dammann O., et. al.: Symptom-limited stair climbing as a predictor of postoperative cardiopulmonary complications after high-risk surgery. Chest 2001; 120: pp. 1147-1151.
- Awdeh H., Kassak K., Sfeir P., et. al.: The SF-36 and 6-minute walk test are significant predictors of complications after major surgery. World J Surg 2015; 39: pp. 1406-1412.
- Fleisher L.A., Beckman J.A., Brown K.A., et. al.: 2009 ACCF/AHA focused update on perioperative beta blockade incorporated into the ACC/AHA 2007 guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2009; 120: pp. e169-e276.
- Naeije R.: Pulmonary hypertension and right heart failure in chronic obstructive pulmonary disease. Proc Am Thorac Soc 2005; 2: pp. 20-22.
- National Emphysema Treatment Trial Research Group : Rationale and design of the National Emphysema Treatment Trial: a prospective randomized trial of lung volume reduction surgery. Chest 1999; 116: pp. 1750-1761.
- Rudski L.G., Lai W.W., Afilalo J., et. al.: Guidelines for the echocardiographic assessment of the right heart in adults: a report from the American Society of Echocardiography endorsed by the European Association of Echocardiography, a registered branch of the European Society of Cardiology, and the Canadian Society of Echocardiography. J Am Soc Echocardiogr 2010; 23: pp. 685-713. quiz 786
- Lai H.C., Lai H.C., Wang K.Y., et. al.: Severe pulmonary hypertension complicates postoperative outcome of non-cardiac surgery. Br J Anaesth 2007; 99: pp. 184-190.
- Goldman L., Caldera D.L., Nussbaum S.R., et. al.: Multifactorial index of cardiac risk in noncardiac surgical procedures. N Engl J Med 1977; 297: pp. 845-850.
- Little A.G., Rusch V.W., Bonner J.A., et. al.: Patterns of surgical care of lung cancer patients. Ann Thorac Surg 2005; 80: pp. 2051-2056. discussion 2056
- Brunelli A., Kim A.W., Berger K.I., et. al.: Physiologic evaluation of the patient with lung cancer being considered for resectional surgery: diagnosis and management of lung cancer, 3rd ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest 2013; 143: pp. e166S-e190S.
- Stéphan F., Boucheseiche S., Hollande J., et. al.: Pulmonary complications following lung resection: a comprehensive analysis of incidence and possible risk factors. Chest 2000; 118: pp. 1263-1270.
- Patel R.L., Townsend E.R., Fountain S.W.: Elective pneumonectomy: factors associated with morbidity and operative mortality. Ann Thorac Surg 1992; 54: pp. 84-88.
- British Thoracic Society : Society of Cardiothoracic Surgeons of Great Britain and Ireland Working Party: BTS guidelines: guidelines on the selection of patients with lung cancer for surgery. Thorax 2001; 56: pp. 89-108.
- Bolliger C.T., Gückel C., Engel H., et. al.: Prediction of functional reserves after lung resection: comparison between quantitative computed tomography, scintigraphy, and anatomy. Respiration 2002; 69: pp. 482-489.
- Ribas J., Díaz O., Barberà J.A., et. al.: Invasive exercise testing in the evaluation of patients at high-risk for lung resection. Eur Respir J 1998; 12: pp. 1429-1435.
- Salati M., Brunelli A.: Risk stratification in lung resection. Curr Surg Rep 2016; 4:
- Shafiek H., Valera J.L., Togores B., et. al.: Risk of postoperative complications in chronic obstructive lung diseases patients considered fit for lung cancer surgery: beyond oxygen consumption. Eur J Cardiothorac Surg 2016; 50: pp. 772-779.
- Levet D, Jack S, Swart M, et al. Perioperative cardiopulmonary exercise testing (CPET): consensus clinical guidelines on indications, organization, conduct, and physiological interpretation. BJA . 2018;120(3):484,e500.

BÌNH LUẬN