Sách Dịch: Các Trường Hợp Cấp Cứu Về Nội Tiết, Ấn Bản Thứ Nhất
Dịch & Chú Giải: Ths.Bs. Lê Đình Sáng
CHƯƠNG 2. NHIỄM ĐỘC GIÁP DO AMIODARON
Amiodarone-Induced Thyrotoxicosis – Anupam Kotwal and Marius N. Stan
Endocrine Emergencies, Chapter 2, 17-28
MỤC LỤC CHƯƠNG
| Giới thiệu
Cơ chế bệnh sinh và các phân typ Đánh giá chẩn đoán và phân loại Xét nghiệm Chẩn đoán hình ảnh Tổng hợp phân loại nhiễm độc giáp do Amiodarone Tiếp cận điều trị Các liệu pháp bổ trợ Vai trò của việc ngưng và tái sử dụng Amiodarone Vai trò của phẫu thuật cắt tuyến giáp trong điều trị Kết luận |
Giới thiệu
Amiodarone là một acid benzofuranic có đặc tính chống loạn nhịp mạnh, chứa một lượng iod chiếm 37% trọng lượng của nó. Do đó, một viên nén 200 mg (liều duy trì hàng ngày điển hình) cung cấp khoảng 70 mg iod, trong đó 50% có sinh khả dụng. Điều này cần được xem xét trong bối cảnh lượng iod khuyến nghị hàng ngày là 150 mcg mỗi người.¹ Do đó, amiodarone gây ra rối loạn chức năng tuyến giáp ở 15% đến 20% các trường hợp, với tỷ lệ nhiễm độc giáp là khoảng 3% đến 9%. Suy giáp do amiodarone phổ biến hơn ở các vùng đủ iod và may mắn là dễ quản lý hơn so với tình trạng nhiễm độc giáp do amiodarone (AIT) ít gặp hơn. Cách tiếp cận AIT có những thách thức về phân loại, chẩn đoán và quản lý, và đôi khi tình trạng này dẫn đến các biến chứng đe dọa tính mạng. Điều này là do nhiều yếu tố, bao gồm việc sử dụng thuốc này ở những bệnh nhân có bệnh tim mạch từ trước, thiếu một liệu pháp hiệu quả ổn định, thời gian bán thải kéo dài của amiodarone (2 đến 3 tháng), và thực tế là việc ngưng thuốc không phải lúc nào cũng khả thi trong bối cảnh các rối loạn nhịp đe dọa tính mạng kháng với các thuốc chống loạn nhịp thông thường.
AIT đặc biệt liên quan đến tăng tỷ lệ tử vong ở người cao tuổi và ở những người có chức năng tâm thất suy giảm, có thể do sự kết hợp của rối loạn chức năng tim có từ trước và tình trạng nhiễm độc giáp cung lượng tim cao chồng lên, thúc đẩy suy tim ở những bệnh nhân này. Yiu và cộng sự đã chứng minh rằng AIT dự đoán một kết cục tim mạch bất lợi ở 31,6% và tử vong do tim mạch ở 12,6% những bệnh nhân này. Tương tự, O’Sullivan và cộng sự đã chứng minh rằng AIT có liên quan đến tỷ lệ tử vong chung là 10%, nhưng lên đến 50% ở những người bị suy tim tâm thu (phân suất tống máu thất trái dưới 45%). Những quan sát này phù hợp với các phát hiện gần đây ở Pháp, nơi AIT được chứng minh là nguyên nhân phổ biến nhất của cơn bão giáp ở những bệnh nhân nhập viện tại đơn vị chăm sóc tích cực (ICU). Từ quan điểm chung, bất kỳ bệnh nhân nào bị AIT đều có nguy cơ diễn tiến xấu đi vì nhiễm độc giáp có thể thúc đẩy rối loạn chức năng tim ngay cả ở những bệnh nhân không có triệu chứng, đặc biệt là ở những người có bệnh tim như suy tim tâm thu, rối loạn nhịp thất và bệnh tim bẩm sinh. Cách tiếp cận chung đối với AIT và vai trò của các phương thức điều trị cụ thể trong việc quản lý nó sẽ được thảo luận trong các phần dưới đây.
Cơ chế bệnh sinh và các phân typ
Amiodarone gây rối loạn chức năng tuyến giáp thông qua một hoặc sự kết hợp của các cơ chế sau: (1) các yếu tố nội tại của thuốc có tác dụng độc trực tiếp phụ thuộc liều lượng lên các tế bào nang tuyến giáp; và (2) tác động của iod bao gồm ức chế sự khử iod của thyroxine (T4) thành triiodothyronine (T3) nhưng còn bị ảnh hưởng bởi sự hiện diện hay không của bệnh tuyến giáp tự miễn hoặc các nhân tuyến giáp. Theo kinh điển, AIT đã được phân loại thành typ 1 hoặc typ 2, nhưng nhiều khi các trường hợp là hỗn hợp, đặc biệt là khi mới biểu hiện, như trong Bảng 2.1. AIT typ 1 được đặc trưng bởi cường giáp do iod gây ra do tổng hợp hormone quá mức, thường xảy ra ở những bệnh nhân có bệnh tuyến giáp tiềm ẩn như bướu giáp nhân hoặc bệnh Graves tiềm ẩn. Ngược lại, AIT typ 2 được đặc trưng bởi viêm tuyến giáp phá hủy gây giải phóng hormone tuyến giáp quá mức và được báo cáo xảy ra ở những bệnh nhân có tuyến giáp bình thường hoặc bướu giáp nhỏ. AIT typ 1 được báo cáo phổ biến hơn ở các khu vực thiếu iod, trong khi AIT typ 2 phổ biến hơn ở các khu vực đủ iod, và là dạng AIT thường gặp nhất nói chung, chiếm 79% các trường hợp trong một chuỗi nghiên cứu lớn. Tuy nhiên, sự phân chia rõ ràng này không rõ ràng trong nhiều trường hợp có vẻ như có biểu hiện hỗn hợp với sự kết hợp của các đặc điểm chẩn đoán và có lẽ là cơ chế bệnh sinh hỗn hợp của cả AIT typ 1 và typ 2.
Đánh giá chẩn đoán và phân loại
Do tỷ lệ rối loạn chức năng tuyến giáp cao, bệnh nhân được điều trị bằng amiodarone nên được sàng lọc rối loạn chức năng tuyến giáp bằng cách theo dõi các xét nghiệm chức năng tuyến giáp (TFTs). Hướng dẫn của Hiệp hội Tuyến giáp Hoa Kỳ (ATA) năm 2016 về Chẩn đoán và Quản lý Cường giáp và các Nguyên nhân khác của Nhiễm độc giáp đề nghị theo dõi TFTs trước khi bắt đầu điều trị và sau 3 tháng đầu tiên kể từ khi bắt đầu dùng amiodarone, và sau đó định kỳ mỗi 3 và 6 tháng. Điều quan trọng là tránh chẩn đoán rối loạn chức năng tuyến giáp khi xét nghiệm sớm sau khi bắt đầu dùng amiodarone, vì nó gây ra những thay đổi thoáng qua trong TFTs ở nhiều bệnh nhân. Nó gây ra những thay đổi này bằng cách ức chế hoạt động của enzyme 5′-deiodinase typ 1, do đó làm giảm sự chuyển đổi T4 thành T3 ở ngoại vi và giảm độ thanh thải của cả T4 và T3 đảo (rT3). Do đó, nồng độ T4 và rT3 trong huyết thanh tăng lên và nồng độ T3 trong huyết thanh giảm từ 20% đến 25%. Sau đó, cơ chế phản hồi ngược dẫn đến tăng hormone kích thích tuyến giáp (TSH), làm tăng sản xuất hormone tuyến giáp ở một tuyến giáp khỏe mạnh và trạng thái cân bằng được phục hồi với sự bình thường hóa của TSH. Những thay đổi này thường giải quyết trong vòng 3 đến 6 tháng đầu tiên. Do đó, chẩn đoán suy giáp nên được thực hiện dựa trên các xét nghiệm chức năng tuyến giáp được lấy sau 3 đến 6 tháng điều trị bằng amiodarone. Tuy nhiên, chẩn đoán AIT có thể được thực hiện sớm hơn nếu có những thay đổi sinh hóa của nhiễm độc giáp và chúng rõ ràng, chẳng hạn như TSH không thể phát hiện được và T4/T3 tăng cao. Mặc dù bệnh nhân có thể có các đặc điểm lâm sàng tương tự như bất kỳ dạng nhiễm độc giáp nào khác, nhưng có những đặc điểm lâm sàng có thể là duy nhất đối với AIT. Tác dụng của amiodarone có thể ngăn chặn sự xuất hiện của nhịp tim nhanh có triệu chứng. Ngoài ra, có khả năng cao hơn về nhiễm độc giáp thờ ơ, trong đó các đặc điểm giao cảm điển hình của nhiễm độc giáp không có nhưng bệnh nhân bị sụt cân, yếu cơ và chức năng tim xấu đi, một mối lo ngại đặc biệt ở bệnh nhân cao tuổi. Một số bệnh nhân có thể chỉ biểu hiện với tình trạng giữ nước ngày càng tồi tệ, suy tim sung huyết, tái phát rối loạn nhịp tiềm ẩn sau một thời gian yên tĩnh, hoặc có thể phát triển một rối loạn nhịp mới, điều này cần làm dấy lên lo ngại về AIT.
Bảng 2.1 So sánh các loại nhiễm độc giáp do Amiodarone
| Đặc điểm của AIT | AIT Typ 1 | AIT Typ 2 | AIT Hỗn hợp |
|---|---|---|---|
| Cơ chế | Tổng hợp hormone tuyến giáp quá mức (do iod) | Giải phóng hormone tuyến giáp quá mức (viêm tuyến giáp phá hủy) | Đặc điểm của cả hai |
| Cấu trúc và chức năng tuyến giáp có từ trước | Bất thường (nhân hoặc bệnh Graves tiềm ẩn) | Dường như bình thường hoặc bướu giáp nhỏ | Đặc điểm của cả hai |
| Độ tập trung iod-123 tại tuyến giáp | Thường là thấp hoặc thấp-bình thường, nhưng đôi khi bình thường hoặc tăng | Thường rất thấp hoặc không có | Đặc điểm của cả hai |
| Siêu âm tuyến giáp với CFDS | Tăng sinh mạch | Không có hoặc giảm sinh mạch | Đặc điểm của cả hai |
| Điều trị ban đầu | Thionamide. Hiếm khi cần thêm kali perchlorate (chưa được FDA chấp thuận) | Liệu pháp kháng viêm như prednisone | Kết hợp cả hai |
AIT, Nhiễm độc giáp do Amiodarone; CFDS, siêu âm Doppler màu; FDA, Cục quản lý Thực phẩm và Dược phẩm.
XÉT NGHIỆM
AIT biểu hiện với các đặc điểm xét nghiệm điển hình của nhiễm độc giáp là TSH bị ức chế và hormone tuyến giáp T4 và/hoặc T3 tăng cao. Nhiễm độc giáp dưới lâm sàng cũng có thể xuất hiện trong các trường hợp nhẹ khi T3/T4 vẫn bình thường kèm theo TSH bị ức chế. Do amiodarone không ảnh hưởng đến nồng độ globulin gắn hormone tuyến giáp (TBG) trong huyết thanh, những thay đổi về nồng độ T4 tự do và T3 tự do phản ánh những thay đổi của T4 toàn phần và T3 toàn phần. Điều quan trọng là phải loại trừ bệnh không do tuyến giáp hoặc các loại thuốc (heparin, dopamine, glucocorticoid và biotin) là nguyên nhân duy nhất gây ra các bất thường trong xét nghiệm tuyến giáp trước khi chẩn đoán AIT. Bệnh nhân AIT, đặc biệt là những người nhập viện, cũng có thể mắc đồng thời bệnh không do tuyến giáp, làm giảm nồng độ T3; do đó, nồng độ này có thể bình thường khi có sự kết hợp của AIT và bệnh không do tuyến giáp. Tỷ lệ T3/T4, có xu hướng cao hơn ở những bệnh nhân cường giáp tự miễn so với viêm tuyến giáp phá hủy, không hữu ích trong việc chẩn đoán AIT do sự ức chế khử iod của T4 liên quan đến amiodarone. Cần thực hiện xét nghiệm tìm nguyên nhân tự miễn vì sự hiện diện của kháng thể kháng thụ thể TSH cho thấy bệnh Graves tiềm ẩn, do đó phân loại AIT là typ 1; kháng thể kháng thyroperoxidase (TPO) thường dương tính trong AIT typ 1, nhưng không phải là dấu hiệu đặc trưng hoặc cần thiết cho chẩn đoán này (Bảng 2.1). Nồng độ Interleukin-6 (IL-6) trước đây được cho là giúp chẩn đoán AIT nhưng xét nghiệm này hiện không được thực hiện thường quy vì nhiều trường hợp có giá trị IL-6 trùng lặp và sự phân biệt dường như không đủ nhạy và đặc hiệu.
CHẨN ĐOÁN HÌNH ẢNH
Siêu âm tuyến giáp đơn thuần có giá trị chẩn đoán thấp trong AIT, nhưng khi kết hợp với siêu âm Doppler màu (CFDS), nó cung cấp một đánh giá không xâm lấn theo thời gian thực về tình trạng mạch máu của tuyến giáp, có thể rất hữu ích trong việc phân biệt các loại AIT. Do đó, thang điểm CFDS từ 0 (không có mạch máu) đến 3 (mạch máu rất đậm đặc) được sử dụng. Thông thường, AIT typ 2 được đặc trưng bởi không có mạch máu ở tuyến giáp (điểm CFDS 0) do viêm tuyến giáp phá hủy, trong khi AIT typ 1 có mạch máu bình thường đến tăng (điểm CFDS 1, 2 hoặc 3) (Bảng 2.1). Mặc dù CFDS là lựa chọn tốt nhất trong các xét nghiệm chẩn đoán để phân loại AIT, nó không phải lúc nào cũng hữu ích. Đã có báo cáo rằng có tới 42% bệnh nhân được phân loại là typ 2 (không có mạch máu) và 64% được phân loại là typ 1 dựa trên CFDS có thể không đáp ứng với liệu pháp tương ứng. Độ chính xác của siêu âm tuyến giáp với CFDS cũng phụ thuộc nhiều vào kỹ năng và chuyên môn của người thực hiện. Do đó, vẫn cần xác định liệu sự thay đổi trong việc giải thích CFDS có liên quan đến việc thu nhận hình ảnh siêu âm hay do sự hiện diện của AIT typ hỗn hợp. Độ tập trung iod-123 hoặc iod-131 trong 24 giờ của tuyến giáp cũng đã được nghiên cứu như một phương thức để phân loại typ AIT. Về lý thuyết, chỉ số này sẽ rất thấp hoặc không có ở AIT typ 2, trong khi có thể thấp, bình thường hoặc cao ở AIT typ 1. Tuy nhiên, ở các khu vực đủ iod, đặc biệt với lượng iod nạp vào từ amiodarone, hầu hết các trường hợp AIT đều có độ tập trung rất thấp hoặc không có bất kể loại nào; do đó phương pháp chẩn đoán này thường không phải là một phương tiện phân biệt hữu ích. Các đồng vị hạt nhân khác đã được sử dụng vì tính chất dự đoán của chúng trong việc phân biệt các loại AIT. Khả năng dự đoán của xạ hình technetium-99m (Tc)-sestamibi đối với AIT là thấp, và số lượng bệnh nhân được báo cáo nghiên cứu bằng các đồng vị này là nhỏ. Do đó, các phương pháp này có giá trị lâm sàng hạn chế trong việc đánh giá chẩn đoán AIT và nên được dành chủ yếu cho các nghiên cứu.
TỔNG HỢP PHÂN LOẠI NHIỄM ĐỘC GIÁP DO AMIODARONE
Cần nỗ lực để phân loại AIT dựa trên các xét nghiệm và chẩn đoán hình ảnh (thường là CFDS); tuy nhiên, nhiều trường hợp cho thấy các đặc điểm của cả hai (Bảng 2.1) hoặc có thể không đáp ứng với các liệu pháp tương ứng được thiết lập dựa trên phân loại ban đầu. Do đó, không có một xét nghiệm nào có thể xác định chính xác chiến lược điều trị tốt nhất, điều này ít nhất một phần là do sự hiện diện của các dạng bệnh hỗn hợp. Tại Mayo Clinic, chúng tôi đã kết hợp các tiêu chí được báo cáo trước đây cũng như kinh nghiệm lâm sàng của mình, ngoài thông tin thu được từ bệnh học phẫu thuật cắt tuyến giáp, để phân loại các phân typ AIT như dưới đây. Chúng tôi đã sử dụng giới hạn dưới của mức bình thường cho độ tập trung iod phóng xạ 24 giờ trong dân số của chúng tôi, như chúng tôi đã báo cáo trong các ấn phẩm trước đây.
- AIT typ 1: tuyến giáp có nhân hoặc bướu giáp lan tỏa lớn hơn 15 g hoặc kháng thể kháng thụ thể TSH dương tính; với mạch máu tuyến giáp bình thường/tăng trên CFDS hoặc độ tập trung iod phóng xạ 24 giờ lớn hơn 8%.
- AIT typ 2: tuyến giáp bình thường hoặc bướu giáp lan tỏa nhỏ dưới 15 g; với kháng thể kháng thụ thể TSH âm tính và mạch máu tuyến giáp thấp trên siêu âm CFDS.
- Hỗn hợp: tuyến giáp có nhân hoặc bướu giáp lan tỏa lớn hơn 15 g hoặc kháng thể kháng tuyến giáp dương tính; với mạch máu tuyến giáp thấp trên siêu âm CFDS.
Từ quan điểm lâm sàng, AIT có thể phát triển bất cứ lúc nào trong hoặc thậm chí sau khi ngưng amiodarone do lượng lớn thuốc ưa mỡ này lắng đọng trong các mô mỡ, điều này giải thích cho thời gian bán thải dài của nó. Theo dõi tiền cứu 200 bệnh nhân AIT, Tomisti và cộng sự đã chỉ ra rằng các trường hợp AIT typ 1 có nồng độ hormone tuyến giáp cao hơn đáng kể và thời gian khởi phát bệnh trung bình sớm hơn sau khi bắt đầu dùng amiodarone so với typ 2 (trung bình 3,5 tháng so với 30 tháng); do đó, mức độ nghiêm trọng cao hơn và khởi phát nhiễm độc giáp sớm hơn có thể được sử dụng làm tiêu chí bổ sung để phân loại AIT là typ 1.
Tiếp cận điều trị
Có một mức độ khác biệt giữa các chuyên gia về tầm quan trọng của việc xác định loại AIT (Bảng 2.1) để hướng dẫn điều trị. Điều này là do dữ liệu về vấn đề này còn hỗn hợp, với một số nghiên cứu ủng hộ rõ ràng vai trò của nó và những nghiên cứu khác cho thấy lựa chọn điều trị ban đầu và đáp ứng sau đó không bị thay đổi bởi loại AIT. Hướng dẫn của ATA năm 2016 về Chẩn đoán và Quản lý Cường giáp và các Nguyên nhân khác của Nhiễm độc giáp cho rằng vì cơ chế bệnh sinh của AIT chưa được hiểu đầy đủ, sự phân chia kinh điển của AIT thành hai phân typ có thể là một sự đơn giản hóa quá mức. Họ cho rằng nhiều bệnh nhân có dạng AIT hỗn hợp, bệnh nhân được phân loại là typ 1 hoặc 2 thường không đáp ứng với liệu pháp nhắm vào phân typ, và cuối cùng, một số trường hợp AIT typ 2 đáp ứng với các biện pháp thường không hữu ích trong viêm tuyến giáp phá hủy, chẳng hạn như perchlorate và các thuốc cản quang đường uống. Có lẽ vì lý do này mà một số chuỗi nghiên cứu gần đây đã không cố gắng phân loại các phân typ AIT. Mặt khác, Hướng dẫn của Hiệp hội Tuyến giáp Châu Âu (ETA) về Quản lý Rối loạn Chức năng Tuyến giáp liên quan đến Amiodarone đề xuất rằng các xét nghiệm nên được thực hiện để phân biệt phân typ AIT tốt nhất có thể nhằm hướng dẫn điều trị ban đầu. Chúng tôi thấy hữu ích khi sử dụng dữ liệu lâm sàng và các xét nghiệm chẩn đoán cho mục đích phân loại AIT và lựa chọn liệu pháp tiếp theo. Ngoài ra, chúng tôi nhấn mạnh sự cần thiết phải xem xét các bệnh lý tim mạch đi kèm cùng với mức độ nghiêm trọng của nhiễm độc giáp trong việc lựa chọn liệu pháp phù hợp cho bệnh nhân. Liệu pháp này sau đó được điều chỉnh dựa trên đáp ứng ban đầu (Hình 2.1). Do đó, trong thực hành của chúng tôi, chúng tôi khuyến cáo rằng những bệnh nhân ổn định về mặt tim mạch và có bằng chứng rõ ràng hỗ trợ một phân typ riêng biệt của AIT rõ rệt, có thể được thử nghiệm đơn trị liệu phù hợp, hoặc là thuốc kháng giáp (thionamide) hoặc glucocorticoid (Hình 2.1). Vì AIT, đặc biệt là hỗn hợp và typ 1, có thể biểu hiện với nhiễm độc giáp nặng hoặc cơn bão giáp, cần đặc biệt xem xét đến cường độ của liệu pháp kháng giáp và các biện pháp hỗ trợ hệ thống cần thiết (được thảo luận trong Chương 1, “Cơn bão giáp: Nhiễm độc giáp cấp tính”). Tuy nhiên, việc quản lý cơn bão giáp liên quan đến AIT so với các nguyên nhân khác của nhiễm độc giáp có một chút khác biệt do thiếu hiệu quả của các liệu pháp dựa trên iod.
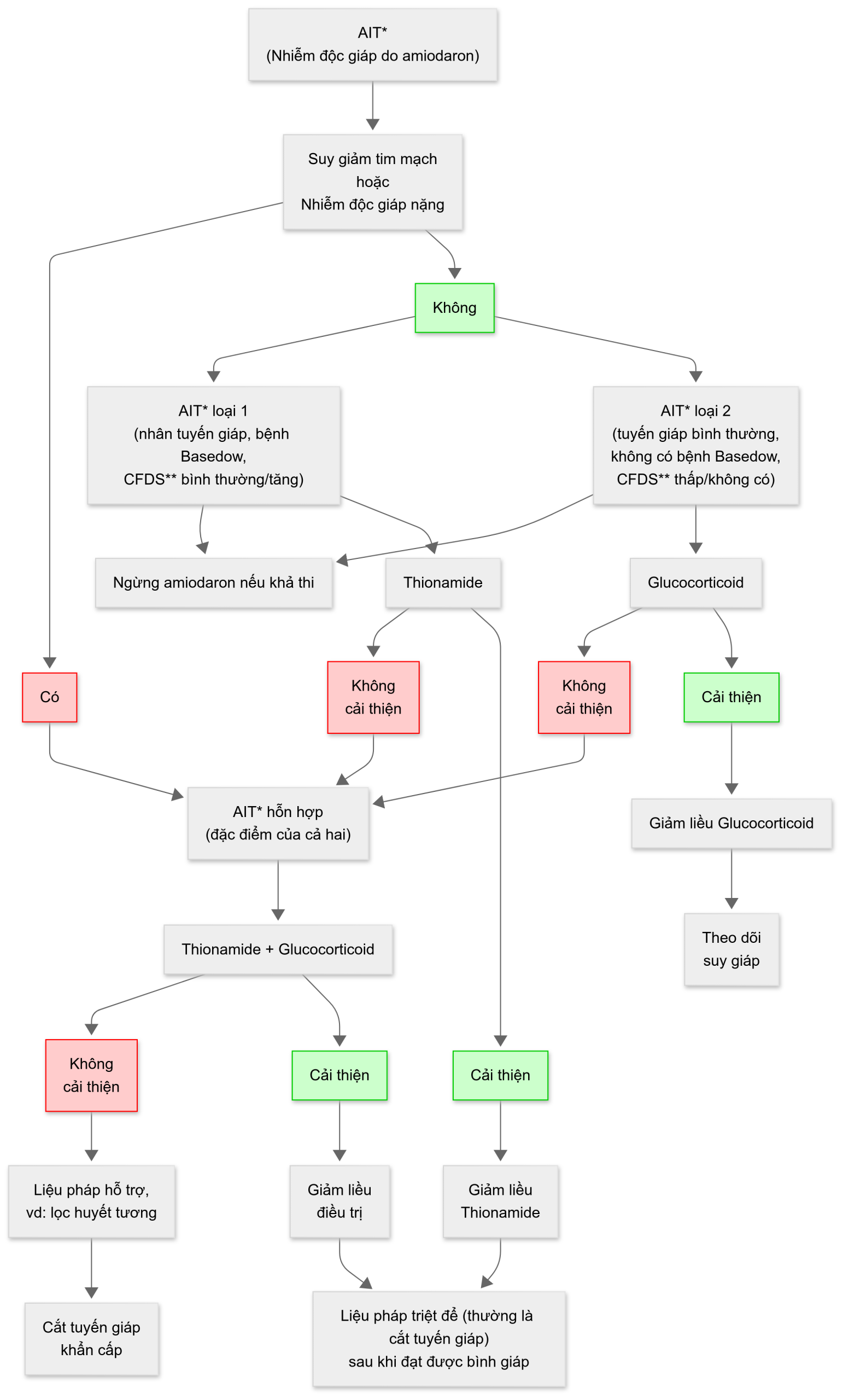
Hình 2.1 Lưu đồ xử trí nhiễm độc giáp do amiodarone. Hộp màu đỏ biểu thị tiên lượng xấu hơn của AIT. Hộp màu xanh lá cây biểu thị tiên lượng khá hoặc đang cải thiện của AIT. AIT, Nhiễm độc giáp do amiodarone; CFDS*, siêu âm Doppler màu; GC*, glucocorticoid.*
AIT typ 1 được điều trị tốt nhất ban đầu bằng thionamide khi liệu pháp nội khoa được khuyến nghị, do cơ chế bệnh sinh được cho là sản xuất hormone tuyến giáp tăng do iod. Thionamide hoạt động bằng cách ức chế enzyme thyroid peroxidase, ức chế sự hữu cơ hóa iod và do đó làm giảm tổng hợp T3 và T4. Vì tuyến giáp chứa đầy iod ít đáp ứng hơn với tác dụng ức chế của các loại thuốc này, nên có thể cần liều cao hơn (40 đến 60 mg/ngày methimazole hoặc liều propylthiouracil tương đương) và thời gian điều trị dài hơn (thường là 3 đến 6 tháng) trước khi đạt được bình giáp. Kali perchlorate (250 mg bốn lần mỗi ngày) có thể được thêm vào thionamide, mặc dù thuốc này không có sẵn thường xuyên ở Hoa Kỳ. Ở liều cao, thuốc này có thể gây mất bạch cầu hạt và thiếu máu bất sản; do đó, liệu pháp nên được giới hạn ở 1 g mỗi ngày và chỉ trong tối đa 4 tuần. Việc ngưng amiodarone trong tình huống này nên được xem xét dựa trên các yếu tố được thảo luận sau. Không có dữ liệu nhất quán về thời gian cần thiết để phục hồi bình giáp trong AIT typ 1; tuy nhiên, nếu nhiễm độc giáp không đáp ứng với thionamide sau 4 đến 6 tuần điều trị, thì trường hợp này nên được coi là AIT hỗn hợp, và nên thêm glucocorticoid. Khi có sẵn perchlorate, nó cũng có thể được thêm vào trước hoặc sau glucocorticoid, với các lưu ý đã được thảo luận trước đó, đặc biệt là xem xét nguy cơ mất bạch cầu hạt khi kết hợp với thionamide. Trong trường hợp không đáp ứng với liệu pháp kết hợp cả thionamide và glucocorticoid hoặc tình trạng tim mạch xấu đi, nên đề nghị phẫu thuật cắt toàn bộ tuyến giáp khẩn cấp (Hình 2.1). Nếu đạt được bình giáp bằng liệu pháp nội khoa, thì nên thực hiện liệu pháp triệt căn dứt điểm, đặc biệt nếu amiodarone được tiếp tục hoặc sẽ được sử dụng lại. Điều này thường là phẫu thuật cắt toàn bộ tuyến giáp, nhưng liệu pháp iod phóng xạ cũng có thể được đề nghị với điều kiện là amiodarone đã được ngưng ít nhất 6 tháng, cùng với việc bình thường hóa bài tiết iod trong nước tiểu và độ tập trung iod phóng xạ 24 giờ của tuyến giáp lớn hơn 8% đến 10%.
AIT typ 2 có xu hướng nhẹ và thường tự khỏi; tuy nhiên, nó có thể làm trầm trọng thêm rối loạn chức năng tim tiềm ẩn và cần được điều trị thích hợp. Glucocorticoid là lựa chọn điều trị, dựa trên các nghiên cứu cho thấy đáp ứng kém với methimazole, acid iopanoic và perchlorate so với glucocorticoid trong AIT typ 2, và được hỗ trợ bởi sinh lý bệnh của nó là viêm tuyến giáp phá hủy. Ngoài việc kiểm soát sự phá hủy viêm của tuyến giáp, glucocorticoid còn ức chế sự chuyển đổi T4 thành T3 ở ngoại vi, do đó hạn chế các biểu hiện của nhiễm độc giáp. Liều khởi đầu thông thường là 0,5 đến 0,7 mg/kg mỗi ngày hoặc 30 đến 40 mg/ngày prednisone trong khoảng 4 tuần, sau đó giảm dần trong 2 đến 3 tháng dựa trên đáp ứng lâm sàng và sinh hóa của bệnh nhân. Sự tái phát của nhiễm độc giáp trong quá trình giảm liều glucocorticoid nên được xử trí bằng cách tạm thời tăng liều và sau đó cố gắng giảm liều chậm hơn. Do tính chất phá hủy của nó, sự hồi phục của AIT typ 2 có thể theo sau bởi suy giáp lâu dài, trong trường hợp đó nên bắt đầu thay thế hormone tuyến giáp. Nếu không có đáp ứng với glucocorticoid sau 4 đến 6 tuần hoặc tình trạng tim mạch xấu đi, thì nên thêm thionamide (Hình 2.1). Nếu, mặc dù đã tăng cường điều trị, tình trạng lâm sàng xấu đi đang xuất hiện hoặc sắp xảy ra, thì nên đề nghị phẫu thuật cắt tuyến giáp.
Thách thức quản lý khó khăn nhất là các dạng AIT hỗn hợp. Trong những trường hợp này, cả hai cơ chế bệnh sinh (tăng tổng hợp hormone tuyến giáp và giải phóng hormone tuyến giáp do tổn thương tuyến) có khả năng đang diễn ra. Do đó, điều trị ban đầu tốt nhất là sự kết hợp của thionamide (có hoặc không có kali perchlorate) và glucocorticoid đường uống (Hình 2.1). Theo hướng dẫn của ATA năm 2016, và phù hợp với thực hành của chúng tôi, điều trị kết hợp cũng nên được bắt đầu trong bối cảnh có tổn thương tim mạch đáng kể (Hình 2.1). Nếu có sự cải thiện nhanh chóng về các đặc điểm lâm sàng và sinh hóa của nhiễm độc giáp, và chức năng tim không xấu đi, rất có thể cơ chế chiếm ưu thế là viêm tuyến giáp phá hủy, và có thể giảm liều thionamide. Liệu pháp dứt điểm nên được thực hiện tương tự sau khi phục hồi bình giáp, như được mô tả cho các trường hợp sau khi bình giáp trong AIT typ 1. Tuy nhiên, nếu tình trạng lâm sàng hoặc sinh hóa không cải thiện sau 4 đến 6 tuần điều trị kết hợp, hoặc nếu tình trạng tim mạch xấu đi, thì nên xem xét phẫu thuật cắt tuyến giáp khẩn cấp (Hình 2.1), với việc quản lý trước phẫu thuật được thảo luận trong một phần riêng.
Các liệu pháp bổ trợ
Một số liệu pháp bổ trợ đã được thử nghiệm cho AIT được kiểm soát kém nhưng không cho thấy hiệu quả nhất quán. Kali perchlorate ức chế symporter natri/iodide và ngăn chặn sự vận chuyển chủ động của iodide vào tuyến giáp và giúp làm cạn kiệt kho dự trữ iod trong tuyến giáp để cải thiện hiệu quả điều trị của thionamide. Kali perchlorate (250 mg bốn lần mỗi ngày) có thể được thêm vào thionamide trong AIT typ 1, nhưng nó không có sẵn thường xuyên ở Hoa Kỳ. Ở liều cao, thuốc này có thể gây mất bạch cầu hạt và thiếu máu bất sản, do đó, liệu pháp nên được giới hạn ở 1 g mỗi ngày và chỉ trong tối đa 4 tuần. Lithium carbonate làm tăng hàm lượng iod trong tuyến giáp và ức chế cả sự hình thành và giải phóng hormone tuyến giáp, nhưng có thể có các tác dụng phụ nổi bật như đái tháo nhạt và rối loạn nhịp tim. Chỉ có một nghiên cứu báo cáo về việc sử dụng nó trong AIT, trong đó sự kết hợp của lithium và propylthiouracil có liên quan đến thời gian đạt được bình giáp ngắn hơn so với chỉ dùng propylthiouracil, nhưng tất cả bệnh nhân cuối cùng đều trở nên bình giáp trong nghiên cứu này. Do đó, bằng chứng còn quá hạn chế để hỗ trợ hiệu quả của nó trong AIT. Acid iopanoic, một chất cản quang chứa iod được sử dụng trong chụp túi mật, ức chế cả sự giải phóng hormone tuyến giáp và sự chuyển đổi T4 thành T3 ở ngoại vi. Ban đầu nó được đề xuất như một liệu pháp nội khoa cho bệnh nhân AIT, nhưng sau đó được Bogazzi và cộng sự chứng minh là kém hiệu quả hơn glucocorticoid trong AIT typ 2. Thuốc này có thể được sử dụng trong việc chuẩn bị bệnh nhân AIT cho phẫu thuật cắt tuyến giáp, vì nó làm giảm nhanh nồng độ T3 trong huyết thanh; tuy nhiên, nó hiện không có sẵn ở Hoa Kỳ. Các chất cô lập acid mật như colestipol và cholestyramine liên kết với các hormone tuyến giáp trong chu trình gan ruột, do đó loại bỏ chúng khỏi tuần hoàn. Chúng có thể được sử dụng như liệu pháp bổ trợ cho thionamide hoặc để kiểm soát nhanh nhiễm độc giáp trong quá trình chuẩn bị phẫu thuật cắt tuyến giáp. Đầy hơi và nhu cầu dùng nhiều liều hàng ngày là những yếu tố hạn chế chính của chúng. Việc điều trị nên được tiếp tục trong 7 đến 10 ngày sau phẫu thuật để ngăn chặn sự tăng vọt T3 sau khi thuốc được ngưng. Lọc huyết tương hoặc trao đổi huyết tương điều trị hoạt động bằng cách loại bỏ các chất phân tử lớn, bao gồm các hormone tuyến giáp gắn với protein, khỏi huyết tương thông qua kỹ thuật lọc máu ngoài cơ thể. Điều này gây ra sự dịch chuyển của các hormone tuyến giáp nội bào vào tuần hoàn, chúng được gắn vào các vị trí gắn kết mới do huyết tương hoặc dung dịch thay thế albumin cung cấp, do đó làm giảm hiệu quả nồng độ hormone tuyến giáp toàn phần. Lọc huyết tương có thể được sử dụng trong các trường hợp nhiễm độc giáp nặng khi cần điều chỉnh nhanh chóng lượng hormone tuyến giáp dư thừa. Dự kiến là một phiên lọc huyết tương có thể làm giảm nồng độ hormone tuyến giáp khoảng 30%; do đó cần nhiều phiên để giảm đáng kể nồng độ hormone tuyến giáp. Liệu pháp này không có tác động đến cơ chế tạo ra hoặc giải phóng hormone tuyến giáp, và tác dụng của nó chỉ là tạm thời. Vai trò chính của nó là cung cấp một cầu nối cho liệu pháp dứt điểm bằng cách nhanh chóng làm giảm nồng độ hormone tuyến giáp lưu hành để chuẩn bị cho phẫu thuật cắt tuyến giáp. Thật không may, nó không phải là không có tác dụng phụ như hạ huyết áp và rối loạn nhịp tim, tính sẵn có hạn chế và chi phí cao, tất cả đều có khả năng ảnh hưởng đến tiện ích của nó trong việc quản lý AIT nặng. Kali iodide, làm giảm cấp tính nồng độ hormone tuyến giáp bằng cách giảm tiết hormone và ức chế sự hữu cơ hóa iodide, đã được sử dụng trước khi phẫu thuật cắt tuyến giáp cho bệnh cường giáp Graves, nhưng không được chỉ định cho AIT.
Vai trò của việc ngưng và tái sử dụng Amiodarone
Hiện tại không có bằng chứng hoặc sự đồng thuận mạnh mẽ nào hỗ trợ việc ngưng amiodarone ở bệnh nhân AIT. Cả hai hướng dẫn của ETA năm 2018 và ATA năm 2016 đều khuyến nghị rằng quyết định này nên được cá nhân hóa đối với việc phân tầng nguy cơ, và được đưa ra một cách đa chuyên khoa với sự tham gia của các bác sĩ tim mạch và nội tiết. Amiodarone nên được tiếp tục nếu chỉ định tim mạch yêu cầu, ví dụ, rối loạn nhịp không kiểm soát được kháng với các thuốc khác. Amiodarone cũng có thể được tiếp tục trong các trường hợp AIT typ 2 rõ ràng, thường nhẹ hơn và sẽ khỏi sau viêm tuyến giáp phá hủy. Điều này được hỗ trợ bởi các quan sát từ một vài nghiên cứu báo cáo không có tác động của việc tiếp tục amiodarone đối với sự hồi phục của AIT typ 2, bao gồm một thử nghiệm lâm sàng ngẫu nhiên của Eskes và cộng sự trên 36 bệnh nhân AIT typ 2, nơi tất cả bệnh nhân đều trở nên bình giáp sau khi điều trị nội khoa AIT mặc dù vẫn đang điều trị bằng amiodarone. Trong một nghiên cứu hồi cứu của Bogazzi và cộng sự, việc tiếp tục amiodarone đã làm trì hoãn việc đạt được bình giáp ở 83 bệnh nhân AIT typ 2 được điều trị bằng prednisone, nhưng AIT đã khỏi ở tất cả, bất kể việc tiếp tục hay ngưng amiodarone.
Vấn đề này trở nên phức tạp trong các trường hợp AIT typ 1 hoặc hỗn hợp, thường nặng hơn và có khả năng có một quá trình kéo dài so với AIT typ 2. Amiodarone có thể được ngưng nếu, sau khi thảo luận với bác sĩ tim mạch, chỉ định tim mạch cho nó đã giải quyết hoặc có thể được quản lý an toàn bằng các liệu pháp khác. Cần lưu ý rằng việc ngưng amiodarone có thể không giúp ích gì trong việc kiểm soát ban đầu của nhiễm độc giáp do thời gian bán thải dài và tính chất ưa mỡ của nó, và nhiễm độc giáp có thể mất tới 8 tháng để giảm bớt sau khi amiodarone được ngưng. Vấn đề khác cần được xem xét ở một bệnh nhân đã ngưng amiodarone là khả năng amiodarone có thể cần được bắt đầu lại vào một thời điểm nào đó sau khi AIT đã khỏi. Thông thường, đây là một vấn đề ở những bệnh nhân đã từng bị AIT typ 1 hoặc hỗn hợp đã được quản lý bằng liệu pháp nội khoa. Trong một nghiên cứu trên 172 bệnh nhân AIT, việc sử dụng lại amiodarone có liên quan đến tái phát AIT trong 30% trường hợp, phần lớn là AIT typ 1 tái phát. Do đó, khi xem xét việc sử dụng lại amiodarone, đội ngũ quản lý nên chú ý đến loại và diễn biến của đợt AIT trước đó. Nếu đợt này kéo dài, nặng, là AIT typ 1 hoặc hỗn hợp, thì nên thực hiện liệu pháp dứt điểm bằng phẫu thuật cắt toàn bộ tuyến giáp. Liệu pháp iod phóng xạ cũng có thể được đề nghị nếu amiodarone đã được ngưng ít nhất 6 tháng, cùng với việc bình thường hóa bài tiết iod trong nước tiểu và độ tập trung iod phóng xạ 24 giờ của tuyến giáp lớn hơn 8% đến 10%. Thường thì nhu cầu sử dụng lại amiodarone đến trong những trường hợp khẩn cấp (rối loạn nhịp nhanh nặng tái phát) và không có cơ hội để triệt căn tuyến giáp dứt điểm. Do đó, Maqdasy và cộng sự đã khám phá vai trò của thionamide dự phòng trước khi tái sử dụng amiodarone và thấy rằng sự tái phát của AIT typ 1 được giảm bớt bằng liệu pháp thionamide dự phòng. Tuy nhiên, không có dữ liệu bổ sung để hỗ trợ mạnh mẽ phương pháp dự phòng này. Hiện tại, phẫu thuật cắt toàn bộ tuyến giáp được ưu tiên là phương pháp quản lý dứt điểm để ngăn ngừa tái phát AIT typ 1 hoặc hỗn hợp trước khi amiodarone được sử dụng lại.
Vai trò của phẫu thuật cắt tuyến giáp trong điều trị
Cả hai hướng dẫn của ETA năm 2018 và ATA năm 2016 đều khuyến nghị phẫu thuật cắt toàn bộ tuyến giáp không chậm trễ khi cần kiểm soát khẩn cấp nhiễm độc giáp ở bệnh nhân AIT (tức là, suy giảm chức năng tim hoặc bệnh tim tiềm ẩn nặng, ở những bệnh nhân có nhiễm độc giáp không đáp ứng với các liệu pháp nội khoa hoặc những người có tác dụng phụ của liệu pháp nội khoa). Thực hành của chúng tôi phù hợp với những khuyến nghị này (Hình 2.1). Vai trò của phẫu thuật cắt tuyến giáp khẩn cấp trong những tình huống này đã được chứng minh bằng các nghiên cứu thuần tập từ một số cơ sở. Họ đã chứng minh hiệu quả và sự an toàn tương đối của can thiệp này đối với các trường hợp AIT nguy kịch, đặc biệt là khi liên quan đến tổn thương tim và kháng với liệu pháp nội khoa. Cappellani và cộng sự đã so sánh quản lý nội khoa với phẫu thuật cắt tuyến giáp trong một đoàn hệ AIT tiền cứu, và thấy rằng phẫu thuật cắt toàn bộ tuyến giáp vượt trội so với liệu pháp nội khoa ở những người bị rối loạn chức năng tâm thu nặng. Nhóm của chúng tôi tại Mayo Clinic đã báo cáo về vai trò của phẫu thuật cắt tuyến giáp trong AIT vào năm 2004 và gần đây hơn là vào năm 2018, cho thấy tỷ lệ biến chứng và tỷ lệ tử vong đã giảm qua các năm (từ 9% xuống 5,4%), và phẫu thuật cắt tuyến giáp vẫn là một lựa chọn có giá trị để quản lý AIT, đặc biệt đối với những bệnh nhân có đáp ứng dưới mức tối ưu với liệu pháp nội khoa và nguy cơ cao bị biến chứng tim, những người chắc chắn có tỷ lệ mắc bệnh và tử vong cao với nhiễm độc giáp không kiểm soát. Trong những tình huống này, phẫu thuật cắt tuyến giáp khẩn cấp không chỉ dẫn đến giải quyết nhiễm độc giáp mà còn cải thiện chức năng tim ở những người có rối loạn chức năng tâm thu từ trước. Nhiễm độc giáp nên được kiểm soát càng nhiều càng tốt bằng thionamide có hoặc không có glucocorticoid, thuốc chẹn beta, hoặc sử dụng tạm thời các liệu pháp bổ trợ (lọc huyết tương ± lithium hoặc chất cô lập acid mật) trước khi phẫu thuật cắt tuyến giáp để giảm thiểu rủi ro phẫu thuật và giảm nguy cơ gây ra cơn bão giáp. Phẫu thuật cắt tuyến giáp cũng được coi là một liệu pháp triệt căn dứt điểm cho những bệnh nhân có nguy cơ tái phát AIT trong khi họ cần tiếp tục hoặc sử dụng lại amiodarone. Để có kết quả phẫu thuật tốt nhất, phẫu thuật cắt tuyến giáp nên được thực hiện bởi một phẫu thuật viên tuyến giáp có kinh nghiệm (người thực hiện hơn 25 ca phẫu thuật tuyến giáp/năm), vì cách tiếp cận này làm giảm đáng kể tỷ lệ biến chứng.
Kết luận
AIT có thể là một thách thức trong chẩn đoán và quản lý. Nó có thể được phân loại là typ 1 hoặc 2 dựa trên rối loạn chức năng tuyến giáp tiềm ẩn và mạch máu của tuyến giáp, nhưng nhiều trường hợp là hỗn hợp. Tỷ lệ mắc bệnh từ AIT đặc biệt cao ở người già và những người có tổn thương tim mạch, đặc biệt là rối loạn chức năng tâm thu. Trong những trường hợp như vậy, nên bắt đầu điều trị kết hợp với thionamide và glucocorticoid. Tình trạng kháng với liệu pháp nội khoa và suy tim mạch là chỉ định cho phẫu thuật cắt toàn bộ tuyến giáp khẩn cấp, giúp điều trị nhiễm độc giáp và cải thiện chức năng tim. Các liệu pháp bổ trợ như lọc huyết tương và chất cô lập acid mật có thể được sử dụng khi có sẵn như một cầu nối cho phẫu thuật cắt tuyến giáp. Chăm sóc đa chuyên khoa bởi các bác sĩ nội tiết, tim mạch, phẫu thuật viên và bác sĩ gây mê là cần thiết để quản lý tối ưu các trường hợp AIT phức tạp và có nguy cơ cao.
Bảng chú giải thuật ngữ Y học Anh-Việt. Chương 2. Nhiễm độc giáp do Amiodarone
| STT | Thuật ngữ tiếng Anh | Cách phát âm (Tham khảo) | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Amiodarone-Induced Thyrotoxicosis | /əˌmi.oʊˈdɑː.roʊn ɪnˈduːst ˌθaɪ.roʊ.tɑːk.sɪˈkoʊ.sɪs/ | Nhiễm độc giáp do Amiodarone |
| 2 | Amiodarone | /əˌmi.oʊˈdɑː.roʊn/ | Amiodarone |
| 3 | Benzofuranic acid | /ˌbɛn.zoʊ.fjʊˈræn.ɪk ˈæs.ɪd/ | Acid benzofuranic |
| 4 | Antiarrhythmic properties | /ˈæn.ti.əˈrɪð.mɪk ˈprɑː.pər.tiz/ | Đặc tính chống loạn nhịp |
| 5 | Iodine | /ˈaɪ.ə.daɪn/ | Iod |
| 6 | Bioavailable | /ˌbaɪ.oʊ.əˈveɪ.lə.bəl/ | Có sinh khả dụng |
| 7 | Recommended iodine intake | /ˌrɛk.əˈmɛn.dɪd ˈaɪ.ə.daɪn ˈɪn.teɪk/ | Lượng iod khuyến nghị |
| 8 | Thyroid dysfunction | /ˈθaɪ.rɔɪd dɪsˈfʌŋk.ʃən/ | Rối loạn chức năng tuyến giáp |
| 9 | Incidence | /ˈɪn.sɪ.dəns/ | Tỷ lệ mắc mới |
| 10 | Thyrotoxicosis | /ˌθaɪ.roʊ.tɑːk.sɪˈkoʊ.sɪs/ | Nhiễm độc giáp |
| 11 | Hypothyroidism | /ˌhaɪ.poʊˈθaɪ.rɔɪ.dɪ.zəm/ | Suy giáp |
| 12 | Iodine-replete regions | /ˈaɪ.ə.daɪn rɪˈpliːt ˈriː.dʒənz/ | Vùng đủ iod |
| 13 | Life-threatening complications | /laɪf ˈθrɛt.nɪŋ ˌkɑːm.plɪˈkeɪ.ʃənz/ | Biến chứng đe dọa tính mạng |
| 14 | Cardiovascular conditions | /ˌkɑːr.di.oʊˈvæs.kjə.lər kənˈdɪʃ.ənz/ | Bệnh lý tim mạch |
| 15 | Half-life | /hæf laɪf/ | Thời gian bán thải |
| 16 | Life-threatening arrhythmias | /laɪf ˈθrɛt.nɪŋ əˈrɪð.mi.əz/ | Rối loạn nhịp đe dọa tính mạng |
| 17 | Refractory | /rɪˈfræk.tə.ri/ | Kháng trị, trơ |
| 18 | Conventional antiarrhythmic medications | /kənˈvɛn.ʃən.əl ˌæn.ti.əˈrɪð.mɪk ˌmɛd.ɪˈkeɪ.ʃənz/ | Thuốc chống loạn nhịp thông thường |
| 19 | Mortality | /mɔːrˈtæl.ə.ti/ | Tỷ lệ tử vong |
| 20 | Impaired ventricular function | /ɪmˈpɛərd vɛnˈtrɪk.jə.lər ˈfʌŋk.ʃən/ | Suy giảm chức năng tâm thất |
| 21 | Preexisting cardiac dysfunction | /ˌpriː.ɪɡˈzɪs.tɪŋ ˈkɑːr.di.æk dɪsˈfʌŋk.ʃən/ | Rối loạn chức năng tim có từ trước |
| 22 | High-output thyrotoxic state | /haɪ ˈaʊt.pʊt ˌθaɪ.roʊˈtɒk.sɪk steɪt/ | Tình trạng nhiễm độc giáp cung lượng tim cao |
| 23 | Heart failure | /hɑːrt ˈfeɪl.jər/ | Suy tim |
| 24 | Adverse cardiovascular outcome | /ˈæd.vɜːrs ˌkɑːr.di.oʊˈvæs.kjə.lər ˈaʊt.kʌm/ | Kết cục tim mạch bất lợi |
| 25 | Cardiovascular mortality | /ˌkɑːr.di.oʊˈvæs.kjə.lər mɔːrˈtæl.ə.ti/ | Tử vong do tim mạch |
| 26 | Systolic heart failure | /sɪsˈtɒl.ɪk hɑːrt ˈfeɪl.jər/ | Suy tim tâm thu |
| 27 | Left ventricular ejection fraction | /lɛft vɛnˈtrɪk.jə.lər ɪˈdʒɛk.ʃən ˈfræk.ʃən/ | Phân suất tống máu thất trái |
| 28 | Thyroid storm | /ˈθaɪ.rɔɪd stɔːrm/ | Cơn bão giáp |
| 29 | Intensive care unit (ICU) | /ɪnˈtɛn.sɪv kɛər ˈjuː.nɪt/ | Đơn vị chăm sóc tích cực (ICU) |
| 30 | Cardiac dysfunction | /ˈkɑːr.di.æk dɪsˈfʌŋk.ʃən/ | Rối loạn chức năng tim |
| 31 | Asymptomatic patients | /ˌeɪ.sɪmp.təˈmæt.ɪk ˈpeɪ.ʃənts/ | Bệnh nhân không có triệu chứng |
| 32 | Ventricular arrhythmias | /vɛnˈtrɪk.jə.lər əˈrɪð.mi.əz/ | Rối loạn nhịp thất |
| 33 | Congenital heart disease | /kənˈdʒɛn.ɪ.təl hɑːrt dɪˈziːz/ | Bệnh tim bẩm sinh |
| 34 | Pathogenesis | /ˌpæθ.əˈdʒɛn.ə.sɪs/ | Cơ chế bệnh sinh |
| 35 | Subtypes | /ˈsʌb.taɪps/ | Các phân typ |
| 36 | Intrinsic drug factors | /ɪnˈtrɪn.zɪk drʌɡ ˈfæk.tərz/ | Các yếu tố nội tại của thuốc |
| 37 | Dose-dependent | /doʊs dɪˈpɛn.dənt/ | Phụ thuộc liều lượng |
| 38 | Direct toxic effect | /dɪˈrɛkt ˈtɒk.sɪk ɪˈfɛkt/ | Tác dụng độc trực tiếp |
| 39 | Thyroid follicular cells | /ˈθaɪ.rɔɪd fəˈlɪk.jə.lər sɛlz/ | Tế bào nang tuyến giáp |
| 40 | Inhibition of deiodination | /ˌɪn.hɪˈbɪʃ.ən əv diːˌaɪ.ə.dɪˈneɪ.ʃən/ | Ức chế sự khử iod |
| 41 | Thyroxine (T4) | /θaɪˈrɒk.siːn/ | Thyroxine (T4) |
| 42 | Triiodothyronine (T3) | /ˌtraɪ.aɪˌoʊ.doʊˈθaɪ.rə.niːn/ | Triiodothyronine (T3) |
| 43 | Autoimmune thyroid disease | /ˌɔː.toʊ.ɪˈmjuːn ˈθaɪ.rɔɪd dɪˈziːz/ | Bệnh tuyến giáp tự miễn |
| 44 | Thyroid nodules | /ˈθaɪ.rɔɪd ˈnɒd.juːlz/ | Nhân tuyến giáp |
| 45 | Type 1 AIT | /taɪp wʌn eɪ aɪ tiː/ | AIT typ 1 |
| 46 | Iodine-induced hyperthyroidism | /ˈaɪ.ə.daɪn ɪnˈduːst ˌhaɪ.pərˈθaɪ.rɔɪ.dɪ.zəm/ | Cường giáp do iod |
| 47 | Excess hormone synthesis | /ɪkˈsɛs ˈhɔːr.moʊn ˈsɪn.θə.sɪs/ | Tổng hợp hormone quá mức |
| 48 | Nodular goiter | /ˈnɒd.jə.lər ˈɡɔɪ.tər/ | Bướu giáp nhân |
| 49 | Latent Graves’ disease | /ˈleɪ.tənt ɡreɪvz dɪˈziːz/ | Bệnh Graves tiềm ẩn |
| 50 | Type 2 AIT | /taɪp tuː eɪ aɪ tiː/ | AIT typ 2 |
| 51 | Destructive thyroiditis | /dɪˈstrʌk.tɪv ˌθaɪ.rɔɪˈdaɪ.tɪs/ | Viêm tuyến giáp phá hủy |
| 52 | Excessive thyroid hormone release | /ɪkˈsɛs.ɪv ˈθaɪ.rɔɪd ˈhɔːr.moʊn rɪˈliːs/ | Giải phóng hormone tuyến giáp quá mức |
| 53 | Small goiter | /smɔːl ˈɡɔɪ.tər/ | Bướu giáp nhỏ |
| 54 | Iodine-deficient areas | /ˈaɪ.ə.daɪn dɪˈfɪʃ.ənt ˈɛə.ri.əz/ | Khu vực thiếu iod |
| 55 | Prevalent | /ˈprɛv.ə.lənt/ | Phổ biến |
| 56 | Mixed presentation | /mɪkst ˌprɛz.ɛnˈteɪ.ʃən/ | Biểu hiện hỗn hợp |
| 57 | Diagnostic features | /ˌdaɪ.əɡˈnɒs.tɪk ˈfiː.tʃərz/ | Đặc điểm chẩn đoán |
| 58 | Mixed pathogenesis | /mɪkst ˌpæθ.əˈdʒɛn.ə.sɪs/ | Cơ chế bệnh sinh hỗn hợp |
| 59 | Diagnostic Evaluation | /ˌdaɪ.əɡˈnɒs.tɪk ɪˌvæl.juˈeɪ.ʃən/ | Đánh giá chẩn đoán |
| 60 | Classification | /ˌklæs.ɪ.fɪˈkeɪ.ʃən/ | Phân loại |
| 61 | Thyroid function tests (TFTs) | /ˈθaɪ.rɔɪd ˈfʌŋk.ʃən tɛsts/ | Các xét nghiệm chức năng tuyến giáp (TFTs) |
| 62 | Hyperthyroidism | /ˌhaɪ.pərˈθaɪ.rɔɪ.dɪ.zəm/ | Cường giáp |
| 63 | Amiodarone initiation | /əˌmi.oʊˈdɑː.roʊn ɪˌnɪʃ.iˈeɪ.ʃən/ | Khởi đầu dùng amiodarone |
| 64 | Transient changes | /ˈtræn.ʒənt ˈtʃeɪn.dʒɪz/ | Những thay đổi thoáng qua |
| 65 | Type 1 5′-deiodinase enzyme | /taɪp wʌn faɪv praɪm diːˈaɪ.ə.dɪ.neɪz ˈɛn.zaɪm/ | Enzyme 5′-deiodinase typ 1 |
| 66 | Peripheral conversion | /pəˈrɪf.ər.əl kənˈvɜːr.ʒən/ | Sự chuyển đổi ở ngoại vi |
| 67 | Clearance | /ˈklɪə.rəns/ | Độ thanh thải |
| 68 | Reverse T3 (rT3) | /rɪˈvɜːrs tiː θriː/ | T3 đảo (rT3) |
| 69 | Feedback mechanism | /ˈfiːd.bæk ˈmɛk.ə.nɪ.zəm/ | Cơ chế phản hồi ngược |
| 70 | Thyroid-stimulating hormone (TSH) | /ˈθaɪ.rɔɪd ˈstɪm.jə.leɪ.tɪŋ ˈhɔːr.moʊn/ | Hormone kích thích tuyến giáp (TSH) |
| 71 | Thyroid hormone production | /ˈθaɪ.rɔɪd ˈhɔːr.moʊn prəˈdʌk.ʃən/ | Sản xuất hormone tuyến giáp |
| 72 | Equilibrium | /ˌiː.kwɪˈlɪb.ri.əm/ | Trạng thái cân bằng |
| 73 | Normalization of TSH | /ˌnɔːr.mə.laɪˈzeɪ.ʃən əv tiː ɛs eɪtʃ/ | Sự bình thường hóa của TSH |
| 74 | Overt | /oʊˈvɜːrt/ | Rõ ràng, rõ rệt |
| 75 | Undetectable TSH | /ˌʌn.dɪˈtɛk.tə.bəl tiː ɛs eɪtʃ/ | TSH không thể phát hiện |
| 76 | Elevated T4/T3 | /ˈɛl.ə.veɪ.tɪd tiː fɔːr tiː θriː/ | T4/T3 tăng cao |
| 77 | Clinical features | /ˈklɪn.ɪ.kəl ˈfiː.tʃərz/ | Đặc điểm lâm sàng |
| 78 | Symptomatic tachycardia | /ˌsɪmp.təˈmæt.ɪk ˌtæk.ɪˈkɑːr.di.ə/ | Nhịp tim nhanh có triệu chứng |
| 79 | Apathetic thyrotoxicosis | /ˌæp.əˈθɛt.ɪk ˌθaɪ.roʊ.tɑːk.sɪˈkoʊ.sɪs/ | Nhiễm độc giáp thờ ơ |
| 80 | Sympathetic features | /ˌsɪm.pəˈθɛt.ɪk ˈfiː.tʃərz/ | Đặc điểm giao cảm |
| 81 | Weight loss | /weɪt lɒs/ | Sụt cân |
| 82 | Muscle weakness | /ˈmʌs.əl ˈwiːk.nəs/ | Yếu cơ |
| 83 | Worsening of cardiac function | /ˈwɜːrs.nɪŋ əv ˈkɑːr.di.æk ˈfʌŋk.ʃən/ | Chức năng tim xấu đi |
| 84 | Elderly patients | /ˈɛl.dər.li ˈpeɪ.ʃənts/ | Bệnh nhân cao tuổi |
| 85 | Fluid retention | /ˈfluː.ɪd rɪˈtɛn.ʃən/ | Giữ nước |
| 86 | Congestive heart failure | /kənˈdʒɛs.tɪv hɑːrt ˈfeɪl.jər/ | Suy tim sung huyết |
| 87 | Recurrence | /rɪˈkɜː.rəns/ | Tái phát |
| 88 | Quiescence | /kwaɪˈɛs.əns/ | Giai đoạn yên tĩnh |
| 89 | New arrhythmia | /njuː əˈrɪð.mi.ə/ | Rối loạn nhịp mới |
| 90 | Laboratory Evaluation | /ˈlæb.rəˌtɔː.ri ɪˌvæl.juˈeɪ.ʃən/ | Xét nghiệm |
| 91 | Suppressed TSH | /səˈprɛst tiː ɛs eɪtʃ/ | TSH bị ức chế |
| 92 | Elevated thyroid hormones | /ˈɛl.ə.veɪ.tɪd ˈθaɪ.rɔɪd ˈhɔːr.moʊnz/ | Hormone tuyến giáp tăng cao |
| 93 | Subclinical thyrotoxicosis | /ˌsʌbˈklɪn.ɪ.kəl ˌθaɪ.roʊ.tɑːk.sɪˈkoʊ.sɪs/ | Nhiễm độc giáp dưới lâm sàng |
| 94 | Thyroid hormone-binding globulin (TBG) | /ˈθaɪ.rɔɪd ˈhɔːr.moʊn ˈbaɪn.dɪŋ ˈɡlɒb.jʊ.lɪn/ | Globulin gắn hormone tuyến giáp (TBG) |
| 95 | Free T4 | /friː tiː fɔːr/ | T4 tự do |
| 96 | Free T3 | /friː tiː θriː/ | T3 tự do |
| 97 | Total T4 | /ˈtoʊ.təl tiː fɔːr/ | T4 toàn phần |
| 98 | Total T3 | /ˈtoʊ.təl tiː θriː/ | T3 toàn phần |
| 99 | Nonthyroidal illness | /nɒn.θaɪˈrɔɪ.dəl ˈɪl.nəs/ | Bệnh không do tuyến giáp |
| 100 | Heparin | /ˈhɛp.ə.rɪn/ | Heparin |
| 101 | Dopamine | /ˈdoʊ.pə.miːn/ | Dopamine |
| 102 | Glucocorticoids | /ˌɡluː.koʊˈkɔːr.tɪ.kɔɪdz/ | Glucocorticoid |
| 103 | Biotin | /ˈbaɪ.ə.tɪn/ | Biotin |
| 104 | Thyroid laboratory abnormalities | /ˈθaɪ.rɔɪd ˈlæb.rəˌtɔː.ri ˌæb.nɔːrˈmæl.ə.tiz/ | Các bất thường xét nghiệm tuyến giáp |
| 105 | Concomitant | /kənˈkɒm.ɪ.tənt/ | Đồng thời |
| 106 | T3/T4 ratio | /tiː θriː tiː fɔːr ˈreɪ.ʃi.oʊ/ | Tỷ lệ T3/T4 |
| 107 | Autonomous hyperthyroidism | /ɔːˈtɒn.ə.məs ˌhaɪ.pərˈθaɪ.rɔɪ.dɪ.zəm/ | Cường giáp tự chủ |
| 108 | Monodeiodination | /ˌmɒ.noʊ.diːˌaɪ.ə.dɪˈneɪ.ʃən/ | Khử một iod |
| 109 | Autoimmune etiology | /ˌɔː.toʊ.ɪˈmjuːn ˌiː.tiˈɒl.ə.dʒi/ | Nguyên nhân tự miễn |
| 110 | TSH receptor antibodies | /tiː ɛs eɪtʃ rɪˈsɛp.tər ˈæn.tɪˌbɒd.iz/ | Kháng thể kháng thụ thể TSH |
| 111 | Thyroid peroxidase (TPO) antibodies | /ˈθaɪ.rɔɪd pəˈrɒk.sɪ.deɪz ˈæn.tɪˌbɒd.iz/ | Kháng thể kháng thyroperoxidase (TPO) |
| 112 | Pathognomonic | /ˌpæθ.əɡ.noʊˈmɒn.ɪk/ | Dấu hiệu đặc trưng |
| 113 | Interleukin-6 (IL-6) | /ˌɪn.tərˈluː.kɪn sɪks/ | Interleukin-6 (IL-6) |
| 114 | Discrimination | /dɪˌskrɪm.ɪˈneɪ.ʃən/ | Sự phân biệt |
| 115 | Sensitive and specific | /ˈsɛn.sɪ.tɪv ænd spəˈsɪf.ɪk/ | Nhạy và đặc hiệu |
| 116 | Radiologic Investigations | /ˌreɪ.di.əˈlɒdʒ.ɪk ɪnˌvɛs.tɪˈɡeɪ.ʃənz/ | Chẩn đoán hình ảnh |
| 117 | Thyroid ultrasonography | /ˈθaɪ.rɔɪd ˌʌl.trə.səˈnɒɡ.rə.fi/ | Siêu âm tuyến giáp |
| 118 | Color-flow Doppler sonography (CFDS) | /ˈkʌl.ər floʊ ˈdɒp.lər səˈnɒɡ.rə.fi/ | Siêu âm Doppler màu (CFDS) |
| 119 | Noninvasive | /ˌnɒn.ɪnˈveɪ.sɪv/ | Không xâm lấn |
| 120 | Real-time assessment | /riːl taɪm əˈsɛs.mənt/ | Đánh giá theo thời gian thực |
| 121 | Thyroid vascularity | /ˈθaɪ.rɔɪd ˌvæs.kjəˈlæ.rə.ti/ | Mạch máu tuyến giáp |
| 122 | Absent vascularity | /ˈæb.sənt ˌvæs.kjəˈlæ.rə.ti/ | Không có mạch máu |
| 123 | Intense vascularity | /ɪnˈtɛns ˌvæs.kjəˈlæ.rə.ti/ | Mạch máu đậm đặc |
| 124 | Hypervascularity | /ˌhaɪ.pərˌvæs.kjəˈlæ.rə.ti/ | Tăng sinh mạch |
| 125 | Decreased vascularity | /dɪˈkriːst ˌvæs.kjəˈlæ.rə.ti/ | Giảm sinh mạch |
| 126 | Operator skills | /ˈɒp.ə.reɪ.tər skɪlz/ | Kỹ năng của người thực hiện |
| 127 | Expertise | /ˌɛk.spɜːrˈtiːz/ | Chuyên môn |
| 128 | Acquisition of the ultrasound images | /ˌæk.wɪˈzɪʃ.ən əv ðə ˈʌl.trə.saʊnd ˈɪm.ɪ.dʒɪz/ | Thu nhận hình ảnh siêu âm |
| 129 | Iodine-123 or iodine-131 uptake | /ˈaɪ.ə.daɪn wʌn tuː θriː ɔːr wʌn θriː wʌn ˈʌp.teɪk/ | Độ tập trung iod-123 hoặc iod-131 |
| 130 | Low, normal, or high uptake | /loʊ, ˈnɔːr.məl, ɔːr haɪ ˈʌp.teɪk/ | Độ tập trung thấp, bình thường, hoặc cao |
| 131 | Iodine load | /ˈaɪ.ə.daɪn loʊd/ | Lượng iod nạp vào |
| 132 | Absent uptake | /ˈæb.sənt ˈʌp.teɪk/ | Không có độ tập trung |
| 133 | Nuclear isotopes | /ˈnuː.kli.ər ˈaɪ.sə.toʊps/ | Đồng vị hạt nhân |
| 134 | Predictive nature | /prɪˈdɪk.tɪv ˈneɪ.tʃər/ | Tính chất dự đoán |
| 135 | Technetium-99m ( |
/tɛkˈniː.ʃi.əm naɪn.ti naɪn ɛm sɛs.təˈmɪ.bi sɪnˈtɪɡ.rə.fi/ | Xạ hình Technetium-99m ( |
| 136 | Limited clinical validation | /ˈlɪm.ɪ.tɪd ˈklɪn.ɪ.kəl ˌvæl.ɪˈdeɪ.ʃən/ | Giá trị lâm sàng hạn chế |
| 137 | Research studies | /rɪˈsɜːrtʃ ˈstʌd.iz/ | Nghiên cứu |
| 138 | Diffuse goiter | /dɪˈfjuːs ˈɡɔɪ.tər/ | Bướu giáp lan tỏa |
| 139 | Positive TSH receptor antibody titer | /ˈpɒz.ə.tɪv tiː ɛs eɪtʃ rɪˈsɛp.tər ˈæn.tɪˌbɒd.i ˈtaɪ.tər/ | Nồng độ kháng thể kháng thụ thể TSH dương tính |
| 140 | 24-hour radioactive iodine uptake | /ˈtwɛn.ti fɔːr ˈaʊ.ər ˌreɪ.di.oʊˈæk.tɪv ˈaɪ.ə.daɪn ˈʌp.teɪk/ | Độ tập trung iod phóng xạ 24 giờ |
| 141 | Negative TSH receptor antibody titer | /ˈnɛɡ.ə.tɪv tiː ɛs eɪtʃ rɪˈsɛp.tər ˈæn.tɪˌbɒd.i ˈtaɪ.tər/ | Nồng độ kháng thể kháng thụ thể TSH âm tính |
| 142 | Low thyroid vascularity | /loʊ ˈθaɪ.rɔɪd ˌvæs.kjəˈlæ.rə.ti/ | Mạch máu tuyến giáp thấp |
| 143 | Positive antithyroid antibodies | /ˈpɒz.ə.tɪv ˌæn.tiˈθaɪ.rɔɪd ˈæn.tɪˌbɒd.iz/ | Kháng thể kháng tuyến giáp dương tính |
| 144 | Lipophilic medication | /ˌlɪp.oʊˈfɪl.ɪk ˌmɛd.ɪˈkeɪ.ʃən/ | Thuốc ưa mỡ |
| 145 | Adipose tissues | /ˈæd.ɪ.poʊz ˈtɪʃ.uːz/ | Mô mỡ |
| 146 | Prospectively | /prəˈspɛk.tɪv.li/ | Tiền cứu |
| 147 | Average onset of disease | /ˈæv.ər.ɪdʒ ˈɒn.sɛt əv dɪˈziːz/ | Thời gian khởi phát bệnh trung bình |
| 148 | Severity | /sɪˈvɛr.ə.ti/ | Mức độ nghiêm trọng |
| 149 | Management | /ˈmæn.ɪdʒ.mənt/ | Điều trị, quản lý |
| 150 | Divergence | /daɪˈvɜːr.dʒəns/ | Sự khác biệt, sự phân kỳ |
| 151 | Initial therapy choice | /ɪˈnɪʃ.əl ˈθɛr.ə.pi tʃɔɪs/ | Lựa chọn điều trị ban đầu |
| 152 | Oversimplification | /ˌoʊ.vər.sɪm.plɪ.fɪˈkeɪ.ʃən/ | Sự đơn giản hóa quá mức |
| 153 | Subtype directed therapy | /ˈsʌb.taɪp dɪˈrɛk.tɪd ˈθɛr.ə.pi/ | Liệu pháp nhắm vào phân typ |
| 154 | Perchlorate | /pərˈklɔː.reɪt/ | Perchlorate |
| 155 | Oral cholecystographic agents | /ˈɔː.rəl ˌkoʊ.lɪ.sɪs.toʊˈɡræf.ɪk ˈeɪ.dʒənts/ | Thuốc cản quang đường uống (chụp túi mật) |
| 156 | Amiodarone-Associated Thyroid Dysfunction | /əˌmi.oʊˈdɑː.roʊn əˈsoʊ.ʃi.eɪ.tɪd ˈθaɪ.rɔɪd dɪsˈfʌŋk.ʃən/ | Rối loạn chức năng tuyến giáp liên quan đến Amiodarone |
| 157 | Subclassification | /ˌsʌbˌklæs.ɪ.fɪˈkeɪ.ʃən/ | Phân loại phụ |
| 158 | Therapy selection | /ˈθɛr.ə.pi sɪˈlɛk.ʃən/ | Lựa chọn liệu pháp |
| 159 | Preexistent cardiovascular comorbidities | /ˌpriː.ɪɡˈzɪs.tɪŋ ˌkɑːr.di.oʊˈvæs.kjə.lər ˌkoʊ.mɔːrˈbɪd.ə.tiz/ | Các bệnh lý tim mạch đi kèm có từ trước |
| 160 | Monotherapy | /ˌmɒn.oʊˈθɛr.ə.pi/ | Đơn trị liệu |
| 161 | Antithyroid drug (thionamide) | /ˌæn.tiˈθaɪ.rɔɪd drʌg (θaɪˈɒn.ə.maɪd)/ | Thuốc kháng giáp (thionamide) |
| 162 | Systemic support measures | /sɪsˈtɛm.ɪk səˈpɔːrt ˈmɛʒ.ərz/ | Các biện pháp hỗ trợ hệ thống |
| 163 | Iodine-based therapies | /ˈaɪ.ə.daɪn beɪst ˈθɛr.ə.piz/ | Các liệu pháp dựa trên iod |
| 164 | Medical therapy | /ˈmɛd.ɪ.kəl ˈθɛr.ə.pi/ | Liệu pháp nội khoa |
| 165 | Presumed pathogenic mechanism | /prɪˈzjuːmd ˌpæθ.ə.dʒəˈnɛt.ɪk ˈmɛk.ə.nɪ.zəm/ | Cơ chế bệnh sinh giả định |
| 166 | Thyroid peroxidase | /ˈθaɪ.rɔɪd pəˈrɒk.sɪ.deɪz/ | Thyroid peroxidase |
| 167 | Iodine organification | /ˈaɪ.ə.daɪn ɔːrˌɡæn.ɪ.fɪˈkeɪ.ʃən/ | Sự hữu cơ hóa iod |
| 168 | Potassium perchlorate | /pəˈtæs.i.əm pərˈklɔː.reɪt/ | Kali perchlorate |
| 169 | Agranulocytosis | /əˌɡræn.jə.loʊ.saɪˈtoʊ.sɪs/ | Mất bạch cầu hạt |
| 170 | Aplastic anemia | /ˌeɪˈplæs.tɪk əˈniː.mi.ə/ | Thiếu máu bất sản |
| 171 | Euthyroidism | /juːˈθaɪ.rɔɪ.dɪ.zəm/ | Bình giáp |
| 172 | Combined therapy | /kəmˈbaɪnd ˈθɛr.ə.pi/ | Liệu pháp kết hợp |
| 173 | Emergency total thyroidectomy | /ɪˈmɜːr.dʒən.si ˈtoʊ.təl ˌθaɪ.rɔɪˈdɛk.tə.mi/ | Phẫu thuật cắt toàn bộ tuyến giáp khẩn cấp |
| 174 | Definitive ablative therapy | /dɪˈfɪn.ɪ.tɪv əˈbleɪ.tɪv ˈθɛr.ə.pi/ | Liệu pháp triệt căn dứt điểm |
| 175 | Radioactive iodine ablation | /ˌreɪ.di.oʊˈæk.tɪv ˈaɪ.ə.daɪn əˈbleɪ.ʃən/ | Liệu pháp iod phóng xạ |
| 176 | Normalized urinary iodine excretion | /ˈnɔːr.mə.laɪzd ˈjʊə.rɪ.nə.ri ˈaɪ.ə.daɪn ɪkˈskriː.ʃən/ | Bài tiết iod trong nước tiểu bình thường |
| 177 | Self-resolving | /sɛlf rɪˈzɒl.vɪŋ/ | Tự khỏi |
| 178 | Iopanoic acid | /ˌaɪ.oʊ.pəˈnoʊ.ɪk ˈæs.ɪd/ | Acid iopanoic |
| 179 | Inflammatory destruction | /ɪnˈflæm.ə.tɔː.ri dɪˈstrʌk.ʃən/ | Sự phá hủy do viêm |
| 180 | Prednisone | /ˈprɛd.nɪ.soʊn/ | Prednisone |
| 181 | Tapered (dose) | /ˈteɪ.pərd (doʊs)/ | Giảm dần (liều) |
| 182 | Biochemical response | /ˌbaɪ.oʊˈkɛm.ɪ.kəl rɪˈspɒns/ | Đáp ứng sinh hóa |
| 183 | Exacerbation | /ɪɡˌzæs.ərˈbeɪ.ʃən/ | Đợt cấp, sự trầm trọng hơn |
| 184 | Long-term hypothyroidism | /lɒŋ tɜːrm ˌhaɪ.poʊˈθaɪ.rɔɪ.dɪ.zəm/ | Suy giáp lâu dài |
| 185 | Thyroid hormone replacement | /ˈθaɪ.rɔɪd ˈhɔːr.moʊn rɪˈpleɪs.mənt/ | Liệu pháp thay thế hormone tuyến giáp |
| 186 | Escalating the therapy | /ˈɛs.kə.leɪ.tɪŋ ðə ˈθɛr.ə.pi/ | Tăng cường điều trị (leo thang) |
| 187 | Clinical deterioration | /ˈklɪn.ɪ.kəl dɪˌtɪə.ri.əˈreɪ.ʃən/ | Tình trạng lâm sàng xấu đi |
| 188 | Adjunct Therapies | /ˈædʒ.ʌŋkt ˈθɛr.ə.piz/ | Các liệu pháp bổ trợ |
| 189 | Sodium/iodide symporter | /ˈsoʊ.di.əm ˈaɪ.ə.daɪd sɪmˈpɔːr.tər/ | Đồng vận chuyển natri/iodide |
| 190 | Intrathyroidal iodine stores | /ˌɪn.trəˈθaɪ.rɔɪ.dəl ˈaɪ.ə.daɪn stɔːrz/ | Kho dự trữ iod trong tuyến giáp |
| 191 | Lithium carbonate | /ˈlɪθ.i.əm ˈkɑːr.bə.neɪt/ | Lithium carbonate |
| 192 | Diabetes insipidus | /ˌdaɪ.əˈbiː.tiːz ɪnˈsɪp.ɪ.dəs/ | Đái tháo nhạt |
| 193 | Radiocontrast medium | /ˌreɪ.di.oʊˈkɒn.træst ˈmiː.di.əm/ | Thuốc cản quang |
| 194 | Cholecystography | /ˌkoʊ.lɪ.sɪˈstɒɡ.rə.fi/ | Chụp túi mật |
| 195 | Bile acid sequestrants | /baɪl ˈæs.ɪd sɪˈkwɛs.trənts/ | Chất cô lập acid mật |
| 196 | Plasmapheresis | /ˌplæz.mə.fəˈriː.sɪs/ | Lọc huyết tương |
| 197 | Therapeutic plasma exchange | /ˌθɛr.əˈpjuː.tɪk ˈplæz.mə ɪksˈtʃeɪndʒ/ | Trao đổi huyết tương điều trị |
| 198 | Extracorporeal blood purification | /ˌɛk.strə.kɔːrˈpɔː.ri.əl blʌd ˌpjʊə.rɪ.fɪˈkeɪ.ʃən/ | Lọc máu ngoài cơ thể |
| 199 | Albumin replacement solution | /ˈæl.bju.mɪn rɪˈpleɪs.mənt səˈluː.ʃən/ | Dung dịch thay thế albumin |
| 200 | Definitive therapy | /dɪˈfɪn.ɪ.tɪv ˈθɛr.ə.pi/ | Liệu pháp dứt điểm |
TÀI LIỆU THAM KHẢO
- Trumbo P., Yates A.A., Schlicker S., Poos M.: Dietary reference intakes: vitamin A, vitamin K, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc. J Am Diet Assoc 2001; 101: pp. 294-301.
- Bogazzi F., Bartalena L., Martino E.: Approach to the patient with amiodarone-induced thyrotoxicosis. J Clin Endocrinol Metab 2010; 95: pp. 2529-2535.
- Batcher E.L., Tang X.C., Singh B.N., et. al.: Thyroid function abnormalities during amiodarone therapy for persistent atrial fibrillation. Am J Med 2007; 120: pp. 880-885.
- Farhan H., Albulushi A., Taqi A., et. al.: Incidence and pattern of thyroid dysfunction in patients on chronic amiodarone therapy: experience at a tertiary care centre in Oman. Open Cardiovasc Med J 2013; 7: pp. 122-126.
- Uchida T., Kasai T., Takagi A., et. al.: Prevalence of amiodarone-induced thyrotoxicosis and associated risk factors in Japanese patients. Int J Endocrinol 2014; 2014:
- Bogazzi F., Bartalena L., Dell’Unto E., et. al.: Proportion of type 1 and type 2 amiodarone-induced thyrotoxicosis has changed over a 27-year period in Italy. Clin Endocrinol (Oxf) 2007; 67: pp. 533-537.
- Martino E., Safran M., Aghini-Lombardi F., et. al.: Environmental iodine intake and thyroid dysfunction during chronic amiodarone therapy. Ann Intern Med 1984; 101: pp. 28-34.
- Plomp T.A., van Rossum J.M., Robles de Medina E.O., van Lier T., Maes R.A.: Pharmacokinetics and body distribution of amiodarone in man. Arzneimittelforschung 1984; 34: pp. 513-520.
- Conen D., Melly L., Kaufmann C., et. al.: Amiodarone-induced thyrotoxicosis: clinical course and predictors of outcome. J Am Coll Cardiol 2007; 49: pp. 2350-2355.
- Bogazzi F., Dell’Unto E., Tanda M.L., et. al.: Long-term outcome of thyroid function after amiodarone-induced thyrotoxicosis, as compared to subacute thyroiditis. J Endocrinol Invest 2006; 29: pp. 694-699.
- Yiu K.H., Jim M.H., Siu C.W., et. al.: Amiodarone-induced thyrotoxicosis is a predictor of adverse cardiovascular outcome. J Clin Endocrinol Metab 2009; 94: pp. 109-114.
- O’Sullivan A.J., Lewis M., Diamond T.: Amiodarone-induced thyrotoxicosis: left ventricular dysfunction is associated with increased mortality. Eur J Endocrinol 2006; 154: pp. 533-536.
- Bourcier S., Coutrot M., Kimmoun A., et. al.: Thyroid storm in the ICU: a retrospective multicenter study. Crit Care Med 2020; 48: pp. 83-90.
- Martino E., Bartalena L., Bogazzi F., Braverman L.E.: The effects of amiodarone on the thyroid. Endocr Rev 2001; 22: pp. 240-254.
- Bogazzi F., Tomisti L., Bartalena L., Aghini-Lombardi F., Martino E.: Amiodarone and the thyroid: a 2012 update. J Endocrinol Invest 2012; 35: pp. 340-348.
- Brennan M.D., Erickson D.Z., Carney J.A., Bahn R.S.: Nongoitrous (type I) amiodarone-associated thyrotoxicosis: evidence of follicular disruption in vitro and in vivo. Thyroid 1995; 5: pp. 177-183.
- Theodoraki A., Vanderpump M.P.: Thyrotoxicosis associated with the use of amiodarone: the utility of ultrasound in patient management. Clin Endocrinol (Oxf) 2015;
- Bartalena L., Bogazzi F., Chiovato L., Hubalewska-Dydejczyk A., Links T.P., Vanderpump M.: 2018 European Thyroid Association (ETA) guidelines for the management of amiodarone-associated thyroid dysfunction. Eur Thyroid J 2018; 7: pp. 55-66.
- Tomisti L., Rossi G., Bartalena L., Martino E., Bogazzi F.: The onset time of amiodarone-induced thyrotoxicosis (AIT) depends on AIT type. Eur J Endocrinol 2014; 171: pp. 363-368.
- Bartalena L., Bogazzi F., Martino E.: Amiodarone-induced thyrotoxicosis: a difficult diagnostic and therapeutic challenge. Clin Endocrinol (Oxf) 2002; 56: pp. 23-24.
- Kotwal A., Touchan B., Seetharaman K.Y., Haas R.A., Lithgow M., Malkani S.: Mixed amiodarone-induced thyrotoxicosis refractory to medical therapy and plasmapheresis. J Endocrinol Metab 2015; 5: pp. 220-223.
- Ross D.S., Burch H.B., Cooper D.S., et. al.: 2016 American Thyroid Association guidelines for diagnosis and management of hyperthyroidism and other causes of thyrotoxicosis. Thyroid 2016; 26: pp. 1343-1421.
- Balzano S., Sau F., Bartalena L., et. al.: Diagnosis of amiodarone-iodine-induced thyrotoxicosis(AIIT) associated with severe nonthyroidal illness. J Endocrinol Invest 1987; 10: pp. 589-591.
- Daniels G.H.: Amiodarone-induced thyrotoxicosis. J Clin Endocrinol Metab 2001; 86: pp. 3-8.
- Tomisti L., Urbani C., Rossi G., et. al.: The presence of anti-thyroglobulin (TgAb) and/or anti-thyroperoxidase antibodies (TPOAb) does not exclude the diagnosis of type 2 amiodarone-induced thyrotoxicosis. J Endocrinol Invest 2016; 39: pp. 585-591.
- Bartalena L., Grasso L., Brogioni S., Aghini-Lombardi F., Braverman L.E., Martino E.: Serum interleukin-6 in amiodarone-induced thyrotoxicosis. J Clin Endocrinol Metab 1994; 78: pp. 423-427.
- Bogazzi F., Martino E., Dell’Unto E., et. al.: Thyroid color flow Doppler sonography and radioiodine uptake in 55 consecutive patients with amiodarone-induced thyrotoxicosis. J Endocrinol Invest 2003; 26: pp. 635-640.
- Loy M., Perra E., Melis A., et. al.: Color-flow Doppler sonography in the differential diagnosis and management of amiodarone-induced thyrotoxicosis. Acta Radiol 2007; 48: pp. 628-634.
- Macedo T.A., Chammas M.C., Jorge P.T., et. al.: Differentiation between the two types of amiodarone-associated thyrotoxicosis using duplex and amplitude Doppler sonography. Acta Radiol 2007; 48: pp. 412-421.
- Eaton S.E., Euinton H.A., Newman C.M., Weetman A.P., Bennet W.M.: Clinical experience of amiodarone-induced thyrotoxicosis over a 3-year period: role of colour-flow Doppler sonography. Clin Endocrinol (Oxf) 2002; 56: pp. 33-38.
- Wong R., Cheung W., Stockigt J.R., Topliss D.J.: Heterogeneity of amiodarone-induced thyrotoxicosis: evaluation of colour-flow Doppler sonography in predicting therapeutic response. Intern Med J 2003; 33: pp. 420-426.
- Pattison D.A., Westcott J., Lichtenstein M., et. al.: Quantitative assessment of thyroid-to-background ratio improves the interobserver reliability of technetium-99m sestamibi thyroid scintigraphy for investigation of amiodarone-induced thyrotoxicosis. Nucl Med Commun 2015; 36: pp. 356-362.
- Piga M., Cocco M.C., Serra A., Boi F., Loy M., Mariotti S.: The usefulness of 99mTc-sestaMIBI thyroid scan in the differential diagnosis and management of amiodarone-induced thyrotoxicosis. Eur J Endocrinol 2008; 159: pp. 423-429.
- Eskes S.A., Wiersinga W.M.: Amiodarone and thyroid. Best Pract Res Clin Endocrinol Metab 2009; 23: pp. 735-751.
- Stan M.N., Ammash N.M., Warnes C.A., et. al.: Body mass index and the development of amiodarone-induced thyrotoxicosis in adults with congenital heart disease–a cohort study. Int J Cardiol 2013; 167: pp. 821-826.
- Stan M.N., Sathananthan M., Warnes C.A., Brennan M.D., Thapa P., Bahn R.S.: Amiodarone-induced thyrotoxicosis in adults with congenital heart disease–clinical presentation and response to therapy. Endocr Pract 2014; 20: pp. 33-40.
- Kotwal A.: Thyroidectomy for amiodarone-induced thyrotoxicosis: Mayo Clinic experience. J Endocr Soc 2018; 2: pp. 1226-1235.
- Huang C.J., Chen P.J., Chang J.W., et. al.: Amiodarone-induced thyroid dysfunction in Taiwan: a retrospective cohort study. Int J Clin Pharm 2014; 36: pp. 405-411.
- Patel N., Inder W.J., Sullivan C., Kaye G.: An audit of amiodarone-induced thyrotoxicosis–do anti-thyroid drugs alone provide adequate treatment?. Heart Lung Circ 2014; 23: pp. 549-554.
- Cooper D.S.: Antithyroid drugs. N Engl J Med 2005; 352: pp. 905-917.
- Osman F., Franklyn J.A., Sheppard M.C., Gammage M.D.: Successful treatment of amiodarone-induced thyrotoxicosis. Circulation 2002; 105: pp. 1275-1277.
- Uzan L., Guignat L., Meune C., et. al.: Continuation of amiodarone therapy despite type II amiodarone-induced thyrotoxicosis. Drug Saf 2006; 29: pp. 231-236.
- Bogazzi F., Tomisti L., Rossi G., et. al.: Glucocorticoids are preferable to thionamides as first-line treatment for amiodarone-induced thyrotoxicosis due to destructive thyroiditis: a matched retrospective cohort study. J Clin Endocrinol Metab 2009; 94: pp. 3757-3762.
- Eskes S.A., Endert E., Fliers E., et. al.: Treatment of amiodarone-induced thyrotoxicosis type 2: a randomized clinical trial. J Clin Endocrinol Metab 2012; 97: pp. 499-506.
- Burrow G.N., Burke W.R., Himmelhoch J.M., Spencer R.P., Hershman J.M.: Effect of lithium on thyroid function. J Clin Endocrinol Metab 1971; 32: pp. 647-652.
- Dickstein G., Shechner C., Adawi F., Kaplan J., Baron E., Ish-Shalom S.: Lithium treatment in amiodarone-induced thyrotoxicosis. Am J Med 1997; 102: pp. 454-458.
- Chopra I.J., Baber K.: Use of oral cholecystographic agents in the treatment of amiodarone-induced hyperthyroidism. J Clin Endocrinol Metab 2001; 86: pp. 4707-4710.
- Bogazzi F., Bartalena L., Cosci C., et. al.: Treatment of type II amiodarone-induced thyrotoxicosis by either iopanoic acid or glucocorticoids: a prospective, randomized study. J Clin Endocrinol Metab 2003; 88: pp. 1999-2002.
- Bogazzi F., Aghini-Lombardi F., Cosci C., et. al.: Iopanoic acid rapidly controls type I amiodarone-induced thyrotoxicosis prior to thyroidectomy. J Endocrinol Invest 2002; 25: pp. 176-180.
- Mercado M., Mendoza-Zubieta V., Bautista-Osorio R., Espinoza-de los Monteros A.L.: Treatment of hyperthyroidism with a combination of methimazole and cholestyramine. J Clin Endocrinol Metab 1996; 81: pp. 3191-3193.
- Jha S., Waghdhare S., Reddi R., Bhattacharya P.: Thyroid storm due to inappropriate administration of a compounded thyroid hormone preparation successfully treated with plasmapheresis. Thyroid 2012; 22: pp. 1283-1286.
- Zhu L., Zainudin S.B., Kaushik M., Khor L.Y., Chng C.L.: Plasma exchange in the treatment of thyroid storm secondary to type II amiodarone-induced thyrotoxicosis. Endocrinol Diabetes Metab Case Rep 2016; 2016:
- Tonnelier A., de Filette J., De Becker A., Deweer S., Velkeniers B.: Successful pretreatment using plasma exchange before thyroidectomy in a patient with amiodarone-induced thyrotoxicosis. Eur Thyroid J 2017; 6: pp. 108-112.
- Szczeklik W., Wawrzycka K., Wludarczyk A., et. al.: Complications in patients treated with plasmapheresis in the intensive care unit. Anaesthesiol Intensive Ther 2013; 45: pp. 7-13.
- Randle R.W., Bates M.F., Long K.L., Pitt S.C., Schneider D.F., Sippel R.S.: Impact of potassium iodide on thyroidectomy for Basedow’ disease: implications for safety and operative difficulty. Surgery 2018; 163: pp. 68-72.
- Sato K., Shiga T., Matsuda N., et. al.: Mild and short recurrence of type II amiodarone-induced thyrotoxicosis in three patients receiving amiodarone continuously for more than 10 years. Endocr J 2006; 53: pp. 531-538.
- Bogazzi F., Bartalena L., Tomisti L., Rossi G., Brogioni S., Martino E.: Continuation of amiodarone delays restoration of euthyroidism in patients with type 2 amiodarone-induced thyrotoxicosis treated with prednisone: a pilot study. J Clin Endocrinol Metab 2011; 96: pp. 3374-3380.
- Maqdasy S., Batisse-Lignier M., Auclair C., et. al.: Amiodarone-induced thyrotoxicosis recurrence after amiodarone reintroduction. Am J Cardiol 2016; 117: pp. 1112-1116.
- Houghton S.G., Farley D.R., Brennan M.D., van Heerden J.A., Thompson G.B., Grant C.S.: Surgical management of amiodarone-associated thyrotoxicosis: Mayo Clinic experience. World J Surg 2004; 28: pp. 1083-1087.
- Tomisti L., Materazzi G., Bartalena L., et. al.: Total thyroidectomy in patients with amiodarone-induced thyrotoxicosis and severe left ventricular systolic dysfunction. J Clin Endocrinol Metab 2012; 97: pp. 3515-3521.
- Cappellani D., Papini P., Pingitore A., et. al.: Comparison between total thyroidectomy and medical therapy for amiodarone-induced thyrotoxicosis. J Clin Endocrinol Metab 2020; 105:
- Adam M.A., Thomas S., Youngwirth L., et. al.: Is there a minimum number of thyroidectomies a surgeon should perform to optimize patient outcomes?. Ann Surg 2017; 265: pp. 402-407.
