[Sách dịch] Sổ tay Bệnh Gan – Handbook of Liver Disease – (C) NXB Elsevier, 2022
Dịch và chú giải: Ths.Bs. Lê Đình Sáng
CHƯƠNG 33: GHÉP GAN
Liver Transplantation
Andres F. Carrion MD and Kalyan Ram Bhamidimarri MD, MPH
Handbook of Liver Disease, Chapter 33, 452-469
NHỮNG ĐIỂM CHÍNH
|
Tổng quan
- Ghép gan (LT) vẫn là phương pháp điều trị triệt để duy nhất cho bệnh gan giai đoạn cuối (ESLD) và suy gan cấp (acute liver failure – ALF), bất kể nguyên nhân.
- Tỷ lệ sống còn sau LT hiện tại là 80% đến 90% sau 1 năm và 60% đến 75% sau 5 năm, phản ánh những tiến bộ lớn trong kỹ thuật phẫu thuật, chăm sóc tích cực chu phẫu, ức chế miễn dịch và lựa chọn ứng viên.
- Dữ liệu từ Mạng lưới Chia sẻ Tạng thống nhất (United Network for Organ Sharing – UNOS) cho thấy có 14.753 bệnh nhân được đưa vào danh sách chờ LT vào năm 2015 tại Hoa Kỳ, nhưng chỉ có 7.127 bệnh nhân thực sự được ghép (48,3%).
- Ghép gan từ người hiến sống (Living donor liver transplantation – LDLT) đã nổi lên như một giải pháp thay thế để tăng số lượng tạng hiến.
- Nguy cơ bệnh tật và tử vong cho người hiến, cũng như sự khác biệt theo vùng và theo từng trung tâm, đã hạn chế khả năng áp dụng rộng rãi của phương pháp này.
- Chỉ có 5,3% các ca ghép gan được thực hiện vào năm 2015 tại Hoa Kỳ là ghép từ người hiến sống.
- Việc lựa chọn ứng viên LT phù hợp đòi hỏi một phương pháp tiếp cận đa chuyên khoa và vẫn là một bước quan trọng trong quá trình đánh giá trước LT, vì nó có ý nghĩa lớn đối với kết quả sau LT.
- Việc phân bổ tạng tại Hoa Kỳ và nhiều quốc gia khác được xác định bởi mức độ nghiêm trọng của bệnh, được phản ánh qua thang điểm MELD (Model for End-stage Liver Disease – Mô hình Bệnh gan Giai đoạn cuối) và PELD (Pediatric End-stage Liver Disease – Mô hình Bệnh gan Giai đoạn cuối ở Trẻ em), dự đoán xác suất tử vong trong khoảng thời gian 3 tháng.
- Thang điểm MELD và PELD được triển khai vào năm 2002 để giảm tỷ lệ tử vong trong danh sách chờ của các ứng viên ghép gan.
- Thang điểm MELD bao gồm tỷ lệ bình thường hóa quốc tế (international normalized ratio – INR) của thời gian prothrombin, bilirubin huyết thanh và creatinine huyết thanh. Thang điểm này được sử dụng cho các ứng viên ghép gan từ 12 tuổi trở lên.
- MELD-Na: Hạ natri máu là một yếu tố dự báo tử vong độc lập ở bệnh nhân xơ gan; do đó, một chính sách mới đã có hiệu lực từ tháng 1 năm 2016 để sử dụng thang điểm MELD-Na. Việc kết hợp thang điểm MELD-Na vào phân bổ tạng được dự kiến sẽ ngăn chặn được 50 đến 60 ca tử vong mỗi năm.
- Các ứng viên người lớn trong danh sách chờ được phân vào một trong các loại sau: (a) Tình trạng 1A, (b) thang điểm MELD tính toán hoặc “sinh học”, (c) thang điểm MELD ngoại lệ, hoặc (d) tình trạng không hoạt động.
- Các ứng viên ghép gan người lớn được liệt kê là tình trạng 1A phải trên 18 tuổi và có một trong các tình trạng sau: ALF với tuổi thọ dự kiến <7 ngày nếu không có LT, bệnh Wilson mất bù cấp, tình trạng không có gan, tạng ghép chính không hoạt động (primary graft nonfunction – PNF) của gan toàn phần hoặc gan chẻ, hoặc suy tạng ghép do huyết khối động mạch gan trong vòng 7 ngày sau LT.
- Thang điểm PELD bao gồm INR, bilirubin, albumin và suy dinh dưỡng nhưng không bao gồm creatinine huyết thanh. Thang điểm này được sử dụng cho các ứng viên ghép gan ≤11 tuổi.
- Đối với bệnh nhi, các ứng viên trong danh sách chờ được phân vào một trong các loại tương tự như người lớn (xem ở trên) nhưng cũng có thể được xếp vào một loại bổ sung, tình trạng 1B ở trẻ em, bao gồm các bệnh nhân bị u nguyên bào gan không di căn, bệnh nhiễm acid hữu cơ hoặc rối loạn chu trình urê.
Chỉ định
Các chỉ định hàng đầu cho LT thay đổi ở các quốc gia và khu vực khác nhau trên thế giới và phần lớn phản ánh tỷ lệ mắc và tỷ lệ hiện mắc của các rối loạn cụ thể; dữ liệu cho Hoa Kỳ được tóm tắt trong Hình 33.1.
Các chỉ định phổ biến nhất cho LT do ESLD ở các nước phương Tây là viêm gan C và xơ gan do rượu, trong khi xơ gan do viêm gan B chiếm ưu thế ở châu Á.
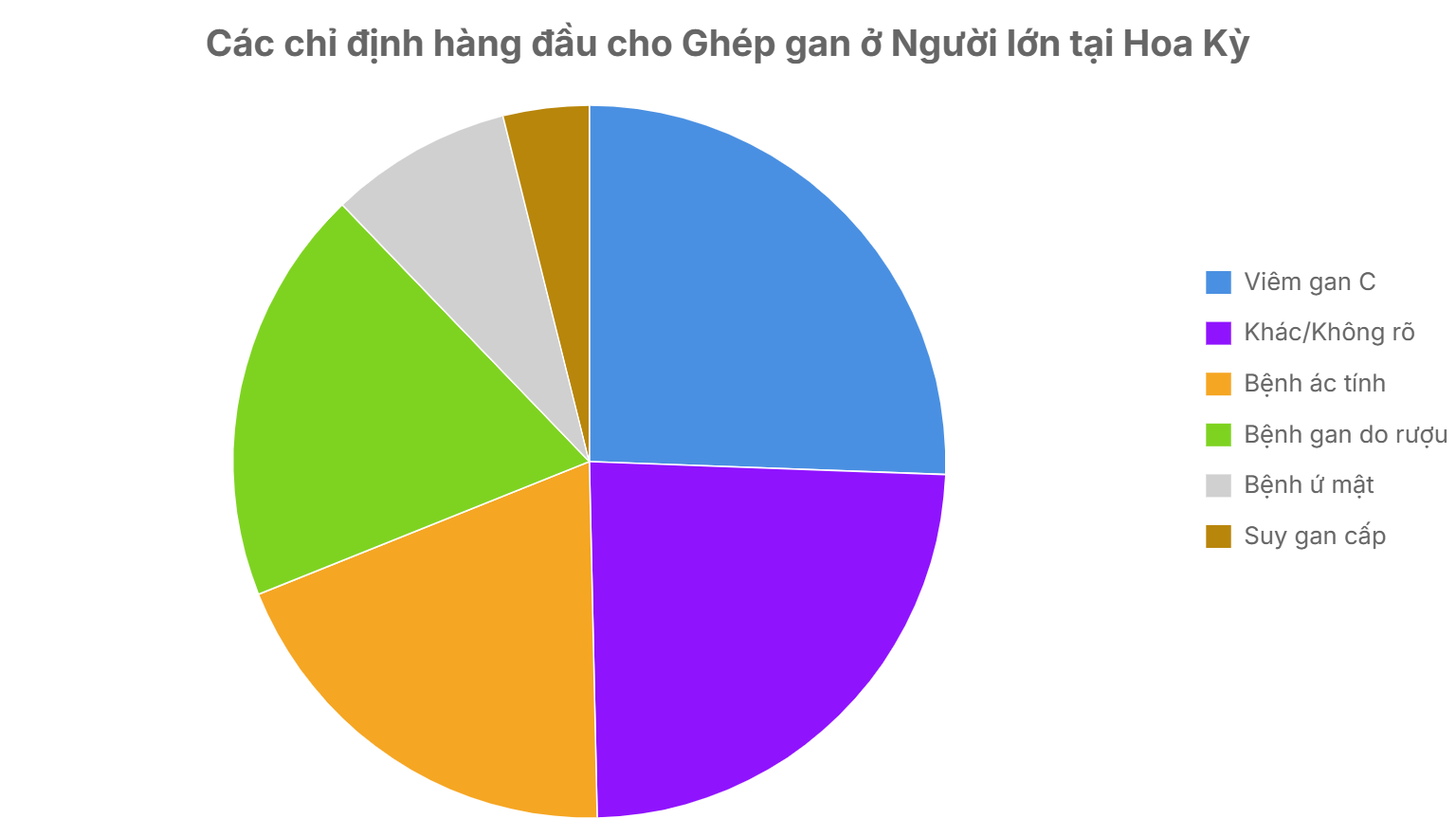
Hình 33.1 Các chỉ định hàng đầu cho ghép gan ở người lớn tại Hoa Kỳ. Các mục theo chiều kim đồng hồ từ trên cùng: Viêm gan C (25.6%), Bệnh ác tính (19.3%), Bệnh gan do rượu (18.9%), Khác/Không rõ (24.1%), Bệnh ứ mật (8.3%), Suy gan cấp (3.9%).
Suy gan cấp (ALF) cần LT chủ yếu do tổn thương gan do thuốc ở các nước phương Tây và do viêm gan siêu vi cấp ở các nước phương Đông.
XƠ GAN VÀ BỆNH GAN GIAI ĐOẠN CUỐI (ESLD) (xem thêm Chương 11 đến 15)
- LT là liệu pháp triệt để duy nhất liên quan đến việc cải thiện đáng kể sự sống còn lâu dài cho bệnh nhân xơ gan mất bù và ESLD, bất kể nguyên nhân.
- Bản thân xơ gan không phải là một chỉ định cho LT. Bệnh nhân nên được giới thiệu để đánh giá ghép gan một khi xuất hiện biến chứng của bệnh gan mạn tính (Bảng 33.1).
- Lợi ích sống còn đáng kể đạt được thông qua LT cho bệnh nhân có điểm MELD ≥15.
- Điều trị nguyên nhân cơ bản của bệnh gan có thể ổn định hoặc cải thiện chức năng gan, và các can thiệp như vậy nên được tích cực theo đuổi (ví dụ, sử dụng liệu pháp kháng vi-rút hiệu quả chống lại viêm gan B hoặc C, liệu pháp ức chế miễn dịch cho viêm gan tự miễn, cai rượu hoàn toàn hoặc các loại thuốc gây hại trong bệnh gan do rượu hoặc do thuốc).
Bảng 33.1: Các giai đoạn lâm sàng của xơ gan, biến chứng và tỷ lệ tử vong
| Giai đoạn | Biến chứng | Tỷ lệ tử vong trong 1 năm |
|---|---|---|
| 1 | Không có giãn tĩnh mạch thực quản cũng không có cổ trướng | 1% |
| 2 | Giãn tĩnh mạch thực quản | 3.4% |
| 3 | Cổ trướng | 20% |
| 4 | Xuất huyết do vỡ giãn tĩnh mạch thực quản | 54% |
| Nguồn: D’Amico G, Garcia-Tsao G, Pagliaro L. J Hepatol. 2006;44:217-231. |
SUY GAN CẤP (xem thêm Chương 2)
- Diễn biến lâm sàng của ALF thường nhanh chóng, và kết quả có thể khó lường, một số bệnh nhân tự hồi phục hoặc với liệu pháp nhắm mục tiêu và những người khác cần LT hoặc tử vong trong quá trình đánh giá.
- Nên sớm chuyển bệnh nhân ALF đến trung tâm LT.
- Bệnh nhân ALF có ưu tiên cao nhất trong việc phân bổ tạng và được liệt kê là tình trạng 1A theo chính sách hiện hành của UNOS (xem ở trên). Các tiêu chí để được chỉ định tình trạng 1A của UNOS được tóm tắt trong Bảng 33.2.
Bảng 33.2: Tiêu chí chỉ định tình trạng 1A của Mạng lưới Chia sẻ Tạng thống nhất (UNOS) trong suy gan cấp
| Tuổi >18 |
| Tuổi thọ dự kiến <7 ngày nếu không ghép gan |
| Khởi phát bệnh não gan trong vòng 8 tuần kể từ triệu chứng đầu tiên của bệnh gan |
| Không có bệnh gan từ trước |
| Nhập viện tại đơn vị chăm sóc tích cực, và một trong những điều sau: |
| Phụ thuộc máy thở |
| Yêu cầu liệu pháp thay thế thận |
| INR >2 |
| Bệnh Wilson thể tối cấp |
| Tạng ghép chính không hoạt động |
| Huyết khối động mạch gan |
| INR, Tỷ lệ bình thường hóa quốc tế. |
CÁC KHỐI U ÁC TÍNH NGUYÊN PHÁT TẠI GAN (xem thêm Chương 29)
- HCC là khối u ác tính nguyên phát tại gan phổ biến nhất ở người lớn.
- Phần lớn bệnh nhân HCC ở các nước phương Tây (95%) có bệnh xơ gan nền, do đó hạn chế khả năng áp dụng phẫu thuật cắt bỏ. Ngược lại, chỉ có 60% bệnh nhân HCC ở các nước phương Đông có bệnh xơ gan nền, phần lớn phản ánh tỷ lệ nhiễm vi-rút viêm gan B cao và khả năng gây ung thư của nó.
- Tiêu chuẩn Milan là tiêu chuẩn tham chiếu cho việc ứng cử LT đối với bệnh nhân HCC: Một khối u duy nhất <5 cm đường kính hoặc không quá ba khối u với khối u lớn nhất <3 cm đường kính, và không có xâm lấn tĩnh mạch cửa và di căn ngoài gan.
- Các tiêu chí để ưu tiên các ứng viên ghép gan bị HCC đã phát triển theo thời gian, và đã có một số thay đổi trong chính sách đưa vào danh sách chờ.
- Theo chính sách hiện hành, bệnh nhân HCC vẫn giữ điểm MELD “sinh học” của họ khi được đưa vào danh sách và tại lần kháng nghị đầu tiên sau 3 tháng nhưng sẽ được cộng điểm ngoại lệ sau lần kháng nghị thứ hai sau 6 tháng, khi họ được nâng lên điểm MELD là 28; sau đó, bệnh nhân tiếp tục được cộng thêm 10% cho đến khi đạt điểm 34, lúc đó điểm ngoại lệ sẽ được giới hạn.
- Để cân bằng các tiêu chí ung thư và không ung thư cho bệnh nhân trong danh sách chờ và để giảm các đặc điểm X-quang dương tính giả, một chính sách đã có hiệu lực vào tháng 10 năm 2015 yêu cầu các trung tâm LT tuân thủ các tiêu chí X-quang nghiêm ngặt để chẩn đoán HCC. Hệ thống Dữ liệu Báo cáo Hình ảnh Gan (Liver Imaging Reporting Data System – LI-RADS) cho HCC sử dụng thuật ngữ nhất quán và cho phép báo cáo được chuẩn hóa bằng cách phân loại các tổn thương theo xác suất là lành tính hay ác tính (Bảng 33.3 và 33.4).
- Các nốt được tìm thấy trên hình ảnh học nên được phân loại theo phân loại của Mạng lưới Mua sắm và Cấy ghép Tạng (Organ Procurement and Transplantation Network – OPTN)/UNOS. Chỉ các nốt loại 5 của OPTN (LI-RADS-5) mới được coi là HCC (Bảng 33.5). Các nốt loại 5 của OPTN được chia thành các loại phụ: 5A (tổn thương T1), 5A-g (tổn thương T1 với sự tăng trưởng kích thước 50% trong khoảng thời gian theo dõi), 5B (tổn thương T2), 5T (tổn thương loại 5 đã được điều trị), và 5X (tổn thương lớn hơn T2), trong đó chỉ có các nốt 5B đủ điều kiện nhận điểm ngoại lệ MELD tiêu chuẩn (xem phần sau).
- Các tổn thương OPTN 5A không đủ điều kiện nhận điểm ngoại lệ MELD tiêu chuẩn trừ khi có nhiều hơn một nốt 5A, hoặc xác định được một hoặc nhiều tổn thương 5B đồng thời.
- Khoảng một phần ba bệnh nhân HCC nằm ngoài tiêu chuẩn Milan (tổn thương OPTN 5X) tại thời điểm chẩn đoán và không đủ điều kiện nhận điểm ngoại lệ MELD, ngay cả khi được hạ giai đoạn. Một trung tâm ghép riêng lẻ có thể xem xét một bệnh nhân như vậy cho LT, nhưng việc đưa vào danh sách sẽ được thực hiện theo điểm MELD/PELD tính toán trừ khi hội đồng xét duyệt khu vực (regional review board – RRB) chấp thuận điểm ngoại lệ.
- Việc sử dụng các tiêu chí mở rộng cho HCC ngoài tiêu chuẩn Milan (ví dụ, tiêu chí của Đại học California, San Francisco, “quy tắc 7”) hiện không được khuyến nghị.
- Sự sống còn sau LT đối với bệnh nhân HCC trong tiêu chuẩn Milan tương đương với bệnh nhân được LT vì các chỉ định khác ngoài HCC.
- Các liệu pháp tại chỗ-tại vùng (ví dụ, đốt sóng cao tần, hóa tắc mạch qua động mạch) được khuyến nghị để ngăn chặn sự tiến triển của các khối u và giảm thiểu việc “rớt khỏi” danh sách chờ.
Bảng 33.3: Các loại và định nghĩa của Hệ thống Dữ liệu Báo cáo Hình ảnh Gan (LI-RADS)
| Loại | Định nghĩa |
|---|---|
| LR-1 | Chắc chắn lành tính |
| LR-2 | Có khả năng lành tính |
| LR-3 | Xác suất trung bình cho HCC |
| LR-4 | Có khả năng là HCC |
| LR-5 (loại 5 OPTN) | Chắc chắn là HCC |
| LR-5V | Chắc chắn là HCC có khối u trong tĩnh mạch |
| LR-M | Có khả năng là ác tính, không đặc hiệu cho HCC |
| HCC, Ung thư biểu mô tế bào gan; OPTN, Mạng lưới Mua sắm và Cấy ghép Tạng. |
Bảng 33.4: Tiêu chí của Hệ thống Dữ liệu Báo cáo Hình ảnh Gan (LI-RADS) cho Ung thư biểu mô tế bào gan
| Thì động mạch giảm hoặc đồng tăng quang | Thì động mạch tăng quang mạnh | |
|---|---|---|
| Đường kính (mm) | <20 | ≥20 |
| Số lượng đặc điểm: | ||
| 0 | LR-3 | LR-3 |
| 1 | LR-3 | LR-4 |
| ≥2 | LR-4 | LR-4 |
| Xem Bảng 33.3 để biết định nghĩa các loại LR. Các đặc điểm bao gồm “thải thuốc” (washout) của khối u trên hình ảnh, sự hiện diện của vỏ bọc, và sự tăng trưởng của khối u theo thời gian. Các tổn thương trong ô này được phân loại là LR-4 trừ khi có sự tăng trưởng kích thước ≥50% trong ≤6 tháng hoặc nếu quan sát thấy hiện tượng thải thuốc và các nốt rõ ràng trên siêu âm trước đó. |
Bảng 33.5: Phân loại các nốt loại 5 của Mạng lưới Mua sắm và Cấy ghép Tạng (OPTN)
| Loại | Đặc điểm | Ưu tiên tự động |
|---|---|---|
| 5A (T1) | Nốt đơn 1-2 cm | Không |
| 5B (T2) | Nốt đơn 2-5 cm | Có |
| 5-g (tăng trưởng) | Nốt đơn 1-2 cm với tăng trưởng 50% theo thời gian trên hình ảnh cắt lớp trong vòng 6 tháng (không áp dụng cho tổn thương đã điều trị) | Có, chỉ sau khi tổn thương phát triển đến T2 |
| 5T (đã điều trị) | Nốt loại 5 sau liệu pháp tại chỗ-tại vùng (HCC tồn tại hoặc tái phát) | Có (theo kháng nghị ban đầu) |
| 5X (>T2) | Tổn thương ngoài tiêu chuẩn Milan/tổn thương >T2 | Không (ứng viên vẫn có thể được đưa vào danh sách với điểm MELD tính toán; cần có sự chấp thuận của RRB để được ưu tiên) |
| HCC, Ung thư biểu mô tế bào gan; MELD, Mô hình Bệnh gan Giai đoạn cuối; RRB, Hội đồng xét duyệt khu vực. |
- Ung thư đường mật trong gan (Intrahepatic cholangiocarcinoma – CC) là khối u ác tính nguyên phát tại gan phổ biến thứ hai ở người lớn. LT không phải là liệu pháp tiêu chuẩn cho khối u này vì LT đối với CC có kết quả kém.
- Tại một số trung tâm ghép, việc sử dụng các phác đồ nghiêm ngặt kết hợp hóa xạ trị tân bổ trợ cho những bệnh nhân được chọn lọc bị CC rốn gan giai đoạn I hoặc II đã mang lại kết quả sau LT được cải thiện (Hình 33.2).
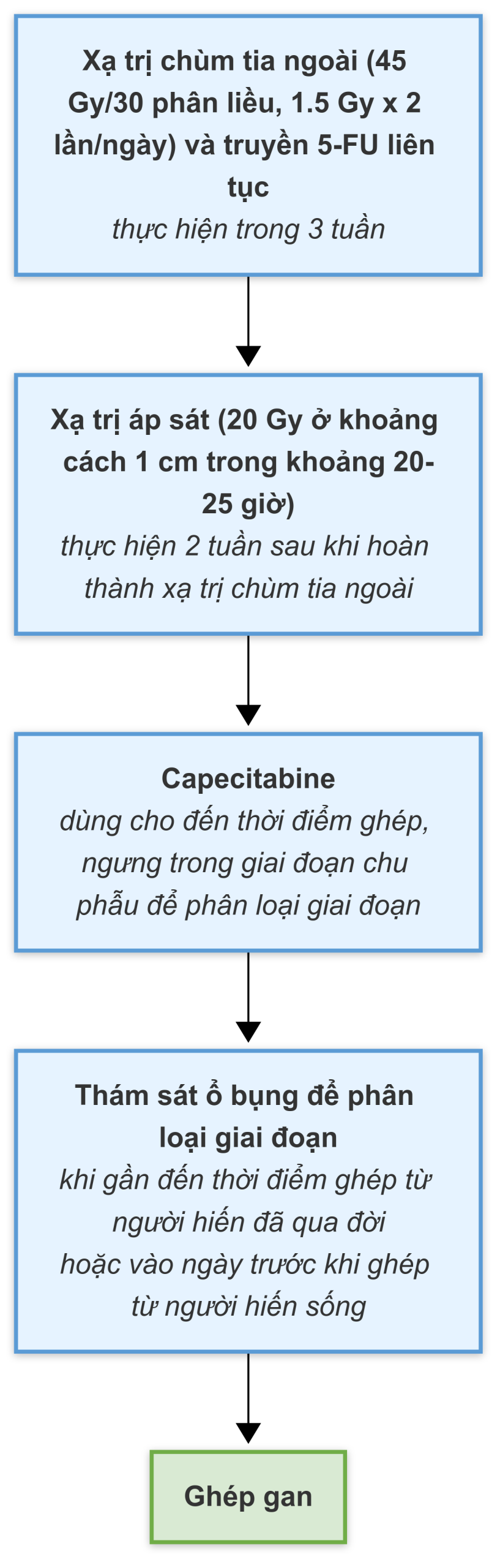
Hình 33.2 Phác đồ hóa xạ trị tân bổ trợ của Mayo Clinic cho ứng viên ghép gan bị ung thư đường mật rốn gan. 5-FU, 5-fluorouracil.
- U nguyên bào gan (Hepatoblastoma) là khối u ác tính nguyên phát tại gan phổ biến nhất ở trẻ em và thường được điều trị bằng hóa trị tân bổ trợ và phẫu thuật cắt bỏ; nó thường xảy ra khi không có xơ hóa gan đáng kể.
- HCC thể sợi dẹt (Fibrolamellar HCC) là một biến thể khối u không phổ biến xảy ra ở người trẻ tuổi không có bệnh xơ gan nền; phẫu thuật cắt bỏ rộng rãi thường có thể được thực hiện với mục đích chữa khỏi.
- Mặc dù LT hiện không phải là một lựa chọn điều trị tiêu chuẩn cho các di căn gan không thể cắt bỏ từ các khối u thần kinh nội tiết, dữ liệu từ cơ sở dữ liệu UNOS cho thấy có 137 ca ghép gan được thực hiện cho chỉ định này từ năm 1988 đến 2009, với tỷ lệ sống còn sau 1 và 5 năm lần lượt là 81% và 49%. Kết quả tương tự đã được báo cáo từ châu Âu: 213 bệnh nhân đã được LT từ năm 1982 đến 2009, với tỷ lệ sống còn sau 1 và 5 năm lần lượt là 81% và 52%.
RỐI LOẠN CHUYỂN HÓA
- Các rối loạn chuyển hóa chủ yếu ảnh hưởng đến gan phổ biến hơn ở bệnh nhi so với bệnh nhân người lớn.
- LT có thể là một can thiệp điều trị hiệu quả cho bệnh nhân mắc các rối loạn chuyển hóa tại gan, giúp chữa khỏi bệnh nền.
- Thiếu hụt Alpha-1 antitrypsin (xem thêm Chương 20)
- Bệnh thừa sắt di truyền (xem thêm Chương 18)
- Bệnh Wilson (xem thêm Chương 19)
- Bệnh đa dây thần kinh amyloid gia đình (xem thêm Chương 24)
- Tăng oxalat niệu nguyên phát (xem thêm Chương 20)
- Xơ nang (xem thêm Chương 20)
- Bệnh dự trữ glycogen loại I và IV (xem thêm Chương 25)
- Bệnh tyrosinemia (xem thêm Chương 25)
- Porphyria cấp tính gián đoạn (xem thêm Chương 20)
Chống chỉ định
- Các chống chỉ định tuyệt đối và tương đối đối với LT tiếp tục phát triển theo thời gian.
- Chống chỉ định tuyệt đối ngụ ý rằng kết quả sau LT thành công là không thể xảy ra và do đó không nên xem xét LT (Bảng 33.6).
- Bệnh nhân có chống chỉ định tương đối có nguy cơ cao gặp phải kết quả không tối ưu; tuy nhiên, LT vẫn có thể được xem xét ở những bệnh nhân được chọn lọc.
- Những bệnh nhân ban đầu được coi là ứng viên phù hợp cho LT có thể phát triển các chống chỉ định tuyệt đối hoặc tương đối sau khi được đưa vào danh sách chờ; do đó, cần phải đánh giá liên tục sau khi đưa vào danh sách.
Bảng 33.6: Các chống chỉ định tuyệt đối đối với ghép gan
| Nhiễm trùng huyết không kiểm soát |
| Hội chứng suy giảm miễn dịch mắc phải (AIDS) |
| Lạm dụng rượu hoặc chất gây nghiện đang hoạt động |
| Bệnh tim hoặc phổi tiến triển nặng |
| Ung thư đường mật trong gan |
| U mạch máu ác tính (Hemangiosarcoma) |
| Ung thư biểu mô tế bào gan có di căn |
| Bệnh ác tính ngoài gan |
| Các bất thường về giải phẫu cản trở việc ghép gan |
| Thiếu sự hỗ trợ xã hội |
| Không tuân thủ điều trị y tế một cách dai dẳng |
Các bệnh đi kèm ảnh hưởng đến việc lựa chọn
BỆNH TIM MẠCH
- Tỷ lệ mắc các bệnh tim mạch ở bệnh nhân ESLD ít nhất bằng hoặc lớn hơn so với dân số chung.
- Đánh giá tim mạch không xâm lấn bằng siêu âm tim gắng sức dobutamine được khuyến nghị cho các ứng viên ghép gan không có bệnh tim mạch rõ ràng khi có từ ba yếu tố nguy cơ trở lên: Tuổi >60, tăng huyết áp hệ thống, đái tháo đường, rối loạn lipid máu, tiền sử cá nhân mắc bệnh tim mạch, phì đại thất trái hoặc tiền sử hút thuốc.
- Chụp mạch vành có thể được yêu cầu ở các ứng viên ghép gan mà các xét nghiệm không xâm lấn không loại trừ chắc chắn bệnh tim mạch.
BỆNH PHỔI
- Ngoài các rối loạn phổi phổ biến trong dân số chung, chẳng hạn như bệnh phổi tắc nghẽn mạn tính, hen suyễn và ngưng thở khi ngủ do tắc nghẽn, các tình trạng phổi cụ thể có thể phát triển ở bệnh nhân ESLD: tràn dịch màng phổi do gan (hepatic hydrothorax), tăng áp động mạch phổi cửa (portopulmonary hypertension – POPH) và hội chứng gan phổi (hepatopulmonary syndrome – HPS).
- Nên tránh đặt ống thông lưu trong điều trị tràn dịch màng phổi do gan ở các ứng viên ghép gan, vì có thể xảy ra nhiễm trùng và gây nguy hiểm cho tư cách ứng viên ghép.
- POPH phải được xác nhận bằng thông tim phải. POPH trung bình (áp lực động mạch phổi trung bình [mPAP] ≥35 mm Hg) làm tăng tỷ lệ tử vong vượt quá ước tính dự đoán bởi điểm MELD và, nếu không đáp ứng với điều trị nội khoa, là một chống chỉ định cho LT vì nó liên quan đến kết quả kém.
- Bệnh nhân POPH đủ điều kiện LT nên có mPAP <35 mm Hg và kháng lực mạch máu phổi (PVR) <400 dynes/giây/cm⁻⁵ sau điều trị.
- Những bệnh nhân như vậy được cộng 22 điểm ngoại lệ MELD, với mức tăng 10% mỗi 3 tháng nếu mPAP vẫn <35 mm Hg.
- Tất cả các ứng viên ghép gan nên được sàng lọc HPS bằng phương pháp đo oxy xung. Trong HPS, độ bão hòa oxy động mạch (SpO₂) <96% ở mực nước biển theo phân tích khí máu động mạch; nếu PaO₂ <60 mm Hg hoặc chênh lệch oxy phế nang-động mạch (A-a) ≥15 mm Hg ở không khí phòng, nên thực hiện chẩn đoán hình ảnh (bắt đầu bằng siêu âm tim cản quang, tiếp theo là xạ hình với albumin đại phân tử được đánh dấu technetium nếu cần) để phát hiện shunt mạch máu trong phổi.
- Bệnh nhân HPS đủ điều kiện nhận điểm ngoại lệ MELD và được cộng 22 điểm với mức tăng 10% mỗi 3 tháng nếu PaO₂ của họ vẫn <60 mm Hg.
NHIỄM TRÙNG
- Nhiễm trùng toàn thân không kiểm soát là một chống chỉ định cho LT.
- Tiêm chủng nên được cập nhật trước khi LT, lý tưởng nhất là trước khi bệnh nhân phát triển ESLD. Việc sử dụng vắc-xin sống giảm độc lực (tức là sởi, quai bị, rubella, thủy đậu, zona, bại liệt uống, rotavirus, cúm dạng xịt mũi, sốt vàng da) bị chống chỉ định 4 tuần trước LT hoặc bất kỳ lúc nào sau LT ở bệnh nhân đang dùng thuốc ức chế miễn dịch điều trị.
- Nhiễm vi-rút suy giảm miễn dịch ở người (HIV)
- LT chỉ được thực hiện ở bệnh nhân nhiễm HIV tại các trung tâm ghép được chọn lọc.
- Tải lượng vi-rút HIV phải không thể phát hiện được.
- Số lượng tế bào T CD4+ phải >100/µL ở các ứng viên ghép gan chưa từng bị nhiễm trùng cơ hội và >200/µL ở những người có tiền sử nhiễm trùng cơ hội.
- Nhiễm vi-rút viêm gan B (HBV) (xem thêm Chương 4)
- Ức chế vi-rút bằng liệu pháp kháng vi-rút ở các ứng viên ghép gan có thể cải thiện chức năng gan và loại bỏ nhu cầu LT ở một số bệnh nhân.
- Các chiến lược để giảm nguy cơ tái phát nhiễm HBV sau LT bao gồm việc sử dụng các chất tương tự nucleos(t)ide mạnh trước và sau LT cũng như sử dụng globulin miễn dịch viêm gan B (HBIG) tại thời điểm LT và tiếp tục trong giai đoạn đầu sau LT.
- Nhiễm vi-rút viêm gan C (HCV) (xem thêm Chương 5)
- Điều trị nhiễm HCV đã được cách mạng hóa với việc cấp phép các thuốc kháng vi-rút tác động trực tiếp (direct-acting antivirals – DAAs) và tiếp tục phát triển khi các tác nhân mới hơn được phê duyệt.
- Không giống như các phác đồ dựa trên interferon, một số phác đồ kháng vi-rút với sự kết hợp của các DAAs là an toàn và hiệu quả ở bệnh nhân xơ gan mất bù.
- Liệu pháp kháng vi-rút hiệu quả chống lại HCV dẫn đến đáp ứng vi-rút bền vững (sustained virologic response – SVR) có thể ổn định hoặc cải thiện chức năng gan ngay cả ở bệnh nhân ESLD; tuy nhiên, bệnh nhân có thể không cải thiện đáng kể về chất lượng cuộc sống hoặc tình trạng chức năng.
- Một số bệnh nhân bị mất bù gan nặng có thể không được hưởng lợi từ việc điều trị HCV trước LT vì họ có thể không dung nạp được một số DAAs, cần thời gian điều trị kéo dài, đạt tỷ lệ SVR thấp, hoặc mất cơ hội rút ngắn thời gian chờ đợi bằng cách chấp nhận tạng từ người hiến dương tính với HCV.
- Trong trường hợp không có SVR trước LT, tái phát nhiễm HCV là phổ biến sau LT và liên quan đến kết quả kém nếu không được điều trị. Liệu pháp kháng vi-rút với DAAs được chỉ định kịp thời cho tất cả những người nhận ghép gan bị nhiễm HCV tái phát.
- Một số phác đồ chứa DAAs được dung nạp tốt và có hiệu quả cao trong điều trị nhiễm HCV ở người nhận ghép gan.
- Do đó, các đội ngũ ghép nên tích cực tham gia vào việc ra quyết định về thời điểm thích hợp nhất để điều trị HCV (trước hoặc sau LT) ở bệnh nhân trong danh sách chờ.
RỐI LOẠN CHỨC NĂNG THẬN
- Tầm quan trọng của rối loạn chức năng thận như một yếu tố dự báo sự sống còn kém không cần ghép ở bệnh nhân ESLD được phản ánh qua việc bao gồm creatinine huyết thanh trong thang điểm MELD.
- Tổn thương thận cấp phổ biến ở bệnh nhân nhập viện với ESLD (20%).
- Hội chứng gan-thận (Hepatorenal syndrome – HRS) (xem thêm Chương 14)
- HRS loại 1 được đặc trưng bởi tổn thương thận cấp tính và tiến triển nhanh chóng, liên quan đến tỷ lệ sống còn cực kỳ kém nếu không có LT.
- HRS loại 2 kéo dài hơn và liên quan đến rối loạn chức năng thận ít nghiêm trọng hơn và thường đi kèm với cổ trướng kháng thuốc lợi tiểu.
- Rối loạn chức năng thận từ trung bình đến nặng trước LT (độ lọc cầu thận [GFR] <40 mL/phút/1.73 m²) có liên quan đến tần suất tăng của tạng ghép gan chính không hoạt động sau LT.
- Nên xem xét ghép gan-thận đồng thời trong các trường hợp sau:
- Xơ gan và bệnh thận mạn với GFR <30 mL/phút/1.73 m²
- Bệnh nhân HRS có creatinine huyết thanh >2 mg/dL và trở nên phụ thuộc vào lọc máu trong hơn 8 tuần
- Suy gan và bệnh thận mạn với bằng chứng xơ cứng cầu thận hoặc xơ hóa cầu thận ở >30% cầu thận trên mẫu sinh thiết thận
- Bệnh thận giai đoạn cuối (GFR <15 mL/phút/1.73 m²) và xơ gan có tăng áp lực tĩnh mạch cửa có triệu chứng và chênh áp tĩnh mạch gan bít ≥10 mm Hg (xem Chương 11)
LẠM DỤNG CHẤT GÂY NGHIỆN VÀ RỐI LOẠN HÀNH VI
- Đánh giá chi tiết về các rối loạn lạm dụng chất gây nghiện là bắt buộc đối với tất cả các bệnh nhân đang được đánh giá cho LT.
- Lạm dụng rượu
- Hầu hết các trung tâm ghép yêu cầu ít nhất 6 tháng kiêng rượu hoàn toàn.
- Các yếu tố dự báo tái nghiện rượu sau LT bao gồm thời gian kiêng rượu trước LT ngắn hơn, tiền sử gia đình có rối loạn lạm dụng rượu, các đợt cai rượu trong quá khứ được ghi nhận, thất bại trong việc cai rượu trong quá khứ, hỗ trợ xã hội kém và tiền sử lạm dụng nhiều loại chất gây nghiện.
- Có tới 25% bệnh nhân xơ gan do rượu trong danh sách chờ LT và được cho là đã kiêng rượu vẫn tiếp tục uống rượu.
- Một lợi ích sống còn quan trọng của LT đã được chứng minh cho bệnh nhân bị viêm gan do rượu cấp tính nặng không đáp ứng với điều trị nội khoa; những bệnh nhân này có thể được LT theo chính sách riêng của trung tâm hoặc, tốt nhất là, bằng cách tham gia các thử nghiệm lâm sàng.
- Việc sử dụng ma túy bất hợp pháp trong quá khứ phải được đánh giá cẩn thận và bị cấm ở tất cả các ứng viên đang được đánh giá LT.
- Việc sử dụng cần sa đã được xem xét kỹ lưỡng từ giữa những năm 2000, nhưng không có hướng dẫn cụ thể nào về việc sử dụng nó và tư cách ứng viên ghép gan.
- Dữ liệu ủng hộ tình trạng xơ hóa nặng hơn ở những người sử dụng cần sa bị nhiễm HCV, và có những báo cáo mới nổi về bệnh nấm aspergillosis phổi sau LT.
- Các chính sách hiện tại tùy thuộc vào từng trung tâm và bao gồm việc đánh giá nghiêm ngặt bởi các bác sĩ tâm thần và các chuyên gia tư vấn về lạm dụng chất gây nghiện.
- Việc hút thuốc lá nên bị cấm ở tất cả các ứng viên ghép gan vì nó làm tăng tỷ lệ biến chứng mạch máu và các bệnh ác tính sau LT; tuy nhiên, hút thuốc không phải là một chống chỉ định tuyệt đối đối với LT.
- Các chuyên gia sức khỏe tâm thần nên quản lý các rối loạn tâm thần trước và sau LT.
CÁC BỆNH ÁC TÍNH NGOÀI GAN
- Tầm soát theo lứa tuổi phải được cập nhật cho tất cả các ứng viên ghép gan.
- Các ứng viên ghép gan bị viêm xơ đường mật nguyên phát (primary sclerosing cholangitis – PSC) nên được nội soi đại tràng tầm soát, bất kể tuổi tác.
- Ở các ứng viên ghép gan có tiền sử bệnh ác tính ngoài gan, bệnh ác tính phải đã được chữa khỏi mà không tái phát trong ít nhất 2 đến 5 năm.
Đánh giá và đưa vào danh sách chờ
- Khuyến nghị xác nhận tính chất không thể đảo ngược của bệnh gan cấp hoặc mạn tính tiềm ẩn.
- Cần có sự chấp thuận cho LT từ công ty bảo hiểm của bệnh nhân trước khi bắt đầu một quá trình đánh giá trước LT tốn kém và sâu rộng.
- Một cuộc đánh giá kỹ lưỡng và đa chuyên khoa được thực hiện qua nhiều lần gặp gỡ với các thành viên của đội ngũ LT để xác định các vấn đề y tế, phẫu thuật, hành vi, xã hội và kinh tế bổ sung có thể ảnh hưởng đến tư cách ứng viên và kết quả LT.
- Các nghiên cứu hình ảnh bụng nên được thực hiện để tầm soát HCC hoặc các khối u khác trong và ngoài gan và để đánh giá giải phẫu của đường mật cũng như các cấu trúc mạch máu trong gan và trong ổ bụng.
- Tư cách ứng viên LT nên được thảo luận chính thức và chi tiết tại một cuộc họp lựa chọn LT tại mỗi trung tâm ghép riêng lẻ.
- Việc đưa vào danh sách chờ chính thức cho LT được thực hiện bởi UNOS.
- Nhóm máu (ABO) là yếu tố quyết định chính về khả năng tương thích của tạng.
- Điểm MELD quyết định mức độ ưu tiên cho việc phân bổ tạng.
- Việc sử dụng thang điểm MELD-Na cho các ứng viên ghép gan hiện đang có hiệu lực theo chính sách của UNOS (xem ở trên).
- Điểm ngoại lệ MELD có thể được cấp tự động nếu bệnh nhân có một tình trạng cụ thể mà UNOS trao thêm điểm hoặc theo từng trường hợp cụ thể khi có yêu cầu gửi đến RRB (xem thảo luận sau trong chương).
NGOẠI LỆ MELD
- Một số nguyên nhân gây bệnh gan mạn tính có thể dẫn đến giảm tuổi thọ không được dự đoán chính xác bởi thang điểm MELD và có thể liên quan đến chất lượng cuộc sống cực kỳ kém; do đó, các ngoại lệ MELD tồn tại.
- Có một số tình trạng mà các tiêu chí ngoại lệ MELD tiêu chuẩn tồn tại và không cần đánh giá đầy đủ của RRB (Bảng 33.7).
- Đối với những bệnh nhân có tình trạng y tế phức tạp liên quan đến bệnh gan của họ (không đủ điều kiện cho ngoại lệ MELD tiêu chuẩn) và liên quan đến tăng tỷ lệ mắc bệnh và tử vong không được phản ánh đầy đủ bởi điểm MELD tính toán hoặc sinh học, trung tâm ghép có thể kiến nghị RRB cộng thêm điểm. Ví dụ về các tình trạng có thể được RRB cấp thêm điểm MELD bao gồm, nhưng không giới hạn ở những điều sau đây:
- Viêm đường mật do vi khuẩn tái phát ở bệnh nhân PSC
- Ngứa khó chữa và làm suy nhược ở bệnh nhân viêm đường mật nguyên phát (primary biliary cholangitis – PBC)
- Cổ trướng kháng trị với liều thuốc lợi tiểu tối đa dung nạp được
- Bệnh não gan kháng trị với điều trị nội khoa
- Xuất huyết do vỡ giãn tĩnh mạch thực quản tái phát mặc dù đã được điều trị đầy đủ
Bảng 33.7: Các tình trạng y tế đủ điều kiện nhận điểm ngoại lệ MELD tiêu chuẩn
| Tình trạng | Ghi chú |
|---|---|
| Ung thư biểu mô tế bào gan | Tổn thương T2 trong tiêu chuẩn Milan |
| Hội chứng gan-phổi | mm Hg ở không khí phòng |
| Tăng áp động mạch phổi cửa | Áp lực động mạch phổi trung bình <35 mm Hg sau điều trị |
| Bệnh đa dây thần kinh amyloid gia đình | Được xác nhận bằng phân tích DNA và mô học |
| Tăng oxalat niệu nguyên phát | Cần ghép gan-thận đồng thời |
| Xơ nang | Thể tích thở ra gắng sức trong 1 giây (FEV1) <40% |
| Ung thư đường mật rốn gan | Giai đoạn I hoặc II; trung tâm ghép gan phải có phác đồ được UNOS phê duyệt (xem Hình 33.2) |
| Huyết khối động mạch gan | Trong vòng 14 ngày sau ghép gan, không đáp ứng tiêu chí tình trạng 1A |
| MELD, Mô hình Bệnh gan Giai đoạn cuối; UNOS, Mạng lưới Chia sẻ Tạng thống nhất. |
Các khía cạnh phẫu thuật
- Tổ chức mua sắm tạng địa phương chịu trách nhiệm thu hoạch tạng một khi người hiến được xác định.
- Thời gian thiếu máu nóng: Khoảng thời gian từ khi trụy tim mạch đến khi lấy tạng ra khỏi người hiến.
- Thời gian thiếu máu lạnh: Khoảng thời gian từ khi lấy tạng ra khỏi người hiến đến khi tái lập nguồn cung cấp máu cho tạng ở người nhận.
- Đánh giá đại thể của gan người hiến được thực hiện tại thời điểm thu hoạch, và một đánh giá mô học nhanh (sinh thiết lạnh) có thể được thực hiện để đánh giá thêm về tạng.
- Việc kết hợp người hiến-người nhận chủ yếu dựa trên sự tương thích ABO và cân nặng của người nhận; sự tương thích dựa trên kháng nguyên bạch cầu người (human leukocyte antigen – HLA) không cần thiết cho LT.
- Tái tạo mạch máu
- Tái tạo dòng chảy tĩnh mạch ra có thể được thực hiện bằng cách nối tĩnh mạch chủ của người hiến và tĩnh mạch chủ của người nhận ở phía trên và dưới tạng ghép hoặc bằng kỹ thuật “cõng” (piggyback) bao gồm một miệng nối trên gan của tĩnh mạch chủ.
- Tĩnh mạch cửa của người hiến và người nhận thường được nối tận-tận.
- Động mạch gan của người hiến và người nhận được nối tận-tận mà không gây căng hoặc để lại một mạch máu dài có thể bị gập. Đây là miệng nối mạch máu quan trọng nhất, và các vấn đề kỹ thuật dẫn đến tăng tỷ lệ mắc bệnh và kết quả kém sau LT.
- Các loại miệng nối đường mật
- Ống mật chủ – ống mật chủ (Choledococholedocostomy): Loại miệng nối được ưu tiên vì nó giống với giải phẫu đường mật bình thường và cho phép tiếp cận nội soi dễ dàng đến các ống mật sau LT.
- Ống gan – hỗng tràng hoặc ống mật chủ – hỗng tràng (Roux-en-Y): Theo truyền thống được thực hiện ở những người nhận có bệnh ống mật nội tại như PSC hoặc khi có sự chênh lệch đáng kể về đường kính của ống mật người hiến và người nhận; tuy nhiên, có bằng chứng cho thấy miệng nối ống-với-ống là an toàn ở những bệnh nhân được chọn lọc bị PSC không có sự tham gia của ống mật ngoài gan và cho phép tiếp tục theo dõi sau LT.
CÁC PHƯƠNG PHÁP MỞ RỘNG NGUỒN CUNG TẠNG HIẾN
- Ghép gan từ người hiến sống (LDLT) Sự thành công của LDLT ở bệnh nhi, cùng với sự khan hiếm tạng hiến đang diễn ra, đã thúc đẩy nhiều trung tâm ghép thực hiện thủ thuật này ở cả người lớn.
- Ưu điểm và nhược điểm của LDLT được trình bày trong Bảng 33.8.
- Hiến tạng sau khi tim ngừng đập dẫn đến thời gian thiếu máu nóng tăng và tần suất biến chứng đường mật cao hơn sau LT.
- Gan ghép từ người hiến dương tính với kháng thể lõi viêm gan B có thể được sử dụng cho người nhận dương tính với kháng nguyên bề mặt viêm gan B (HBsAg) hoặc thậm chí người nhận âm tính với HBsAg, với điều kiện là các biện pháp dự phòng hiệu quả cho HBV được áp dụng sau LT (xem thêm Chương 4).
- Sự sẵn có của các phác đồ kháng vi-rút hiệu quả và an toàn với DAAs để điều trị nhiễm HCV đã dẫn đến việc sử dụng các tạng ghép từ người hiến dương tính với HCV, đặc biệt là cho người nhận dương tính với HCV, với điều kiện không có xơ hóa đáng kể trong tạng ghép.
- Chẻ các tạng phù hợp thành các mảnh ghép mở rộng bên phải và bên trái để sử dụng cho một người nhận người lớn và một người nhận trẻ em, tương ứng, có thể giúp giải quyết tình trạng thiếu tạng hiến đang diễn ra.
Bảng 33.8: Ưu điểm và nhược điểm của ghép gan từ người hiến sống
| Ưu điểm | Nhược điểm |
|---|---|
| Quá trình sàng lọc người hiến kỹ lưỡng | Chỉ được cung cấp tại các trung tâm ghép gan chọn lọc |
| Thời gian ghép gan có thể lựa chọn, cho phép tối ưu hóa các liệu pháp | Bệnh tật và tử vong của người hiến |
| Giảm thời gian chờ đợi với việc giảm hệ quả số ca “rớt khỏi danh sách” | Nguy cơ biến chứng đường mật cao hơn ở người hiến và người nhận |
| Thời gian thiếu máu lạnh tối thiểu |
Ức chế miễn dịch
- Mục tiêu chính của liệu pháp ức chế miễn dịch trong LT là ngăn ngừa thải ghép và đồng thời giảm thiểu các phản ứng có hại.
- Các phác đồ ức chế miễn dịch hiện đang được sử dụng có tỷ lệ thải ghép từ 35% đến 40%, nhưng mất tạng ghép do thải ghép là không phổ biến (<5%).
- Các phác đồ ức chế miễn dịch khác nhau giữa các trung tâm LT.
- Dung nạp miễn dịch có thể phát triển ở những bệnh nhân được chọn lọc, do đó cho phép ngừng ức chế miễn dịch mà không bị mất tạng ghép.
GLUCOCORTICOIDS
- Thường được sử dụng để ức chế miễn dịch tấn công (induction).
- Trụ cột trong điều trị thải ghép cấp tế bào (acute cellular rejection – ACR): Methylprednisolone 500 đến 1000 mg tiêm tĩnh mạch cách ngày, tổng cộng ba liều.
- Khoảng 90% các đợt ACR đáp ứng với glucocorticoid liều cao.
- Liên quan đến mức RNA HCV cao hơn và sự tái phát viêm gan C nghiêm trọng hơn, do đó dẫn đến giảm tuổi thọ.
- Tác dụng phụ: Đái tháo đường, tăng huyết áp, nhiễm trùng, loãng xương, tăng lipid máu và các triệu chứng tâm thần kinh.
CÁC CHẤT ỨC CHẾ CALCINEURIN (CNIS)
- Các chất ức chế mạnh đáp ứng tế bào T thông qua việc phong tỏa sản xuất interleukin-2 (IL-2).
- Chuyển hóa Cyclosporine phụ thuộc nhiều vào hoạt động của cytochrome P-450 3A4 (CYP3A4), có thể có các biến thể di truyền quan trọng và có thể bị ảnh hưởng đáng kể (gây cảm ứng hoặc ức chế) bởi các tương tác thuốc-thuốc và chức năng của tạng ghép.
- Nồng độ cyclosporine cần được theo dõi chặt chẽ bởi các nhà cung cấp dịch vụ ghép có kinh nghiệm.
- Nồng độ đáy điều trị mục tiêu từ 200 đến 300 ng/mL là mong muốn trong 3 tháng đầu sau LT và từ 80 đến 125 ng/mL sau đó.
- Tacrolimus mạnh hơn cyclosporine 100 lần, và nó cũng được chuyển hóa rộng rãi bởi CYP3A4.
- Thuốc ức chế miễn dịch hàng đầu được sử dụng bởi hầu hết các trung tâm LT.
- Nồng độ đáy ngay sau LT nên từ 7 đến 10 ng/mL.
- Nồng độ đáy khoảng 6 ng/mL là thỏa đáng sau 6 tháng đầu, và 4 đến 6 ng/mL thường được chấp nhận là mức mục tiêu để duy trì sau năm đầu tiên sau LT.
- Tác dụng phụ phổ biến nhất: Độc tính trên thận, tăng huyết áp, độc tính thần kinh, đái tháo đường, tăng lipid máu và tăng kali máu.
- Tacrolimus so với cyclosporine
- Tacrolimus có liên quan đến việc cải thiện sự sống còn của bệnh nhân và tạng ghép và ít đợt ACR hơn.
- Đái tháo đường mới mắc phổ biến hơn với tacrolimus.
- Các biến cố bất lợi về thần kinh phổ biến hơn với tacrolimus.
- Rậm lông và tăng sản nướu là các biến cố bất lợi đặc trưng của cyclosporine.
- Tần suất rối loạn tăng sinh lympho sau ghép (posttransplant lymphoproliferative disorders – PTLD) là tương đương đối với cả hai tác nhân.
MYCOPHENOLATE MOFETIL VÀ AXIT MYCOPHENOLIC
- Mycophenolate mofetil được chuyển đổi thành hợp chất hoạt động axit mycophenolic trong quá trình chuyển hóa lần đầu qua gan.
- Axit mycophenolic ngăn chặn sự tăng sinh của tế bào lympho thông qua việc ức chế tổng hợp các nucleotide guanine.
- Các tác nhân này không liên quan đến độc tính trên thận và cho phép sử dụng liều thấp hơn của CNI.
- Liệu pháp đơn trị với mycophenolate mofetil hoặc axit mycophenolic không được khuyến nghị cho người nhận ghép gan vì nó có liên quan đến tỷ lệ ACR cao.
- Không cần theo dõi nồng độ thuốc trong điều trị.
- Tác dụng phụ phổ biến nhất: Các triệu chứng tiêu hóa và ức chế tủy xương.
- Tiêu chảy là tác dụng phụ giới hạn liều phổ biến nhất, nhưng đau bụng, buồn nôn và nôn cũng phổ biến.
- Một công thức bao tan trong ruột của axit mycophenolic có sẵn và đã cải thiện khả năng dung nạp đường tiêu hóa.
CÁC CHẤT ỨC CHẾ MỤC TIÊU CỦA RAPAMYCIN Ở ĐỘNG VẬT CÓ VÚ (mTOR)
- Sirolimus và everolimus ức chế sự tăng sinh của tế bào T và B thông qua việc phong tỏa tín hiệu truyền dẫn từ thụ thể IL-2.
- Sirolimus được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ cấp phép sử dụng cho người nhận ghép thận; việc sử dụng nó ở người nhận ghép gan là ngoài nhãn. Everolimus được cấp phép sử dụng cho cả người nhận ghép thận và gan.
- Cả hai tác nhân đều có thể được sử dụng như một phần của phác đồ ức chế miễn dịch bảo vệ thận ở người nhận ghép gan bị độc tính trên thận do CNI gây ra.
- Cả hai tác nhân đều có đặc tính chống tăng sinh và có khả năng, mặc dù chưa được chứng minh, mang lại lợi thế không tái phát ở những người nhận ghép gan bị HCC.
- Tác dụng phụ: Ức chế tủy xương, huyết khối động mạch gan, chậm lành vết thương, tăng lipid máu, phù ngoại biên và các triệu chứng tiêu hóa.
LIỆU PHÁP KHÁNG THỂ
- Globulin kháng thymocyte là một kháng thể đa dòng làm suy giảm tế bào được sử dụng như một tác nhân tấn công hoặc để điều trị thải ghép kháng glucocorticoid.
- Muromonab-CD3 (OKT3) là một kháng thể đơn dòng của chuột được sử dụng để tấn công ức chế miễn dịch và điều trị thải ghép kháng glucocorticoid.
- Hội chứng giải phóng cytokine thường xảy ra với những liều đầu tiên; nên điều trị trước bằng một glucocorticoid, acetaminophen và thuốc kháng histamine.
- Sự tái phát sớm và nghiêm trọng của nhiễm HCV có thể xảy ra.
- Có khả năng liên quan đến tăng tỷ lệ PTLD.
- Basiliximab là một kháng thể đơn dòng dạng khảm chặn thụ thể IL-2 (CD25) và ức chế sự tăng sinh của tế bào T.
- Được cấp phép để phòng ngừa thải ghép trong ghép thận.
- Đã được sử dụng ngoài nhãn như một tác nhân tấn công ở người nhận ghép gan bị suy thận hoặc như một phần của các phác đồ không chứa glucocorticoid.
- Alemtuzumab là một kháng thể đơn dòng tái tổ hợp được nhân hóa chống lại CD52, làm suy giảm sâu sắc các tế bào lympho thông qua sự ly giải tế bào qua trung gian tế bào phụ thuộc kháng thể sau khi liên kết với tế bào lympho T và B.
- Được cấp phép để điều trị bệnh bạch cầu lympho bào mạn tính dòng B nhưng không được sử dụng cho người nhận ghép gan.
- Ban đầu được đề xuất như một tác nhân thay thế có thể cho phép giảm việc sử dụng glucocorticoid và CNI ở người nhận ghép gan (sử dụng ngoài nhãn), nhưng tình trạng ức chế miễn dịch sâu sắc, nguy cơ nhiễm trùng và PTLD cao, và thiếu bằng chứng mạnh mẽ hỗ trợ lợi ích đã làm giảm sự nhiệt tình đối với tác nhân này.
Biến chứng
TẠNG GHÉP BAN ĐẦU KHÔNG HOẠT ĐỘNG (PNF)
- Chức năng ban đầu của tạng ghép là một yếu tố quyết định quan trọng cho sự thành công lâu dài của LT.
- Một dạng cực đoan của tổn thương do bảo quản xảy ra ở khoảng 3% đến 6% các tạng ghép.
- Biểu hiện lâm sàng như ALF
- Bệnh não gan
- Bệnh đông máu
- Vàng da
- Tăng nồng độ aminotransferase huyết thanh
- Các yếu tố nguy cơ của PNF
- Tuổi người hiến >50
- Gan nhiễm mỡ >30% thể tích gan
- Hiến tạng sau khi tim ngừng đập
- Tạng ghép giảm kích thước
- Tăng natri máu nặng ở người hiến
- Thời gian thiếu máu lạnh kéo dài
- Ghép lại là lựa chọn điều trị duy nhất cho PNF.
THẢI GHÉP TỐI CẤP
- Thải ghép biểu hiện trong vòng vài giờ sau LT.
- Gây ra bởi các kháng thể được hình thành từ trước của người nhận chống lại các tế bào nội mô của tạng ghép.
- Biểu hiện lâm sàng không thể phân biệt được với PNF; do đó, cần sinh thiết gan khẩn cấp để chẩn đoán: hoại tử sung huyết và xuất huyết trong các xoang gan của tạng ghép.
- Tương tự như PNF; ghép lại là lựa chọn điều trị duy nhất.
THẢI GHÉP CẤP TẾ BÀO (ACR)
- Thường biểu hiện dưới dạng các bất thường trong các xét nghiệm sinh hóa gan.
- Sinh thiết gan vẫn là tiêu chuẩn vàng để chẩn đoán. Các đặc điểm mô học bao gồm:
- Thâm nhiễm viêm hỗn hợp trong các khoảng cửa
- Viêm nội mô (viêm tiểu tĩnh mạch)
- Viêm đường mật không sinh mủ liên quan đến các ống mật gian tiểu thùy
- Nền tảng của điều trị là glucocorticoid liều cao: Methylprednisolone 500 đến 1000 mg cách ngày trong ba liều, có thể theo sau (hoặc không) bởi một đợt giảm liều prednisone ngắn. ACR kháng glucocorticoid có thể cần điều trị bằng thymoglobulin.
THẢI GHÉP MẠN TÍNH
- Đặc trưng về mặt mô học bởi tình trạng giảm ống mật và các cụm tế bào bọt hoặc viêm động mạch tắc nghẽn.
- Thải ghép mạn tính sớm có thể hồi phục nếu được chẩn đoán và quản lý hợp lý, nhưng thải ghép mạn tính muộn thường không thể hồi phục. Có thể cần ghép lại nếu thải ghép mạn tính dẫn đến suy tạng ghép.
THẢI GHÉP QUA TRUNG GIAN KHÁNG THỂ (AMR)
- Thải ghép qua trung gian kháng thể đơn thuần (AMR) hiếm gặp ở các tạng ghép tương thích ABO.
- Đặc trưng bởi các kháng thể kháng HLA đặc hiệu của người hiến, tổn thương nội mô vi mạch, và kiểu nhuộm hóa mô miễn dịch C4d dạng thẳng trong các xoang gan.
- Các liệu pháp làm suy giảm kháng thể như thay huyết tương và/hoặc rituximab được sử dụng để điều trị AMR; truyền gamma globulin tĩnh mạch cũng đã được sử dụng.
BIẾN CHỨNG MẠCH MÁU
- Huyết khối động mạch gan (HAT)
- Biến chứng mạch máu phổ biến nhất sau LT (được báo cáo ở 4% đến 15% người nhận ghép gan; aspirin liều thấp được sử dụng để phòng ngừa tiên phát).
- Thường xảy ra tại miệng nối của động mạch gan gốc và động mạch gan của người hiến.
- Biểu hiện lâm sàng phụ thuộc vào thời điểm: HAT sớm có thể dẫn đến suy tạng ghép cấp; HAT muộn có thể dẫn đến bệnh lý đường mật do thiếu máu cục bộ.
- Siêu âm Doppler là xét nghiệm chẩn đoán ban đầu, nhưng chụp mạch thường được yêu cầu để xác nhận chẩn đoán.
- Các kỹ thuật can thiệp nội mạch có thể loại bỏ nhu cầu phẫu thuật sửa chữa; có thể cần ghép lại cho các trường hợp không thể điều trị.
- Tắc nghẽn dòng chảy tĩnh mạch ra
- Biểu hiện lâm sàng là cổ trướng kháng trị, phù và rối loạn chức năng gan tiến triển.
- Không có sự khác biệt về tỷ lệ mắc giữa thay thế tĩnh mạch chủ tiêu chuẩn và tái tạo kiểu “cõng”.
- Can thiệp nội mạch là phương pháp điều trị được lựa chọn.
BIẾN CHỨNG ĐƯỜNG MẬT
- Nguyên nhân quan trọng gây bệnh tật và tử vong, xảy ra ở 5% đến 25% người nhận ghép gan và ảnh hưởng xấu đến sự sống còn của bệnh nhân và tạng ghép.
- Các biến chứng đường mật bao gồm hẹp, rò mật, các khuyết lấp đầy trong ống mật và rối loạn chức năng cơ vòng Oddi.
- LDLT có liên quan đến nguy cơ biến chứng đường mật cao hơn so với LT từ người hiến đã qua đời.
- Các nghiên cứu hình ảnh bao gồm siêu âm qua ổ bụng và chụp cộng hưởng từ đường mật là những công cụ quan trọng để chẩn đoán. Siêu âm nội soi cũng có thể hữu ích để chẩn đoán trong các trường hợp được chọn lọc. Nội soi mật tụy ngược dòng được sử dụng cho các can thiệp điều trị.
- Hẹp đường mật là biến chứng đường mật phổ biến nhất và có thể được phân loại là tại miệng nối hoặc không tại miệng nối và khác nhau về nguyên nhân, thời điểm chẩn đoán, số lượng, hình ảnh X-quang và sự thành công của liệu pháp nội soi.
NHIỄM TRÙNG
- Nhiễm trùng do vi khuẩn thường xảy ra sớm sau LT và liên quan đến các biến chứng phẫu thuật.
- Viêm phổi do Pneumocystis jiroveci có thể xảy ra do ức chế miễn dịch; dự phòng bằng thuốc được chỉ định trong 6 đến 12 tháng đầu sau LT.
- Trimethoprim-sulfamethoxazole là tác nhân hàng đầu.
- Pentamidine hoặc atovaquone có thể được sử dụng ở những người nhận ghép gan bị dị ứng với sulfonamide.
- Nhiễm nấm xâm lấn là một mối đe dọa lớn đối với người nhận ghép gan; dự phòng kháng nấm thường được sử dụng trong giai đoạn ngay sau LT.
- Nguy cơ nhiễm cytomegalovirus (CMV) có liên quan đến tình trạng CMV của người nhận và người hiến.
- Nguy cơ cao nhất đối với các cặp người nhận âm tính/người hiến dương tính.
- Các yếu tố nguy cơ khác bao gồm việc sử dụng thymoglobulin và ghép lại.
- Dự phòng bằng thuốc kháng vi-rút là thực hành tiêu chuẩn, và thời gian phụ thuộc vào phân tầng nguy cơ: 6 tháng đối với các cặp người hiến dương tính/người nhận âm tính, 3 tháng đối với tất cả các trường hợp khác.
- Các tác nhân kháng vi-rút như valganciclovir được sử dụng để ngăn ngừa nhiễm CMV thường cũng có hoạt tính chống lại vi-rút Epstein-Barr (EBV) (xem phần sau).
Chăm sóc dài hạn cho người nhận ghép gan
- Chăm sóc y tế chung cho các bệnh đi kèm nên được thực hiện với sự hợp tác của trung tâm ghép.
- Tăng huyết áp hệ thống phổ biến ở bệnh nhân được điều trị bằng CNI; thuốc chẹn kênh canxi là các tác nhân được lựa chọn.
- Tăng lipid máu có thể được điều trị an toàn bằng statin.
- Đái tháo đường mới mắc thường là thứ phát sau khi sử dụng glucocorticoid hoặc CNI dài hạn.
- Rối loạn chức năng thận phổ biến ở người nhận ghép gan; mặc dù CNI là một nguy cơ quan trọng, các yếu tố nguy cơ chuyển hóa là nguyên nhân phổ biến nhất.
- Kiểm soát đường huyết đầy đủ và điều trị tăng huyết áp là cần thiết để giảm nguy cơ rối loạn chức năng thận.
- Điều chỉnh các phác đồ CNI hoặc sử dụng các thuốc ức chế miễn dịch bổ sung có thể cho phép giảm đáng kể liều CNI mà không gây nguy hiểm cho sức khỏe của tạng ghép.
- Xác định sớm các yếu tố nguy cơ và thực hiện các chiến lược để ngăn ngừa rối loạn chức năng thận giúp cải thiện kết quả lâu dài.
- Mất khoáng xương là một vấn đề phổ biến ở người nhận ghép gan.
- Thường cần bổ sung canxi và vitamin D.
- Xét nghiệm đo mật độ xương bằng phương pháp hấp thụ tia X năng lượng kép (DEXA) được chỉ định định kỳ để xác định sự tiến triển của tình trạng mất khoáng xương.
- Bisphosphonates có thể được chỉ định để điều trị loãng xương.
- Ức chế miễn dịch dài hạn có liên quan đến tăng nguy cơ mắc các khối u ác tính ngoài gan.
- Phải tiếp tục tầm soát theo lứa tuổi đối với ung thư đại tràng, ung thư vú, ung thư cổ tử cung và ung thư tuyến tiền liệt.
- Bệnh nhân nên tránh tiếp xúc trực tiếp với ánh nắng mặt trời quá mức và không cần thiết. Nên sử dụng quần áo bảo vệ và kem chống nắng và khám da liễu hàng năm do nguy cơ ung thư da tăng.
- PTLD là một biến chứng hiếm gặp nhưng đáng ngại ở người nhận ghép gan có thể do nhiễm EBV nguyên phát hoặc tái hoạt động của nó. Giảm ức chế miễn dịch thường là chiến lược quản lý ban đầu, và một số trường hợp cần hóa trị.
- Tần suất tái phát của bệnh gan nguyên phát ở người nhận ghép gan là khác nhau và phần lớn được quyết định bởi nguyên nhân ban đầu.
- Tái phát nhiễm HCV là phổ biến nếu không có SVR trước LT.
- Các phác đồ bao gồm các tác nhân kháng vi-rút và/hoặc HBIG làm giảm đáng kể sự tái phát của nhiễm HBV.
- Các bệnh gan tự miễn có tỷ lệ tái phát tương đối cao sau LT; nên theo dõi tích cực.
- Nên tiếp tục theo dõi HCC ở người nhận ghép gan nếu HCC là chỉ định cho LT hoặc nếu nó được phát hiện tình cờ trong gan bệnh.
- Các bệnh đi kèm chuyển hóa như béo phì, đái tháo đường, tăng lipid máu và tăng huyết áp phổ biến ở người nhận ghép gan và dẫn đến tăng nguy cơ mắc các bệnh tim mạch. Viêm gan nhiễm mỡ không do rượu tái phát hoặc mới mắc cũng được báo cáo với tần suất khác nhau và có liên quan đến sự hiện diện của các yếu tố nguy cơ chuyển hóa. Thay đổi lối sống và điều chỉnh ức chế miễn dịch phù hợp là các bước cần thiết trong quản lý.
- Việc sử dụng rượu và thuốc lá phải được theo dõi cẩn thận.
- Việc mang thai nên được trì hoãn ít nhất 1 năm sau LT, và nên được quản lý bởi một bác sĩ sản khoa nguy cơ cao.
- Tacrolimus, cyclosporine, sirolimus, và everolimus là các thuốc thuộc nhóm C trong thai kỳ.
- Mycophenolate mofetil và axit mycophenolic là các thuốc thuộc nhóm D trong thai kỳ.
- Nên khuyến khích kiểm soát cân nặng thông qua thay đổi chế độ ăn và hoạt động thể chất ở tất cả những người nhận ghép gan.
TÀI LIỆU THAM KHẢO
- Clavien PA, Lesurtel M, Bossuyt PM, et al. Recommendations for liver transplantation for hepatocellular carcinoma: an international consensus conference report. Lancet Oncol. 2012;13:e11-e22.
- D’Amico G, Garcia-Tsao G, Pagliaro L. Natural history and prognostic indicators of survival in cirrhosis: a systematic review of 118 studies. J Hepatol. 2006;44:217-231.
- Darwish Murad S, Kim WR, Harnois DM, et al. Efficacy of neoadjuvant chemoradiation, followed by liver transplantation, for perihilar cholangiocarcinoma at 12 US centers. Gastroenterology. 2012;143:88-98.
- Eason JD, Gonwa TA, Davis CL, et al. Proceedings of Consensus Conference on Simultaneous Liver Kidney Transplantation (SLK). Am J Transplant. 2008;8:2243-2251.
- Gedaly R, Daily MF, Davenport D, et al. Liver transplantation for the treatment of liver metastases from neuroendocrine tumors: an analysis of the UNOS database. Arch Surg. 2011;146:953-958.
- Lentine KL, Costa SP, Weir MR, et al. Cardiac disease evaluation and management among kidney and liver transplantation candidates: a scientific statement from the American Heart Association and the American College of Cardiology Foundation. J Am Coll Cardiol. 2012;60:434-480.
- Lucey MR, Terrault N, Ojo L, et al. Long-term management of the successful adult liver transplant: 2012 practice guideline by the American Association for the Study of Liver Diseases and the American Society of Transplantation. Liver Transpl. 2013;19:3-26.
- Martin P, DiMartini A, Feng S, et al. Evaluation for liver transplantation in adults: 2013 practice guideline by the American Association for the Study of Liver Diseases and the American Society of Transplantation. Hepatology. 2014;59:1144-1165.
- Muzaale AD, Dagher NN, Montgomery RA, et al. Estimates of early death, acute liver failure, and long-term mortality among live liver donors. Gastroenterology. 2012;142:273-280.
- Porrett PM, Hashmi SK, Shaked A. Immunosuppression: trends and tolerance? Clin Liver Dis. 2014;18:687-716.
- Sharr WW, Chan SC, Lo CM. Current status of downstaging of hepatocellular carcinoma before liver transplantation. Transplantation. 2014;97:S10-S17.
- Terrault NA, Roland ME, Schiano T, et al. Outcomes of liver transplant recipients with hepatitis C and human immunodeficiency virus coinfection. Liver Transpl. 2012;18:716-726.
- Tiukinhoy-Laing SD, Rossi JS, Bayram M, et al. Cardiac hemodynamic and coronary angiographic characteristics of patients being evaluated for liver transplantation. Am J Cardiol. 2006;98:178-181.
- Wells MM, Croome KP, Boyce E, et al. Roux-en-Y choledochojejunostomy versus duct-to-duct biliary anastomosis in liver transplantation for primary sclerosing cholangitis: a meta-analysis. Transplant Proc. 2013;45:2263-2271.
Bảng chú giải thuật ngữ Y học Anh Việt
| STT | Thuật ngữ tiếng Anh | Phiên âm IPA | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Liver transplantation (LT) | /ˈlɪvər ˌtrænsplænˈteɪʃən/ | Ghép gan |
| 2 | Acute liver failure (ALF) | /əˈkjut ˈlɪvər ˈfeɪljər/ | Suy gan cấp |
| 3 | End-stage liver disease (ESLD) | /ɛnd-steɪdʒ ˈlɪvər dɪˈziz/ | Bệnh gan giai đoạn cuối |
| 4 | Inherited liver diseases | /ɪnˈhɛrɪtɪd ˈlɪvər dɪˈzizɪz/ | Bệnh gan di truyền |
| 5 | Metabolic liver diseases | /ˌmɛtəˈbɒlɪk ˈlɪvər dɪˈzizɪz/ | Bệnh gan chuyển hóa |
| 6 | Hepatic malignancies | /hɪˈpætɪk məˈlɪgnənsiz/ | Bệnh lý ác tính ở gan |
| 7 | Hepatocellular carcinoma (HCC) | /hɪˌpætoʊˈsɛljələr ˌkɑrsɪˈnoʊmə/ | Ung thư biểu mô tế bào gan |
| 8 | Cholangiocarcinoma (CC) | /koʊˌlændʒioʊˌkɑrsɪˈnoʊmə/ | Ung thư đường mật |
| 9 | Neuroendocrine tumors | /ˌnʊəroʊˈɛndəkrɪn ˈtumərz/ | Khối u thần kinh nội tiết |
| 10 | Surgical techniques | /ˈsɜrdʒɪkəl tɛkˈniks/ | Kỹ thuật phẫu thuật |
| 11 | Perioperative management | /ˌpɛriˈɒpərətɪv ˈmænɪdʒmənt/ | Quản lý chu phẫu |
| 12 | Immunosuppressive regimens | /ˌɪmjunoʊsəˈprɛsɪv ˈrɛdʒɪmənz/ | Phác đồ ức chế miễn dịch |
| 13 | Liver transplant recipients | /ˈlɪvər ˈtrænsplænt rɪˈsɪpiənts/ | Người nhận ghép gan |
| 14 | Comorbid conditions | /ˈkoʊˈmɔrbɪd kənˈdɪʃənz/ | Bệnh đi kèm |
| 15 | Posttransplant outcomes | /poʊstˈtrænsplænt ˈaʊtˌkʌmz/ | Kết quả sau ghép |
| 16 | Live-donor LT | /laɪv-ˈdoʊnər ɛl-ti/ | Ghép gan từ người hiến sống |
| 17 | Split LT | /splɪt ɛl-ti/ | Ghép gan chẻ |
| 18 | Extended criteria grafts | /ɪkˈstɛndɪd kraɪˈtɪriə græfts/ | Tạng hiến mở rộng tiêu chuẩn |
| 19 | Donor organs | /ˈdoʊnər ˈɔrgənz/ | Tạng hiến |
| 20 | Graft outcomes | /græft ˈaʊtˌkʌmz/ | Kết quả tạng ghép |
| 21 | Survival rates | /sərˈvaɪvəl reɪts/ | Tỷ lệ sống còn |
| 22 | Perioperative intensive care | /ˌpɛriˈɒpərətɪv ɪnˈtɛnsɪv kɛr/ | Chăm sóc tích cực chu phẫu |
| 23 | United Network for Organ Sharing (UNOS) | /juˈnaɪtɪd ˈnɛtˌwɜrk fɔr ˈɔrgən ˈʃɛrɪŋ/ | Mạng lưới Chia sẻ Tạng thống nhất |
| 24 | Living donor liver transplantation (LDLT) | /ˈlɪvɪŋ ˈdoʊnər ˈlɪvər ˌtrænsplænˈteɪʃən/ | Ghép gan từ người hiến sống |
| 25 | Morbidity | /mɔrˈbɪdɪti/ | Bệnh tật |
| 26 | Mortality | /mɔrˈtælɪti/ | Tử vong |
| 27 | Organ allocation | /ˈɔrgən ˌæləˈkeɪʃən/ | Phân bổ tạng |
| 28 | Disease severity | /dɪˈziz sɪˈvɛrɪti/ | Mức độ nghiêm trọng của bệnh |
| 29 | Model for End-stage Liver Disease (MELD) | /ˈmɒdəl fɔr ɛnd-steɪdʒ ˈlɪvər dɪˈziz/ | Mô hình Bệnh gan Giai đoạn cuối |
| 30 | Pediatric End-stage Liver Disease (PELD) | /ˌpidiˈætrɪk ɛnd-steɪdʒ ˈlɪvər dɪˈziz/ | Mô hình Bệnh gan Giai đoạn cuối ở Trẻ em |
| 31 | Waitlist mortality | /ˈweɪtlɪst mɔrˈtælɪti/ | Tỷ lệ tử vong trong danh sách chờ |
| 32 | International normalized ratio (INR) | /ˌɪntərˈnæʃənəl ˈnɔrməˌlaɪzd ˈreɪʃioʊ/ | Tỷ lệ bình thường hóa quốc tế |
| 33 | Prothrombin time | /proʊˈθrɒmbɪn taɪm/ | Thời gian prothrombin |
| 34 | Serum bilirubin | /ˈsɪrəm ˌbɪlɪˈrubɪn/ | Bilirubin huyết thanh |
| 35 | Serum creatinine | /ˈsɪrəm kriˈætɪˌnin/ | Creatinine huyết thanh |
| 36 | Hyponatremia | /ˌhaɪpoʊnəˈtrimiə/ | Hạ natri máu |
| 37 | Cirrhosis | /səˈroʊsɪs/ | Xơ gan |
| 38 | Status 1A | /ˈstætəs wʌn eɪ/ | Tình trạng 1A |
| 39 | Biological MELD score | /ˌbaɪəˈlɒdʒɪkəl mɛld skɔr/ | Điểm MELD sinh học |
| 40 | Exception MELD score | /ɪkˈsɛpʃən mɛld skɔr/ | Điểm MELD ngoại lệ |
| 41 | Inactive status | /ɪnˈæktɪv ˈstætəs/ | Tình trạng không hoạt động |
| 42 | Life expectancy | /laɪf ɪkˈspɛktənsi/ | Tuổi thọ dự kiến |
| 43 | Decompensated Wilson disease | /diˈkɒmpənˌseɪtɪd ˈwɪlsənz dɪˈziz/ | Bệnh Wilson mất bù |
| 44 | Anhepatic state | /ˌæn.həˈpæt.ɪk steɪt/ | Tình trạng không có gan |
| 45 | Primary graft nonfunction (PNF) | /ˈpraɪˌmɛri græft ˌnɒnˈfʌŋkʃən/ | Tạng ghép chính không hoạt động |
| 46 | Hepatic artery thrombosis | /hɪˈpætɪk ˈɑrtəri θrɒmˈboʊsɪs/ | Huyết khối động mạch gan |
| 47 | Albumin | /ælˈbjumɪn/ | Albumin |
| 48 | Growth failure | /groʊθ ˈfeɪljər/ | Suy dinh dưỡng |
| 49 | Pediatric status 1B | /ˌpidiˈætrɪk ˈstætəs wʌn bi/ | Tình trạng 1B ở trẻ em |
| 50 | Hepatoblastoma | /hɪˌpætoʊblæsˈtoʊmə/ | U nguyên bào gan |
| 51 | Organic acidemia | /ɔrˈgænɪk ˌæsɪˈdimiə/ | Bệnh nhiễm acid hữu cơ |
| 52 | Urea cycle defects | /jʊˈriə ˈsaɪkəl ˈdiˌfɛkts/ | Rối loạn chu trình urê |
| 53 | Cholestatic diseases | /ˌkoʊlɪˈstætɪk dɪˈzizɪz/ | Bệnh ứ mật |
| 54 | Alcoholic liver disease | /ˌælkəˈhɒlɪk ˈlɪvər dɪˈziz/ | Bệnh gan do rượu |
| 55 | Drug-induced liver injury | /drʌg-ɪnˈdust ˈlɪvər ˈɪndʒəri/ | Tổn thương gan do thuốc |
| 56 | Acute viral hepatitis | /əˈkjut ˈvaɪrəl ˌhɛpəˈtaɪtɪs/ | Viêm gan siêu vi cấp |
| 57 | Decompensated cirrhosis | /diˈkɒmpənˌseɪtɪd səˈroʊsɪs/ | Xơ gan mất bù |
| 58 | Varices | /ˈvɛrəˌsiz/ | Giãn tĩnh mạch thực quản |
| 59 | Ascites | /əˈsaɪtiz/ | Cổ trướng |
| 60 | Variceal hemorrhage | /ˌvɛrɪˈsiəl ˈhɛmərɪdʒ/ | Xuất huyết do vỡ giãn tĩnh mạch |
| 61 | Antiviral therapy | /ˌæntiˈvaɪrəl ˈθɛrəpi/ | Liệu pháp kháng vi-rút |
| 62 | Autoimmune hepatitis | /ˌɔtoʊɪˈmjun ˌhɛpəˈtaɪtɪs/ | Viêm gan tự miễn |
| 63 | Encephalopathy | /ɛnˌsɛfəˈlɒpəθi/ | Bệnh não gan |
| 64 | Ventilator dependence | /ˈvɛntəˌleɪtər dɪˈpɛndəns/ | Phụ thuộc máy thở |
| 65 | Renal replacement therapy | /ˈrinəl rɪˈpleɪsmənt ˈθɛrəpi/ | Liệu pháp thay thế thận |
| 66 | Fulminant Wilson disease | /ˈfʊlmɪnənt ˈwɪlsənz dɪˈziz/ | Bệnh Wilson thể tối cấp |
| 67 | Surgical resection | /ˈsɜrdʒɪkəl riˈsɛkʃən/ | Phẫu thuật cắt bỏ |
| 68 | Portal vein invasion | /ˈpɔrtəl veɪn ɪnˈveɪʒən/ | Xâm lấn tĩnh mạch cửa |
| 69 | Extrahepatic metastasis | /ˌɛkstrəhɪˈpætɪk mɪˈtæstəsɪs/ | Di căn ngoài gan |
| 70 | Milan criteria | /mɪˈlæn kraɪˈtɪriə/ | Tiêu chuẩn Milan |
| 71 | Liver Imaging Reporting Data System (LI-RADS) | /ˈlɪvər ˈɪmɪdʒɪŋ rɪˈpɔrtɪŋ ˈdeɪtə ˈsɪstəm/ | Hệ thống Dữ liệu Báo cáo Hình ảnh Gan |
| 72 | Benign | /bɪˈnaɪn/ | Lành tính |
| 73 | Malignant | /məˈlɪgnənt/ | Ác tính |
| 74 | Organ Procurement and Transplantation Network (OPTN) | /ˈɔrgən proʊˈkjʊrmənt ænd ˌtrænsplænˈteɪʃən ˈnɛtˌwɜrk/ | Mạng lưới Mua sắm và Cấy ghép Tạng |
| 75 | Regional review board (RRB) | /ˈridʒənəl rɪˈvju bɔrd/ | Hội đồng xét duyệt khu vực |
| 76 | Downstaging | /ˌdaʊnˈsteɪdʒɪŋ/ | Hạ giai đoạn |
| 77 | Radiofrequency ablation | /ˌreɪdioʊˈfrikwənsi ˌæbˈleɪʃən/ | Đốt sóng cao tần |
| 78 | Transarterial chemoembolization | /trænsɑrˈtɪriəl ˌkimoʊˌɛmbələˈzeɪʃən/ | Hóa tắc mạch qua động mạch |
| 79 | Intrahepatic cholangiocarcinoma | /ˌɪntrəhɪˈpætɪk koʊˌlændʒioʊˌkɑrsɪˈnoʊmə/ | Ung thư đường mật trong gan |
| 80 | Neoadjuvant chemoradiation | /ˌnioʊˈædʒəvənt ˌkimoʊˌreɪdiˈeɪʃən/ | Hóa xạ trị tân bổ trợ |
| 81 | Perihilar CC | /ˌpɛrɪˈhaɪlər si-si/ | Ung thư đường mật rốn gan |
| 82 | Fibrolamellar HCC | /ˌfaɪbroʊləˈmɛlər eɪtʃ-si-si/ | Ung thư biểu mô tế bào gan thể sợi dẹt |
| 83 | Hepatic metastases | /hɪˈpætɪk mɪˈtæstəˌsiz/ | Di căn gan |
| 84 | Alpha-1 antitrypsin deficiency | /ˈælfə wʌn ˌæntiˈtrɪpsɪn dɪˈfɪʃənsi/ | Thiếu hụt Alpha-1 antitrypsin |
| 85 | Hereditary hemochromatosis | /həˈrɛdɪˌtɛri ˌhimoʊˌkroʊməˈtoʊsɪs/ | Bệnh thừa sắt di truyền |
| 86 | Familial amyloid polyneuropathy | /fəˈmɪliəl ˌæməˌlɔɪd ˌpɒliˌnʊˈrɒpəθi/ | Bệnh đa dây thần kinh amyloid gia đình |
| 87 | Primary hyperoxaluria | /ˈpraɪˌmɛri ˌhaɪpərˌɒksəˈlʊriə/ | Tăng oxalat niệu nguyên phát |
| 88 | Cystic fibrosis | /ˈsɪstɪk faɪˈbroʊsɪs/ | Xơ nang |
| 89 | Glycogen storage diseases | /ˈglaɪkədʒən ˈstɔrɪdʒ dɪˈzizɪz/ | Bệnh dự trữ glycogen |
| 90 | Tyrosinemia | /ˌtaɪroʊsɪˈnimiə/ | Bệnh tyrosinemia |
| 91 | Acute intermittent porphyria | /əˈkjut ˌɪntərˈmɪtənt pɔrˈfɪriə/ | Porphyria cấp tính gián đoạn |
| 92 | Uncontrolled sepsis | /ˌʌnkənˈtroʊld ˈsɛpsɪs/ | Nhiễm trùng huyết không kiểm soát |
| 93 | Acquired immunodeficiency syndrome (AIDS) | /əˈkwaɪərd ˌɪmjunoʊdɪˈfɪʃənsi ˈsɪnˌdroʊm/ | Hội chứng suy giảm miễn dịch mắc phải |
| 94 | Hemangiosarcoma | /hɪˌmændʒioʊˌsɑrˈkoʊmə/ | U mạch máu ác tính |
| 95 | Nonadherence | /ˌnɒnədˈhɪrəns/ | Không tuân thủ |
| 96 | Cardiovascular disease | /ˌkɑrdioʊˈvæskjələr dɪˈziz/ | Bệnh tim mạch |
| 97 | Dobutamine stress echocardiography | /doʊˈbjutəˌmin strɛs ˌɛkoʊˌkɑrdiˈɒgrəfi/ | Siêu âm tim gắng sức dobutamine |
| 98 | Systemic hypertension | /sɪˈstɛmɪk ˌhaɪpərˈtɛnʃən/ | Tăng huyết áp hệ thống |
| 99 | Dyslipidemia | /ˌdɪsˌlɪpɪˈdimiə/ | Rối loạn lipid máu |
| 100 | Left ventricular hypertrophy | /lɛft vɛnˈtrɪkjələr haɪˈpɜrtrəfi/ | Phì đại thất trái |
| 101 | Coronary angiography | /ˈkɔrəˌnɛri ˌændʒiˈɒgrəfi/ | Chụp mạch vành |
| 102 | Pulmonary disease | /ˈpʊlməˌnɛri dɪˈziz/ | Bệnh phổi |
| 103 | Chronic obstructive pulmonary disease (COPD) | /ˈkrɒnɪk əbˈstrʌktɪv ˈpʊlməˌnɛri dɪˈziz/ | Bệnh phổi tắc nghẽn mạn tính |
| 104 | Obstructive sleep apnea | /əbˈstrʌktɪv slip ˈæpniə/ | Ngưng thở khi ngủ do tắc nghẽn |
| 105 | Hepatic hydrothorax | /hɪˈpætɪk ˌhaɪdroʊˈθɔræks/ | Tràn dịch màng phổi do gan |
| 106 | Portopulmonary hypertension (POPH) | /ˈpɔrtoʊˈpʊlməˌnɛri ˌhaɪpərˈtɛnʃən/ | Tăng áp động mạch phổi cửa |
| 107 | Hepatopulmonary syndrome (HPS) | /hɪˌpætoʊˈpʊlməˌnɛri ˈsɪnˌdroʊm/ | Hội chứng gan phổi |
| 108 | Indwelling catheters | /ˌɪnˈdwɛlɪŋ ˈkæθɪtərz/ | Ống thông lưu |
| 109 | Right heart catheterization | /raɪt hɑrt ˌkæθətərɪˈzeɪʃən/ | Thông tim phải |
| 110 | Mean pulmonary arterial pressure (mPAP) | /min ˈpʊlməˌnɛri ɑrˈtɪriəl ˈprɛʃər/ | Áp lực động mạch phổi trung bình |
| 111 | Pulmonary vascular resistance (PVR) | /ˈpʊlməˌnɛri ˈvæskjələr rɪˈzɪstəns/ | Kháng lực mạch máu phổi |
| 112 | Pulse oximetry | /pʌls ɒkˈsɪmɪtri/ | Đo oxy xung |
| 113 | Arterial oxygen saturation (SpO2) | /ɑrˈtɪriəl ˈɒksɪdʒən ˌsæʧəˈreɪʃən/ | Độ bão hòa oxy động mạch |
| 114 | Arterial blood gas analysis | /ɑrˈtɪriəl blʌd gæs əˈnælɪsɪs/ | Phân tích khí máu động mạch |
| 115 | Alveolar-arterial (A-a) gradient | /ælˈviələr-ɑrˈtɪriəl ˈgreɪdiənt/ | Chênh lệch oxy phế nang-động mạch |
| 116 | Contrast-enhanced echocardiography | /ˈkɒntræst-ɪnˈhænst ˌɛkoʊˌkɑrdiˈɒgrəfi/ | Siêu âm tim cản quang |
| 117 | Technetium-labeled macroaggregated albumin scanning | /tɛkˈniʃiəm-ˈleɪbəld ˌmækroʊˈægrəˌgeɪtɪd ælˈbjumɪn ˈskænɪŋ/ | Xạ hình với albumin đại phân tử được đánh dấu technetium |
| 118 | Intrapulmonary vascular shunts | /ˌɪntrəˈpʊlməˌnɛri ˈvæskjələr ʃʌnts/ | Shunt mạch máu trong phổi |
| 119 | Live-attenuated vaccines | /laɪv-əˈtɛnjuˌeɪtɪd vækˈsinz/ | Vắc-xin sống giảm độc lực |
| 120 | Human immunodeficiency virus (HIV) | /ˈhjumən ˌɪmjunoʊdɪˈfɪʃənsi ˈvaɪrəs/ | Vi-rút suy giảm miễn dịch ở người |
| 121 | Opportunistic infection | /ˌɒpərˌtunɪstɪk ɪnˈfɛkʃən/ | Nhiễm trùng cơ hội |
| 122 | Viral suppression | /ˈvaɪrəl səˈprɛʃən/ | Ức chế vi-rút |
| 123 | Hepatitis B immunoglobulin (HBIG) | /ˌhɛpəˈtaɪtɪs bi ˌɪmjunoʊˈglɒbjəlɪn/ | Globulin miễn dịch viêm gan B |
| 124 | Direct-acting antivirals (DAAs) | /dɪˈrɛkt-ˈæktɪŋ ˌæntiˈvaɪrəlz/ | Thuốc kháng vi-rút tác động trực tiếp |
| 125 | Sustained virologic response (SVR) | /səˈsteɪnd ˌvaɪrəˈlɒdʒɪk rɪˈspɒns/ | Đáp ứng vi-rút bền vững |
| 126 | Acute kidney injury | /əˈkjut ˈkɪdni ˈɪndʒəri/ | Tổn thương thận cấp |
| 127 | Hepatorenal syndrome (HRS) | /hɪˌpætoʊˈrinəl ˈsɪnˌdroʊm/ | Hội chứng gan-thận |
| 128 | Glomerular filtration rate (GFR) | /gloʊˈmɛrjulər fɪlˈtreɪʃən reɪt/ | Độ lọc cầu thận |
| 129 | Glomerulosclerosis | /gləˌmɛrjəloʊskləˈroʊsɪs/ | Xơ cứng cầu thận |
| 130 | Glomerular fibrosis | /gləˈmɛrjulər faɪˈbroʊsɪs/ | Xơ hóa cầu thận |
| 131 | Wedged hepatic vein pressure gradient | /wɛdʒd hɪˈpætɪk veɪn ˈprɛʃər ˈgreɪdiənt/ | Chênh áp tĩnh mạch gan bít |
| 132 | Substance abuse | /ˈsʌbstəns əˈbjus/ | Lạm dụng chất gây nghiện |
| 133 | Abstinence | /ˈæbstɪnəns/ | Kiêng khem |
| 134 | Recidivism | /rɪˈsɪdɪˌvɪzəm/ | Tái nghiện |
| 135 | Acute alcoholic hepatitis | /əˈkjut ˌælkəˈhɒlɪk ˌhɛpəˈtaɪtɪs/ | Viêm gan do rượu cấp tính |
| 136 | Pulmonary aspergillosis | /ˈpʊlməˌnɛri ˌæspərˌdʒɪˈloʊsɪs/ | Bệnh nấm aspergillosis phổi |
| 137 | Primary sclerosing cholangitis (PSC) | /ˈpraɪˌmɛri ˈsklɪəroʊsɪŋ ˌkoʊlənˈdʒaɪtɪs/ | Viêm xơ đường mật nguyên phát |
| 138 | Colonoscopy | /ˌkoʊləˈnɒskəpi/ | Nội soi đại tràng |
| 139 | Warm ischemia time | /wɔrm ɪˈskimiə taɪm/ | Thời gian thiếu máu nóng |
| 140 | Cold ischemia time | /koʊld ɪˈskimiə taɪm/ | Thời gian thiếu máu lạnh |
| 141 | Human leukocyte antigen (HLA) | /ˈhjumən ˈlukoʊˌsaɪt ˈæntɪdʒən/ | Kháng nguyên bạch cầu người |
| 142 | Piggyback technique | /ˈpɪgiˌbæk tɛkˈnik/ | Kỹ thuật cõng |
| 143 | Choledococholedocostomy | /koʊˌlɛdəkoʊkoʊˌlɛdəˈkɒstəmi/ | Miệng nối ống mật chủ – ống mật chủ |
| 144 | Hepaticojejunostomy | /hɪˌpætɪkoʊˌdʒɛdʒəˈnɒstəmi/ | Miệng nối ống gan – hỗng tràng |
| 145 | Roux-en-Y | /ru-ɛn-waɪ/ | Roux-en-Y |
| 146 | Donation after cardiac death | /doʊˈneɪʃən ˈæftər ˈkɑrdiæk dɛθ/ | Hiến tạng sau khi tim ngừng đập |
| 147 | Hepatitis B core antibody | /ˌhɛpəˈtaɪtɪs bi kɔr ˈæntiˌbɒdi/ | Kháng thể lõi viêm gan B |
| 148 | Hepatitis B surface antigen (HBsAg) | /ˌhɛpəˈtaɪtɪs bi ˈsɜrfəs ˈæntɪdʒən/ | Kháng nguyên bề mặt viêm gan B |
| 149 | Immune tolerance | /ɪˈmjun ˈtɒlərəns/ | Dung nạp miễn dịch |
| 150 | Glucocorticoids | /ˌglukoʊˈkɔrtɪˌkɔɪdz/ | Glucocorticoid |
| 151 | Acute cellular rejection (ACR) | /əˈkjut ˈsɛljələr rɪˈdʒɛkʃən/ | Thải ghép cấp tế bào |
| 152 | Osteoporosis | /ˌɒstioʊpəˈroʊsɪs/ | Loãng xương |
| 153 | Hyperlipidemia | /ˌhaɪpərˌlɪpɪˈdimiə/ | Tăng lipid máu |
| 154 | Calcineurin inhibitors (CNIs) | /ˌkælsɪˈnʊrɪn ɪnˈhɪbɪtərz/ | Các chất ức chế calcineurin |
| 155 | Cyclosporine | /ˌsaɪkloʊˈspɔrin/ | Cyclosporine |
| 156 | Cytochrome P-450 3A4 (CYP3A4) | /ˈsaɪtəˌkroʊm pi-fɔr-ˈfɪfti θri-eɪ-fɔr/ | Cytochrome P-450 3A4 |
| 157 | Trough levels | /trɔf ˈlɛvəlz/ | Nồng độ đáy |
| 158 | Tacrolimus | /təˈkroʊlɪməs/ | Tacrolimus |
| 159 | Nephrotoxicity | /ˌnɛfroʊtɒkˈsɪsɪti/ | Độc tính trên thận |
| 160 | Neurotoxicity | /ˌnʊəroʊtɒkˈsɪsɪti/ | Độc tính thần kinh |
| 161 | Hirsutism | /ˈhɜrsəˌtɪzəm/ | Rậm lông |
| 162 | Gingival hyperplasia | /ˈdʒɪndʒɪvəl ˌhaɪpərˈpleɪʒə/ | Tăng sản nướu |
| 163 | Posttransplant lymphoproliferative disorders (PTLD) | /poʊstˈtrænsplænt ˌlɪmfoʊprəˈlɪfərətɪv dɪsˈɔrdərz/ | Rối loạn tăng sinh lympho sau ghép |
| 164 | Mycophenolate mofetil | /ˌmaɪkoʊˈfɛnəˌleɪt ˈmɒfətɪl/ | Mycophenolate mofetil |
| 165 | Mycophenolic acid | /ˌmaɪkoʊfɪˈnɒlɪk ˈæsɪd/ | Axit mycophenolic |
| 166 | Enteric-coated formulation | /ɛnˈtɛrɪk-ˈkoʊtɪd ˌfɔrmjəˈleɪʃən/ | Công thức bao tan trong ruột |
| 167 | Mammalian target of rapamycin (mTOR) inhibitors | /məˈmeɪliən ˈtɑrgət ʌv ˌræpəˈmaɪsɪn ɪnˈhɪbɪtərz/ | Các chất ức chế mTOR |
| 168 | Sirolimus | /ˌsaɪroʊˈlaɪməs/ | Sirolimus |
| 169 | Everolimus | /ˌɛvəˈroʊlɪməs/ | Everolimus |
| 170 | Renal-sparing | /ˈrinəl-ˈspɛrɪŋ/ | Bảo vệ thận |
| 171 | Antithymocyte globulin | /ˌæntiˌθaɪmoʊsaɪt ˈglɒbjəlɪn/ | Globulin kháng thymocyte |
| 172 | Muromonab-CD3 (OKT3) | /ˌmjʊəroʊˈmoʊnæb-si-di-θri/ | Muromonab-CD3 |
| 173 | Cytokine release syndrome | /ˈsaɪtəˌkaɪn rɪˈlis ˈsɪnˌdroʊm/ | Hội chứng giải phóng cytokine |
| 174 | Basiliximab | /ˌbæsɪˈlɪksɪˌmæb/ | Basiliximab |
| 175 | Alemtuzumab | /ˌæləmˈtuzəˌmæb/ | Alemtuzumab |
| 176 | Preservation injury | /ˌprɛzərˈveɪʃən ˈɪndʒəri/ | Tổn thương do bảo quản |
| 177 | Graft steatosis | /græft ˌstiəˈtoʊsɪs/ | Gan nhiễm mỡ của tạng ghép |
| 178 | Hyperacute rejection | /ˌhaɪpərˈkjut rɪˈdʒɛkʃən/ | Thải ghép tối cấp |
| 179 | Endotheliitis | /ˌɛndoʊˌθiliˈaɪtɪs/ | Viêm nội mô |
| 180 | Nonsuppurative cholangitis | /ˌnɒnsəˈpjʊərətɪv ˌkoʊlənˈdʒaɪtɪs/ | Viêm đường mật không sinh mủ |
| 181 | Chronic rejection | /ˈkrɒnɪk rɪˈdʒɛkʃən/ | Thải ghép mạn tính |
| 182 | Ductopenia | /ˌdʌktoʊˈpiniə/ | Giảm ống mật |
| 183 | Obliterative arteriopathy | /əˈblɪtəˌreɪtɪv ɑrˌtɪriˈɒpəθi/ | Bệnh lý động mạch tắc nghẽn |
| 184 | Antibody-mediated rejection (AMR) | /ˈæntiˌbɒdi-ˈmidiˌeɪtɪd rɪˈdʒɛkʃən/ | Thải ghép qua trung gian kháng thể |
| 185 | Plasmapheresis | /ˌplæzməfəˈrisɪs/ | Thay huyết tương |
| 186 | Rituximab | /rɪˈtʌksɪˌmæb/ | Rituximab |
| 187 | Ischemic cholangiopathy | /ɪˈskemɪk ˌkoʊlənˈdʒiˈɒpəθi/ | Bệnh lý đường mật do thiếu máu cục bộ |
| 188 | Biliary strictures | /ˈbɪliˌɛri ˈstrɪktʃərz/ | Hẹp đường mật |
| 189 | Bile leaks | /baɪl liks/ | Rò mật |
| 190 | Sphincter of Oddi dysfunction | /ˈsfɪŋktər ʌv ˈoʊdi dɪsˈfʌŋkʃən/ | Rối loạn chức năng cơ vòng Oddi |
| 191 | Endoscopic retrograde cholangiography | /ˌɛndoʊˈskɒpɪk ˈrɛtroʊˌgreɪd koʊˌlændʒiˈɒgrəfi/ | Nội soi mật tụy ngược dòng |
| 192 | Anastomotic strictures | /əˌnæstəˈmɒtɪk ˈstrɪktʃərz/ | Hẹp tại miệng nối |
| 193 | Pneumocystis jiroveci pneumonia | /ˌnumoʊˈsɪstɪs ˌjɪroʊˈvɛtʃi njuˈmoʊniə/ | Viêm phổi do Pneumocystis jiroveci |
| 194 | Cytomegalovirus (CMV) | /ˌsaɪtoʊˌmɛgəloʊˈvaɪrəs/ | Cytomegalovirus |
| 195 | Epstein-Barr virus (EBV) | /ˈɛpstaɪn-bɑr ˈvaɪrəs/ | Vi-rút Epstein-Barr |
| 196 | Bone demineralization | /boʊn diˌmɪnərəlɪˈzeɪʃən/ | Mất khoáng xương |
| 197 | Dual-energy x-ray absorptiometry (DEXA) | /duəl-ˈɛnərdʒi ˈɛks-reɪ əbˌsɔrpʃiˈɒmɪtri/ | Đo mật độ xương bằng phương pháp hấp thụ tia X năng lượng kép |
| 198 | Bisphosphonates | /bɪsˈfɒsfəˌneɪts/ | Bisphosphonat |
| 199 | Nonalcoholic steatohepatitis (NASH) | /ˌnɒnˌælkəˈhɒlɪk ˌstiətoʊˌhɛpəˈtaɪtɪs/ | Viêm gan nhiễm mỡ không do rượu |
| 200 | Pregnancy category | /ˈprɛgnənsi ˈkætəˌgɔri/ | Phân loại thuốc cho thai kỳ |
