[Sách dịch] Sổ tay Bệnh Gan – Handbook of Liver Disease – (C) NXB Elsevier, 2022
Dịch và chú giải: Ths.Bs. Lê Đình Sáng
Chương 18. Bệnh Nhiễm Sắc Tố Sắt Mô
Hemochromatosis
Nicholas J. Procaccini MD, JD, MS and Kris V. Kowdley MD, FACP
Handbook of Liver Disease, Chapter 18, 243-252
NHỮNG ĐIỂM CHÍNH
|
Dịch tễ học và Di truyền học
- Ở người da trắng, khoảng 1 trên 200 đến 1 trên 250 người là đồng hợp tử, và 1 trên 8 đến 1 trên 12 người là dị hợp tử cho đột biến C282Y của gen HFE, đây là khiếm khuyết di truyền phổ biến nhất trong bệnh HH.
- Độ biểu hiện lâm sàng của đột biến C282Y là thấp (Bảng 18.1).
- Bệnh HH liên quan đến các đột biến khác như HH ở tuổi vị thành niên và các đột biến của gen vận chuyển ferroportin là hiếm gặp (Bảng 18.2).
Phân loại
BỆNH NHIỄM SẮC TỐ SẮT MÔ DO GEN HFE (LOẠI 1)
- Gen HFE là một gen giống lớp I của phức hợp hòa hợp mô chính (major histocompatibility complex – MHC) và nằm trên nhánh ngắn của nhiễm sắc thể số 6, ở đầu tận cùng so với locus hòa hợp mô lớp I A3 của MHC.
- Đột biến đồng hợp tử C282Y chiếm khoảng 85% đến 90% các cá nhân mắc bệnh HH.
- Tình trạng đồng hợp tử cho H63D, một đột biến khác của gen HFE, có liên quan đến tình trạng quá tải sắt ít nghiêm trọng hơn và hiếm khi dẫn đến biểu hiện kiểu hình lâm sàng của bệnh HH.
- Tình trạng dị hợp tử kép C282Y/H63D chiếm 5% đến 7% các trường hợp HH có biểu hiện lâm sàng.
- Gen HFE được biểu hiện chủ yếu ở các tế bào tuyến (crypt cells) của tá tràng, nơi nó tương tác với thụ thể transferrin và beta-2 microglobulin.
- Hepcidin là một protein được cho là có vai trò trong chuyển hóa sắt bằng cách liên kết với ferroportin và làm giảm xuất khẩu sắt từ các tế bào biểu mô ruột (enterocytes) và đại thực bào. Trong bệnh HH, sự biểu hiện của hepcidin giảm, dẫn đến tăng hấp thu sắt từ tế bào biểu mô ruột và tăng giải phóng sắt từ đại thực bào.
- Có sự khác biệt về độ biểu hiện và biểu hiện lâm sàng ở những người đồng hợp tử C282Y. Ít hơn 10% sẽ phát triển bệnh ở các cơ quan đích.
- Ảnh hưởng của các gen điều chỉnh (modifying genes) cũng được giả thuyết là góp phần vào sự biểu hiện bệnh theo kiểu hình khác nhau.
Bảng 18.1 Độ biểu hiện của đột biến C282Y
| Loại độ biểu hiện | Định nghĩa | Tần suất ở người đồng hợp tử C282Y (%) |
|---|---|---|
| Nữ Nam | ||
| Sinh hóa | Tăng độ bão hòa transferrin và nồng độ ferritin huyết thanh | 50 75 |
| Lâm sàng | Ung thư biểu mô tế bào gan, xơ hóa hoặc xơ gan, viêm khớp bàn ngón tay, hoặc tăng nồng độ aminotransferase huyết thanh | Hiếm 28 |
Bảng 18.2 Các gen bị đột biến trong từng loại bệnh nhiễm sắc tố sắt mô di truyền
| Loại | Tên thường gọi | Gen (và sản phẩm gen) |
|---|---|---|
| 1 | Bệnh nhiễm sắc tố sắt mô kinh điển | HFE (HFE) |
| 2A | Bệnh nhiễm sắc tố sắt mô vị thành niên | HFE2 (hemojuvelin) |
| 2B | Bệnh nhiễm sắc tố sắt mô vị thành niên | HAMP (hepcidin) |
| 3 | Bệnh nhiễm sắc tố sắt mô liên quan Tfr2 | Tfr2 (thụ thể transferrin-2) |
| 4 | Quá tải sắt liên quan Ferroportin | SLC40A1 (ferroportin) |
BỆNH NHIỄM SẮC TỐ SẮT MÔ KHÔNG DO GEN HFE
- Bệnh HH liên quan đến các đột biến ở các gen khác là hiếm gặp (xem Bảng 18.2).
- Không giống như HH do HFE, có rất nhiều đột biến khác nhau liên quan đến từng loại HH không do HFE.
- Bệnh HH loại 2 (bệnh nhiễm sắc tố sắt mô vị thành niên) có liên quan đến tình trạng quá tải sắt và tổn thương mô nghiêm trọng hơn, phát triển sớm hơn so với HH do HFE.
- Bệnh HH loại 3 có các biểu hiện lâm sàng tương tự như HH do HFE.
- Bệnh HH loại 4 có các biểu hiện lâm sàng và mô học riêng biệt.
- Độ bão hòa transferrin huyết thanh có thể bình thường với nồng độ ferritin huyết thanh tăng.
- Sắt được lắng đọng chủ yếu trong các tế bào của hệ võng nội mô trong gan.
- Bệnh nhân có thể dung nạp kém với liệu pháp trích máu tĩnh mạch.
- Tất cả các dạng HH đều được di truyền theo kiểu lặn trên nhiễm sắc thể thường, ngoại trừ HH loại 4, được di truyền theo kiểu trội trên nhiễm sắc thể thường.
Sinh lý bệnh
HẤP THU SẮT
- Sắt trong chế độ ăn được hấp thu chủ yếu ở các tế bào tuyến của tá tràng. Chỉ khoảng 10% sắt trong chế độ ăn được hấp thu ở người có sinh lý bình thường, với sự hấp thu được điều hòa theo lượng sắt dự trữ của cơ thể.
- Ở người bình thường, sự hấp thu sắt được điều hòa giảm khi độ bão hòa transferrin huyết thanh cao và sau khi ăn nhiều sắt.
- Ở những người mắc bệnh HH, sự hấp thu sắt tăng lên và không được điều hòa giảm như ở người bình thường, do đó dẫn đến cân bằng sắt dương tính.
- Nồng độ ferritin và mRNA ferritin ở niêm mạc ruột non giảm một cách không phù hợp trong bệnh HH; kiểu hình này thường liên quan đến tình trạng thiếu sắt và được điều chỉnh bằng cách bổ sung sắt.
- Sự hấp thu sắt bao gồm việc lấy sắt từ lòng ruột vào tế bào biểu mô ruột và sau đó chuyển từ tế bào biểu mô ruột vào huyết tương. Cả hai quá trình này đều tăng trong bệnh HH. Các nghiên cứu động học in vivo chỉ ra rằng sự vận chuyển sắt tăng từ phía màng đáy của ruột vào huyết tương là động lực chính làm tăng hấp thu sắt.
- Ảnh hưởng của đột biến HFE được cho là qua trung gian bởi sự thiếu biểu hiện đầy đủ của hepcidin trong gan để đáp ứng với lượng sắt dự trữ ở mức tế bào gan; điều này lần lượt dẫn đến thất bại trong việc ức chế hấp thu sắt ở tá tràng, gây ra tình trạng quá tải sắt.
LẮNG ĐỌNG SẮT Ở NHU MÔ TRONG BỆNH NHIỄM SẮC TỐ SẮT MÔ DI TRUYỀN LOẠI 1 ĐẾN 3
- Sắt lắng đọng ở nhiều cơ quan bao gồm gan, tim, tụy, khớp, da, tuyến sinh dục và các cơ quan nội tiết khác.
- Vị trí lắng đọng sắt chính trong bệnh HH là gan, phù hợp với vai trò của gan là cơ quan dự trữ sắt chính.
- Sắt được lắng đọng chủ yếu trong tế bào gan dưới dạng ferritin và sau đó cũng dưới dạng hemosiderin, với gradient giảm dần của sự hấp thu sắt từ vùng quanh khoảng cửa (vùng 1) đến vùng quanh tĩnh mạch trung tâm (vùng 3) của tiểu thùy gan.
- Ở giai đoạn muộn của bệnh, sắt có thể lắng đọng trong tế bào Kupffer và tế bào ống mật.
- Sự bão hòa của transferrin huyết thanh đi trước sự tích tụ sắt ở gan và chịu trách nhiệm cho sự gia tăng ban đầu trong việc cung cấp sắt đến các mô.
- Sau đó, sắt không gắn với transferrin có thể đóng vai trò trong việc cung cấp và gây độc tính của sắt.
- Cũng có thể có một khiếm khuyết trong việc lưu trữ sắt ở các tế bào hệ võng nội mô.
ẢNH HƯỞNG CỦA VIỆC UỐNG RƯỢU
- Uống rượu quá mức có liên quan đến nồng độ sắt huyết thanh cao hơn, mức độ nghiêm trọng của bệnh lâm sàng tăng lên, và tăng nguy cơ xơ gan và ung thư biểu mô tế bào gan (hepatocellular carcinoma – HCC) ở những người đồng hợp tử C282Y.
- Xơ hóa gan và xơ gan xảy ra ở độ tuổi sớm hơn và ở mức độ sắt gan thấp hơn ở những người này.
- Tương tự, bệnh HH có thể làm trầm trọng thêm sự phát triển của bệnh gan do rượu (alcoholic liver disease – ALD), có khả năng thông qua sự hình thành quá mức các gốc tự do khi có tình trạng quá tải sắt.
ẢNH HƯỞNG CỦA BỆNH GAN NHIỄM MỠ KHÔNG DO RƯỢU
- Tương tự như ALD, bệnh gan nhiễm mỡ không do rượu (nonalcoholic fatty liver disease – NAFLD) cùng tồn tại có liên quan đến việc tăng nồng độ sắt huyết thanh và độ bão hòa transferrin.
- Điều này có thể đẩy nhanh quá trình tiến triển của xơ hóa trong bệnh HH.
- Bệnh nhân bị viêm gan nhiễm mỡ không do rượu (nonalcoholic steatohepatitis – NASH) với chỉ số sắt cao hơn có điểm hoạt động NASH cao hơn và tiến triển xơ hóa nhanh hơn (xem Chương 9).
TỔN THƯƠNG GAN
- Sắt dư thừa có thể gây tổn thương gan hoặc thúc đẩy xơ hóa gan qua nhiều cơ chế.
- Sắt có thể xúc tác cho sự hình thành các gốc tự do, có thể làm hỏng các bào quan của tế bào.
- Sắt có thể làm hỏng DNA trực tiếp và do đó dẫn đến đột biến và gây ung thư.
- Sắt có thể kích thích sự phát triển của xơ hóa gan bằng cách tăng tổng hợp collagen.
- Uống rượu quá mức có thể gây tổn thương gan thông qua tổn thương mô được đẩy nhanh qua trung gian các cơ chế oxy hóa và không oxy hóa.
- Bệnh gan trong HH được đặc trưng bởi xơ hóa tiến triển, mặc dù mô học đặc trưng không cho thấy tình trạng viêm đáng kể.
- Sự hiện diện của viêm gan (những thay đổi viêm) có thể gợi ý một bệnh nhiễm virus cùng tồn tại, NASH, hoặc ALD.
- Xơ gan và HCC phát triển với tình trạng quá tải sắt kéo dài; tuy nhiên, HCC không có xơ gan là hiếm gặp.
- Nồng độ sắt trong gan cao hơn làm tăng nguy cơ xơ hóa và cuối cùng là xơ gan.
- Nguy cơ xơ hóa và xơ gan tăng lên khi nam giới đến tuổi 40 và ở phụ nữ trên 50 tuổi, mặc dù có thể sớm hơn nếu có các yếu tố cùng tồn tại (ví dụ, viêm gan virus, NASH, uống rượu quá mức).
Đặc điểm lâm sàng
- Trước năm 1960, bệnh HH thường được nhận biết trên lâm sàng ở giai đoạn muộn với tổn thương cơ quan đích bao gồm “đái tháo đường nhiễm đồng”, viêm khớp, bệnh gan và suy tim.
- Với nhận thức ngày càng tăng về bệnh, chẩn đoán hiện nay thường được thực hiện ở giai đoạn không có triệu chứng thông qua các xét nghiệm.
- Chẩn đoán bệnh HH không triệu chứng thường được thực hiện sau khi phát hiện các chỉ số sắt huyết thanh bất thường trong các tình huống lâm sàng sau:
- Tăng nồng độ aminotransferase huyết thanh
- Tăng dự trữ sắt
- Tầm soát gia đình hoặc quần thể
- Khi chẩn đoán được thực hiện sau khi có triệu chứng, các triệu chứng phổ biến nhất hiện nay tại thời điểm chẩn đoán bao gồm:
- Yếu, mệt mỏi, hoặc lơ mơ
- Đau khớp hoặc viêm khớp (phụ nữ thường gặp hơn nam giới)
- Đau không đặc hiệu ở hạ sườn phải
- Giảm ham muốn tình dục hoặc liệt dương (nam giới)
- Các biểu hiện khác bao gồm:
- Tăng sắc tố da
- Đái tháo đường
- Vô kinh (phụ nữ)
- Bệnh gan
- Suy tim
BỆNH GAN
- Tăng nồng độ sắt trong gan có ở những bệnh nhân HH do HFE và có nồng độ ferritin huyết thanh tăng.
- Bệnh gan là dạng tổn thương cơ quan đích phổ biến nhất được thấy trong bệnh HH.
- Mức độ nghiêm trọng của bệnh gan thường tương quan với mức độ nghiêm trọng của tình trạng quá tải sắt ở gan, mặc dù các bệnh gan cùng tồn tại có thể làm tăng tổn thương gan.
- Mức độ tăng aminotransferase huyết thanh thường ở mức độ nhẹ, và nồng độ aminotransferase huyết thanh thường trở về bình thường sau khi lượng sắt dư thừa được loại bỏ.
- Nếu việc thải sắt được thực hiện và duy trì trước khi phát triển xơ hóa hoặc xơ gan, các biến chứng gan tiếp theo sẽ được ngăn chặn.
- Một khi xơ gan đã phát triển, bệnh nhân vẫn có nguy cơ cao bị HCC ngay cả sau khi đã thải sắt.
- Tỷ lệ mắc viêm gan B và C mạn tính, NASH, và uống rượu quá mức đã được báo cáo tăng ở những bệnh nhân có kiểu hình HH.
- Sử dụng rượu quá mức có liên quan đến tăng tỷ lệ bệnh tật ở bệnh nhân HH.
BỆNH TIM
- Bệnh HH (đặc biệt là loại 2) có thể liên quan đến rối loạn chức năng tim và loạn nhịp tim.
- Rối loạn chức năng tim có thể biểu hiện dưới dạng bệnh cơ tim hạn chế hoặc bệnh cơ tim giãn.
- Loạn nhịp nhĩ và thất có thể xảy ra.
- Tổn thương tim xảy ra tương đối muộn trong quá trình tiến triển của bệnh HH do HFE, và việc thải sắt trước khi phát triển bệnh cơ tim giãn giúp cải thiện chức năng tim. Rối loạn chức năng tim đã trở nên ít phổ biến hơn với việc chẩn đoán và điều trị sớm hơn bệnh HH.
- Bệnh cơ tim là nguyên nhân chính gây ra bệnh suất và tử suất sau phẫu thuật ghép gan cho bệnh HH.
ĐÁI THÁO ĐƯỜNG
- Đái tháo đường có lẽ là kết quả của sự lắng đọng sắt trong tuyến tụy.
- Nó có thể liên quan đến việc tăng nồng độ insulin huyết tương, một phát hiện cho thấy sự đề kháng insulin ngoại biên (loại 2), đặc biệt khi kết hợp với bệnh gan.
BỆNH KHỚP
- Bệnh khớp là một nguyên nhân chính gây ra bệnh suất.
- Nó đặc trưng bởi việc ảnh hưởng đến các khớp bàn ngón tay thứ hai và thứ ba; các khớp bàn ngón tay khác và khớp cổ tay cũng thường bị ảnh hưởng. Các khớp ít bị ảnh hưởng hơn bao gồm vai, hông, gối và mắt cá chân.
- Các đặc điểm bệnh học bao gồm hẹp khe khớp, vôi hóa sụn khớp (chondrocalcinosis), hình thành nang dưới sụn và loãng xương (osteopenia).
- Bệnh khớp không cải thiện khi thải sắt.
NHIỄM TRÙNG
- Bệnh nhân HH có nguy cơ cao bị nhiễm trùng do vi khuẩn, virus và nấm.
- Cơ chế làm tăng nguy cơ nhiễm trùng chưa được biết rõ nhưng được giả thuyết là liên quan đến sự suy giảm các phản ứng miễn dịch bẩm sinh và mắc phải qua trung gian sắt.
- Nhiễm trùng có thể do các vi khuẩn hiếm gặp sau đây gây ra:
- Vibrio vulnificus
- Yersinia enterocolitica
- Yersinia pseudotuberculosis
- Listeria monocytogenes
Diễn tiến tự nhiên và Tiên lượng
- Bệnh gan tiến triển chậm nhưng thường ở mức độ nhẹ (trừ khi có viêm gan virus hoặc lạm dụng rượu kèm theo) khi nồng độ sắt trong gan < 200 μmol/g trọng lượng khô của gan.
- Mất bù gan và HCC là những biểu hiện cơ quan đích phổ biến nhất của bệnh HH và chiếm 60% tỷ lệ tử vong liên quan đến quá tải sắt.
- Bệnh nhân HH và xơ gan có nguy cơ bị HCC tăng đáng kể (gấp 20 đến 200 lần) và nên được tầm soát HCC định kỳ.
- Nguy cơ tăng ung thư biểu mô đường mật-tế bào gan hỗn hợp cũng đã được báo cáo.
- Có lo ngại về nguy cơ tăng các bệnh ung thư không liên quan đến gan mật trong bệnh HH, nhưng dữ liệu còn mâu thuẫn.
- Một số biểu hiện cải thiện khi thải sắt (khó chịu, mệt mỏi, tăng sắc tố da, đái tháo đường, đau bụng, rối loạn chức năng tim, giảm năng lượng, tăng nồng độ aminotransferase huyết thanh, xơ hóa gan không do xơ gan), trong khi những biểu hiện khác thì không (bệnh khớp, suy sinh dục, xơ gan).
- Bệnh nhân không bị xơ gan hoặc đái tháo đường có tuổi thọ bình thường nếu việc thải sắt được duy trì.
- Bệnh nhân bị xơ gan hoặc đái tháo đường có tuổi thọ giảm đáng kể, nhưng tiên lượng được cải thiện sau khi điều trị thải sắt.
- Bệnh nhân HH có thể cần ghép gan do bệnh gan giai đoạn cuối hoặc HCC.
- Ghép gan ở bệnh nhân HH có liên quan đến nguy cơ tăng nhiễm trùng, đặc biệt là nhiễm nấm, các biến cố tim mạch và giảm tỷ lệ sống còn.
- Bệnh HH đã được báo cáo là có liên quan đến kết quả sau ghép thậm chí còn tồi tệ hơn so với các nguyên nhân khác gây quá tải sắt; tuy nhiên, kết quả ghép gan dường như đã được cải thiện.
Chẩn đoán
NGHI NGỜ LÂM SÀNG VÀ CÁC XÉT NGHIỆM
- Bệnh HH nên được xem xét trong các tình trạng sau đây (Hình 18.1):
- Bệnh khớp thoái hóa
- Gan to hoặc bệnh gan không rõ nguyên nhân
- Suy sinh dục không rõ nguyên nhân
- Tăng độ bão hòa transferrin hoặc nồng độ ferritin huyết thanh
- Tăng nồng độ aminotransferase huyết thanh
- Độ bão hòa transferrin và nồng độ ferritin huyết thanh là các xét nghiệm ban đầu nếu nghi ngờ bệnh HH.
- Độ bão hòa transferrin huyết thanh nhạy và đặc hiệu hơn nồng độ ferritin huyết thanh đối với bệnh HH.
- Tăng độ bão hòa transferrin là biểu hiện sớm nhất của bệnh HH.
- Ferritin huyết thanh là một chất phản ứng pha cấp và có thể tăng trong các tình trạng viêm và các bệnh gan mạn tính khác (ví dụ, NASH, viêm gan C mạn tính, ALD).
- Sự thay đổi theo nhịp ngày đêm và sau bữa ăn của độ bão hòa transferrin có thể là một nguồn gây sai số xét nghiệm; do đó bệnh nhân nên nhịn ăn trước khi xét nghiệm.
- Độ bão hòa transferrin trên 45% cần được đánh giá thêm để tìm bệnh HH.
- Tăng ferritin huyết thanh đơn độc với độ bão hòa transferrin bình thường có thể chỉ ra bệnh HH loại 4, đặc biệt ở những bệnh nhân không phải người da trắng.
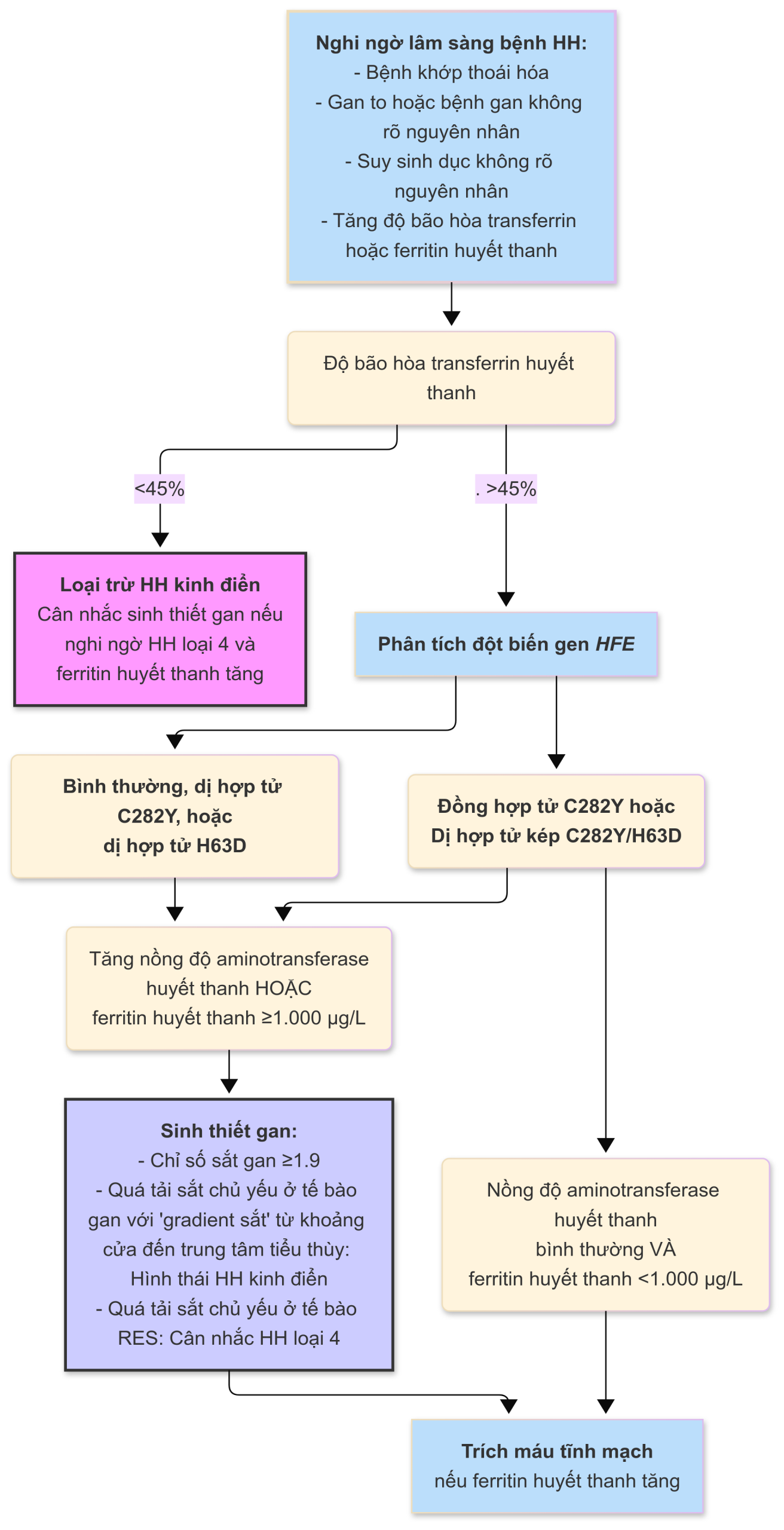
Hình 18.1 Sơ đồ chẩn đoán và điều trị bệnh nhiễm sắc tố sắt mô di truyền (HH)
Chú thích: HH, Bệnh nhiễm sắc tố sắt mô di truyền; RES, Hệ võng nội mô.
XÉT NGHIỆM KIỂU GEN
- Phân tích đột biến gen HFE nên được thực hiện ở tất cả những người có độ bão hòa transferrin tăng kéo dài, đặc biệt nếu nồng độ ferritin huyết thanh cũng tăng.
- Sự hiện diện của tình trạng đồng hợp tử C282Y hoặc dị hợp tử kép C282Y/H63D xác nhận chẩn đoán HH do HFE trong bối cảnh lâm sàng phù hợp.
- Các xét nghiệm di truyền cho bệnh HH không do HFE hiện không có sẵn để sử dụng trên lâm sàng.
Bảng 18.3 Các xét nghiệm được sử dụng để đánh giá tình trạng quá tải sắt ở gan trong mẫu sinh thiết gan
| Xét nghiệm | Bình luận |
|---|---|
| Chỉ số sắt gan (nồng độ sắt gan tính bằng μmol/g trọng lượng khô chia cho tuổi của bệnh nhân tính bằng năm) được đo trong mô tươi hoặc mô được bảo quản | Chỉ số sắt gan ≥1.9 thường được quan sát thấy ở những bệnh nhân có kiểu hình HH, nhưng ở nhiều người đồng hợp tử C282Y, chỉ số này <1.9. |
| Nhuộm tìm sắt ở gan (nhuộm xanh Phổ Perls) | Việc nhuộm tìm sắt ở gan rất quan trọng vì sự thay đổi do lấy mẫu có thể cho chỉ số sắt gan thấp. |
Chú thích: HH, Bệnh nhiễm sắc tố sắt mô di truyền.
SINH THIẾT GAN
- Các chỉ định hiện tại cho sinh thiết gan còn hạn chế.
- Để chẩn đoán khi xét nghiệm kiểu gen HFE âm tính ở bệnh nhân nghi ngờ mắc bệnh HH không do HFE.
- Để phân giai đoạn (có hoặc không có xơ gan) ở bệnh nhân đã xác nhận mắc bệnh HH do HFE khi nồng độ ferritin huyết thanh vượt quá 1000 μg/L hoặc khi nồng độ alanine hoặc aspartate aminotransferase huyết thanh tăng.
- Sinh thiết gan để chẩn đoán bao gồm hai nghiên cứu (Bảng 18.3): Chỉ số sắt gan và nhuộm tìm sắt ở gan.
- Sinh thiết gan để phân giai đoạn rất quan trọng vì những lý do sau:
- Mô bệnh học vẫn là tiêu chuẩn vàng để xác định sự hiện diện của xơ gan khi không có bằng chứng rõ ràng như tăng áp lực tĩnh mạch cửa.
- Sự hiện diện của xơ gan có liên quan đến tăng nguy cơ tử vong và HCC.
- Việc biết có hay không có xơ gan có thể ảnh hưởng đến việc quản lý (ví dụ, bệnh nhân xơ gan cần được tầm soát HCC).
CÁC XÉT NGHIỆM KHÁC
- Chụp cộng hưởng từ có thể ước tính lượng sắt trong gan một cách định lượng theo phương pháp không xâm lấn.
- Trích máu tĩnh mạch định lượng rất hữu ích để ước tính tình trạng quá tải sắt khi không cần sinh thiết gan. Mỗi lần trích máu thường lấy đi 500 mL máu (khoảng 250 mg sắt); nhu cầu loại bỏ 4 g sắt trở lên trước khi bắt đầu tình trạng tạo hồng cầu giới hạn do sắt kèm theo thiếu máu cho thấy sự hiện diện của tình trạng quá tải sắt đáng kể.
Chẩn đoán phân biệt
- Quá tải sắt thứ phát có thể xảy ra trong các tình huống sau:
- Tăng chu chuyển hồng cầu (ví dụ, các rối loạn tạo hồng cầu không hiệu quả)
- Truyền máu lặp lại
- Sự kết hợp của các yếu tố này
- Các nguyên nhân chính gây quá tải sắt thứ phát có thể được phân loại như sau: a. Các bệnh thiếu máu gây quá tải sắt có hoặc không có truyền máu * Thalassemia thể nặng * Thiếu máu nguyên hồng cầu sắt * Các bệnh thiếu máu tan máu mạn tính b. Quá tải sắt do chế độ ăn (hiếm gặp) c. Quá tải sắt liên quan đến bệnh gan mạn tính bao gồm * ALD * Viêm gan B và C mạn tính * NAFLD d. Các nguyên nhân khác * Porphyria cutanea tarda * Quá tải sắt ở người châu Phi * Bệnh nhiễm sắc tố sắt mô sơ sinh * Bệnh không có ceruloplasmin trong máu (Aceruloplasminemia) * Bệnh không có transferrin trong máu (Atransferrinemia)
- Các đặc điểm sau đây hữu ích trong việc phân biệt quá tải sắt thứ phát liên quan đến các bệnh thiếu máu mạn tính với bệnh HH:
- Sinh thiết gan trong quá tải sắt thứ phát cho thấy tình trạng quá tải sắt chủ yếu ở tế bào Kupffer và các tế bào hệ võng nội mô khác, với ít sắt trong tế bào gan. “Gradient sắt” từ quanh khoảng cửa đến quanh tĩnh mạch trung tâm cũng không được quan sát thấy trong các tình trạng này; tuy nhiên, một kiểu hình tương tự có thể được quan sát thấy trong bệnh HH loại 4.
- Quá tải sắt thứ phát thường nhẹ hơn (1+ đến 2+).
- Trích máu tĩnh mạch định lượng cho thấy sự khởi đầu của tình trạng tạo hồng cầu giới hạn do sắt kèm theo thiếu máu trước khi loại bỏ được 4 g sắt trở lên.
Điều trị
- Thải sắt bằng cách trích máu tĩnh mạch hàng loạt vẫn là nền tảng của liệu pháp điều trị bệnh HH. Phác đồ đề xuất cho việc trích máu tĩnh mạch hàng loạt:
- Trích máu được thực hiện, lấy đi 500 mL máu (khoảng 250 mg sắt) hàng tuần hoặc hai tuần một lần cho đến khi ferritin huyết thanh giảm xuống còn 50 đến 100 μg/L.
- Nên kiểm tra giá trị hematocrit hoặc hemoglobin trước mỗi lần trích máu, và nên đánh giá nồng độ ferritin huyết thanh mỗi 3 tháng (sau mỗi 10 đến 12 lần trích máu).
- Nếu giá trị hematocrit <32%, nên hoãn trích máu và giảm tần suất xuống còn hai tuần một lần.
- Khi nồng độ ferritin huyết thanh <50 μg/L, nên kiểm tra nó mỗi 3 đến 4 tháng, với việc trích máu được lặp lại khi cần thiết để duy trì nồng độ ferritin huyết thanh ở mức 50 đến 100 μg/L.
- Tần suất trích máu duy trì cần thiết phụ thuộc vào tốc độ tích tụ sắt và thường cần thực hiện mỗi 2 đến 4 tháng một lần.
- Các biện pháp phòng ngừa trong quá trình trích máu:
- Nên ngăn ngừa thiếu máu bằng cách theo dõi giá trị hematocrit trước mỗi lần trích máu và đảm bảo cung cấp đủ protein, vitamin B12 và folate trong chế độ ăn.
- Nên tránh dùng liều cao axit ascorbic và axit citric, cũng như chế độ ăn giàu sắt. Tiêu thụ thịt đỏ ở mức độ vừa phải là được phép.
- Nên tránh uống rượu trong khi đang tiến hành liệu pháp thải sắt.
- Trong quá trình trích máu duy trì, việc ức chế axit dạ dày bằng thuốc ức chế bơm proton có thể cho phép giảm tần suất trích máu, có lẽ bằng cách giảm hấp thu sắt ở tá tràng.
- Do tăng tính nhạy cảm với nhiễm trùng V. vulnificus, bệnh nhân nên tránh ăn hải sản sống và để vết thương hở tiếp xúc với nước biển ven bờ ấm. Tính nhạy cảm với nhiễm trùng V. vulnificus không hết sau khi điều trị thải sắt.
- Các thuốc thải sắt (deferoxamine, deferiprone, deferasirox) kém hiệu quả hơn và đắt hơn so với trích máu tĩnh mạch và có liên quan đến các tác dụng phụ. Những loại thuốc này chỉ được sử dụng ở những bệnh nhân bị thiếu máu hoặc những người không thể dung nạp trích máu tĩnh mạch.
Tầm soát
TẦM SOÁT GIA ĐÌNH
- Tất cả những người thân cấp một của bệnh nhân đã được xác nhận mắc bệnh HH nên được tầm soát bệnh HH.
- Phân tích đột biến gen HFE hoặc xét nghiệm độ bão hòa transferrin lúc đói và ferritin được đề xuất để tầm soát.
- Những người thân của bệnh nhân mắc bệnh HH do HFE có kết quả âm tính với đột biến HFE không cần xét nghiệm thêm.
- Những người thân có kết quả dương tính với đột biến HFE nên được theo dõi bằng nồng độ ferritin huyết thanh hàng năm, và nên bắt đầu trích máu tĩnh mạch khi thích hợp.
TẦM SOÁT QUẦN THỂ
- Tầm soát quần thể đối với bệnh HH thường không được khuyến nghị.
- Một số mô hình kinh tế đã cho thấy việc tầm soát quần thể không hiệu quả về mặt chi phí.
- Tầm soát kiểu hình (độ bão hòa transferrin) có thể được xem xét ở các quần thể có nguy cơ cao, nhưng kết quả âm tính ở người trẻ tuổi nên được diễn giải một cách thận trọng vì độ bão hòa transferrin có thể tăng lên theo tuổi tác.
TÀI LIỆU THAM KHẢO
- Adams PC, Barton JC. Haemochromatosis. Lancet. 2007;370:1855-1860.
- Allen KJ, Gurrin LC, Constantine CC, et al. Iron-overload-related disease in HFE hereditary hemochromatosis. N Engl J Med. 2008;358:221-230.
- Bacon BR, Adams PC, Kowdley KV, et al. Diagnosis and management of hemochromatosis: 2011 practice guidelines by the American Association for the Study of Liver Diseases. Hepatology. 2011;54:328-343.
- Fix OK, Kowdley KV. Hereditary hemochromatosis. Minerva Med. 2008;99:605-617.
- Franchini M. Hereditary iron overload: update on pathophysiology, diagnosis, and treatment. Am J Hematol. 2006;81:202-209.
- Kowdley KV, Brandhagen DJ, Gish RG, et al. Survival after liver transplantation in patients with hepatic iron overload: the national hemochromatosis transplant registry. Gastroenterology. 2005;129:494-503.
- Olynyk JK, Trinder D, Ramm GA, et al. Hereditary hemochromatosis in the post-HFE era. Hepatology. 2008;48:991-1001.
- Online Mendelian Inheritance in Man (OMIM). Johns Hopkins University, Baltimore. MIM No. 235200. 2010 Jan 7.
- Pietrangelo A. Hemochromatosis: an endocrine liver disease. Hepatology. 2007;46:1291-1301.
- Weiss G. Genetic mechanisms and modifying factors in hereditary hemochromatosis. Nat Rev Gastroenterol Hepatol. 2010;7:50-58.
Bảng chú giải thuật ngữ Y học Anh Việt
| STT | Thuật ngữ tiếng Anh | Phiên âm IPA | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Hemochromatosis | /ˌhiːməʊˌkroʊməˈtoʊsɪs/ | Bệnh nhiễm sắc tố sắt mô |
| 2 | Iron-mediated | /ˈaɪərn ˈmiːdieɪtɪd/ | Qua trung gian sắt |
| 3 | Tissue injury | /ˈtɪʃuː ˈɪndʒəri/ | Tổn thương mô |
| 4 | Intestinal iron absorption | /ɪnˈtɛstɪnl ˈaɪərn əbˈsɔːrpʃn/ | Hấp thu sắt ở ruột |
| 5 | Hereditary hemochromatosis (HH) | /həˈrɛdɪˌtɛri ˌhiːməʊˌkroʊməˈtoʊsɪs/ | Bệnh nhiễm sắc tố sắt mô di truyền |
| 6 | Autosomal recessive inheritance | /ˌɔːtəˈsoʊməl rɪˈsɛsɪv ɪnˈhɛrɪtəns/ | Di truyền lặn trên nhiễm sắc thể thường |
| 7 | HFE gene | /eɪtʃ ɛf iː dʒiːn/ | Gen HFE |
| 8 | Hemojuvelin | /ˌhiːmoʊˈdʒuːvəlɪn/ | Hemojuvelin |
| 9 | Hepcidin | /hɛpˈsaɪdɪn/ | Hepcidin |
| 10 | Transferrin receptor 2 | /trænsˈfɛrɪn rɪˈsɛptər tuː/ | Thụ thể transferrin 2 |
| 11 | Ferroportin | /ˌfɛroʊˈpɔːrtɪn/ | Ferroportin |
| 12 | Caucasian population | /kɔːˈkeɪʒən ˌpɒpjəˈleɪʃn/ | Quần thể người da trắng |
| 13 | Clinical penetrance | /ˈklɪnɪkl ˈpɛnɪtrəns/ | Độ biểu hiện lâm sàng |
| 14 | Homozygous | /ˌhoʊmoʊˈzaɪɡəs/ | Đồng hợp tử |
| 15 | Phenotype | /ˈfiːnoʊˌtaɪp/ | Kiểu hình |
| 16 | Cirrhosis | /səˈroʊsɪs/ | Xơ gan |
| 17 | Diabetes mellitus | /ˌdaɪəˈbiːtiːz ˈmɛlɪtəs/ | Đái tháo đường |
| 18 | Cardiomyopathy | /ˌkɑːrdioʊmaɪˈɒpəθi/ | Bệnh cơ tim |
| 19 | Iron depletion therapy | /ˈaɪərn dɪˈpliːʃn ˈθɛrəpi/ | Liệu pháp thải sắt |
| 20 | Phlebotomy | /fləˈbɒtəmi/ | Trích máu tĩnh mạch |
| 21 | Life expectancy | /laɪf ɪkˈspɛktənsi/ | Tuổi thọ |
| 22 | Biochemical markers | /ˌbaɪoʊˈkɛmɪkl ˈmɑːrkərz/ | Các chỉ số sinh hóa |
| 23 | Serum transferrin saturation | /ˈsɪərəm trænsˈfɛrɪn ˌsæʧəˈreɪʃn/ | Độ bão hòa transferrin huyết thanh |
| 24 | Ferritin | /ˈfɛrɪtɪn/ | Ferritin |
| 25 | HFE gene mutation analysis | /eɪtʃ ɛf iː dʒiːn mjuːˈteɪʃn əˈnælɪsɪs/ | Phân tích đột biến gen HFE |
| 26 | Liver biopsy | /ˈlɪvər ˈbaɪɒpsi/ | Sinh thiết gan |
| 27 | Staging | /ˈsteɪdʒɪŋ/ | Phân giai đoạn |
| 28 | Epidemiology | /ˌɛpɪˌdiːmiˈɒlədʒi/ | Dịch tễ học |
| 29 | Genetics | /dʒəˈnɛtɪks/ | Di truyền học |
| 30 | Heterozygous | /ˌhɛtəroʊˈzaɪɡəs/ | Dị hợp tử |
| 31 | Genetic defect | /dʒəˈnɛtɪk ˈdiːfɛkt/ | Khiếm khuyết di truyền |
| 32 | Juvenile hemochromatosis | /ˈdʒuːvənaɪl ˌhiːməʊˌkroʊməˈtoʊsɪs/ | Bệnh nhiễm sắc tố sắt mô vị thành niên |
| 33 | Classification | /ˌklæsɪfɪˈkeɪʃn/ | Phân loại |
| 34 | Major histocompatibility complex (MHC) | /ˈmeɪdʒər ˌhɪstoʊkəmˌpætəˈbɪlɪti ˈkɒmplɛks/ | Phức hợp hòa hợp mô chính |
| 35 | Chromosome | /ˈkroʊməˌsoʊm/ | Nhiễm sắc thể |
| 36 | Telomeric | /ˌtɛləˈmɛrɪk/ | Ở đầu tận cùng |
| 37 | Locus | /ˈloʊkəs/ | Locus (vị trí gen) |
| 38 | Compound heterozygosity | /ˈkɒmpaʊnd ˌhɛtəroʊzaɪˈɡɒsɪti/ | Tình trạng dị hợp tử kép |
| 39 | Crypt cells | /krɪpt sɛlz/ | Tế bào tuyến |
| 40 | Duodenum | /ˌdjuːəˈdiːnəm/ | Tá tràng |
| 41 | Beta-2 microglobulin | /ˈbeɪtə tuː ˌmaɪkroʊˈɡlɒbjəlɪn/ | Beta-2 microglobulin |
| 42 | Iron metabolism | /ˈaɪərn məˈtæbəlɪzəm/ | Chuyển hóa sắt |
| 43 | Enterocytes | /ˈɛntərəˌsaɪts/ | Tế bào biểu mô ruột |
| 44 | Macrophages | /ˈmækroʊˌfeɪdʒɪz/ | Đại thực bào |
| 45 | End-organ disease | /ɛnd ˈɔːrɡən dɪˈziːz/ | Bệnh ở cơ quan đích |
| 46 | Modifying genes | /ˈmɒdɪfaɪɪŋ dʒiːnz/ | Gen điều chỉnh |
| 47 | Histologic manifestations | /ˌhɪstəˈlɒdʒɪk ˌmænɪfɛˈsteɪʃənz/ | Biểu hiện mô học |
| 48 | Reticuloendothelial system | /rɪˌtɪkjəloʊˌɛndoʊˈθiːliəl ˈsɪstəm/ | Hệ võng nội mô |
| 49 | Autosomal dominant trait | /ˌɔːtəˈsoʊməl ˈdɒmɪnənt treɪt/ | Tính trạng trội trên nhiễm sắc thể thường |
| 50 | Pathophysiology | /ˌpæθoʊˌfɪziˈɒlədʒi/ | Sinh lý bệnh |
| 51 | Dietary iron | /ˈdaɪəˌtɛri ˈaɪərn/ | Sắt trong chế độ ăn |
| 52 | Body iron stores | /ˈbɒdi ˈaɪərn stɔːrz/ | Lượng sắt dự trữ của cơ thể |
| 53 | Positive iron balance | /ˈpɒzətɪv ˈaɪərn ˈbæləns/ | Cân bằng sắt dương tính |
| 54 | Ferritin mRNA | /ˈfɛrɪtɪn ɛm ɑːr ɛn eɪ/ | mRNA Ferritin |
| 55 | Iron repletion | /ˈaɪərn rɪˈpliːʃn/ | Bổ sung sắt |
| 56 | Intestinal lumen | /ɪnˈtɛstɪnl ˈluːmən/ | Lòng ruột |
| 57 | Plasma | /ˈplæzmə/ | Huyết tương |
| 58 | In vivo | /ɪn ˈviːvoʊ/ | Trong cơ thể sống |
| 59 | Kinetic studies | /kɪˈnɛtɪk ˈstʌdiz/ | Nghiên cứu động học |
| 60 | Serosal side | /səˈroʊsəl saɪd/ | Phía màng đáy |
| 61 | Hepatocyte | /ˈhɛpətəˌsaɪt/ | Tế bào gan |
| 62 | Parenchymal iron deposition | /pəˈrɛŋkɪməl ˈaɪərn ˌdɛpəˈzɪʃən/ | Lắng đọng sắt ở nhu mô |
| 63 | Pancreas | /ˈpæŋkriəs/ | Tụy |
| 64 | Joints | /dʒɔɪnts/ | Khớp |
| 65 | Skin | /skɪn/ | Da |
| 66 | Gonads | /ˈɡoʊnædz/ | Tuyến sinh dục |
| 67 | Endocrine organs | /ˈɛndoʊkrɪn ˈɔːrɡənz/ | Cơ quan nội tiết |
| 68 | Hemosiderin | /ˌhiːmoʊˈsɪdərɪn/ | Hemosiderin |
| 69 | Periportal | /ˌpɛriˈpɔːrtl/ | Quanh khoảng cửa |
| 70 | Pericentral | /ˌpɛriˈsɛntrəl/ | Quanh tĩnh mạch trung tâm |
| 71 | Kupffer cells | /ˈkʊpfər sɛlz/ | Tế bào Kupffer |
| 72 | Bile duct cells | /baɪl dʌkt sɛlz/ | Tế bào ống mật |
| 73 | Non-transferrin-bound iron | /nɒn trænsˈfɛrɪn baʊnd ˈaɪərn/ | Sắt không gắn với transferrin |
| 74 | Alcohol intake | /ˈælkəhɒl ˈɪnteɪk/ | Việc uống rượu |
| 75 | Serum iron levels | /ˈsɪərəm ˈaɪərn ˈlɛvəlz/ | Nồng độ sắt huyết thanh |
| 76 | Hepatocellular carcinoma (HCC) | /hɪˌpætoʊˈsɛljələr ˌkɑːrsɪˈnoʊmə/ | Ung thư biểu mô tế bào gan |
| 77 | Liver fibrosis | /ˈlɪvər faɪˈbroʊsɪs/ | Xơ hóa gan |
| 78 | Hepatic iron | /hɪˈpætɪk ˈaɪərn/ | Sắt gan |
| 79 | Alcoholic liver disease (ALD) | /ˌælkəˈhɒlɪk ˈlɪvər dɪˈziːz/ | Bệnh gan do rượu |
| 80 | Free radicals | /friː ˈrædɪkəlz/ | Gốc tự do |
| 81 | Nonalcoholic fatty liver disease (NAFLD) | /ˌnɒnælkəˈhɒlɪk ˈfæti ˈlɪvər dɪˈziːz/ | Bệnh gan nhiễm mỡ không do rượu |
| 82 | Nonalcoholic steatohepatitis (NASH) | /ˌnɒnælkəˈhɒlɪk ˌstiːətoʊˌhɛpəˈtaɪtɪs/ | Viêm gan nhiễm mỡ không do rượu |
| 83 | Liver damage | /ˈlɪvər ˈdæmɪdʒ/ | Tổn thương gan |
| 84 | Cell organelles | /sɛl ˌɔːrɡəˈnɛlz/ | Bào quan tế bào |
| 85 | DNA | /diː ɛn eɪ/ | DNA |
| 86 | Carcinogenesis | /ˌkɑːrsɪnoʊˈdʒɛnɪsɪs/ | Quá trình sinh ung thư |
| 87 | Collagen synthesis | /ˈkɒlədʒən ˈsɪnθəsɪs/ | Tổng hợp collagen |
| 88 | Oxidative mechanisms | /ˈɒksɪdeɪtɪv ˈmɛkənɪzəmz/ | Cơ chế oxy hóa |
| 89 | Inflammation | /ˌɪnfləˈmeɪʃən/ | Viêm |
| 90 | Viral infection | /ˈvaɪrəl ɪnˈfɛkʃən/ | Nhiễm virus |
| 91 | Clinical features | /ˈklɪnɪkl ˈfiːtʃərz/ | Đặc điểm lâm sàng |
| 92 | Bronze diabetes mellitus | /brɒnz ˌdaɪəˈbiːtiːz ˈmɛlɪtəs/ | Đái tháo đường nhiễm đồng |
| 93 | Arthritis | /ɑːrˈθraɪtɪs/ | Viêm khớp |
| 94 | Heart failure | /hɑːrt ˈfeɪljər/ | Suy tim |
| 95 | Asymptomatic phase | /ˌeɪsɪmptəˈmætɪk feɪz/ | Giai đoạn không triệu chứng |
| 96 | Laboratory testing | /ˈlæbrəˌtɔːri ˈtɛstɪŋ/ | Xét nghiệm |
| 97 | Serum aminotransferase levels | /ˈsɪərəm əˌmiːnoʊˈtrænsfəˌreɪz ˈlɛvəlz/ | Nồng độ aminotransferase huyết thanh |
| 98 | Population screening | /ˌpɒpjəˈleɪʃn ˈskriːnɪŋ/ | Tầm soát quần thể |
| 99 | Onset of symptoms | /ˈɒnsɛt əv ˈsɪmptəmz/ | Khởi phát triệu chứng |
| 100 | Weakness | /ˈwiːknəs/ | Yếu |
| 101 | Lethargy | /ˈlɛθərdʒi/ | Lơ mơ |
| 102 | Fatigue | /fəˈtiːɡ/ | Mệt mỏi |
| 103 | Arthralgia | /ɑːrˈθrældʒə/ | Đau khớp |
| 104 | Right upper quadrant pain | /raɪt ˈʌpər ˈkwɒdrənt peɪn/ | Đau hạ sườn phải |
| 105 | Loss of libido | /lɒs əv lɪˈbiːdoʊ/ | Giảm ham muốn tình dục |
| 106 | Potency | /ˈpoʊtənsi/ | Khả năng cương dương |
| 107 | Skin pigmentation | /skɪn ˌpɪɡmɛnˈteɪʃən/ | Sắc tố da |
| 108 | Amenorrhea | /əˌmɛnəˈriːə/ | Vô kinh |
| 109 | Liver disease | /ˈlɪvər dɪˈziːz/ | Bệnh gan |
| 110 | Hepatic iron concentration | /hɪˈpætɪk ˈaɪərn ˌkɒnsənˈtreɪʃən/ | Nồng độ sắt trong gan |
| 111 | Liver injury | /ˈlɪvər ˈɪndʒəri/ | Tổn thương gan |
| 112 | Hepatic complications | /hɪˈpætɪk ˌkɒmplɪˈkeɪʃənz/ | Biến chứng gan |
| 113 | Chronic hepatitis B and C | /ˈkrɒnɪk ˌhɛpəˈtaɪtɪs biː ænd siː/ | Viêm gan B và C mạn tính |
| 114 | Morbidity | /mɔːrˈbɪdɪti/ | Tỷ lệ bệnh tật |
| 115 | Cardiac disease | /ˈkɑːrdiæk dɪˈziːz/ | Bệnh tim |
| 116 | Cardiac dysfunction | /ˈkɑːrdiæk dɪsˈfʌŋkʃən/ | Rối loạn chức năng tim |
| 117 | Arrhythmias | /əˈrɪðmiəz/ | Loạn nhịp tim |
| 118 | Restrictive cardiomyopathy | /rɪˈstrɪktɪv ˌkɑːrdioʊmaɪˈɒpəθi/ | Bệnh cơ tim hạn chế |
| 119 | Dilated cardiomyopathy | /daɪˈleɪtɪd ˌkɑːrdioʊmaɪˈɒpəθi/ | Bệnh cơ tim giãn |
| 120 | Atrial and ventricular dysrhythmias | /ˈeɪtriəl ænd vɛnˈtrɪkjələr dɪsˈrɪðmiəz/ | Loạn nhịp nhĩ và thất |
| 121 | Postoperative morbidity | /ˌpoʊstˈɒpərətɪv mɔːrˈbɪdɪti/ | Bệnh suất sau phẫu thuật |
| 122 | Mortality | /mɔːrˈtæləti/ | Tử suất |
| 123 | Liver transplantation | /ˈlɪvər ˌtrænsplænˈteɪʃən/ | Ghép gan |
| 124 | Plasma insulin levels | /ˈplæzmə ˈɪnsəlɪn ˈlɛvəlz/ | Nồng độ insulin huyết tương |
| 125 | Peripheral insulin resistance | /pəˈrɪfərəl ˈɪnsəlɪn rɪˈzɪstəns/ | Đề kháng insulin ngoại biên |
| 126 | Joint disease | /dʒɔɪnt dɪˈziːz/ | Bệnh khớp |
| 127 | Metacarpophalangeal joints | /ˌmɛtəˌkɑːrpoʊfəˈlændʒiəl dʒɔɪnts/ | Khớp bàn ngón tay |
| 128 | Wrist joints | /rɪst dʒɔɪnts/ | Khớp cổ tay |
| 129 | Pathologic features | /ˌpæθəˈlɒdʒɪk ˈfiːtʃərz/ | Đặc điểm bệnh học |
| 130 | Joint space narrowing | /dʒɔɪnt speɪs ˈnæroʊɪŋ/ | Hẹp khe khớp |
| 131 | Chondrocalcinosis | /ˌkɒndroʊˌkælsɪˈnoʊsɪs/ | Vôi hóa sụn khớp |
| 132 | Subchondral cyst | /sʌbˈkɒndrəl sɪst/ | Nang dưới sụn |
| 133 | Osteopenia | /ˌɒstioʊˈpiːniə/ | Loãng xương |
| 134 | Arthropathy | /ɑːrˈθrɒpəθi/ | Bệnh khớp |
| 135 | Infections | /ɪnˈfɛkʃənz/ | Nhiễm trùng |
| 136 | Bacterial, viral, and fungal infections | /bækˈtɪəriəl, ˈvaɪrəl, ænd ˈfʌŋɡəl ɪnˈfɛkʃənz/ | Nhiễm trùng do vi khuẩn, virus và nấm |
| 137 | Innate and acquired immune responses | /ɪˈneɪt ænd əˈkwaɪərd ɪˈmjuːn rɪˈspɒnsɪz/ | Phản ứng miễn dịch bẩm sinh và mắc phải |
| 138 | Vibrio vulnificus | /ˈvɪbrioʊ vʌlˈnɪfɪkəs/ | Vibrio vulnificus |
| 139 | Yersinia enterocolitica | /jərˈsɪniə ˌɛntəroʊkoʊˈlɪtɪkə/ | Yersinia enterocolitica |
| 140 | Listeria monocytogenes | /lɪˈstɪəriə ˌmɒnoʊsaɪˈtɒdʒɪniːz/ | Listeria monocytogenes |
| 141 | Natural history | /ˈnætʃərəl ˈhɪstəri/ | Diễn tiến tự nhiên |
| 142 | Prognosis | /prɒɡˈnoʊsɪs/ | Tiên lượng |
| 143 | Hepatic decompensation | /hɪˈpætɪk ˌdiːkɒmpɛnˈseɪʃən/ | Mất bù gan |
| 144 | Surveillance for HCC | /sərˈveɪləns fɔːr eɪtʃ siː siː/ | Tầm soát HCC |
| 145 | Mixed HCC-cholangiocarcinoma | /mɪkst eɪtʃ siː siː ˌkoʊlændʒioʊˌkɑːrsɪˈnoʊmə/ | Ung thư biểu mô đường mật-tế bào gan hỗn hợp |
| 146 | Nonhepatobiliary cancers | /nɒn hɪˌpætoʊˈbɪliəri ˈkænsərz/ | Ung thư không liên quan đến gan mật |
| 147 | Malaise | /məˈleɪz/ | Khó chịu |
| 148 | Abdominal pain | /æbˈdɒmɪnəl peɪn/ | Đau bụng |
| 149 | Noncirrhotic hepatic fibrosis | /nɒn səˈrɒtɪk hɪˈpætɪk faɪˈbroʊsɪs/ | Xơ hóa gan không do xơ gan |
| 150 | Hypogonadism | /ˌhaɪpoʊˈɡoʊnæˌdɪzəm/ | Suy sinh dục |
| 151 | End-stage liver disease | /ɛnd steɪdʒ ˈlɪvər dɪˈziːz/ | Bệnh gan giai đoạn cuối |
| 152 | Cardiac events | /ˈkɑːrdiæk ɪˈvɛnts/ | Biến cố tim mạch |
| 153 | Posttransplant outcomes | /ˌpoʊsttrænsˈplænt ˈaʊtkʌmz/ | Kết quả sau ghép |
| 154 | Diagnosis | /ˌdaɪəɡˈnoʊsɪs/ | Chẩn đoán |
| 155 | Degenerative arthropathy | /dɪˈdʒɛnərətɪv ɑːrˈθrɒpəθi/ | Bệnh khớp thoái hóa |
| 156 | Hepatomegaly | /ˌhɛpətoʊˈmɛɡəli/ | Gan to |
| 157 | Acute phase reactant | /əˈkjuːt feɪz riˈæktənt/ | Chất phản ứng pha cấp |
| 158 | Inflammatory conditions | /ɪnˈflæmətɔːri kənˈdɪʃənz/ | Tình trạng viêm |
| 159 | Circadian variations | /sərˈkeɪdiən ˌvɛəriˈeɪʃənz/ | Thay đổi theo nhịp ngày đêm |
| 160 | Postprandial variations | /ˌpoʊstˈprændiəl ˌvɛəriˈeɪʃənz/ | Thay đổi sau bữa ăn |
| 161 | Genotyping | /ˌdʒiːnoʊˈtaɪpɪŋ/ | Xét nghiệm kiểu gen |
| 162 | Hepatic iron index | /hɪˈpætɪk ˈaɪərn ˈɪndɛks/ | Chỉ số sắt gan |
| 163 | Perls Prussian blue stain | /pɜːrlz ˈprʌʃən bluː steɪn/ | Nhuộm xanh Phổ Perls |
| 164 | Portal hypertension | /ˈpɔːrtl ˌhaɪpərˈtɛnʃən/ | Tăng áp lực tĩnh mạch cửa |
| 165 | Magnetic resonance imaging | /mæɡˈnɛtɪk ˈrɛzənəns ˈɪmɪdʒɪŋ/ | Chụp cộng hưởng từ |
| 166 | Quantitative phlebotomy | /ˈkwɒntɪˌteɪtɪv fləˈbɒtəmi/ | Trích máu tĩnh mạch định lượng |
| 167 | Iron-limited erythropoiesis | /ˈaɪərn ˈlɪmɪtɪd ɪˌrɪθroʊpɔɪˈiːsɪs/ | Tạo hồng cầu giới hạn do sắt |
| 168 | Anemia | /əˈniːmiə/ | Thiếu máu |
| 169 | Differential diagnosis | /ˌdɪfəˈrɛnʃəl ˌdaɪəɡˈnoʊsɪs/ | Chẩn đoán phân biệt |
| 170 | Secondary iron overload | /ˈsɛkənˌdɛri ˈaɪərn ˈoʊvərˌloʊd/ | Quá tải sắt thứ phát |
| 171 | Red blood cell turnover | /rɛd blʌd sɛl ˈtɜːrnoʊvər/ | Chu chuyển hồng cầu |
| 172 | Ineffective erythropoiesis | /ˌɪnɪˈfɛktɪv ɪˌrɪθroʊpɔɪˈiːsɪs/ | Tạo hồng cầu không hiệu quả |
| 173 | Blood transfusions | /blʌd trænsˈfjuːʒənz/ | Truyền máu |
| 174 | Iron-loading anemias | /ˈaɪərn ˈloʊdɪŋ əˈniːmiəz/ | Thiếu máu gây quá tải sắt |
| 175 | Thalassemia major | /ˌθæləˈsiːmiə ˈmeɪdʒər/ | Thalassemia thể nặng |
| 176 | Sideroblastic anemia | /ˌsɪdəroʊˈblæstɪk əˈniːmiə/ | Thiếu máu nguyên hồng cầu sắt |
| 177 | Chronic hemolytic anemias | /ˈkrɒnɪk ˌhiːməˈlɪtɪk əˈniːmiəz/ | Thiếu máu tan máu mạn tính |
| 178 | Porphyria cutanea tarda | /pɔːrˈfɪəriə kjuːˈteɪniə ˈtɑːrdə/ | Porphyria cutanea tarda |
| 179 | African iron overload | /ˈæfrɪkən ˈaɪərn ˈoʊvərˌloʊd/ | Quá tải sắt ở người châu Phi |
| 180 | Neonatal hemochromatosis | /ˌniːoʊˈneɪtəl ˌhiːməʊˌkroʊməˈtoʊsɪs/ | Bệnh nhiễm sắc tố sắt mô sơ sinh |
| 181 | Aceruloplasminemia | /əˌsɪəruloʊˌplæzmɪˈniːmiə/ | Bệnh không có ceruloplasmin trong máu |
| 182 | Atransferrinemia | /əˌtrænsˌfɛrɪˈniːmiə/ | Bệnh không có transferrin trong máu |
| 183 | Treatment | /ˈtriːtmənt/ | Điều trị |
| 184 | Serial phlebotomy | /ˈsɪəriəl fləˈbɒtəmi/ | Trích máu tĩnh mạch hàng loạt |
| 185 | Hematocrit | /hɪˈmætəˌkrɪt/ | Hematocrit |
| 186 | Hemoglobin | /ˌhiːməˈɡloʊbɪn/ | Hemoglobin |
| 187 | Dietary protein | /ˈdaɪəˌtɛri ˈproʊtiːn/ | Protein trong chế độ ăn |
| 188 | Vitamin B12 | /ˈvaɪtəmɪn biː twɛlv/ | Vitamin B12 |
| 189 | Folate | /ˈfoʊleɪt/ | Folate |
| 190 | Ascorbic acid | /əˈskɔːrbɪk ˈæsɪd/ | Axit ascorbic |
| 191 | Citric acid | /ˈsɪtrɪk ˈæsɪd/ | Axit citric |
| 192 | Gastric acid suppression | /ˈɡæstrɪk ˈæsɪd səˈprɛʃən/ | Ức chế axit dạ dày |
| 193 | Proton pump inhibitor | /ˈproʊtɒn pʌmp ɪnˈhɪbɪtər/ | Thuốc ức chế bơm proton |
| 194 | Iron chelators | /ˈaɪərn ˈkiːleɪtərz/ | Thuốc thải sắt |
| 195 | Deferoxamine | /dɪˌfɛrɒksəˈmiːn/ | Deferoxamine |
| 196 | Deferiprone | /dɪˈfɛrɪˌproʊn/ | Deferiprone |
| 197 | Deferasirox | /dɪˈfɛrəsɪrɒks/ | Deferasirox |
| 198 | Screening | /ˈskriːnɪŋ/ | Tầm soát |
| 199 | First-degree relatives | /fɜːrst dɪˈɡriː ˈrɛlətɪvz/ | Người thân cấp một |
| 200 | Cost effective | /kɒst ɪˈfɛktɪv/ | Hiệu quả về chi phí |
