[Sách dịch] Sổ tay Bệnh Gan – Handbook of Liver Disease – (C) NXB Elsevier, 2022 – Dịch và chú giải: Ths.Bs. Lê Đình Sáng
CHƯƠNG 4. VIÊM GAN B VÀ VIÊM GAN D
Hepatitis B and Hepatitis D
Tram T. Tran MD
Handbook of Liver Disease, Chapter 4, 51-65
NHỮNG ĐIỂM CHÍNH
|
Virus Viêm gan B
VIRUS HỌC
- Là thành viên lây nhiễm cho người trong họ Hepadnaviridae, nhóm các virus chứa DNA hướng gan.
- Tám genotype (A-H): Genotype C dường như liên quan đến bệnh mạn tính nặng hơn.
- Hạt virus hình cầu đường kính 42-nm với các thành phần sau:
- Lõi nucleocapsid đậm đặc điện tử, đường kính 27-nm.
- Lớp vỏ lipoprotein bên ngoài dày 7-nm.
- Lõi HBV chứa DNA vòng, sợi đôi một phần (dài 3.2 kb) và các thành phần sau:
- Protein DNA polymerase có hoạt tính men phiên mã ngược.
- Kháng nguyên lõi viêm gan B (HBcAg), một protein cấu trúc của nucleocapsid, không lưu hành trong huyết thanh.
- Kháng nguyên e của viêm gan B (HBeAg), một protein không cấu trúc, có khả năng bài tiết, tương quan không hoàn hảo với sự nhân lên tích cực của HBV.
- Protein X của viêm gan B, một chất kích hoạt phiên mã, liên quan đến sự hình thành ung thư gan.
- Vỏ lipoprotein bên ngoài của HBV, chứa các thành phần sau:
- Kháng nguyên bề mặt viêm gan B (HBsAg), với 3 protein vỏ: Protein chính, lớn và trung bình.
- Thành phần lipid và carbohydrate phụ.
- HBsAg hiện diện dưới dạng các hạt hình cầu hoặc hình ống 22-nm không lây nhiễm, với số lượng vượt trội so với các hạt HBV hoàn chỉnh.
- Các biến thể
a. Một serotype chính; nhiều subtype dựa trên sự đa dạng của protein HBsAg.
b. Các virus đột biến HBV xuất hiện tự phát do khả năng sửa lỗi kém của men phiên mã ngược hoặc do sự xuất hiện của tình trạng kháng thuốc kháng virus trong quá trình điều trị:
* Các đột biến vùng precore hoặc core promoter gây âm tính HBeAg.
* Các đột biến thoát ly do vắc-xin HBV (hiếm gặp).
* Các đột biến kháng thuốc do nucleos(t)ide. - Sự nhân lên xảy ra thông qua quá trình phiên mã ngược của RNA tiền bộ gen (pregenomic RNA).
- Gan là vị trí chính, nhưng không phải duy nhất, của sự nhân lên của HBV.
- Sự nhân lên in vitro bị hạn chế trong các tế bào gan người trưởng thành và thai nhi nguyên phát.
DỊCH TỄ HỌC
- Thời gian ủ bệnh: 15 đến 180 ngày (trung bình, 60 đến 90 ngày).
- Tình trạng nhiễm virus huyết (viremia) HBV kéo dài trong nhiều tuần đến nhiều tháng sau khi nhiễm cấp tính.
- Nhiễm trùng mạn tính với tình trạng nhiễm virus huyết dai dẳng phát triển ở 1% đến 5% người trưởng thành, 90% trẻ sơ sinh bị nhiễm và 50% trẻ nhỏ.
- Nhiễm trùng mạn tính có liên quan đến viêm gan mạn, xơ gan, HCC và tử vong sớm.
- Nhiễm trùng mạn tính có thể gây ra các bệnh ngoài gan: viêm mạch, u lympho, viêm cầu thận màng.
- Phân bố trên toàn thế giới: Tỷ lệ người mang HBV <1% ở Hoa Kỳ và 5% đến 15% ở châu Á và châu Phi cận Sahara; tỷ lệ mắc bệnh đã giảm ở những khu vực mở rộng việc sử dụng vắc-xin HBV.
- HBV có trong máu, tinh dịch, dịch tiết âm đạo-cổ tử cung, nước bọt và các chất dịch cơ thể khác.
- Nguy cơ lây truyền HBV tương quan với nồng độ HBV DNA huyết thanh và sự hiện diện của HBeAg.
- Các phương thức lây truyền
a. Qua đường máu * Truyền máu và các chế phẩm máu. * Sử dụng ma túy đường tiêm chích. * Chạy thận nhân tạo. * Phơi nhiễm với máu ở nhân viên y tế và các ngành nghề khác.
b. Qua đường tình dục: Chịu trách nhiệm cho 50% các ca cấp tính ở Hoa Kỳ.
c. Xuyên qua mô (qua da) hoặc qua niêm mạc
* Tai nạn do kim đâm.
* Phơi nhiễm niêm mạc với dịch cơ thể.
* Tái sử dụng thiết bị y tế bị ô nhiễm.
* Dùng chung dao cạo.
* Xăm mình.
* Châm cứu, xỏ khuyên trên cơ thể.
* Dùng chung bàn chải đánh răng.
d. Từ mẹ sang trẻ sơ sinh và từ mẹ sang trẻ nhỏ
* Lây truyền chu sinh có liên quan đến nồng độ HBV DNA huyết thanh của mẹ > 1.000.000 copies/mL (200.000 IU/mL).
* Nguy cơ cao nhất với HBV DNA huyết thanh của mẹ > copies/mL ( IU/mL).
e. Không có bằng chứng về lây truyền qua đường phân-miệng.
f. Không xác định được yếu tố nguy cơ trong 25% các trường hợp.
VIÊM GAN B CẤP TÍNH
Bệnh sinh
- Các cơ chế miễn dịch qua trung gian tế bào chịu trách nhiệm chính cho tổn thương tế bào gan, bao gồm thoái hóa và chết theo chương trình của tế bào gan.
- Đáp ứng tế bào T CD8+ và CD4+.
- Sản xuất các cytokine trong gan và toàn thân.
- Hiệu ứng gây bệnh trực tiếp của virus
- Được giả thuyết ở những bệnh nhân suy giảm miễn dịch có mức độ nhân lên của virus cực kỳ cao (bằng chứng là gián tiếp).
Đặc điểm lâm sàng
- Mức độ nghiêm trọng của bệnh dao động từ viêm gan không triệu chứng (cận lâm sàng), đến viêm gan cấp có triệu chứng lâm sàng, đến suy gan cấp (Hình 4.1); mức độ nghiêm trọng tăng lên ở những người có bệnh gan từ trước hoặc tuổi .
- Hội chứng lâm sàng ban đầu tương tự như nhiễm virus thông thường, với các triệu chứng toàn thân và tiêu hóa không đặc hiệu.
- Mệt mỏi, chán ăn, buồn nôn và nôn.
- Các triệu chứng giống cúm, bao gồm viêm họng, ho, sổ mũi, sợ ánh sáng, đau đầu và đau cơ.
- Các triệu chứng thường khởi phát âm thầm.
- Sốt không phổ biến.
- Một hội chứng qua trung gian phức hợp miễn dịch giống bệnh huyết thanh xảy ra ở <10% bệnh nhân nhiễm HBV; bao gồm viêm đa khớp, đau đa khớp, phù mạch, phát ban dạng sẩn, ban xuất huyết, đốm xuất huyết, và hiếm hơn là tiểu máu và protein niệu hoặc viêm mạch ở da hoặc toàn thân.
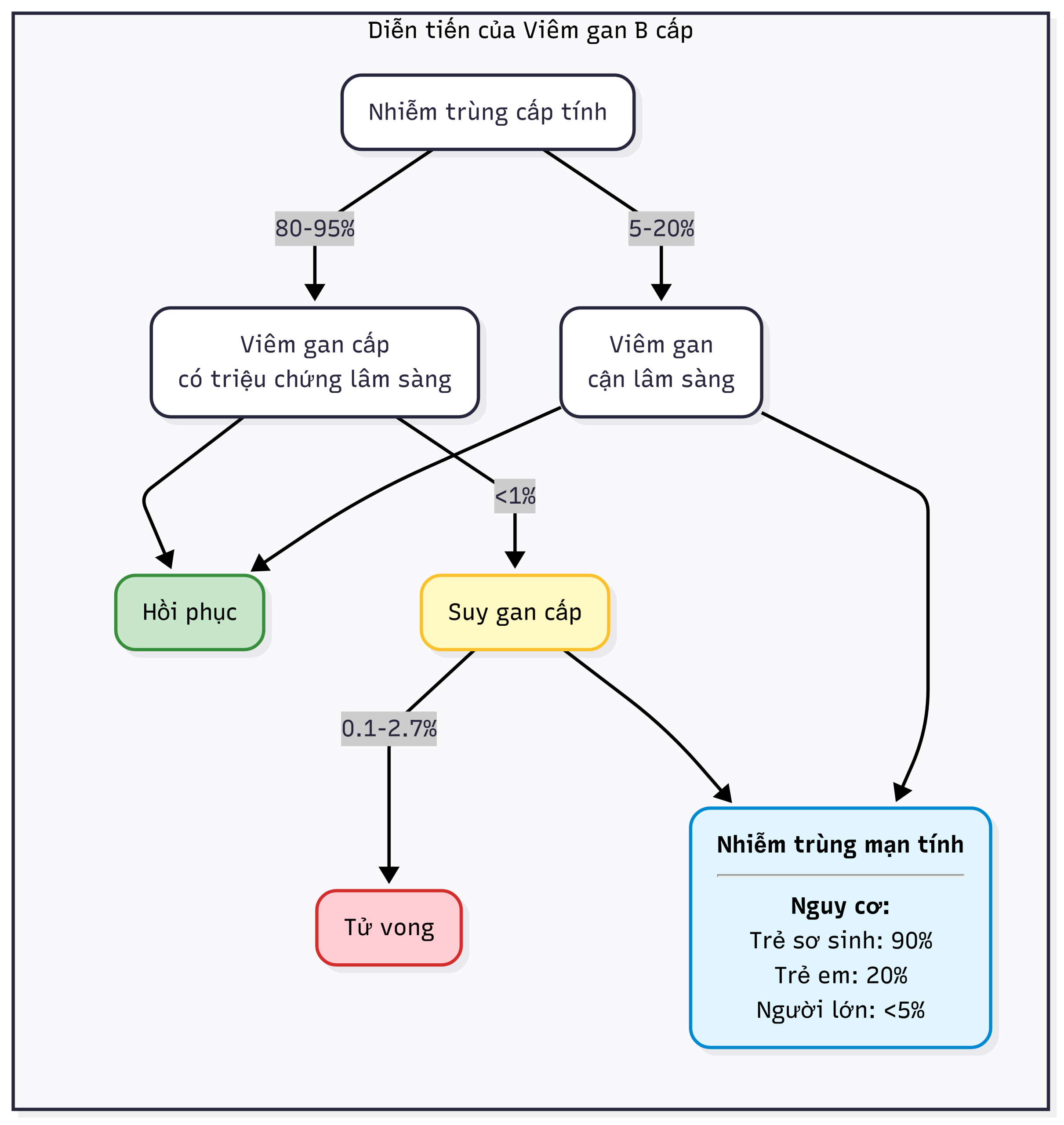
Hình 4.1 Diễn tiến của viêm gan B cấp tính. (Phỏng theo Hyams KC. Risks of chronicity following acute hepatitis B virus infection: a review. Clin Infect Dis 1995:20:992-1000; Liang TJ. Hepatitis B: the virus and disease. Hepatology. 2009;49:S13-S21.)
- Các triệu chứng tiền triệu giảm bớt hoặc biến mất khi bắt đầu có vàng da, mặc dù chán ăn, mệt mỏi và yếu có thể kéo dài.
- Vàng da (giai đoạn hoàng đản) được báo hiệu bằng sự xuất hiện của nước tiểu sẫm màu và phân nhạt màu; ngứa (thường nhẹ và thoáng qua) có thể xảy ra khi vàng da tăng lên.
- Giai đoạn hoàng đản kéo dài từ 1 đến 3 tuần và theo sau là giai đoạn hồi phục có thể kéo dài hàng tháng, trong đó vàng da và các triệu chứng giảm bớt và HBsAg, HBeAg, và HBV DNA biến mất khỏi huyết thanh.
- Khám thực thể cho thấy gan to nhẹ và hơi đau khi ấn.
- Lách to nhẹ và hạch bạch huyết cổ sau được ghi nhận ở 15% đến 20% bệnh nhân.
Đặc điểm cận lâm sàng
- Đặc điểm sinh hóa nổi bật nhất: Tăng rõ rệt nồng độ alanine (ALT) và aspartate (AST) aminotransferase huyết thanh.
- Nồng độ aminotransferase đỉnh thay đổi từ 500 đến 5000 U/L; nồng độ ALT thường cao hơn nồng độ AST.
- Nồng độ bilirubin huyết thanh hiếm khi cao hơn 10 mg/dL, ngoại trừ trong bệnh nặng, suy gan cấp và viêm gan ứ mật.
- Nồng độ phosphatase kiềm huyết thanh bình thường hoặc tăng nhẹ.
- Thời gian prothrombin bình thường hoặc tăng từ 1 đến 3 giây.
- Nồng độ albumin huyết thanh bình thường hoặc giảm ở mức tối thiểu.
- Công thức máu ngoại vi: Bình thường hoặc giảm bạch cầu nhẹ có hoặc không có tăng lympho bào tương đối.
- Chẩn đoán huyết thanh học dựa trên việc phát hiện HBsAg và kháng thể immunoglobulin (Ig)M kháng HBcAg (anti-HBc) trong huyết thanh (Bảng 4.1).
Nhiễm HBV cấp và Suy gan
- Suy gan cấp được đặc trưng bởi rối loạn đông máu đáng kể với thời gian prothrombin kéo dài (INR ) (xem Chương 2).
- Tăng bạch cầu, hạ natri máu và hạ kali máu là phổ biến.
- Hạ đường huyết.
- Tăng rõ rệt nồng độ bilirubin và aminotransferase huyết thanh, nhưng nồng độ aminotransferase có thể giảm về mức bình thường mặc dù bệnh tiến triển.
- Giảm albumin máu từ nhẹ đến trung bình.
Bảng 4.1: Diễn giải các dấu ấn huyết thanh HBV
| HBsAg | IgG anti-HBc | IgM anti-HBc | Anti-HBs | Diễn giải |
|---|---|---|---|---|
| – | – | – | – | Chưa bao giờ nhiễm và không có miễn dịch |
| + | + | – | – | Nhiễm mạn tính |
| + | + | + | – | Nhiễm cấp tính hoặc đợt bùng phát bệnh ở người mang virus mạn tính |
| – | + | – | + | Đã khỏi bệnh trong quá khứ và có miễn dịch |
| – | – | – | + | Có miễn dịch do tiêm vắc-xin |
| Anti-HBc, Kháng thể kháng kháng nguyên lõi viêm gan B; anti-HBs, kháng thể kháng kháng nguyên bề mặt viêm gan B; HBsAg, kháng nguyên bề mặt viêm gan B; HBV, virus viêm gan B; IgG, immunoglobulin G; IgM, immunoglobulin M. |
Điều trị
- Theo dõi ngoại trú là phù hợp trừ khi nôn mửa hoặc chán ăn nghiêm trọng kéo dài và dẫn đến mất nước, hoặc xuất hiện các đặc điểm của suy gan cấp.
- Nên duy trì lượng calo và chất lỏng nạp vào.
- Không có khuyến nghị chế độ ăn uống cụ thể.
- Cấm uống rượu trong giai đoạn cấp tính.
- Nên tránh hoạt động thể chất gắng sức hoặc kéo dài.
- Nên hạn chế các hoạt động hàng ngày, với các giai đoạn nghỉ ngơi được xác định bởi mức độ mệt mỏi và khó chịu.
- Nên ngưng tất cả các loại thuốc không cần thiết.
- Liệu pháp kháng virus
- Không cần thiết vì >95% người trưởng thành có hệ miễn dịch bình thường sẽ tự khỏi.
- Điều trị bằng liệu pháp kháng virus chưa cho thấy sự cải thiện về nồng độ các xét nghiệm sinh hóa gan hoặc tỷ lệ mất HBsAg.
- Nếu một bệnh nhân bị suy gan cấp do nhiễm HBV và có thể cần ghép gan, điều trị kháng virus thường được bắt đầu và có thể làm giảm khả năng tái nhiễm HBV sau ghép.
- Nên xem xét điều trị kháng virus trong các trường hợp nhiễm HBV cấp tính nặng kéo dài (vàng da sâu và thời gian prothrombin kéo dài rõ rệt); các lựa chọn điều trị hàng đầu là entecavir và tenofovir (xem thảo luận sau trong chương này).
VIÊM GAN B MẠN TÍNH
Bệnh sinh và Bệnh học
- Hầu hết tổn thương gan do HBV là do đáp ứng miễn dịch của vật chủ với đáp ứng qua trung gian tế bào nhắm vào HBcAg.
- Tế bào lympho T gây độc tế bào (CTL) là các tế bào hiệu ứng gây ra tổn thương tế bào.
- Các đáp ứng miễn dịch không đặc hiệu với kháng nguyên, chẳng hạn như các đáp ứng qua trung gian cytokine viêm (yếu tố hoại tử khối u alpha, gamma interferon), có thể quan trọng hơn cho việc loại bỏ virus so với các cơ chế qua trung gian CTL.
- Đáp ứng quá mức của vật chủ có thể dẫn đến viêm gan tối cấp, trong khi đáp ứng giảm của vật chủ làm tăng nguy cơ nhiễm trùng mạn tính.
- Ở những bệnh nhân không loại bỏ được virus, số lượng tế bào T CD4+ và CD8+ đều giảm rõ rệt.
- Các phát hiện mô học không đặc hiệu bao gồm thâm nhiễm chủ yếu là tế bào lympho, có thể hoặc không thể giới hạn trong các khoảng cửa.
- Các phát hiện mô học đặc trưng của viêm gan B mạn tính bao gồm các tế bào gan dạng kính mờ, trong đó bào tương được nhuộm màu hồng bằng hematoxylin-eosin để đáp ứng với việc sản xuất hàng loạt HBsAg. HBcAg có thể được chứng minh trong nhân tế bào gan, trong bào tương và trên màng tế bào.
- Nhiều hệ thống có sẵn để đánh giá mức độ (mức độ nghiêm trọng của hoại tử-viêm) và giai đoạn (mức độ nghiêm trọng của xơ hóa); giai đoạn xơ hóa là yếu tố tiên lượng mô học phù hợp nhất.
Đặc điểm lâm sàng
- Triệu chứng của HBV mạn tính dao động từ không có, đến các than phiền không đặc hiệu (mệt mỏi, đau hạ sườn phải), đến các biến chứng của xơ gan.
- Các biểu hiện ngoài gan xảy ra ở tối đa 20% bệnh nhân nhiễm HBV mạn tính và bao gồm đau khớp, viêm đa động mạch nút, viêm cầu thận, cryoglobulin máu hỗn hợp thiết yếu và các hội chứng hiếm gặp khác.
- Nguy cơ chuyển sang mạn tính phụ thuộc vào độ tuổi và chức năng miễn dịch khi một người bị nhiễm lần đầu, như sau:
- 90% trẻ sơ sinh bị nhiễm trong năm đầu đời.
- 30% đến 50% trẻ em bị nhiễm từ 1 đến 4 tuổi.
- Khoảng 5% người trưởng thành khỏe mạnh.
-
50% người trưởng thành suy giảm miễn dịch.
- Khoảng 25% người trưởng thành bị nhiễm mạn tính trong thời thơ ấu sẽ chết vì xơ gan hoặc ung thư gan liên quan đến HBV.
- Bốn giai đoạn trong diễn tiến tự nhiên về huyết thanh học, virus học và sinh hóa của nhiễm HBV mạn tính được tóm tắt trong Hình 4.2.
- Sự tiến triển từ giai đoạn này sang giai đoạn khác và ngược lại (đảo ngược) có thể xảy ra.
- Tỷ lệ hiện mắc HBeAg ở những người bị viêm gan B mạn tính giảm theo tuổi, với sự mất HBeAg tự phát ở 7% đến 20% bệnh nhân mỗi năm.
- Mất HBsAg tự phát trong huyết thanh xảy ra không thường xuyên (0.5% đến 1% mỗi năm), với sự phát triển kháng thể kháng HBsAg (anti-HBs) ở hầu hết những người mất HBsAg.
- Diễn tiến tự nhiên và kết cục lâm sàng của viêm gan B mạn tính được trình bày trong Hình 4.3.
- Các yếu tố liên quan đến sự tiến triển của viêm gan B mạn tính bao gồm tuổi cao hơn (thời gian nhiễm bệnh dài hơn), genotype C của HBV, lạm dụng rượu, nồng độ HBV DNA huyết thanh cao, đồng nhiễm với các virus khác (virus gây suy giảm miễn dịch ở người [HIV], virus viêm gan C, HDV), các yếu tố môi trường (hút thuốc, aflatoxin), béo phì và đái tháo đường.
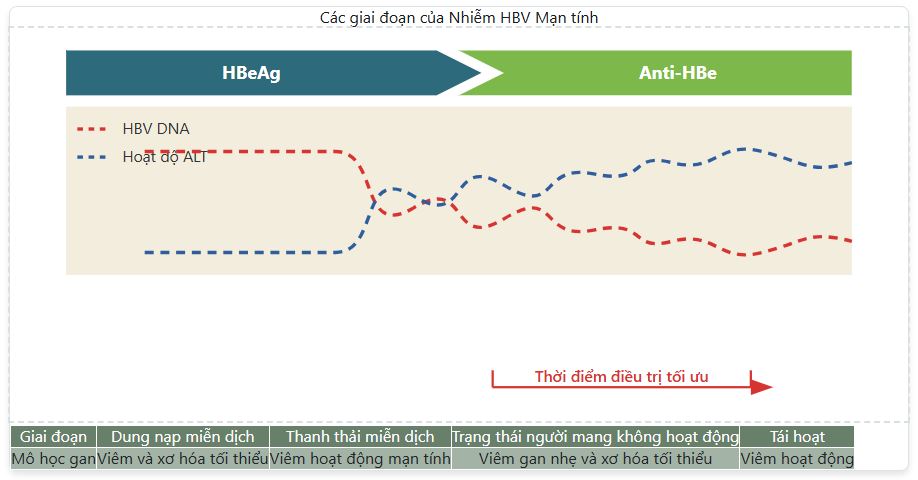
Hình 4.2 Các giai đoạn của nhiễm virus viêm gan B (HBV) mạn tính. ALT, Alanine aminotransferase; anti-HBe, kháng thể kháng kháng nguyên e của viêm gan B; HBeAg, kháng nguyên e của viêm gan B.
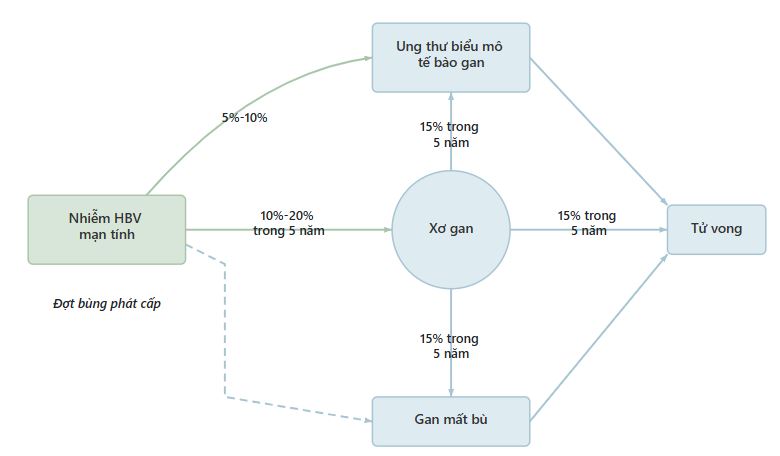
Hình 4.3. Diễn tiến tự nhiên của viêm gan B mạn tính. HBV, Virus viêm gan B.
Chẩn đoán
- Chẩn đoán nhiễm HBV ban đầu dựa vào việc phát hiện HBsAg.
- Khi HBsAg có thể phát hiện được, cần thực hiện các xét nghiệm cận lâm sàng sâu hơn để đánh giá tình trạng bệnh và nhu cầu điều trị (Hình 4.4; xem Hình 4.2 và Bảng 4.1):
- Định lượng HBV DNA bằng một xét nghiệm nhạy.
- Nồng độ ALT huyết thanh: Nồng độ ALT nên được đo mỗi 3 đến 6 tháng nếu ALT bình thường dai dẳng và thường xuyên hơn nếu nó tăng.
- HBeAg và anti-HBe: Xác định loại viêm gan B mạn tính (tức là, HBeAg dương tính hoặc HBeAg âm tính) và điểm kết thúc điều trị (tức là, mất HBeAg ở bệnh nhân HBeAg dương tính).
- Các xét nghiệm về mức độ nghiêm trọng của bệnh gan: Bilirubin toàn phần, albumin huyết thanh, và thời gian prothrombin; tỷ lệ chuẩn hóa quốc tế (INR); và số lượng tiểu cầu (xem Chương 1).
- Sinh thiết gan: Tùy chọn trong nhiễm HBV nhưng có thể xác định mức độ viêm mô học và giai đoạn xơ hóa và xác định các bệnh gan cùng tồn tại như viêm gan nhiễm mỡ, quá tải sắt, hoặc viêm gan tự miễn. Đo độ đàn hồi gan bằng siêu âm hoặc các phương pháp không xâm lấn khác để xác định giai đoạn xơ hóa có thể được sử dụng thay cho sinh thiết gan để hỗ trợ quyết định điều trị. Sinh thiết gan vẫn có thể cần thiết để xác định mức độ viêm (xem Chương 1).
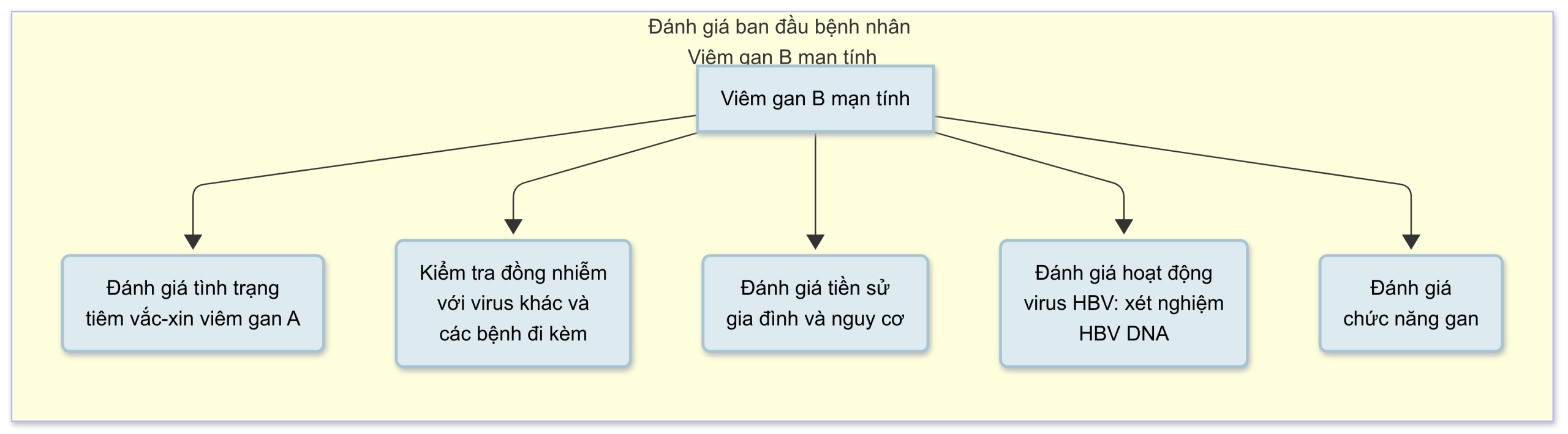
Hình 4.4 Đánh giá ban đầu bệnh nhân viêm gan B mạn tính. HBV, Virus viêm gan B.
Điều trị
- Mục tiêu
- Ngăn ngừa các biến chứng lâu dài (xơ gan, HCC) và tử vong bằng cách ức chế bền vững HBV DNA huyết thanh.
- Điểm kết thúc điều trị chính: Giảm bền vững HBV DNA huyết thanh xuống mức thấp hoặc không thể phát hiện (<10 đến 15 IU/mL).
- Điểm kết thúc điều trị phụ: Giảm hoặc bình thường hóa nồng độ ALT huyết thanh, cải thiện mô học gan, mất HBeAg có hoặc không có chuyển đổi huyết thanh thành anti-HBe, mất HBsAg hoặc chuyển đổi huyết thanh thành anti-HBs và ngăn ngừa lây lan thứ phát của nhiễm trùng.
- Tiêu chí điều trị viêm gan B mạn tính (Bảng 4.2)
- Các thông số lâm sàng và cận lâm sàng không cho thấy sự tương quan nhất quán với mô học gan; các hướng dẫn quản lý khuyến nghị sinh thiết gan ở những bệnh nhân chọn lọc dựa trên tuổi, nồng độ HBV DNA huyết thanh và tình trạng HBeAg.
- Chỉ định điều trị HBV (Bảng 4.3)
- Các tác nhân điều trị cho HBV mạn tính (Bảng 4.4)
- Các thuốc đường uống: Các liệu pháp hàng đầu là entecavir và tenofovir.
- Các chất tương tự nucleos(t)ide: Mặc dù có hiệu lực kháng virus cao (cao hơn interferon), những loại thuốc này không thể loại bỏ hoàn toàn HBV khỏi gan, nhưng chúng có thể duy trì sự ức chế nhân lên bền vững.
- Ưu điểm: Hiệu lực mạnh; tác dụng phụ không đáng kể; dùng đường uống; an toàn và hiệu quả cho mọi lứa tuổi; phù hợp cho bệnh nhân xơ gan và đồng nhiễm HIV.
- Nhược điểm: Tỷ lệ chuyển đổi huyết thanh HBeAg và HBsAg thấp hơn so với interferon; cần điều trị kéo dài, có thể dẫn đến tăng nguy cơ kháng thuốc kháng virus.
- Entecavir (chất tương tự nucleoside): Hoạt tính kháng virus mạnh với hàng rào di truyền cao đối với sự đề kháng và tỷ lệ đề kháng thấp; liều, 0.5 đến 1 mg mỗi ngày; các biến cố bất lợi bao gồm nhiễm toan lactic (hiếm gặp).
- Tenofovir (chất tương tự nucleotide): Mạnh, với hàng rào di truyền cao đối với sự đề kháng và tỷ lệ đề kháng thấp; ít độc cho thận hơn adefovir, một chất tương tự nucleotide khác; liều, 300 mg mỗi ngày (tenofovir disoproxil fumarate) hoặc 25 mg mỗi ngày (tenofovir alafenamide); các biến cố bất lợi bao gồm hội chứng Fanconi (hiếm gặp) và giảm mật độ xương.
- Tác nhân tiêm: Pegylated interferon
- Peginterferon alfa: Xem xét ở những bệnh nhân trẻ, không xơ gan có nồng độ HBV DNA thấp, nồng độ ALT huyết thanh cao và genotype thuận lợi (A > B > C > D). Điều trị bao gồm 180 µg/tuần tiêm dưới da trong 48 tuần.
- Ưu điểm: Thời gian điều trị có giới hạn; không có đề kháng; chuyển đổi huyết thanh HBeAg ở tối đa 32% bệnh nhân HBeAg dương tính sau 48 tuần điều trị; làm sạch HBsAg ở 6% bệnh nhân.
- Nhược điểm: Nhiều tác dụng phụ; tiêm dưới da; thường có chống chỉ định.
- Tránh sử dụng các tác nhân cũ hơn—lamivudine, telbivudine, và adefovir—vì tỷ lệ đề kháng cao và/hoặc hiệu lực thấp.
- Các thuốc đường uống: Các liệu pháp hàng đầu là entecavir và tenofovir.
- Điểm kết thúc điều trị
- Chuyển đổi huyết thanh HBsAg là điểm kết thúc mong muốn nhất nhưng nó xảy ra với tỷ lệ thấp.
- Đối với bệnh nhân HBeAg dương tính: Điều trị cho đến khi chuyển đổi huyết thanh HBeAg, và ngưng thuốc sau giai đoạn củng cố từ 6 đến 12 tháng sau khi chuyển đổi huyết thanh HBeAg. Tái chuyển đổi huyết thanh là phổ biến, đặc biệt ở bệnh nhân châu Á.
- Đối với bệnh nhân HBeAg âm tính: Điều trị vô thời hạn vì tái phát là phổ biến sau khi ngưng điều trị.
- Đề kháng thuốc kháng virus
a. Chẩn đoán đề kháng
* Sự tái bùng phát virus ít nhất 1.0 so với điểm thấp nhất; được xác nhận bằng xét nghiệm HBV DNA lặp lại.
* Loại trừ các nguyên nhân thất bại không liên quan đến HBV (tức là, tuân thủ kém).
* Xác nhận đề kháng genotype bằng cách phát hiện đột biến HBV, nếu có: Đột biến(s) polymerase của HBV có liên quan đến sự đề kháng.
* Xác nhận đề kháng kiểu hình: Giảm tính nhạy cảm in vitro với một tác nhân kháng virus ở những bệnh nhân tuân thủ điều trị.
b. Tần suất tích lũy của đề kháng thuốc kháng virus thấp (0% đến 1%) đối với các liệu pháp đường uống hàng đầu.
c. Theo dõi đề kháng thuốc:
* Đo lường ALT và HBV DNA huyết thanh lặp lại.
* Sử dụng một xét nghiệm HBV DNA nhạy và cùng một xét nghiệm theo thời gian.
* Tần suất đánh giá dựa trên mức độ nghiêm trọng của bệnh: Đối với bệnh gan nhẹ, ít nhất mỗi 6 tháng; đối với bệnh tiến triển hoặc xơ gan, mỗi 3 tháng.
Bảng 4.2: Tiêu chí điều trị Viêm gan B Mạn tính
| Hướng dẫn | HBeAg+ | HBeAg- | ||
|---|---|---|---|---|
| HBV DNA (IU/mL) | ALT (U/L) | HBV DNA (IU/mL) | ALT (U/L) | |
| Hội nghị Đồng thuận NIH 2009 | >20.000 | >2x ULN hoặc + sinh thiết | x ULN hoặc + sinh thiết | |
| EASL 2012 | >2.000 | >ULN | >2.000 | >ULN |
| Thuật toán Hoa Kỳ 2015 | >ULN hoặc + sinh thiết | >ULN hoặc + sinh thiết | ||
| APASL 2012 | >2x ULN | ULN | ||
| AASLD 2009 | >2x ULN hoặc + sinh thiết | >2.000 | x ULN hoặc + sinh thiết | |
| Mẫu sinh thiết cho thấy viêm tế bào gan hoạt động. | ||||
| AASLD, Hiệp hội Nghiên cứu Bệnh gan Hoa Kỳ; ALT, alanine aminotransferase; APASL, Hiệp hội Nghiên cứu Bệnh gan Châu Á-Thái Bình Dương; EASL, Hiệp hội Nghiên cứu Gan Châu Âu; HBeAg, kháng nguyên e của viêm gan B; HBV, virus viêm gan B; NIH, Viện Y tế Quốc gia; ULN, giới hạn trên của mức bình thường. |
Bảng 4.3: Các tình trạng có và không có chỉ định điều trị HBV
| Có chỉ định | Không có chỉ định |
|---|---|
| Viêm gan B mạn tính với nồng độ ALT tăng và HBV DNA >2000 UI/mL | Viêm gan B cấp tính |
| Bệnh nhân xơ gan dương tính với HBV DNA | Giai đoạn dung nạp miễn dịch |
| Bệnh nhân xơ gan mất bù | Người mang virus mạn tính không hoạt động |
| Suy gan cấp | |
| Bệnh nhân HBsAg dương tính sắp bị ức chế miễn dịch | |
| ALT, Alanine aminotransferase; HBsAg, kháng nguyên bề mặt viêm gan B; HBV, virus viêm gan B. |
Bảng 4.4: Các liệu pháp được FDA chấp thuận cho nhiễm HBV
| Tác nhân | Tên thương mại | Nhà sản xuất | Năm được chấp thuận |
|---|---|---|---|
| Liệu pháp hàng đầu | |||
| Entecavir | Baraclude | Bristol-Myers Squibb | 2005 |
| Tenofovir | Viread | Gilead Sciences | 2008 |
| Peginterferon alfa-2a | Pegasys | Roche Laboratories | 2005 |
| Liệu pháp hàng hai | |||
| Adefovir dipivoxil | Hepsera | Gilead Sciences | 2002 |
| Telbivudine | Tyzeka | Idenix and Novartis | 2006 |
| Liệu pháp hàng ba | |||
| Lamivudine | Epivir-HBV | GlaxoSmithKline | 1998 |
| FDA, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ. |
Viêm gan B ở các quần thể đặc biệt
THAI KỲ (HÌNH 4.5)
- Đối với phụ nữ trong độ tuổi sinh đẻ bị nhiễm HBV mạn tính và hiện không đang điều trị và muốn có thai: a. Đánh giá mức độ nghiêm trọng của bệnh gan: Nếu không có bằng chứng về bệnh gan tiến triển ở mẹ (xơ gan hoặc xơ hóa tiến triển), có thể hoãn điều trị cho đến tam cá nguyệt thứ ba để giảm nguy cơ lây truyền từ mẹ sang con. b. Nếu có bằng chứng lâm sàng về bệnh gan tiến triển ở mẹ, hãy bắt đầu điều trị bằng một tác nhân kháng virus đường uống để duy trì sự ổn định lâm sàng và ngăn ngừa đợt bùng phát hoặc mất bù. * Tenofovir là lựa chọn ưu tiên (loại B theo Cục Quản lý Thực phẩm và Dược phẩm [FDA]).
- Đối với phụ nữ trong độ tuổi sinh đẻ đã đang dùng thuốc và có thai:
- Tiếp tục điều trị theo chỉ định cho tình trạng bệnh của mẹ.
- Đối với phụ nữ trong độ tuổi sinh đẻ có sự nhân lên của virus tích cực, hãy xem xét điều trị (xem thảo luận ở phần trước của chương).
- Cho con bú được coi là an toàn với nguy cơ lây truyền HBV thấp.
TÁI HOẠT
Tái hoạt HBV lâm sàng nặng có thể xảy ra khi có ức chế miễn dịch ở những bệnh nhân có bằng chứng nhiễm HBV (dương tính với HBsAg) hoặc bằng chứng nhiễm trùng trước đó (dương tính với anti-HBc).
- Tất cả bệnh nhân cần ức chế miễn dịch nên được sàng lọc nhiễm HBV (HBsAg, IgG anti-HBc) (Hình 4.6).
- Nếu bệnh nhân dương tính với HBsAg, nên bắt đầu điều trị kháng virus đường uống trước khi bắt đầu liệu pháp ức chế miễn dịch và tiếp tục ít nhất 6 đến 12 tháng sau khi hoàn thành liệu pháp ức chế miễn dịch. Entecavir hoặc tenofovir là các lựa chọn hàng đầu vì hiệu lực và nguy cơ kháng thuốc thấp.
- Nếu bệnh nhân âm tính với HBsAg nhưng dương tính với anti-HBc, sự tái hoạt vẫn có thể xảy ra trong bối cảnh ức chế miễn dịch nguy cơ cao (ví dụ, với rituximab). Tái hoạt ở những người dương tính với anti-HBc vẫn có thể xảy ra ngay cả khi họ cũng dương tính với anti-HBs.
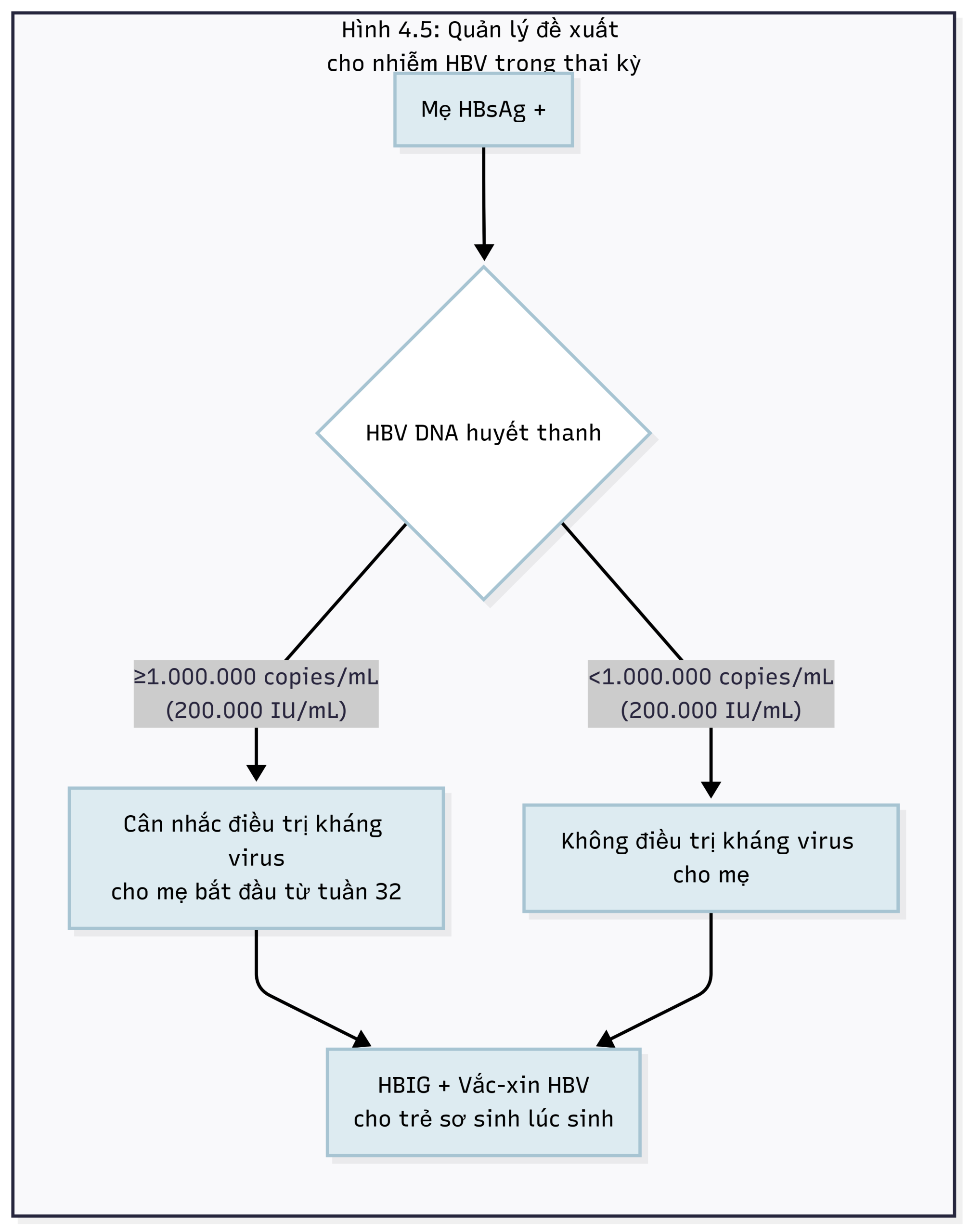
Hình 4.5 Quản lý đề xuất cho nhiễm virus viêm gan B (HBV) trong thai kỳ. HBIG, globulin miễn dịch viêm gan B; HBsAg, kháng nguyên bề mặt viêm gan B.
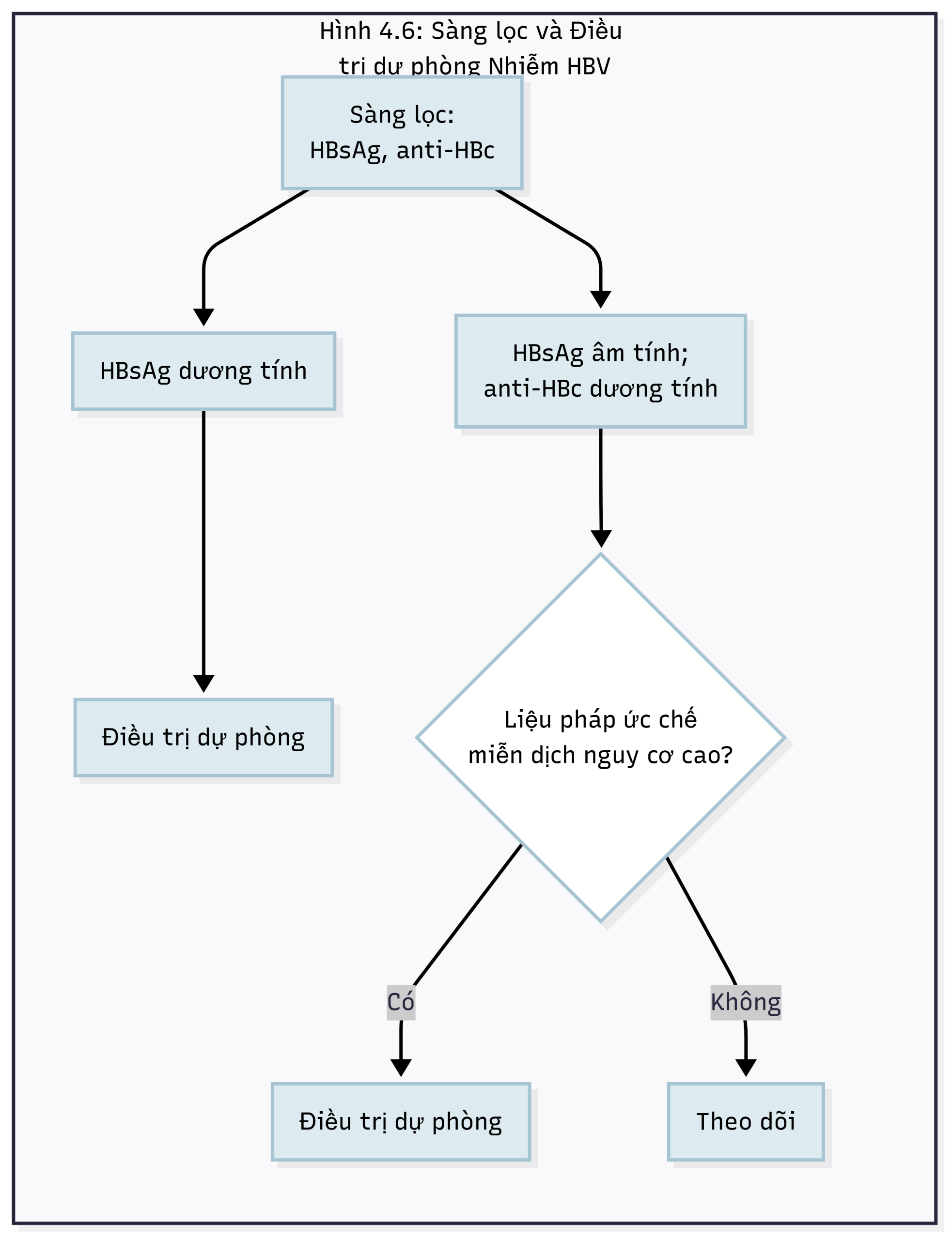
Hình 4.6 Sàng lọc và điều trị dự phòng kháng virus cho nhiễm virus viêm gan B ở bệnh nhân đang hóa trị hoặc điều trị ức chế miễn dịch. Những người âm tính với các dấu ấn virus viêm gan B không cần điều trị dự phòng kháng virus. Các lựa chọn bao gồm lamivudine, telbivudine, và tenofovir. Anti-HBc, Kháng thể kháng kháng nguyên lõi viêm gan B; HBsAg, kháng nguyên bề mặt viêm gan B.
DỰ PHÒNG
Nền tảng của dự phòng miễn dịch là việc sử dụng vắc-xin HBV trước phơi nhiễm.
- Dự phòng miễn dịch trước phơi nhiễm bằng vắc-xin HBV
a. Vắc-xin tái tổ hợp có nguồn gốc từ nấm men
* Chứa HBsAg làm kháng nguyên.
* Tính sinh miễn dịch cao; gây ra nồng độ anti-HBs bảo vệ ở >95% người nhận trẻ khỏe mạnh (<40 tuổi) sau cả ba liều.
* Hiệu quả từ 85% đến 95% trong việc ngăn ngừa nhiễm HBV hoặc viêm gan B lâm sàng.
* Các tác dụng phụ chính bao gồm:
* Đau thoáng qua tại chỗ tiêm ở 10% đến 25% bệnh nhân.
* Sốt nhẹ, ngắn ngày ở <3% bệnh nhân.
* Một liều tăng cường của vắc-xin có thể không cần thiết ngay cả sau 20 năm kể từ lần tiêm chủng ban đầu (tức là, vắc-xin có thể cung cấp sự bảo vệ suốt đời).
* Một liều tăng cường của vắc-xin được chỉ định ở những người suy giảm miễn dịch nếu nồng độ anti-HBs của họ <10 mU/mL.
* Tiêm vắc-xin HBV không có giá trị điều trị miễn dịch đã được chứng minh ở những người đã bị nhiễm HBV.
b. Liều lượng và lịch tiêm vắc-xin HBV
* Engerix-B (GlaxoSmithKline) được tiêm bắp (cơ delta) với liều 20 µg protein HBsAg cho người lớn và 10 µg cho trẻ sơ sinh và trẻ em đến 19 tuổi, lặp lại sau 1 và 6 tháng; đối với bệnh nhân chạy thận nhân tạo, liều 40 µg (liều gấp đôi của chế phẩm 20 µg) được tiêm vào các tháng 0, 1, 2 và 6.
* Recombivax HB (Merck) được tiêm bắp (cơ delta) với liều 10 µg protein HBsAg cho người lớn và liều 5 µg cho trẻ em đến 19 tuổi, lặp lại sau 1 và 6 tháng; trẻ em từ 11 đến 15 tuổi có thể nhận 10 µg Recombivax HB ban đầu với một liều tăng cường duy nhất sau 4 đến 6 tháng; đối với bệnh nhân chạy thận nhân tạo, có sẵn lịch tiêm 3 liều 40 µg.
c. Chỉ định
* Tiêm chủng toàn dân cho trẻ sơ sinh được khuyến nghị ngay sau khi sinh.
* Tiêm chủng đuổi cho thanh thiếu niên đến 19 tuổi (nếu chưa được tiêm trước đó) được khuyến nghị.
* Các nhóm nguy cơ cao được nhắm mục tiêu:
* Người tiếp xúc trong gia đình và vợ/chồng của người mang HBV.
* Người bản địa Alaska, người dân đảo Thái Bình Dương và người Mỹ bản địa. * Nhân viên y tế và những người khác tiếp xúc với máu (bao gồm cả những người ứng cứu đầu tiên).
* Người tiêm chích ma túy.
* Nam giới (bao gồm cả thanh thiếu niên) có quan hệ tình dục với nam giới, bao gồm cả người lưỡng tính.
* Người có nhiều bạn tình.
* Nhân viên trong các cơ sở dành cho người khuyết tật phát triển.
* Người nhận các sản phẩm máu có nguy cơ cao.
* Bệnh nhân và nhân viên chạy thận nhân tạo định kỳ.
* Người bị giam giữ (nơi có thể xảy ra hành vi tiêm chích ma túy và đồng tính luyến ái).
* Người tiếp xúc trong gia đình với trẻ được nhận nuôi từ các vùng lưu hành bệnh.
* Người có bệnh gan từ trước (ví dụ, viêm gan C mạn tính). - Dự phòng miễn dịch sau phơi nhiễm bằng vắc-xin HBV và globulin miễn dịch viêm gan B (HBIG), một chế phẩm globulin miễn dịch chứa nồng độ anti-HBs cao.
a. Chỉ định
* Người tiếp xúc tình dục nhạy cảm của người nhiễm HBV cấp tính.
* HBIG 0.04 đến 0.07 mL/kg càng sớm càng tốt sau khi phơi nhiễm.
* Liều vắc-xin HBV đầu tiên trong ba liều được tiêm tại một vị trí khác (cơ delta) đồng thời hoặc trong vòng vài ngày.
* Liều vắc-xin thứ hai và thứ ba được tiêm sau 1 và 6 tháng.
* Trẻ sơ sinh của các bà mẹ HBsAg dương tính được xác định trong thai kỳ.
* HBIG liều 0.5 mL được tiêm trong vòng 12 giờ sau khi sinh vào cơ trước ngoài của đùi.
* Vắc-xin HBV liều 5 đến 10 µg được tiêm trong vòng 12 giờ sau khi sinh (tại một vị trí khác ở cơ trước ngoài), lặp lại sau 1 và 6 tháng.
* Hiệu quả bảo vệ >95%.
b. Ngăn ngừa lây truyền từ mẹ sang con
* Nồng độ virus huyết cao ở mẹ (1.000.000 copies/mL hoặc >200.000 IU/mL) có liên quan đến nguy cơ lây truyền chu sinh tăng (8% đến 10%) ngay cả khi trẻ sơ sinh được tiêm phòng đầy đủ.
* Xem Hình 4.5 để biết chiến lược quản lý đề xuất cho phụ nữ bị HBV trong thai kỳ.
* Trẻ sơ sinh của các bà mẹ nhiễm HBV nên được tiêm vắc-xin tiêu chuẩn và HBIG trong vòng 12 giờ sau khi sinh (xem thảo luận trước đó).
* Nếu liệu pháp kháng virus được bắt đầu để giảm lây truyền từ mẹ sang con, nó có thể được ngưng sau khi sinh, với việc theo dõi mẹ về một đợt bùng phát sau đó; theo dõi (ALT và HBV DNA huyết thanh) ít nhất mỗi 1 đến 3 tháng trong 6 tháng sau sinh được đề xuất.
* Tất cả phụ nữ nhiễm HBV nên được theo dõi về đợt bùng phát trong và sau thai kỳ do những thay đổi miễn dịch trong thai kỳ có thể gây ra đợt bùng phát.
Virus Viêm gan D
VIRUS HỌC
Một virus vệ tinh RNA khiếm khuyết (giống viroid) cần chức năng hỗ trợ của HBV để biểu hiện và gây bệnh nhưng không cần cho sự nhân lên của nó.
- Chỉ có 1 serotype được công nhận; 8 genotype.
- Hạt hình cầu đường kính 35-nm đến 37-nm, được bao bọc bởi lớp vỏ lipoprotein của HBV (HBsAg).
- Cấu trúc giống lõi 19-nm chứa một phosphoprotein nhân kháng nguyên (kháng nguyên HDV).
- Liên kết với RNA.
- Tồn tại ở hai dạng đồng phân: protein nhỏ hơn 195 axit amin và protein lớn hơn 214 axit amin.
- Kháng nguyên HDV nhỏ hơn vận chuyển RNA vào nhân: Cần thiết cho sự nhân lên của HDV.
- Kháng nguyên HDV lớn hơn được prenyl hóa: Ức chế sự nhân lên của HDV RNA và tham gia vào quá trình lắp ráp HDV.
- HDV RNA dài 1.7 kb, sợi đơn, vòng, khép kín cộng hóa trị.
- Antigenome của HDV, một bộ gen bổ sung, và RNA vòng được tìm thấy trong các tế bào gan bị nhiễm và, ở mức độ thấp hơn nhiều, trong các hạt HDV đã được tinh sạch.
- HDV RNA là bộ gen RNA nhỏ nhất trong số các virus động vật; HDV giống với các virus vệ tinh thực vật.
- Bộ gen RNA có thể tạo thành một cấu trúc dạng que, không phân nhánh bằng cách tự gấp lại thông qua sự ghép cặp base nội phân tử.
- Sự nhân lên chỉ giới hạn ở các tế bào gan.
- Các dòng tế bào HCC nguyên phát của tinh tinh, marmota và người đã được chuyển nạp với các cấu trúc cDNA của HDV biểu hiện HDV RNA và kháng nguyên HDV.
BỆNH SINH VÀ BỆNH HỌC
- HDV dường như gây độc tế bào trực tiếp; tổn thương tế bào qua trung gian miễn dịch cũng xảy ra.
- Hoạt động hoại tử-viêm thường nặng, nhưng các đặc điểm mô học không đặc hiệu cho nhiễm HDV mạn tính.
- Kháng nguyên HDV (HDVAg) dễ dàng được chứng minh trong nhân và ở mức độ thấp hơn trong bào tương của các tế bào gan bị nhiễm.
ĐẶC ĐIỂM LÂM SÀNG VÀ DIỄN TIẾN TỰ NHIÊN
- Thời gian ủ bệnh: Ước tính từ 4 đến 7 tuần.
- Lưu hành ở lưu vực Địa Trung Hải, bán đảo Balkan, Trung Âu, một phần châu Phi, Trung Đông và lưu vực sông Amazon.
- Tỷ lệ mắc bệnh đã giảm với việc sử dụng vắc-xin HBV ngày càng tăng.
- Nhiễm HDV xảy ra ở 2% đến 5% bệnh nhân viêm gan B mạn tính ở Hoa Kỳ.
- Nhiễm virus huyết HDV có thể ngắn (nhiễm cấp tính) hoặc kéo dài (nhiễm mạn tính).
- Nhiễm HDV chỉ xảy ra ở những người có nguy cơ nhiễm HBV (đồng nhiễm hoặc bội nhiễm).
- Các phương thức lây truyền
a. Qua đường máu
* Sử dụng ma túy đường tiêm chích là phương thức lây lan chủ yếu ở Hoa Kỳ.
* Người nhận các sản phẩm máu có nguy cơ cao.
b. Tình dục
* Nam giới quan hệ tình dục với nam giới.
* Lây truyền qua đường tình dục khác giới không hiệu quả.
c. Từ mẹ sang con, nhưng tần suất không chắc chắn. - Các triệu chứng của nhiễm HDV không đặc hiệu.
- Nên nghi ngờ nhiễm HDV trong các trường hợp sau:
- Nhiễm HBV tối cấp.
- Nhiễm HBV cấp tính có cải thiện ban đầu nhưng sau đó tái phát.
- Nhiễm HBV mạn tính tiến triển trong khi không có sự nhân lên tích cực của HBV.
- Đồng nhiễm HDV và HBV
- Bệnh cấp tính thường nặng hơn so với đơn nhiễm HBV.
- Nguy cơ suy gan cấp tăng.
- Tỷ lệ mạn tính tương tự như nhiễm HBV cấp tính đơn thuần (<5%).
- Bội nhiễm HDV ở bệnh nhân nhiễm HBV mạn tính làm tăng tốc diễn tiến tự nhiên của viêm gan B mạn tính.
- Có mối liên quan giữa HDV và nguy cơ HCC (cơ chế chưa rõ).
XÉT NGHIỆM HUYẾT THANH VÀ VIRUS HỌC
- Cả xét nghiệm miễn dịch enzyme (EIA) và xét nghiệm miễn dịch phóng xạ (RIA) đều có sẵn để phát hiện tổng kháng thể và kháng thể IgM kháng HDV (anti-HDV).
- Sự tồn tại của IgM anti-HDV hoặc hiệu giá IgG anti-HDV >1:1000 tương quan với sự hiện diện của sự nhân lên virus đang diễn ra.
- Xét nghiệm HDV RNA chỉ có sẵn trên cơ sở nghiên cứu, nhưng nó có ích trong việc phân biệt nhiễm trùng đang diễn ra với nhiễm trùng trong quá khứ.
- Đồng nhiễm và bội nhiễm được phân biệt bởi sự hiện diện hoặc vắng mặt của IgM anti-HBc trong huyết thanh.
- Việc phát hiện HDVAg bằng phân tích hóa mô miễn dịch của mô gan được coi là tiêu chuẩn vàng để chẩn đoán nhiễm HDV dai dẳng; tuy nhiên, nhuộm HDVAg chỉ có sẵn trong các phòng thí nghiệm nghiên cứu.
DỰ PHÒNG
- Không có sẵn globulin miễn dịch chứa anti-HDV nồng độ cao đặc hiệu cũng như vắc-xin HDV.
- Dự phòng miễn dịch HDV phụ thuộc vào việc phòng ngừa HBV bằng cách sử dụng vắc-xin HBV.
ĐIỀU TRỊ
- Thuốc
- Interferon alpha liều cao (9 MU ba lần một tuần) và peginterferon alfa, dùng trong 1 năm, đã cho thấy một số hiệu quả trong điều trị viêm gan D mạn tính.
- Hiệu quả của liệu pháp interferon alpha nên được đánh giá sau 24 tuần bằng cách đo nồng độ HDV RNA.
- Liệu pháp kéo dài hơn 1 năm có thể cần thiết nhưng hiệu quả chưa được chứng minh.
- Một số bệnh nhân trở nên âm tính với HDV RNA và thậm chí âm tính với HBsAg trong huyết thanh, kèm theo sự cải thiện về các đặc điểm mô học.
- Các chất tương tự nucleos(t)ide dường như không ảnh hưởng đến sự nhân lên của HDV và bệnh liên quan.
- Ghép gan (xem Chương 33)
- Bệnh nhân nhiễm HDV mạn tính có nguy cơ tái phát HBV thấp hơn so với những người chỉ nhiễm HBV mạn tính.
- Tái phát HDV có thể được phát hiện trước các dấu hiệu tái hoạt HBV.
- Tỷ lệ tái phát giảm và tỷ lệ sống còn cải thiện ở bệnh nhân xơ gan do HDV so với xơ gan do HBV có thể là do tác dụng ức chế của HDV đối với sự nhân lên của HBV.
- Không có điều trị đặc hiệu nào để ngăn ngừa tái phát nhiễm HDV sau ghép, nhưng có vẻ thận trọng khi điều trị kết hợp với một nucleot(s)ide đường uống và HBIG như đối với bệnh nhân nhiễm HBV sau ghép.
TÀI LIỆU THAM KHẢO
- Asselah T, Marcellin P, eds. Hepatitis B virus. Clin Liver Dis. 2013;17:375-506.
- Fattovich G. Natural history and prognosis of hepatitis B. Sem Liver Dis. 2003;23:47-58.
- Fung J, Lai CL, Tanaka Y, et al. The duration of lamivudine therapy for chronic hepatitis B: cessation vs. continuation of treatment after HBeAg seroconversion. Am J Gastroenterol. 2009;104:1940-1946.
- Heller T, Rotman Y, Koh C, et al. Long-term therapy of chronic delta hepatitis with peginterferon alfa. Aliment Pharmacol Ther. 2014;40:93-104.
- Iloeje UH, Yang HI, Su J, et al. Predicting cirrhosis risk based on the level of circulating hepatitis B viral load. Gastroenterology. 2006;130:678-686.
- LeFevre ML. U.S. Preventive Services Task Force. Screening for hepatitis B virus infection in nonpregnant adolescents and adults: U.S. Preventive Services Task Force recommendation statement. Ann Intern Med. 2014;161:58-66.
- Lok A, McMahon B, Brown R, et al. Antiviral therapy for chronic hepatitis B virus infection in adults: a systematic review and meta-analysis. Hepatology. 2015;63. 284-206.
- McMahon BJ, Bulkow L, Simons B, et al. Relationship between level of hepatitis B virus DNA and liver disease: a population-based study of hepatitis B e antigen-negative persons with hepatitis B. Clin Gastroenterol Hepatol. 2014;12:701-706.
- Romeo R, Del Ninno E, Rumi M, et al. A 28-year study of the course of hepatitis Delta infection: a risk factor for cirrhosis and hepatocellular carcinoma. Gastroenterology. 2009;136:1629-1638.
- Terrault N, Bzowej N, Chang KM, et al. AASLD guidelines for treatment of chronic hepatitis B. Hepatology. 2016;63:261-283.
- Wedemeyer H, Manns MP. Epidemiology, pathogenesis and management of hepatitis D: update and challenges ahead. Nat Rev Gastroenterol Hepatol. 2010;7:31-40.
- Weinbaum C, Williams I, Mast E, et al. Recommendations for identification and public health management of persons with chronic hepatitis B virus infection. MMWR Recomm Rep. 2008;57:1-20.
- WHO. Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection. Geneva, Switzerland: World Health Organization; May 12, 2015.
BẢNG CHÚ GIẢI THUẬT NGỮ Y HỌC ANH-VIỆT
| STT | Thuật ngữ tiếng Anh | Cách phát âm | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Hepatitis B virus (HBV) | /ˌhep.əˈtaɪ.tɪs ˈbiː ˌvaɪ.rəs/ | Virus viêm gan B |
| 2 | Acute liver failure | /əˈkjuːt ˈlɪv.ər ˈfeɪ.ljər/ | Suy gan cấp |
| 3 | Cirrhosis | /səˈroʊ.sɪs/ | Xơ gan |
| 4 | Hepatocellular carcinoma (HCC) | /həˌpæt.oʊˈsel.jə.lər ˌkɑːr.sɪˈnoʊ.mə/ | Ung thư biểu mô tế bào gan |
| 5 | Hepatitis B vaccination | /ˌhep.əˈtaɪ.tɪs ˈbiː ˌvæk.sɪˈneɪ.ʃən/ | Tiêm vắc-xin viêm gan B |
| 6 | Acute HBV infection | /əˈkjuːt eɪtʃ.biː.viː ɪnˈfek.ʃən/ | Nhiễm HBV cấp tính |
| 7 | Immunocompetent | /ˌɪm.jə.noʊˈkɒm.pɪ.tənt/ | Có hệ miễn dịch bình thường |
| 8 | Symptomatic | /ˌsɪmp.təˈmæt.ɪk/ | Có triệu chứng |
| 9 | Chronic infection | /ˈkrɒn.ɪk ɪnˈfek.ʃən/ | Nhiễm trùng mạn tính |
| 10 | Immunocompromised | /ˌɪm.jə.noʊˈkɒm.prə.maɪzd/ | Suy giảm miễn dịch |
| 11 | Hemodialysis | /ˌhiː.moʊ.daɪˈæl.ə.sɪs/ | Chạy thận nhân tạo |
| 12 | Noncirrhotic liver | /ˌnɒn.səˈrɒt.ɪk ˈlɪv.ər/ | Gan không xơ |
| 13 | Serum HBV DNA | /ˈsɪə.rəm eɪtʃ.biː.viː diː.en.eɪ/ | HBV DNA trong huyết thanh |
| 14 | Antiviral therapy | /ˌæn.tiˈvaɪ.rəl ˈθer.ə.pi/ | Liệu pháp kháng virus |
| 15 | Viral replication | /ˈvaɪ.rəl ˌrep.lɪˈkeɪ.ʃən/ | Sự nhân lên của virus |
| 16 | Aminotransferase | /əˌmiː.noʊˈtræns.fə.reɪs/ | Aminotransferase (men gan) |
| 17 | Pregnant patients | /ˈpreɡ.nənt ˈpeɪ.ʃənts/ | Bệnh nhân mang thai |
| 18 | Immunosuppressive therapy | /ˌɪm.jə.noʊ.səˈpres.ɪv ˈθer.ə.pi/ | Liệu pháp ức chế miễn dịch |
| 19 | Entecavir | /enˈtek.ə.vɪər/ | Entecavir |
| 20 | Tenofovir | /təˈnɒf.ə.vɪər/ | Tenofovir |
| 21 | Pegylated interferon | /ˈpeɡ.ɪ.leɪ.tɪd ˌɪn.təˈfɪə.rɒn/ | Pegylated interferon |
| 22 | Liver transplantation | /ˈlɪv.ər ˌtræns.plɑːnˈteɪ.ʃən/ | Ghép gan |
| 23 | Decompensated cirrhosis | /ˌdiː.kəm.penˈseɪ.tɪd səˈroʊ.sɪs/ | Xơ gan mất bù |
| 24 | Fibrosis | /faɪˈbroʊ.sɪs/ | Xơ hóa |
| 25 | Serial liver biopsies | /ˈsɪə.ri.əl ˈlɪv.ər ˈbaɪ.ɒp.siz/ | Sinh thiết gan hàng loạt |
| 26 | Hepatitis D virus (HDV) | /ˌhep.əˈtaɪ.tɪs ˈdiː ˌvaɪ.rəs/ | Virus viêm gan D |
| 27 | Virology | /vaɪˈrɒl.ə.dʒi/ | Virus học |
| 28 | Hepadnaviridae | /ˌhep.əd.nəˈvɪər.ɪ.deɪ/ | Họ Hepadnaviridae |
| 29 | Hepatotropic | /ˌhep.ə.toʊˈtroʊ.pɪk/ | Hướng gan |
| 30 | Genotype | /ˈdʒen.ə.taɪp/ | Kiểu gen (genotype) |
| 31 | Nucleocapsid core | /ˌnjuː.kli.oʊˈkæp.sɪd kɔːr/ | Lõi nucleocapsid |
| 32 | Lipoprotein envelope | /ˌlaɪ.poʊˈproʊ.tiːn ˈen.və.loʊp/ | Vỏ lipoprotein |
| 33 | Double-stranded DNA | /ˈdʌb.əl ˌstræn.dɪd diː.en.eɪ/ | DNA sợi đôi |
| 34 | DNA polymerase | /diː.en.eɪ pəˈlɪm.ə.reɪs/ | DNA polymerase |
| 35 | Reverse transcriptase | /rɪˌvɜːs trænˈskrɪp.teɪs/ | Men phiên mã ngược |
| 36 | Hepatitis B core antigen (HBcAg) | /… kɔːr ˈæn.tɪ.dʒən/ | Kháng nguyên lõi viêm gan B |
| 37 | Hepatitis B e antigen (HBeAg) | /… iː ˈæn.tɪ.dʒən/ | Kháng nguyên e của viêm gan B |
| 38 | Secretory protein | /sɪˈkriː.tər.i ˈproʊ.tiːn/ | Protein bài tiết |
| 39 | Transcriptional activator | /trænˈskrɪp.ʃən.əl ˈæk.tɪ.veɪ.tər/ | Chất kích hoạt phiên mã |
| 40 | Hepatocarcinogenesis | /həˌpæt.oʊˌkɑː.sɪ.noʊˈdʒen.ə.sɪs/ | Sự hình thành ung thư gan |
| 41 | Hepatitis B surface antigen (HBsAg) | /… ˈsɜː.fɪs ˈæn.tɪ.dʒən/ | Kháng nguyên bề mặt viêm gan B |
| 42 | Serotype | /ˈsɪə.roʊ.taɪp/ | Huyết thanh học (serotype) |
| 43 | Subtype | /ˈsʌb.taɪp/ | Dưới type (subtype) |
| 44 | Mutant viruses | /ˈmjuː.tənt ˈvaɪ.rəs.ɪz/ | Virus đột biến |
| 45 | Precore/core promoter mutants | /ˈpriː.kɔːr / kɔːr prəˈmoʊ.tər ˈmjuː.tənts/ | Đột biến vùng precore/core promoter |
| 46 | Vaccine-induced escape mutants | /ˌvæk.siːn ɪnˈdjuːst ɪˈskeɪp ˈmjuː.tənts/ | Đột biến thoát ly do vắc-xin |
| 47 | Nucleos(t)ide-induced resistant mutants | /ˈnjuː.kli.ə.saɪd … rɪˈzɪs.tənt ˈmjuː.tənts/ | Đột biến kháng thuốc do nucleos(t)ide |
| 48 | Pregenomic RNA | /ˌpriː.dʒəˈnoʊ.mɪk ɑːr.en.eɪ/ | RNA tiền bộ gen |
| 49 | In vitro | /ɪn ˈviː.troʊ/ | Trong ống nghiệm |
| 50 | Primary hepatocytes | /ˈpraɪ.mər.i həˈpæt.ə.saɪts/ | Tế bào gan nguyên phát |
| 51 | Epidemiology | /ˌep.ɪ.diː.miˈɒl.ə.dʒi/ | Dịch tễ học |
| 52 | Incubation period | /ˌɪŋ.kjəˈbeɪ.ʃən ˈpɪə.ri.əd/ | Thời gian ủ bệnh |
| 53 | Viremia | /vaɪˈriː.mi.ə/ | Nhiễm virus huyết |
| 54 | Neonates | /ˈniː.oʊ.neɪts/ | Trẻ sơ sinh |
| 55 | Chronic hepatitis | /ˈkrɒn.ɪk ˌhep.əˈtaɪ.tɪs/ | Viêm gan mạn |
| 56 | Premature mortality | /ˌprem.əˈtʃʊər mɔːˈtæl.ə.ti/ | Tử vong sớm |
| 57 | Extrahepatic diseases | /ˌek.strə.hɪˈpæt.ɪk dɪˈziːz.ɪz/ | Bệnh ngoài gan |
| 58 | Vasculitis | /ˌvæs.kjəˈlaɪ.tɪs/ | Viêm mạch |
| 59 | Lymphoma | /lɪmˈfoʊ.mə/ | U lympho |
| 60 | Membranous glomerulonephritis | /ˈmem.brə.nəs ɡloʊˌmer.jə.loʊ.neˈfraɪ.tɪs/ | Viêm cầu thận màng |
| 61 | Carrier prevalence | /ˈkær.i.ər ˈprev.əl.əns/ | Tỷ lệ người mang mầm bệnh |
| 62 | Cervicovaginal secretions | /ˌsɜː.vɪ.koʊ.væˈdʒaɪ.nəl sɪˈkriː.ʃənz/ | Dịch tiết âm đạo-cổ tử cung |
| 63 | Transmission | /trænzˈmɪʃ.ən/ | Sự lây truyền |
| 64 | Blood-borne | /ˈblʌd.bɔːn/ | Lây qua đường máu |
| 65 | Transfusion | /trænsˈfjuː.ʒən/ | Truyền máu |
| 66 | Injection drug use | /ɪnˈdʒek.ʃən drʌɡ juːs/ | Sử dụng ma túy đường tiêm chích |
| 67 | Percutaneous | /ˌpɜː.kjəˈteɪ.ni.əs/ | Qua da |
| 68 | Permucosal | /ˌpɜː.mjuːˈkoʊ.səl/ | Qua niêm mạc |
| 69 | Needlestick accidents | /ˈniː.dəl.stɪk ˈæk.sɪ.dənts/ | Tai nạn do kim đâm |
| 70 | Tattoos | /tæˈtuːz/ | Xăm mình |
| 71 | Acupuncture | /ˈæk.jə.pʌŋk.tʃər/ | Châm cứu |
| 72 | Body piercing | /ˈbɒd.i ˈpɪə.sɪŋ/ | Xỏ khuyên cơ thể |
| 73 | Maternal-neonatal transmission | /məˌtɜː.nəl ˌniː.oʊˈneɪ.təl trænzˈmɪʃ.ən/ | Lây truyền từ mẹ sang con (sơ sinh) |
| 74 | Perinatal transmission | /ˌper.ɪˈneɪ.təl trænzˈmɪʃ.ən/ | Lây truyền chu sinh |
| 75 | Fecal-oral spread | /ˈfiː.kəl ˈɔː.rəl spred/ | Lây qua đường phân-miệng |
| 76 | Pathogenesis | /ˌpæθ.əˈdʒen.ə.sɪs/ | Bệnh sinh |
| 77 | Cell-mediated immune mechanisms | /sel ˌmiː.di.eɪ.tɪd ɪˈmjuːn ˈmek.ə.nɪ.zəmz/ | Cơ chế miễn dịch qua trung gian tế bào |
| 78 | Hepatocyte degeneration | /həˈpæt.ə.saɪt dɪˌdʒen.əˈreɪ.ʃən/ | Thoái hóa tế bào gan |
| 79 | Apoptosis | /ˌæp.əpˈtoʊ.sɪs/ | Chết theo chương trình |
| 80 | T cell responses | /tiː sel rɪˈspɒns.ɪz/ | Đáp ứng tế bào T |
| 81 | Cytokines | /ˈsaɪ.tə.kaɪnz/ | Cytokine |
| 82 | Viral cytopathic effect | /ˈvaɪ.rəl ˌsaɪ.toʊˈpæθ.ɪk ɪˈfekt/ | Hiệu ứng gây bệnh trực tiếp của virus |
| 83 | Subclinical hepatitis | /ˌsʌbˈklɪn.ɪ.kəl ˌhep.əˈtaɪ.tɪs/ | Viêm gan cận lâm sàng |
| 84 | Preexisting liver disease | /ˌpriː.ɪɡˈzɪs.tɪŋ ˈlɪv.ər dɪˈziːz/ | Bệnh gan từ trước |
| 85 | Constitutional symptoms | /ˌkɒn.stɪˈtjuː.ʃən.əl ˈsɪmp.təmz/ | Triệu chứng toàn thân |
| 86 | Gastrointestinal symptoms | /ˌɡæs.troʊ.ɪnˈtes.tɪ.nəl ˈsɪmp.təmz/ | Triệu chứng tiêu hóa |
| 87 | Malaise | /məˈleɪz/ | Mệt mỏi, khó chịu |
| 88 | Anorexia | /ˌæn.əˈrek.si.ə/ | Chán ăn |
| 89 | Pharyngitis | /ˌfær.ɪnˈdʒaɪ.tɪs/ | Viêm họng |
| 90 | Coryza | /kəˈraɪ.zə/ | Sổ mũi |
| 91 | Photophobia | /ˌfoʊ.təˈfoʊ.bi.ə/ | Sợ ánh sáng |
| 92 | Myalgias | /maɪˈæl.dʒi.əz/ | Đau cơ |
| 93 | Insidious onset | /ɪnˈsɪd.i.əs ˈɒn.set/ | Khởi phát âm thầm |
| 94 | Immune complex mediated | /ɪˈmjuːn ˈkɒm.pleks ˌmiː.di.eɪ.tɪd/ | Qua trung gian phức hợp miễn dịch |
| 95 | Serum sickness | /ˈsɪə.rəm ˈsɪk.nəs/ | Bệnh huyết thanh |
| 96 | Polyarthritis | /ˌpɒl.i.ɑːˈθraɪ.tɪs/ | Viêm đa khớp |
| 97 | Polyarthralgias | /ˌpɒl.i.ɑːˈθræl.dʒi.əz/ | Đau đa khớp |
| 98 | Angioedema | /ˌæn.dʒi.oʊ.ɪˈdiː.mə/ | Phù mạch |
| 99 | Urticaria | /ˌɜː.tɪˈkeə.ri.ə/ | Mề đay |
| 100 | Maculopapular eruptions | /ˌmæk.jə.loʊˈpæp.jə.lər ɪˈrʌp.ʃənz/ | Phát ban dạng sẩn |
| 101 | Purpura | /ˈpɜː.pjə.rə/ | Ban xuất huyết |
| 102 | Petechiae | /pəˈtiː.ki.aɪ/ | Đốm xuất huyết |
| 103 | Hematuria | /ˌhiː.məˈtʃʊə.ri.ə/ | Tiểu máu |
| 104 | Proteinuria | /ˌproʊ.tiːˈnjʊə.ri.ə/ | Protein niệu |
| 105 | Cutaneous vasculitis | /kjuːˈteɪ.ni.əs ˌvæs.kjəˈlaɪ.tɪs/ | Viêm mạch ở da |
| 106 | Prodromal symptoms | /prəʊˈdroʊ.məl ˈsɪmp.təmz/ | Triệu chứng tiền triệu |
| 107 | Jaundice | /ˈdʒɔːn.dɪs/ | Vàng da |
| 108 | Icteric phase | /ɪkˈter.ɪk feɪz/ | Giai đoạn hoàng đản |
| 109 | Dark urine | /dɑːk ˈjʊə.rɪn/ | Nước tiểu sẫm màu |
| 110 | Pruritus | /prʊəˈraɪ.təs/ | Ngứa |
| 111 | Convalescent phase | /ˌkɒn.vəˈles.ənt feɪz/ | Giai đoạn hồi phục |
| 112 | Splenomegaly | /ˌspliː.nəˈmeɡ.əl.i/ | Lách to |
| 113 | Lymphadenopathy | /lɪmˌfæd.əˈnɒp.ə.θi/ | Bệnh hạch bạch huyết |
| 114 | Laboratory features | /ˈlæb.rə.tər.i ˈfiː.tʃərz/ | Đặc điểm cận lâm sàng |
| 115 | Alanine aminotransferase (ALT) | /ˈæl.ə.niːn əˌmiː.noʊˈtræns.fə.reɪs/ | Alanine aminotransferase |
| 116 | Aspartate aminotransferase (AST) | /ˈæs.pɑː.teɪt əˌmiː.noʊˈtræns.fə.reɪs/ | Aspartate aminotransferase |
| 117 | Bilirubin | /ˌbɪl.ɪˈruː.bɪn/ | Bilirubin |
| 118 | Cholestatic hepatitis | /ˌkɒl.ɪˈstæt.ɪk ˌhep.əˈtaɪ.tɪs/ | Viêm gan ứ mật |
| 119 | Alkaline phosphatase | /ˈæl.kə.laɪn ˈfɒs.fə.teɪs/ | Phosphatase kiềm |
| 120 | Prothrombin time | /proʊˈθrɒm.bɪn taɪm/ | Thời gian prothrombin |
| 121 | Albumin | /ælˈbjuː.mɪn/ | Albumin |
| 122 | Leukopenia | /ˌluː.kəˈpiː.ni.ə/ | Giảm bạch cầu |
| 123 | Lymphocytosis | /ˌlɪm.foʊ.saɪˈtoʊ.sɪs/ | Tăng lympho bào |
| 124 | Serologic diagnosis | /ˌsɪə.rəˈlɒdʒ.ɪk ˌdaɪ.əɡˈnoʊ.sɪs/ | Chẩn đoán huyết thanh học |
| 125 | Immunoglobulin (Ig) | /ˌɪm.jə.noʊˈɡlɒb.jə.lɪn/ | Globulin miễn dịch |
| 126 | Coagulopathy | /koʊˌæɡ.jəˈlɒp.ə.θi/ | Rối loạn đông máu |
| 127 | Leukocytosis | /ˌluː.koʊ.saɪˈtoʊ.sɪs/ | Tăng bạch cầu |
| 128 | Hyponatremia | /ˌhaɪ.poʊ.nəˈtriː.mi.ə/ | Hạ natri máu |
| 129 | Hypokalemia | /ˌhaɪ.poʊ.kəˈliː.mi.ə/ | Hạ kali máu |
| 130 | Hypoglycemia | /ˌhaɪ.poʊ.ɡlaɪˈsiː.mi.ə/ | Hạ đường huyết |
| 131 | Hypoalbuminemia | /ˌhaɪ.poʊ.ælˌbjuː.mɪˈniː.mi.ə/ | Giảm albumin máu |
| 132 | Outpatient observation | /ˈaʊtˌpeɪ.ʃənt ˌɒb.zəˈveɪ.ʃən/ | Theo dõi ngoại trú |
| 133 | Dehydration | /ˌdiː.haɪˈdreɪ.ʃən/ | Mất nước |
| 134 | Pathology | /pəˈθɒl.ə.dʒi/ | Bệnh học (mô bệnh học) |
| 135 | Cytotoxic T lymphocytes (CTLs) | /ˌsaɪ.toʊˈtɒk.sɪk tiː ˈlɪm.fə.saɪts/ | Tế bào lympho T gây độc tế bào |
| 136 | Tumor necrosis factor alpha | /ˈtjuː.mər nəˈkroʊ.sɪs ˈfæk.tər ˈæl.fə/ | Yếu tố hoại tử khối u alpha |
| 137 | Gamma interferon | /ˈɡæm.ə ˌɪn.təˈfɪə.rɒn/ | Gamma interferon |
| 138 | Fulminant hepatitis | /ˈfʊl.mɪ.nənt ˌhep.əˈtaɪ.tɪs/ | Viêm gan tối cấp |
| 139 | Lymphocytic infiltrate | /ˌlɪm.fəˈsɪt.ɪk ˈɪn.fɪl.treɪt/ | Thâm nhiễm tế bào lympho |
| 140 | Portal tracts | /ˈpɔː.təl træks/ | Khoảng cửa |
| 141 | Ground-glass hepatocytes | /ɡraʊnd ɡlɑːs həˈpæt.ə.saɪts/ | Tế bào gan dạng kính mờ |
| 142 | Hematoxylin-eosin | /ˌhiː.mə.təˈzɒk.sɪ.lɪn ˌiː.əˈsɪn/ | Nhuộm Hematoxylin-eosin |
| 143 | Necroinflammation | /ˌnek.roʊ.ɪn.fləˈmeɪ.ʃən/ | Hoại tử-viêm |
| 144 | Histologic prognostic factor | /ˌhɪs.təˈlɒdʒ.ɪk prɒɡˈnɒs.tɪk ˈfæk.tər/ | Yếu tố tiên lượng mô học |
| 145 | Right upper quadrant pain | /raɪt ˈʌp.ər ˈkwɒd.rənt peɪn/ | Đau hạ sườn phải |
| 146 | Polyarteritis nodosa | /ˌpɒl.i.ɑː.təˈraɪ.tɪs noʊˈdoʊ.sə/ | Viêm đa động mạch nút |
| 147 | Mixed essential cryoglobulinemia | /mɪkst ɪˈsen.ʃəl ˌkraɪ.oʊˌɡlɒb.jə.lɪˈniː.mi.ə/ | Cryoglobulin máu hỗn hợp thiết yếu |
| 148 | Seroconversion | /ˌsɪə.roʊ.kənˈvɜː.ʃən/ | Chuyển đổi huyết thanh |
| 149 | Aflatoxin | /ˌæf.ləˈtɒk.sɪn/ | Aflatoxin |
| 150 | Obesity | /əʊˈbiː.sə.ti/ | Béo phì |
| 151 | Diabetes mellitus | /ˌdaɪ.əˈbiː.tiːz ˈmel.ɪ.təs/ | Đái tháo đường |
| 152 | Quantitative HBV DNA | /ˈkwɒn.tɪ.tə.tɪv eɪtʃ.biː.viː diː.en.eɪ/ | Định lượng HBV DNA |
| 153 | International normalized ratio (INR) | /… ˈnɔː.mə.laɪzd ˈreɪ.ʃi.oʊ/ | Tỷ lệ chuẩn hóa quốc tế |
| 154 | Steatohepatitis | /ˌstiː.ə.toʊˌhep.əˈtaɪ.tɪs/ | Viêm gan nhiễm mỡ |
| 155 | Iron overload | /ˈaɪən ˈəʊ.və.loʊd/ | Quá tải sắt |
| 156 | Autoimmune hepatitis | /ˌɔː.toʊ.ɪˈmjuːn ˌhep.əˈtaɪ.tɪs/ | Viêm gan tự miễn |
| 157 | Ultrasound elastography | /ˈʌl.trə.saʊnd ɪˌlæsˈtɒɡ.rə.fi/ | Đo độ đàn hồi gan bằng siêu âm |
| 158 | Noninvasive methods | /ˌnɒn.ɪnˈveɪ.sɪv ˈmeθ.ədz/ | Phương pháp không xâm lấn |
| 159 | Durable suppression | /ˈdʒʊə.rə.bəl səˈpreʃ.ən/ | Ức chế bền vững |
| 160 | Seroreversion | /ˌsɪə.roʊ.rɪˈvɜː.ʃən/ | Tái chuyển đổi huyết thanh |
| 161 | Relapse | /rɪˈlæps/ | Tái phát |
| 162 | Viral rebound | /ˈvaɪ.rəl ˈriː.baʊnd/ | Tái bùng phát virus |
| 163 | Poor adherence | /pʊər ədˈhɪə.rəns/ | Tuân thủ kém |
| 164 | Genotypic resistance | /ˌdʒen.əˈtɪp.ɪk rɪˈzɪs.təns/ | Đề kháng genotype |
| 165 | Phenotypic resistance | /ˌfiː.nəˈtɪp.ɪk rɪˈzɪs.təns/ | Đề kháng kiểu hình |
| 166 | In vitro susceptibility | /ɪn ˈviː.troʊ səˌsep.təˈbɪl.ə.ti/ | Tính nhạy cảm trong ống nghiệm |
| 167 | Cumulative frequency | /ˈkjuː.mjə.lə.tɪv ˈfriː.kwən.si/ | Tần suất tích lũy |
| 168 | Tamponade (Third trimester) | /ˈθɜːd traɪˈmes.tər/ | Tam cá nguyệt thứ ba |
| 169 | Reactivation | /ˌriː.æk.tɪˈveɪ.ʃən/ | Tái hoạt |
| 180 | Screening | /ˈskriː.nɪŋ/ | Sàng lọc |
| 181 | Rituximab | /rɪˈtʌk.sɪ.mæb/ | Rituximab |
| 182 | Immunoprophylaxis | /ˌɪm.jə.noʊˌproʊ.fɪˈlæk.sɪs/ | Dự phòng miễn dịch |
| 183 | Preexposure | /ˌpriː.ɪkˈspoʊ.ʒər/ | Trước phơi nhiễm |
| 184 | Recombinant | /ˌriːˈkɒm.bɪ.nənt/ | Tái tổ hợp |
| 185 | Immunogen | /ˈɪm.jə.nə.dʒən/ | Kháng nguyên (sinh miễn dịch) |
| 186 | Immunogenic | /ˌɪm.jə.noʊˈdʒen.ɪk/ | Sinh miễn dịch |
| 187 | Booster dose | /ˈbuː.stər doʊs/ | Liều tăng cường |
| 188 | Immunotherapeutic value | /ˌɪm.jə.noʊˌθer.əˈpjuː.tɪk ˈvæl.juː/ | Giá trị điều trị miễn dịch |
| 189 | Postexposure | /ˌpoʊst.ɪkˈspoʊ.ʒər/ | Sau phơi nhiễm |
| 190 | Hepatitis B immune globulin (HBIG) | /… ɪˈmjuːn ˈɡlɒb.jə.lɪn/ | Globulin miễn dịch viêm gan B |
| 191 | Satellite virus | /ˈsæt.əl.aɪt ˈvaɪ.rəs/ | Virus vệ tinh |
| 192 | Viroidlike | /ˈvaɪ.rɔɪd.laɪk/ | Giống viroid |
| 193 | Pathogenicity | /ˌpæθ.ə.dʒəˈnɪs.ə.ti/ | Khả năng gây bệnh |
| 194 | Phosphoprotein | /ˌfɒs.foʊˈproʊ.tiːn/ | Phosphoprotein |
| 195 | Isoforms | /ˈaɪ.soʊ.fɔːmz/ | Dạng đồng phân |
| 196 | Prenylated | /ˈpriː.nɪ.leɪ.tɪd/ | Được prenyl hóa |
| 197 | Antigenome | /ˈæn.ti.dʒi.noʊm/ | Antigenome (bộ gen đối) |
| 198 | Transfected | /trænsˈfekt.ɪd/ | Được chuyển nạp |
| 199 | Coinfection | /ˌkoʊ.ɪnˈfek.ʃən/ | Đồng nhiễm |
| 200 | Superinfection | /ˌsuː.pər.ɪnˈfek.ʃən/ | Bội nhiễm |
