Cẩm nang Hô hấp Can thiệp. Practical Guide to Interventional Pulmonology
Bản quyền (C) 2024 Nhà xuất bản Elsevier.
Ts.Bs. Lê Nhật Huy – Ths.Bs. Lê Đình Sáng (Dịch và chú giải)
LỜI GIỚI THIỆU
Momen M. Wahidi và David E. Ost
Trong thập kỷ qua, Hô hấp Can thiệp (IP) đã phát triển thành một chuyên ngành được công nhận, cung cấp các dịch vụ tư vấn và thủ thuật chuyên sâu cho bệnh nhân mắc bệnh lý ác tính lồng ngực, bệnh lý đường thở về mặt giải phẫu và bệnh lý màng phổi. Giống như nhiều chuyên ngành y khoa thiên về thủ thuật khác, không phải lúc nào cũng có đủ dữ liệu để định hướng cho mọi khía cạnh của việc thực hiện một thủ thuật Hô hấp Can thiệp nhất định. Do đó, có sự khác biệt đáng kể giữa các bác sĩ trong cách thực hiện thủ thuật. Nhiều ấn phẩm tập trung vào bằng chứng về hiệu quả của các can thiệp IP nhưng lại không cung cấp lời khuyên thiết thực về cách thực hiện các thủ thuật đó. Các chi tiết thủ thuật thường chỉ được gói gọn trong một đoạn văn duy nhất ở phần phương pháp của các nghiên cứu gốc. Điều này khiến các học viên và bác sĩ đang hành nghề khi học một thủ thuật mới bị thiếu hụt thông tin thực tế về cách thực sự tiến hành chúng.
Trong cuốn sách này, chúng tôi hướng đến việc trình bày một phương pháp tiếp cận thực tế đối với các thủ thuật IP, tập trung vào việc lựa chọn bệnh nhân, chuẩn bị trước thủ thuật (bao gồm trang thiết bị, nhân sự và môi trường thực hiện), kỹ thuật thực hiện thủ thuật, các biến chứng và tóm tắt ngắn gọn về bằng chứng. Cuốn sách được sắp xếp thành các chương bao gồm các thủ thuật IP chẩn đoán và điều trị, cũng như các phương pháp tiếp cận đa mô thức đối với tắc nghẽn đường thở ác tính và lành tính, và kết thúc bằng một số lời khuyên thiết thực về cách xây dựng và lãnh đạo một chương trình IP. Chúng tôi đã thiết kế các chương về thủ thuật theo một trình tự tương tự và trình bày nhất quán các bước thực hành đã đề cập của các thủ thuật IP. Chúng tôi cũng bổ sung cho cuốn sách những hình ảnh màu và hình minh họa gốc.
Mục tiêu của cuốn sách này là nắm bắt được “bí quyết thủ thuật” cũng như nền tảng khoa học trong thực hành IP. “Bí quyết thủ thuật” trong bối cảnh này thực sự đề cập đến cách thực hiện một thủ thuật. Nó bao gồm các mẹo và thủ thuật từ các bác sĩ giàu kinh nghiệm, những điều có thể chưa đạt đến mức độ bằng chứng cần thiết cho một hướng dẫn nhưng lại hữu ích và thường là thiết yếu cho thực hành hàng ngày. Để đạt được mục tiêu này, mỗi chương được viết bởi các chuyên gia trong lĩnh vực, những người sử dụng các kỹ thuật này trong thực hành hàng ngày của họ. Suy cho cùng, khi học lái máy bay, bạn muốn học từ ai hơn: một kỹ sư hàng không vũ trụ có bằng tiến sĩ hay một phi công giàu kinh nghiệm, người lái cùng loại máy bay mà bạn sắp lái?
Cuốn sách này bao gồm các thủ thuật IP được thực hiện thường xuyên nhất, nhưng một số thủ thuật IP hiếm gặp không được đưa vào. Mặc dù nội dung có thể được xem là lý tưởng cho những người mới bắt đầu với các thủ thuật IP, chẳng hạn như các học viên chuyên khoa Hô hấp, Hô hấp Can thiệp và Phẫu thuật Lồng ngực, nó thực sự là một tài liệu tổng quan tuyệt vời cho các bác sĩ lâm sàng đã thực hiện các thủ thuật này. Đây là cơ hội để đánh giá xem liệu có những phong cách thực hiện khác nhau cho một số thủ thuật nhất định hay không, hoặc đơn giản là để ôn lại toàn bộ phổ các thủ thuật IP: cả cũ và mới. Hãy pha một tách cà phê hoặc trà vào buổi sáng Chủ nhật này và đắm mình trong nội dung phong phú, dễ đọc cùng với các mẹo và thủ thuật từ các chuyên gia trong lĩnh vực đang phát triển mạnh mẽ này.
LỜI TỰA – CHO BẢN DỊCH TIẾNG VIỆT |
Quý đồng nghiệp và bạn đọc thân mến,
Hô hấp Can thiệp là một chuyên ngành tương đối mới nhưng đã có những bước phát triển vượt bậc trong thập kỷ qua, trở thành một phần không thể thiếu trong chẩn đoán và điều trị các bệnh lý lồng ngực, đặc biệt là bệnh lý ác tính, bệnh lý đường thở và màng phổi. Cùng với sự phát triển của y học thế giới, các bác sĩ chuyên khoa Hô hấp tại Việt Nam cũng đang không ngừng học hỏi, cập nhật và ứng dụng những kỹ thuật tiên tiến nhất để nâng cao chất lượng chăm sóc người bệnh.
Trong bối cảnh đó, việc tiếp cận với các tài liệu y văn chất lượng, cập nhật và mang tính thực tiễn cao là vô cùng cần thiết. Cuốn sách “Practical Guide to Interventional Pulmonology” của hai chuyên gia hàng đầu là GS. Momen M. Wahidi và GS. David E. Ost đã được cộng đồng y khoa quốc tế đánh giá rất cao như một cẩm nang toàn diện, ngắn gọn, dựa trên bằng chứng và đặc biệt chú trọng vào kinh nghiệm thực hành. Cuốn sách không chỉ trình bày kiến thức khoa học mà còn chia sẻ những “bí quyết thủ thuật” quý báu, từ việc lựa chọn bệnh nhân, chuẩn bị thủ thuật cho đến các kỹ thuật chi tiết và xử trí biến chứng.
Với mong muốn mang nguồn tri thức quý giá này đến gần hơn với các đồng nghiệp tại Việt Nam, chúng tôi đã quyết định thực hiện chuyển thể cuốn sách sang tiếng Việt với tựa đề “Cẩm nang Hô hấp Can thiệp”. Đây là tâm huyết của đội ngũ biên dịch với hy vọng cuốn sách sẽ trở thành người bạn đồng hành đáng tin cậy cho các bác sĩ, học viên chuyên khoa Hô hấp, Hô hấp Can thiệp và Phẫu thuật Lồng ngực trên con đường học tập và hành nghề.
Bản dịch tiếng Việt này không chỉ nỗ lực truyền tải chính xác nội dung của bản gốc mà còn được bổ sung những điểm nhấn riêng biệt nhằm tối ưu hóa trải nghiệm cho độc giả Việt Nam:
- Bảng chú giải thuật ngữ Y học Anh – Việt: Mỗi chương đều được đính kèm một bảng chú giải chi tiết các thuật ngữ chuyên ngành xuất hiện trong chương, giúp bạn đọc dễ dàng tra cứu, đối chiếu và nâng cao vốn từ vựng tiếng Anh y khoa.
- Hình ảnh và sơ đồ trực quan: Toàn bộ các lược đồ, sơ đồ trong sách đã được đội ngũ kỹ thuật vẽ lại một cách tỉ mỉ để đảm bảo tính thẩm mỹ, trực quan và dễ hiểu hơn, trong khi vẫn giữ vững sự chính xác về mặt khoa học so với bản gốc.
Chúng tôi tin rằng, với những nỗ lực này, “Cẩm nang Hô hấp Can thiệp” sẽ là một công cụ học tập và tham khảo hữu ích, giúp quý đồng nghiệp tự tin hơn trong thực hành lâm sàng hàng ngày.
Cuốn sách này được cung cấp bản đọc trực tuyến miễn phí tại website yhoclamsang.net và có thể tải xuống dạng ebook PDF (miễn phí) dành cho thành viên của Thư viện Y học Medipharm trên nền tảng sachyhoc.com.
Xin trân trọng giới thiệu cuốn sách đến quý bạn đọc.
Vinh, ngày 01 tháng 07 năm 2025
TS.BS. Lê Nhật Huy – ThS.BS. Lê Đình Sáng

| Chương 2: Siêu âm nội soi phế quản đầu dò lồi (Linear EBUS) Linear Endobronchial Ultrasound Terunaga Inage Yasufuku, Alexander Gregor, and Tsukasa Ishiwata, Kazuhiro Practical Guide to Interventional Pulmonology, 2, 5-16 |
GIỚI THIỆU
Năm 2002, một loại ống nội soi phế quản mới được phát triển bằng cách tích hợp một đầu dò siêu âm dạng lồi (convex) ở đầu ống và được đưa vào ứng dụng lâm sàng. Siêu âm nội soi phế quản đầu dò lồi (CP-EBUS), còn được gọi là EBUS đầu dò lồi (linear EBUS), có thể kết hợp với một kim sinh thiết chuyên dụng để thực hiện chọc hút bằng kim xuyên thành phế quản dưới hướng dẫn của siêu âm nội soi thời gian thực (EBUS-TBNA) đối với các tổn thương phổi cạnh phế quản ở trung tâm, các hạch bạch huyết trung thất và hạch rốn phổi. EBUS-TBNA sử dụng đầu dò lồi là một phương thức xâm lấn tối thiểu đã được công nhận rộng rãi để chẩn đoán và phân giai đoạn ung thư phổi. Các hướng dẫn điều trị ung thư phổi khuyến nghị kết hợp EBUS-TBNA với chọc hút bằng kim nhỏ qua siêu âm nội soi (EUS-FNA, còn gọi là EUS-B-FNA nếu ống nội soi EBUS được sử dụng trong thủ thuật kết hợp) là xét nghiệm đầu tay tốt nhất để phân giai đoạn hạch trung thất trong ung thư phổi. Trong 20 năm qua, vai trò của phương thức xâm lấn tối thiểu này đã được mở rộng, bao gồm tái phân giai đoạn sau điều trị tân bổ trợ và lấy thêm mẫu để xét nghiệm dấu ấn sinh học. Những tiến bộ trong phân tích hình ảnh siêu âm đã mở rộng khả năng của EBUS đầu dò lồi. Do đó, EBUS-TBNA hiện nay cũng đã trở thành một công cụ chẩn đoán xâm lấn tối thiểu cho u lympho, sarcoidosis, lao, các nang trung thất và các bệnh lý ác tính khác trong lồng ngực. Các loại kim sinh thiết mới sẽ tiếp tục mở rộng tiềm năng của EBUS-TBNA trong chuyên ngành hô hấp. Việc sử dụng EBUS đầu dò lồi như một phương thức điều trị, thông qua tiêm xuyên thành phế quản, cũng ngày càng nhận được nhiều sự quan tâm và bằng chứng. EBUS đầu dò lồi tiếp tục đóng một vai trò thiết yếu trong chẩn đoán bệnh và đang đảm nhận những chỉ định mới với những ý nghĩa lâm sàng tiềm năng quan trọng.
CHUẨN BỊ TRƯỚC THỦ THUẬT
Chỉ định của Siêu âm nội soi phế quản đầu dò lồi
Chỉ định ban đầu của EBUS đầu dò lồi là chẩn đoán và phân giai đoạn hạch trong ung thư phổi. Nghi ngờ các bệnh lý ác tính khác trong lồng ngực, chẳng hạn như u lympho, sarcoma, u trung biểu mô và các di căn trung thất khác, cũng như các tình trạng lành tính như sarcoidosis, lao và nang trung thất, cũng có thể được xem là chỉ định sinh thiết bằng EBUS-TBNA. Các can thiệp điều trị dưới hướng dẫn của EBUS đang được nghiên cứu. Có nhiều loại ống nội soi phế quản EBUS khác nhau. Tuy nhiên, nhìn chung, kích thước và độ linh hoạt của các ống nội soi EBUS hiện có cho phép tiếp cận đáng tin cậy nhất đến các tổn thương trung tâm và trong nhiều trường hợp là vùng giữa phổi của các thùy dưới. Khả năng tiếp cận của các ống nội soi EBUS hiện tại đến các phế quản cụ thể bị hạn chế hơn so với các ống nội soi phế quản thông thường, đặc biệt là khi đưa kim sinh thiết vào kênh thủ thuật. Việc tiếp cận các thùy trên, đặc biệt là ngoại vi thùy trên, có thể khó khăn hơn. Các ống nội soi phế quản EBUS và kim linh hoạt hơn giúp cải thiện khả năng tiếp cận vùng ngoại vi đang được phát triển.
Trang thiết bị
- Ống nội soi phế quản siêu âm đầu dò lồi
- Bộ xử lý siêu âm đa năng
- Kim EBUS-TBNA (kích thước 19-gauge [G], 21-G, 22-G, và/hoặc 25-G)
Nhân sự
- Bác sĩ nội soi phế quản
- Kỹ thuật viên nội soi/hô hấp
- Điều dưỡng phụ trách an thần hoặc đội ngũ gây mê
- Bác sĩ giải phẫu bệnh tế bào (tùy chọn)
- Kỹ thuật viên giải phẫu bệnh tế bào (tùy chọn)
Môi trường thực hiện
Thủ thuật có thể được thực hiện trong phòng nội soi hoặc phòng mổ, với an thần tỉnh hoặc gây mê toàn thân. Ống nội soi phế quản siêu âm đầu dò lồi có thể được đưa vào đường thở qua đường miệng. Có thể tùy chọn sử dụng ống nội khí quản hoặc mặt nạ thanh quản.
KỸ THUẬT THỰC HIỆN THỦ THUẬT
Chuẩn bị chung cho EBUS/EBUS-TBNA đầu dò lồi
Một bóng cao su chuyên dụng được gắn vào đầu dò của ống nội soi EBUS bằng dụng cụ gắn bóng và được bơm căng bằng nước muối sinh lý trong quá trình EBUS-TBNA. Một bơm tiêm 20 mL và dây nối dài chứa đầy nước muối được kết nối với kênh dẫn bóng. Cần khoảng 0,3 đến 0,5 mL nước muối để bơm căng bóng thích hợp. Vì bóng được làm bằng cao su, không thể sử dụng cho bệnh nhân dị ứng với cao su.
EBUS-TBNA có thể được thực hiện dưới gây tê tại chỗ với an thần tỉnh nhẹ hoặc gây mê toàn thân. Với gây tê tại chỗ, ống nội soi EBUS được đưa vào qua đường miệng và 1% lidocain (liều bolus 2 mL) được bơm nhẹ nhàng vào đường thở qua kênh dụng cụ. Với gây mê toàn thân, thường sử dụng ống nội khí quản (đường kính trong ít nhất 8,0 mm) hoặc mặt nạ thanh quản (số 4). Gây mê toàn thân với các dụng cụ đường thở này mang lại một số lợi thế như đưa ống nội soi EBUS vào dễ dàng hơn và giảm ho. Điều này phải được cân bằng với các cân nhắc về hậu cần và an toàn của gây mê toàn thân.
Sau khi an thần hoặc khởi mê, một ống nội soi phế quản mềm thông thường được đưa vào đường thở trước. Nội soi phế quản chẩn đoán ban đầu giúp thực hiện EBUS an toàn hơn thông qua việc làm sạch dịch tiết, xác định các tổn thương đường thở, xác minh giải phẫu cây phế quản và sử dụng thêm thuốc tê tại chỗ nếu cần. Sau khi hoàn tất, ống nội soi mềm được rút ra và có thể bắt đầu sinh thiết dưới hướng dẫn của EBUS. Việc đưa và thao tác ống nội soi phế quản EBUS có thể khó khăn hơn so với ống nội soi phế quản mềm thông thường. Hệ thống quang học của ống nội soi phế quản EBUS bị giới hạn bởi góc nhìn chéo về phía trước so với vị trí trung tính của ống nội soi và đầu dò siêu âm. Việc gập ống nội soi xuống để có góc nhìn “trực diện” truyền thống trong quá trình đưa ống EBUS có thể vô tình gây tổn thương do kéo mạnh đầu dò siêu âm. Thay vào đó, ống nội soi phế quản EBUS nên được đưa vào ở vị trí trung tính, thỉnh thoảng dừng lại và gập xuống để xác nhận vị trí nếu cần.
EBUS/EBUS-TBNA cho các tổn thương cụ thể
Nếu EBUS được thực hiện để lấy mô từ một tổn thương phổi hoặc trung thất cụ thể, ống nội soi phế quản EBUS được điều hướng đến khu vực đã được lên kế hoạch dựa trên việc xem xét hình ảnh trước thủ thuật. Bóng siêu âm nên được bơm căng nhẹ nhàng và ống nội soi gập lên trên để tối đa hóa sự tiếp xúc với thành phế quản. Khi tổn thương đã được định vị ở trung tâm trên hình ảnh siêu âm, vỏ kim EBUS được đẩy ra ngoài kênh thủ thuật, sau đó là kim sinh thiết. Cần chú ý theo dõi cả hình ảnh ánh sáng trắng và hình ảnh siêu âm trong quá trình đẩy kim, vì ống nội soi có thể di chuyển khi kim được đẩy về phía trước. Lý tưởng nhất, đối với các tổn thương trung thất, kim nên được triển khai vào các khoảng trống giữa các vòng sụn.
EBUS/EBUS-TBNA hạch bạch huyết để phân giai đoạn ung thư phổi
Phân giai đoạn hạch bạch huyết nên được thực hiện một cách nhất quán, có hệ thống để thúc đẩy việc phân giai đoạn chính xác. Các hạch bạch huyết được kiểm tra bằng EBUS để ghi nhận vị trí, kích thước và các đặc điểm siêu âm khác (xem phần sau), theo hệ thống phân giai đoạn của Ủy ban Liên hợp về Ung thư Hoa Kỳ (AJCC)/Hiệp hội Kiểm soát Ung thư Quốc tế (UICC). EBUS-TBNA có khả năng tiếp cận hạn chế đối với các hạch bạch huyết ở xa đường thở trung tâm như hạch trước mạch máu (vị trí 3a), hạch dưới quai động mạch chủ/cạnh động mạch chủ (vị trí 5 và 6), và hạch cạnh thực quản/dây chằng phổi (vị trí 8 và 9). Tuy nhiên, cả hai thủ thuật nội soi siêu âm qua phế quản và qua thực quản đều có thể được thực hiện bằng một ống nội soi EBUS duy nhất, thường được gọi là EUS-B-FNA, có thể tạo điều kiện tiếp cận các vị trí 8 và 9 cũng như các đường tiếp cận thay thế cho các vị trí khác. EUS-B-FNA mang lại những lợi thế tiềm năng về mặt hậu cần. Tuy nhiên, nếu đang cân nhắc EUS-B-FNA, chúng tôi khuyên nên thực hiện phần qua thực quản sau phần qua phế quản của thủ thuật để tránh nhiễm bẩn hệ hô hấp.
Một kim TBNA chuyên dụng được đưa qua kênh thủ thuật của ống nội soi phế quản EBUS, và hạch bạch huyết được chỉ định sẽ được chọc dưới sự hướng dẫn của EBUS thời gian thực. Bệnh phẩm hút ra sau đó có thể được gửi đi để chẩn đoán tế bào học/bệnh học. Có một nguy cơ lý thuyết về việc nhiễm bẩn kim sinh thiết hoặc kênh thủ thuật khi ống nội soi được di chuyển từ hạch bạch huyết này sang hạch khác, có nguy cơ làm tăng giai đoạn bệnh. Do đó, thường khuyến nghị sinh thiết hạch N3 trước, sau đó là N2, rồi đến N1. Mặc dù không cần thiết, một bác sĩ giải phẫu bệnh tế bào tại chỗ có thể cung cấp phản hồi ngay lập tức về chất lượng của mẫu sinh thiết và có thể đưa ra chẩn đoán sơ bộ. Thông tin này có thể được sử dụng để đưa ra quyết định về việc lặp lại sinh thiết trong cùng một thủ thuật.
BIẾN CHỨNG
EBUS-TBNA với EBUS đầu dò lồi là một phương thức xâm lấn tối thiểu an toàn và đã được công nhận để lấy mẫu các tổn thương cạnh phế quản ở trung tâm. Tỷ lệ biến chứng rất thấp, nhưng các biến chứng nghiêm trọng bao gồm chảy máu, nhiễm trùng, liệt dây thần kinh quặt ngược và tử vong đã được báo cáo.
BẰNG CHỨNG
Ung thư phổi
Phân giai đoạn hạch trong ung thư phổi
Tiên lượng và khả năng phẫu thuật của một bệnh nhân ung thư phổi bị ảnh hưởng bởi sự hiện diện của di căn hạch bạch huyết trung thất. Một phân tích tổng hợp đã tính toán độ nhạy gộp là 0,93 (khoảng tin cậy [CI] 95%, 0,91-0,94) và độ đặc hiệu gộp là 1,00 (KTC 95%, 0,99-1,00) để phát hiện bệnh lý hạch trung thất qua 11 nghiên cứu. Độ nhạy, độ đặc hiệu và độ chính xác của EBUS-TBNA cao hơn so với chụp cắt lớp phát xạ positron (PET) hoặc PET-chụp cắt lớp vi tính (PET-CT) trong hai thử nghiệm tiền cứu. Sự kết hợp giữa EBUS-TBNA và EUS-FNA có độ chính xác phân giai đoạn cao hơn so với từng thủ thuật riêng lẻ đối với bệnh nhân ung thư phổi, với độ nhạy là 0,86 (KTC 95%, 0,82-0,90) và độ đặc hiệu là 1,00 (KTC 95%, 0,99-1,00) trong một phân tích tổng hợp bao gồm tám nghiên cứu. Trong thử nghiệm ASTER, phân giai đoạn kết hợp với EBUS-TBNA cộng với EUS-FNA ban đầu, sau đó là phân giai đoạn phẫu thuật cho thấy hiệu quả chẩn đoán cao hơn và ít trường hợp mở lồng ngực không cần thiết hơn so với chỉ phân giai đoạn phẫu thuật. Các hướng dẫn được công bố gần đây về phân giai đoạn trung thất ban đầu trong ung thư phổi khuyến nghị rằng sinh thiết bằng kim dưới hướng dẫn siêu âm (EBUS-TBNA và/hoặc EUS-FNA) là phương thức lựa chọn đầu tay so với phân giai đoạn phẫu thuật. Tuy nhiên, nếu kết quả sinh thiết EBUS/EUS âm tính, khuyến nghị thực hiện phân giai đoạn phẫu thuật thông qua nội soi trung thất hoặc nội soi trung thất qua video.
Phân tích hình ảnh siêu âm của hạch bạch huyết
Trong quá trình EBUS-TBNA, các đặc điểm siêu âm rất hữu ích để phân biệt hạch bạch huyết ác tính và lành tính. Một số đặc điểm trên hình ảnh B-mode, chẳng hạn như kích thước (trục ngắn), hình dạng (bầu dục so với tròn), bờ (không rõ so với rõ), độ hồi âm (đồng nhất so với không đồng nhất), cấu trúc rốn hạch trung tâm (CHS) (có so với không có), và dấu hiệu hoại tử đông (có so với không có), đã được chứng minh là những dấu hiệu dự báo tốt cho di căn hạch bạch huyết trong ung thư phổi không tế bào nhỏ (NSCLC). Fujiwara và cộng sự đã báo cáo hình dạng tròn, bờ rõ, độ hồi âm không đồng nhất và sự hiện diện của dấu hiệu hoại tử đông là các yếu tố nguy cơ độc lập cho di căn. Alici và cộng sự đã tích hợp kết cấu thang độ xám (trống âm, giảm âm, đồng âm, hoặc tăng âm) với sáu đặc điểm trước đó để tạo ra một thuật toán sửa đổi. Độ nhạy, độ đặc hiệu, giá trị dự báo dương tính (PPV), giá trị dự báo âm tính (NPV) và độ chính xác chẩn đoán của thuật toán này để phát hiện hạch di căn lần lượt là 100%, 51,2%, 50,6%, 100% và 67,5%. Hình ảnh Doppler cho phép đánh giá lưu lượng máu và các dạng mạch máu của hạch. Nakajima và cộng sự đã phân loại các hạch bạch huyết theo các dấu hiệu Doppler: độ 0, không có dòng chảy hoặc lượng dòng chảy nhỏ; độ I, một vài mạch máu chính chạy về phía trung tâm của hạch bạch huyết từ rốn hạch; độ II, một vài tín hiệu dòng chảy hình nêm hoặc hình que, hoặc một vài mạch máu nhỏ được tìm thấy dưới dạng một dải dài cong; và độ III, dòng chảy phong phú với hơn bốn mạch máu có đường kính khác nhau và/hoặc tín hiệu dòng chảy xoắn/xoắn ốc. Độ nhạy, độ đặc hiệu và độ chính xác chẩn đoán của hệ thống phân loại này (độ 0/I lành tính so với độ II/III ác tính) lần lượt là 87,7%, 69,6% và 78,0%. Wang và cộng sự đã phân loại các dạng mạch máu Doppler thành không có mạch, dạng rốn hạch và không phải rốn hạch (trung tâm, bao hạch, hoặc hỗn hợp); các tác giả đã kết hợp các đặc điểm mạch máu này với sáu đặc điểm siêu âm trước đó để dự đoán tình trạng hạch bạch huyết lành tính. Độ nhạy, độ đặc hiệu, PPV và NPV để dự đoán hạch lành tính lần lượt là 81,3%, 90,9%, 85,3% và 88,2%.
Siêu âm đàn hồi mô (Elastography) là một kỹ thuật hình ảnh biến dạng để đánh giá độ cứng của mô, được hiển thị dưới dạng một lớp phủ màu trên hình ảnh siêu âm B-mode. Hầu hết các hệ thống xác định các mô cứng, trung gian và mềm tương ứng với màu xanh dương, xanh lá cây và vàng/đỏ. Izumo và cộng sự đã phân loại các mẫu hình ảnh siêu âm đàn hồi mô thành loại 1 (chủ yếu không phải màu xanh dương), loại 2 (một phần xanh dương, một phần không phải xanh dương), và loại 3 (chủ yếu màu xanh dương). Độ nhạy, độ đặc hiệu, PPV, NPV và độ chính xác chẩn đoán của hệ thống phân loại này (loại 1 lành tính so với loại 3 ác tính) lần lượt là 100,0%, 92,3%, 94,6%, 100,0% và 96,7%. Nakajima và cộng sự đã so sánh các hạch theo tỷ lệ diện tích cứng (diện tích màu xanh dương cứng chia cho tổng diện tích hạch bạch huyết) và thấy rằng tỷ lệ độ cứng trung bình ở các hạch di căn (0,48) cao hơn đáng kể so với các hạch lành tính (0,22, P=0,0002). Khi sử dụng ngưỡng tỷ lệ 0,31, độ nhạy và độ đặc hiệu lần lượt là 81% và 85%.
Một lĩnh vực đang được chú trọng phát triển là ứng dụng công nghệ trí tuệ nhân tạo để phân tầng nguy cơ ác tính trên hình ảnh EBUS. Một nghiên cứu năm 2008 của Tagoya và cộng sự đã phát triển một mạng nơ-ron nhân tạo để dự đoán sự hiện diện của di căn hạch bằng hình ảnh EBUS B-mode, cuối cùng đạt độ chính xác chẩn đoán là 91%. Độ nhạy, độ đặc hiệu và độ chính xác của hệ thống này lần lượt là 87,0%, 82,1% và 85,4%. Việc ứng dụng trí tuệ nhân tạo có thể tạo ra những tiến bộ đáng kể trong tương lai cho việc phân tích hình ảnh EBUS.
Tái phân giai đoạn sau điều trị tân bổ trợ
Hiện tại, phương pháp điều trị được khuyến nghị cho NSCLC giai đoạn IIIA-cN2 là hóa xạ trị. Tuy nhiên, phẫu thuật cắt bỏ sau hóa trị hoặc hóa xạ trị tân bổ trợ có thể cải thiện sự sống còn của bệnh nhân mắc bệnh giai đoạn IIIA-cN2. Việc tái phân giai đoạn chính xác các hạch bạch huyết trung thất trong những trường hợp này là rất quan trọng để xác nhận sự giảm giai đoạn của trung thất trước khi xem xét phẫu thuật. Nội soi trung thất lặp lại cũng có thể được xem xét; tuy nhiên, nội soi trung thất sau điều trị tân bổ trợ có thể khó khăn và hiệu quả chẩn đoán bị giảm do sự phát triển của xơ hóa và dính. Một tổng quan hệ thống gồm năm nghiên cứu đã tính toán độ nhạy gộp, độ đặc hiệu và tỷ lệ âm tính giả của nội soi trung thất lặp lại sau điều trị tân bổ trợ lần lượt là 63%, 100% và 22%. Phẫu thuật cắt bỏ hạch trung thất mở rộng qua đường cổ đã cho thấy độ nhạy 96,6% trong tái phân giai đoạn trung thất ở bệnh nhân NSCLC sau điều trị tân bổ trợ. Tỷ lệ tử vong và bệnh suất lần lượt là 0,3% và 6,4%. Tương tự, tái phân giai đoạn bằng EBUS-TBNA sau điều trị tân bổ trợ được báo cáo là có độ nhạy thấp hơn so với EBUS-TBNA được sử dụng trong quá trình phân giai đoạn ung thư phổi ban đầu. Một tổng quan hệ thống và phân tích tổng hợp bao gồm 10 nghiên cứu cho thấy sinh thiết bằng kim dưới hướng dẫn của nội soi siêu âm (EBUS-TBNA, EUS-FNA, hoặc siêu âm nội soi kết hợp qua thực quản và phế quản [CUS]) để tái phân giai đoạn trung thất có độ nhạy gộp là 67% (KTC 95%, 56-77) và độ đặc hiệu gộp là 99% (KTC 95%, 89-100). Sự khác biệt về hiệu quả chẩn đoán giữa phân giai đoạn ban đầu và tái phân giai đoạn có thể liên quan đến khó khăn trong việc lấy đủ mẫu từ các hạch đã giảm giai đoạn, vốn có thể nhỏ hơn, xơ hóa và/hoặc hoại tử sau điều trị tân bổ trợ. Cũng có khó khăn trong việc phân biệt hình dạng siêu âm của di căn với các dính sau viêm và các thay đổi thoái hóa. Kết hợp EBUS-TBNA và EUS-FNA có thể cho phép tái phân giai đoạn trung thất xâm lấn tối thiểu chính xác hơn. Các hướng dẫn hiện hành khuyến nghị EBUS-TBNA và/hoặc EUS-FNA để tái phân giai đoạn trung thất sau điều trị tân bổ trợ, tránh nội soi trung thất lặp lại.
Xét nghiệm phân tử sử dụng mẫu EBUS-TBNA
Khi việc điều trị NSCLC giai đoạn tiến xa đã chuyển sang liệu pháp nhắm trúng đích phân tử, xét nghiệm dấu ấn sinh học đã trở nên cần thiết để xác định phương pháp điều trị tối ưu cho bệnh nhân mới được chẩn đoán NSCLC. Các đột biến nhạy cảm trong gen EGFR lần đầu tiên được mô tả vào năm 2004, là loại liệu pháp nhắm trúng đích phân tử đầu tiên. Kể từ đó, tái sắp xếp gen hợp nhất anaplastic lymphoma kinase (ALK), tái sắp xếp gen ROS1 và đột biến BRAF đã được xác định là các mục tiêu điều trị tiềm năng. Các liệu pháp kết hợp, bao gồm hóa trị độc tế bào và liệu pháp gen nhắm trúng đích, đã cải thiện tỷ lệ đáp ứng chung, tăng thời gian sống không tiến triển bệnh và có thể liên quan đến việc cải thiện thời gian sống còn chung ở NSCLC giai đoạn tiến xa khi so sánh với chỉ hóa trị độc tế bào. Hướng dẫn Thực hành Lâm sàng năm 2018 của Mạng lưới Ung thư Toàn diện Quốc gia (NCCN) dành cho NSCLC khuyến nghị chẩn đoán, phân giai đoạn và lấy đủ vật liệu để lập hồ sơ phân tử đồng thời nhằm cải thiện việc chăm sóc bệnh nhân NSCLC. Tầm quan trọng của việc lấy mô để lập hồ sơ phân tử là rõ ràng. Một tổng quan hệ thống và phân tích tổng hợp bao gồm 33 nghiên cứu (tổng cộng 2698 người tham gia) cho thấy việc sử dụng EBUS-TBNA để lập hồ sơ phân tử về tình trạng đột biến EGFR có xác suất gộp lấy đủ mô là 94,5% (KTC 95%, 93,2%-96,4%). Để xác định đột biến ALK, xác suất gộp là 94,9% (KTC 95%, 89,4%-98,8%). Có một số mục tiêu và liệu pháp phân tử mới nổi trong NSCLC, chẳng hạn như đột biến PIK3CA, đột biến AKTI KRAS, tái sắp xếp RET, đột biến bỏ qua MET exon 14 và đột biến HER2 kích hoạt. Do đó, hướng dẫn của NCCN năm 2018 khuyến nghị xét nghiệm bằng giải trình tự gen trên diện rộng, chẳng hạn như giải trình tự thế hệ mới (NGS). Một nghiên cứu bao gồm 54 mẫu TBNA/FNA cho thấy một bảng xét nghiệm 50 gen đã thành công trong 97,5% và 100% các mẫu kim 22-G và 25-G, tương ứng. Một bảng xét nghiệm lớn hơn với 1231 gen đã thành công trong 91,3% và 100% các mẫu kim 22-G và 25-G, tương ứng. Một nghiên cứu khác bao gồm 115 mẫu được thực hiện một bảng xét nghiệm NGS lớn (341-469 gen) cho thấy EBUS-TBNA đã lấy đủ mô trong 86,1% các mẫu. Sinh thiết lại bằng EBUS-TBNA để lập hồ sơ phân tử theo dõi có thể được thực hiện an toàn sau điều trị ban đầu. Trong kỷ nguyên quản lý ung thư dựa trên dấu ấn sinh học, khả năng phân tích các mẫu EBUS-TBNA cho nhiều dấu ấn sinh học là rất quan trọng trong việc lựa chọn một kế hoạch điều trị tối ưu, được cá nhân hóa cho mỗi bệnh nhân.
U lympho (Lymphoma)
Khoảng 10% các trường hợp u lympho được chẩn đoán lần đầu ở ngực, thường là một khối u trung thất. Phân loại phụ, vốn định hướng điều trị và tiên lượng, dựa trên các đặc điểm hình thái, kiểu hình, kiểu gen và phân tử. Chẩn đoán và phân giai đoạn sớm là chìa khóa để cải thiện sự sống còn ở những bệnh nhân được chẩn đoán mắc u lympho. Khi có sẵn, EBUS-TBNA là một phương pháp tiếp cận thay thế hữu ích để chẩn đoán và phân loại phụ u lympho nội ngực so với các phương pháp “tiêu chuẩn vàng” là nội soi trung thất, nội soi lồng ngực và/hoặc mở lồng ngực. Trong một tổng quan hệ thống và phân tích tổng hợp bao gồm 14 nghiên cứu, độ nhạy và độ đặc hiệu chung của EBUS-TBNA để chẩn đoán u lympho lần lượt là 66,2% (KTC 95%, 55%-75,8%) và 99,3% (KTC 95%, 98,2%-99,7%). Trong phân tích phân nhóm, độ nhạy và độ đặc hiệu của EBUS-TBNA trong chẩn đoán ban đầu u lympho lần lượt là 67,1% (KTC 95%, 54,2%-77,9%) và 99,6% (KTC 95%, 99,1%-99,8%). EBUS-TBNA hoạt động tốt hơn một chút trong chẩn đoán tái phát u lympho, với độ nhạy là 77,8% (KTC 95%, 68,1%-85,2%) và độ đặc hiệu là 99,5% (KTC 95%, 98,9%-99,8%). Các chỉ số chẩn đoán này tương đương với dữ liệu lịch sử về việc sử dụng nội soi trung thất để chẩn đoán u lympho trung thất. Để phân loại phụ u lympho, EBUS-TBNA đã lấy đủ mẫu cho các xét nghiệm bổ trợ (ví dụ: đếm tế bào dòng chảy, lai tại chỗ phát huỳnh quang) trong 63% các mẫu dương tính về mặt mô học. Điều này cho thấy EBUS-TBNA là một phương thức lựa chọn đầu tay thích hợp ở những bệnh nhân nghi ngờ u lympho để chẩn đoán cả bệnh ban đầu và bệnh tái phát.
Bệnh Sarcoidosis
Chẩn đoán sarcoidosis yêu cầu đáp ứng các tiêu chí sau: biểu hiện lâm sàng và X-quang tương thích, bằng chứng bệnh học về u hạt không hoại tử bã đậu, và loại trừ các bệnh khác có biểu hiện tương tự (ví dụ: nhiễm trùng, ác tính). Sinh thiết xuyên thành phế quản (TBB) và TBNA thông thường trong lịch sử là các thủ thuật phổ biến nhất để thu được bằng chứng bệnh học về u hạt không hoại tử bã đậu. Hiệu quả chẩn đoán của TBNA và TBNA + TBB được báo cáo lần lượt là 62% và 83%. EBUS-TBNA đặc biệt hữu ích cho sarcoidosis giai đoạn I/II, trong đó bệnh hạch bạch huyết là một đặc điểm phổ biến. Một phân tích tổng hợp bao gồm 15 nghiên cứu cho thấy EBUS-TBNA có độ chính xác chẩn đoán gộp là 79% (KTC 95%, 71%-86%). Hiệu quả của EBUS-TBNA cao hơn so với TBNA hoặc TBB đơn độc. Tuy nhiên, một phân tích tổng hợp riêng biệt bao gồm 16 nghiên cứu cho thấy hiệu quả chẩn đoán của kết hợp EBUS-TBNA + TBB + sinh thiết nội phế quản (EBB) là 89,7% và hiệu quả hơn so với EBUS-TBNA đơn độc (82,7%) trong chẩn đoán sarcoidosis. Tỷ số chênh chẩn đoán gộp cho hai nhóm là 0,55 (KTC 95%, 0,39-0,78, P=0,0007). Những kết quả này cho thấy EBUS-TBNA, khi kết hợp với TBB và/hoặc EBB, có thể là một phương pháp tiếp cận xâm lấn tối thiểu hiệu quả để xác nhận chẩn đoán sarcoidosis.
Lao, nang trung thất và các bệnh ác tính khác
Lao phổi thường liên quan đến bệnh hạch bạch huyết trung thất hoặc rốn phổi. Tiềm năng hữu ích của EBUS-TBNA trong chẩn đoán lao đã được báo cáo trước đây. Một phân tích tổng hợp gần đây cho thấy độ nhạy và độ đặc hiệu gộp của EBUS-TBNA trong chẩn đoán lao nội ngực lần lượt là 80% (KTC 95%, 0,74-0,85) và 100% (KTC 95%, 0,99-1,00).
Một tổng quan hệ thống bao gồm 26 nghiên cứu và 32 trường hợp đã nêu bật tiện ích của các phương pháp tiếp cận siêu âm xuyên thành phế quản chẩn đoán và điều trị trong chẩn đoán nang trung thất. Tuy nhiên, bốn trường hợp nhiễm trùng sau thủ thuật đã được xác định sau TBNA.
Rice và cộng sự đã báo cáo một loạt ca bệnh về phân giai đoạn hạch bằng EBUS-TBNA trong u trung biểu mô màng phổi ác tính, bao gồm 38 trường hợp EBUS-TBNA và 50 trường hợp nội soi trung thất. Độ nhạy và NPV lần lượt là 28% và 49% đối với nội soi trung thất so với 59% và 57% đối với EBUS. Czarnecka-Kujawa và cộng sự cũng đã công bố một loạt ca bệnh bao gồm 48 bệnh nhân bị u trung biểu mô màng phổi ác tính đã trải qua EBUS-TBNA để phân giai đoạn hạch. Độ nhạy, độ đặc hiệu, PPV, NPV và độ chính xác chẩn đoán lần lượt là 16,7%, 100%, 100%, 68,8% và 70,6%. Mặc dù không có nghiên cứu đoàn hệ lớn nào điều tra hiệu quả của EBUS-TBNA trong chẩn đoán sarcoma, một số tác giả đã mô tả việc lấy mô thành công trong các loạt ca bệnh nhỏ.
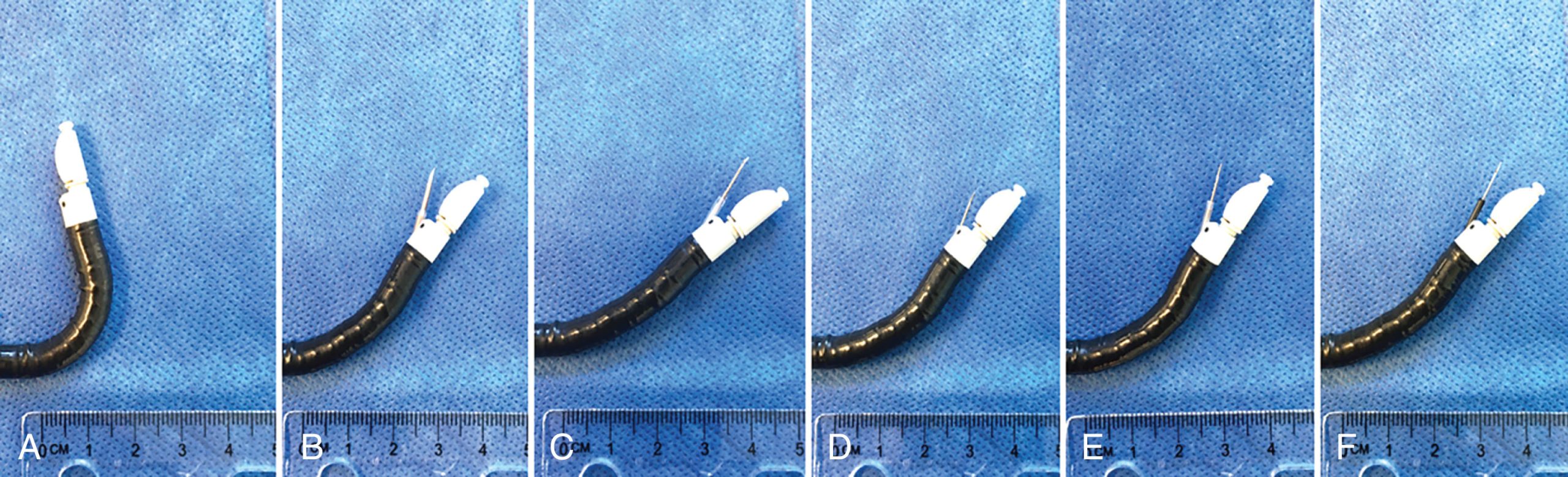
Hình 2.1 Độ linh hoạt của kim chọc hút xuyên thành phế quản qua siêu âm nội soi (EBUS-TBNA) và góc gập lên tối đa của ống nội soi EBUS (BF-UC180F, Olympus, Tokyo, Nhật Bản). (A) BF-UC180F không có kim. (B) Kim ViziShot2 FLEX 19-G (Olympus Surgical Technologies America, Westborough, MA, Hoa Kỳ). (C) Kim ViziShot 22-G (Olympus, Tokyo, Nhật Bản). (D) Kim ViziShot2 25-G (Olympus, Tokyo, Nhật Bản). (E) Kim Expect Pulmonary 25-G (Boston Scientific, Marlborough, MA, Hoa Kỳ). (F) EchoTip ProCore HD 25-G (Cook Medical, Bloomington, IN, Hoa Kỳ).
Kim EBUS
Hiện có một số loại kim EBUS với nhiều kích cỡ khác nhau (25-, 22-, 21-, hoặc 19-G). Kích thước của kim có thể ảnh hưởng đến số lượng mô thu được, mức độ chấn thương mô, lượng máu hút ra (có thể ảnh hưởng đến chất lượng bệnh phẩm), hiệu quả chẩn đoán và phạm vi góc gập tối đa của ống nội soi phế quản EBUS (Hình 2.1). Số lượng kim EBUS-TBNA ngày càng tăng đã thúc đẩy một số nghiên cứu về hiệu quả chẩn đoán so sánh của chúng. Các loại kim phổ biến nhất là kim 22-G và 21-G; tuy nhiên, có rất ít dữ liệu hỗ trợ việc sử dụng loại này hơn loại kia về kích thước. Một đoàn hệ lớn gồm 1299 bệnh nhân cho thấy không có sự khác biệt về hiệu quả chẩn đoán của kim 22-G và 21-G trong chẩn đoán và phân giai đoạn NSCLC. Các mẫu đủ tiêu chuẩn đã được thu thập ở 94,9% nhóm kim 22-G và 94,6% nhóm kim 21-G (P=0,81). Chẩn đoán bệnh học đã được thực hiện ở 51,4% nhóm 22-G và 51,3% nhóm 21-G (P=0,98). Những kết quả này cho thấy có rất ít sự khác biệt khi lựa chọn giữa kim 22-G và 21-G để đánh giá tế bào học qua TBNA.
Kim EBUS-TBNA 19-G
Kim EBUS-TBNA 19-G được coi là kim mô học, với giả thuyết rằng việc lấy sinh thiết lõi có thể cải thiện hiệu quả chẩn đoán. Kinoshita và cộng sự đã đánh giá hồi cứu hai nguyên mẫu kim EBUS-TBNA 19-G. Trong nghiên cứu này, bao gồm 82 tổn thương mục tiêu (72 hạch bạch huyết và 10 khối u phổi) ở 45 bệnh nhân, các tác giả nhận thấy hiệu quả chẩn đoán gộp của kim EBUS-TBNA 19-G là 100%, với 28% bệnh phẩm đủ cho chẩn đoán mô bệnh học. Gần đây, một kim 19-G chuyên dụng cho EBUS-TBNA (NA-U402SX-4019; Olympus, Tokyo, Nhật Bản) đã có mặt trên thị trường. Kim này có một đoạn đầu linh hoạt giúp bảo tồn tốt hơn góc gập của ống nội soi trong khi vẫn duy trì đường kính trong lớn hơn (0,69 mm so với 0,41 mm với kim 22-G). Một số nghiên cứu kể từ đó đã báo cáo về hiệu suất của kim 19-G thương mại này (Bảng 2.1). Doom và cộng sự đã chứng minh hiệu quả chẩn đoán xuất sắc (39/39, 100%) tương tự như khi sử dụng kim 21-G (39/39, 100%) trong một thử nghiệm đối chứng ngẫu nhiên. Trong nghiên cứu này, họ thấy rằng các mẫu mô 19-G có nhiều máu hơn và có diện tích bề mặt mô lớn hơn so với các mẫu 21-G. Một thử nghiệm ngẫu nhiên tiền cứu khác bao gồm 107 bệnh nhân cũng cho thấy các mẫu 19-G chứa nhiều mô hơn đáng kể so với các mẫu 21-G (20,0 so với 10,2 mg, P=0,0119). Tuy nhiên, kích thước kim lớn hơn một lần nữa lại liên quan đến các mẫu có nhiều máu hơn đáng kể (P=0,029). Hiệu quả chẩn đoán tương tự với cả hai loại kim. Những kết quả này cho thấy, với hiệu suất vốn đã xuất sắc của các kim tế bào học 22-G và 21-G, lợi ích bổ sung của kim 19-G không liên quan đến việc cải thiện hiệu quả chẩn đoán. Thay vào đó, việc thu được khối lượng mô lớn hơn một cách đáng tin cậy có thể tạo điều kiện thuận lợi cho việc sử dụng nhiều xét nghiệm phân tử (ví dụ: NGS) và bệnh học (ví dụ: nhuộm programmed death-ligand 1 [PD-L1]). Cần có nghiên cứu sâu hơn để đánh giá việc sử dụng như vậy.
Bảng 2.1 Các nghiên cứu về hiệu quả chẩn đoán của kim 19-G
| Tài liệu tham khảo | Năm | Thiết kế nghiên cứu | Số lượng | Hiệu quả chẩn đoán chung | Hiệu quả chẩn đoán bệnh ác tính | Hiệu quả chẩn đoán bệnh không ác tính | Biến chứng |
|---|---|---|---|---|---|---|---|
| Pickering và cs. | 2019 | Tiền cứu quan sát | 47 | 46/47 (97%) | KĐG | KĐG | Không |
| Dooms và cs. | 2018 | Thử nghiệm đối chứng ngẫu nhiên | 39 | 39/39 (100%) | 32/32 (100%) | 7/7 (100%) | Không |
| Tremblay và cs. | 2018 | Hồi cứu | 154 | 119/154 (77%) | KĐG | KĐG | Một ca chảy máu trung bình |
| Jones và cs. | 2018 | Hồi cứu | 100 | 96/100 (96%) | KĐG | KĐG | Không |
| Balwan và cs. | 2018 | Hồi cứu | 15 | 14/15 (93%) | 14/15 (93%) | KĐG | Không |
| Garrison và cs. | 2018 | Hồi cứu | 48 | 45/48 (94%) | KĐG | KĐG | Không |
| Minami và cs. | 2018 | Hồi cứu | 11 | 9/11 (81%) | KĐG | KĐG | Không |
| Chaddha và cs. | 2017 | Tiền cứu quan sát | 56 hạch | 52/56 (93%) | KĐG | KĐG | Không |
| Tyan và cs. | 2017 | Hồi cứu | 47 | 42/47 (89%) | 24/27 (89%) | 18/20 (90%) | Một ca chảy máu trung bình |
| Gnass và cs. | 2017 | Hồi cứu | 22 | 22/22 (100%) | 15/15 (100%) | 7/7 (100%) | Không |
| Trisolini và cs. | 2017 | Hồi cứu | 13 | 13/13 (100%) | 12/12 (100%) | 1/1 (100%) | Một ca chảy máu nhẹ |
| Tổng cộng | n=552 | Hiệu quả chẩn đoán gộp 84.6% |
Chú thích: KĐG, không đánh giá
Kim EBUS-TBNA 25-G
Hiện tại, có ba loại kim EBUS-TBNA 25-G trên thị trường: Echo Tip ProCore HD (Cook Medical, Bloomington, IN, Hoa Kỳ), kim Expect Pulmonary (Boston Scientific, Watertown, MA, Hoa Kỳ), và ViziShot2 (Olympus, Tokyo, Nhật Bản) (Hình 2.2). Lý do cơ bản cho sự phát triển của những loại kim này là để giảm chấn thương cho hạch và mô phổi được sinh thiết, cũng như giảm nhiễm bẩn. Tuy nhiên, chỉ có một số lượng hạn chế các nghiên cứu đã được công bố (Bảng 2.2). Một nghiên cứu hồi cứu của Di Felice và cộng sự đã đánh giá 158 hạch bạch huyết, cho thấy kim 25-G và 22-G đạt được độ đầy đủ của mẫu tương đương (P=1) với độ chính xác chẩn đoán tương tự (P=0,7); độ nhạy, độ đặc hiệu, NPV và độ chính xác chẩn đoán của kim 25-G lần lượt là 88,9% (KTC 95%, 51,8%-99,7%), 100% (KTC 95%, 92,1%-100%), 97,8% (KTC 95%, 87,6%-99,7%) và 98,2% (KTC 95%, 90,1%-100%). So sánh, độ nhạy, độ đặc hiệu, NPV và độ chính xác chẩn đoán ở nhóm 22-G là 77,8% (KTC 95%, 40%-97,2%), 100% (KTC 95%, 86,8%-100%), 92,9% (KTC 95%, 79,3%-97,8%) và 94,3% (KTC 95%, 80,8%-99,3%). Một nghiên cứu hồi cứu khác cũng cho thấy độ chính xác chẩn đoán tương tự với kim 25-G (100%, 25/25) và 22-G (90,7%, 68/75). Stoy và cộng sự đã đánh giá hồi cứu 104 bệnh nhân, cho thấy kim 25-G cung cấp các mẫu đủ cho NGS thường xuyên như các mẫu kim 22-G. Cần có nghiên cứu sâu hơn để đánh giá các đặc điểm chi tiết hơn của kim 25-G và các mẫu sinh thiết.
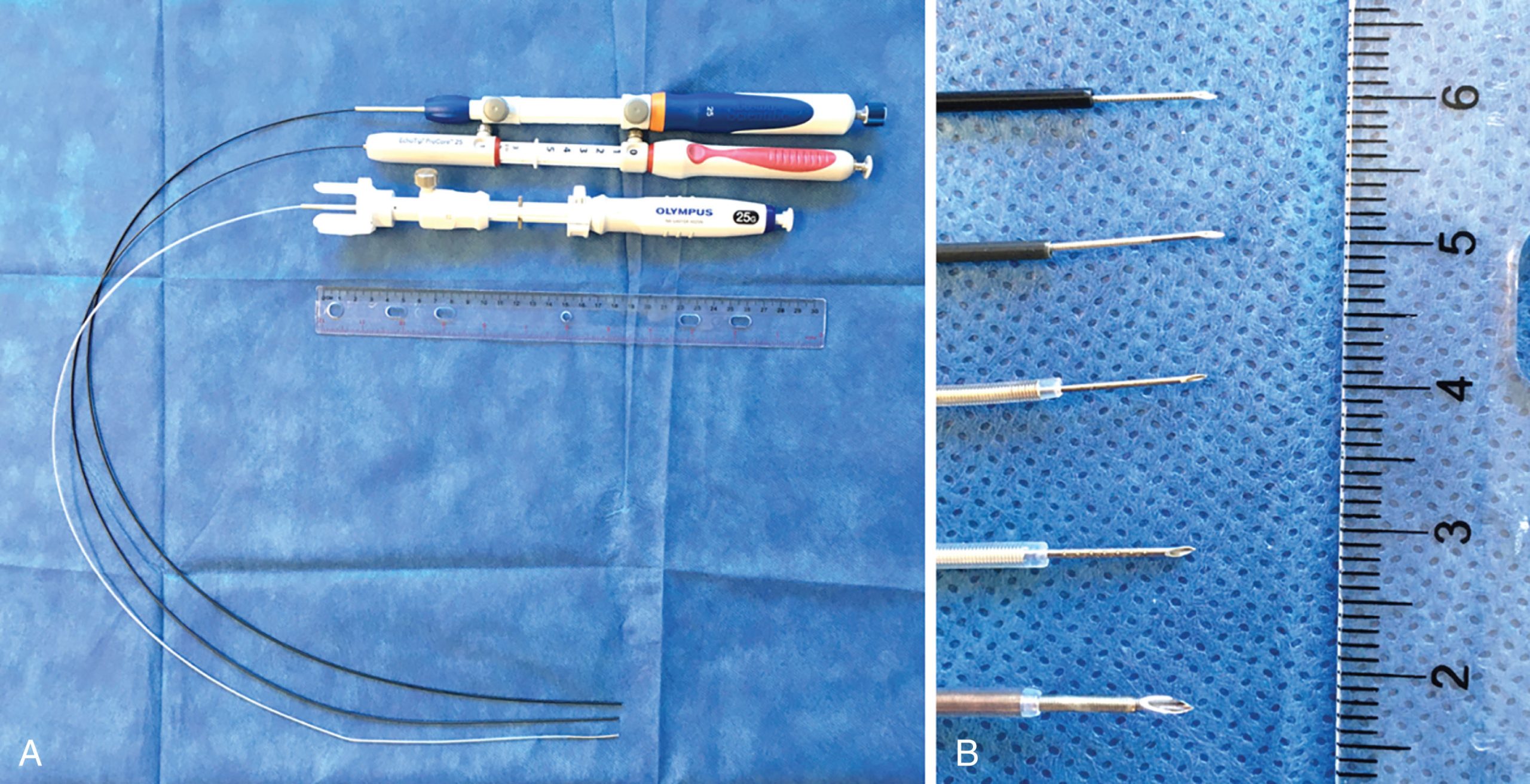 Hình 2.2 So sánh các loại kim chọc hút xuyên thành phế quản qua siêu âm nội soi (EBUS-TBNA). (A) Từ trên xuống dưới, kim Expect Pulmonary 25-G (Boston Scientific, Marlborough, MA, Hoa Kỳ), EchoTip ProCore HD 25-G (Cook Medical, Bloomington, IN, Hoa Kỳ), và kim ViziShot2 25-G (Olympus, Tokyo, Nhật Bản). (B) Từ trên xuống dưới, kim Expect Pulmonary 25-G (Boston Scientific, Marlborough, MA, Hoa Kỳ), EchoTip ProCore HD 25-G (Cook Medical, Bloomington, IN, Hoa Kỳ), kim ViziShot2 25-G (Olympus, Tokyo Nhật Bản), kim ViziShot 22-G (Olympus, Tokyo, Nhật Bản), và kim ViziShot2 FLEX 19-G (Olympus Surgical Technologies America, Westborough, MA, Hoa Kỳ).
Hình 2.2 So sánh các loại kim chọc hút xuyên thành phế quản qua siêu âm nội soi (EBUS-TBNA). (A) Từ trên xuống dưới, kim Expect Pulmonary 25-G (Boston Scientific, Marlborough, MA, Hoa Kỳ), EchoTip ProCore HD 25-G (Cook Medical, Bloomington, IN, Hoa Kỳ), và kim ViziShot2 25-G (Olympus, Tokyo, Nhật Bản). (B) Từ trên xuống dưới, kim Expect Pulmonary 25-G (Boston Scientific, Marlborough, MA, Hoa Kỳ), EchoTip ProCore HD 25-G (Cook Medical, Bloomington, IN, Hoa Kỳ), kim ViziShot2 25-G (Olympus, Tokyo Nhật Bản), kim ViziShot 22-G (Olympus, Tokyo, Nhật Bản), và kim ViziShot2 FLEX 19-G (Olympus Surgical Technologies America, Westborough, MA, Hoa Kỳ).
Bảng 2.2 Các nghiên cứu và ca lâm sàng về kim 25-G
| Tài liệu tham khảo | Năm | Thiết kế nghiên cứu | Số lượng | Hiệu quả chẩn đoán | Biến chứng |
|---|---|---|---|---|---|
| Di Felice và cs. | 2018 | Hồi cứu | 79 | 73/79 (92%) | Không |
| Matsumoto và cs. | 2017 | Hồi cứu | 29 | 29/29 (100%) | KĐG |
| Okubo và cs. | 2017 | Báo cáo ca | 1 | 1/1 (100%) | Không |
| Waheed và cs. | 2017 | Báo cáo ca | 1 | 1/1 (100%) | Không |
Chú thích: KĐG, không đánh giá
Tiêm kim xuyên thành phế quản dưới hướng dẫn của siêu âm nội soi phế quản trị liệu
Tiêm kim xuyên thành phế quản (TBNI) qua ống nội soi phế quản thông thường đã được sử dụng trước đây để đưa các tác nhân điều trị khác nhau để điều trị các bệnh ác tính hoặc rò phế quản. EBUS-TBNI là một kỹ thuật tương đối mới đã được mô tả để điều trị NSCLC tái phát. Mehta và cộng sự đã mô tả việc tiêm cisplatin vào tổng cộng 41 vị trí ở 36 bệnh nhân bằng EBUS-TBNI. Đáp ứng hoàn toàn hoặc một phần được quan sát thấy ở 69% (24/35) và thời gian sống trung vị của nhóm là 8 tháng (KTC 95%, 6-11 tháng). EBUS-TBNI có thể có tiềm năng hữu ích cho các tình trạng lành tính, mặc dù dữ liệu cũng chỉ giới hạn ở các báo cáo ca. Parikh và cộng sự đã mô tả một phụ nữ 71 tuổi bị u nấm aspergillus đã được tiêm amphotericin B vào trong tổn thương (tổng liều 175 mg; 2,5 mg/kg) bằng EBUS-TBNI.
TÓM TẮT
EBUS-TBNA qua EBUS đầu dò lồi đã mang lại một sự thay đổi mô hình trong phân giai đoạn hạch ở ung thư phổi. Việc sử dụng EBUS-TBNA từ đó đã mở rộng để bao gồm việc lấy mô để chẩn đoán ngày càng nhiều bệnh lý nội ngực và xét nghiệm dấu ấn sinh học cho y học chính xác. Gần đây hơn, tiềm năng hữu ích của EBUS đầu dò lồi như một phương thức điều trị (qua TBNI) đã nhận được sự chú ý ngày càng tăng. Các chỉ định rộng rãi và tỷ lệ biến chứng thấp làm cho EBUS trở thành một kỹ năng kỹ thuật quan trọng đối với các bác sĩ chuyên về các thủ thuật hô hấp can thiệp.
TÀI LIỆU THAM KHẢO
- Yasufuku K, Chiyo M, Sekine Y, et al. Real-time endobronchial ultrasound-guided transbronchial needle aspiration of mediastinal and hilar lymph nodes. Chest. 2004;126(1):122-128.
- Gu P, Zhao YZ, Jiang LY, Zhang W, Xin Y, Han BH. Endobronchial ultrasound-guided transbronchial needle aspiration for staging of lung cancer: A systematic review and meta-analysis. Eur J Cancer. 2009;45(8):1389-1396.
- Labarca G, Sierra-Ruiz M, Kheir F, et al. Diagnostic accuracy of endobronchial ultrasound transbronchial needle aspiration in lymphoma. A systematic review and meta-analysis. Ann Am Thorac Soc. 2019;16(11): 1432-1439.
- Shingyoji M, Ikebe D, Itakura M, et al. Pulmonary artery sarcoma diagnosed by endobronchial ultrasound-guided transbronchial needle aspiration. Ann Thorac Surg. 2013;96(2):e33-e35.
- Rice DC, Steliga MA, Stewart J, et al. Endoscopic ultrasound-guided fine needle aspiration for staging of malignant pleural mesothelioma. Ann Thorac Surg. 2009;88(3):862-868. discussion 868-869.
- Liberman M, Hanna N, Duranceau A, Thiffault V, Ferraro P. Endobronchial ultrasonography added to endoscopic ultrasonography improves staging in esophageal cancer. Ann Thorac Surg. 2013;96(1):232-236. discussion 236-238.
- Val-Bernal JE, Martino M, Romay F, Yllera E. Endobronchial ultrasound-guided transbronchial needle aspiration in the diagnosis of mediastinal metastases of clear cell renal cell carcinoma. Pathol Res Pract. 2018;214(7): 949-956.
- Agarwal R, Srinivasan A, Aggarwal AN, Gupta D. Efficacy and safety of convex probe EBUS-TBNA in sarcoidosis: A systematic review and meta-analysis. Respir Med. 2012;106(6):883-892.
- Ye W, Zhang R, Xu X, Liu Y, Ying K. Diagnostic efficacy and safety of endobronchial ultrasound-guided transbronchial needle aspiration in intrathoracic tuberculosis: A meta-analysis. J Ultrasound Med. 2015;34(9): 1645-1650.
- Maturu VN, Dhooria S, Agarwal R. Efficacy and safety of transbronchial needle aspiration in diagnosis and treatment of mediastinal bronchogenic cysts: Systematic review of case reports. J Bronchology Interv Pulmonol. 2015;22(3):195-203.
- Kinsey CM. Endobronchial ultrasound-guided-transbronchial needle injection for direct therapy of lung cancer. AME Med J. 2018
- Hwangbo B, Lee GK, Lee HS, et al. Transbronchial and transesophageal fine-needle aspiration using an ultrasound bronchoscope in mediastinal staging of potentially operable lung cancer. Chest. 2010;138(4): 795-802.
- Oki M, Saka H, Ando M, et al. Transbronchial vs transesophageal needle aspiration using an ultrasound bronchoscope for the diagnosis of mediastinal lesions: A randomized study. Chest. 2015;147(5): 1259-1266.
- Kuijvenhoven JC, Leoncini F, Crombag LC, et al. Endobronchial ultrasound for the diagnosis of centrally located lung tumors: A systematic review and meta-analysis. Respiration. 2020;99(5):441-450.
- Vaidya PJ, Munavvar M, Leuppi JD, Mehta AC, Chhajed PN. Endobronchial ultrasound-guided transbronchial needle aspiration: Safe as it sounds. Respirology. 2017;22(6):1093-1101.
- Yasufuku K, Nakajima T, Motoori K, et al. Comparison of endobronchial ultrasound, positron emission tomography, and ct for lymph node staging of lung cancer. Chest. 2006;130(3):710-718.
- Hwangbo B, Kim SK, Lee HS, et al. Application of endobronchial ultrasound-guided transbronchial needle aspiration following integrated PET/CT in mediastinal staging of potentially operable non-small cell lung cancer. Chest. 2009;135(5):1280-1287.
- Zhang R, Ying K, Shi L, Zhang L, Zhou L. Combined endobronchial and endoscopic ultrasound-guided fine needle aspiration for mediastinal lymph node staging of lung cancer: A meta-analysis. Eur J Cancer. 2013;49(8):1860-1867.
- Annema JT, van Meerbeeck JP, Rintoul RC, et al. Mediastinoscopy vs endosonography for mediastinal nodal staging of lung cancer: A randomized trial. JAMA. 2010;304(20):2245-2252.
- Vilmann P, Clementsen PF, Colella S, et al. Combined endobronchial and esophageal endosonography for the diagnosis and staging of lung cancer: European Society of Gastrointestinal Endoscopy (ESGE) guideline, in cooperation with the European Respiratory Society (ERS) and the European Society of Thoracic Surgeons (ESTS). Endoscopy. 2015;47(6):545-559.
- De Leyn P, Dooms C, Kuzdzal J, et al. Revised ESTS guidelines for preoperative mediastinal lymph node staging for non-small-cell lung cancer. Eur J Cardiothorac Surg. 2014;45(5):787-798.
- Silvestri GA, Gonzalez AV, Jantz MA, et al. Methods for staging non-small cell lung cancer: Diagnosis and management of lung cancer, 3rd ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest. 2013;143(5 Suppl):e211S-e250S.
- Fujiwara T, Yasufuku K, Nakajima T, et al. The utility of sonographic features during endobronchial ultrasound-guided transbronchial needle aspiration for lymph node staging in patients with lung cancer: A standard endobronchial ultrasound image classification system. Chest. 2010;138(3):641-647.
- Alici IO, Yilmaz Demirci N, Yilmaz A, Karakaya J, Ozaydin E. The sonographic features of malignant mediastinal lymph nodes and a proposal for an algorithmic approach for sampling during endobronchial ultrasound. Clin Respir J. 2016;10(5):606-613.
- Nakajima T, Anayama T, Shingyoji M, Kimura H, Yoshino I, Yasufuku K. Vascular image patterns of lymph nodes for the prediction of metastatic disease during EBUS-TBNA for mediastinal staging of lung cancer. J Thorac Oncol. 2012;7(6):1009-1014.
- Wang L, Wu W, Teng J, Zhong R, Han B, Sun J. Sonographic features of endobronchial ultrasound in differentiation of benign lymph nodes. Ultrasound Med Biol. 2016;42(12):2785-2793.
- Izumo T, Sasada S, Chavez C, Matsumoto Y, Tsuchida T. Endobronchial ultrasound elastography in the diagnosis of mediastinal and hilar lymph nodes. Jpn J Clin Oncol. 2014;44(10):956-962.
- Nakajima T, Inage T, Sata Y, et al. Elastography for predicting and localizing nodal metastases during endobronchial ultrasound. Respiration. 2015;90(6):499-506.
- Tagaya R, Kurimoto N, Osada H, Kobayashi A. Automatic objective diagnosis of lymph nodal disease by B-mode images from convex-type echobronchoscopy. Chest. 2008;133(1):137-142.
- Ettinger DS, Wood DE, Aisner DL, et al. Non-small cell lung cancer, version 5.2017, NCCN clinical practice guidelines in oncology. J Natl Compr Canc Netw. 2017;15(4):504-535.
- Betticher DC, Hsu Schmitz SF, Totsch M, et al. Mediastinal lymph node clearance after docetaxel-cisplatin neoadjuvant chemotherapy is prognostic of survival in patients with stage IIIA pN2 non-small-cell lung cancer: A multicenter phase II trial. J Clin Oncol. 2003;21(9):1752-1759.
- Lorent N, De Leyn P, Lievens Y, et al. Long-term survival of surgically staged IIIA-N2 non-small-cell lung cancer treated with surgical combined modality approach: Analysis of a 7-year prospective experience. Ann Oncol. 2004;15(11):1645-1653.
- De Leyn P, Stroobants S, De Wever W, et al. Prospective comparative study of integrated positron emission tomography-computed tomography scan compared with remediastinoscopy in the assessment of residual mediastinal lymph node disease after induction chemotherapy for mediastinoscopy-proven stage IIIA-N2 non-small-cell lung cancer: A Leuven Lung Cancer Group study. J Clin Oncol. 2006;24(21):3333-3339.
- Marra A, Hillejan L, Fechner S, Stamatis G. Remediastinoscopy in restaging of lung cancer after induction therapy. J Thorac Cardiovasc Surg. 2008;135(4):843-849.
- De Waele M, Serra-Mitjans M, Hendriks J, et al. Accuracy and survival of repeat mediastinoscopy after induction therapy for non-small cell lung cancer in a combined series of 104 patients. Eur J Cardiothorac Surg. 2008;33(5):824-828.
- de Cabanyes Candela S, Detterbeck FC. A systematic review of restaging after induction therapy for stage IIIA lung cancer: Prediction of pathologic stage. J Thorac Oncol. 2010;5(3):389-398.
- Zielinski M, Szlubowski A, Kolodziej M, et al. Comparison of endobronchial ultrasound and/or endoesophageal ultrasound with transcervical extended mediastinal lymphadenectomy for staging and restaging of non-small-cell lung cancer. J Thorac Oncol. 2013;8(5):630-636.
- Nasir BS, Bryant AS, Minnich DJ, Wei B, Dransfield MT, Cerfolio RJ. The efficacy of restaging endobronchial ultrasound in patients with non-small cell lung cancer after preoperative therapy. Ann Thorac Surg. 2014;98(3): 1008-1012.
- Herth FJ, Annema JT, Eberhardt R, et al. Endobronchial ultrasound with transbronchial needle aspiration for restaging the mediastinum in lung cancer. J Clin Oncol. 2008;26(20):3346-3350.
- Muthu V, Sehgal IS, Dhooria S, Aggarwal AN, Agarwal R. Efficacy of endosonographic procedures in mediastinal restaging of lung cancer after neoadjuvant therapy: A systematic review and diagnostic accuracy meta-analysis. Chest. 2018;154(1):99-109.
- Lynch TJ, Bell DW, Sordella R, et al. Activating mutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer to gefitinib. N Engl J Med. 2004;350(21):2129-2139.
- Soda M, Choi YL, Enomoto M, et al. Identification of the transforming EML4-ALK fusion gene in non-small-cell lung cancer. Nature. 2007;448(7153):561-566.
- Rimkunas VM, Crosby KE, Li D, et al. Analysis of receptor tyrosine kinase ROS1-positive tumors in non-small cell lung cancer: Identification of a FIG-ROS1 fusion. Clin Cancer Res. 2012;18(16):4449-4457.
- Marchetti A, Felicioni L, Malatesta S, et al. Clinical features and outcome of patients with non-small-cell lung cancer harboring BRAF mutations. J Clin Oncol. 2011;29(26):3574-3579.
- Blumenthal GM, Karuri SW, Zhang H, et al. Overall response rate, progression-free survival, and overall survival with targeted and standard therapies in advanced non-small-cell lung cancer: US Food and Drug Administration trial-level and patient-level analyses. J Clin Oncol. 2015;33(9):1008-1014.
- Ettinger DS, Aisner DL, Wood DE, et al. NCCN guidelines insights: Non-small cell lung cancer, version 5.2018. J Natl Compr Canc Netw. 2018;16(7): 807-821.
- Labarca G, Folch E, Jantz M, Mehta HJ, Majid A, Fernandez-Bussy S. Adequacy of samples obtained by endobronchial ultrasound with transbronchial needle aspiration for molecular analysis in patients with non-small cell lung cancer. Systematic review and meta-analysis. Ann Am Thorac Soc. 2018;15(10):1205-1216.
- Stoy SP, Segal JP, Mueller J, et al. Feasibility of endobronchial ultrasound-guided transbronchial needle aspiration cytology specimens for next generation sequencing in non-small-cell lung cancer. Clin Lung Cancer. 2018;19 (3):230-238. e232.
- Turner SR, Buonocore D, Desmeules P, et al. Feasibility of endobronchial ultrasound transbronchial needle aspiration for massively parallel next-generation sequencing in thoracic cancer patients. Lung Cancer. 2018;119:85-90.
- Elia S, Cecere C, Giampaglia F, Ferrante G. Mediastinoscopy vs. anterior mediastinotomy in the diagnosis of mediastinal lymphoma: A randomized trial. Eur J Cardiothorac Surg. 1992;6(7):361-365.
- Statement on sarcoidosis Joint statement of the American Thoracic Society (ATS), the European Respiratory Society (ERS) and the World Association of Sarcoidosis and Other Granulomatous Disorders (WASOG) adopted by the ATS board of directors and by the ERS executive committee, February 1999. Am J Respir Crit Care Med. 1999;160(2):736-755.
- Agarwal R, Aggarwal AN, Gupta D. Efficacy and safety of conventional transbronchial needle aspiration in sarcoidosis: A systematic review and meta-analysis. Respir Care. 2013;58(4):683-693.
- Trisolini R, Lazzari Agli L, Tinelli C, De Silvestri A, Scotti V, Patelli M. Endobronchial ultrasound-guided transbronchial needle aspiration for diagnosis of sarcoidosis in clinically unselected study populations. Respirology. 2015;20(2):226-234.
- Hu LX, Chen RX, Huang H, et al. Endobronchial ultrasound-guided transbronchial needle aspiration versus standard bronchoscopic modalities for diagnosis of sarcoidosis: A meta-analysis. Chin Med J (Engl). 2016;129(13):1607-1615.
- Navani N, Molyneaux PL, Breen RA, et al. Utility of endobronchial ultrasound-guided transbronchial needle aspiration in patients with tuberculous intrathoracic lymphadenopathy: A multicentre study. Thorax. 2011;66(10):889-893.
- Czarnecka-Kujawa K, de Perrot M, Keshavjee S, Yasufuku K. Endobronchial ultrasound-guided transbronchial needle aspiration mediastinal lymph node staging in malignant pleural mesothelioma. J Thorac Dis. 2019;11(2):602-612.
- Sanchez-Font A, Chalela R, Martin-Ontiyuelo C, et al. Molecular analysis of peripheral lung adenocarcinoma in brush cytology obtained by EBUS plus fluoroscopy-guided bronchoscopy. Cancer Cytopathol. 2018;126(10):860-871.
- Dalal S, Nicholson 3rd CE, Jhala D. Unusual presentation of poorly differentiated primary pulmonary synovial sarcoma (PD-PPSS) diagnosed by EBUS-TBNA with cytogenetic confirmation-a diagnostic challenge. Diagn Cytopathol. 2018;46(1):72-78.
- Yarmus LB, Akulian J, Lechtzin N, et al. Comparison of 21-gauge and 22-gauge aspiration needle in endobronchial ultrasound-guided transbronchial needle aspiration: Results of the American College of Chest Physicians quality improvement registry, education, and evaluation registry. Chest. 2013;143(4):1036-1043.
- Kinoshita T, Ujiie H, Schwock J, et al. Clinical evaluation of the utility of a flexible 19-gauge EBUS-TBNA needle. J Thorac Dis. 2018;10(4):2388-2396.
- Tyan C, Patel P, Czarnecka K, et al. Flexible 19-gauge endobronchial ultrasound-guided transbronchial needle aspiration needle: First experience. Respiration. 2017;94(1):52-57.
- Dooms C, Vander Borght S, Yserbyt J, et al. A randomized clinical trial of Flex 19G needles versus 22G needles for endobronchial ultrasonography in suspected lung cancer. Respiration. 2018;96(3):275-282.
- Wolters C, Darwiche K, Franzen D, et al. A prospective, randomized trial for the comparison of 19-G and 22-G endobronchial ultrasound-guided transbronchial aspiration needles; introducing a novel end point of sample weight corrected for blood content. Clin Lung Cancer. 2019;20(3):e265-e273.
- Pickering EM, Holden VK, Heath JE, Verceles AC, Kalchiem-Dekel O, Sachdeva A. Tissue acquisition during EBUS-TBNA: Comparison of cell blocks obtained from a 19G versus 21G needle. J Bronchology Interv Pulmonol. 2019;26(4):237-244.
- Tremblay A, McFadden S, Bonifazi M, et al. Endobronchial ultrasound-guided transbronchial needle aspiration with a 19-G needle device. J Bronchology Interv Pulmonol. 2018;25(3):218-223.
- Jones RC, Bhatt N, Medford ARL. The effect of 19-gauge endobronchial ultrasound-guided transbronchial needle aspiration biopsies on characterisation of malignant and benign disease. The Bristol experience. Monaldi Arch Chest Dis. 2018;88(2):915.
- Balwan A. Endobronchial ultrasound-guided transbronchial needle aspiration using 19-G needle for sarcoidosis. J Bronchology Interv Pulmonol. 2018;25(4):260-263.
- Garrison G, Leclair T, Balla A, et al. Use of an additional 19-G EBUS-TBNA needle increases the diagnostic yield of EBUS-TBNA. J Bronchology Interv Pulmonol. 2018;25(4):269-273.
- Minami D, Ozeki T, Okawa S, et al. Comparing the clinical performance of the new 19-G ViziShot FLEX and 21-or 22-G ViziShot 2 endobronchial ultrasound-guided transbronchial needle aspiration needles. Intern Med. 2018;57(24):3515-3520.
- Chaddha U, Ronaghi R, Elatre W, Chang CF, Mahdavi R. Comparison of sample adequacy and diagnostic yield of 19- and 22-G EBUS-TBNA needles. J Bronchology Interv Pulmonol. 2018;25(4):264-268.
- Gnass M, Sola J, Filarecka A, et al. Initial polish experience of flexible 19 gauge endobronchial ultrasound-guided transbronchial needle aspiration. Adv Respir Med. 2017;85(2):64-68.
- Di Felice C, Young B, Matta M. Comparison of specimen adequacy and diagnostic accuracy of a 25-gauge and 22-gauge needle in endobronchial ultrasound-guided transbronchial needle aspiration. J Thorac Dis. 2019;11(8):3643-3649.
- Matsumoto Y, Okubo Y, Tanaka M, et al. The utility of new 25 gauge endobronchial ultrasound-guided transbronchial needle in lymph node staging. Respirology. 2017;22(S3):27.
- Okubo Y, Matsumoto Y, Nakai T, et al. The new transbronchial diagnostic approach for the metastatic lung tumor from renal cell carcinoma-a case report. J Thorac Dis. 2017;9(9):E762-E766.
- Waheed SA, Goyal A. A case of adapting to antiplatelets: Successful diagnosis of nocardia via endobronchial ultrasound using a 25 gauge needle. D31. Interventional pulmonary: Case reports II. Am J Respir Crit Care Med. 2018;197:A6430-A6430.
- Seymour CW, Krimsky WS, Sager J, et al. Transbronchial needle injection: A systematic review of a new diagnostic and therapeutic paradigm. Respiration. 2006;73(1): 78-89.
- Khan F, Anker CJ, Garrison G, Kinsey CM. Endobronchial ultrasound-guided transbronchial needle injection for local control of recurrent non-small cell lung cancer. Ann Am Thorac Soc. 2015;12(1):101-104.
- Mehta HJ, Begnaud A, Penley AM, et al. Treatment of isolated mediastinal and hilar recurrence of lung cancer with bronchoscopic endobronchial ultrasound guided intratumoral injection of chemotherapy with cisplatin. Lung Cancer. 2015;90(3):542-547.
- Parikh MS, Seeley E, Nguyen-Tran E, Krishna G. Endobronchial ultrasound-guided transbronchial needle injection of liposomal amphotericin B for the treatment of symptomatic aspergilloma. J Bronchology Interv Pulmonol. 2017;24(4):330-333.
BẢNG CHÚ GIẢI THUẬT NGỮ Y HỌC ANH – VIỆT
| STT | Thuật ngữ tiếng Anh | Phiên âm IPA | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Convex probe endobronchial ultrasound (CP-EBUS) | /ˈkɒnvɛks proʊb ˌɛndoʊˈbrɒŋkiəl ˈʌltrəˌsaʊnd/ | Siêu âm nội soi phế quản đầu dò lồi |
| 2 | Linear EBUS | /ˈlɪniər ˈiːbʌs/ | EBUS đầu dò lồi |
| 3 | Real-time endobronchial ultrasound-guided transbronchial needle aspiration (EBUS-TBNA) | /ˈriːlˌtaɪm ˌɛndoʊˈbrɒŋkiəl ˈʌltrəˌsaʊnd ˈɡaɪdɪd ˌtrænzˈbrɒŋkiəl ˈniːdəl ˌæspəˈreɪʃən/ | Chọc hút bằng kim xuyên thành phế quản dưới hướng dẫn của siêu âm nội soi thời gian thực |
| 4 | Peribronchial lung lesions | /ˌpɛrɪˈbrɒŋkiəl lʌŋ ˈliːʒənz/ | Tổn thương phổi cạnh phế quản |
| 5 | Mediastinal lymph nodes | /ˌmiːdiəˈstaɪnəl lɪmf noʊdz/ | Hạch bạch huyết trung thất |
| 6 | Hilar lymph nodes | /ˈhaɪlər lɪmf noʊdz/ | Hạch rốn phổi |
| 7 | Minimally invasive modality | /ˈmɪnɪməli ɪnˈveɪsɪv moʊˈdæləti/ | Phương thức xâm lấn tối thiểu |
| 8 | Lung cancer | /lʌŋ ˈkænsər/ | Ung thư phổi |
| 9 | Endoscopic ultrasound-fine-needle aspiration (EUS-FNA) | /ˌɛndoʊˈskɒpɪk ˈʌltrəˌsaʊnd faɪn ˈniːdəl ˌæspəˈreɪʃən/ | Chọc hút bằng kim nhỏ qua siêu âm nội soi |
| 10 | Mediastinal nodal staging | /ˌmiːdiəˈstaɪnəl ˈnoʊdəl ˈsteɪdʒɪŋ/ | Phân giai đoạn hạch trung thất |
| 11 | Neoadjuvant therapy | /ˌniːoʊˈædʒəvənt ˈθɛrəpi/ | Điều trị tân bổ trợ |
| 12 | Biomarker testing | /ˈbaɪoʊˌmɑːrkər ˈtɛstɪŋ/ | Xét nghiệm dấu ấn sinh học |
| 13 | Ultrasonography image analysis | /ˌʌltrəˌsɒnəˈɡræfi ˈɪmɪdʒ əˈnæləsɪs/ | Phân tích hình ảnh siêu âm |
| 14 | Lymphoma | /lɪmˈfoʊmə/ | U lympho |
| 15 | Sarcoidosis | /ˌsɑːrkɔɪˈdoʊsɪs/ | Bệnh Sarcoidosis |
| 16 | Tuberculosis | /tjuːˌbɜːrkjəˈloʊsɪs/ | Bệnh lao |
| 17 | Mediastinal cysts | /ˌmiːdiəˈstaɪnəl sɪsts/ | Nang trung thất |
| 18 | Intrathoracic malignancies | /ˌɪntrəθəˈræsɪk məˈlɪɡnənsiz/ | Bệnh lý ác tính trong lồng ngực |
| 19 | Transbronchial injection | /ˌtrænzˈbrɒŋkiəl ɪnˈdʒɛkʃən/ | Tiêm xuyên thành phế quản |
| 20 | Nodal staging | /ˈnoʊdəl ˈsteɪdʒɪŋ/ | Phân giai đoạn hạch |
| 21 | Sarcoma | /sɑːrˈkoʊmə/ | Sarcoma (U mô liên kết ác tính) |
| 22 | Mesothelioma | /ˌmiːzoʊˌθiːliˈoʊmə/ | U trung biểu mô |
| 23 | Mediastinal metastases | /ˌmiːdiəˈstaɪnəl məˈtæstəsiːz/ | Di căn trung thất |
| 24 | Therapeutic interventions | /ˌθɛrəˈpjuːtɪk ˌɪntərˈvɛnʃənz/ | Can thiệp điều trị |
| 25 | Upper lobes | /ˈʌpər loʊbz/ | Thùy trên (phổi) |
| 26 | Working channel | /ˈwɜːrkɪŋ ˈtʃænəl/ | Kênh thủ thuật |
| 27 | Universal ultrasound processor | /ˌjuːnɪˈvɜːrsəl ˈʌltrəˌsaʊnd ˈproʊsɛsər/ | Bộ xử lý siêu âm đa năng |
| 28 | Gauge (G) | /ɡeɪdʒ/ | Đơn vị đo đường kính kim |
| 29 | Bronchoscopist | /brɒŋˈkɒskəpɪst/ | Bác sĩ nội soi phế quản |
| 30 | Endoscopy technician | /ɛnˈdɒskəpi tɛkˈnɪʃən/ | Kỹ thuật viên nội soi |
| 31 | Respiratory technician | /rɪˈspɪrətəri tɛkˈnɪʃən/ | Kỹ thuật viên hô hấp |
| 32 | Sedation nurse | /sɪˈdeɪʃən nɜːrs/ | Điều dưỡng an thần |
| 33 | Anesthesia team | /ˌænəsˈθiːʒə tiːm/ | Đội ngũ gây mê |
| 34 | Cytopathologist | /ˌsaɪtoʊpəˈθɒlədʒɪst/ | Bác sĩ giải phẫu bệnh tế bào |
| 35 | Cytopathology technician | /ˌsaɪtoʊpəˈθɒlədʒi tɛkˈnɪʃən/ | Kỹ thuật viên giải phẫu bệnh tế bào |
| 36 | Endoscopy suite | /ɛnˈdɒskəpi swiːt/ | Phòng nội soi |
| 37 | Operating room | /ˈɒpəreɪtɪŋ ruːm/ | Phòng mổ |
| 38 | Moderate/conscious sedation | /ˈmɒdərət /ˈkɒnʃəs sɪˈdeɪʃən/ | An thần tỉnh/An thần mức độ trung bình |
| 39 | General anesthesia | /ˈdʒɛnərəl ˌænəsˈθiːʒə/ | Gây mê toàn thân |
| 40 | Oral route | /ˈɔːrəl ruːt/ | Đường miệng |
| 41 | Endotracheal tube | /ˌɛndoʊˈtreɪkiəl tjuːb/ | Ống nội khí quản |
| 42 | Laryngeal mask airway | /læˈrɪndʒiəl mæsk ˈɛərweɪ/ | Mặt nạ thanh quản |
| 43 | Latex balloon | /ˈleɪtɛks bəˈluːn/ | Bóng cao su |
| 44 | Balloon applicator | /bəˈluːn ˈæplɪkeɪtər/ | Dụng cụ gắn bóng |
| 45 | Normal saline | /ˈnɔːrməl ˈseɪliːn/ | Nước muối sinh lý |
| 46 | Instrument channel | /ˈɪnstrəmənt ˈtʃænəl/ | Kênh dụng cụ |
| 47 | Lidocaine | /ˈlaɪdəkeɪn/ | Lidocain |
| 48 | Diagnostic bronchoscopy | /ˌdaɪəɡˈnɒstɪk brɒŋˈkɒskəpi/ | Nội soi phế quản chẩn đoán |
| 49 | Secretions | /sɪˈkriːʃənz/ | Dịch tiết |
| 50 | Bronchial tree anatomy | /ˈbrɒŋkiəl triː əˈnætəmi/ | Giải phẫu cây phế quản |
| 51 | Forward oblique angle | /ˈfɔːrwərd əˈbliːk ˈæŋɡəl/ | Góc nhìn chéo về phía trước |
| 52 | End-on view | /ɛnd-ɒn vjuː/ | Góc nhìn trực diện |
| 53 | Preprocedural imaging | /ˌpriːprəˈsiːdʒərəl ˈɪmɪdʒɪŋ/ | Hình ảnh học trước thủ thuật |
| 54 | Bronchial wall | /ˈbrɒŋkiəl wɔːl/ | Thành phế quản |
| 55 | Needle sheath | /ˈniːdəl ʃiːθ/ | Vỏ kim |
| 56 | White-light image | /waɪt-laɪt ˈɪmɪdʒ/ | Hình ảnh ánh sáng trắng |
| 57 | Cartilage rings | /ˈkɑːrtəlɪdʒ rɪŋz/ | Vòng sụn |
| 58 | AJCC/UICC staging systems | /ˌeɪ dʒeɪ siː siː / ˌjuː aɪ siː siː ˈsteɪdʒɪŋ ˈsɪstəmz/ | Hệ thống phân giai đoạn AJCC/UICC |
| 59 | Prevascular nodes | /ˌpriːˈvæskjələr noʊdz/ | Hạch trước mạch máu |
| 60 | Subaortic nodes | /sʌb.eɪˈɔːrtɪk noʊdz/ | Hạch dưới quai động mạch chủ |
| 61 | Paraaortic nodes | /ˌpærə.eɪˈɔːrtɪk noʊdz/ | Hạch cạnh động mạch chủ |
| 62 | Paraesophageal nodes | /ˌpærə.iːˌsɒfəˈdʒiːəl noʊdz/ | Hạch cạnh thực quản |
| 63 | Pulmonary ligament nodes | /ˈpʊlmənəri ˈlɪɡəmənt noʊdz/ | Hạch dây chằng phổi |
| 64 | Transesophageal | /ˌtrænsiːˌsɒfəˈdʒiːəl/ | Qua thực quản |
| 65 | Contamination | /kənˌtæmɪˈneɪʃən/ | Nhiễm bẩn |
| 66 | Over-staging | /ˈoʊvər-ˈsteɪdʒɪŋ/ | Tăng giai đoạn (sai) |
| 67 | On-site cytopathologist | /ɒn-saɪt ˌsaɪtoʊpəˈθɒlədʒɪst/ | Bác sĩ giải phẫu bệnh tế bào tại chỗ |
| 68 | Bleeding | /ˈbliːdɪŋ/ | Chảy máu |
| 69 | Infection | /ɪnˈfɛkʃən/ | Nhiễm trùng |
| 70 | Recurrent nerve paralysis | /rɪˈkɜːrənt nɜːrv pəˈræləsɪs/ | Liệt dây thần kinh quặt ngược |
| 71 | Mortality | /mɔːrˈtæləti/ | Tỷ lệ tử vong |
| 72 | Meta-analysis | /ˈmɛtə-əˈnæləsɪs/ | Phân tích tổng hợp |
| 73 | Pooled sensitivity | /puːld ˌsɛnsɪˈtɪvəti/ | Độ nhạy gộp |
| 74 | Confidence interval (CI) | /ˈkɒnfɪdəns ˈɪntərvəl/ | Khoảng tin cậy |
| 75 | Pooled specificity | /puːld ˌspɛsɪˈfɪsəti/ | Độ đặc hiệu gộp |
| 76 | Positron emission tomography (PET) | /ˈpɒzɪtrɒn ɪˈmɪʃən təˈmɒɡrəfi/ | Chụp cắt lớp phát xạ positron |
| 77 | PET-computed tomography (PET-CT) | /pɛt kəmˈpjuːtɪd təˈmɒɡrəfi/ | Chụp PET-CT |
| 78 | Thoracotomy | /ˌθɔːrəˈkɒtəmi/ | Mở lồng ngực |
| 79 | Mediastinoscopy | /ˌmiːdiəˌstaɪˈnɒskəpi/ | Nội soi trung thất |
| 80 | Video-assisted mediastinoscopy | /ˈvɪdioʊ əˈsɪstɪd ˌmiːdiəˌstaɪˈnɒskəpi/ | Nội soi trung thất qua video |
| 81 | B-mode imaging | /biː-moʊd ˈɪmɪdʒɪŋ/ | Hình ảnh B-mode |
| 82 | Short axis | /ʃɔːrt ˈæksɪs/ | Trục ngắn |
| 83 | Margin | /ˈmɑːrdʒɪn/ | Bờ (tổn thương) |
| 84 | Echogenicity | /ˌɛkoʊdʒəˈnɪsəti/ | Độ hồi âm |
| 85 | Homogeneous | /ˌhoʊməˈdʒiːniəs/ | Đồng nhất |
| 86 | Heterogeneous | /ˌhɛtəroʊˈdʒiːniəs/ | Không đồng nhất |
| 87 | Central hilar structure (CHS) | /ˈsɛntrəl ˈhaɪlər ˈstrʌktʃər/ | Cấu trúc rốn hạch trung tâm |
| 88 | Coagulation necrosis sign | /koʊˌæɡjəˈleɪʃən nɛˈkroʊsɪs saɪn/ | Dấu hiệu hoại tử đông |
| 89 | Non-small cell lung cancer (NSCLC) | /nɒn-smɔːl sɛl lʌŋ ˈkænsər/ | Ung thư phổi không tế bào nhỏ |
| 90 | Grayscale texture | /ˈɡreɪskeɪl ˈtɛkstʃər/ | Kết cấu thang độ xám |
| 91 | Anechoic | /ˌænɛˈkoʊɪk/ | Trống âm |
| 92 | Hypoechoic | /ˌhaɪpoʊɛˈkoʊɪk/ | Giảm âm |
| 93 | Isoechoic | /ˌaɪsoʊɛˈkoʊɪk/ | Đồng âm |
| 94 | Hyperechoic | /ˌhaɪpərɛˈkoʊɪk/ | Tăng âm |
| 95 | Positive predictive value (PPV) | /ˈpɒzətɪv prɪˈdɪktɪv ˈvæljuː/ | Giá trị dự báo dương tính |
| 96 | Negative predictive value (NPV) | /ˈnɛɡətɪv prɪˈdɪktɪv ˈvæljuː/ | Giá trị dự báo âm tính |
| 97 | Diagnostic accuracy | /ˌdaɪəɡˈnɒstɪk ˈækjərəsi/ | Độ chính xác chẩn đoán |
| 98 | Doppler imaging | /ˈdɒplər ˈɪmɪdʒɪŋ/ | Hình ảnh Doppler |
| 99 | Vascular patterns | /ˈvæskjələr ˈpætərnz/ | Các dạng mạch máu |
| 100 | Elastography | /ˌiːlæˈstɒɡrəfi/ | Siêu âm đàn hồi mô |
| 101 | Strain imaging | /streɪn ˈɪmɪdʒɪŋ/ | Hình ảnh biến dạng |
| 102 | Tissue stiffness | /ˈtɪʃuː ˈstɪfnəs/ | Độ cứng của mô |
| 103 | Stiff area ratio | /stɪf ˈɛəriə ˈreɪʃioʊ/ | Tỷ lệ diện tích cứng |
| 104 | Artificial intelligence | /ˌɑːrtɪˈfɪʃəl ɪnˈtɛlɪdʒəns/ | Trí tuệ nhân tạo |
| 105 | Artificial neural network | /ˌɑːrtɪˈfɪʃəl ˈnjʊərəl ˈnɛtwɜːrk/ | Mạng nơ-ron nhân tạo |
| 106 | Restaging | /ˌriːˈsteɪdʒɪŋ/ | Tái phân giai đoạn |
| 107 | Stage IIIA-cN2 NSCLC | /steɪdʒ θriː eɪ siː ɛn tuː ˌɛn ɛs siː ɛl siː/ | NSCLC giai đoạn IIIA-cN2 |
| 108 | Chemoradiotherapy | /ˌkiːmoʊˌreɪdioʊˈθɛrəpi/ | Hóa xạ trị |
| 109 | Neoadjuvant chemotherapy | /ˌniːoʊˈædʒəvənt ˌkiːmoʊˈθɛrəpi/ | Hóa trị tân bổ trợ |
| 110 | Down-staging | /daʊn-ˈsteɪdʒɪŋ/ | Giảm giai đoạn |
| 111 | Fibrosis | /faɪˈbroʊsɪs/ | Xơ hóa |
| 112 | Adhesions | /ədˈhiːʒənz/ | Dính |
| 113 | Remediastinoscopy | /ˌriːˌmiːdiəˌstaɪˈnɒskəpi/ | Nội soi trung thất lặp lại |
| 114 | False-negative rate | /fɔːls-ˈnɛɡətɪv reɪt/ | Tỷ lệ âm tính giả |
| 115 | Transcervical extended mediastinal lymphadenectomy | /ˌtrænzˈsɜːrvɪkəl ɪkˈstɛndɪd ˌmiːdiəˈstaɪnəl ˌlɪmfædəˈnɛktəmi/ | Phẫu thuật cắt bỏ hạch trung thất mở rộng qua đường cổ |
| 116 | Endosonographic-guided needle biopsy | /ˌɛndoʊsəˌnɒɡrəfɪk-ˈɡaɪdɪd ˈniːdəl ˈbaɪɒpsi/ | Sinh thiết bằng kim dưới hướng dẫn của nội soi siêu âm |
| 117 | Postinflammatory adhesions | /ˌpoʊstɪnˈflæmətəri ədˈhiːʒənz/ | Dính sau viêm |
| 118 | Degenerative changes | /dɪˈdʒɛnərətɪv ˈtʃeɪndʒɪz/ | Thay đổi thoái hóa |
| 119 | Molecular testing | /məˈlɛkjələr ˈtɛstɪŋ/ | Xét nghiệm phân tử |
| 120 | Molecular targeted therapy | /məˈlɛkjələr ˈtɑːrɡɪtɪd ˈθɛrəpi/ | Liệu pháp nhắm trúng đích phân tử |
| 121 | Sensitizing mutations | /ˈsɛnsɪtaɪzɪŋ mjuːˈteɪʃənz/ | Đột biến nhạy cảm |
| 122 | EGFR gene | /ˌiː dʒiː ɛf ɑːr dʒiːn/ | Gen EGFR |
| 123 | Anaplastic lymphoma kinase (ALK) gene fusion | /ˌænəˈplæstɪk lɪmˈfoʊmə ˈkaɪneɪs dʒiːn ˈfjuːʒən/ | Gen hợp nhất ALK |
| 124 | ROS1 gene rearrangements | /rɒs wʌn dʒiːn ˌriːəˈreɪndʒmənts/ | Tái sắp xếp gen ROS1 |
| 125 | BRAF mutations | /biː ɑːr eɪ ɛf mjuːˈteɪʃənz/ | Đột biến BRAF |
| 126 | Cytotoxic chemotherapy | /ˌsaɪtoʊˈtɒksɪk ˌkiːmoʊˈθɛrəpi/ | Hóa trị độc tế bào |
| 127 | Progression-free survival | /prəˈɡrɛʃən-friː sərˈvaɪvəl/ | Thời gian sống không tiến triển bệnh |
| 128 | National Comprehensive Cancer Network (NCCN) | /ˈnæʃənəl ˌkɒmprɪˈhɛnsɪv ˈkænsər ˈnɛtwɜːrk/ | Mạng lưới Ung thư Toàn diện Quốc gia (Hoa Kỳ) |
| 129 | Molecular profiling | /məˈlɛkjələr ˈproʊfaɪlɪŋ/ | Lập hồ sơ phân tử |
| 130 | Next-generation sequencing (NGS) | /nɛkst-ˌdʒɛnəˈreɪʃən ˈsiːkwənsɪŋ/ | Giải trình tự thế hệ mới |
| 131 | Programmed death-ligand 1 (PD-L1) staining | /ˈproʊɡræmd dɛθ-ˈlaɪɡənd wʌn ˈsteɪnɪŋ/ | Nhuộm PD-L1 |
| 132 | PIK3CA mutation | /pɪk θriː siː eɪ mjuːˈteɪʃən/ | Đột biến PIK3CA |
| 133 | KRAS mutation | /ˈkeɪræs mjuːˈteɪʃən/ | Đột biến KRAS |
| 134 | RET rearrangements | /rɛt ˌriːəˈreɪndʒmənts/ | Tái sắp xếp RET |
| 135 | MET exon 14 skipping mutations | /mɛt ˈɛksɒn fɔːrˈtiːn ˈskɪpɪŋ mjuːˈteɪʃənz/ | Đột biến bỏ qua MET exon 14 |
| 136 | HER2 mutations | /hɜːr tuː mjuːˈteɪʃənz/ | Đột biến HER2 |
| 137 | Rebiopsy | /ˌriːˈbaɪɒpsi/ | Sinh thiết lại |
| 138 | Personalized treatment plan | /ˈpɜːrsənəlaɪzd ˈtriːtmənt plæn/ | Kế hoạch điều trị cá nhân hóa |
| 139 | Subclassification | /ˌsʌbˌklæsɪfɪˈkeɪʃən/ | Phân loại phụ |
| 140 | Morphologic features | /ˌmɔːrfəˈlɒdʒɪk ˈfiːtʃərz/ | Đặc điểm hình thái |
| 141 | Phenotypic features | /ˌfiːnoʊˈtɪpɪk ˈfiːtʃərz/ | Đặc điểm kiểu hình |
| 142 | Genotypic features | /ˌdʒiːnoʊˈtɪpɪk ˈfiːtʃərz/ | Đặc điểm kiểu gen |
| 143 | Thoracoscopy | /ˌθɔːrəˈkɒskəpi/ | Nội soi lồng ngực |
| 144 | Ancillary testing | /ænˈsɪləri ˈtɛstɪŋ/ | Xét nghiệm bổ trợ |
| 145 | Flow cytometry | /floʊ saɪˈtɒmətri/ | Đếm tế bào dòng chảy |
| 146 | Fluorescence in situ hybridization (FISH) | /flʊəˈrɛsəns ɪn ˈsaɪtuː ˌhaɪbrɪdaɪˈzeɪʃən/ | Lai tại chỗ phát huỳnh quang |
| 147 | Lymphoma recurrence | /lɪmˈfoʊmə rɪˈkɜːrəns/ | U lympho tái phát |
| 148 | Noncaseating granulomas | /nɒnˈkeɪsieɪtɪŋ ˌɡrænjəˈloʊməz/ | U hạt không hoại tử bã đậu |
| 149 | Conventional transbronchial biopsy (TBB) | /kənˈvɛnʃənəl ˌtrænzˈbrɒŋkiəl ˈbaɪɒpsi/ | Sinh thiết xuyên thành phế quản thông thường |
| 150 | Lymphadenopathy | /ˌlɪmfædəˈnɒpəθi/ | Bệnh hạch bạch huyết |
| 151 | Endobronchial biopsy (EBB) | /ˌɛndoʊˈbrɒŋkiəl ˈbaɪɒpsi/ | Sinh thiết nội phế quản |
| 152 | Diagnostic odds ratio | /ˌdaɪəɡˈnɒstɪk ɒdz ˈreɪʃioʊ/ | Tỷ số chênh chẩn đoán |
| 153 | Pulmonary tuberculosis | /ˈpʊlmənəri tjuːˌbɜːrkjəˈloʊsɪs/ | Lao phổi |
| 154 | Intrathoracic tuberculosis | /ˌɪntrəθəˈræsɪk tjuːˌbɜːrkjəˈloʊsɪs/ | Lao nội ngực |
| 155 | Mediastinal cysts | /ˌmiːdiəˈstaɪnəl sɪsts/ | Nang trung thất |
| 156 | Malignant pleural mesothelioma | /məˈlɪɡnənt ˈplʊərəl ˌmiːzoʊˌθiːliˈoʊmə/ | U trung biểu mô màng phổi ác tính |
| 157 | Core biopsy | /kɔːr ˈbaɪɒpsi/ | Sinh thiết lõi |
| 158 | Histopathologic diagnosis | /ˌhɪstoʊˌpæθəˈlɒdʒɪk ˌdaɪəɡˈnoʊsɪs/ | Chẩn đoán mô bệnh học |
| 159 | Flexible tip segment | /ˈflɛksəbəl tɪp ˈsɛɡmənt/ | Đoạn đầu linh hoạt |
| 160 | Tissue surface area | /ˈtɪʃuː ˈsɜːrfəs ˈɛəriə/ | Diện tích bề mặt mô |
| 161 | Randomized control trial | /ˈrændəmaɪzd kənˈtroʊl ˈtraɪəl/ | Thử nghiệm đối chứng ngẫu nhiên |
| 162 | Specimen adequacy | /ˈspɛsəmən ˈædɪkwəsi/ | Độ đầy đủ của mẫu |
| 163 | Transbronchial needle injection (TBNI) | /ˌtrænzˈbrɒŋkiəl ˈniːdəl ɪnˈdʒɛkʃən/ | Tiêm kim xuyên thành phế quản |
| 164 | Bronchial fistulas | /ˈbrɒŋkiəl ˈfɪstjələz/ | Rò phế quản |
| 165 | Cisplatin injection | /sɪsˈplætɪn ɪnˈdʒɛkʃən/ | Tiêm Cisplatin |
| 166 | Complete response | /kəmˈpliːt rɪˈspɒns/ | Đáp ứng hoàn toàn |
| 167 | Partial response | /ˈpɑːrʃəl rɪˈspɒns/ | Đáp ứng một phần |
| 168 | Median survival | /ˈmiːdiən sərˈvaɪvəl/ | Thời gian sống trung vị |
| 169 | Aspergilloma | /ˌæspərdʒɪˈloʊmə/ | U nấm Aspergillus |
| 170 | Intralesional amphotericin B | /ˌɪntrəˈliːʒənəl ˌæmfəˈtɛrəsɪn biː/ | Amphotericin B tiêm trong tổn thương |
| 171 | Paradigm shift | /ˈpærədaɪm ʃɪft/ | Sự thay đổi mô hình |
| 172 | Precision medicine | /prɪˈsɪʒən ˈmɛdɪsɪn/ | Y học chính xác |
| 173 | Interventional pulmonary procedures | /ˌɪntərˈvɛnʃənəl ˈpʊlmənəri prəˈsiːdʒərz/ | Các thủ thuật hô hấp can thiệp |
| 174 | Malignancy | /məˈlɪɡnənsi/ | Bệnh ác tính |
| 175 | Benign conditions | /bɪˈnaɪn kənˈdɪʃənz/ | Tình trạng lành tính |
| 176 | Cytology | /saɪˈtɒlədʒi/ | Tế bào học |
| 177 | Pathology | /pəˈθɒlədʒi/ | Bệnh học |
| 178 | Biopsy | /ˈbaɪɒpsi/ | Sinh thiết |
| 179 | Aspiration | /ˌæspəˈreɪʃən/ | Chọc hút |
| 180 | Lesion | /ˈliːʒən/ | Tổn thương |
| 181 | Tumor | /ˈtjuːmər/ | Khối u |
| 182 | Diagnosis | /ˌdaɪəɡˈnoʊsɪs/ | Chẩn đoán |
| 183 | Prognosis | /prɒɡˈnoʊsɪs/ | Tiên lượng |
| 184 | Treatment | /ˈtriːtmənt/ | Điều trị |
| 185 | Complication | /ˌkɒmplɪˈkeɪʃən/ | Biến chứng |
| 186 | Evidence | /ˈɛvɪdəns/ | Bằng chứng |
| 187 | Guideline | /ˈɡaɪdlaɪn/ | Hướng dẫn |
| 188 | Sensitivity | /ˌsɛnsɪˈtɪvəti/ | Độ nhạy |
| 189 | Specificity | /ˌspɛsɪˈfɪsəti/ | Độ đặc hiệu |
| 190 | Prospective trial | /prəˈspɛktɪv ˈtraɪəl/ | Thử nghiệm tiền cứu |
| 191 | Retrospective study | /ˌrɛtrəˈspɛktɪv ˈstʌdi/ | Nghiên cứu hồi cứu |
| 192 | Algorithm | /ˈælɡərɪðəm/ | Thuật toán |
| 193 | Bronchoscope | /ˈbrɒŋkoʊskoʊp/ | Ống nội soi phế quản |
| 194 | Ultrasound probe | /ˈʌltrəˌsaʊnd proʊb/ | Đầu dò siêu âm |
| 195 | Local anesthesia | /ˈloʊkəl ˌænəsˈθiːʒə/ | Gây tê tại chỗ |
| 196 | Airway | /ˈɛərweɪ/ | Đường thở |
| 197 | Thoracic | /θəˈræsɪk/ | (Thuộc) lồng ngực |
| 198 | Staging | /ˈsteɪdʒɪŋ/ | Phân giai đoạn |
| 199 | Biopsy needle | /ˈbaɪɒpsi ˈniːdəl/ | Kim sinh thiết |
| 200 | Diagnostic yield | /ˌdaɪəɡˈnɒstɪk jiːld/ | Hiệu quả chẩn đoán |
