SÁCH DỊCH “Y HỌC CHU PHẪU: QUẢN LÝ HƯỚNG ĐẾN KẾT QUẢ, ẤN BẢN THỨ 2”
Được dịch và chuyển thể sang tiếng Việt từ sách gốc “Perioperative Medicine: Managing for Outcome, 2nd Edition”
Dịch và chú giải: Ths.Bs. Lê Đình Sáng – Hiệu đính: Ts.Bs.Lê Nhật Huy
Chương 42. Rối loạn nhận thức và sảng sau phẫu thuật
Postoperative Cognitive Dysfunction and Delirium – Mark F. Newman, Miles Berger and Joseph P. Mathew
Perioperative Medicine, 42, 613-627
Giới thiệu
Kể từ khi kỹ thuật gây mê ra đời và mở rộng khả năng thực hiện phẫu thuật, một số người bệnh đã xuất hiện những thay đổi về chức năng nhận thức hậu phẫu. Người bệnh cao tuổi có nguy cơ cao hơn đối với những thay đổi chức năng thần kinh nhận thức này, có lẽ do giảm dự trữ nhận thức và gia tăng xơ vữa động mạch não. Những thay đổi về chức năng nhận thức này liên quan đến suy giảm khả năng thực hiện các hoạt động sinh hoạt hàng ngày, làm giảm đáng kể chất lượng cuộc sống ở người bệnh cao tuổi. Nhiều thuật ngữ đã được sử dụng để mô tả những thay đổi chức năng thần kinh nhận thức hậu phẫu, từ “sảng hậu phẫu” (POD – Postoperative Delirium) đến “rối loạn nhận thức hậu phẫu” (POCD – Postoperative Cognitive Dysfunction) hoặc “rối loạn chức năng thần kinh nhận thức hậu phẫu” (POND – Postoperative Neurocognitive Dysfunction). Một ấn phẩm đồng thuận gần đây khuyến nghị sử dụng thuật ngữ “rối loạn thần kinh nhận thức quanh phẫu thuật” như một khái niệm bao quát cho suy giảm nhận thức được xác định trong giai đoạn trước hoặc sau phẫu thuật. Thuật ngữ này bao gồm suy giảm nhận thức được chẩn đoán trước phẫu thuật (được mô tả là rối loạn thần kinh nhận thức), các biến cố cấp tính (sảng hậu phẫu), và suy giảm nhận thức được chẩn đoán tới 30 ngày sau thủ thuật (phục hồi thần kinh nhận thức chậm) và tới 12 tháng (rối loạn thần kinh nhận thức hậu phẫu). Trong chương này, tập trung vào các biến chứng hậu phẫu, thuật ngữ POCD được sử dụng để phù hợp với tài liệu khoa học hiện có. Có khả năng các khuyến nghị về thuật ngữ mới sẽ giúp xác định rõ ràng hơn về mốc thời gian và tỷ lệ của POCD và sảng trong tương lai; tuy nhiên, một số tác giả hiện vẫn còn bày tỏ quan ngại về những khuyến nghị này.
Các cơ chế bệnh sinh cơ bản của sảng hậu phẫu và POCD là yếu tố then chốt để xác định các phương pháp tiếp cận nhằm giảm tỷ lệ mắc. Việc hiểu rõ nguyên nhân của những thay đổi quanh phẫu thuật này trở nên phức tạp bởi nhiều yếu tố. Trên thực tế, gây mê và phẫu thuật hiếm khi được thực hiện tách biệt, do đó khó có thể phân định rõ tác động riêng biệt của từng yếu tố lên chức năng nhận thức. Bên cạnh đó, người bệnh đến phòng mổ với các mức độ bệnh đồng mắc khác nhau có thể ảnh hưởng đến nhận thức (như bệnh mạch máu não) và các mức độ khác nhau của yếu tố bảo vệ có thể hỗ trợ duy trì nhận thức bình thường hậu phẫu (như trình độ học vấn cao). Sự kết hợp giữa các yếu tố liên quan đến thủ thuật và đặc điểm người bệnh này tạo nên các yếu tố quan trọng góp phần gây ra các vấn đề thần kinh nhận thức hậu phẫu.
An toàn trong gây mê và phẫu thuật đã có những tiến bộ vượt bậc qua nhiều thập kỷ đến mức ngay cả những người bệnh cao tuổi và suy yếu cũng có thể trải qua các thủ thuật phức tạp mà vẫn đảm bảo an toàn với nguy cơ biến chứng nặng và tử vong thấp; tuy nhiên, nhóm dân số này lại có nguy cơ cao về rối loạn chức năng thần kinh nhận thức. Chương này thảo luận về những thay đổi nhận thức thường gặp hậu phẫu và gây mê, cách xác định người bệnh có nguy cơ bị sảng hậu phẫu và/hoặc rối loạn nhận thức, và các biện pháp mà các bác sĩ lâm sàng có thể áp dụng để tối ưu hóa chức năng nhận thức hậu phẫu. Tuyên bố đồng thuận gần đây đã cố gắng xác định tác động lâm sàng của suy giảm nhận thức liên quan đến giai đoạn quanh phẫu thuật. Những đánh giá này định nghĩa lại POCD theo các cấu trúc y học lão khoa để có thể đánh giá hoặc dự đoán tốt hơn về tác động lâm sàng và chức năng trong ngắn hạn, trung hạn và dài hạn.
TỔN THƯƠNG HOẶC RỐI LOẠN CHỨC NĂNG HỆ THẦN KINH TRUNG ƯƠNG CHU PHẪU
Rối loạn chức năng hệ thần kinh trung ương (CNS) hậu phẫu bao gồm sảng khi tỉnh, kích động khi tỉnh, sảng hậu phẫu, POCD, hành vi thích ứng kém hậu phẫu và đột quỵ hậu phẫu. Những chẩn đoán này có các đặc điểm tương tự nhưng có thể được phân biệt chủ yếu qua thời gian diễn tiến khác nhau (Hình 42.1). Có sự chồng chéo đáng kể về các yếu tố nguy cơ và cơ chế bệnh sinh giữa sảng hậu phẫu và POCD, trong đó sảng dường như có tác động đến sự phát triển của cả rối loạn nhận thức hậu phẫu sớm và suy giảm nhận thức dài hạn.
SẢNG HẬU PHẪU
Sảng là một rối loạn về sự chú ý và nhận thức thể hiện sự thay đổi so với trạng thái nền, đi kèm với rối loạn nhận thức, và không phải do một bệnh lý có sẵn gây ra hoặc không xảy ra trong bối cảnh mức độ tỉnh táo bị giảm nặng. Tỷ lệ sảng hậu phẫu dao động từ 14% đến trên 50%, có thể phản ánh mức độ khác nhau của các yếu tố nguy cơ (như tuổi cao và các yếu tố khác). Tỷ lệ sảng thường bị báo cáo thấp hơn thực tế trong thực hành lâm sàng thường quy.
RỐI LOẠN NHẬN THỨC HẬU PHẪU TRONG PHẪU THUẬT TIM
Nhiều nghiên cứu đã sử dụng đánh giá thần kinh tâm lý trước và sau phẫu thuật để xác định POCD sau phẫu thuật tim và phẫu thuật không phải tim, với nhiều ngưỡng đánh giá thiếu hụt khác nhau để định nghĩa POCD. POCD trong khoảng 1 đến 3 tháng sau phẫu thuật tim và phẫu thuật không phải tim có tỷ lệ mắc được báo cáo rất đa dạng. Hầu hết các nghiên cứu cho thấy tỷ lệ rối loạn nhận thức hậu phẫu giảm dần theo thời gian từ 3 tháng đến 1 năm sau phẫu thuật. Một số yếu tố quan trọng cần xem xét khi diễn giải các nghiên cứu này. Thứ nhất, với hầu hết các bài kiểm tra thần kinh tâm lý, điểm số thường được cải thiện khi lặp lại kiểm tra trong khoảng thời gian ngắn (hiệu ứng học tập). Vấn đề này có thể được giảm thiểu một phần bằng cách kết hợp nhiều bài kiểm tra để đánh giá từng lĩnh vực nhận thức và sử dụng các phương pháp như phân tích yếu tố để tạo ra điểm số tổng thể cho từng lĩnh vực nhận thức. Do đó, một bộ đánh giá nhận thức tối ưu cần bao gồm các đánh giá trên các lĩnh vực nhận thức và phạm vi khả năng nhận thức đa dạng.
Ngoài ra, những thay đổi nhận thức hậu phẫu ở người lớn tuổi xảy ra chồng lên các thay đổi sinh lý thần kinh/nhận thức liên quan đến lão hóa bình thường, bao gồm cả bệnh lý thoái hóa thần kinh đã có sẵn. Do bệnh lý liên quan đến Alzheimer bắt đầu hình thành nhiều thập kỷ trước khi xuất hiện các triệu chứng nhận thức rõ ràng (như suy giảm trí nhớ), nhiều người bệnh cao tuổi có thể đã có bệnh lý thần kinh liên quan đến Alzheimer chưa biểu hiện lâm sàng; những người bệnh này có nguy cơ cao phát triển sảng hậu phẫu và POCD.
Nhiều ngưỡng thống kê và lâm sàng khác nhau đã được sử dụng để định nghĩa rối loạn nhận thức hậu phẫu. Một số ngưỡng dựa trên thay đổi trong một hoặc hai bài kiểm tra, một số dựa vào thay đổi trong các lĩnh vực nhận thức lớn hơn như sự chú ý và trí nhớ từ ngữ, và một số khác đo lường sự thay đổi tổng thể trong toàn bộ bộ kiểm tra nhận thức. Tùy thuộc vào ngưỡng và quy tắc thống kê được áp dụng, POCD có thể biểu hiện dưới dạng thiếu hụt ở một lĩnh vực đơn lẻ hoặc nhiều lĩnh vực về trí nhớ, chức năng điều hành hoặc các lĩnh vực khác. Hiện vẫn chưa rõ quỹ đạo nhận thức dài hạn khác nhau như thế nào khi phân tích theo từng lĩnh vực cụ thể (trí nhớ so với chức năng điều hành). Việc xem xét thời điểm đánh giá trước và sau phẫu thuật cũng rất quan trọng. Rối loạn nhận thức sớm sau phẫu thuật thường bị ảnh hưởng bởi đau hậu phẫu, các thuốc như opioid và quá trình hồi phục hậu phẫu cấp tính.
Rối loạn nhận thức toàn thể 1 năm sau phẫu thuật bắc cầu động mạch vành (CABG) có tương quan trực tiếp với chất lượng cuộc sống suy giảm, và cả rối loạn nhận thức toàn thể lẫn chất lượng cuộc sống giảm sút 1 năm sau CABG đều liên quan đến gia tăng triệu chứng trầm cảm tự báo cáo (nhưng không liên quan đến tăng triệu chứng lo âu). Mối tương quan giữa rối loạn nhận thức tổng thể và chất lượng cuộc sống vẫn tiếp tục được ghi nhận sau hơn 5 năm phẫu thuật tim, với mối liên hệ tương tự giữa cả hai thông số này và triệu chứng trầm cảm tự báo cáo. Mối tương quan giữa POCD và chất lượng cuộc sống xuất hiện trong toàn bộ phổ mức độ nghiêm trọng của rối loạn nhận thức ở thời điểm 1 và 5 năm sau phẫu thuật; ngay cả những thiếu hụt nhận thức hậu phẫu tương đối nhỏ cũng liên quan đến chất lượng cuộc sống suy giảm. Do đó, rối loạn nhận thức nên được xem như một hội chứng với phân bố mức độ nghiêm trọng khác nhau. Quan điểm cho rằng những thiếu hụt nhận thức hậu phẫu “dưới ngưỡng” vẫn có ý nghĩa đối với người bệnh phù hợp với xu hướng mới trong y học, coi nhiều quá trình bệnh lý như một phổ liên tục thay vì các đặc điểm tách biệt.
POCD LIÊN QUAN ĐẾN PHẪU THUẬT KHÔNG PHẢI TIM
POCD, một biến chứng đã được công nhận trong phẫu thuật tim, trước đây ít được đánh giá hoặc xác định sau phẫu thuật không phải tim cho đến khoảng 20 năm gần đây. Năm 1998, Nghiên cứu Quốc tế về Rối loạn Nhận thức Hậu phẫu (ISPOCD-1) đã đánh giá suy giảm nhận thức ở 1218 người bệnh cao tuổi trải qua phẫu thuật lớn không phải tim và phát hiện rằng rối loạn nhận thức xuất hiện ở 25% người bệnh sau 1 tuần phẫu thuật và ở 10% người bệnh sau 3 tháng phẫu thuật.
Để nghiên cứu sâu hơn về POCD sau phẫu thuật không phải tim, Monk và cộng sự đã thực hiện đánh giá tiền cứu trên 1064 người bệnh trải qua phẫu thuật không phải tim tự chọn. Nghiên cứu này phân chia đối tượng thành nhóm trẻ (18-39 tuổi), trung niên (40-59 tuổi) và người cao tuổi (≥60 tuổi). Một nhóm gồm 210 thành viên gia đình chính được sử dụng làm đối chứng để cung cấp điểm thay đổi tương tự như trong ISPOCD. Các người bệnh hoàn thành một loạt các bài kiểm tra nhận thức tại thời điểm cơ sở (trước phẫu thuật) và tại thời điểm 1 tuần và 3 tháng sau phẫu thuật.
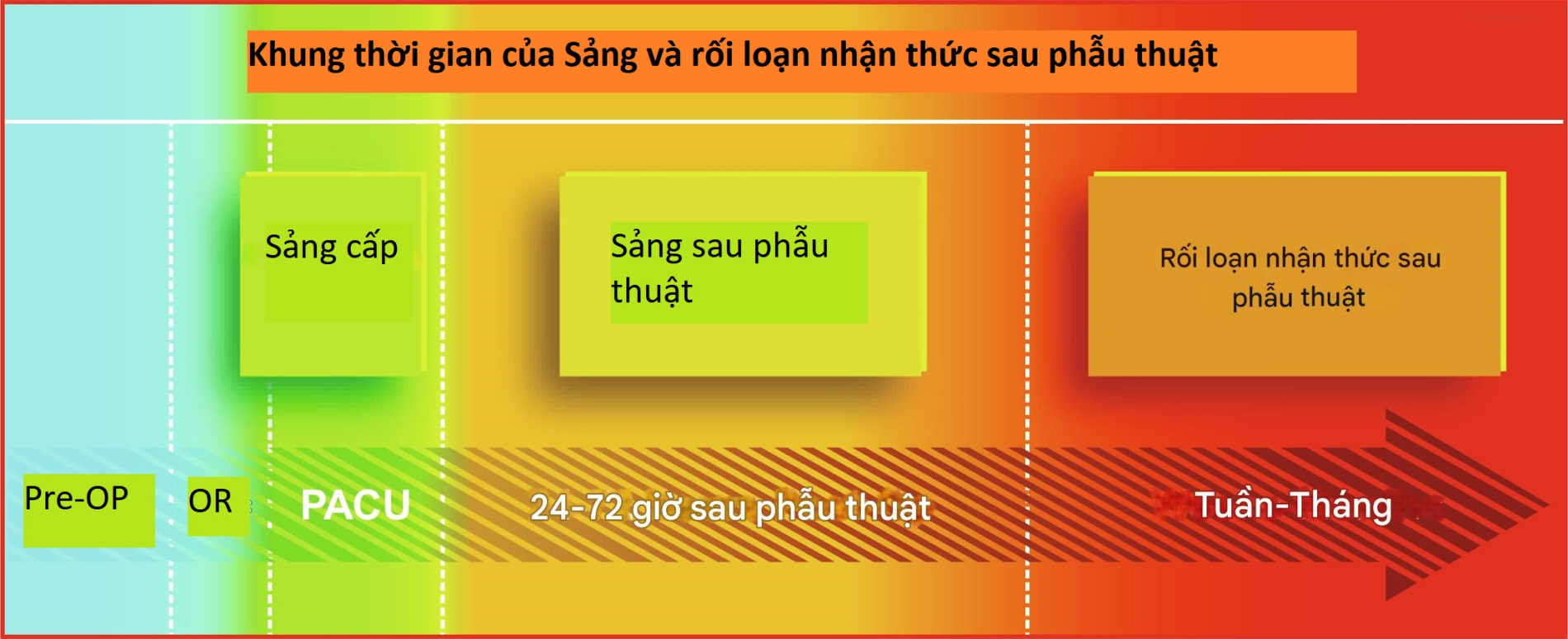
Hình 42.1 Một trong những đặc điểm phân biệt chính giữa sảng hậu phẫu (Post-Op) và rối loạn nhận thức hậu phẫu (POCD) là khung thời gian xuất hiện. Sảng khi tỉnh xảy ra trong phòng mổ (OR) hoặc ngay sau đó trong đơn vị hồi sức hậu phẫu (PACU). Sảng hậu phẫu xuất hiện trong khoảng 24 đến 72 giờ sau phẫu thuật. POCD được đánh giá từ vài tuần đến vài tháng sau phẫu thuật và gây mê. Pre-Op: Tiền phẫu.
Hình 42.2 cho thấy tỷ lệ POCD tại thời điểm xuất viện và 3 tháng hậu phẫu dựa trên đánh giá thần kinh tâm lý. Tại thời điểm xuất viện, tỷ lệ POCD là 36% ở người trẻ, 30,4% ở người trung niên và 41,4% ở người bệnh cao tuổi. Tỷ lệ suy giảm nhận thức thấp hơn đáng kể ở người bệnh trung niên so với người bệnh cao tuổi (P=0,01), nhưng không có sự khác biệt giữa người trẻ so với người cao tuổi hoặc người trẻ so với người trung niên. Tỷ lệ suy giảm nhận thức tương tự ở các đối tượng đối chứng cho tất cả các nhóm tuổi tại buổi kiểm tra hậu phẫu đầu tiên: 4,1% ở người trẻ, 2,8% ở người trung niên và 5,1% ở người bệnh cao tuổi. Tuy nhiên, sự khác biệt về suy giảm nhận thức giữa đối chứng theo độ tuổi và người bệnh là đáng kể đối với tất cả các nhóm tuổi (P<0,001). Sau 3 tháng phẫu thuật, POCD được xác định ở 5,7% người trẻ, 5,6% người trung niên và 12,7% người bệnh cao tuổi. POCD cao hơn đáng kể ở người cao tuổi so với người trẻ hoặc trung niên (P=0,001). Không có sự khác biệt về tỷ lệ POCD giữa đối tượng đối chứng cùng tuổi và người bệnh trong nhóm trẻ và trung niên. Tuy nhiên, người bệnh cao tuổi có tỷ lệ suy giảm nhận thức cao hơn đáng kể sau 3 tháng phẫu thuật so với đối tượng đối chứng cùng tuổi (P<0,001). Trong số các yếu tố dự đoán đơn biến có ý nghĩa đối với POCD sau 3 tháng phẫu thuật, chỉ có tuổi cao, trình độ học vấn thấp và POCD tại thời điểm xuất viện vẫn có ý nghĩa thống kê trong phân tích hồi quy logistic đa biến.
Kết quả của nghiên cứu này chỉ ra rằng rối loạn nhận thức hậu phẫu phổ biến ở tất cả các nhóm tuổi tại thời điểm 1 tuần. Tuy nhiên, sau 3 tháng phẫu thuật, tỷ lệ POCD cao hơn ở người cao tuổi có trình độ học vấn thấp. Monk và cộng sự không chỉ báo cáo về tỷ lệ POCD, mà còn theo dõi người bệnh sau 1 năm để thu thập dữ liệu tử vong. Họ phát hiện tỷ lệ tử vong 3 tháng tăng liên quan đến POCD tại thời điểm xuất viện so với những người không có POCD tại thời điểm xuất viện (P=0,02). Họ cũng phát hiện rằng những người bệnh có POCD cả tại thời điểm xuất viện và sau 3 tháng có tỷ lệ tử vong sau 1 năm cao hơn đáng kể so với bất kỳ nhóm nào khác (Hình 42.3).
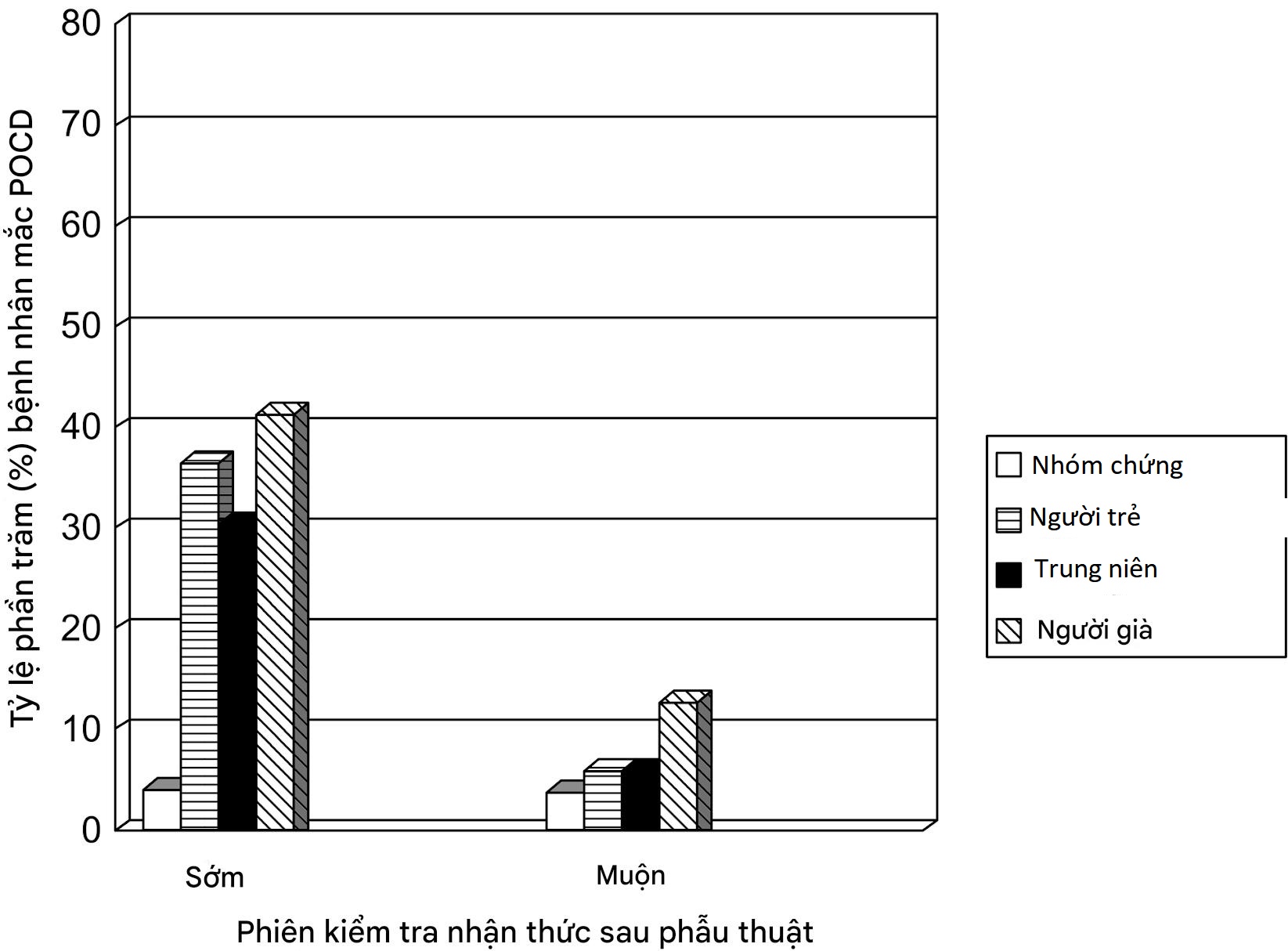
Hình 42.2 Tỷ lệ rối loạn nhận thức hậu phẫu (POCD) ở người bệnh trưởng thành sau phẫu thuật không phải tim: định nghĩa theo điểm Z.
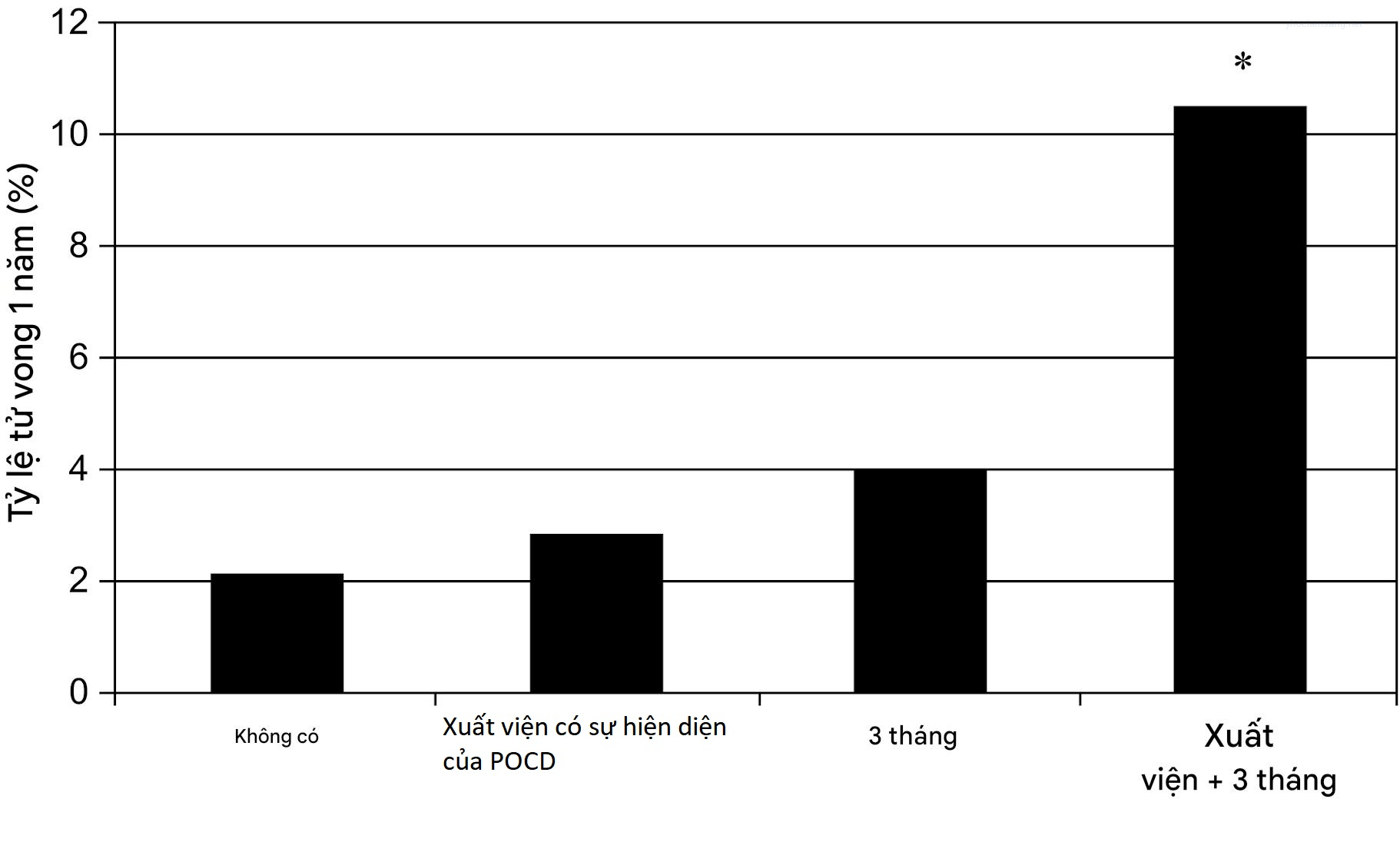
Hình 42.3 Mối quan hệ giữa sự hiện diện của rối loạn nhận thức hậu phẫu (POCD) và tỷ lệ tử vong trong năm đầu tiên sau phẫu thuật. Biểu đồ này chỉ bao gồm những người bệnh sống sót đến thời điểm kiểm tra 3 tháng. Hình bao gồm bốn nhóm: không có POCD (người bệnh không gặp POCD ở bất kỳ thời điểm kiểm tra nào), xuất viện (người bệnh chỉ có POCD tại thời điểm xuất viện), 3 tháng (người bệnh chỉ có POCD tại buổi kiểm tra 3 tháng), và xuất viện + 3 tháng (người bệnh có POCD cả tại thời điểm xuất viện và 3 tháng). Nhóm xuất viện + 3 tháng có tỷ lệ tử vong khác biệt đáng kể so với 3 nhóm còn lại, P=0,02*.
BỆNH SINH CỦA RỐI LOẠN THẦN KINH NHẬN THỨC HẬU PHẪU
Nhìn chung, POCD có nguồn gốc đa yếu tố. Các yếu tố nguy cơ và cơ chế góp phần gây ra sảng hậu phẫu và rối loạn nhận thức hậu phẫu có thể được phân loại theo nhiều cách. Các yếu tố nguy cơ của người bệnh được xác định rõ ràng bao gồm những yếu tố hiện diện trước phẫu thuật và những yếu tố xuất hiện trong và sau phẫu thuật và gây mê (như tuần hoàn ngoài cơ thể hoặc liều gây mê) (Bảng 42.1). Sự phân chia này có giá trị giúp xác định các mục tiêu để dự báo hoặc phòng ngừa POCD tại các thời điểm cụ thể trong quá trình chăm sóc quanh phẫu thuật. Cũng cần lưu ý rằng một số yếu tố nguy cơ và cơ chế bệnh sinh có thể điều chỉnh được trong khi một số khác thì không.
Một cách khác để phân loại nguyên nhân là theo các quá trình bệnh sinh tiềm ẩn, chẳng hạn như viêm, tổn thương thần kinh, tổn thương mạch máu/thuyên tắc, rối loạn điều hòa tự động não và cung cấp oxy, bệnh lý thoái hóa thần kinh và rối loạn chức năng mạng lưới não. Những yếu tố này có sự chồng chéo và sẽ được thảo luận chi tiết trong các phần tiếp theo.
Bảng 42.1 Các yếu tố có thể điều chỉnh, một phần có thể điều chỉnh và không thể điều chỉnh có thể góp phần gây ra sảng hậu phẫu và/hoặc rối loạn nhận thức hậu phẫu sau phẫu thuật tim.
| Tiền phẫu/hậu phẫu | Trong phẫu thuật |
|---|---|
| Có thể điều chỉnh | |
| (1) Kiểm soát huyết áp tiền phẫu | (1) Sử dụng tuần hoàn ngoài cơ thể |
| (2) Kiểm soát đường huyết tiền phẫu | (2) Quản lý nhiệt độ |
| (3) Gián đoạn giấc ngủ/ngưng thở khi ngủ | (3) Thời gian phẫu thuật |
| (4) Lạm dụng rượu | (4) Quản lý huyết áp động mạch |
| (5) Giảm đau hậu phẫu, kiểm soát sảng | (5) Kiểm soát đường huyết |
| (6) Pha loãng máu | |
| Một phần có thể điều chỉnh | |
| (1) Tình trạng suy yếu của người bệnh | (1) Phương pháp phẫu thuật (đường giữa xương ức so với mở ngực bên), Có hoặc Không tuần hoàn ngoài cơ thể |
| (2) Chức năng nhận thức tiền phẫu | (2) Liều lượng gây mê và đáp ứng EEG |
| (3) Dự trữ thần kinh nhận thức tiền phẫu | |
| (4) Trầm cảm | |
| Không thể điều chỉnh | |
| (1) Tuổi của người bệnh | (1) Tổn thương cơ tim trực tiếp |
CPB: Tuần hoàn ngoài cơ thể; EEG: điện não đồ.
VIÊM
Quá trình viêm liên quan đến phẫu thuật và gây mê đóng vai trò quan trọng trong cơ chế gây sảng và rối loạn nhận thức hậu phẫu. Chấn thương mô trong phẫu thuật dẫn đến giải phóng các cytokine và chemokine liên quan đến tổn thương. Những chất trung gian này kích hoạt đáp ứng viêm toàn thân làm tăng giải phóng interleukin IL-1 và IL-6, yếu tố hoại tử u (TNF)-α, và các phân tử liên quan đến tổn thương như high mobility group box-1 và các protein gắn canxi S100 (Hình 42.4). Các chất trung gian viêm toàn thân có thể xâm nhập vào não do sự phá vỡ hàng rào máu não sau phẫu thuật. Rối loạn chức năng hàng rào máu não thường gặp ở người cao tuổi (ngay cả khi không phẫu thuật) và đã được ghi nhận ở 50% người bệnh sau phẫu thuật tim. Hơn nữa, mức độ phá vỡ hàng rào máu não hậu phẫu có tương quan với mức độ rối loạn nhận thức sau phẫu thuật tim. Viêm thần kinh có đủ tác động bất lợi để gây ra thiếu hụt về nhận thức, trí nhớ và hành vi, và đã được chứng minh liên quan đến các tình trạng từ rối loạn tâm trạng đến bệnh thoái hóa thần kinh và rối loạn nhận thức hậu phẫu.
Vai trò của viêm thần kinh trong rối loạn nhận thức hậu phẫu được củng cố bởi các nghiên cứu chứng minh rằng các đa hình gen điều hòa viêm (ví dụ: CRP, SELP, GPIIIA và iNOS) có liên quan đến nguy cơ rối loạn nhận thức hậu phẫu. Viêm trong phẫu thuật tim trở nên trầm trọng hơn do máu tiếp xúc với bề mặt ngoại lai của mạch tuần hoàn ngoài cơ thể (CPB) gây viêm ngoại biên đáng kể, bao gồm tăng nhiều lần các cytokine tiền viêm interleukin 6 và 8 (IL-6, IL-8) cũng thấy trong phẫu thuật không phải tim. Thác bổ thể cổ điển cũng có thể được kích hoạt bởi các phức hợp heparin-protamine sau CPB. Mở xương ức và rạch da cũng làm tăng mức cytokine tiền viêm ở chuột, và có thể ở người, mặc dù một số nghiên cứu không lặp lại được những phát hiện này.

Hình 42.4 Cơ chế bệnh sinh có thể đóng vai trò trong rối loạn nhận thức hậu phẫu (POCD) và/hoặc sảng. Theo chiều kim đồng hồ từ phía trên cùng, các hộp mở rộng đại diện cho các cơ chế cấp tế bào/phân tử và synap thần kinh (như bệnh lý liên quan đến Alzheimer), theo dõi oxy não, liều lượng gây mê, quá trình giải quyết viêm, cơ chế mạch máu (như thuyên tắc) và rối loạn chức năng hàng rào máu não, có thể liên quan đến POCD và sảng. APP: protein tiền chất amyloid; CNS: hệ thần kinh trung ương; RBC: hồng cầu.
Ngoài ra, chính các thuốc gây mê, dù trong phẫu thuật tim hay không phải tim, cũng có thể điều hòa quá trình viêm. Thuốc mê hít có tác dụng tiền viêm trên tế bào hỗ trợ thần kinh (microglia) và opioid cùng heparin cũng có thể điều hòa viêm và chức năng tế bào đơn nhân in vitro. Do đó, thuốc được sử dụng trong phẫu thuật có thể có tác động đáng kể đến cân bằng tổng thể của các cytokine tiền viêm và kháng viêm, từ đó ảnh hưởng đến kết quả của người bệnh. Xét tổng thể, những phát hiện này cho thấy việc tiếp xúc với thuốc gây mê và các thuốc khác trong phẫu thuật, cùng với tác động của chấn thương phẫu thuật hoặc các yếu tố khác như vết cắt, mở xương ức, tổn thương mô và tổn thương do thiếu máu tái tưới, có thể góp phần gây viêm thần kinh và dẫn đến sảng hậu phẫu và rối loạn nhận thức hậu phẫu tiếp theo.
Trong các mô hình chuột, phẫu thuật tim gây viêm thần kinh kéo dài hơn và có phổ suy giảm hành vi rộng hơn so với phẫu thuật bụng, mặc dù cả hai loại phẫu thuật đều làm giảm tạo thần kinh mới ở hồi hải mã và mức độ yếu tố dinh dưỡng thần kinh (như yếu tố dinh dưỡng thần kinh có nguồn gốc từ não). Terrando đã phát hiện ra viêm thần kinh tương tự và những thay đổi hành vi sau phẫu thuật chỉnh hình ở chuột, cho thấy rằng các cơ chế chung liên quan đến giảm tạo thần kinh mới ở hồi hải mã, truyền tín hiệu đau tủy sống và viêm thần kinh trung ương có thể dẫn đến rối loạn trí nhớ sau cả phẫu thuật chỉnh hình và tim. Việc ức chế viêm thần kinh và hoạt hóa tế bào hỗ trợ thần kinh làm giảm thiếu hụt trí nhớ hậu phẫu trong các mô hình chuột, mặc dù những can thiệp này chưa được thử nghiệm ở người.
Một số thử nghiệm thuốc kháng viêm đã không thành công trong việc ngăn ngừa sảng hoặc rối loạn nhận thức hậu phẫu tim, bao gồm lidocaine, magie, các chất ức chế bổ thể và điều trị acetylcholinesterase hậu phẫu. Steroid liều cao trong mổ cũng không hiệu quả, có lẽ vì steroid cũng có thể gây sảng và ảo giác, có thể khởi phát tác dụng đối nghịch với tác dụng kháng viêm thần kinh cải thiện nhận thức. Điều trị ketamine trong mổ làm giảm sảng và rối loạn nhận thức sau phẫu thuật tim trong các nghiên cứu thí điểm nhỏ, nhưng không làm giảm sảng trong một thử nghiệm ngẫu nhiên đa trung tâm lớn (bao gồm cả người bệnh phẫu thuật tim và không phải tim). Dexmedetomidine cũng không có tác dụng giảm tỷ lệ sảng sau phẫu thuật tim trong một thử nghiệm ngẫu nhiên đa trung tâm gần đây, mặc dù nó có tác dụng hỗn hợp đối với sảng sau phẫu thuật không phải tim; những kết quả khác biệt này có thể do tốc độ truyền và thời gian dexmedetomidine khác nhau giữa các nghiên cứu. Sự chiếm ưu thế của các kết quả nghiên cứu âm tính có thể phản ánh sự phức tạp của sảng và rối loạn nhận thức hậu phẫu, điều này cũng có thể giải thích thành công tương đối lớn hơn của các can thiệp đa phương thức. Các chiến lược thay thế nhằm mục tiêu cụ thể hơn vào quá trình viêm hậu phẫu có thể hiệu quả hơn trong việc ngăn ngừa sảng hậu phẫu và rối loạn nhận thức hậu phẫu.
TẢI THUYÊN TẮC
Gánh nặng thuyên tắc cũng có thể đóng vai trò trong rối loạn thần kinh nhận thức sau phẫu thuật tim và không phải tim. Thao tác trực tiếp với động mạch chủ trong phẫu thuật tim thường phá vỡ các mảng xơ vữa. Tăng gánh nặng mảng xơ vữa trong mổ đã được ghi nhận ở người bệnh có rối loạn nhận thức hậu phẫu (so với những người không có rối loạn nhận thức hậu phẫu) tại tuần thứ 1, nhưng không tại tuần 3 hoặc 12, sau phẫu thuật tim. Hướng dẫn hiện hành khuyến nghị đánh giá mảng xơ vữa động mạch chủ bằng siêu âm ngoài thành động mạch chủ ở người bệnh có nguy cơ đột quỵ tăng, bao gồm những người có tiền sử bệnh mạch máu và những người có bằng chứng khác về xơ vữa động mạch chủ hoặc vôi hóa. Sự phá vỡ mảng xơ vữa động mạch chủ có thể giải phóng vi thuyên tắc có thể di chuyển đến não. Những vi thuyên tắc này có thể được phát hiện bằng siêu âm Doppler xuyên sọ, mặc dù phần lớn các tín hiệu Doppler xuyên sọ thực ra đại diện cho các thuyên tắc khí nhỏ.
Vi thuyên tắc khí xảy ra thường xuyên trong các ca phẫu thuật van tim với buồng tim hở, điều này đã khiến nhiều trung tâm tiến hành bơm carbon dioxide vào buồng tim hở, vì carbon dioxide hòa tan tốt hơn không khí và do đó thúc đẩy sự tái hấp thu của các thuyên tắc khí. Tuy nhiên, một thử nghiệm ngẫu nhiên cho thấy việc bơm trường phẫu thuật với carbon dioxide so với không khí y tế không có tác dụng cải thiện chức năng nhận thức 6 tuần sau phẫu thuật.
Vi thuyên tắc cũng có thể được phát hiện bằng cộng hưởng từ trọng số khuếch tán (MRI) hậu phẫu, mặc dù cần có hình ảnh MRI trước phẫu thuật để phân biệt vi thuyên tắc mới với các tổn thương đã có trước đó. Tỷ lệ phần trăm người bệnh phẫu thuật tim có vi thuyên tắc có thể phát hiện được vượt xa tỷ lệ phần trăm người bệnh có đột quỵ hậu phẫu lâm sàng rõ ràng. Nhiều chuyên gia gọi những thuyên tắc này và những bất thường trên MRI trọng số khuếch tán là “đột quỵ kín về mặt lâm sàng,” vì chúng không liên quan đến các bất thường thần kinh phát hiện được trong khám lâm sàng thông thường.
Mặc dù dường như hợp lý khi cho rằng gánh nặng thuyên tắc vào não và tăng tín hiệu chất trắng trên MRI T2 sẽ có tác động bất lợi đến chức năng thần kinh nhận thức, nhưng mối tương quan giữa gánh nặng thuyên tắc và thay đổi nhận thức hậu phẫu không nhất quán. Vấn đề này phức tạp và các nghiên cứu quan sát đã phát hiện ra rằng những “đột quỵ kín về mặt lâm sàng” này có liên quan đến nguy cơ đột quỵ, suy giảm nhận thức và bệnh Alzheimer trong tương lai. Tương tác giữa gánh nặng thuyên tắc, viêm thần kinh trung ương và các biến số khác có thể phối hợp theo cách hiệp đồng để gây ra rối loạn thần kinh nhận thức hậu phẫu.
DÒNG MÁU NÃO, ĐIỀU HÒA TỰ ĐỘNG VÀ CUNG CẤP OXY
Kể từ khi áp dụng CPB với dòng máu không đập, áp lực tưới máu thấp đã bị cho là nguyên nhân gây ra cả đột quỵ và POCD. Hơn nữa, tỷ lệ ngày càng tăng của người bệnh phẫu thuật cao tuổi (cả tim và không phải tim) bị tăng huyết áp, có thể làm thay đổi phạm vi điều hòa tự động bình thường của dòng máu não (thường được cho là từ 60 đến 160 mmHg) và do đó làm tăng nguy cơ giảm tưới máu. Phạm vi điều hòa tự động thực tế cho mỗi người bệnh là không xác định, và giới hạn dưới của điều hòa tự động trong CPB có thể dao động từ 45 đến 80 mmHg. Newman và cộng sự phát hiện ra sự suy giảm đáng kể về điều hòa tự động não ở 215 người bệnh trong phẫu thuật tim, nhưng không tìm thấy mối tương quan với rối loạn nhận thức hậu phẫu. Tương tự, Joshi và cộng sự phát hiện ra rằng tới 20% người bệnh phẫu thuật tim có điều hòa tự động suy giảm và những người bệnh có dòng máu não “thụ động theo áp lực” này có tỷ lệ đột quỵ quanh phẫu thuật tăng. Hơn nữa, điều hòa tự động não trong mổ có thể thay đổi động học đáp ứng với những thay đổi sinh lý trong mổ, cho thấy sự cần thiết của việc đo lường điều hòa tự động não theo thời gian thực.
Các nghiên cứu về mối quan hệ giữa quản lý huyết áp động mạch trung bình (MAP) và thay đổi nhận thức hậu phẫu đã cho thấy kết quả khác nhau. Ví dụ, duy trì MAP trong mổ từ 80-90 mmHg, thay vì 60-70 mmHg, liên quan đến giảm tỷ lệ sảng hậu phẫu và giảm mức suy giảm điểm Kiểm tra Tình trạng Tâm thần Tối thiểu sau phẫu thuật. Gold và cộng sự phát hiện ra rằng mục tiêu MAP cao hơn (80-100 mmHg so với 50-60 mmHg) có liên quan đến tỷ lệ biến chứng tim và thần kinh thấp hơn (như đột quỵ); tuy nhiên, họ không tìm thấy sự khác biệt về nhận thức hậu phẫu giữa các nhóm. Phần lớn sự thay đổi này, đặc biệt là tỷ lệ đột quỵ, sau đó được xác định chủ yếu liên quan đến mức độ xơ vữa động mạch chủ, với áp lực chỉ có tác dụng đáng kể ở những người bệnh có xơ vữa động mạch chủ nặng. Giá trị MAP hậu phẫu dưới giới hạn thấp của điều hòa tự động cũng đã được liên hệ với sự gia tăng dấu ấn sinh học tổn thương tế bào thần kinh đệm (glial fibrillary acidic protein), nhấn mạnh tầm quan trọng của việc duy trì MAP trong phạm vi điều hòa tự động. Tuy nhiên, các nghiên cứu quan sát cũng phát hiện ra rằng việc duy trì huyết áp trên giới hạn trên của điều hòa tự động não có liên quan đến tỷ lệ sảng hậu phẫu tăng, cho thấy rằng cần tránh cả MAP trên và dưới phạm vi điều hòa tự động của mỗi người bệnh.
QUẢN LÝ NHIỆT ĐỘ TRONG PHẪU THUẬT TIM
Tốc độ chuyển hóa oxy ở não (CMRO2) có liên quan chặt chẽ với nhiệt độ, điều này dẫn đến thực hành giảm tốc độ chuyển hóa oxy não bằng cách gây hạ thân nhiệt, từ đó giảm thiếu oxy não và tổn thương thần kinh nhận thức trong thời gian giảm cung cấp oxy. Hạ thân nhiệt làm giảm tổn thương thần kinh trong các mô hình động vật về thiếu máu cục bộ não và hồi sức tim phổi. Ngược lại, tăng thân nhiệt làm tăng tốc độ chuyển hóa oxy não và có liên quan đến kết quả thần kinh nhận thức xấu hơn và tăng nguy cơ tử vong trong nhiều tình huống lâm sàng. Do đó, các nghiên cứu đã đánh giá liệu việc giảm tốc độ chuyển hóa oxy não bằng cách gây hạ thân nhiệt trong CPB có cải thiện chức năng thần kinh nhận thức hậu phẫu hay không. Nghiên cứu ban đầu cho thấy người bệnh trải qua CPB bình thường (tức là “ấm” hoặc >35°C) có tỷ lệ đột quỵ cao gấp ba lần so với những người trải qua CPB hạ thân nhiệt (tức là “lạnh” hoặc <28°C). Tuy nhiên, một thử nghiệm ngẫu nhiên không tìm thấy lợi ích của hạ thân nhiệt (28-30°C) so với bình thường thân nhiệt (35,5-36,5°C) trong CPB đối với thay đổi nhận thức từ trước phẫu thuật tim đến 6 tuần sau phẫu thuật. Mặc dù vậy, nhiệt độ tối đa hậu phẫu sau phẫu thuật tim có liên quan đến mức độ nghiêm trọng của rối loạn nhận thức 6 tuần sau phẫu thuật, nhấn mạnh tầm quan trọng của việc tránh tăng thân nhiệt hậu phẫu.
Khái niệm này có thể giúp giải thích dữ liệu cho thấy rằng làm ấm lại đến nhiệt độ thấp hơn (34°C so với 37°C) có liên quan đến tỷ lệ rối loạn nhận thức thấp hơn 1 tuần sau phẫu thuật và cải thiện hiệu suất trong nghiệm pháp định hướng không gian bằng chốt (một nhiệm vụ về khéo léo tay và tốc độ xử lý thị giác-vận động) sau 3 tháng phẫu thuật, mặc dù không có lợi ích nhận thức tổng thể sau 3 tháng phẫu thuật. Về cơ bản, lợi ích nhận thức sớm của việc làm ấm lại đến mức nhiệt thấp hơn trong nghiên cứu này có thể là nhờ ngăn ngừa tăng thân nhiệt hậu phẫu. Nhóm nghiên cứu này cũng không tìm thấy sự khác biệt về kết quả thần kinh nhận thức giữa các người bệnh CABG được chọn ngẫu nhiên để trải qua CPB bình thường thân nhiệt (37°C) hoặc CPB hạ thân nhiệt (34°C) mà không làm ấm lại trong phòng mổ ở cả hai nhóm; do đó, tránh tăng thân nhiệt trung tâm trong quá trình làm ấm lại có thể giúp tối ưu hóa chức năng nhận thức hậu phẫu. Tương tự, một thử nghiệm ngẫu nhiên gần đây cho thấy việc đạt được nhiệt độ cơ thể trung tâm thấp hơn (thông qua làm mát đầu bên ngoài) trong CPB có liên quan đến giảm rối loạn nhận thức 10 ngày sau phẫu thuật tim.
Mặc dù có nhiều nghiên cứu, vẫn còn tranh luận về quản lý nhiệt độ trong phẫu thuật tim. Các khuyến nghị lâm sàng hiện tại chỉ kêu gọi tránh tăng thân nhiệt (nhiệt độ máu ra ở động mạch ≥37°C) trong phẫu thuật tim và giữ tốc độ làm ấm lại ≤0,5°C/phút khi nhiệt độ vượt quá 30°C. Làm ấm lại chậm có thể giúp tránh thiếu máu não vì làm ấm lại nhanh đã được chứng minh gây tăng tốc độ chuyển hóa oxy não trước khi có sự tăng tương ứng của dòng máu não.
CÂN BẰNG GLUCOSE TRONG PHẪU THUẬT TIM
Chức năng thần kinh nhận thức thường không bị ảnh hưởng bởi thay đổi glucose trong giới hạn sinh lý bình thường. Do nhiều người bệnh phẫu thuật bị tiểu đường và đáp ứng stress phẫu thuật có thể làm giảm độ nhạy insulin ngoại vi, dẫn đến tăng đường huyết, các nghiên cứu đã đánh giá mối quan hệ giữa quản lý glucose trong mổ và kết quả thần kinh nhận thức hậu phẫu. Một nghiên cứu hồi cứu cho thấy tăng đường huyết trong mổ (glucose >200 mg/dL) có liên quan đến chức năng nhận thức hậu phẫu xấu đi ở người bệnh không tiểu đường, nhưng không ở người bệnh tiểu đường. Điều này dễ hiểu vì người bệnh tiểu đường thường xuyên bị tăng đường huyết, kích hoạt các cơ chế bù trừ sinh lý (như giảm điều hòa chất vận chuyển glucose ở mao mạch não) để giảm lượng glucose vào não quá mức. Sự thích nghi này giúp giải thích tại sao tăng đường huyết trong mổ có thể có hại hơn cho não của người bệnh không tiểu đường. Tuy nhiên, giải thích này bị thách thức bởi kết quả của một thử nghiệm ngẫu nhiên lớn (n=381) cho thấy truyền insulin trong mổ (lên đến 4 đơn vị/giờ) ở người bệnh không tiểu đường không cải thiện kết quả thần kinh nhận thức.
Quan điểm cho rằng tăng đường huyết có hại cho não đã dẫn đến các nghiên cứu can thiệp đánh giá liệu kiểm soát glucose chặt chẽ hơn có cải thiện nhận thức hậu phẫu hay không. Tuy nhiên, kiểm soát glucose chặt chẽ trong mổ với kẹp bình thường đường huyết tăng insulin (mục tiêu glucose 80-110 mg/dL) so với liệu pháp tiêu chuẩn (mục tiêu glucose <150 mg/dL) trong phẫu thuật tim lại có liên quan đến tỷ lệ sảng tăng, có lẽ do tăng nguy cơ hạ đường huyết trong nhóm kiểm soát glucose chặt chẽ. Một nghiên cứu khác cho thấy việc sử dụng truyền glucose và insulin để duy trì glucose huyết thanh ở 64-110 mg/dL có tác dụng bảo tồn khả năng học tập âm thanh và chức năng điều hành sau phẫu thuật tim, cho thấy rằng tránh tăng đường huyết có thể dẫn đến cải thiện chức năng nhận thức hậu phẫu. Những dữ liệu này cho thấy việc tránh cả hạ đường huyết và tăng đường huyết đều quan trọng để ngăn ngừa sảng hậu phẫu và rối loạn nhận thức hậu phẫu. Các thích nghi sinh lý đối với tăng đường huyết mạn tính ở người bệnh tiểu đường gợi ý rằng kiểm soát đường huyết trong mổ nên được cá nhân hóa.
TRẦM CẢM
Nghiên cứu về trầm cảm liên quan đến phẫu thuật tim cho thấy trầm cảm tiền phẫu có liên quan đến giảm tỷ lệ sống sót dài hạn hậu phẫu và cũng dự báo sự phát triển của rối loạn nhận thức hậu phẫu. Mối quan hệ nhân quả chính xác giữa trầm cảm tiền phẫu và hậu phẫu, chất lượng cuộc sống và rối loạn nhận thức vẫn cần được làm rõ hơn.
YẾU TỐ DI TRUYỀN
Một phát triển thú vị trong lĩnh vực bảo vệ thần kinh liên quan đến xu hướng di truyền hoặc tính nhạy cảm với tổn thương não liên quan đến phẫu thuật. Khả năng bộ gen di truyền có thể ảnh hưởng đến kết quả nhận thức sau phẫu thuật tim lần đầu tiên được mô tả trong một nghiên cứu năm 1997. Trong nghiên cứu đó, giả thuyết apolipoprotein E đã được đề xuất, cho rằng người bệnh mang alen Apo E4 có kết quả nhận thức kém hơn sau CPB. Mặc dù không phải tất cả các nghiên cứu đều lặp lại được phát hiện này, việc xem xét mối liên hệ giữa rối loạn nhận thức hậu phẫu và sảng với các cơ chế tương tự như trong bệnh Alzheimer đã dẫn đến nhiều nghiên cứu sâu hơn. Những nghiên cứu này cho kết quả không nhất quán; nhìn chung, người mang ApoE4 dường như không có nguy cơ phát triển sảng hậu phẫu sớm hoặc rối loạn nhận thức hậu phẫu cao hơn, nhưng lại có quỹ đạo nhận thức dài hạn kém hơn sau phẫu thuật tim. Phát hiện này có thể liên quan đến tác động bất lợi dài hạn đã biết của alen ApoE4 lên nhận thức, và/hoặc đến sự gia tăng gánh nặng mảng xơ vữa cung động mạch chủ thấy ở những người mang ApoE4, dẫn đến tăng nguy cơ vi thuyên tắc não trong phẫu thuật tim. Một số đa hình gen khác gần đây đã được phát hiện có liên quan đến nguy cơ bệnh Alzheimer, và việc kiểm tra mối liên hệ giữa các đa hình gen này với rối loạn nhận thức hậu phẫu hoặc nguy cơ sảng sau phẫu thuật sẽ là một hướng nghiên cứu quan trọng.
Để nghiên cứu thêm về vai trò tiềm tàng của viêm và hình thành huyết khối trong POCD, Mathew và cộng sự đã mô tả đặc điểm đa hình PlA2 của thụ thể tích hợp tiểu cầu GP IIb/IIIa, và đánh giá ảnh hưởng của nó đến kết quả nhận thức sau phẫu thuật tim. Phân tích đa biến cho thấy kiểu gen PlA2 có liên quan đáng kể với sự suy giảm lớn hơn trên Kiểm tra Tình trạng Tâm thần Tối thiểu (P=0,036). Cơ chế có thể liên quan đến vai trò tăng đông, đã được chứng minh trong các nghiên cứu về huyết khối động mạch vành và nhồi máu cơ tim. Nhìn chung, sự tiến triển của các dự đoán di truyền về suy giảm nhận thức quanh phẫu thuật phản ánh sự phát triển chung của các nghiên cứu di truyền, từ việc nghiên cứu một gen ứng cử viên đơn lẻ đến nhiều gen ứng cử viên và sau đó đến phân tích toàn bộ hệ gen khi công nghệ phát triển.
Mathew và cộng sự cũng đưa ra giả thuyết rằng các đa hình gen ứng cử viên trong các con đường sinh học điều hòa viêm, tương tác/kết dính chất nền tế bào, đông máu-huyết khối, chuyển hóa lipid và phản ứng mạch máu có liên quan đến POCD. Trong một nghiên cứu đoàn hệ tiến cứu trên 513 người bệnh (86% là người Mỹ gốc Âu) trải qua phẫu thuật CABG với tuần hoàn ngoài cơ thể, một bảng gồm 37 SNP đã được phân tích kiểu gen bằng phương pháp phổ khối lượng. Mối liên hệ giữa các SNP này và thiếu hụt nhận thức sau 6 tuần phẫu thuật được đánh giá bằng phân tích hồi quy logistic đa biến có điều chỉnh cho tuổi, trình độ học vấn, nhận thức cơ bản và cấu trúc dân số. Phân tích hoán vị được sử dụng để kiểm soát đa phép thử. Mathew phát hiện ở người Mỹ gốc Âu (n=443), các alen ít gặp của SNP CRP 1059G/C (OR: 0,37; 95% CI: 0,16-0,78; P=0,013) và SNP SELP 1087G/A (OR: 0,51; 95% CI: 0,30-0,85; P=0,011) có liên quan đến giảm thiếu hụt nhận thức. Mức giảm nguy cơ tuyệt đối của POCD là 20,6% ở những người mang alen CRP 1059C và 15,2% ở những người mang alen SELP 1087A, so với tỷ lệ suy giảm trên 40% ở những người bệnh không mang alen này (Hình 42.5). Nồng độ CRP huyết thanh quanh phẫu thuật và mức độ hoạt hóa tiểu cầu cũng thấp hơn đáng kể ở người bệnh có một bản sao của các alen ít gặp, cung cấp cơ sở sinh học cho mối liên hệ alen quan sát được. Những kết quả này gợi ý vai trò của các gen P-selectin và CRP trong việc điều hòa tính nhạy cảm với suy giảm nhận thức sau phẫu thuật tim, mở ra tiềm năng xác định quần thể có nguy cơ có thể được hưởng lợi từ các chiến lược kháng viêm quanh phẫu thuật có mục tiêu. Việc xác định các yếu tố di truyền và cơ chế liên quan đến giảm tỷ lệ tổn thương và biến chứng giúp chúng ta xác định các phương pháp bảo vệ thần kinh và tạo cơ hội sàng lọc di truyền tiền phẫu để xác định người bệnh có nguy cơ tổn thương não và những người có khả năng được hưởng lợi nhất từ các chiến lược can thiệp bảo vệ.

Hình 42.5 Tỷ lệ thiếu hụt nhận thức hậu phẫu theo kiểu gen CRP 1059G/C và SELP 1087G/A. Tỷ lệ thiếu hụt nhận thức là 16,7% ở những người mang các alen ít gặp ở cả hai vị trí, so với 42,9% ở người bệnh đồng hợp tử đối với alen phổ biến (n=386).
GÂY MÊ, PHẪU THUẬT VÀ BỆNH ALZHEIMER
Suy giảm nhận thức xảy ra đến 6 tuần sau phẫu thuật tim đã được so sánh với suy giảm nhận thức sau phẫu thuật không phải tim bởi nhóm ISPOCD và Monk và cộng sự. Tỷ lệ POCD trong phẫu thuật không phải tim ban đầu có vẻ thấp hơn so với tỷ lệ trong phẫu thuật tim, như được ghi nhận bởi các nhóm nghiên cứu khác nhau, và tương đương với nhóm người bệnh dưới 60 tuổi. Tuy nhiên, khi dân số phẫu thuật không phải tim già đi, đã có sự ghi nhận ngày càng tăng về suy giảm nhận thức ở người bệnh phẫu thuật cao tuổi, cho thấy rằng POCD có thể độc lập với loại phẫu thuật.
Mối liên hệ giữa POCD sớm và suy giảm nhận thức dài hạn, được đề cập bởi Newman và đồng nghiệp, đã làm tăng sự quan tâm đến mối liên hệ giữa POCD và bệnh Alzheimer, nguyên nhân phổ biến nhất gây sa sút trí tuệ ở người cao tuổi. Bệnh Alzheimer liên quan đến sự sản xuất và tích tụ protein β-amyloid từ sự phân hủy protein tiền chất amyloid β (Aβ), và sự tích tụ trong tế bào của các đám rối protein tau. Một số bằng chứng cho thấy gây mê và phẫu thuật có thể làm tăng nguy cơ bệnh Alzheimer. Các nghiên cứu tiền lâm sàng đã chứng minh rằng thuốc gây mê và stress phẫu thuật có thể thúc đẩy bệnh lý Aβ và τ in vitro và trong mô hình động vật. Một số nhà nghiên cứu đã phát hiện thay đổi trong các dấu ấn dịch não tủy của bệnh Alzheimer ở người bệnh sau gây mê và phẫu thuật. Các nghiên cứu khác cũng xác định rằng người bệnh đã trải qua gây mê và phẫu thuật có nguy cơ phát triển bệnh Alzheimer cao hơn. Từ các nghiên cứu này, sự chú ý đáng kể đã được tập trung vào việc xác định liệu POCD có phải là yếu tố nguy cơ cho sự phát triển bệnh Alzheimer sau này hay không, và/hoặc liệu gây mê và phẫu thuật có làm tăng nguy cơ phát triển bệnh Alzheimer hay không – những vấn đề hiện vẫn còn nhiều tranh cãi và đang được nghiên cứu chuyên sâu.
Mặc dù có bằng chứng ở cấp độ tế bào, nhưng còn ít dữ liệu lâm sàng ủng hộ cho quan điểm cho rằng tiếp xúc lặp đi lặp lại với gây mê toàn thân có liên quan đến POCD. Hơn nữa, các nghiên cứu so sánh POCD ở người bệnh được gây mê toàn thân và gây mê vùng đã không phát hiện tác dụng bảo vệ của gây mê vùng, cho thấy rằng ảnh hưởng của gây mê có thể đóng vai trò ít quan trọng hơn so với bản thân phẫu thuật. Tuy nhiên, kết quả này bị hạn chế bởi thực tế là nhiều người bệnh trong nhóm “gây mê vùng” vẫn nhận được thuốc an thần tĩnh mạch ở mức độ tương tự như gây mê toàn thân.
Mặc dù dường như hợp lý khi cho rằng các thủ thuật phẫu thuật lớn hơn (với tổn thương mô và đáp ứng viêm nhiều hơn) sẽ liên quan đến nguy cơ POCD cao hơn, nhưng hiện có ít bằng chứng ủng hộ lý luận này. Evered đã so sánh tỷ lệ POCD sau chụp mạch vành với an thần nhẹ, thay khớp háng toàn bộ dưới gây mê toàn thân, và phẫu thuật bắc cầu động mạch vành dưới gây mê toàn thân. Mặc dù tỷ lệ POCD trong các nhóm CABG cao hơn đáng kể so với nhóm thay khớp háng ở ngày thứ 7, đến tháng thứ 3 họ không tìm thấy sự khác biệt đáng kể giữa ba nhóm, tiếp tục gợi ý rằng POCD có thể độc lập với loại phẫu thuật và gây mê. Cần có thêm các thử nghiệm tiến cứu dọc để xác định liệu các kỹ thuật gây mê hoặc phẫu thuật cụ thể có liên quan đến kết quả nhận thức kém hơn hay không.
CƠ CHẾ CẤP ĐỘ HỆ THỐNG CỦA RỐI LOẠN NHẬN THỨC HẬU PHẪU TIM
Các tiến bộ trong chụp cấu trúc và chức năng thần kinh đã được ứng dụng để xác định cơ sở giải phẫu thần kinh của rối loạn nhận thức sau phẫu thuật. Ví dụ, người bệnh phẫu thuật tim có bằng chứng MRI về tăng kích thước não thất (một dấu hiệu có thể của teo vỏ não) có nguy cơ phát triển sảng hậu phẫu cao hơn. MRI chức năng đo hoạt động trong các vùng não cụ thể thông qua mức oxy máu, một tương quan huyết động của hoạt động thần kinh, và có thể được sử dụng để đánh giá thay đổi hoạt động não hậu phẫu. Một nghiên cứu trên 25 người bệnh trải qua phẫu thuật tim đã đánh giá quét MRI chức năng phụ thuộc mức oxy máu trước và 4 tuần sau phẫu thuật ở người bệnh phẫu thuật tim có và không có tuần hoàn ngoài cơ thể, trong khi họ thực hiện một nhiệm vụ trí nhớ làm việc. Người bệnh trải qua phẫu thuật tim có tuần hoàn ngoài cơ thể (không phải những người phẫu thuật tim không tuần hoàn ngoài cơ thể) cho thấy sự giảm hậu phẫu trong hoạt động vỏ não trước trán trong nhiệm vụ chú ý đòi hỏi nhất, điều kiện 3-back. Các nghiên cứu trong tương lai sẽ cần thiết để xác định liệu những thay đổi trong hoạt động vỏ não trước trán này có liên quan đến các triệu chứng chủ quan về nhận thức sau phẫu thuật tim có tuần hoàn ngoài cơ thể hay không.
MRI chức năng cũng có thể đo lường các mô hình hoạt động giữa các vùng não, được gọi là kết nối chức năng, ngay cả trong các vùng không được kết nối về mặt giải phẫu. Nhiều mạng lưới não “kết nối chức năng” đóng vai trò quan trọng trong các quá trình nhận thức cụ thể (Hình 42.6). Browndyke gần đây đã kiểm tra những thay đổi nhận thức và kết nối chức năng ở 12 người bệnh trước và 6 tuần sau phẫu thuật tim và trong cùng khoảng thời gian, ở 12 đối tượng đối chứng không phẫu thuật có bệnh tim. Nghiên cứu ghi nhận sự suy giảm nhận thức rõ rệt hơn sau phẫu thuật tim so với cùng khoảng thời gian ở nhóm đối chứng không phẫu thuật. Hơn nữa, ở người bệnh phẫu thuật tim, mức độ rối loạn nhận thức toàn thể hậu phẫu tương quan với mức độ giảm kết nối chức năng ở vỏ não đai sau và hồi trán trên phải, hai vùng chính của mạng chế độ mặc định của não. Sự thay đổi kết nối tương tự giữa vỏ não đai sau (một trung tâm mạng chế độ mặc định) và vỏ não trước trán cũng đã được quan sát thấy ở người bệnh bị sảng, cho thấy khả năng rối loạn kết nối chức năng mạng chế độ mặc định có thể là cơ chế chung trong cả sảng hậu phẫu và rối loạn nhận thức hậu phẫu.

Hình 42.6 Mạng kết nối chức năng trong não người. Các bản đồ vùng quan tâm mạng não chức năng này được tạo ra từ phân tích thành phần độc lập của dữ liệu chụp cộng hưởng từ chức năng tín hiệu phụ thuộc mức oxy máu tần số thấp từ bộ dữ liệu Dự án Connectome Con người (n=497). (A) Vùng quan tâm mạng chế độ mặc định (màu xanh dương), vùng quan tâm mạng hiển nhiên (màu đỏ). (B) Vùng quan tâm mạng chú ý lưng (màu đen), vùng quan tâm mạng trán-đỉnh (màu xanh lá cây nhạt). (C) Vùng quan tâm mạng ngôn ngữ (màu tím), vùng quan tâm mạng thị giác (màu hồng). (D) Vùng quan tâm mạng tiểu não (màu vàng), vùng quan tâm mạng cảm giác-vận động (màu xanh lá cây).
CAN THIỆP TRONG TƯƠNG LAI ĐỂ NGĂN NGỪA HOẶC ĐIỀU TRỊ RỐI LOẠN NHẬN THỨC HẬU PHẪU VÀ/HOẶC SẢNG
Khi hiểu biết của chúng ta về sự phức tạp của POCD và các tổn thương thần kinh liên quan ngày càng sâu sắc, nhiều phương pháp tiếp cận mới đã được đề xuất để cải thiện chức năng thần kinh nhận thức ở người lớn tuổi, từ đào tạo não dựa trên trò chơi điện tử đến kích thích dây thần kinh phế vị, kích thích não không xâm lấn qua xuyên sọ từ và điện, can thiệp chế độ ăn uống, tập thể dục và đi lại sớm hậu phẫu. Nhiều phương pháp tiếp cận này có thể được điều chỉnh để đáp ứng với các mô hình hoạt động não bệnh lý cụ thể và/hoặc thiếu hụt nhận thức ở từng người bệnh. Những phương pháp mới này chưa được áp dụng trong thực hành lâm sàng để ngăn ngừa hoặc điều trị POCD hoặc sảng ở người bệnh phẫu thuật.
Nhiều chiến lược bảo vệ não và giảm POCD thông qua can thiệp vào các cơ chế đã biết liên quan đến tổn thương thần kinh đã được đề xuất hoặc thử nghiệm. Như đã thảo luận trong các phần trước, các biện pháp giảm viêm, tránh tăng thân nhiệt, giảm thuyên tắc và duy trì tưới máu đầy đủ đều là những thành phần trong chiến lược lâm sàng nhằm giảm đột quỵ, POCD và sảng. Mặc dù đã có bằng chứng về cải thiện tổn thương thần kinh khu trú, việc chứng minh hiệu quả của các chiến lược này trong giảm POCD một cách nhất quán vẫn còn nhiều thách thức.
Kết luận
Sự phức tạp của não và các quá trình của nó khiến não vừa là cơ quan thú vị nhất vừa là cơ quan khó hiểu và dự đoán nhất. Thêm vào đó là sự khác biệt đáng kể về cấu trúc giải phẫu và chức năng giữa não của từng người bệnh phẫu thuật. Tối ưu hóa chức năng thần kinh nhận thức hậu phẫu có lẽ sẽ đòi hỏi một phương pháp tiếp cận cá nhân hóa, tập trung vào người bệnh để quản lý đồng thời nhiều yếu tố quyết định chức năng não – từ cung cấp oxy và glucose, điều chỉnh áp lực tưới máu não, can thiệp dược lý để điều hòa hoạt động mạng lưới thần kinh, đến kiểm soát đáp ứng stress phẫu thuật và quá trình viêm. Điều này cho thấy việc cải thiện chức năng nhận thức sau gây mê và phẫu thuật sẽ là một nhiệm vụ phức tạp và đầy thách thức. Một khó khăn bổ sung cho các nghiên cứu can thiệp trong tương lai là việc theo dõi đồng thời nhiều yếu tố có thể ảnh hưởng đến chức năng nhận thức hậu phẫu và/hoặc sảng, bởi các can thiệp nhắm vào một yếu tố nguy cơ đơn lẻ có thể gây ra tác động cân bằng ngược nếu làm phân tán sự chú ý khỏi các mục tiêu trong mổ khác. Do đó, một nhiệm vụ quan trọng là phát triển các phác đồ được thiết kế để tối ưu hóa đồng thời và thực tiễn nhiều biến số trong và sau mổ để hỗ trợ chức năng nhận thức hậu phẫu cho người bệnh cao tuổi. Các chiến lược nhằm giảm đột quỵ quanh phẫu thuật và sảng sẽ tiếp tục là một phần quan trọng trong kế hoạch đa chiến lược nhằm cải thiện hoặc giảm thiểu POCD.
HẾT CHƯƠNG 42.
Bảng đối chiếu thuật ngữ Y học Anh – Việt – Chương 42.
| STT | Thuật ngữ tiếng Anh | Cách phát âm | Nghĩa Tiếng Việt |
| 1 | Postoperative Cognitive Dysfunction (POCD) | /poʊst’ɒpərətɪv ‘kɒgnɪtɪv dɪs’fʌŋkʃən/ | Rối loạn nhận thức hậu phẫu (tình trạng suy giảm chức năng trí nhớ, chú ý và các khả năng nhận thức khác sau phẫu thuật) |
| 2 | Postoperative Delirium (POD) | /poʊst’ɒpərətɪv dɪ’lɪriəm/ | Sảng hậu phẫu (tình trạng rối loạn ý thức và nhận thức cấp tính sau phẫu thuật) |
| 3 | Postoperative Neurocognitive Dysfunction (POND) | /poʊst’ɒpərətɪv ‘njʊəroʊ’kɒgnɪtɪv dɪs’fʌŋkʃən/ | Rối loạn chức năng thần kinh nhận thức hậu phẫu |
| 4 | Perioperative neurocognitive disorders | /pɛri’ɒpərətɪv ‘njʊəroʊ’kɒgnɪtɪv dɪs’ɔːdəz/ | Rối loạn thần kinh nhận thức quanh phẫu thuật |
| 5 | Neurocognitive recovery | /’njʊəroʊ’kɒgnɪtɪv rɪ’kʌvəri/ | Phục hồi thần kinh nhận thức |
| 6 | Cognitive reserve | /’kɒgnɪtɪv rɪ’zɜːv/ | Dự trữ nhận thức (khả năng bù trừ của não đối với tổn thương thần kinh) |
| 7 | Cerebral atherosclerosis | /sə’riːbrəl ,æθəroʊsklə’roʊsɪs/ | Xơ vữa động mạch não |
| 8 | Activities of daily living | /æk’tɪvɪtiz əv ‘deɪli ‘lɪvɪŋ/ | Hoạt động sinh hoạt hàng ngày |
| 9 | Comorbidities | /,kɒmɔː’bɪdɪtiz/ | Bệnh đồng mắc (các bệnh lý xảy ra đồng thời với bệnh chính) |
| 10 | Emergence delirium | /ɪ’mɜːdʒəns dɪ’lɪriəm/ | Sảng khi tỉnh (sau gây mê) |
| 11 | Emergence agitation | /ɪ’mɜːdʒəns ,ædʒɪ’teɪʃən/ | Kích động khi tỉnh (sau gây mê) |
| 12 | Maladaptive behavior | /,mælə’dæptɪv bɪ’heɪvjər/ | Hành vi thích ứng kém |
| 13 | Postoperative stroke | /poʊst’ɒpərətɪv stroʊk/ | Đột quỵ hậu phẫu |
| 14 | Neuropsychological testing | /,njʊəroʊsaɪkə’lɒdʒɪkəl ‘testɪŋ/ | Kiểm tra thần kinh tâm lý |
| 15 | Learning effect | /’lɜːnɪŋ ɪ’fekt/ | Hiệu ứng học tập (cải thiện điểm số do làm quen với bài kiểm tra) |
| 16 | Factor analysis | /’fæktər ə’næləsɪs/ | Phân tích yếu tố |
| 17 | Neurodegenerative pathology | /,njʊəroʊdɪ’dʒenərətɪv pə’θɒlədʒi/ | Bệnh lý thoái hóa thần kinh |
| 18 | Alzheimer’s disease-related pathology | /’æltshaɪməz dɪ’ziːz rɪ’leɪtɪd pə’θɒlədʒi/ | Bệnh lý liên quan đến bệnh Alzheimer |
| 19 | Executive function | /ɪg’zekjʊtɪv ‘fʌŋkʃən/ | Chức năng điều hành (khả năng lập kế hoạch, ra quyết định và thực hiện nhiệm vụ) |
| 20 | Verbal memory | /’vɜːbəl ‘meməri/ | Trí nhớ từ ngữ |
| 21 | Coronary artery bypass grafting (CABG) | /’kɒrənəri ‘ɑːtəri ‘baɪpæs ‘grɑːftɪŋ/ | Phẫu thuật bắc cầu động mạch vành |
| 22 | Non-cardiac surgery | /nɒn’kɑːdɪæk ‘sɜːdʒəri/ | Phẫu thuật không phải tim |
| 23 | Z-score | /’zed skɔː/ | Điểm Z (điểm chuẩn hóa trong thống kê) |
| 24 | Logistic regression | /lə’dʒɪstɪk rɪ’greʃən/ | Hồi quy logistic (phương pháp thống kê) |
| 25 | Perioperative blood pressure | /pɛri’ɒpərətɪv ‘blʌd ‘preʃə/ | Huyết áp quanh phẫu thuật |
| 26 | Preoperative blood glucose | /pri:’ɒpərətɪv ‘blʌd ‘gluːkoʊs/ | Đường huyết tiền phẫu |
| 27 | Sleep disruption/sleep apnea | /sliːp dɪs’rʌpʃən/sliːp ‘æpnɪə/ | Gián đoạn giấc ngủ/ngưng thở khi ngủ |
| 28 | Alcohol abuse | /’ælkəhɒl ə’bjuːs/ | Lạm dụng rượu |
| 29 | Postoperative pain management | /poʊst’ɒpərətɪv peɪn ‘mænɪdʒmənt/ | Kiểm soát đau hậu phẫu |
| 30 | Hemodilution | /,hiːmoʊdaɪ’luːʃən/ | Pha loãng máu |
| 31 | Frailty | /’freɪlti/ | Tình trạng suy yếu (sức khỏe) |
| 32 | Preoperative cognitive function | /pri:’ɒpərətɪv ‘kɒgnɪtɪv ‘fʌŋkʃən/ | Chức năng nhận thức tiền phẫu |
| 33 | Depression | /dɪ’preʃən/ | Trầm cảm |
| 34 | Neuroinflammation | /,njʊəroʊɪnflə’meɪʃən/ | Viêm thần kinh |
| 35 | Cytokines | /’saɪtoʊkaɪnz/ | Cytokine (protein điều hòa miễn dịch và viêm) |
| 36 | Chemokines | /’kiːmoʊkaɪnz/ | Chemokine (cytokine có tác dụng hóa hướng động) |
| 37 | Interleukin IL-1 | /,ɪntə’luːkɪn aɪ el wʌn/ | Interleukin IL-1 (cytokine tiền viêm) |
| 38 | Interleukin IL-6 | /,ɪntə’luːkɪn aɪ el sɪks/ | Interleukin IL-6 (cytokine tiền viêm) |
| 39 | Tumor necrosis factor (TNF)-α | /’tjuːmə nə’kroʊsɪs ‘fæktər ‘ælfə/ | Yếu tố hoại tử u alpha |
| 40 | Blood-brain barrier | /’blʌd breɪn ‘bæriə/ | Hàng rào máu não |
| 41 | Neurogenesis | /,njʊəroʊ’dʒenəsɪs/ | Tạo thần kinh mới |
| 42 | Hippocampal neurogenesis | /,hɪpə’kæmpəl ,njʊəroʊ’dʒenəsɪs/ | Tạo thần kinh mới ở hồi hải mã |
| 43 | Neurotrophic factors | /njʊəroʊ’trɒfɪk ‘fæktəz/ | Yếu tố dinh dưỡng thần kinh |
| 44 | Brain-derived neurotrophic factor | /breɪn dɪ’raɪvd njʊəroʊ’trɒfɪk ‘fæktə/ | Yếu tố dinh dưỡng thần kinh có nguồn gốc từ não |
| 45 | Complement cascade | /’kɒmplɪment kæs’keɪd/ | Thác bổ thể |
| 46 | Heparin-protamine complexes | /’hepərɪn ‘proʊtəmiːn ‘kɒmpleksɪz/ | Phức hợp heparin-protamine |
| 47 | Sternotomy | /stɜː’nɒtəmi/ | Mở xương ức |
| 48 | Skin incision | /skɪn ɪn’sɪʒən/ | Rạch da |
| 49 | Inhaled anesthetics | /ɪn’heɪld ,ænəs’θetɪks/ | Thuốc mê hít |
| 50 | Microglial cells | /maɪ’kroʊgliəl selz/ | Tế bào vi thần kinh đệm |
| 51 | Opioids | /’oʊpiɔɪdz/ | Opioid (thuốc giảm đau họ morphine) |
| 52 | Cytokine balance | /’saɪtoʊkaɪn ‘bæləns/ | Cân bằng cytokine |
| 53 | Lidocaine | /’laɪdəkeɪn/ | Lidocaine (thuốc gây tê cục bộ) |
| 54 | Magnesium | /mæg’niːziəm/ | Magie |
| 55 | Complement inhibitors | /’kɒmplɪment ɪn’hɪbɪtəz/ | Chất ức chế bổ thể |
| 56 | Acetylcholinesterase | /ə,siːtaɪl,koʊlɪn’esterəs/ | Acetylcholinesterase (enzyme phân giải acetylcholine) |
| 57 | Ketamine | /’ketəmiːn/ | Ketamine (thuốc gây mê tĩnh mạch) |
| 58 | Dexmedetomidine | /,deksmɪ’detəmɪdiːn/ | Dexmedetomidine (thuốc an thần chọn lọc) |
| 59 | Embolic load | /em’bɒlɪk loʊd/ | Gánh nặng thuyên tắc |
| 60 | Aortic atheroma | /eɪ’ɔːtɪk ,æθə’roʊmə/ | Mảng xơ vữa động mạch chủ |
| 61 | Trans-cranial Doppler ultrasound | /træns’kreɪniəl ‘dɒplər ‘ʌltrəsaʊnd/ | Siêu âm Doppler xuyên sọ |
| 62 | Diffusion-weighted MRI | /dɪ’fjuːʒən ‘weɪtɪd em ɑː aɪ/ | Cộng hưởng từ trọng số khuếch tán |
| 63 | “Silent clinical strokes” | /’saɪlənt ‘klɪnɪkəl stroʊks/ | “Đột quỵ kín về mặt lâm sàng” |
| 64 | T2 MRI white matter hyperintensities | /tiː tuː em ɑː aɪ waɪt ‘mætər ,haɪpər-ɪn’tensɪtiz/ | Tăng tín hiệu chất trắng trên MRI T2 |
| 65 | Non-pulsatile flow | /nɒn’pʌlsətaɪl floʊ/ | Dòng máu không đập |
| 66 | Cerebral autoregulation | /sə’riːbrəl ,ɔːtoʊregjʊ’leɪʃən/ | Cơ chế tự điều hòa tuần hoàn não |
| 67 | Mean arterial pressure (MAP) | /miːn ɑː’tɪəriəl ‘preʃə/ | Huyết áp động mạch trung bình |
| 68 | Cerebral oxygen metabolism rate (CMRO2) | /sə’riːbrəl ‘ɒksɪdʒən mə’tæbəlɪzəm reɪt/ | Tốc độ chuyển hóa oxy não |
| 69 | Hypothermia | /,haɪpoʊ’θɜːmiə/ | Hạ thân nhiệt |
| 70 | Normothermia | /,nɔːmoʊ’θɜːmiə/ | Bình thường thân nhiệt |
| 71 | Central rewarming | /’sentrəl riː’wɔːmɪŋ/ | Làm ấm lại trung tâm |
| 72 | External head cooling | /ɪk’stɜːnəl hed ‘kuːlɪŋ/ | Làm mát đầu bên ngoài |
| 73 | Hyperglycemia | /,haɪpəglaɪ’siːmiə/ | Tăng đường huyết |
| 74 | Normoglycemic hyperinsulinemic clamp | /,nɔːmoʊglaɪ’siːmɪk ,haɪpərɪnsjʊlɪ’niːmɪk klæmp/ | Kẹp bình thường đường huyết tăng insulin |
| 75 | Hypoglycemia | /,haɪpoʊglaɪ’siːmiə/ | Hạ đường huyết |
| 76 | Genetic predisposition | /dʒə’netɪk ,priːdɪspə’zɪʃən/ | Xu hướng di truyền |
| 77 | Apolipoprotein E | /,æpoʊ’lɪpoʊproʊtiːn iː/ | Apolipoprotein E |
| 78 | Apo E4 allele | /,æpoʊ iː fɔː ə’liːl/ | Alen Apo E4 |
| 79 | PlA2 polymorphism | /pi el eɪ tuː ‘pɒlimɔːfɪzəm/ | Đa hình PlA2 |
| 80 | GP IIb/IIIa platelet integrin receptor | /dʒiː piː tuː biː θriː eɪ ‘pleɪtlət ‘ɪntəgrɪn rɪ’septə/ | Thụ thể tích hợp tiểu cầu GP IIb/IIIa |
| 81 | Mini-Mental State Examination | /’mɪni ‘mentl steɪt ɪg,zæmɪ’neɪʃən/ | Kiểm tra Tình trạng Tâm thần Tối thiểu |
| 82 | Hypercoagulable state | /,haɪpəkoʊ’ægjʊləbl steɪt/ | Tình trạng tăng đông |
| 83 | Coronary artery thrombosis | /’kɒrənəri ‘ɑːtəri θrɒm’boʊsɪs/ | Huyết khối động mạch vành |
| 84 | Myocardial infarction | /,maɪoʊ’kɑːdiəl ɪn’fɑːkʃən/ | Nhồi máu cơ tim |
| 85 | Candidate gene | /’kændɪdeɪt dʒiːn/ | Gen ứng cử viên |
| 86 | Genome-wide scan | /dʒiː’noʊm waɪd skæn/ | Quét toàn bộ hệ gen |
| 87 | Single nucleotide polymorphisms (SNPs) | /’sɪŋgl ‘njuːkliətaɪd ‘pɒlimɔːfɪzəmz/ | Đa hình đơn nucleotide |
| 88 | Cohort study | /’koʊhɔːt ‘stʌdi/ | Nghiên cứu đoàn hệ |
| 89 | Mass spectrometry | /mæs spek’trɒmətri/ | Phổ khối lượng |
| 90 | CRP 1059G/C SNP | /siː ɑː piː wʌn ziːroʊ faɪv naɪn dʒiː siː es en piː/ | SNP CRP 1059G/C |
| 91 | SELP 1087G/A SNP | /es iː el piː wʌn ziːroʊ eɪt sevən dʒiː eɪ es en piː/ | SNP SELP 1087G/A |
| 92 | Odds ratio (OR) | /ɒdz ‘reɪʃioʊ/ | Tỷ số odds (tỷ số khả năng) |
| 93 | Confidence interval (CI) | /’kɒnfɪdəns ‘ɪntəvəl/ | Khoảng tin cậy |
| 94 | Absolute risk reduction | /’æbsəluːt rɪsk rɪ’dʌkʃən/ | Giảm nguy cơ tuyệt đối |
| 95 | Perioperative serum CRP | /pɛri’ɒpərətɪv ‘sɪərəm siː ɑː piː/ | CRP huyết thanh quanh phẫu thuật |
| 96 | Platelet activation | /’pleɪtlət ,æktɪ’veɪʃən/ | Hoạt hóa tiểu cầu |
| 97 | β-amyloid protein | /biːtə ‘æmɪlɔɪd ‘proʊtiːn/ | Protein β-amyloid |
| 98 | Amyloid β precursor protein (Aβ) | /’æmɪlɔɪd biːtə pri’kɜːsə ‘proʊtiːn/ | Protein tiền chất amyloid β |
| 99 | Tau protein tangles | /taʊ ‘proʊtiːn ‘tæŋglz/ | Đám rối protein tau |
| 100 | Cerebrospinal fluid markers | /,serəbroʊ’spaɪnəl ‘fluːɪd ‘mɑːkəz/ | Dấu ấn dịch não tủy |
| 101 | General anesthesia | /’dʒenərəl ,ænəs’θiːziə/ | Gây mê toàn thân |
| 102 | Regional anesthesia | /’riːdʒənəl ,ænəs’θiːziə/ | Gây mê vùng |
| 103 | Ventricular enlargement | /ven’trɪkjʊlə ɪn’lɑːdʒmənt/ | Tăng kích thước não thất |
| 104 | Cortical atrophy | /’kɔːtɪkəl ‘ætrəfi/ | Teo vỏ não |
| 105 | Functional MRI | /’fʌŋkʃənəl em ɑː aɪ/ | MRI chức năng |
| 106 | Blood oxygen level-dependent | /blʌd ‘ɒksɪdʒən ‘levəl dɪ’pendənt/ | Phụ thuộc vào mức oxy máu |
| 107 | Prefrontal cortical activity | /priː’frʌntəl ‘kɔːtɪkəl æk’tɪvɪti/ | Hoạt động vỏ não trước trán |
| 108 | Working memory task | /’wɜːkɪŋ ‘meməri tɑːsk/ | Nhiệm vụ trí nhớ làm việc |
| 109 | Functional connectivity | /’fʌŋkʃənəl ,kɒnek’tɪvɪti/ | Kết nối chức năng, liên kết chức năng |
| 110 | Default mode network | /dɪ’fɔːlt moʊd ‘netwɜːk/ | Mạng chế độ mặc định |
| 111 | Posterior cingulate cortex | /pɒ’stɪəriə ‘sɪŋgjʊlət ‘kɔːteks/ | Vỏ não đai sau |
| 112 | Superior frontal gyrus | /sjʊ’pɪəriə ‘frʌntəl ‘dʒaɪrəs/ | Hồi trán trên |
| 113 | Video game-based brain training | /’vɪdioʊ geɪm beɪsd breɪn ‘treɪnɪŋ/ | Đào tạo não dựa trên trò chơi điện tử |
| 114 | Vagus nerve stimulation | /’veɪgəs nɜːv ,stɪmjʊ’leɪʃən/ | Kích thích dây thần kinh phế vị |
| 115 | Transcranial magnetic stimulation | /træns’kreɪniəl mæg’netɪk ,stɪmjʊ’leɪʃən/ | Kích thích từ xuyên sọ |
| 116 | Transcranial electrical stimulation | /træns’kreɪniəl ɪ’lektrɪkəl ,stɪmjʊ’leɪʃən/ | Kích thích điện xuyên sọ |
| 117 | Dietary interventions | /’daɪətəri ,ɪntə’venʃənz/ | Can thiệp chế độ ăn uống |
| 118 | Early postoperative ambulation | /’ɜːli poʊst’ɒpərətɪv ,æmbjʊ’leɪʃən/ | Đi lại sớm hậu phẫu |
| 119 | Neurophysiology | /,njʊəroʊfɪzi’ɒlədʒi/ | Sinh lý thần kinh |
| 120 | Cognitive complaints | /’kɒgnɪtɪv kəm’pleɪnts/ | Triệu chứng nhận thức chủ quan |
| 121 | Cardiac surgery with pump | /’kɑːdɪæk ‘sɜːdʒəri wɪð pʌmp/ | Phẫu thuật tim có bơm (tuần hoàn ngoài cơ thể) |
| 122 | Cardiac surgery without pump | /’kɑːdɪæk ‘sɜːdʒəri wɪðaʊt pʌmp/ | Phẫu thuật tim không bơm |
| 123 | 3-back condition | /θriː bæk kən’dɪʃən/ | Điều kiện 3-back (nhiệm vụ ghi nhớ) |
| 124 | Focal neurologic injury | /’foʊkəl ,njʊərə’lɒdʒɪk ‘ɪndʒəri/ | Tổn thương thần kinh khu trú |
| 125 | Multi-modal interventions | /mʌlti ‘moʊdəl ,ɪntə’venʃənz/ | Can thiệp đa phương thức |
| 126 | Physiologic variables | /,fɪziə’lɒdʒɪk ‘veəriəblz/ | Biến số sinh lý |
| 127 | Neural network activity | /’njʊərəl ‘netwɜːk æk’tɪvɪti/ | Hoạt động mạng lưới thần kinh |
| 128 | Cerebral perfusion pressure | /sə’riːbrəl pə’fjuːʒən ‘preʃə/ | Áp lực tưới máu não |
| 129 | Stress response | /stres rɪ’spɒns/ | Đáp ứng stress |
| 130 | Inflammatory response | /ɪn’flæmətəri rɪ’spɒns/ | Đáp ứng viêm |
| 131 | Preoperative genetic screening | /pri:’ɒpərətɪv dʒə’netɪk ‘skriːnɪŋ/ | Sàng lọc di truyền tiền phẫu |
| 132 | Orthopedic surgery | /,ɔːθə’piːdɪk ‘sɜːdʒəri/ | Phẫu thuật chỉnh hình |
| 133 | Mild sedation | /maɪld sɪ’deɪʃən/ | An thần nhẹ |
| 134 | Coronary angiography | /’kɒrənəri ,ændʒi’ɒgrəfi/ | Chụp mạch vành |
| 135 | Total hip replacement | /’toʊtəl hɪp rɪ’pleɪsmənt/ | Thay khớp háng toàn bộ |
| 136 | Cardiopulmonary bypass (CPB) | /,kɑːdioʊ’pʌlmənəri ‘baɪpæs/ | Tuần hoàn ngoài cơ thể |
| 137 | Electroencephalogram (EEG) | /ɪ’lektroʊən’sefələgræm/ | Điện não đồ |
| 138 | Subjective cognitive decline | /səb’dʒektɪv ‘kɒgnɪtɪv dɪ’klaɪn/ | Suy giảm nhận thức chủ quan |
| 139 | High mobility group box-1 | /haɪ moʊ’bɪlɪti gruːp bɒks wʌn/ | Protein HMGB1 |
| 140 | S100 calcium-binding proteins | /es wʌn ‘hʌndrəd ‘kælsiəm ‘baɪndɪŋ ‘proʊtiːnz/ | Protein gắn canxi S100 |
| 141 | Blood-brain barrier disruption | /’blʌd breɪn ‘bæriə dɪs’rʌpʃən/ | Phá vỡ hàng rào máu não |
| 142 | Microglia activation | /maɪ’kroʊgliə ,æktɪ’veɪʃən/ | Hoạt hóa tế bào hỗ trợ thần kinh |
| 143 | Spinal pain processing | /’spaɪnəl peɪn ‘proʊsesɪŋ/ | Xử lý tín hiệu đau tủy sống |
| 144 | Aortic arch | /eɪ’ɔːtɪk ɑːtʃ/ | Cung động mạch chủ |
| 145 | Microemboli | /maɪkroʊ’embəlaɪ/ | Vi thuyên tắc |
| 146 | Cortical representation | /’kɔːtɪkəl ,reprɪzen’teɪʃən/ | Biểu hiện vỏ não |
| 147 | Peg orientation test | /peg ,ɔːrien’teɪʃən test/ | Nghiệm pháp định hướng không gian bằng chốt |
| 148 | Visual-motor processing speed | /’vɪʒuəl ‘moʊtə ‘proʊsesɪŋ spiːd/ | Tốc độ xử lý thị giác-vận động |
| 149 | Rewarming rate | /riː’wɔːmɪŋ reɪt/ | Tốc độ làm ấm lại |
| 150 | Personalized approach | /’pɜːsənəlaɪzd ə’proʊtʃ/ | Phương pháp tiếp cận cá nhân hóa |
TÀI LIỆU THAM KHẢO
- Newman M.F., Grocott H.P., Mathew J.P., et. al.: Report of the substudy assessing the impact of neurocognitive function on quality of life 5 years after cardiac surgery. Stroke 2001; 32: pp. 2874-2881.
- Evered L., Silbert B., Knopman D.S.: Nomenclature Consensus Working Group, et al: Recommendations for the nomenclature of cognitive change associated with anaesthesia and surgery. Anesth Analg 2018; 127: pp. 1189-1195.
- Mathew J.P., Welsh-Bohmer K.A., Newman M.F.: Nomenclature for perioperative cognitive disorders: Comment. Anesthesiology 2019; 131: pp. 443-444.
- McDonagh D.L., Berger M., Mathew J.P., Graffagnino C., Milano C.A., Newman M.F.: Neurological complications of cardiac surgery. Lancet Neurology 2014; 13: pp. 490-502.
- Nadelson M.R., Sanders R.D., Avidan M.S.: Perioperative cognitive trajectory in adults. Br J Anaesth 2014; 112: pp. 440-451.
- Berger M., Terrando N., Smith S.K., Browndyke J.N., Newman M.F., Mathew J.P.: Neurocognitive function after cardiac surgery: from phenotypes to mechanisms. Anesthesiology 2018; 129: pp. 829-851.
- Silverstein J.H., Timberger M., Reich D.L., et. al.: Central nervous system dysfunction after noncardiac surgery and anesthesia in the elderly. Anesthesiology 2007; 106: pp. 622-628.
- Silverstein J.H., Timberger M., Reich D.L., Uysal S.: Central nervous system dysfunction after noncardiac surgery and anesthesia in the elderly. Anesthesiology 2007; 106: pp. 622-628.
- Hudetz J.A., Patterson K.M., Byrne A.J., Pagel P.S., Warltier D.C.: Postoperative delirium is associated with postoperative cognitive dysfunction at one week after cardiac surgery with cardiopulmonary bypass. Psychol Rep 2009; 105: pp. 921-932. Pt 1
- Rudolph J.L., Marcantonio E.R., Culley D.J., et. al.: Delirium is associated with early postoperative cognitive dysfunction. Anaesthesia 2008; 63: pp. 941-947.
- Saczynski J.S., Marantonio E.R., Quach L., et. al.: Cognitive trajectories after postoperative delirium. N Engl J Med 2012; 367: pp. 30-39.
- Association AP : Diagnostic and Statistical Manual of Mental Disorders.ed 52013.American Psychiatric AssociationWashington, DC
- Sauër A.M., Slooter A.J., Veldhuijzen D.S., van Eijk M.M., Devlin J.W., van Dijk D.: Intraoperative dexamethasone and delirium after cardiac surgery: A randomized clinical trial. Anesth Analg 2014; 19: pp. 1046-1052.
- Rudolph J.L., Jones R.N., Levkoff S.E., et. al.: Derivation and validation of a perioperative prediction rule for delirium after cardiac surgery. Circulation 2009; 119: pp. 229-236.
- Berger M., Browndyke J., Mathew J.P.: Intraoperative glycemic control to prevent delirium after cardiac surgery: Steering a course between Scylla and Charybdis. Anesthesiology 2015; 122: pp. 1186-1188.
- Brown C.H.I.V., Neufeld K.J., Needham D.M.: Delirium, steroids, and cardiac surgery. Anesth Analg 2014; 119: pp. 1011-10113.
- McCoy T.H., Snapper L., Stern T.A., Perlis R.H.: Underreporting of delirium in statewide claims data: Implications for clinical care and predictive modeling. Psychosomatics 2016; 57: pp. 480-488.
- Mathew J.P., White W.D., Schinderle D.B., et. al.: Neurologic Outcome Research Group (NORG) of the Duke Heart Center: Intraoperative magnesium administration does not improve neurocognitive function after cardiac surgery. Stroke 2013; 44: pp. 3407-3413.
- Newman M.F., Kirchner J.L., Phillips-Bute B., et. al.: Neurologic Outcome Research Group and the Cardiothoracic Anesthesiology Research Endeavors Investigators: Longitudinal assessment of neurocognitive function after coronary-artery bypass surgery. N Engl J Med 2001; 344: pp. 395-402.
- Newman M.F., Kirchner J.L., Phillips-Bute B., et. al.: Longitudinal assessment of neurocognitive function after coronary-artery bypass surgery. N Engl J Med 2001; 344: pp. 1885-1896.
- Evered L., Scott D.A., Silbert B., Maruff P.: Postoperative cognitive dysfunction is independent of the type of surgery and anesthetic. Anesth Analg 2011; 112: pp. 1179-1185.
- Mathew J.P., Mackensen G.B., Phillips-Bute B., et. al.: Neurologic Outcome Research Group (NORG) of the Duke Heart Center: Randomized, double-blinded, placebo, controlled study of neuroprotection with lidocaine in cardiac surgery. Stroke 2009; 40: pp. 880-887.
- Murkin J.M., Newman S.P., Stump D.A., Blumenthal J.A.: Statement of consensus on assessment of neurobehavioral outcomes after cardiac surgery. Ann Thorac Surg 1995; 59: pp. 1289-1295.
- Cabeza R.: Cognitive neuroscience of aging: Contributions of functional neuroimaging. Scand J Psychol 2001; 42: pp. 277-286.
- Wang W.C., Dew I.T., Cabeza R.: Age-related differences in medial temporal lobe involvement during conceptual fluency. Brain Res 2015; 1612: pp. 48-58.
- Jack C.R., Knopman D.S., Jagust W.J., et. al.: Tracking pathophysiological processes in Alzheimer’s disease: An updated hypothetical model of dynamic biomarkers. Lancet Neurol 2013; 12: pp. 207-216.
- Bateman R.J., Xiong C., Benzinger T.L., et. al.: Dominantly Inherited Alzheimer Network: Clinical and biomarker changes in dominantly inherited Alzheimer’s disease. N Engl J Med 2012; 367: pp. 795-804.
- Xie Z., Swain C.A., Ward S.A., et. al.: Perioperative cerebrospinal fluid β-Amyloid/Tau ratio and postoperative delirium. Ann Clin Transl Neurol 2014; 1: pp. 319-328.
- Xie Z., McAuliffe S., Swain C.A., et. al.: Cerebrospinal fluid Aβ to tau ratio and postoperative cognitive change. Ann Surg 2013; 258: pp. 364-369.
- Evered L., Silbert B., Da Scott, Ames D., Maruff P., Blennow K.: Cerebrospinal fluid biomarker for Alzheimer disease predicts postoperative cognitive dysfunction. Anesthesiology 2016; 124: pp. 353-361.
- Tang L., Kazan R., Taddei R., Zaouter C., Cyr S., Hemmerling T.M.: Reduced cerebral oxygen saturation during thoracic surgery predicts early postoperative cognitive dysfunction. BR J Anaesth 2012; 108: pp. 623-629.
- Evered L.A., Silbert B.S., Scott D.A.: Postoperative cognitive dysfunction and aortic atheroma. Ann Thorac Surg 2010; 89: pp. 1091-1097.
- Browndyke J.N., Berger M., Harshbarger T.B., et. al.: Resting-state functional connectivity and cognition after major cardiac surgery in older adults without perioperative cognitive impact impairment: Preliminary findings. J Am Geriatr Soc 2017; 65: pp. e6-e12.
- Evered L., Silbert B., Knopman D.S., et. al.: Recommendations for the nomenclature of cognitive change associated with anesthesia and surgery. Anesthesiology 2017; In Press
- Phillips-Bute B., Mathew J.P., Blumenthal J.A., et. al.: Association of neurocognitive function and quality of life 1 year after coronary artery bypass graft (CABG) surgery. Psychosom Med 2006; 68: pp. 369-375.
- Newman M.F., Grocott H.P., Mathew J.P., et. al.: Neurologic Outcome Research Group and the Cardiothoracic Anesthesia Research Endeavors (CARE) Investigators of the Duke Heart Center: Report of the substudy assessing the impact of neurocognitive function on quality of life 5 years after cardiac surgery. Stroke 2001; 32: pp. 2874-2881.
- Berger M., Nadler J.W., Browndyke J., et. al.: Postoperative cognitive dysfunction: Minding the gaps in our knowledge of a common postoperative complication in the elderly. Anesthesiol Clin 2015; 33: pp. 517-550.
- Terrando N., Eriksson L.I., Eckenhoff R.G.: Postoperative neurotoxicity in the elderly: Summary of the 4 th International Workshop. Anesth Analg 2015; 13: pp. 225-232.
- Moller J.T., Cluitmans P., Rasmussen L.S., et. al.: Long-term postoperative cognitive dysfunction in the elderly ISPOCD1 study. ISPOCD investigators. International Study of Post-Operative Cognitive Dysfunction. Lancet 1998; 351: pp. 857-861.
- Monk T.G., Weldon B.C., Garvan C.W., et. al.: Predictors of cognitive dysfunction after major noncardiac surgery. Anesthesiology 2008; 108: pp. 18-30.
- Vasunilashorn S.M., Ngo L., Inouye S.K., et. al.: Cytokines and postoperative delirium in older patients undergoing major elective surgery. J Gerontol A Biol Sci med Sci 2015; 70: pp. 1289-1295.
- Liu P., Li Y.W., Wang X.S., et. al.: High serum interleukin-6 level is associated with increased risk of delirium in elderly patients after noncardiac surgery: A prospective cohort study. Chin Med J (Engl) 2013; 126: pp. 3621-3627.
- Hovens I.B., van Leeuwen B.L., Nyakas C., Heineman E., van der Zee E.A., Schoemaker R.G.: Prior infection exacerbates postoperative cognitive dysfunction in aged rats. Am J Physiol Regul Integr Comp Physiol 2015; 309: pp. R148-R159.
- Terrando N., Eriksson L.I., Ryu J.K., Yang T., Manaco C., Maze M.: Resolving postoperative neuroinflammation and cognitive decline. Ann Neurol 2011; 70: pp. 986-995.
- Terrando N., Monaco C., Ma D., Foxwell B.M., Feldmann M., Maze M.: Tumor necrosis factor-alpha triggers a cytokine cascade yielding postoperative cognitive decline. Proc Natl Aca Sci USA 2010; 107: pp. 20518-20522.
- Degos V., Vacas S., Han Z., et. al.: Depletion of bone marrow-derived macrophages perturbs the innate immune response to surgery and reduces postoperative memory dysfunction. Anesthesiology 2013; 118: pp. 527-536.
- He H.J., Wang Y., le Y., et. al.: Surgery upregulates high mobility group box-1 and disrupts the blood-brain barrier causing cognitive dysfunction in aged rats. CNS Neurosci Ther 2012; 18: pp. 994-1002.
- Lu S.M., Yu C.J., Liu Y.H., et. al.: S100A8 contributes to postoperative cognitive dysfunction in mice undergoing tibial fracture surgery by activating the TLR4/MyD88 pathway. Brain Behav Immun 2015; 44: pp. 221-234.
- Haque A., Kunimoto F., Narahara H., et. al.: High mobility group box 1 levels in on and off-pump cardiac surgery patients. Int Heart J 2011; 52: pp. 170-174.
- Zhang Q., Raoof M., Chen Y., et. al.: Circulating mitochondrial DAMPs cause inflammatory responses to injury. Nature 2010; 464: pp. 104-107.
- Lord J.M., Midwinter M.J., Chen Y.F., et. al.: The systemic immune response to trauma: An overview of pathophysiology and treatment. Lancet 2014; 384: pp. 1455-1465.
- Terrando N., Yang T., Wang X., et. al.: Systemic HMGB1 neutralization prevents postoperative neurocognitive dysfunction in aged rats. Front Immunol 2016; 7: pp. 441.
- Bartels K., Ma Q., Venkatraman T.N., et. al.: Effects of deep hypothermic circulatory arrest on the blood brain barrier in a cardiopulmonary bypass model—a pilot study. Heart Lung Circ 2014; 23: pp. 981-984.
- Reis H.J., Teixeira A.L., Kálmán J., et. al.: Different inflammatory biomarker patterns in the cerebro-spinal fluid following heart surgery and major noncardiac operations. Curr Drug Metab 2007; 8: pp. 639-642.
- Reinsfelt B., Ricksten S.E., Zetterberg H., Blennow K., Fredén-Lindqvist J., Westerlind A.: Cerebrospinal fluid markers of brain injury, inflammation, and blood-brain barrier dysfunction in cardiac surgery. Ann Thorac Surg 2012; 94: pp. 549-555.
- Hainsworth A.H., Minett T., Andoh J., et. al.: Neuropathology of white matter lesions, blood-brain barrier dysfunction, and dementia. Stroke 2017; 48: pp. 2799-2804.
- Merino J.G., Latour L.L., Tso A., et. al.: Blood-brain barrier disruption after cardiac surgery. AJNR Am J Neuroradiol 2013; 34: pp. 518-523.
- Abrahamov D., Levran O., Napartsek S., et. al.: Blood-brain barrier disruption after cardiopulmonary bypass: Diagnosis and correlation to cognition. Ann Thorac Surg 2017; 104: pp. 161-169.
- Capuron L., Miller A.H., et. al.: Immune system to brain signaling: Neuropsychopharmacological implications. Pharmacol Ther 2011; 130: pp. 226-238.
- Najjar S., Pearlman D.M., Alper K., Najjar A., Devinsky O.: Neuroinflammation and psychiatric illness. J Neuroinflammation 2013; 10: pp. 43.
- Heneka M.T., Carson M.J., El Khoury J., et. al.: Neuroinflammation in Alzheimer’s disease. Lancet Neurol 2015; 14: pp. 388-405.
- Mathew J.P., Podgoreanu M.V., Grocott H.P., et. al.: Pegasus Investigative Team: Genetic variance P-selectin and C-reactive protein influence susceptibility to cognitive decline after cardiac surgery. J Am Coll Cardiol 2001; 49: pp. 1934-1942.
- Mathew J.P., Rinder C.S., Howe J.G., et. al.: Platelet P1A2 polymorphism enhances risk of neurocognitive decline after cardiopulmonary bypass. Multicenter Study of Perioperative Ischemia (McSPI) Research Group. Ann Thorac Surg 2001; 71: pp. 663-666.
- Yocum G.T., Gaudet J.G., Lee S.S., et. al.: Inducible nitric oxide synthase promoter polymorphism affords protection against cognitive dysfunction after carotid endarterectomy. Stroke 2009; 40: pp. 1597-1603.
- Steinberg B.M., Grossi E.A., Schwartz D.S., et. al.: Heparin bonding of bypass circuits reduces cytokine release during cardiopulmonary bypass. Ann Thorac Surg 1995; 60: pp. 525-529.
- Hovens I.B., Schoemaker R.G., van der Zee E.A., Absalom A.R., Heineman E., van Leeuwan B.L.: Postoperative cognitive dysfunction: involvement of neuroinflammation and neuronal functioning. Brain Behav Immun 2014; 38: pp. 202-210.
- Bruins P., te Velthuis H., Erenberg-Belmer A.J., et. al.: Heparin-protamine complexes and C-reactive protein induce activation of the classical complement pathway: Studies in patients undergoing cardiac surgery in vitro . Thromb Haemost 2000; 84: pp. 237-243.
- Hayashi Y., Sawa Y., Nishimura M., Satoh H., Ohtake S., Matsuda H.: Avoidance of full-sternotomy: Effect on inflammatory cytokine production during cardiopulmonary bypass in rats. J Card 2003; 18: pp. 390-395.
- Gu Y.J., Mariani M.A., Boonstra P.W., Grandjean J.G., van Oeveren W.: Complement activation in coronary artery bypass grafting patients without cardiopulmonary bypass: The role of tissue injury by surgical incision. Chest 1999; 116: pp. 892-898.
- Friscia M.E., Zhu K., Kloff J.W., et. al.: Cytokine response is lower after lung volume reduction through bilateral thoracoscopy versus sternotomy. Ann Thorac Surg 2007; 83: pp. 252-256.
- Diegeler A., Doll N., Rauch T., et. al.: Humoral immune response during coronary artery bypass grafting: A comparison of limited approach, “off-pump” technique, and conventional cardiopulmonary bypass. Circulation 2000; 102: pp. 95-100.
- Gulielmos V., Menschikowski M., Dill H., et. al.: Interleukin-1, interleukin-6 and myocardial enzyme response after coronary artery bypass grafting – a prospective randomized comparison of the conventional and three minimally invasive surgical techniques. Eur J Cardiothorac Surg 2000; 18: pp. 594-601.
- Ye X., lian Q., Eckenhoff M.F., Eckenhoff R.G., Pan J.Z.: Differential general anesthetic effects on microglial cytokine expression. PLoS One 2013; 8:
- McBride W.T., Armstrong M.A., McMurray T.J.: An investigation of the effects of heparin, protamine, and fentanyl on the balance of pro- and anti-inflammatory cytokines in in-vitro monocyte cultures. Anaesthesia 1996; 51: pp. 634-640.
- McBride W.T., McBride S.J.: The balance of pro- and anti-inflammatory cytokines in cardiac surgery. Curr Opin Anaesthesiol 1998; 11: pp. 15-22.
- Vacas S., Degos V., Tracey K.J., Maze M.: High-mobility group box 1 protein initiates postoperative cognitive decline by engaging bone-marrow derived macrophages. Anaesthesiology 2014; 120: pp. 1160-1167.
- Zhang M.D., Barde S., Yang T., et. al.: Orthopedic surgery modulates neuropeptides and BDNF expression at the spinal and hippocampal levels. Proc Natl Acad Sci USA 2016; 113: pp. 6686-6695.
- Feng X., Valdearcos M., Uchida Y., Lutrin D., Maze M., Koliwad S.K.: Microglia mediate postoperative hippocampal inflammation and cognitive decline in mice. JCI Insight 2017; 2:
- Mathew J.P., Macksen G.B., Phillips-Bute B., et. al., Neurologic Outcome Research Group (NORG) : A randomized, double-blind, placebo controlled study of neuroprotection with lidocaine in cardiac surgery. Stroke 2009; 40: pp. 880-887.
- Mathew J.P., Shernan S.K., White W.D., et. al.: Preliminary report of the effects of complement suppression with pexelizumab on neurocognitive decline after coronary artery bypass graft surgery. Stroke 2004; 35: pp. 2335-2339.
- Doraiswamy P.M., Babyak M.A., Hennig T., et. al.: Donepezil for cognitive decline following coronary artery bypass surgery: A pilot randomized controlled trial. Psychopharmacol Bull 2007; 40: pp. 54-62.
- Gamberini M., Bolliger D., Lurati Buse G.A., et. al.: Rivastigmine for the prevention of postoperative delirium in the steroids in cardiac surgery-a randomized controlled trial. Crit Care Med 2009; 37: pp. 1762-1768.
- Ottens T.H., Dieleman J.M., Sauër A.M., et. al.: DExamethasone for Cardiac Surgery (DECS) Study Group: Effects of dexamethasone on cognitive decline after cardiac surgery: A randomized clinical trial. Anesthesiology 2004; 121: pp. 492-500.
- Royse C.F., Saager L., Whitlock R., et. al.: Impact of methylprednisolone on postoperative quality of recovery and delirium in the steroids in cardiac surgery trial: A randomized, double-blind, placebo-controlled substudy. Anesthesiology 2017; 126: pp. 223-233.
- Whitlock R.P., Devereaux P.J., Teoh K.H., et. al.: Methylprednisolone in patients undergoing cardiopulmonary bypass (SIRS): A randomized, double-blind, placebo-controlled trial. Lancet 2015; 386: pp. 1243-1253.
- Kenna H.A., Poon A.W., de los Angeles C.P., Koran L.M.: Psychiatric complications of treatment with corticosteroids: Review with case report. Psychiatry Clin Neurosci 2011; 65: pp. 549-560.
- Hudetz J.A., Iqbal Z., Gandhi S.D., et. al.: Ketamine attenuates delirium after cardiac surgery with cardiopulmonary bypass. J Cardiothorac Vasc Anesth 2009; 23: pp. 651-657.
- Hudetz J.A., Iqbal Z., Gandhi S.D., et. al.: Ketamine attenuates post-operative cognitive dysfunction after cardiac surgery. Acta Anaesthesiol Scand 2009; 53: pp. 864-872.
- Avidan M.S., Maybrier H.R., Abdallah A.B., et. al.: PODCAST Research Group: Intraoperative ketamine for prevention of postoperative delirium or pain after major surgery in older adults: An international, multicentre, double-blind, randomized clinical trial. Lancet 2017; 390: pp. 267-275.
- Li X., Yang J., Nie X.L., et. al.: Impact of dexmedetomidine on the incidence of delirium in elderly patients after cardiac surgery: A randomized controlled trial. PLoS One 2017; 12:
- Deiner S., Luo X., Lin H.M., et. al.: and the Dexlirium Writing Group. Intraoperative infusion of dexmedetomidine for prevention of postoperative delirium and cognitive dysfunction in elderly patients undergoing major elective noncardiac surgery: A randomized clinical trial. JAMA Surg 2017; 152:
- Su X., Meng Z.T., Wu X.H., et. al.: Dexmedetomidine for prevention of delirium in elderly patients after non-cardiac surgery: A randomized, double-blind, placebo-controlled trial. Lancet 2016; 388: pp. 1893-1902.
- Palmbergen W.A., van Sonderen A., Keyhan-Falsafi A.M., Keunen R.W., Wolterbeek R.: Improved perioperative neurological monitoring of coronary artery bypass graft patients reduces the incidence of postoperative delirium: The Haga Brain Care Strategy. Interact Cardiovasc Thorac Surg 2012; 15: pp. 671-677.
- Glas K.E., Swaminathan M., Reeves S.T., et. al.: Council for Intraoperative Echocardiography of the American Society of Echocardiography; society of Cardiovascular Anesthesiologists; Society of Thoracic Surgeons: Guidelines for the performance of a comprehensive intraoperative epiaortic ultrasonographic examination: Recommendations of the American Society of Echocardiography and the Society of Anesthesiologists; endorsed by the Society of Thoracic Surgeons. Anesth Analg 2008; 106: pp. 1376-1384.
- Doblar D.D.: Intraoperative transcranial ultrasonic monitoring for cardiac and vascular surgery. Semin Cardiothorac Vasc Anesth 2004; 8: pp. 127-145.
- Geurrieri Wolf L., Choudhary B.P., Abu-Omar Y., Taggart D.P.: Solid and gaseous cerebral microembolization after biologic and mechanical aortic valve replacement: Investigation with multirange and multifrequency transcranial Doppler ultrasound. J Thorac Cardiovasc Surg 2008; 135: pp. 512-520.
- Chadhuri K., Marasco S.F.: The effect of carbon dioxide insufflation on cognitive function during cardiac surgery. J Card Surg 2011; 26: pp. 189-196.
- Chadhuri K., Storey E., Lee G.A., et. al.: Carbon dioxide insufflation in open-chamber cardiac surgery: A double-blind, randomized clinical trial or neurocognitive effects. J Thorac Cardiovasc Surg 2012; 144: pp. 646-653.
- Mirow N., Zittermann A., Körperich H., et. al.: Diffusion-weighted magnetic resonance imaging for the detection of ischemic brain lesions in coronary artery bypass graft surgery: Relation to extracorporeal circulation and heparinization. J Cardiovasc Surg 2011; 52: pp. 117-126.
- Hlatky M.A., Boothroyd D.B., Bravata D.M., et. al.: Coronary artery bypass surgery compared with percutaneous coronary interventions for multivessel disease: a collaborative analysis of individual patient data from ten randomized trials. Lancet 2009; 373: pp. 1190-1197.
- Cook D.J., Hutson J., Trenerry M.R., Brown R.D., Zehr K.J., Sundt T.M.: Postcardiac surgical cognitive impairment in the aged using diffusion-weighted magnetic resonance imaging. Ann Thorac Surg 2007; 83: pp. 1389-1395.
- Knipp S.C., Matatko N., Wilhelm H., Schlamann M., et. al.: Evaluation of brain injury after coronary artery bypass grafting. A prospective study using neuropsychological assessment and diffusion-weighted magnetic resonance imaging. Eur J Cardiothorac Surg 2004; 25: pp. 791-800.
- Fairbain T.A., Mather A.N., Bijsterveld P., et. al.: Diffusion-weighted MRI determined cerebral embolic infarction following transcatheter aortic valve implantation: Assessment of predictive risk factors and the relationship to subsequent health status. Heart 2012; 98: pp. 18-23.
- Bernick C., Kuller L., Dullberg C., et. al.: Cardiovascular Health Study Collaborative Research Group: Silent MRI infarcts and the risk of future stroke: The cardiovascular health study. Neurology 2001; 57: pp. 1222-1229.
- Vermeer S.E., Hollander M., van Dijk E.J., Hofman A., Koudstaal P.J., Breteler M.M.: Silent brain infarcts and white matter lesions increase stroke risk in the general population: The Rotterdam Scan Study. Stroke 2003; 34: pp. 1126-1129.
- Vermeer S.E., Prins N.D., den Heijer T., Hofman A., Koudstaal P.J., Breteler M.M.: Silent brain infarcts and the risk of dementia and cognitive decline. N Engl J Med 2003; 348: pp. 1215-1222.
- Hassell M.E., Nijveldt R., Roos Y.B., et. al.: Silent cerebral infarcts associated with cardiac disease and procedures. Nat Rev Cardiol 2013; 10: pp. 696-706.
- Brady K., Joshi B., Zweifel C., et. al.: Real-time continuous monitoring of cerebral blood flow autoregulation using near-infrared spectroscopy in patients undergoing cardiopulmonary bypass. Stroke 2010; 41: pp. 1951-1956.
- Ahlgren E., Lundqvist A., Nordlund A., Aren C., Rutberg H.: Neurocognitive impairment and driving performance after coronary artery bypass surgery. Eur J Cardiothorac Surg 2003; 23: pp. 334-340.
- Newman M.F., Croughwell N.D., White W.D., et. al.: Effect of perfusion pressure on cerebral blood flow during normothermic cardiopulmonary bypass. Circulation 1996; 94: pp. 353-357.
- Joshi B., Brady K., Lee J., et. al.: Impaired autoregulation of cerebral blood flow during rewarming from hypothermic cardiopulmonary bypass and its potential association with stroke. Anesth Analg 2010; 110: pp. 321-328.
- Severdija E.E., Gommer E.D., Weerwind P.W., Reulen J.P., Mess Wh., Maessen J.G.: Assessment of dynamic cerebral autoregulation and cerebral carbon dioxide reactivity during normothermic cardiopulmonary bypass. Med Biol Eng Comput 2015; 53: pp. 195-203.
- Severdija E.E., Vranken N.P., Simons A.P., et. al.: Hemodilution combined with hypercapnia impairs cerebral autoregulation during normothermic cardiopulmonary bypass. J Cardiothorac Vasc Anesth 2015; 29: pp. 1194-1199.
- Siepe M., Pfeiffer T., Gieringer A., et. al.: Increased systemic perfusion pressure during cardiopulmonary bypass is associated with less early postoperative cognitive dysfunction and delirium. Eur J Cardiothorac Surg 2011; 40: pp. 200-207.
- Gold J.P., Charlson M.E., Williams-Russo P., et. al.: Improvement of outcomes after coronary artery bypass. A randomized trial comparing intraoperative high versus low mean arterial pressure. J Thorac Cardiovasc Surg 1995; 110: pp. 1302-1311.
- Hartman G.S., Yao F.S., Bruefach M., et. al.: Severity of aortic atheromatous disease diagnosed by transesophageal echocardiography predicts stroke and other outcomes associated with coronary artery surgery: a prospective study. Anesth Analg 1996; 83: pp. 701-708.
- Hori D., Ono M., Rappold T.E., et. al.: Hypotension after cardiac operations based on autoregulation monitoring leads to brain cellular injury. Ann Thorac Surg 2015; 100: pp. 487-493.
- Hori D., Max L., Laflam A., et. al.: Blood pressure deviations from optimal mean arterial pressure during cardiac surgery measured with a novel monitor of cerebral blood flow and risk for perioperative delirium: A pilot study. J Cardiothorac Vasc Anesth 2016; 30: pp. 606-612.
- Hori D., Brown C., Ono M., et. al.: Arterial pressure above the upper cerebral autoregulation limit during cardiopulmonary bypass is associated with postoperative delirium. Br J Anaesth 2014; 113: pp. 1009-1017.
- Choi K.E., Hall C.L., Sun J.M., et. al.: A novel stroke therapy of pharmacologically induced hypothermia after focal cerebral ischemia in mice. FASEB J 2012; 26: pp. 2690-2696.
- Nozari A., Safar P., Stezoski S.W., et. al.: Critical time window for intra-arrest cooling with cold saline flush in a dog model of cardiopulmonary resuscitation. Circulation 2006; 113: pp. 2690-2696.
- Grossestreuer A.V., Gaieski D.F., Donnino M.W., Wiebe D.J., Abella B.S.: Magnitude of temperature elevation is associated with neurologic and survival outcomes in resuscitated cardiac arrest patients with postwarming pyrexia. J Crit Care 2017; 32: pp. 124-129.
- Meier K., Lee K.: Neurogenic fever. J Intensive Care Med 2017; 32: pp. 124-129.
- Kasdorf E., Perlman J.M.: Hyperthermia, inflammation, and perinatal brain injury. Pediatr Neurol 2013; 49: pp. 8-14.
- Martin T.D., Craver J.M., Gott J.P., et. al.: Prospective, randomized trial of retrograde warm blood cardioplegia: myocardial benefit and neurologic threat. Ann Thorac Surg 1994; 57: pp. 298-302.
- Grigore A.M., Mathew J., Grocott H.P., et. al.: Prospective randomized trial of normothermic versus hypothermic cardiopulmonary bypass on cognitive function after coronary artery bypass graft surgery. Neurological Outcome Research Group; CARE Investigators of the Duke Heart Center Anesthesiology 2001; 95: pp. 1110-1119.
- Grocott H.P., Mackensen G.B., Am Grigore, et. al.: Neurologic Outcome Research Group (NORG); Cardiothoracic Anesthesiology Research Endeavors (CARE) Investigators of the Duke Heart Center: Postoperative hyperthermia is associated with cognitive dysfunction after coronary artery bypass graft surgery. Stroke 2002; 33: pp. 537-541.
- Nathan H.J., Wells G.A., Munson J.L., Wozny D.: Neuroprotective effect of mild hypothermia in patients undergoing coronary artery surgery with cardiopulmonary bypass: A randomized trial. Circulation 2001; 104: pp. 85-91.
- Boodhwani M., Rubens F., Wozny D., Rodriguez R., Nathan H.J.: Effects of sustained mild hypothermia on neurocognitive function after coronary artery bypass surgery: A randomized, double-blind study. J Thorac Cardiovasc Surg 2007; 134: pp. 443-450.
- Sirvinskas E., Usas E., Mankute A., et. al.: Effects of intraoperative external head cooling on short-term cognitive function in patients after coronary artery bypass graft surgery. Perfusion 2014; 29: pp. 124-129.
- Grigore A.M., Murray C.F., Ramakrishna H., Djaiani G.: A core review of temperature regimens and neuroprotection during cardiopulmonary bypass: Does rewarming rate matter?. Anesth Analg 2009; 109: pp. 1741-1751.
- Hogan A.M., Shipolini A., Brown M.M., Hurley R., Cormack F.: Fixing hearts and protecting minds: A review of the multiple, interacting factors influencing cognitive function after coronary artery bypass graft surgery. Circulation 2013; 128: pp. 162-171.
- Cook D.J.: CON: Temperature regimens and neuroprotection during cardiopulmonary bypass: Does rewarming rate matter?. Anesth Analg 2009; 109: pp. 1733-1737.
- Grocott H.P.: PRO: Temperature regimens and neuroprotection during cardiopulmonary bypass: Does rewarming rate matter?. Anesth Analg 2009; 109: pp. 1738-1740.
- Engleman R., Baker R.A., Likosky D.S., et. al.: The Society of Thoracic Surgeons; The Society of Cardiovascular Anesthesiologists, Clinical Practice Guidelines for Cardiopulmonary Bypass – Temperature Management during Cardiopulmonary Bypass. J Extra Corpor Technol 2015; 47: pp. 145-154.
- Enmoto S., Hindman B.J., Dexter F., Smith T., Cutkomp J.: Rapid rewarming causes an increase in the cerebral metabolic rate for oxygen that is temporarily unmatched by cerebral blood flow. A study during cardiopulmonary bypass in rabbits. Anesthesiology 1996; 84: pp. 1392-1400.
- Lindgren M., Eckert B., Stenberg G., Agardh C.D.: Restitution of neurophysiological functions, performance, and subjective symptoms after moderate insulin-induced hypoglycemia in non-diabetic men. Diabet Med 1996; 13: pp. 218-225.
- Schafer R.J., Page K.A., Arora J., Sherwin R., Constable R.T.: BOLD response to semantic and syntactic processing during hypoglycemia is load-dependent. Brain Lang 2012; 120: pp. 1-14.
- Davis E.A., Soong S.A., Byrne G.C., Jones T.W.: Acute hyperglycemia and cognitive function in children with IDDM. J Pediatr Endocrinol Metab 1996; 9: pp. 455-461.
- Puskas F., Grocott H.P., White W.D., Mathew J.P., Newman M.F., Bar-Yosef S.: Intraoperative hyperglycemia and cognitive decline after CABG. Ann Thorac Surg 2007; 84: pp. 1467-1473.
- Cornford E.M., Hyman S., Cornford M.E., Clare-Salzler M.: Down-regulation of blood-brain glucose transport in the hyperglycemic nonobese diabetic mouse. Neurochem Res 1995; 20: pp. 869-873.
- Butterworth J., Wagenknecht L.E., Legault C., et. al.: Attempted control of hyperglycemia during cardiopulmonary bypass fails to improve neurologic or neurobehavioral outcomes in patients without diabetes mellitus undergoing coronary artery bypass grafting. J Thorac Cardiovasc Surg 2005; 130: pp. 1319.
- Saager L., Duncan A.E., Yared J.P., et. al.: Intraoperative tight glucose control using hyperinsulinemic normoglycemia increases delirium after cardiac surgery. Anesthesiology 2015; 122: pp. 1214-1223.
- Schricker T., Sato H., Beaudry T., Codere T., Hatzakorzian R., Pruessner J.C.: Intraoperative maintenance of normoglycemia with insulin and glucose preserves verbal learning after cardiac surgery. PLoS One 2014; 9:
- Blumenthal J.A., Lett H.S., Babyak M.A., et. al.: Depression is a risk factor for mortality after coronary artery bypass surgery. Lancet 2003; 362: pp. 604-609.
- Kadoi Y., Kawauchi C., Ide M., et. al.: Preoperative depression is a risk factor for postoperative short-term and long-term cognitive dysfunction in patients with diabetes mellitus. J Anesth 2011; 25: pp. 10-17.
- Folks D.G., Freeman A.M., Sokol R.S., Govier A.V., Reves J.G., Baker D.M.: Cognitive dysfunction after coronary artery bypass surgery: a case-controlled study. South Med J 1988; 81: pp. 202-206.
- Tardiff B.E., Newman M.F., Saunders A.M., et. al.: Preliminary report of a genetic basis of cognitive decline after cardiac operations. The Neurologic Outcome Research group of the Duke Heart Center. Ann Thorac Surg 1997; 64: pp. 715-720.
- McDonagh D.L., Mathew J.P., White W.D., et. al.: Cognitive function after major noncardiac surgery, apolipoprotein E4 genotype, and biomarkers of brain injury. Anesthesiology 2010; 112: pp. 852-859.
- Lelis R.G., Krieger J.E., Pereira A.C., et. al.: Apolipoprotein E4 genotype increases the risk of postoperative cognitive dysfunction in patients undergoing coronary artery bypass graft surgery. J Cardiovasc Surg (Torino) 2006; 47: pp. 451-456.
- Bartels K., Li Y.J., Li Y.W., et. al.: Apolipoprotein epsilon 4 genotype is associated with less improvement in cognitive function five years after cardiac surgery: a retrospective cohort study. Can J Anaesth 2015; 62: pp. 618-626.
- Schenning K.J., Murchison C.F., Mattek Nora, et. al.: Surgery is associated with ventricular enlargement, cognitive and functional decline. Alzheimers Dement 2016; 12: pp. 590-597.
- Steed L., Kong R., Stygall J., et. al.: The role of the apolipoprotein E in cognitive decline after cardiac operation. Thorac Surg 2001; 71: pp. 823-826.
- Evered L., Scott D.A., Silbert B., Maruff P.: Postoperative cognitive dysfunction is independent of type of surgery and anesthetic. Anesth Analg 2011; 112: pp. 1179-1185.
- Tagarakis G.I., Tsolaki-Tagaraki F., Tsolaki M., Diegeler A., Tsilmingas N.B., Papassotiropoulos A.: The role of apolipoprotein E in cognitive decline and delirium after bypass heart operations. Am J Alzheimers Dis Other Demen 2007; 22: pp. 223-228.
- Askar F.Z., Cetin H.Y., Kumral E., et. al.: Apolipoprotein E epsilon4 allele and neurobehavioral status after on-pump coronary artery bypass grafting. J Card Surg 2005; 20: pp. 501-505.
- Silbert B.S., Evered L.A., Scott D.A., Cowie T.F.: The apolipoprotein E epsilon4 allele is not associated with cognitive dysfunction in cardiac surgery. Ann Thorac Surg 2008; 86: pp. 841-847.
- Abelha F.J., Fernandes V., Botelho M., et. al.: Apolipoprotein E e4 allele does not increase the risk of early postoperative delirium after major surgery. J Anesth 2012; 26: pp. 412-421.
- Leung J.M., Sands L.P., Wang Y., et. al.: Apolipoprotein Ee4 allele increases the risk of early postoperative delirium in older patients undergoing noncardiac surgery. Anesthesiology 2007; 107: pp. 406-411.
- Ti L.K., Mackensen G.B., Grocott H.P., et. al.: Neurologic Outcome Research Group: Apolipoprotein E4 increases aortic atheroma burden in cardiac surgical patients. J Thorac Cardiovasc Surg 2003; 125: pp. 211-213.
- Benitez B.A., Jin S.C., Guerreiro Graham R., et. al.: 3C Study Group; EADI consortium; Alzheimer’s Disease Genetic Consortium (ADGC); Alzheimer’s Disease Neuroimaging Initiative (ADNI); GERAD Consortium; Missense variant in TREML2 protects against Alzheimer’s disease. Neurobiol Aging 2014; 35: pp. 1510.
- Carrasquillo M.M., Belbin O., Hunter T.A., et. al.: Replication of CLU, CR1, and PICALM associations with Alzheimer disease. Arch Neurol 2010; 67: pp. 961-964.
- Chen L.H., Kao P.Y., Fan Y.H., et. al.: Polymorphisms of CR1, CLU and PICALM confer susceptibility of Alzheimer’s disease in a southern Chinese population. Neurobiol Aging 2012; 33: pp. 210.
- Lambert J.C., Heath S., Even G., et. al.: European Alzheimer’s Disease Initiative Investigators: Genome-wide association study identifies variants at CLU and CR1 associated with Alzheimer’s disease. Nat Genet 2009; 41: pp. 1094-1099.
- Luo J., Li S., Qin X., et. al.: Meta-analysis of the association between CR1 polymorphisms and risk of late-onset Alzheimer’s disease. Neurosci Lett 2014; 578: pp. 165-170.
- Augoustides J.G.: The inflammatory response to cardiac surgery with cardiopulmonary bypass: should steroid prophylaxis be routine?. J Cardiothorac Vasc Anesth 2012; 26: pp. 952-958.
- Ridker P.M., Hennekens C.H., Schmitz C., Stampfer M.J., Lindpaintner K.: PIA1/A2 polymorphism of platelet glycoprotein Illa and risks of myocardial infarction, stroke, and venous thrombosis. Lancet 1997; 349: pp. 385-388.
- Weiss E.J., Bray P.F., Tayback M., et. al.: A polymorphism of a platelet glycoprotein receptor as an inherited risk factor for coronary thrombosis. N Engl J Med 1996; 334: pp. 1090-1094.
- Mathew J.P., Podgoreanu M.V., Grocott H.P., et. al.: Genetic variants in P-selectin and C-reactive protein influence susceptibility to cognitive decline after cardiac surgery. J Am Coll Cardiol 2007; 49: pp. 1934-1942.
- Eckenhoff R.G., Johansson J.S., Wei H., et. al.: Inhaled anesthetic enhancement of amyloid-beta oligomerization and cytotoxicity. Anesthesiology 2004; 101: pp. 703-709.
- Zhang Y., Dong Y., Wu X., et. al.: The mitochondrial pathway of anesthetic isoflurane-induced apoptosis. J Biol Chem 2010; 285: pp. 4025-4037.
- Tang J.X., Mardini F., Janik L.S., et. al.: Modulation of murine Alzheimer pathogenesis and behavior by surgery. Ann Surg 2013; 257: pp. 439-448.
- Whittington R.A., Virag L., Marcouiller F., et. al.: Propofol directly increases tau phosphorylation. PLoS One 2011; 6:
- Planel E., Bretteville A., Liu L., et. al.: Acceleration and persistence of neurofibrillary pathology in a mouse model of tauopathy following anesthesia. FASEB J 2009; 23: pp. 2595-2604.
- Xie Z., Culley D.J., Dong Y., et. al.: The common inhalation anesthetic isoflurane induces caspase activation and increases amyloid beta-protein level in vivo. Ann Neurol 2008; 64: pp. 618-627.
- Berger M., Burke J., Eckenhoff R., Mathew J.: Alzheimer’s disease, anesthesia, and surgery: a clinically focused review. J Cardiothorac Vasc Anesth 2014; 28: pp. 1609-1623.
- Reinsfelt B., Westerlind A., Blennow K., Zetterberg H., Ricksten S.E.: Open-heart surgery increases cerebrospinal fluid levels of Alzheimer-associated amyloid beta. Acta Anaesthesiol Scand 2013; 57: pp. 82-88.
- Palotas A., Reis H.J., Bogats G., et. al.: Coronary artery bypass surgery provokes Alzheimer’s disease-like changes in the cerebrospinal fluid. J Alzheimers Dis 2010; 21: pp. 1153-1164.
- Anckarsater R., Anckarsater H., Bromander S., Blennow K., Wass C., Zetterberg H.: Non-neurological surgery and cerebrospinal fluid biomarkers for neuronal and astroglial integrity. J Neural Transm 2014; 121: pp. 649-653.
- Tang J.X., Baranoc D., Hammond M., Shaw L.M., Eckenhoff M.F., Eckenhoff R.G.: Human Alzheimer and inflammation biomarkers after anesthesia and surgery. Anesthesiology 2011; 115: pp. 727-732.
- Chen P.L., Yang C.W., Tseng Y.K., et. al.: Risk of dementia after anaesthesia and surgery. Br J Psychiatry 2014; 204: pp. 188-193.
- Chen C.W., Lin C.C., Chen K.B., Kuo Y.C., Li C.Y., Chung C.J.: Increased risk of dementia in people with previous exposure to general anesthesia: A nationwide population-based case-control study. Alzheimers Dement 2014; 10: pp. 196-204.
- Evered L.: Response to: Avidan and Evers. J Alzheimer’s Dis 2011; 24: pp. 201-216. J Alzheimers Disease 2014
- Terrando N., Eriksson L.I., Eckenhoff R.G.: Perioperative neurotoxicity in the elderly: Summary of the 4 th International Workshop. Anesth Analg 2015; 120: pp. 649-652.
- Guay J.: General anaesthesia does not contribute to long-term post-operative cognitive dysfunction in adults: A meta-analysis. Indian J Anaesth 2011; 55: pp. 358-363.
- Mason S.E., Noel-Storr A., Ritchie C.W.: The impact of general and regional anesthesia on the incidence of post-operative cognitive dysfunction and post-operative delirium: a systematic review with meta-analysis. J Alzheimers Dis 2010; 22: pp. 67-79.
- Brown C.H., Faigle R., Klinker L., et. al.: The association of brain MRI characteristics and postoperative delirium in cardiac surgery patients. Clin Ther 2015; 37: pp. 2686-2699.
- Abu-Omar Y., Cader S., Guerrieri Wolf L., Pigott D., Matthews P.M., Taggart D.P.: Short-term changes in cerebral activity in on-pump and off-pump cardiac surgery defined by functional magnetic resonance imaging and their relationship to microembolization. J Thorac Cardiovasc Surg 2006; 132: pp. 1119-1125.
- Van Essen D.C., Smith S.M., Barch D.M., Behrens T.E., Yacoub E., Ugurbil K.: WU-Minn HCP Consortium: The WU-Minn Human Connectome Project: An overview. Neuroimage 2013; 80: pp. 62-79.
- Huang H., Tanner J., Parvataneni H., et. al.: Impact of total knee arthroplasty with general anesthesia on brain networks: cognitive efficiency and ventricular volume predict functional connectivity decline in older adults. J Alzheimers Dis 2018; 62: pp. 319-333.
- Raichle M.E.: The brain’s default mode network. Annu Rev Neurosci 2015; 38: pp. 433-447.
- Raichle M.E., MacLeod A.M., Snyder A.Z., Powers W.J., Gusnard D.A., Shulman G.L.: A default mode of brain function. Proc Natl Acad Sci USA 2001; 98: pp. 676-682.
- Choi S.H., Lee H., Chung T.S., et. al.: Neural network functional connectivity during and after an episode of delirium. Am J Psychiatry 2012; 169: pp. 498-507.
- Anguera J.A., Boccanfuso J., Rintoul J.L., et. al.: Video game training enhances cognitive control in older adults. Nature 2013; 501: pp. 97-101.
- Vonck K., Raedt R., Naulaerts J., et. al.: Vagus nerve stimulation…25 years later! What do we know about the effects on cognition?. Neurosci Biobehav Rev 2014; 45: pp. 63-71.
- Nilakantan A.S., Bridge D.J., Gagnon E.P., VanHaerents S.A., Voss J.L.: Stimulation of the posterior cortical-hippocampal network enhances precision of memory recollection. Curr Biol 2017; 27: pp. 465-470.
- Wang J.X., Rogers L.M., Gross E.Z., et. al.: Targeted enhancement of cortical-hippocampal brain networks and associative memory. Science 2014; 345: pp. 1054-1057.
- Stephens J.A., Berryhill M.E.: Older adults improve on everyday tasks after working memory training and neurostimulation. Brain Stimul 2016; 9: pp. 553-559.
- Masana M.F., Koyanagi A., Haro J.M., Tryovolas S.: n-3 Fatty acids, Mediterranean diet and cognitive function in normal aging: A systematic review. Exp Gerontol 2017; 91: pp. 39-50.
- Culley D.J., Crosby G.: Prehabilitation for prevention of postoperative cognitive dysfunction?. Anesthesiology 2015; 123: pp. 7-9.
- Kawano T., Eguchi S., Iwata H., Tamura T., Kumagai N., Yokoyama M.: Impact of preoperative environmental enrichment on prevention of development of cognitive impairment following abdominal surgery in a rat model. Anesthesiology 2015; 123: pp. 160-170.
- Aldecoa C., Bettelli G., Bilotta F., et. al.: European Society of Anaesthesiology evidence-based and consensus-based guideline on postoperative delirium. Eur J Anaesthesiol 2017; 34: pp. 192-214.
- Ely E.W.: The ABCDEF Bundle: Science and philosophy of how ICU liberation serves patients and families. Crit Care Med 2017; 45: pp. 321-330.
- Vincent J.L., Shehabi Y., Walsh T.S., et. al.: Comfort and patient-centered care without excessive sedation: the eCASH concept. Intensive Care Med 2016; 42: pp. 962-971.
- Stiegler M.P., Tung A.: Cognitive processes in anesthesiology decision making. Anesthesiology 2014; 120: pp. 204-217.
