Điều trị Trầm cảm Kháng trị - Dược lý Thần kinh và Kích thích Thần kinh, ấn bản 2025 | Therapies for Treatment-Resistant Depression: Neuropharmacology and Neurostimulation 1st Edition | Chủ biên: James Murrough MD PhD, Dennis Charney MD | (C) Nhà xuất Bản ELSEVIER. Dịch và Chú giải tiếng Việt: Ths.BS. Lê Đình Sáng - BSCKII. Nguyễn Văn Phi
CHƯƠNG 6. KETAMINE VÀ ESKETAMINE TRONG ĐIỀU TRỊ RỐI LOẠN TRẦM CẢM KHÁNG TRỊ
Gerard Sanacora1, Sina Nikayin1, Dennis S. Charney2,3, và James W. Murrough2,3,4
1 Khoa Tâm thần học, Trường Y khoa, Đại học Yale, New Haven, CT, Hoa Kỳ 2 Khoa Tâm thần học, Khoa học Thần kinh, và Khoa học Dược lý, Trường Y khoa Icahn tại Mount Sinai, New York, NY, Hoa Kỳ 3 Khoa Tâm thần học và Khoa học Thần kinh, Trường Y khoa Icahn tại Mount Sinai, New York, NY, Hoa Kỳ 4 Trung tâm Lâm sàng, Nghiên cứu và Giáo dục về Bệnh Tâm thần VISN 2 (MIRECC), Trung tâm Y tế VA James J. Peters, Bronx, NY, Hoa Kỳ
6.1 Giới Thiệu Và Lịch Sử Của Ketamine
Trong chương này, chúng tôi sẽ thảo luận về việc sử dụng ketamine và esketamine trong điều trị bệnh trầm cảm kháng trị (treatment-resistant depression - TRD). Chúng tôi sẽ điểm lại ngắn gọn lịch sử của ketamine, sau đó phác thảo những hiểu biết hiện tại của chúng ta về hiệu quả và tính an toàn của cả ketamine và esketamine, và cuối cùng, chúng tôi sẽ thảo luận về những lĩnh vực cần nghiên cứu thêm.
Calvin Stevens đã phát hiện ra ketamine vào năm 1962 trong nỗ lực tìm kiếm một hợp chất tương tự như phencyclidine (phencyclidine - PCP) nhưng có hồ sơ an toàn tốt hơn. Hợp chất này được đặt tên là ketamine do sự hiện diện của một nhóm xeton (ketone) và một nhóm amin (amine) trong cấu trúc của nó. Ban đầu được phát triển để sử dụng trong thú y vào năm 1963, các bác sĩ đã sử dụng ketamine lần đầu tiên trên người vào năm 1964, và sau đó thuốc đã nhận được sự chấp thuận của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (U.S. Food and Drug Administration - FDA) (dưới tên thương mại là Ketalar) để sử dụng làm thuốc gây mê (anesthetic) trên người vào năm 1970. Do hồ sơ an toàn tương đối thuận lợi khi làm thuốc gây mê và được sử dụng trên toàn thế giới, ketamine đã nằm trong Danh sách Thuốc Thiết yếu (Essential Medicines Lists) của Tổ chức Y tế Thế giới (World Health Organization - WHO) kể từ năm 1985.
Báo cáo nghiên cứu đầu tiên về ketamine trong lĩnh vực tâm thần học bắt nguồn từ năm 1973, khi các bác sĩ sử dụng thuốc này trong một nghiên cứu nhãn mở (open-label study) để điều trị cho 100 người bệnh mắc các rối loạn tâm thần khác nhau, dựa trên ý tưởng rằng thuốc sẽ tạo điều kiện thuận lợi cho quá trình phân tâm học (psychoanalytic process). Phương pháp điều trị này dường như đã đạt được thành công đáng kể ở nhiều người bệnh. Tuy nhiên, phát hiện này đã không thúc đẩy thêm các nghiên cứu tiếp theo và dường như đã bị chìm vào quên lãng trong y văn. Sự quan tâm nghiêm túc đối với ketamine như một phương pháp điều trị chống trầm cảm (antidepressant treatment) đã không xuất hiện trở lại cho đến đầu những năm 1990. Vào thời điểm đó, một nhóm các nhà khoa học tại Viện Y tế Quốc gia Hoa Kỳ (National Institutes of Health - NIH) làm việc trên các mô hình động vật bị stress và tập trung vào vai trò của các thụ thể N-methyl-D-aspartate (N-methyl-D-aspartate receptors - NMDARs) đã đưa ra một giả thuyết quan trọng. Vì các NMDAR đóng vai trò thiết yếu trong việc tạo ra sự điện thế hóa dài hạn (long-term potentiation) – một quá trình bị suy yếu trong mô hình động vật gặm nhấm bị stress không thể trốn thoát (inescapable stress) dùng để nghiên cứu bệnh trầm cảm – họ cho rằng NMDAR có thể đang góp phần vào sinh lý bệnh của bệnh trầm cảm. Các nhà nghiên cứu lập luận xa hơn rằng việc đối kháng NMDAR có thể tạo ra các tác dụng chống trầm cảm. Sau đó, họ đã tiến hành chứng minh tác dụng này bằng cách sử dụng các chất đối kháng NMDAR cạnh tranh và không cạnh tranh cũng như một chất chủ vận một phần (partial agonist) trên các mô hình động vật gặm nhấm mắc bệnh trầm cảm.
Song song đó, ngày càng có nhiều bằng chứng khác cho thấy hệ thống dẫn truyền thần kinh glutamatergic (glutamatergic neurotransmitter system) có thể đóng một vai trò quan trọng trong sinh lý bệnh của rối loạn trầm cảm nặng (major depressive disorder - MDD). Các nhà khoa học đã báo cáo nồng độ glutamate ngoại bào gia tăng và những thay đổi trong quá trình vận chuyển màng của NMDAR, ngoài các thụ thể alpha-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid (AMPA), nhằm đáp ứng với tình trạng stress cấp tính trên các mô hình động vật. Các nghiên cứu khác đã tìm thấy bằng chứng chứng minh tình trạng stress mạn tính điều chỉnh sự điều hòa glutamate bên trong vỏ não trước trán (prefrontal cortex - PFC). Cùng với nhau, những phát hiện này gợi ý một vai trò gây bệnh có thể có của độc tính liên quan đến glutamate (glutamate-related toxicity) trong các rối loạn khí sắc (mood disorders). Bằng chứng ngày càng tăng cho thấy trầm cảm là một rối loạn chức năng vỏ não-hệ viền (cortico-limbic function), với sự điều hòa chủ yếu bởi glutamatergic và gamma-aminobutyric acid (GABA)-ergic. Kết hợp với bằng chứng về những thay đổi trong dẫn truyền thần kinh glutamatergic liên quan đến sinh lý bệnh của các rối loạn khí sắc, điều này đã truyền cảm hứng cho nghiên cứu nền tảng của Berman và cộng sự. Họ đã khám phá tác dụng chống trầm cảm tiềm năng của ketamine, với tư cách là một chất đối kháng NMDAR không cạnh tranh có ái lực cao (high-affinity non-competitive NMDAR antagonist). Xem bên dưới để biết phần thảo luận chi tiết về các thử nghiệm lâm sàng kiểm tra tác dụng chống trầm cảm của ketamine. Hình dưới đây trình bày dòng thời gian về sự phát triển và nghiên cứu ketamine từ góc độ của bệnh trầm cảm (Hình 6.1).
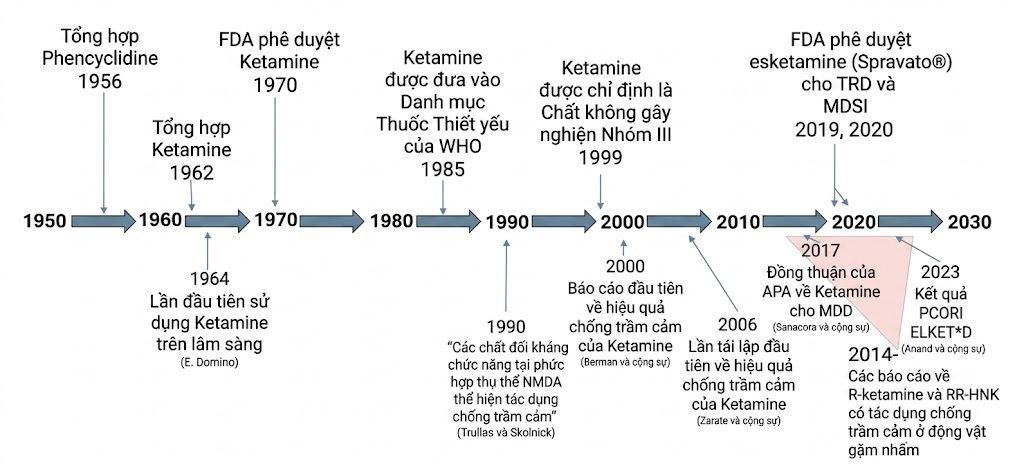
Hình 6.1 Lịch sử của ketamine trong bệnh trầm cảm. Hình ảnh minh họa dòng thời gian của các sự kiện được chọn lọc có liên quan đến sự phát triển của ketamine và các nghiên cứu về việc sử dụng nó cho bệnh trầm cảm. TRD, trầm cảm kháng trị; MDSI, rối loạn trầm cảm nặng kèm theo ý tưởng tự sát.
6.2 Dược Lý Học Của Ketamine
6.2.1 Cấu Trúc Phân Tử Và Dược Lực Học
Ketamine là một phân tử bất đối xứng (chiral molecule) bao gồm hai đồng phân quang học (enantiomers): S(+)-ketamine ("esketamine") và R(-)-ketamine ("arketamine"). Mặc dù ketamine được biết là có nhiều đích tác dụng dược lực học, nhưng tác dụng dược lực học gần nhất và đáng kể nhất liên quan đến hiệu quả của nó (như một thuốc gây mê và rất có thể cũng là thuốc chống trầm cảm) vẫn là đặc tính đối kháng NMDAR. Đặc biệt liên quan đến các đặc tính chống trầm cảm của nó, các liều dưới mức gây mê (subanesthetic doses) của ketamine được cho là ưu tiên phong tỏa các NMDAR hiện diện trên các nơ-ron ức chế GABA-ergic, dẫn đến sự gia tăng giải phóng glutamate. Điều này cuối cùng thúc đẩy sự tăng cường điện thế hóa synapse (synaptic potentiation). Sự giải phóng glutamate thoáng qua này kích thích thụ thể AMPA chứa GluA1 ở màng sau synapse, được xem như một bước có khả năng đóng vai trò quan trọng trong việc gia tăng độ mềm dẻo của synapse (synaptic plasticity) do ketamine đã được quan sát thấy. Sự điều hòa tăng (up-regulation) của yếu tố dinh dưỡng thần kinh có nguồn gốc từ não (brain-derived neurotrophic factor - BDNF) và sự kích thích phức hợp đích cơ học của rapamycin 1 (mechanistic target of rapamycin complex 1 - mTORC1) tại synapse glutamate dường như cũng rất quan trọng đối với cơ chế tác dụng chống trầm cảm của ketamine, ít nhất là trong bối cảnh của các mô hình động vật gặm nhấm (Hình 6.2). Các nhà khoa học đã xác định được nhiều con đường khác, có lẽ là bổ sung cho nhau, có thể đóng góp vào tác dụng chống trầm cảm của ketamine. Một số quá trình này bao gồm độ mềm dẻo synapse nội môi (homeostatic synaptic plasticity) và các đích thụ thể bao gồm thụ thể opioid muy và các thụ thể sigma, cùng với các thụ thể khác.
Esketamine được ghi nhận là có ái lực với NMDAR lớn hơn gấp 3-4 lần so với arketamine. Hiệu lực cao hơn của esketamine (cho phép hiệu quả tương tự nhưng làm giảm phơi nhiễm ketamine tổng thể) đã dẫn đến việc sử dụng rộng rãi đồng phân quang học esketamine như một thuốc gây mê ở nhiều nơi trên thế giới. Những quan sát này có thể đã góp phần tạo nên cơ sở lý luận cho việc phát triển esketamine (thay vì arketamine hoặc ketamine racemic) để điều trị bệnh trầm cảm kháng trị. Arketamine thực sự có đặc tính đối kháng NMDAR yếu hơn, mặc dù có thể có các đặc tính độc đáo khác sẽ được thảo luận ở phần sau của chương này. Hiện tại FDA chưa phê duyệt arketamine để sử dụng trên lâm sàng.
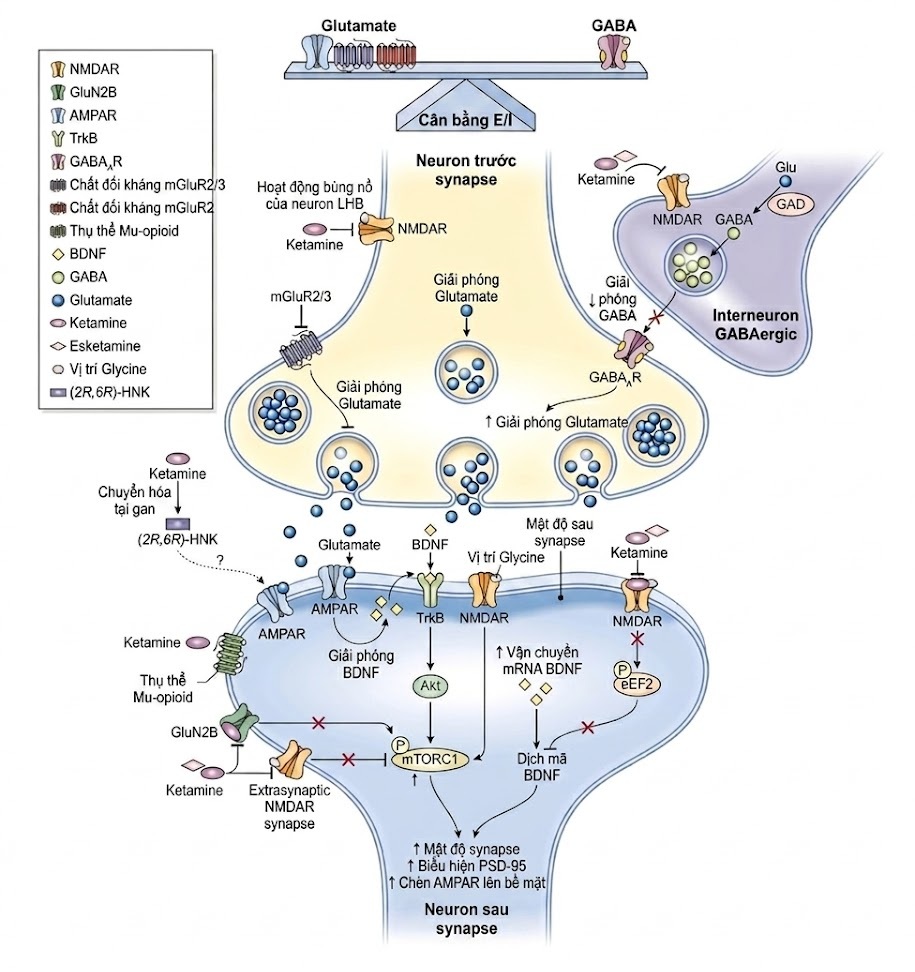
Hình 6.2 Tác dụng dược lực học của ketamine. Các tác dụng giống thuốc chống trầm cảm tác dụng nhanh của ketamine dường như được trung gian chủ yếu thông qua sự đối kháng NMDAR và hoạt động của thụ thể AMPA. Việc phong tỏa các NMDAR bởi ketamine racemic và esketamine trên các nơ-ron trung gian GABAergic làm giảm sự ức chế đối với các nơ-ron tháp (pyramidal neurons), dẫn đến tăng giải phóng glutamate. Sự gia tăng xác suất giải phóng glutamate này kích hoạt các cơ chế xuôi dòng làm tăng tín hiệu mTORC1, dẫn đến điều hòa tăng mật độ synapse, PSD-95 và chèn thụ thể AMPA chứa GluA1 vào bề mặt. Ngoài ra, việc phong tỏa các NMDAR ngoại synapse khử phosphoryl hóa eEF2, dẫn đến tăng dịch mã BDNF và hoạt động mTORC1. Các nhà nghiên cứu cũng đã giả định rằng ketamine gắn kết với các thụ thể opioid muy, mặc dù cơ chế xuôi dòng chính xác vẫn chưa được biết rõ. Cuối cùng, ketamine có thể phong tỏa hoạt động bùng phát của LHb thông qua đối kháng NMDAR trên các nơ-ron LHb. Nhìn chung, những thay đổi này dẫn đến cải thiện sự cân bằng kích thích/ức chế (E/I) giữa glutamate và GABA để tạo ra các tác dụng điều trị. Chữ viết tắt: AMPAR thụ thể alpha-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid, BDNF yếu tố dinh dưỡng thần kinh có nguồn gốc từ não, eEF2 yếu tố kéo dài nhân thực (eukaryotic elongation factor), E/I Kích thích/ức chế (Excitatory/inhibitory), GABA gamma-aminobutyric acid, GAD glutamate decarboxylase, Glu glutamate, HNK hydroxynorketamine, LHb cuống tuyến tùng bên (lateral habenula), mGluR thụ thể glutamate chuyển hóa (metabotropic glutamate receptor), mRNA axit ribonucleic thông tin, mTORC1 phức hợp đích cơ học của rapamycin 1, NMDAR thụ thể N-methyl-D-aspartate, PSD-95 protein tỷ trọng sau synapse 95 (post-synaptic density 95), TrkB thụ thể tropomyosin kinase B. Nguồn: Từ Kadriu và cộng sự (2019).
6.2.2 Dược Động Học
🔰Bạn cần đăng nhập để có thể xem tiếp toàn bộ nội dung của chương sách này cũng như có thể truy cập toàn bộ nội dung của tất cả các cuốn sách Y học được dịch và chú giải và các tài nguyên Y học bản quyền được xuất bản đầu tiên và duy nhất trên THƯ VIỆN Y HỌC MEDIPHARM. Tài khoản đọc sách Medipharm cho phép bạn xem toàn bộ mọi nội dung có sẵn bao gồm sách dịch, tổng quan lâm sàng, guidelines hướng dẫn chẩn đoán và điều trị được dịch và hiệu đính bởi các chuyên gia đầu ngành trong từng lĩnh vực đảm bảo tính chính xác về học thuật, hỗ trợ chú giải thuật ngữ song ngữ Anh - Việt giúp bạn trau dồi không chỉ kiến thức học thuật mà còn vốn từ vựng Y khoa chuyên ngành.
👩🏻🔬Bạn chưa có tài khoản đọc sách Medipharm? → VUI LÒNG ĐĂNG KÝ TÀI KHOẢN TẠI ĐÂY.
Hoặc nhập thông tin ĐĂNG NHẬP BÊN DƯỚI nếu đã có tài khoản đọc sách Medipharm.
