Cẩm nang Hô hấp Can thiệp. Practical Guide to Interventional Pulmonology
Bản quyền (C) 2024 Nhà xuất bản Elsevier.
Ts.Bs. Lê Nhật Huy – Ths.Bs. Lê Đình Sáng (Dịch và chú giải)
Chương 11: Sử dụng thuốc qua nội soi đường thở
The Endoscopic Application of Medication to the Airway
Megan Acho; Roy Semaan; Lonny Yarmus
Practical Guide to Interventional Pulmonology, 11, 113-125
MỤC LỤC CHƯƠNG
| GIỚI THIỆU
BỆNH LÝ LỒNG NGỰC ÁC TÍNH BỆNH LÝ LỒNG NGỰC KHÔNG ÁC TÍNH SỬ DỤNG THUỐC QUA NỘI SOI VÀ LỰA CHỌN KỸ THUẬT TÓM TẮT |
GIỚI THIỆU
Kể từ khi được phát hiện vào năm 1876, nội soi phế quản đã đóng một vai trò cơ bản trong chẩn đoán và quản lý bệnh lý phổi. Trong vài thập kỷ qua, khả năng điều trị của nội soi phế quản đã phát triển vượt bậc. Thật vậy, các công nghệ như liệu pháp laser, đông huyết tương argon, liệu pháp lạnh, xạ trị áp sát và đặt stent nội phế quản đã cách mạng hóa việc quản lý bệnh lý đường thở trung tâm ác tính và không ác tính, mở ra một kỷ nguyên mới của chuyên ngành hô hấp can thiệp. Gần đây, ngày càng có nhiều sự quan tâm đến việc đưa thuốc trực tiếp vào đường thở bằng phương pháp nội soi phế quản. Chương này thảo luận về việc sử dụng thuốc qua nội soi cho một loạt các bệnh lý lồng ngực ác tính và không ác tính.
BỆNH LÝ LỒNG NGỰC ÁC TÍNH
Tiêm xuyên thành phế quản qua kim
Bất chấp các chiến dịch chống thuốc lá và các sáng kiến tầm soát ung thư phổi rộng rãi, ung thư phổi vẫn là nguyên nhân gây tử vong do ung thư hàng đầu tại Hoa Kỳ với tỷ lệ tử vong dự kiến hơn 147.000 ca chỉ riêng trong năm 2019. Phần lớn các ca ung thư phổi là ung thư phổi không tế bào nhỏ (NSCLC), nhiều trong số đó đã ở giai đoạn tiến triển tại thời điểm chẩn đoán ban đầu. Với bệnh suất và tử suất đáng kể liên quan đến ung thư phổi, việc chẩn đoán sớm có tầm quan trọng tối cao. Vào cuối những năm 1970, Ko-Pen Wang đã phát triển kỹ thuật chọc hút bằng kim xuyên thành phế quản qua nội soi phế quản ống mềm (TBNA), cho phép lấy mẫu mô qua nội soi với khả năng đánh giá nhanh tại chỗ (ROSE) các mẫu bệnh phẩm mô bệnh học. Việc sử dụng TBNA để chẩn đoán và phân giai đoạn ung thư phổi đã tăng lên đáng kể sau sự ra đời của siêu âm nội phế quản (EBUS). EBUS cho phép quan sát trực tiếp tổn thương đang được sinh thiết, không chỉ làm tăng hiệu suất chẩn đoán của thủ thuật mà còn giúp thủ thuật an toàn hơn bằng cách cho phép người thực hiện quan sát việc đưa vào và rút kim ra theo thời gian thực. Ngày nay, TBNA có hướng dẫn của EBUS đã trở thành một thành phần không thể thiếu trong chẩn đoán bệnh ác tính ở lồng ngực và phân giai đoạn hạch trung thất, cung cấp một phương pháp thay thế ít xâm lấn hơn so với nội soi trung thất và phẫu thuật lồng ngực có hỗ trợ video để chẩn đoán và phân giai đoạn ung thư phổi. EBUS-TBNA trước đây cũng đã được chứng minh là làm giảm thời gian chẩn đoán ung thư phổi, cho phép bắt đầu điều trị sớm hơn, cũng như phối hợp chăm sóc nhanh chóng giữa bệnh nhân, bác sĩ ung thư, bác sĩ hô hấp và bác sĩ phẫu thuật.
| Với khả năng chẩn đoán ấn tượng của TBNA, đặc biệt khi kết hợp với EBUS, ngày càng có nhiều sự quan tâm đến vai trò của tiêm xuyên thành phế quản qua kim (TBNI) như một phương thức điều trị. Điều này đặc biệt phù hợp với ung thư phổi. Việc điều trị NSCLC dựa trên phân giai đoạn ung thư, với các giai đoạn tiến triển (II-IV) thường yêu cầu xạ trị và/hoặc hóa trị. Trong số các bệnh nhân được chẩn đoán mắc ung thư phổi, khoảng 20%-30% sẽ phát triển một mức độ tắc nghẽn đường thở do ác tính. Những tổn thương gây tắc nghẽn này có thể liên quan đến tình trạng khó thở ngày càng nặng, dẫn đến giảm chất lượng cuộc sống. Tắc nghẽn đường thở do ác tính cũng có thể dẫn đến các biến chứng như ho ra máu, viêm phổi sau tắc nghẽn, và trong các trường hợp nặng là suy hô hấp. Trong những tình huống này, việc tái thông đường thở nhanh chóng, an toàn và hiệu quả là bắt buộc. |
Trái ngược với các liệu pháp tĩnh mạch, TBNI cho phép đưa thuốc (thường là thuốc độc tế bào) khu trú vào các tổn thương này, không chỉ có khả năng giảm thiểu độc tính toàn thân liên quan đến các tác nhân này mà còn làm tăng nồng độ thuốc trong khối u. Vào những năm 1980, TBNI (không có EBUS) đã được sử dụng để đưa ethanol vào các khối u trong lòng phế quản với mục tiêu làm giảm tắc nghẽn đường thở trung tâm và giảm thiểu chảy máu từ khối u. Fujisawa và cộng sự đã tiêm 0,5-3 mL ethanol 99,5% vào khối u của 13 bệnh nhân có khối u khí-phế quản xâm lấn đường thở trung tâm để tăng cường hoại tử mô, cho phép các mảnh khối u hoại tử được cắt lọc bằng kẹp nhằm cải thiện sự thông thoáng của đường thở. Sawa và cộng sự đã thực hiện một can thiệp tương tự, tiêm trung bình 4,5 mL ethanol 99% vào các tổn thương trong lòng phế quản của tám bệnh nhân, sử dụng hệ thống thông tin video nội soi để đánh giá sự rò rỉ ethanol ra ngoài rìa khối u.
Ngoài ethanol, các hóa chất cũng đã được tiêm trực tiếp vào các khối u trong và ngoài lòng phế quản qua nội soi. Khi hóa trị được thực hiện qua TBNI, thủ thuật này được gọi là hóa trị nội u trong lòng phế quản (EITC). Một trong những mô tả đầu tiên về EITC đến từ Celikoglu và cộng sự ở Thổ Nhĩ Kỳ. Nghiên cứu này được thiết kế để đánh giá EITC như một can thiệp giảm nhẹ tiềm năng cho những người bị ung thư phổi (chủ yếu là ung thư biểu mô tế bào vảy) không thể phẫu thuật. Chín mươi ba bệnh nhân bị ung thư không thể phẫu thuật và có bằng chứng tắc nghẽn dạng sùi hơn 50% ở ít nhất một đường thở chính đã được đưa vào nghiên cứu. Trong số những bệnh nhân này, 68 người được chẩn đoán mắc ung thư biểu mô phế quản chưa được điều trị (với kế hoạch bắt đầu hóa trị và xạ trị toàn thân sau khi điều trị bằng tiêm nội u), trong khi 25 người có tiền sử ung thư đã tái phát mặc dù đã được điều trị trước đó bằng hóa trị và/hoặc xạ trị. Sử dụng ống nội soi phế quản mềm và kim mềm 23-gauge (G) (Olympus Corp, Tokyo, Nhật Bản), các tác giả đã tiêm 1-3 mL mỗi loại thuốc gồm 5-fluorouracil 50 mg/mL, mitomycin 1 mg/mL, methotrexate 5 mg/mL, bleomycin 10 mg/mL và mitoxantrone 2 mg/mL vào các vị trí khác nhau trên khối u. Việc tiêm được thực hiện trong một đến sáu buổi. Sau khi điều trị, các tác giả ghi nhận sự giảm kích thước khối u và cải thiện tình trạng tắc nghẽn đường thở ở 81 bệnh nhân, trong đó 39 người có đường kính lòng đường thở tăng tương đối hơn 50%. Các tác giả đã báo cáo sốt sau thủ thuật ở một tỷ lệ nhỏ bệnh nhân, mặc dù không có biến cố bất lợi đáng kể nào được ghi nhận.
Một nghiên cứu tiếp theo được thực hiện bởi Celikoglu sử dụng đơn trị liệu 5-fluorouracil nội u để quản lý giảm nhẹ tình trạng tắc nghẽn đường thở nghiêm trọng. Các tác giả một lần nữa nghiên cứu các bệnh nhân bị tắc nghẽn nghiêm trọng ở ít nhất một đường thở chính. Trong số 65 bệnh nhân được ghi danh, mức độ thông thoáng lòng đường thở trung bình trước điều trị là 22%; 56 bệnh nhân đã cải thiện về mặt giải phẫu tình trạng tắc nghẽn đường thở với độ thông thoáng lòng đường thở trung bình là 58,5% sau khi tiêm 0,5-1 g 5-fluorouracil 50 mg/mL qua nội soi phế quản mềm bằng kim TBNA 23-G. Một lần nữa, không có tác dụng phụ đáng kể nào được ghi nhận.
Ngoài 5-fluorouracil, còn có dữ liệu hỗ trợ việc sử dụng các hóa chất khác. Các nghiên cứu bổ sung đã được thực hiện chứng minh tính an toàn và hiệu quả của việc tiêm nội u paclitaxel, carboplatin, và cisplatin, với nhiều nghiên cứu gần đây sử dụng cisplatin. Thuốc được lựa chọn dựa trên đặc tính dược lý của chúng về cả tính an toàn và chuyển hóa sinh học. Về mặt an toàn, các hóa chất được chọn cho EITC phải có tác dụng độc tế bào trực tiếp nhưng không gây hoại tử ở các mô khỏe mạnh liền kề với tổn thương ác tính. Ngoài ra, về mặt chuyển hóa, thuốc không được yêu cầu chuyển hóa toàn thân để có hiệu quả. Mặc dù liều tối ưu của cisplatin vẫn chưa rõ ràng, các nghiên cứu mô hình hóa tính toán đã chỉ ra rằng có thể đạt được liều tích lũy thấp hơn bằng cách thực hiện nhiều lần tiêm cisplatin liều nhỏ, cách quãng thay vì tiêm một liều lớn (bolus) vào trung tâm khối u. Cần phải thực hiện nhiều nghiên cứu hơn để xác định loại hóa chất và liều lượng nào là phù hợp nhất, cũng như số lần tiêm tối ưu và vị trí của chúng. Ngoài ra, cần phải có thêm dữ liệu theo dõi dọc của những bệnh nhân đã trải qua TBNI để xác định thời gian điều trị thích hợp và các tác động lâu dài của can thiệp điều trị này.
TBNI có hướng dẫn của EBUS
Gần đây, EBUS đã được sử dụng để giúp tăng cường tính an toàn của EITC. Khan và cộng sự đã mô tả lần đầu tiên sử dụng TBNI có hướng dẫn của EBUS vào năm 2014, trong đó các tác giả đã sử dụng TBNI có hướng dẫn của EBUS để tiêm cisplatin vào một tổn thương trong lòng phế quản ở một bệnh nhân bị ung thư biểu mô tế bào vảy tái phát đã được điều trị trước đó (Hình 11.1).
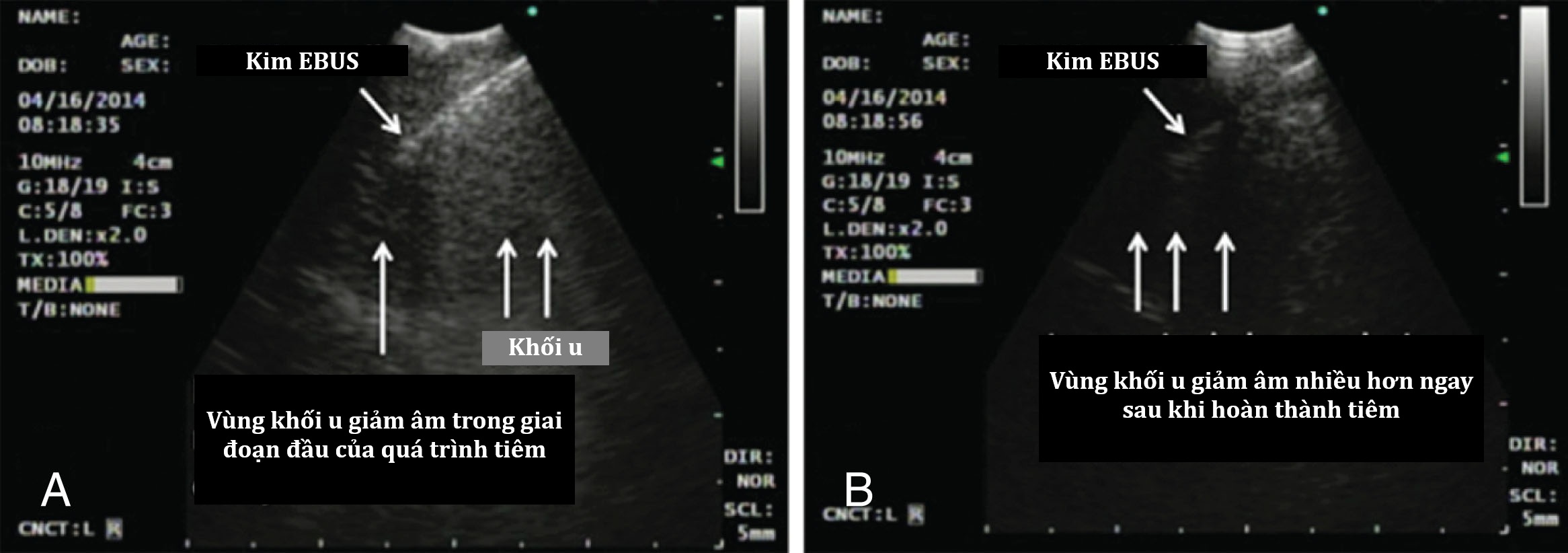
Hình 11.1 Tiêm Cisplatin vào một tổn thương trong lòng phế quản qua EBUS-TBNI. (A) Vùng khối u giảm âm trong giai đoạn đầu của quá trình tiêm. (B) Vùng khối u giảm âm nhiều hơn ngay sau khi hoàn thành tiêm. Nguồn: Khan F, Anker CJ, Garrison G, Kinsey CM. Endobronchial ultrasound-guided transbronchial needle injection for local control of recurrent non-small cell lung cancer. Ann Am Thorac Soc. 2015;12:101-104.
Họ ghi nhận rằng EBUS không chỉ cho phép quan sát trực tiếp việc tiêm thuốc vào khối u mà còn cho phép sử dụng siêu âm Doppler, giúp giảm thiểu nguy cơ kim có thể được đưa vào một vùng giàu mạch máu.
Catheter bóng đưa thuốc nội phế quản
TBNI được sử dụng kết hợp với ống nội soi phế quản mềm hoặc cứng có thể dẫn đến những khó khăn về mặt kỹ thuật khi tiêm vào các tổn thương nằm vuông góc với thành đường thở. TBNI cổ điển vào thành đường thở cũng có thể dẫn đến sự thâm nhập sâu của thuốc với nguy cơ bục đường thở. Một catheter bóng đưa thuốc nội phế quản mới (Catheter Blowfish, Mercator MedSystems, Inc., CA, Hoa Kỳ) gần đây đã được phát triển có thể được đưa qua ống nội soi phế quản mềm. Sau khi được triển khai qua kênh làm việc của ống nội soi phế quản, quả bóng ở đầu xa được bơm phồng lên và đẩy ra một vi kim 34-G vuông góc với catheter (Hình 11.2). Thuốc sau đó có thể được tiêm qua kim này vào khối u và thành phế quản trực tiếp vào lớp dưới niêm mạc và lớp vỏ ngoài phế quản, nhưng không vượt qua lớp sụn. Các nghiên cứu trên lợn cho thấy catheter Blowfish có thể tiêm thuốc theo chu vi vào 60% thành đường thở mỗi lần tiêm.
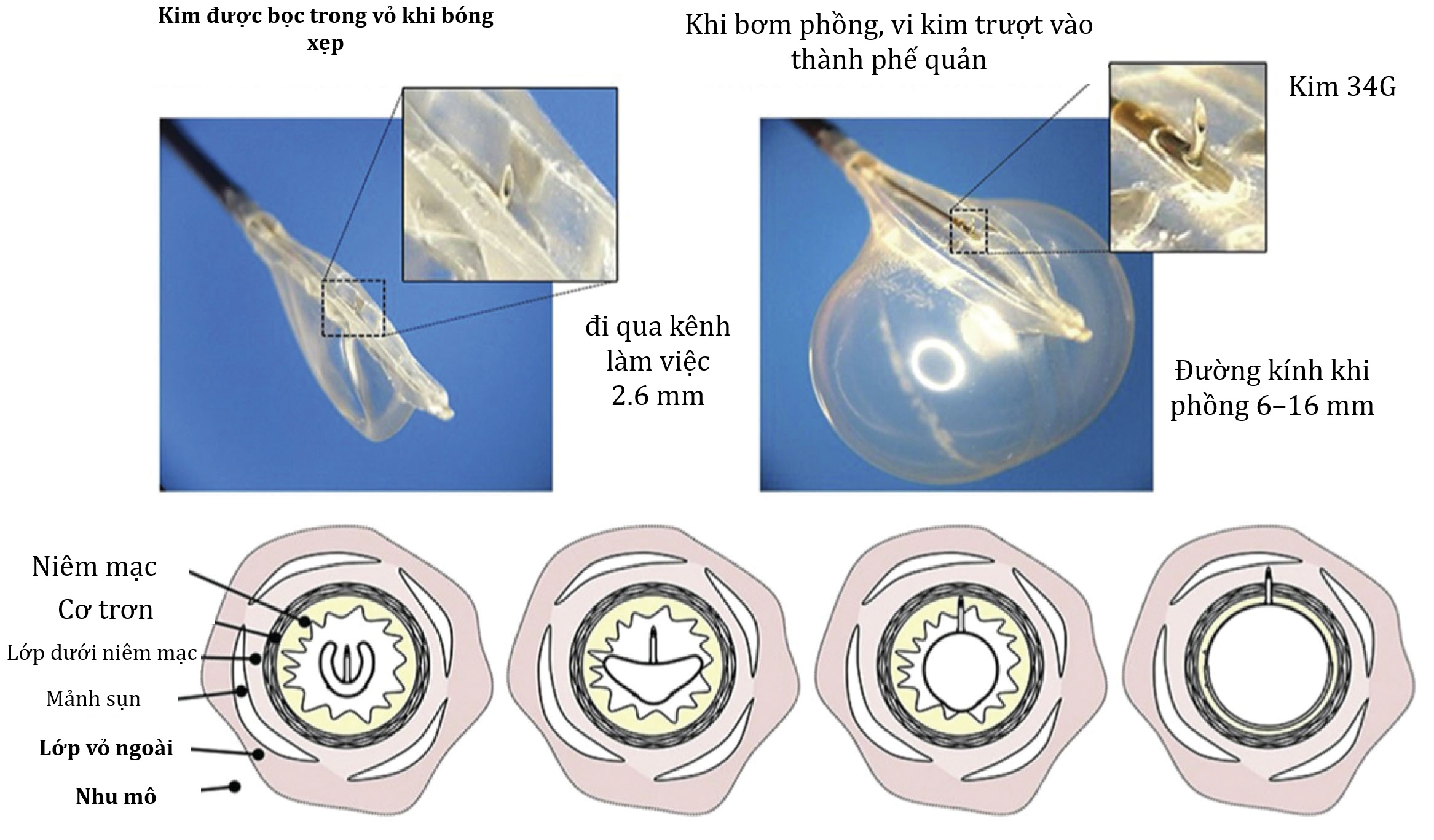
Hình 11.2 Catheter Blowfish với bóng xẹp và bóng phồng. Nguồn: Yarmus L, Mallow C, Akulian J, et al. Prospective multicentered safety and feasibility pilot for endobronchial intratumoral chemotherapy. Chest. 2019;156:562-570.
Catheter này đã được nghiên cứu trong một thử nghiệm thí điểm đa trung tâm về tính an toàn và khả thi trên người, xem xét hiệu quả của việc tiêm một liều tích lũy 1,5 mg paclitaxel ở 19 bệnh nhân NSCLC và tắc nghẽn đường thở trung tâm do ác tính (Hình 11.3). Tất cả bệnh nhân đều được nội soi phế quản ống cứng để tái thông đường thở và tiêm thành công paclitaxel bằng catheter vi tiêm Blowfish. Điều này yêu cầu trung bình 3,4 lần tiêm cho mỗi bệnh nhân. Các tác giả ghi nhận tình trạng hẹp đường thở giảm đáng kể sau can thiệp và không báo cáo biến cố bất lợi đáng kể nào. Không có bệnh nhân nào trong nghiên cứu cần can thiệp thêm trong giai đoạn theo dõi 6 tuần. Không có bệnh nhân nào cần đặt stent đường thở.
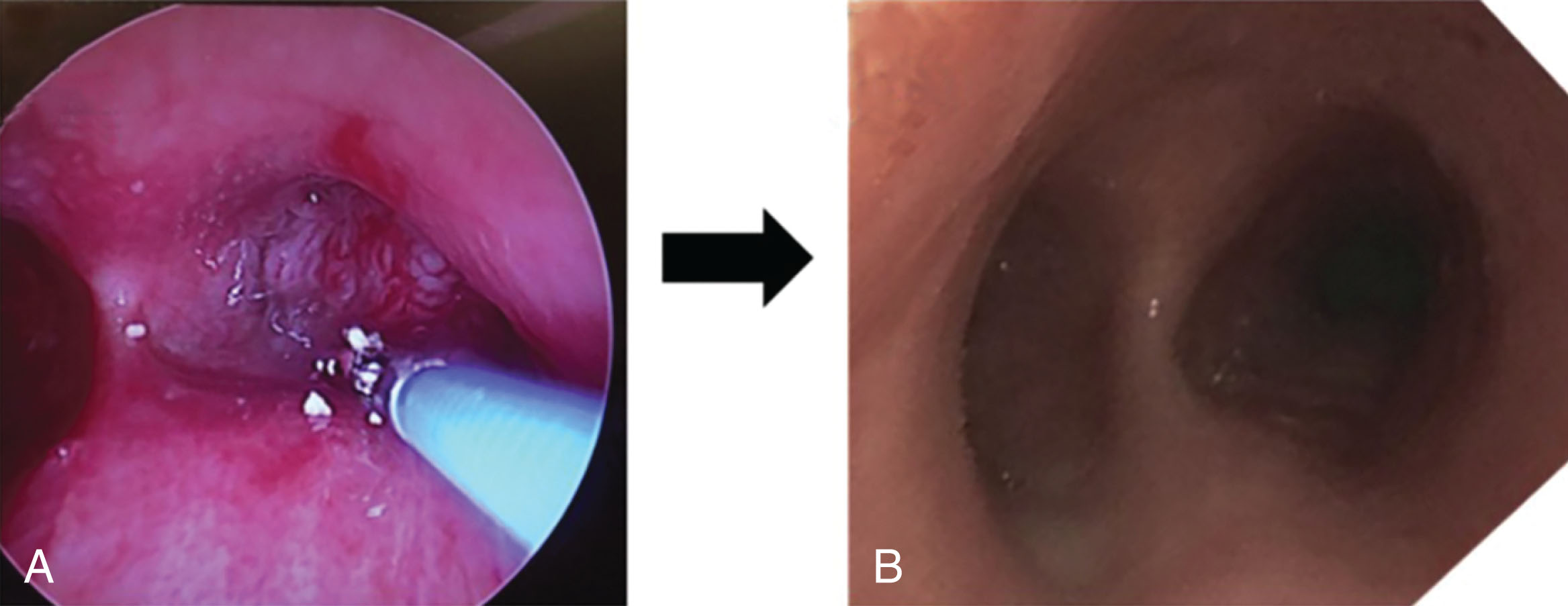
Hình 11.3 (A) Tắc nghẽn 100% phế quản gốc phải do tắc nghẽn đường thở ác tính. (B) Phế quản gốc phải thông thoáng 6 tuần sau khi tiêm paclitaxel. Nguồn: Yarmus L, Mallow C, Akulian J, et al. Prospective multicentered safety and feasibility pilot for endobronchial intratumoral chemotherapy. Chest. 2019;156:562-570.
Liệu pháp gen
Có những nghiên cứu rất sớm và sơ bộ về liệu pháp gen ức chế khối u được đưa vào qua TBNI. Bất thường di truyền phổ biến nhất liên quan đến ung thư phổi là đột biến gen ức chế khối u p53. Vào những năm 1990, Roth và cộng sự đã sử dụng TBNI để đưa các bản sao p53 loại hoang dã thông qua một vector retrovirus vào các tổn thương trong lòng phế quản của bốn bệnh nhân NSCLC tái phát. Các tác giả đã báo cáo sự thoái triển của khối u ở ba bệnh nhân trong các lần kiểm tra nội soi phế quản sau đó, với sinh thiết theo dõi không cho thấy khối u còn sống (mặc dù bệnh nhân đã có sự tiến triển của bệnh ở nơi khác). Gần đây hơn, nhiều nghiên cứu đã được thực hiện bằng cách sử dụng các vector adenovirus tái tổ hợp. Weill và cộng sự đã đưa gen p53 qua trung gian adenovirus (Adp53) thông qua TBNI cho 12 bệnh nhân NSCLC trong lòng phế quản có liên quan đến đột biến p53 đã biết; họ ghi nhận sự cải thiện đáng kể về tắc nghẽn đường thở ở một nửa số bệnh nhân. Các tác giả báo cáo độc tính tối thiểu liên quan đến liệu pháp. Điều quan trọng cần lưu ý là trong nhóm này, 5 trong số 12 bệnh nhân chỉ nhận Adp53, trong khi 7 người nhận Adp53 kết hợp với cisplatin; trong các phân nhóm này, chỉ có một trong những bệnh nhân nhận Adp53 đơn độc có sự cải thiện đáng kể về tắc nghẽn trong lòng phế quản, trong khi 5 trong số 7 người trong nhóm Adp53/cisplatin có sự cải thiện. Một nghiên cứu bổ sung đã xem xét việc sử dụng đồng thời Adp53 và cisplatin ở 24 bệnh nhân NSCLC; 17 bệnh nhân có sự biến mất của các tổn thương trong lòng phế quản sau điều trị trong ít nhất 4 tuần dựa trên hình ảnh và/hoặc khám thực thể, trong khi 2 bệnh nhân cho thấy đáp ứng một phần.
Ngoài cisplatin, các liệu pháp khác đã được sử dụng cùng với p53. Schuler và cộng sự đã nghiên cứu việc sử dụng đồng thời tiêm nội u gen p53 loại hoang dã qua trung gian adenovirus với carboplatin/paclitaxel hoặc cisplatin/vinorelbine. Cuối cùng, các tác giả không phát hiện sự khác biệt về tỷ lệ đáp ứng giữa những người nhận hóa trị và p53 so với những người chỉ nhận hóa trị. Tuy nhiên, họ ghi nhận rằng sự thoái triển khối u tại chỗ dường như có ý nghĩa hơn ở những người nhận cisplatin/vinorelbine và p53 so với những người nhận carboplatin/paclitaxel và p53.
Tác động của việc tiêm gen ức chế khối u cũng đã được xem xét trong bối cảnh xạ trị. Swisher và cộng sự đã nghiên cứu các bệnh nhân NSCLC không di căn không đủ điều kiện để hóa trị hoặc can thiệp phẫu thuật. Bệnh nhân được tiêm nội u Adp53 trong bối cảnh cũng đang được xạ trị (ở mức 60 Gy) trong 6 tuần. Sau vài tháng, sinh thiết của 12 trong số 19 bệnh nhân cho thấy không còn khối u sống.
Tất cả các nghiên cứu này đều khá sơ bộ và thiếu cỡ mẫu để chứng minh hoặc bác bỏ hiệu quả của các tác nhân khác nhau được đưa vào qua nội soi phế quản. Do đó, dữ liệu nên được xem là mang tính thăm dò, với trọng tâm chính ở đây là nội soi phế quản như một nền tảng để đưa thuốc và các tác nhân điều trị khác đang bắt đầu được khám phá. Trong bối cảnh này, điều quan trọng là bác sĩ nội soi can thiệp phải hiểu dữ liệu có sẵn, những hạn chế của dữ liệu này và các khía cạnh thủ thuật của việc đưa thuốc qua nội soi phế quản trong trường hợp cần thiết.
BỆNH LÝ LỒNG NGỰC KHÔNG ÁC TÍNH
Hẹp thanh-khí quản sau đặt nội khí quản hoặc mở khí quản
Ngoài ung thư phổi, có một loạt các bệnh lý tập trung vào đường thở không ác tính có thể được hưởng lợi từ các loại thuốc được sử dụng qua nội soi phế quản. Một trong những rối loạn đó, hẹp thanh-khí quản lành tính, thường thấy nhất ở những bệnh nhân trước đây đã cần đặt nội khí quản và/hoặc mở khí quản trong một thời gian dài (thường hơn 7-10 ngày). Các yếu tố nguy cơ khác để phát triển hẹp thanh-khí quản bao gồm tiền sử đặt nội khí quản khó hoặc cấp cứu, đặt ống nội khí quản quá lớn, hoặc áp lực bóng chèn quá cao. Các triệu chứng của hẹp thanh-khí quản có thể mất vài tuần đến vài tháng sau khi rút ống nội khí quản hoặc rút canuyn mở khí quản để biểu hiện. Bệnh nhân thường phàn nàn về tình trạng khó thở bán cấp, tiến triển, cũng như thở khò khè không đáp ứng với điều trị bằng thuốc giãn phế quản. Hẹp thanh-khí quản có thể được phân loại thành hẹp đơn giản và hẹp phức tạp. Các tổn thương đơn giản được định nghĩa là những tổn thương ảnh hưởng đến một vùng ngắn (dài dưới 1 cm) của đường thở mà không có bằng chứng về nhuyễn khí quản. Ngược lại, các tổn thương phức tạp là những tổn thương liên quan đến các khu vực hẹp rộng (dài hơn 1 cm) và/hoặc có sự tham gia của sụn và nhuyễn khí quản. Hẹp đơn giản thường có thể được can thiệp bằng nội soi phế quản, thường bao gồm rạch theo hình nan hoa (ví dụ, bằng dao điện) sau đó nong bóng. Hẹp phức tạp có thể cần nhiều lần can thiệp lặp đi lặp lại bao gồm đặt stent đường thở, đông huyết tương argon, liệu pháp lạnh, nong bóng, hoặc cuối cùng là phẫu thuật cắt bỏ.
Gần đây, việc sử dụng mitomycin C trong quản lý hẹp thanh-khí quản lành tính đang ngày càng phổ biến. Mitomycin C là một tác nhân chống tân sinh có nguồn gốc từ Streptomyces caespitosus. Nó đã được sử dụng trong lịch sử để điều trị một loạt các bệnh ung thư, bao gồm ung thư vú, ung thư đại trực tràng, ung thư dạ dày và NSCLC, và việc sử dụng nó như một tác nhân chống tăng sinh trong điều trị các bệnh như bệnh tăng nhãn áp (glôcôm) đã được xác lập rõ ràng trong y văn nhãn khoa. Dalar và cộng sự đã báo cáo về việc sử dụng mitomycin C 0,2 mg/mL tại chỗ ở một số ít bệnh nhân bị hẹp khí quản đơn giản và phức tạp (Hình 11.4). Các tác giả ghi nhận rằng mitomycin dường như làm trì hoãn thời gian giữa các lần nong stent liên tiếp ở bệnh nhân bị hẹp phức tạp và giảm nhu cầu nong lặp lại ở bệnh nhân bị hẹp đơn giản. Mặc dù chưa có thử nghiệm ngẫu nhiên có đối chứng nào nghiên cứu tác động của mitomycin C đối với tình trạng này, Perepelitsyn và Shapshay đã thực hiện một nghiên cứu đoàn hệ hồi cứu so sánh hiệu quả của việc rạch bằng laser carbon dioxide kết hợp với chỉ nong bằng nội soi phế quản so với tiêm steroid so với bôi mitomycin C tại chỗ. Họ báo cáo sự cải thiện triệu chứng ở nhóm nhận mitomycin C tại chỗ. Cũng có một số dữ liệu cho thấy rằng hai lần bôi mitomycin C, cách nhau khoảng 1 tháng, có thể giúp trì hoãn (nhưng không ngăn chặn) các đợt tái hẹp. Cần phải thực hiện thêm nghiên cứu để khám phá sâu hơn những kết quả này và xác định tần suất dùng thuốc tối ưu của mitomycin C tại chỗ ở những bệnh nhân này.
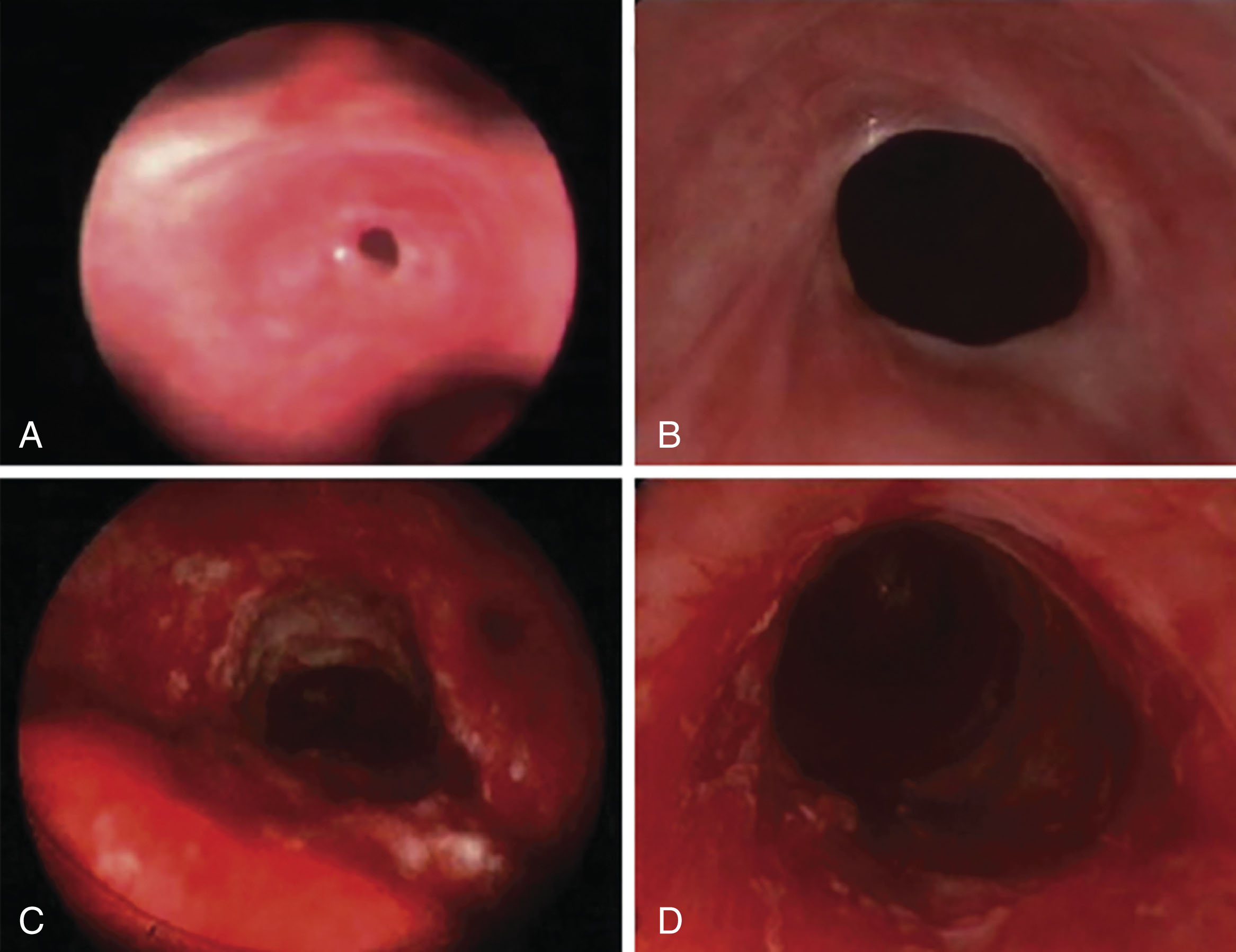
Hình 11.4 Hẹp khí quản sau đặt nội khí quản (A) và phóng to (B), trước khi can thiệp nội soi phế quản. Cùng một khí quản được quan sát lại (C) và phóng to (D) sau ba lần điều trị bằng mitomycin tại chỗ. Nguồn: Dalar L, Karasulu L, Abul Y, et al. Bronchoscopic treatment in the management of benign tracheal stenosis: choices for simple and complex tracheal stenosis. Ann Thorac Surg. 2016;101:1310-1317
Bệnh u hạt kèm viêm đa mạch
Bệnh u hạt kèm viêm đa mạch (GPA, trước đây là bệnh u hạt Wegener) là một dạng viêm mạch liên quan đến kháng thể kháng bào tương bạch cầu trung tính (ANCA) ở các mạch máu nhỏ. Theo Hội Thấp khớp học Hoa Kỳ, có bốn tiêu chí được sử dụng để chẩn đoán bệnh:
- Cặn lắng nước tiểu bất thường
- Phát hiện bất thường trên hình ảnh ngực
- Sự hiện diện của loét miệng hoặc chảy dịch mũi
- Sự hiện diện của u hạt trên sinh thiết.
Từ góc độ phổi, GPA có thể có nhiều biểu hiện đa dạng, bao gồm các nốt phổi (có thể dạng hang), tổn thương dạng kính mờ trong bối cảnh chảy máu phế nang, hẹp đường thở và loét niêm mạc. Bệnh thường được quản lý bằng liệu pháp ức chế miễn dịch toàn thân và tránh các thao tác trên đường thở, vì điều này có thể dẫn đến tình trạng viêm nặng hơn và hẹp thêm trong tương lai. Tuy nhiên, tổn thương đường thở trung tâm có thể là rối loạn chính ở một tỷ lệ nhỏ bệnh nhân và có thể tiến triển ngay cả khi được điều trị toàn thân thích hợp; tình huống này có thể cần can thiệp nội soi.
Tổn thương đường hô hấp trên tương đối phổ biến trong GPA, đặc biệt liên quan đến vùng hạ thanh môn của khí quản. Thật vậy, 16% bệnh nhân có bệnh đang hoạt động phát triển hẹp hạ thanh môn, có thể đe dọa tính mạng. Nhiều nghiên cứu đã đề xuất vai trò của việc tiêm glucocorticoid qua nội soi, được thực hiện kết hợp với nong bằng nội soi phế quản. Ngoài ra, nghiên cứu trước đây đã chứng minh rằng bệnh nhân có thể phát triển hẹp hạ thanh môn trong khi đang được ức chế miễn dịch toàn thân, cho thấy liệu pháp ức chế miễn dịch không phải lúc nào cũng đủ để ngăn ngừa/quản lý biến chứng này. Hoffman và cộng sự đã thực hiện tiêm corticosteroid tác dụng kéo dài nội tổn thương và nong ở 21 bệnh nhân GPA có biến chứng hẹp hạ thanh môn. Trong nghiên cứu này, 40 mg/mL methylprednisolone acetate đã được tiêm vào lớp dưới niêm mạc của vùng hẹp bằng kim thanh quản 20-G theo phân bố bốn góc phần tư. Họ ghi nhận rằng những bệnh nhân không có sẹo đường thở trước đó cần trung bình 2,4 thủ thuật cách nhau khoảng 12 tháng để duy trì sự thông thoáng của vùng hạ thanh môn. Ngược lại, những bệnh nhân có bằng chứng sẹo đường thở (từ các thủ thuật trước đó) cần trung bình 4,1 thủ thuật cách nhau khoảng 7 tháng để duy trì sự thông thoáng của vùng. Dựa trên những phát hiện của họ, các tác giả đề nghị rằng tiêm steroid và nong là một phương thức điều trị hợp lý cho những bệnh nhân bị hẹp hạ thanh môn và GPA không đáp ứng với điều trị toàn thân.
Bệnh Sarcoidosis
Sarcoidosis là một bệnh đa hệ thống được đặc trưng bởi sự hiện diện của các u hạt không hoại tử bã đậu. Mặc dù các biểu hiện của sarcoidosis có thể thay đổi đáng kể dựa trên các hệ cơ quan bị ảnh hưởng, hệ hô hấp bị ảnh hưởng trong hơn 90% các trường hợp. Các biểu hiện ở phổi của sarcoidosis bao gồm bệnh lý hạch rốn phổi hai bên, các vi nốt ở phổi, tổn thương dạng kính mờ, và trong bệnh tiến triển là xơ hóa. Tổn thương đường thở của bệnh thường là dấu hiệu của sự hiện diện của các u hạt niêm mạc nội phế quản, gây ra sẹo và hẹp. Sự thu hẹp đường thở kết quả có thể được phát hiện trên X-quang và nội soi phế quản và thường dẫn đến các triệu chứng khó thở và thở khò khè. Trên hình ảnh, tổn thương lan rộng của các đường thở nhỏ có thể dẫn đến bằng chứng về bẫy khí trên phim chụp thì thở ra.
Corticosteroid là một trong những liệu pháp được sử dụng phổ biến nhất cho sarcoidosis đang hoạt động. Khi tổn thương đường thở trong lòng phế quản xảy ra trong sarcoidosis, việc tiêm corticosteroid trong lòng đường thở (bao gồm dexamethasone và triamcinolone) có thể có lợi, mặc dù dữ liệu về hiệu quả còn hạn chế. Butler và cộng sự đã thực hiện một tổng quan biểu đồ hồi cứu của 10 bệnh nhân có tổn thương thanh quản do sarcoidosis. Trong số những bệnh nhân này, sáu người có sarcoidosis giới hạn ở thanh quản, trong khi bốn người có các biểu hiện toàn thân khác; hai bệnh nhân có triệu chứng nặng đến mức họ cần mở khí quản cấp cứu. Tất cả đều đã nhận liều cao corticosteroid toàn thân trước khi can thiệp. Bệnh nhân đã trải qua nhiều lần tiêm steroid vào đáy của mỗi tổn thương, sử dụng 40-120 mg methylprednisolone acetate 40 mg/mL, cũng như giảm quang đông bằng laser carbon dioxide. Họ đã hoàn thành từ một đến bốn buổi. Các tác giả báo cáo sự cải thiện đáng kể trong thang điểm khó thở của Hội đồng Nghiên cứu Y khoa (MRC) của bệnh nhân sau điều trị, cũng như giảm đáng kể việc sử dụng steroid toàn thân.
Cũng có thể có vai trò của mitomycin C tại chỗ trong việc quản lý sarcoidosis của đường thở. Trong một báo cáo ca bệnh mô tả một phụ nữ bị tổn thương nội phế quản do sarcoidosis đã thất bại với liệu pháp steroid toàn thân, nong bóng và bôi mitomycin C 0,4 mg/mL tại chỗ đã dẫn đến sự cải thiện tạm thời các triệu chứng của bệnh nhân. Cần phải thực hiện thêm nghiên cứu về vai trò tiềm năng của mitomycin C trong việc quản lý sarcoidosis liên quan đến đường thở.
Hẹp thanh-khí quản vô căn
Hẹp thanh-khí quản vô căn là một rối loạn viêm hiếm gặp gần như chỉ ảnh hưởng đến phụ nữ, điển hình là những người ở độ tuổi tiền mãn kinh và quanh mãn kinh. Bệnh nhân thường có biểu hiện khó thở khi gắng sức, thở khò khè, và đôi khi, thay đổi chất lượng giọng nói. Như tên gọi của nó, hẹp thanh-khí quản vô căn là một chẩn đoán loại trừ. Do đó, nhà cung cấp dịch vụ y tế có nhiệm vụ loại trừ các quá trình nhiễm trùng, chấn thương và thấp khớp để đưa ra chẩn đoán. Gần đây, các rối loạn về estrogen và progesterone, như có thể thấy tại thời điểm mãn kinh, đã được nghiên cứu như những yếu tố có thể góp phần vào cơ chế bệnh sinh của rối loạn này.
Hẹp thanh-khí quản vô căn được đặc trưng bởi hẹp trong đường thở trên, thường ảnh hưởng đến vùng hạ thanh môn. Về mặt mô bệnh học, có bằng chứng về viêm xơ trong lớp đệm của vùng hạ thanh môn và khí quản gần. Theo truyền thống, rối loạn này đã được quản lý bằng phẫu thuật, với việc cắt và tái tạo thanh-khí quản hoặc khí quản. Kết quả với phương pháp phẫu thuật này đã thuận lợi. Một nghiên cứu đã mô tả 73 bệnh nhân đã trải qua can thiệp phẫu thuật cho hẹp thanh-khí quản vô căn; trong nhóm này, 19 bệnh nhân không mô tả khó khăn nào trong việc thở hoặc chất lượng giọng nói sau phẫu thuật, 47 người báo cáo một số khó khăn trong việc nói to sau phẫu thuật, 5 người báo cáo một số khó thở hoặc thở rít liên tục, và 1 người cần quản lý liên tục bằng nong.
Mặc dù hiệu quả của phẫu thuật, ngày càng có nhiều sự quan tâm đến vai trò của nội soi phế quản trong việc quản lý rối loạn này, vì việc cắt bỏ phẫu thuật rộng rãi có thể không được một bộ phận lớn bệnh nhân mắc bệnh này dung nạp do các bệnh đi kèm. Tương tự như hẹp thanh-khí quản lành tính, các can thiệp nội soi phế quản cho hẹp vô căn bao gồm nong bóng, laser cũng như các liệu pháp nhiệt-đốt khác, đặt stent và liệu pháp lạnh. Shabani và cộng sự đã thử nong bóng nội soi và tiêm steroid ở 37 bệnh nhân bị hẹp hạ thanh môn do hẹp thanh-khí quản vô căn. Trong số 37 bệnh nhân, 13 người đã nhận tiêm steroid (triamcinolone hoặc dexamethasone) cho tất cả các thủ thuật, trong khi 4 người không nhận tiêm steroid đồng thời. Mặc dù kết quả không đạt được ý nghĩa thống kê, các tác giả ghi nhận rằng những bệnh nhân nhận tiêm steroid có xu hướng cần ít lần nong hơn (trung bình, khoảng 4 so với 7) với thời gian dài hơn giữa các lần nong (trung bình, khoảng 556 ngày so với 283 ngày) so với những người không nhận tiêm steroid. Với cỡ mẫu nhỏ, cần phải thực hiện thêm nghiên cứu để xác định tính hữu dụng của việc tiêm steroid đồng thời, cũng như thời điểm tối ưu của các phương pháp điều trị này.
U nhú đường hô hấp tái phát
U nhú đường hô hấp tái phát (RRP) là một rối loạn lành tính được đặc trưng bởi sự phát triển của nhiều tổn thương dạng nhú, dạng sùi khắp đường hô hấp. Rất hiếm khi có thể có tổn thương nhu mô của RRP, được đặc trưng bởi sự hiện diện của các nốt phổi đặc hoặc dạng hang. Bệnh được cho là do nhiễm virus u nhú ở người (HPV), phổ biến nhất là các phân týp 6 và 11, chiếm hơn 90% các trường hợp RRP. Có sự đồng thuận chung rằng HPV 11 đại diện cho chủng độc lực cao hơn, vì những bệnh nhân mắc RRP do HPV 11 thường là những người cần các can thiệp đường thở tích cực hơn (bao gồm cả mở khí quản) và có nguy cơ chuyển dạng ác tính cao hơn. RRP có thể ảnh hưởng đến trẻ em, những người thường nhiễm HPV tại thời điểm sinh qua đường sinh dục âm đạo, mặc dù có bằng chứng cho thấy một số trẻ bị nhiễm qua lây truyền qua nhau thai. Người lớn cũng có thể nhiễm HPV và phát triển RRP sau khi quan hệ tình dục bằng miệng.
Phương pháp quản lý truyền thống của RRP đã tập trung vào việc phẫu thuật giảm kích thước khối u nhú, thường sử dụng liệu pháp laser, để phục hồi sự thông thoáng của đường thở. Tuy nhiên, do tính chất tái phát của bệnh, có thể cần phải phẫu thuật thường xuyên, khiến bệnh nhân (thường là trẻ em) có nguy cơ bị hẹp và sẹo thanh-khí quản, bỏng và hình thành lỗ rò. Do đó, đã có sự tập trung ngày càng tăng vào các liệu pháp bổ trợ nhằm giảm thiểu nhu cầu can thiệp phẫu thuật lặp đi lặp lại. Việc sử dụng cidofovir nội tổn thương đã được đánh giá như một can thiệp tiềm năng để giảm thiểu nhu cầu thực hiện các thủ thuật xâm lấn ở nhóm dân số này. Cidofovir là một loại thuốc kháng virus ức chế DNA polymerase của virus. Phần lớn dữ liệu mô tả việc sử dụng cidofovir đến từ các báo cáo ca bệnh, với các mô tả khác nhau về hiệu quả của thuốc. Wierzbicka và cộng sự ghi nhận sự lui bệnh hoàn toàn ở 18 trong số 32 bệnh nhân mắc bệnh u nhú tái phát đã được tiêm cidofovir nội tổn thương (từ tổng số một đến bảy lần tiêm, sử dụng tổng cộng 2-33 mL cidofovir 5 mg/mL); điều quan trọng là các tác giả báo cáo rằng một bệnh nhân đã phát triển các triệu chứng tiêu hóa sau thủ thuật, trong khi hai người khác bị tăng men gan thoáng qua. Naiman và cộng sự đã thực hiện tiêm nội tổn thương hàng tháng 5 mg/mL cidofovir ở 26 bệnh nhân (bao gồm cả người lớn và trẻ em). Nội soi lặp lại được thực hiện sau 3 tháng để đánh giá gánh nặng bệnh tật đang diễn ra và, nếu có, việc tiêm cidofovir được lặp lại vào thời điểm đó trên các u nhú còn sót lại. Các tác giả báo cáo sự lui bệnh hoàn toàn ở tám bệnh nhân (trong đó 2 người đã trải qua 1 lần tiêm, 2 người có 2 lần tiêm, và 4 người có trung bình 4,2 lần tiêm). Mười bảy bệnh nhân có bệnh nhẹ vào cuối thử nghiệm điều trị. Các tác giả không ghi nhận bất kỳ biến cố bất lợi đáng kể nào.
Hiện tại có dữ liệu hạn chế mô tả hiệu quả lâu dài của việc tiêm cidofovir để quản lý RRP. Milczuk đã theo dõi bốn trẻ em mắc RRP, mỗi trẻ đã trải qua sáu lần điều trị, cách nhau 6-8 tuần, bao gồm cắt bỏ u nhú bằng phẫu thuật và tiêm cidofovir nội tổn thương. Một năm sau khi hoàn thành điều trị, một bệnh nhân tiếp tục lui bệnh, trong khi hai bệnh nhân bị tái phát triệu chứng (bắt đầu tái phát trong quá trình điều trị ban đầu). Bệnh nhân thứ tư không đáp ứng với tiêm cidofovir. Tanna và cộng sự đã theo dõi 13 người lớn trước đây đã lui bệnh sau trung bình sáu lần tiêm cidofovir, báo cáo rằng 6 người không cần can thiệp sau đó, trong khi 7 người cần điều trị thêm RRP của họ sau trung bình 1 năm. Cần phải thực hiện thêm nghiên cứu để xác định hiệu quả lâu dài của việc tiêm cidofovir nội tổn thương.
Hẹp phế quản liên quan đến ghép phổi
Mặc dù có những cải tiến trong kỹ thuật phẫu thuật trong vài thập kỷ qua, các biến chứng đường thở vẫn là một biến chứng tương đối phổ biến của ghép phổi, với khoảng 15% người nhận ghép phổi bị ảnh hưởng. Các biến chứng đường thở có thể có những tác động to lớn đến chất lượng cuộc sống của bệnh nhân, thường gây ra ho, khó thở tiến triển và/hoặc nhiễm trùng tái phát. Những biến chứng này thường đòi hỏi nhiều can thiệp sau ghép tùy thuộc vào nguyên nhân cơ bản của biến chứng. Có rất nhiều biến chứng đường thở, bao gồm hoại tử và bục miệng nối, nhiễm trùng miệng nối, rò (phế quản-màng phổi, phế quản-mạch máu, hoặc phế quản-trung thất), và phổ biến nhất là hẹp phế quản. Hẹp phế quản có thể xảy ra tại hoặc xa vị trí miệng nối và có thể phát triển từ vài tháng đến nhiều năm sau khi ghép. Theo một bài tổng quan của Yousem và cộng sự, các nghiên cứu mô bệnh học về sụn phế quản ở người nhận sau ghép cho thấy sự cốt hóa, vôi hóa và sự phát triển của mô xơ-mạch, có lẽ là do (ít nhất một phần) viêm và giảm tưới máu phế quản sau khi ghép.
Việc quản lý hẹp phế quản sau ghép bằng nội soi phế quản bao gồm một loạt các can thiệp nhằm nong rộng đường thở. Trong lịch sử, nội soi phế quản ống cứng với nong bằng que nong (bougie) là phương thức điều trị tiêu chuẩn, mặc dù nội soi phế quản ống mềm với nong bóng đã trở nên ngày càng phổ biến trong những năm gần đây. Các can thiệp khác bao gồm đặt stent đường thở, liệu pháp lạnh, dao điện, liệu pháp laser và xạ trị áp sát nội phế quản. Cũng có dữ liệu hỗ trợ việc bôi các tác nhân tại chỗ qua nội soi phế quản, đáng chú ý nhất là mitomycin C, vào các vùng bị ảnh hưởng bởi hẹp phế quản. Erard và cộng sự đã công bố báo cáo ca bệnh đầu tiên mô tả việc bôi mitomycin C tại chỗ trong hẹp phế quản tái phát vào năm 2001 (Hình 11.5). Họ mô tả một bệnh nhân có tiền sử xơ nang và nhiễm Burkholderia cepacia đa kháng thuốc đã trải qua ghép phổi hai bên bị biến chứng hẹp phế quản tái phát mặc dù đã được điều trị bằng đông điện bằng laser argon và nhiều lần cố gắng nong và đặt stent. Vào tuần thứ 42 sau phẫu thuật, các tác giả đã bôi một miếng gạc bông tẩm dung dịch mitomycin C 2 mg/mL lên mô hạt trong phế quản thùy trên phải và phế quản trung gian bị hẹp của bệnh nhân trong 2 phút. Họ báo cáo sự cải thiện thể tích thở ra gắng sức trong giây đầu tiên (FEV₁) của bệnh nhân kéo dài trong vài tháng, mặc dù họ ghi nhận rằng bệnh nhân đã phát triển một chỗ hẹp tái phát trong phế quản trung gian, được điều trị lại bằng mitomycin C tại chỗ với hiệu quả tốt.
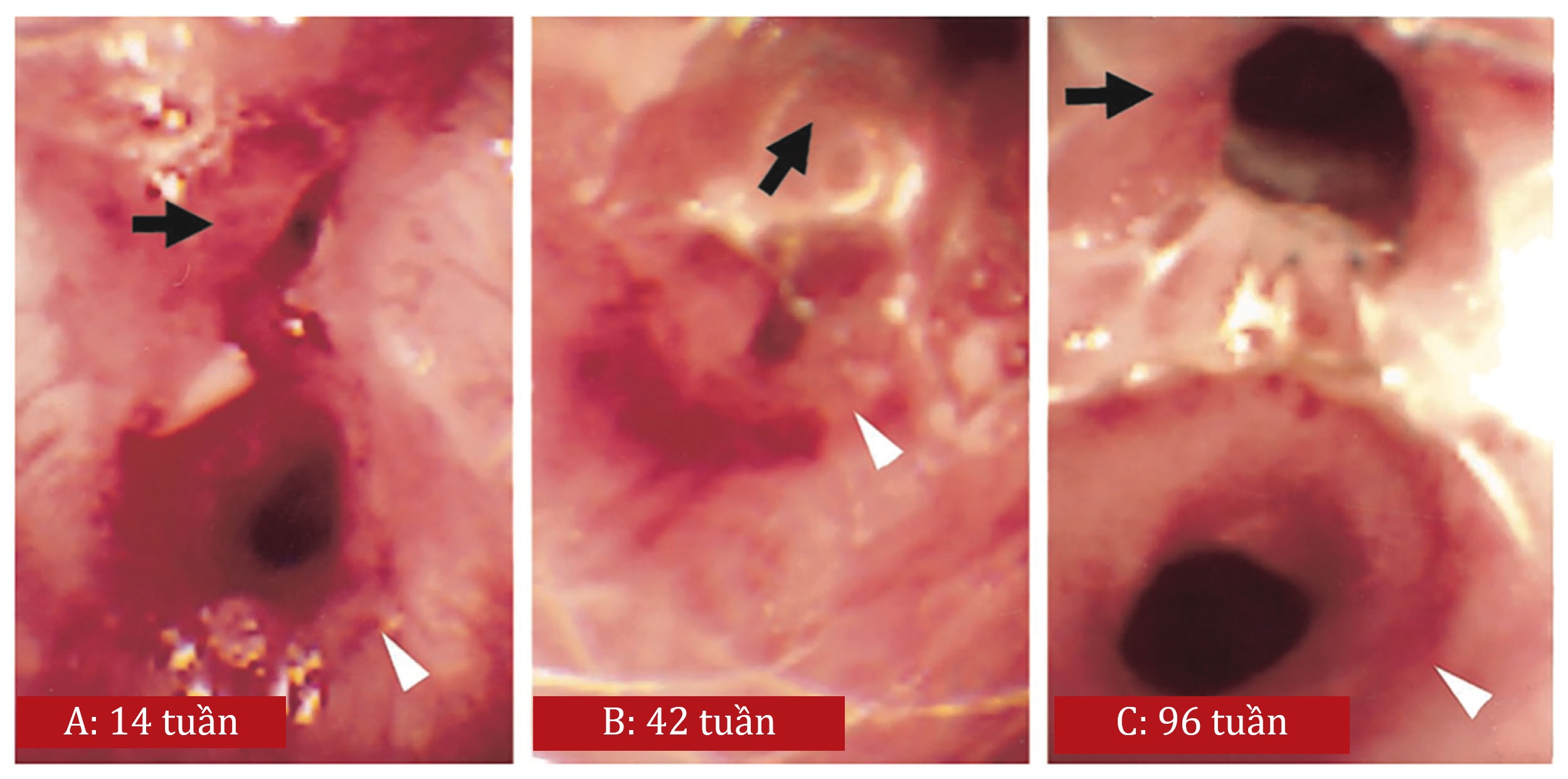
Hình 11.5 Hẹp phế quản ở một bệnh nhân ghép phổi. (A) Hẹp phế quản thùy trên phải và phế quản trung gian 14 tuần sau ghép; (B) 42 tuần sau ghép, sau khi đặt stent vào phế quản thùy trên phải; (C) 96 tuần sau ghép, sau khi bôi mitomycin C tại chỗ. Nguồn: Erard AC, Monnier P, Spiliopoulos A, Nicod L. Mitomycin C for control of recurrent bronchial stenosis: a case report. Chest. 2001 120:2103-2105.
Một nghiên cứu đoàn hệ hồi cứu gần đây từ Đại học Duke đã đánh giá các bệnh nhân sau ghép bị hẹp phế quản được tiêm mitomycin C dưới niêm mạc vào đường thở bị hẹp. Nghiên cứu bao gồm 11 bệnh nhân đã trải qua ghép phổi bị biến chứng hẹp đường thở tái phát mặc dù đã nong bóng và/hoặc đặt stent đường thở. Bệnh nhân đã được nội soi phế quản với tạo hình phế quản bằng bóng, sau đó 5 mL dung dịch mitomycin C 0,4 mg/mL được tiêm dưới niêm mạc bằng kim 21-G. Để xác định tác động của việc tiêm mitomycin C, các tác giả đã so sánh số lần nong đường thở được thực hiện trong những tháng trước can thiệp và trong những tháng sau liệu pháp này. Họ báo cáo rằng trung bình ba lần nong đã được thực hiện cho mỗi bệnh nhân trong 6 tháng trước can thiệp, so với hai lần nong trong 6 tháng tiếp theo. Các tác giả cũng mô tả những cải thiện không đáng kể về giá trị FEV₁ và dung tích sống gắng sức (FVC) của bệnh nhân và ghi nhận rằng việc tiêm được dung nạp tốt.
SỬ DỤNG THUỐC QUA NỘI SOI VÀ LỰA CHỌN KỸ THUẬT
Việc sử dụng thuốc qua nội soi có thể được thực hiện bằng bốn kỹ thuật chung:
|
Bôi thuốc tại chỗ nói chung là kỹ thuật ít xâm lấn nhất trong số các kỹ thuật này và ít có khả năng gây thâm nhập sâu; do đó, thường có ít biến chứng liên quan đến kỹ thuật này hơn. Việc bôi thuốc tại chỗ có thể được thực hiện bằng cách ngâm miếng gạc nhỏ trong thuốc mong muốn, kẹp miếng gạc bằng kẹp cứng, và cuối cùng, đặt miếng gạc đã ngâm lên tổn thương đường thở trung tâm. Thời gian cần thiết để áp miếng gạc thay đổi từ 30 giây đến vài phút, tùy thuộc vào chỉ định. Lượng thuốc được hấp thụ vào niêm mạc sẽ thay đổi tùy thuộc vào nồng độ của dung dịch mà miếng gạc được ngâm, thời gian miếng gạc được giữ trên niêm mạc, và số lần bôi. Cần lưu ý rằng kỹ thuật này cũng có thể được thực hiện bằng cách kẹp miếng gạc bằng kẹp mềm qua ống nội soi phế quản, mặc dù điều này thường dẫn đến sự áp sát của miếng gạc vào đường thở kém mạnh hơn và do đó, nồng độ hấp thụ thuốc thấp hơn.
Trái ngược với bôi tại chỗ, thuốc cũng có thể được tiêm qua nội soi. Việc tiêm các tác nhân qua nội soi có thể được thực hiện dưới quan sát trực tiếp qua kim TBNA hoặc sử dụng hướng dẫn siêu âm qua kim EBUS-TBNA. Tiêm trực tiếp bằng kim TBNA tiêu chuẩn có thể được thực hiện dễ dàng bằng ống nội soi phế quản mềm và nên được xem xét ở những bệnh nhân có tổn thương lan vào lòng đường thở trung tâm và/hoặc gây tắc nghẽn hoàn toàn đường thở. Ngược lại, EBUS-TBNA được ưu tiên cho các khối u trung thất không nhìn thấy được trong các đường thở trung tâm. Tuy nhiên, cả hai phương thức điều trị này vẫn còn mang tính thử nghiệm, vì thể tích, nồng độ và loại thuốc hiệu quả nhất vẫn chưa được biết.
Cuối cùng, thuốc cũng có thể được sử dụng bằng catheter bóng nội phế quản mềm (Blowfish), được mô tả ở phần đầu của chương này. Thiết bị này bao gồm một catheter hai lòng được đưa qua ống nội soi phế quản mềm với bóng xẹp và kim được bọc lại. Một lòng bơm phồng một quả bóng nội phế quản ở đầu catheter, sau đó đẩy ra một kim 34-G vuông góc. Kim này sau đó được đưa vào lớp dưới niêm mạc. Khi bóng được bơm phồng hoàn toàn, thuốc được đưa xuống lòng thứ hai qua kim. Nói chung, bốn lần tiêm được hoàn thành theo kiểu chu vi. Thuốc cản quang có thể được trộn với thuốc đang được tiêm nhằm theo dõi mức độ thoát mạch của thuốc vào lớp dưới niêm mạc, mặc dù điều này không hoàn toàn cần thiết.
TÓM TẮT
| Chương này cung cấp một cái nhìn tổng quan ngắn gọn về các cách mà một loạt các bệnh lý phổi có thể được quản lý thông qua việc sử dụng thuốc qua nội soi. Tất cả các lựa chọn điều trị này vẫn chưa được xác nhận thông qua các thử nghiệm ngẫu nhiên có đối chứng quy mô lớn, và do đó, mức độ bằng chứng đằng sau các can thiệp này còn hạn chế. Hiệu quả của việc đưa thuốc qua nội soi phế quản vào đường thở thay đổi không chỉ theo bệnh, mà còn theo loại thuốc được đưa vào. Liều lượng và lịch trình đưa thuốc thích hợp của mỗi loại thuốc cần được xác định và xác nhận. Tương tự, phương pháp đưa thuốc (ví dụ, tiêm với quan sát trực tiếp bằng kim TBNA cổ điển, TBNI có hỗ trợ EBUS, hoặc catheter bóng đưa thuốc phế quản) có khả năng ảnh hưởng đến kết quả. Mặc dù có những hạn chế này, dữ liệu có sẵn cho thấy rằng việc sử dụng nội soi phế quản như một nền tảng đưa thuốc cho các bệnh đường thở chọn lọc có thể là đáng giá. Cần có nghiên cứu bổ sung để xác định các chỉ định thích hợp cho việc sử dụng thuốc qua nội soi phế quản, cũng như liều lượng thuốc, phương pháp đưa thuốc và tần suất sử dụng tối ưu. |
TÀI LIỆU THAM KHẢO
- Panchabhai TS, Mehta AC. Historical perspectives of bronchoscopy. Connecting the dots. Ann Am Thorac Soc. 2015;12:631-641.
- Siegel RL, Miller KD, Jemal A. Cancer statistics, 2019. CA Cancer J Clin. 2019;69:7-34.
- Reck M, Heigener DE, Mok T, Soria JC, Rabe KF. Management of non-small-cell lung cancer: recent developments. Lancet. 2013;382:709-719.
- Hurter T, Hanrath P. Endobronchial sonography: feasibility and preliminary results. Thorax. 1992;47:565-567.
- Herth F, Becker HD, Ernst A. Conventional vs endobronchial ultrasound-guided transbronchial needle aspiration: a randomized trial. Chest. 2004;125:322-325.
- Gomez M, Silvestri GA. Endobronchial ultrasound for the diagnosis and staging of lung cancer. Proc Am Thorac Soc. 2009;6:180-186.
- Andolfi M, Potenza R, Capozzi R, Liparulo V, Puma F, Yasufuku K. The role of bronchoscopy in the diagnosis of early lung cancer: a review. J Thorac Dis. 2016;8:3329-3337.
- Krasnik M, Vilmann P, Larsen SS, Jacobsen GK. Preliminary experience with a new method of endoscopic transbronchial real time ultrasound guided biopsy for diagnosis of mediastinal and hilar lesions. Thorax. 2003;58:1083-1086.
- Navani N, Nankivell M, Lawrence DR, et al. Lung cancer diagnosis and staging with endobronchial ultrasound-guided transbronchial needle aspiration compared with conventional approaches: an open-label, pragmatic, randomised controlled trial. Lancet Respir Med. 2015;3:282-289.
- Ernst A, Feller-Kopman D, Becker HD, Mehta AC. Central airway obstruction. Am J Respir Crit Care Med. 2004;169:1278-1297.
- Seymour CW, Krimsky WS, Sager J, et al. Transbronchial needle injection: a systematic review of a new diagnostic and therapeutic paradigm. Respiration. 2006;73:78-89.
- Fujisawa T, Hongo H, Yamaguchi Y, et al. Intratumoral ethanol injection for malignant tracheobronchial lesions: a new bronchofiberscopic procedure. Endoscopy. 1986;18:188-191.
- Sawa T, Ikoma T, Yoshida T, et al. [Intratumoral ethanol injection therapy using endoscopic video information system]. Gan To Kagaku Ryoho. 1999;26:1865-1868.
- Celikoglu F, Celikoglu SI, Goldberg EP. Bronchoscopic intratumoral chemotherapy of lung cancer. Lung Cancer. 2008;61:1-12.
- Celikoglu SI, Karayel T, Demirci S, Celikoglu F, Cagatay T. Direct injection of anti-cancer drugs into endobronchial tumours for palliation of major airway obstruction. Postgrad Med J. 1997;73:159-162.
- Celikoglu F, Celikoglu SI. Intratumoural chemotherapy with 5-fluorouracil for palliation of bronchial cancer in patients with severe airway obstruction. J Pharm Pharmacol. 2003;55:1441-1448.
- Yarmus L, Mallow C, Akulian J, et al. Prospective multicentered safety and feasibility pilot for endobronchial intratumoral chemotherapy. Chest. 2019;156:562-570.
- Liu M, Ma P, Lu Z. [Local chemotherapy by fibrobronchoscopy for advanced bronchogenic carcinoma]. Zhonghua Jie He He Hu Xi Za Zhi. 2000;23:550-551.
- Mehta HJ, Begnaud A, Penley AM, et al. Treatment of isolated mediastinal and hilar recurrence of lung cancer with bronchoscopic endobronchial ultrasound guided intratumoral injection of chemotherapy with cisplatin. Lung Cancer. 2015;90:542-547.
- Celikoglu SI, Celikoglu F, Goldberg EP. Endobronchial intratumoral chemotherapy (EITC) followed by surgery in early non-small cell lung cancer with polypoid growth causing erroneous impression of advanced disease. Lung Cancer. 2006;54:339-346.
- Khan F, Anker CJ, Garrison G, Kinsey CM. Endobronchial ultrasound-guided transbronchial needle injection for local control of recurrent non-small cell lung cancer. Ann Am Thorac Soc. 2015;12:101-104.
- Mori V, Roy GS, Bates JHT, Kinsey CM. Cisplatin pharmacodynamics following endobronchial ultrasound-guided transbronchial needle injection into lung tumors. Sci Rep. 2019;9:6819.
- Tsukada H, Seward KP, Rafeq S, Kocher O, Ernst A. Experimental pilot study of a novel endobronchial drug delivery catheter. J Bronchology Interv Pulmonol. 2015;22:312-318.
- Harris K, Puchalski J, Sterman D. Recent advances in bronchoscopic treatment of peripheral lung cancers. Chest. 2017;151:674-685.
- Lubin R, Zalcman G, Bouchet L, et al. Serum p53 antibodies as early markers of lung cancer. Nat Med. 1995;1:701-702.
- Iggo R, Gatter K, Bartek J, Lane D, Harris AL. Increased expression of mutant forms of p53 oncogene in primary lung cancer. Lancet. 1990;335:675-679.
- Roth JA, Nguyen D, Lawrence DD, et al. Retrovirus-mediated wild-type p53 gene transfer to tumors of patients with lung cancer. Nat Med. 1996;2:985-991.
- Weill D, Mack M, Roth J, et al. Adenoviral-mediated p53 gene transfer to non-small cell lung cancer through endobronchial injection. Chest. 2000;118:966-970.
- Nemunaitis J, Swisher SG, Timmons T, et al. Adenovirus-mediated p53 gene transfer in sequence with cisplatin to tumors of patients with non-small-cell lung cancer. J Clin Oncol. 2000;18:609-622.
- Schuler M, Herrmann R, De Greve JL, et al. Adenovirus-mediated wild-type p53 gene transfer in patients receiving chemotherapy for advanced non-small-cell lung cancer: results of a multicenter phase II study. J Clin Oncol. 2001;19:1750-1758.
- Swisher SG, Roth JA, Komaki R, et al. Induction of p53-regulated genes and tumor regression in lung cancer patients after intratumoral delivery of adenoviral p53 (INGN 201) and radiation therapy. Clin Cancer Res. 2003;9:93-101.
- Whited RE. A prospective study of laryngotracheal sequelae in long-term intubation. Laryngoscope. 1984;94:367-377.
- Tadie JM, Behm E, Lecuyer L, et al. Post-intubation laryngeal injuries and extubation failure: a fiberoptic endoscopic study. Intensive Care Med. 2010;36:991-998.
- Spittle N, McCluskey A. Lesson of the week: tracheal stenosis after intubation. BMJ. 2000;321:1000-1002.
- Dalar L, Karasulu L, Abul Y, et al. Bronchoscopic treatment in the management of benign tracheal stenosis: choices for simple and complex tracheal stenosis. Ann Thorac Surg. 2016;101:1310-1317.
- Verweij J, Pinedo HM. Mitomycin C: mechanism of action, usefulness and limitations. Anticancer Drugs. 1990;1:5-13.
- Cheng JW, Cai JP, Li Y, Wei RL. Intraoperative mitomycin C for nonpenetrating glaucoma surgery: a systematic review and meta-analysis. J Glaucoma. 2011;20:322-326.
- Perepelitsyn I, Shapshay SM. Endoscopic treatment of laryngeal and tracheal stenosis-has mitomycin C improved the outcome? Otolaryngol Head Neck Surg. 2004;131:16-20.
- Smith ME, Elstad M. Mitomycin C and the endoscopic treatment of laryngotracheal stenosis: are two applications better than one? Laryngoscope. 2009;119:272-283.
- Leavitt RY, Fauci AS, Bloch DA, et al. The American College of Rheumatology 1990 criteria for the classification of Wegener’s granulomatosis. Arthritis Rheum. 1990;33:1101-1107.
- Ananthakrishnan L, Sharma N, Kanne JP. Wegener’s granulomatosis in the chest: high-resolution CT findings. AJR Am J Roentgenol. 2009;192:676-682.
- Hoffman GS, Thomas-Golbanov CK, Chan J, Akst LM, Eliachar I. Treatment of subglottic stenosis, due to Wegener’s granulomatosis, with intralesional corticosteroids and dilation. J Rheumatol. 2003;30:1017-1021.
- Stappaerts I, Van Laer C, Deschepper K, Van de Heyning P, Vermeire P. Endoscopic management of severe subglottic stenosis in Wegener’s granulomatosis. Clin Rheumatol. 2000;19:315-317.
- Girard C, Charles P, Terrier B, et al. Tracheobronchial stenoses in granulomatosis with polyangiitis (Wegener’s): a report on 26 cases. Medicine (Baltimore). 2015;94:e1088.
- Nouraei SA, Obholzer R, Ind PW, et al. Results of endoscopic surgery and intralesional steroid therapy for airway compromise due to tracheobronchial Wegener’s granulomatosis. Thorax. 2008;63:49-52.
- Langford CA, Sneller MC, Hallahan CW, et al. Clinical features and therapeutic management of subglottic stenosis in patients with Wegener’s granulomatosis. Arthritis Rheum. 1996;39:1754-1760.
- Polychronopoulos VS, Prakash UBS. Airway involvement in sarcoidosis. Chest. 2009;136:1371-1380.
- Westcott JL, Noehren TH. Bronchial stenosis in chronic sarcoidosis. Chest. 1973;63:893-897.
- Nunes H, Uzunhan Y, Gille T, Lamberto C, Valeyre D, Brillet PY. Imaging of sarcoidosis of the airways and lung parenchyma and correlation with lung function. Eur Respir J. 2012;40:750-765.
- Judson MA. An approach to the treatment of pulmonary sarcoidosis with corticosteroids: the six phases of treatment. Chest. 1999;115:1158-1165.
- Judson MA, Uflacker R. Treatment of a solitary pulmonary sarcoidosis mass by CT-guided direct intralesional injection of corticosteroid. Chest. 2001;120:316-317.
- Butler CR, Nouraei SA, Mace AD, Khalil S, Sandhu SK, Sandhu GS. Endoscopic airway management of laryngeal sarcoidosis. Arch Otolaryngol Head Neck Surg. 2010;136:251-255.
- Bestall JC, Paul EA, Garrod R, Garnham R, Jones PW, Wedzicha JA. Usefulness of the Medical Research Council (MRC) dyspnoea scale as a measure of disability in patients with chronic obstructive pulmonary disease. Thorax. 1999;54:581-586.
- Teo F, Anantham D, Feller-Kopman D, Ernst A. Bronchoscopic management of sarcoidosis related bronchial stenosis with adjunctive topical mitomycin C. Ann Thorac Surg. 2010;89:2005-2007.
- Costantino CL, Mathisen DJ. Idiopathic laryngotracheal stenosis. J Thorac Dis. 2016;8:S204-S209.
- Fiz I, Bittar Z, Piazza C, et al. Hormone receptors analysis in idiopathic progressive subglottic stenosis. Laryngoscope. 2018;128:E72-E77.
- Grillo HC, Mark EJ, Mathisen DJ, Wain JC. Idiopathic laryngotracheal stenosis and its management. Ann Thorac Surg. 1993;56:80-87.
- Shabani S, Hoffman MR, Brand WT, Dailey SH. Endoscopic Management of idiopathic subglottic stenosis. Ann Otol Rhinol Laryngol. 2017;126:96-102.
- Taylor SC, Clayburgh DR, Rosenbaum JT, Schindler JS. Clinical manifestations and treatment of idiopathic and Wegener granulomatosis-associated subglottic stenosis. JAMA Otolaryngol Head Neck Surg. 2013;139:76-81.
- Grillo HC, Mathisen DJ, Ashiku SK, Wright CD, Wain JC. Successful treatment of idiopathic laryngotracheal stenosis by resection and primary anastomosis. Ann Otol Rhinol Laryngol. 2003;112:798-800.
- Marchiori E, Araujo Neto C, Meirelles GS, et al. Laryngotracheobronchial papillomatosis: findings on computed tomography scans of the chest. J Bras Pneumol. 2008;34:1084-1089.
- Donne AJ, Hampson L, Homer JJ, Hampson IN. The role of HPV type in recurrent respiratory papillomatosis. Int J Pediatr Otorhinolaryngol. 2010;74:7-14.
- Rombaldi RL, Serafini EP, Mandelli J, Zimmermann E, Losquiavo KP. Transplacental transmission of human papillomavirus. Virol J. 2008;5:106.
- Fortes HR, von Ranke FM, Escuissato DL, et al. Recurrent respiratory papillomatosis: a state-of-the-art review. Respir Med. 2017;126:116-121.
- Carifi M, Napolitano D, Morandi M, Dall’Olio D. Recurrent respiratory papillomatosis: current and future perspectives. Ther Clin Risk Manag. 2015;11:731-738.
- Wierzbicka M, Jackowska J, Bartochowska A, Jozefiak A, Szyfter W, Kedzia W. Effectiveness of cidofovir intralesional treatment in recurrent respiratory papillomatosis. Eur Arch Otorhinolaryngol. 2011;268:1305-1311.
- Dikkers FG. Treatment of recurrent respiratory papillomatosis with microsurgery in combination with intralesional cidofovir-a prospective study. Eur Arch Otorhinolaryngol. 2006;263:440-443.
- Lee AS, Rosen CA. Efficacy of cidofovir injection for the treatment of recurrent respiratory papillomatosis. J Voice. 2004;18:551-556.
- Shehab N, Sweet BV, Hogikyan ND. Cidofovir for the treatment of recurrent respiratory papillomatosis: a review of the literature. Pharmacotherapy. 2005;25:977-989.
- Cundy KC. Clinical pharmacokinetics of the antiviral nucleotide analogues cidofovir and adefovir. Clin Pharmacokinet. 1999;36:127-143.
- Naiman AN, Ceruse P, Coulombeau B, Froehlich P. Intralesional cidofovir and surgical excision for laryngeal papillomatosis. Laryngoscope. 2003;113:2174-2181.
- Milczuk HA. Intralesional cidofovir for the treatment of severe juvenile recurrent respiratory papillomatosis: long-term results in 4 children. Otolaryngol Head Neck Surg. 2003;128:788-794.
- Tanna N, Sidell D, Joshi AS, Bielamowicz SA. Adult intralesional cidofovir therapy for laryngeal papilloma: a 10-year perspective. Arch Otolaryngol Head Neck Surg. 2008;134:497-500.
- Frye L, Machuzak M. Airway complications after lung transplantation. Clin Chest Med. 2017;38:693-706.
- Oberg CL, Holden VK, Channick CL. Benign central airway obstruction. Semin Respir Crit Care Med. 2018;39:731-746.
- Yousem SA, Dauber JH, Griffith BP. Bronchial cartilage alterations in lung transplantation. Chest. 1990;98:1121-1124.
- Chhajed PN, Malouf MA, Tamm M, Spratt P, Glanville AR. Interventional bronchoscopy for the management of airway complications following lung transplantation. Chest. 2001;120:1894-1899.
- Erard AC, Monnier P, Spiliopoulos A, Nicod L. Mitomycin C for control of recurrent bronchial stenosis: a case report. Chest. 2001;120:2103-2105.
- Davidson KR, Elmasri M, Wahidi MM, Shofer SL, Cheng GZ, Mahmood K. Management of lung transplant bronchial stenosis with mitomycin C. J Bronchology Interv Pulmonol. 2019;26:124-128.
BẢNG CHÚ GIẢI THUẬT NGỮ Y HỌC ANH-VIỆT
| STT | Thuật ngữ tiếng Anh | Phiên âm IPA | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Bronchoscopy | /brɒŋˈkɒskəpi/ | Nội soi phế quản |
| 2 | Pulmonary disease | /ˈpʌlmənəri dɪˈziːz/ | Bệnh lý phổi |
| 3 | Therapeutic capabilities | /ˌθerəˈpjuːtɪk ˌkeɪpəˈbɪlətiz/ | Khả năng điều trị |
| 4 | Laser therapy | /ˈleɪzə ˈθerəpi/ | Liệu pháp laser |
| 5 | Argon plasma coagulation | /ˈɑːɡɒn ˈplæzmə kəʊˌæɡjʊˈleɪʃən/ | Đông huyết tương argon (APC) |
| 6 | Cryotherapy | /kraɪəʊˈθerəpi/ | Liệu pháp lạnh |
| 7 | Brachytherapy | /ˌbrækiˈθerəpi/ | Xạ trị áp sát |
| 8 | Endobronchial stenting | /ˌendəʊˈbrɒŋkiəl ˈstentɪŋ/ | Đặt stent nội phế quản |
| 9 | Malignant | /məˈlɪɡnənt/ | Ác tính |
| 10 | Nonmalignant | /ˌnɒnməˈlɪɡnənt/ | Không ác tính (lành tính) |
| 11 | Central airway disease | /ˈsentrəl ˈeəweɪ dɪˈziːz/ | Bệnh lý đường thở trung tâm |
| 12 | Interventional pulmonology | /ˌɪntəˈvenʃənəl ˌpʌlməˈnɒlədʒi/ | Hô hấp can thiệp |
| 13 | Thoracic diseases | /θəˈræsɪk dɪˈziːzɪz/ | Bệnh lý lồng ngực |
| 14 | Transbronchial needle injections (TBNI) | /ˌtrænzˈbrɒŋkiəl ˈniːdl ɪnˈdʒekʃənz/ | Tiêm xuyên thành phế quản qua kim |
| 15 | Lung cancer | /lʌŋ ˈkænsə/ | Ung thư phổi |
| 16 | Mortality | /mɔːˈtæləti/ | Tỷ lệ tử vong |
| 17 | Non-small cell lung cancer (NSCLC) | /nɒn-smɔːl sel lʌŋ ˈkænsə/ | Ung thư phổi không tế bào nhỏ |
| 18 | Morbidity | /mɔːˈbɪdəti/ | Bệnh suất |
| 19 | Flexible transbronchial needle aspiration (TBNA) | /ˈfleksəbl ˌtrænzˈbrɒŋkiəl ˈniːdl ˌæspəˈreɪʃən/ | Chọc hút bằng kim xuyên thành phế quản qua nội soi phế quản ống mềm |
| 20 | Fiberoptic bronchoscope | /ˌfaɪbərˈɒptɪk ˈbrɒŋkəskəʊp/ | Ống soi phế quản sợi quang |
| 21 | Rapid on-site evaluation (ROSE) | /ˈræpɪd ɒn-saɪt ɪˌvæljuˈeɪʃən/ | Đánh giá nhanh tại chỗ |
| 22 | Histopathologic specimens | /ˌhɪstəʊˌpæθəˈlɒdʒɪk ˈspesɪmənz/ | Mẫu bệnh phẩm mô bệnh học |
| 23 | Endobronchial ultrasonography (EBUS) | /ˌendəʊˈbrɒŋkiəl ˌʌltrəsəˈnɒɡrəfi/ | Siêu âm nội phế quản |
| 24 | Diagnostic yield | /ˌdaɪəɡˈnɒstɪk jiːld/ | Hiệu suất chẩn đoán |
| 25 | Mediastinal lymph node staging | /ˌmiːdiəˈstaɪnəl lɪmf nəʊd ˈsteɪdʒɪŋ/ | Phân giai đoạn hạch trung thất |
| 26 | Mediastinoscopy | /ˌmiːdiəˌstaɪˈnɒskəpi/ | Nội soi trung thất |
| 27 | Video-assisted thoracoscopic surgery (VATS) | /ˈvɪdiəʊ-əˈsɪstɪd ˌθɔːrəkəʊˈskɒpɪk ˈsɜːdʒəri/ | Phẫu thuật lồng ngực có hỗ trợ video |
| 28 | Therapeutic modality | /ˌθerəˈpjuːtɪk məʊˈdæləti/ | Phương thức điều trị |
| 29 | Chemotherapeutic agents | /ˌkiːməʊˌθerəˈpjuːtɪk ˈeɪdʒənts/ | Hóa chất, tác nhân hóa trị |
| 30 | Malignant airway obstruction | /məˈlɪɡnənt ˈeəweɪ əbˈstrʌkʃən/ | Tắc nghẽn đường thở do ác tính |
| 31 | Dyspnea | /ˈdɪspniə/ | Khó thở |
| 32 | Hemoptysis | /hiːˈmɒptəsɪs/ | Ho ra máu |
| 33 | Postobstructive pneumonia | /ˌpəʊstəbˈstrʌktɪv njuːˈməʊniə/ | Viêm phổi sau tắc nghẽn |
| 34 | Respiratory failure | /rɪˈspɪrətəri ˈfeɪljə/ | Suy hô hấp |
| 35 | Recanalization | /ˌriːˌkænəlaɪˈzeɪʃən/ | Tái thông |
| 36 | Intravenous therapies | /ˌɪntrəˈviːnəs ˈθerəpiz/ | Liệu pháp tĩnh mạch |
| 37 | Cytotoxic | /ˌsaɪtəʊˈtɒksɪk/ | Độc tế bào |
| 38 | Systemic toxicities | /sɪˈstemɪk tɒkˈsɪsətiz/ | Độc tính toàn thân |
| 39 | Intratumoral concentrations | /ˌɪntrəˈtjuːmərəl ˌkɒnsənˈtreɪʃənz/ | Nồng độ trong khối u |
| 40 | Ethanol | /ˈeθənɒl/ | Ethanol |
| 41 | Tissue necrosis | /ˈtɪʃuː nəˈkrəʊsɪs/ | Hoại tử mô |
| 42 | Airway patency | /ˈeəweɪ ˈpeɪtənsi/ | Sự thông thoáng của đường thở |
| 43 | Endobronchial intratumoral chemotherapy (EITC) | /ˌendəʊˈbrɒŋkiəl ˌɪntrəˈtjuːmərəl ˌkiːməʊˈθerəpi/ | Hóa trị nội u trong lòng phế quản |
| 44 | Squamous cell carcinoma | /ˈskweɪməs sel ˌkɑːsɪˈnəʊmə/ | Ung thư biểu mô tế bào vảy |
| 45 | Palliative intervention | /ˈpæliətɪv ˌɪntəˈvenʃən/ | Can thiệp giảm nhẹ |
| 46 | Exophytic obstruction | /ˌeksəʊˈfɪtɪk əbˈstrʌkʃən/ | Tắc nghẽn dạng sùi |
| 47 | Bronchogenic carcinoma | /ˌbrɒŋkəʊˈdʒenɪk ˌkɑːsɪˈnəʊmə/ | Ung thư biểu mô phế quản |
| 48 | 5-fluorouracil | /faɪv-ˌflʊərəʊˈjʊərəsɪl/ | 5-fluorouracil |
| 49 | Mitomycin | /ˌmaɪtəʊˈmaɪsɪn/ | Mitomycin |
| 50 | Methotrexate | /ˌmeθəʊˈtrekseɪt/ | Methotrexate |
| 51 | Bleomycin | /ˌbliːəʊˈmaɪsɪn/ | Bleomycin |
| 52 | Mitoxantrone | /ˌmaɪtəʊˈzæntrəʊn/ | Mitoxantrone |
| 53 | Luminal diameter | /ˈluːmɪnl daɪˈæmɪtə/ | Đường kính lòng (đường thở) |
| 54 | Adverse events | /ˈædvɜːs ɪˈvents/ | Biến cố bất lợi |
| 55 | Paclitaxel | /ˌpæklɪˈtæksel/ | Paclitaxel |
| 56 | Carboplatin | /ˌkɑːbəʊˈplætɪn/ | Carboplatin |
| 57 | Cisplatin | /sɪsˈplætɪn/ | Cisplatin |
| 58 | Pharmacologic profile | /ˌfɑːməkəˈlɒdʒɪk ˈprəʊfaɪl/ | Đặc tính dược lý |
| 59 | Biometabolism | /ˌbaɪəʊməˈtæbəlɪzəm/ | Chuyển hóa sinh học |
| 60 | Cumulative doses | /ˈkjuːmjʊlətɪv dəʊsɪz/ | Liều tích lũy |
| 61 | Bolus injection | /ˈbəʊləs ɪnˈdʒekʃən/ | Tiêm một liều lớn (bolus) |
| 62 | Doppler ultrasonography | /ˈdɒplər ˌʌltrəsəˈnɒɡrəfi/ | Siêu âm Doppler |
| 63 | Vascularized region | /ˈvæskjʊləraɪzd ˈriːdʒən/ | Vùng giàu mạch máu |
| 64 | Airway dehiscence | /ˈeəweɪ dɪˈhɪsns/ | Bục đường thở |
| 65 | Microneedle | /ˈmaɪkrəʊˌniːdl/ | Vi kim |
| 66 | Submucosa | /ˌsʌbmjuːˈkəʊsə/ | Lớp dưới niêm mạc |
| 67 | Bronchial adventitia | /ˈbrɒŋkiəl ˌædvenˈtɪʃə/ | Lớp vỏ ngoài phế quản |
| 68 | Cartilaginous layer | /ˌkɑːtɪˈlædʒɪnəs ˈleɪə/ | Lớp sụn |
| 69 | Circumferentially | /ˌsɜːkəmˌfrenʃəli/ | Theo chu vi |
| 70 | Rigid bronchoscopy | /ˈrɪdʒɪd brɒŋˈkɒskəpi/ | Nội soi phế quản ống cứng |
| 71 | Airway stenosis | /ˈeəweɪ stəˈnəʊsɪs/ | Hẹp đường thở |
| 72 | Gene therapy | /dʒiːn ˈθerəpi/ | Liệu pháp gen |
| 73 | Tumor suppressor gene | /ˈtjuːmə səˈpresə dʒiːn/ | Gen ức chế khối u |
| 74 | Retroviral vector | /ˌretrəʊˈvaɪrəl ˈvektə/ | Vector retrovirus |
| 75 | Adenoviral vectors | /ˌædɪnəʊˈvaɪrəl ˈvektəz/ | Vector adenovirus |
| 76 | Vinorelbine | /vɪˈnɒrelbiːn/ | Vinorelbine |
| 77 | Radiation therapy | /ˌreɪdiˈeɪʃən ˈθerəpi/ | Xạ trị |
| 78 | Laryngotracheal stenosis | /ləˌrɪŋɡəʊˈtreɪkiəl stəˈnəʊsɪs/ | Hẹp thanh-khí quản |
| 79 | Endotracheal intubation | /ˌendəʊˈtreɪkiəl ˌɪntjuːˈbeɪʃən/ | Đặt nội khí quản |
| 80 | Tracheostomy | /ˌtreɪkiˈɒstəmi/ | Mở khí quản |
| 81 | Extubation | /ˌekstjuːˈbeɪʃən/ | Rút ống nội khí quản |
| 82 | Decannulation | /diːˌkænjʊˈleɪʃən/ | Rút canuyn mở khí quản |
| 83 | Wheezing | /ˈwiːzɪŋ/ | Thở khò khè |
| 84 | Bronchodilators | /ˌbrɒŋkəʊdaɪˈleɪtəz/ | Thuốc giãn phế quản |
| 85 | Tracheomalacia | /ˌtreɪkiəʊməˈleɪʃə/ | Nhuyễn khí quản |
| 86 | Electrocautery knife | /ɪˌlektrəʊˈkɔːtəri naɪf/ | Dao điện |
| 87 | Balloon dilation | /bəˈluːn daɪˈleɪʃən/ | Nong bóng |
| 88 | Surgical resection | /ˈsɜːdʒɪkəl rɪˈsekʃən/ | Phẫu thuật cắt bỏ |
| 89 | Mitomycin C | /ˌmaɪtəʊˈmaɪsɪn siː/ | Mitomycin C |
| 90 | Antineoplastic agent | /ˌæntiniːəʊˈplæstɪk ˈeɪdʒənt/ | Tác nhân chống tân sinh |
| 91 | Colorectal cancer | /ˌkəʊləʊˈrektəl ˈkænsə/ | Ung thư đại trực tràng |
| 92 | Gastric cancer | /ˈɡæstrɪk ˈkænsə/ | Ung thư dạ dày |
| 93 | Antiproliferative agent | /ˌæntiprəˈlɪfərətɪv ˈeɪdʒənt/ | Tác nhân chống tăng sinh |
| 94 | Glaucoma | /ɡlɔːˈkəʊmə/ | Bệnh tăng nhãn áp (glôcôm) |
| 95 | Topical | /ˈtɒpɪkəl/ | Tại chỗ |
| 96 | Restenosis | /ˌriːstəˈnəʊsɪs/ | Tái hẹp |
| 97 | Granulomatosis with polyangiitis (GPA) | /ˌɡrænjʊləməˈtəʊsɪs wɪð ˌpɒliˌændʒiˈaɪtɪs/ | Bệnh u hạt kèm viêm đa mạch |
| 98 | Vasculitis | /ˌvæskjʊˈlaɪtɪs/ | Viêm mạch |
| 99 | Antineutrophil cytoplasmic antibodies (ANCA) | /ˌæntɪˈnjuːtrəfɪl ˌsaɪtəʊˈplæzmɪk ˈæntɪˌbɒdiz/ | Kháng thể kháng bào tương bạch cầu trung tính |
| 100 | Urinary sediment | /ˈjʊərɪnəri ˈsedɪmənt/ | Cặn lắng nước tiểu |
| 101 | Oral ulcers | /ˈɔːrəl ˈʌlsəz/ | Loét miệng |
| 102 | Nasal discharge | /ˈneɪzəl ˈdɪstʃɑːdʒ/ | Chảy dịch mũi |
| 103 | Granulomas | /ˌɡrænjʊˈləʊməz/ | U hạt |
| 104 | Cavitary lung nodules | /ˈkævɪtəri lʌŋ ˈnɒdjuːlz/ | Nốt phổi dạng hang |
| 105 | Ground-glass opacities | /ɡraʊnd-ɡlɑːs əʊˈpæsətiz/ | Tổn thương dạng kính mờ |
| 106 | Alveolar hemorrhage | /ælˈviːələr ˈhemərɪdʒ/ | Chảy máu phế nang |
| 107 | Mucosal ulcerations | /mjuːˈkəʊsəl ˌʌlsəˈreɪʃənz/ | Loét niêm mạc |
| 108 | Immunosuppressive therapy | /ɪˌmjuːnəʊsəˈpresɪv ˈθerəpi/ | Liệu pháp ức chế miễn dịch |
| 109 | Subglottic region | /sʌbˈɡlɒtɪk ˈriːdʒən/ | Vùng hạ thanh môn |
| 110 | Subglottic stenosis | /sʌbˈɡlɒtɪk stəˈnəʊsɪs/ | Hẹp hạ thanh môn |
| 111 | Glucocorticoid | /ˌɡluːkəʊˈkɔːtɪkɔɪd/ | Glucocorticoid |
| 112 | Intralesional | /ˌɪntrəˈliːʒənəl/ | Nội tổn thương |
| 113 | Methylprednisolone acetate | /ˌmeθɪlpredˈnɪsələʊn ˈæsɪteɪt/ | Methylprednisolone acetate |
| 114 | Laryngeal needle | /ləˈrɪndʒiəl ˈniːdl/ | Kim thanh quản |
| 115 | Sarcoidosis | /ˌsɑːkɔɪˈdəʊsɪs/ | Bệnh Sarcoidosis |
| 116 | Noncaseating granulomas | /nɒnˈkeɪsieɪtɪŋ ˌɡrænjʊˈləʊməz/ | U hạt không hoại tử bã đậu |
| 117 | Bilateral hilar adenopathy | /baɪˈlætərəl ˈhaɪlər ˌædɪˈnɒpəθi/ | Bệnh lý hạch rốn phổi hai bên |
| 118 | Pulmonary micronodules | /ˈpʌlmənəri ˌmaɪkrəʊˈnɒdjuːlz/ | Các vi nốt ở phổi |
| 119 | Fibrosis | /faɪˈbrəʊsɪs/ | Xơ hóa |
| 120 | Endobronchial mucosal granulomas | /ˌendəʊˈbrɒŋkiəl mjuːˈkəʊsəl ˌɡrænjʊˈləʊməz/ | U hạt niêm mạc nội phế quản |
| 121 | Air-trapping | /ˈeə-ˌtræpɪŋ/ | Bẫy khí |
| 122 | Expiratory films | /ɪkˈspaɪərətəri fɪlmz/ | Phim chụp thì thở ra |
| 123 | Corticosteroids | /ˌkɔːtɪkəʊˈstɪərɔɪdz/ | Corticosteroid |
| 124 | Dexamethasone | /ˌdeksəˈmeθəsəʊn/ | Dexamethasone |
| 125 | Triamcinolone | /ˌtraɪæmˈsɪnələʊn/ | Triamcinolone |
| 126 | Laryngeal involvement | /ləˈrɪndʒiəl ɪnˈvɒlvmənt/ | Tổn thương thanh quản |
| 127 | Medical Research Council (MRC) dyspnea scale | /ˈmedɪkəl rɪˈsɜːtʃ ˈkaʊnsəl ˈdɪspniə skeɪl/ | Thang điểm khó thở của Hội đồng Nghiên cứu Y khoa (MRC) |
| 128 | Systemic steroid | /sɪˈstemɪk ˈstɪərɔɪd/ | Steroid toàn thân |
| 129 | Idiopathic laryngotracheal stenosis | /ˌɪdiəˈpæθɪk ləˌrɪŋɡəʊˈtreɪkiəl stəˈnəʊsɪs/ | Hẹp thanh-khí quản vô căn |
| 130 | Inflammatory disorder | /ɪnˈflæmətəri dɪsˈɔːdə/ | Rối loạn viêm |
| 131 | Pre- and perimenopausal | /priː- ənd ˌperɪˌmenəˈpɔːzəl/ | Tiền mãn kinh và quanh mãn kinh |
| 132 | Exertional dyspnea | /ɪɡˈzɜːʃənəl ˈdɪspniə/ | Khó thở khi gắng sức |
| 133 | Diagnosis of exclusion | /ˌdaɪəɡˈnəʊsɪs əv ɪkˈskluːʒən/ | Chẩn đoán loại trừ |
| 134 | Estrogen | /ˈiːstrədʒən/ | Estrogen |
| 135 | Progesterone | /prəˈdʒestərəʊn/ | Progesterone |
| 136 | Fibrous inflammation | /ˈfaɪbrəs ˌɪnfləˈmeɪʃən/ | Viêm xơ |
| 137 | Lamina propria | /ˈlæmɪnə ˈprəʊpriə/ | Lớp đệm |
| 138 | Tracheal resection | /ˈtreɪkiəl rɪˈsekʃən/ | Cắt bỏ khí quản |
| 139 | Reconstruction | /ˌriːkənˈstrʌkʃən/ | Tái tạo |
| 140 | Thermal ablative therapies | /ˈθɜːməl əˈbleɪtɪv ˈθerəpiz/ | Liệu pháp nhiệt-đốt |
| 141 | Stridor | /ˈstraɪdɔː/ | Thở rít |
| 142 | Recurrent respiratory papillomatosis (RRP) | /rɪˈkʌrənt rɪˈspɪrətəri ˌpæpɪləməˈtəʊsɪs/ | U nhú đường hô hấp tái phát |
| 143 | Papillomatous | /ˌpæpɪˈlɒmətəs/ | Dạng nhú |
| 144 | Exophytic lesions | /ˌeksəʊˈfɪtɪk ˈliːʒənz/ | Tổn thương dạng sùi |
| 145 | Parenchymal involvement | /pəˈreŋkɪməl ɪnˈvɒlvmənt/ | Tổn thương nhu mô |
| 146 | Human papillomavirus (HPV) | /ˈhjuːmən ˌpæpɪˈləʊməˌvaɪrəs/ | Virus u nhú ở người |
| 147 | Virulent strain | /ˈvɪrʊlənt streɪn/ | Chủng độc lực cao |
| 148 | Malignant transformation | /məˈlɪɡnənt ˌtrænsfəˈmeɪʃən/ | Chuyển dạng ác tính |
| 149 | Placental transmission | /pləˈsentl trænzˈmɪʃən/ | Lây truyền qua nhau thai |
| 150 | Orogenital sexual contact | /ˌɔːrəʊˈdʒenɪtl ˈsekʃuəl ˈkɒntækt/ | Quan hệ tình dục bằng miệng |
| 151 | Surgical debulking | /ˈsɜːdʒɪkəl diːˈbʌlkɪŋ/ | Phẫu thuật giảm kích thước khối u |
| 152 | Adjuvant therapies | /ˈædʒʊvənt ˈθerəpiz/ | Liệu pháp bổ trợ |
| 153 | Intralesional cidofovir | /ˌɪntrəˈliːʒənəl saɪˈdəʊfəvɪə/ | Cidofovir nội tổn thương |
| 154 | Antiviral medication | /ˌæntiˈvaɪrəl ˌmedɪˈkeɪʃən/ | Thuốc kháng virus |
| 155 | DNA polymerases | /ˌdiːenˈeɪ pəˈlɪməreɪzɪz/ | DNA polymerase |
| 156 | Complete remission | /kəmˈpliːt rɪˈmɪʃən/ | Lui bệnh hoàn toàn |
| 157 | Gastrointestinal symptoms | /ˌɡæstrəʊɪnˈtestɪnl ˈsɪmptəmz/ | Triệu chứng tiêu hóa |
| 158 | Transient transaminitis | /ˈtrænziənt ˌtrænsˌæmɪˈnaɪtɪs/ | Tăng men gan thoáng qua |
| 159 | Lung transplantation | /lʌŋ ˌtrænspɑːnˈteɪʃən/ | Ghép phổi |
| 160 | Anastomotic necrosis | /əˌnæstəˈmɒtɪk nəˈkrəʊsɪs/ | Hoại tử miệng nối |
| 161 | Dehiscence | /dɪˈhɪsns/ | Bục, toác (vết mổ) |
| 162 | Anastomotic infections | /əˌnæstəˈmɒtɪk ɪnˈfekʃənz/ | Nhiễm trùng miệng nối |
| 163 | Fistulas | /ˈfɪstjʊləz/ | Rò |
| 164 | Bronchopleural | /ˌbrɒŋkəʊˈplʊərəl/ | Phế quản-màng phổi |
| 165 | Bronchovascular | /ˌbrɒŋkəʊˈvæskjʊlər/ | Phế quản-mạch máu |
| 166 | Bronchomediastinal | /ˌbrɒŋkəʊˌmiːdiəˈstaɪnəl/ | Phế quản-trung thất |
| 167 | Bronchial stenosis | /ˈbrɒŋkiəl stəˈnəʊsɪs/ | Hẹp phế quản |
| 168 | Anastomotic site | /əˌnæstəˈmɒtɪk saɪt/ | Vị trí miệng nối |
| 169 | Ossification | /ˌɒsɪfɪˈkeɪʃən/ | Cốt hóa |
| 170 | Calcification | /ˌkælsɪfɪˈkeɪʃən/ | Vôi hóa |
| 171 | Fibrovascular ingrowth | /ˌfaɪbrəʊˈvæskjʊlər ˈɪnɡrəʊθ/ | Sự phát triển của mô xơ-mạch |
| 172 | Bronchial perfusion | /ˈbrɒŋkiəl pəˈfjuːʒən/ | Tưới máu phế quản |
| 173 | Bougie dilation | /ˈbuːʒi daɪˈleɪʃən/ | Nong bằng que nong (bougie) |
| 174 | Endobronchial brachytherapy | /ˌendəʊˈbrɒŋkiəl ˌbrækiˈθerəpi/ | Xạ trị áp sát nội phế quản |
| 175 | Cystic fibrosis | /ˈsɪstɪk faɪˈbrəʊsɪs/ | Xơ nang |
| 176 | Burkholderia cepacia | /bɜːkˌhəʊlˈdɪəriə səˈpeɪʃiə/ | Burkholderia cepacia |
| 177 | Argon laser electrocoagulation | /ˈɑːɡɒn ˈleɪzər ɪˌlektrəʊkəʊˌæɡjʊˈleɪʃən/ | Đông điện bằng laser argon |
| 178 | Granulation tissue | /ˌɡrænjʊˈleɪʃən ˈtɪʃuː/ | Mô hạt |
| 179 | Bronchus intermedius | /ˈbrɒŋkəs ˌɪntəˈmiːdiəs/ | Phế quản trung gian |
| 180 | Forced expiratory volume in the first second (FEV₁) | /fɔːst ɪkˈspaɪərətəri ˈvɒljuːm ɪn ðə fɜːst ˈsekənd/ | Thể tích thở ra gắng sức trong giây đầu tiên |
| 181 | Balloon bronchoplasty | /bəˈluːn ˈbrɒŋkəʊˌplæsti/ | Tạo hình phế quản bằng bóng |
| 182 | Forced vital capacity (FVC) | /fɔːst ˈvaɪtl kəˈpæsəti/ | Dung tích sống gắng sức |
| 183 | Topical application | /ˈtɒpɪkəl ˌæplɪˈkeɪʃən/ | Bôi tại chỗ |
| 184 | Injection under direct visualization | /ɪnˈdʒekʃən ˈʌndə dɪˈrekt ˌvɪʒuəlaɪˈzeɪʃən/ | Tiêm dưới quan sát trực tiếp |
| 185 | Injection under ultrasound visualization | /ɪnˈdʒekʃən ˈʌndə ˈʌltrəsaʊnd ˌvɪʒuəlaɪˈzeɪʃən/ | Tiêm dưới hướng dẫn của siêu âm |
| 186 | Circumferential injection | /ˌsɜːkəmˌfrenʃəl ɪnˈdʒekʃən/ | Tiêm theo chu vi |
| 187 | Endobronchial balloon catheter | /ˌendəʊˈbrɒŋkiəl bəˈluːn ˈkæθɪtə/ | Catheter bóng nội phế quản |
| 188 | Pledget | /ˈpledʒɪt/ | Miếng gạc nhỏ |
| 189 | Forceps | /ˈfɔːseps/ | Kẹp (forceps) |
| 190 | Apposition | /ˌæpəˈzɪʃən/ | Sự áp sát |
| 191 | TBNA needle | /ˈtiː biː en eɪ ˈniːdl/ | Kim TBNA |
| 192 | EBUS-TBNA needle | /ˈiːbʌs-ˈtiː biː en eɪ ˈniːdl/ | Kim EBUS-TBNA |
| 193 | Double lumen catheter | /ˈdʌbl ˈluːmən ˈkæθɪtə/ | Catheter hai lòng |
| 194 | Contrast dye | /ˈkɒntrɑːst daɪ/ | Thuốc cản quang |
| 195 | Extravasation | /ɪkˌstrævəˈseɪʃən/ | Thoát mạch |
| 196 | Randomized controlled trials | /ˈrændəmaɪzd kənˈtrəʊld ˈtraɪəlz/ | Thử nghiệm ngẫu nhiên có đối chứng |
| 197 | Dosing | /ˈdəʊsɪŋ/ | Liều lượng |
| 198 | Delivery schedule | /dɪˈlɪvəri ˈʃedjuːl/ | Lịch trình đưa thuốc |
| 199 | Drug delivery platform | /drʌɡ dɪˈlɪvəri ˈplætfɔːm/ | Nền tảng đưa thuốc |
| 200 | Frequency of administration | /ˈfriːkwənsi əv ədˌmɪnɪˈstreɪʃən/ | Tần suất sử dụng |
