Cẩm nang Hô hấp Can thiệp. Practical Guide to Interventional Pulmonology
Bản quyền (C) 2024 Nhà xuất bản Elsevier.
Ts.Bs. Lê Nhật Huy – Ths.Bs. Lê Đình Sáng (Dịch và chú giải)
Chương 17: Soi lồng ngực nội khoa
Medical Thoracoscopy
Pyng Lee
Practical Guide to Interventional Pulmonology, 17, 179-190
MỤC LỤC CHƯƠNG
| GIỚI THIỆU TRANG THIẾT BỊ Dụng cụ Cứng Ống soi Lồng ngực Mềm-Cứng CHỐNG CHỈ ĐỊNH CHUẨN BỊ BỆNH NHÂN VÔ CẢM KỸ THUẬT Sinh thiết Màng phổi Thành có Hướng dẫn qua Nội soi lồng ngực Xử trí Xuất huyết Gây dính Màng phổi bằng Bột Talc qua Nội soi lồng ngực BIẾN CHỨNG ỨNG DỤNG LÂM SÀNG Tràn dịch Màng phổi không rõ Nguyên nhân Ung thư Phổi U trung biểu mô Ác tính Tràn dịch Màng phổi do Lao TÓM TẮT |
GIỚI THIỆU
Soi lồng ngực, phẫu thuật lồng ngực có hỗ trợ bằng video (VATS), soi lồng ngực nội khoa (MT), và soi màng phổi là những thủ thuật xâm lấn tối thiểu giúp tiếp cận khoang màng phổi. Chúng chỉ khác nhau ở phương pháp vô cảm. Trong bài tổng quan này, trọng tâm là soi lồng ngực nội khoa chẩn đoán.
VATS được thực hiện bởi một bác sĩ phẫu thuật trong phòng mổ, thường với thông khí một phổi, ba cổng vào và các dụng cụ cứng. Sinh thiết phổi bằng dập ghim, cắt bỏ các nốt phổi, cắt thùy phổi, cắt toàn bộ phổi, cắt thực quản và mở cửa sổ màng ngoài tim được thực hiện bằng VATS, ngoài ra còn có sinh thiết màng phổi thành có hướng dẫn, dẫn lưu tràn dịch màng phổi hoặc tràn mủ màng phổi, và gây dính màng phổi¹ (Bảng 17.1). Mặt khác, soi lồng ngực nội khoa được thực hiện bởi một bác sĩ chuyên khoa hô hấp trong phòng nội soi dưới gây tê tại chỗ và an thần mức độ vừa. Soi lồng ngực nội khoa cho phép sinh thiết màng phổi thành dưới quan sát trực tiếp với độ chính xác cao. Ngoài ra, nó còn hỗ trợ các can thiệp điều trị như dẫn lưu dịch, đặt ống dẫn lưu ngực có hướng dẫn và gây dính màng phổi. Các bác sĩ ở châu Âu còn thực hiện cắt hạch giao cảm qua soi lồng ngực nội khoa để điều trị chứng tăng tiết mồ hôi vô căn và sinh thiết phổi trong bệnh phổi lan tỏa.
Bảng 17.1 VATS so với Soi lồng ngực Nội khoa (Soi màng phổi)
| Thủ thuật | VATS | Soi lồng ngực Nội khoa |
|---|---|---|
| Nơi thực hiện | Phòng mổ (OR) | Phòng nội soi hoặc phòng mổ |
| Người thực hiện | Bác sĩ phẫu thuật | Bác sĩ không phải phẫu thuật viên đã được đào tạo |
| Vô cảm | Gây mê toàn thân, Đặt nội khí quản hai nòng, Thông khí một phổi | Gây tê tại chỗ, An thần tỉnh, Tự thở |
| Chỉ định | Sinh thiết màng phổi thành, gây dính màng phổi, bóc vỏ màng phổi, sinh thiết phổi bằng dập ghim, cắt bỏ nốt phổi, cắt thùy phổi, cắt toàn bộ phổi, mở cửa sổ màng ngoài tim, cắt thực quản | Sinh thiết màng phổi thành, gây dính màng phổi, đặt ống dẫn lưu ngực dưới quan sát trực tiếp |
| VATS, Phẫu thuật lồng ngực có hỗ trợ bằng video. |
Năm 1910, Hans Christian Jacobaeus, một bác sĩ nội khoa người Thụy Điển, đã mô tả việc thăm khám khoang lồng ngực bằng một ống soi bàng quang cứng gắn với một đèn điện là “thorakoskopie”. Sau đó, ông đã cải tiến kỹ thuật này bao gồm cả việc gỡ dính màng phổi bằng dao đốt điện, còn được gọi là phẫu thuật Jacobaeus, để làm xẹp phổi bị lao vì vào thời điểm đó chưa có liệu pháp kháng lao hiệu quả. ⁵⁶ Tại một buổi thuyết trình trước Hiệp hội Bác sĩ Phẫu thuật Hoa Kỳ, Jacobaeus cho rằng “trong việc chẩn đoán phân biệt giữa các khối u và viêm màng phổi do nguyên nhân khác, soi lồng ngực có giá trị không nhỏ”. Ông là người ủng hộ mạnh mẽ cho việc sinh thiết có hướng dẫn qua nội soi lồng ngực trong đánh giá tràn dịch màng phổi không rõ nguyên nhân và đã áp dụng soi lồng ngực như một công cụ chẩn đoán và điều trị.
TRANG THIẾT BỊ
Dụng cụ Cứng
Trong lịch sử, các dụng cụ cứng như trocars và ống soi bằng thép không gỉ là trung tâm của kỹ thuật này.³⁻⁹ Soi lồng ngực bằng dụng cụ cứng đòi hỏi nguồn sáng xenon lạnh, một camera nội soi gắn vào thị kính của ống soi, một màn hình video và máy ghi hình (Hình 17.1). Ống soi 0 độ hữu ích cho việc quan sát trực tiếp trong khi các ống soi góc nghiêng (30 hoặc 50 độ) và ống soi tiềm vọng (90 độ) cung cấp một cái nhìn toàn cảnh khoang màng phổi. Việc lựa chọn trocars với các kích cỡ khác nhau (đường kính 5-13 mm) và làm bằng nhựa dùng một lần hoặc thép không gỉ tái sử dụng, cũng như các ống soi cứng với các góc nhìn khác nhau, phụ thuộc vào sở thích của người thực hiện và tình trạng của bệnh nhân. Một trocar lớn có thể chứa một ống soi lớn hơn với quang học tốt hơn sẽ cải thiện chất lượng thăm khám; tuy nhiên, việc chèn ép dây thần kinh liên sườn trong quá trình thao tác trocar có thể gây khó chịu nhiều hơn, đặc biệt nếu soi lồng ngực nội khoa được thực hiện dưới gây tê tại chỗ và an thần mức độ vừa. Một trocar 7 mm, ống soi 0 độ 4 mm hoặc 7 mm, và kìm sinh thiết quang học 5 mm thường cho phép sinh thiết màng phổi hiệu quả mà không cần đến cổng thứ hai và thường là phương pháp tiếp cận ban đầu được sử dụng cho soi lồng ngực bằng dụng cụ cứng.⁴,⁸,⁹
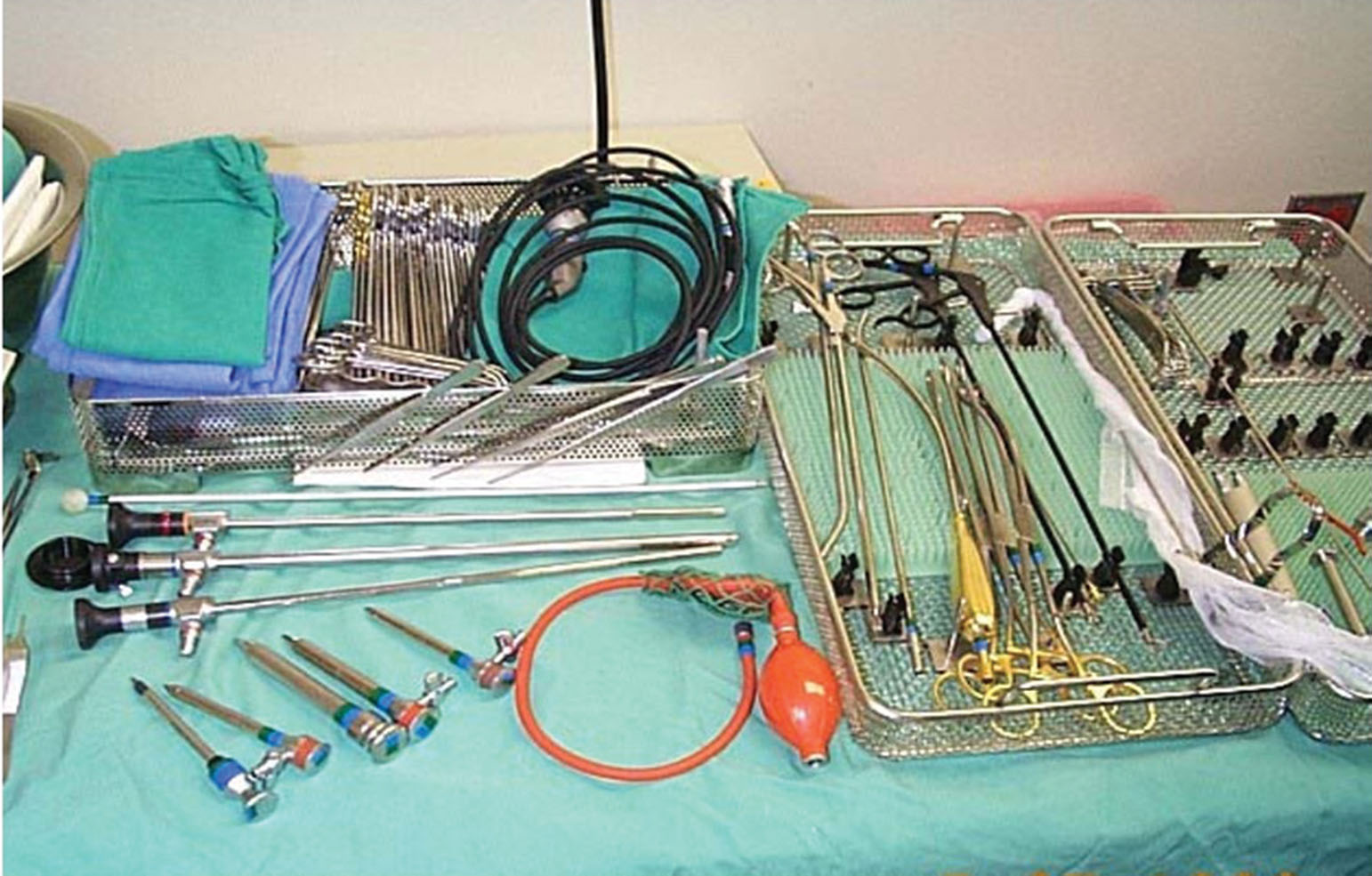
Hình 17.1 Dụng cụ trocars cứng, ống soi và các phụ kiện.
Tassi và Marchetti đã báo cáo về chất lượng hình ảnh tuyệt vời của khoang màng phổi khi sử dụng ống soi 3.3 mm cho một nhóm bệnh nhân bị tràn dịch màng phổi khu trú nhỏ mà không thể tiếp cận bằng các dụng cụ kích thước tiêu chuẩn. Hai trocars 3.8 mm đã được sử dụng: một cho ống soi 3.3 mm và một cho kìm sinh thiết 3 mm. Hiệu suất chẩn đoán đạt 93.4%, tương đương với hiệu suất đạt được khi sử dụng kìm sinh thiết 5 mm thông thường.¹⁰
Ống soi Lồng ngực Mềm-Cứng
Ống soi lồng ngực mềm-cứng là một tiến bộ trong lĩnh vực soi lồng ngực nội khoa vì nó được thiết kế giống như một ống soi phế quản, giúp các bác sĩ đã thành thạo kỹ năng soi phế quản dễ dàng học hơn. Ống soi lồng ngực mềm-cứng có thể hấp tiệt trùng (LTF 160 hoặc 240, Olympus, Tokyo, Nhật Bản) có một tay cầm và một thân ống có đường kính ngoài 7 mm và dài 27 cm. Đoạn gần 22 cm là cứng, trong khi đoạn xa 5 cm là mềm với khả năng gập góc hai chiều (160 độ lên và 130 độ xuống). Nó có một kênh làm việc 2.8 mm có thể chứa kìm sinh thiết, kim, các phụ kiện phẫu thuật lạnh và phẫu thuật điện (Hình 17.2), cũng như tương thích với các bộ xử lý hiện có (CV-160, CLV-U40) và nguồn sáng (CV-240, EVIS-100 hoặc 140, EVIS EXERA-145 hoặc 160) của cùng nhà sản xuất có sẵn trong hầu hết các đơn vị nội soi mà không tốn thêm chi phí.³,¹¹,¹² Thủ thuật thường được thực hiện trong phòng soi phế quản bằng gây tê tại chỗ và an thần mức độ vừa.³,¹² Cần một đường rạch da duy nhất dài 1 cm để đặt trocar mềm dùng một lần để thực hiện soi lồng ngực bằng ống mềm-cứng. Ống soi lồng ngực mềm-cứng cũng được trang bị hình ảnh dải tần hẹp (NBI), một công nghệ làm nổi bật các bất thường niêm mạc và các mẫu mạch máu liên quan đến bệnh ác tính. NBI có thể hỗ trợ phát hiện và sinh thiết các tổn thương màng phổi giai đoạn sớm.
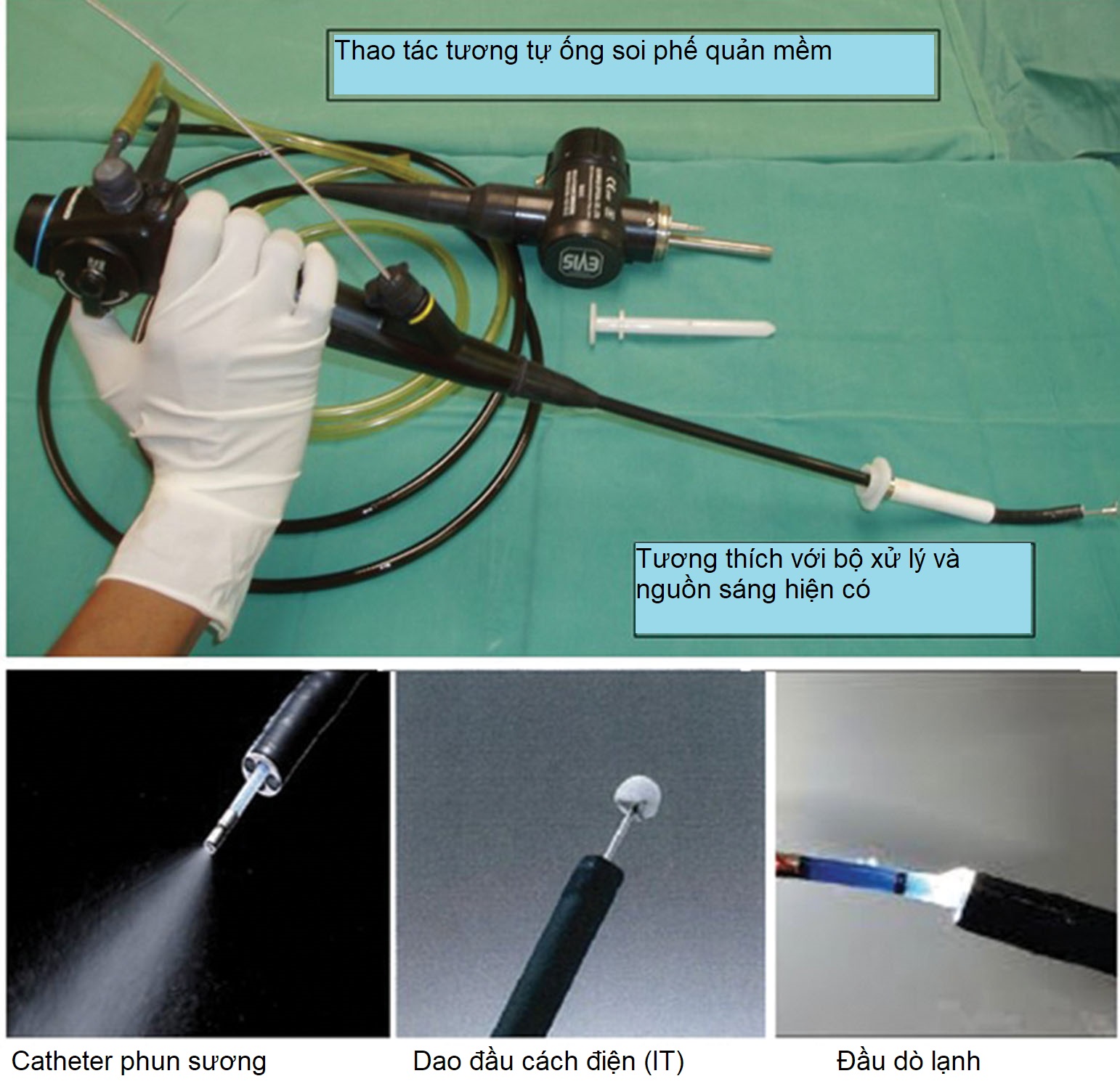
Hình 17.2 Ống soi lồng ngực mềm-cứng (LTF 160/240, Olympus, Tokyo, Nhật Bản). Catheter phun sương, dao đầu cách điện (IT) và đầu dò lạnh.
CHỐNG CHỈ ĐỊNH
Chống chỉ định duy nhất là không có khoang màng phổi do dính. Tuy nhiên, Marchetti và các đồng nghiệp đã chứng minh rằng soi lồng ngực nội khoa có thể được thực hiện an toàn bởi các bác sĩ được đào tạo ở những bệnh nhân không có tràn dịch màng phổi tại các vị trí quan sát thấy dấu hiệu trượt của phổi trên siêu âm lồng ngực. Vì soi lồng ngực nội khoa được thực hiện dưới an thần mức độ vừa ở những bệnh nhân tự thở với phổi xẹp một phần hoặc gần như toàn bộ, bệnh nhân không được có tình trạng thiếu oxy không liên quan đến tràn dịch màng phổi, tình trạng tim mạch không ổn định, tạng xuất huyết, ho khó chữa, hoặc dị ứng với các loại thuốc được sử dụng trong quá trình soi lồng ngực nội khoa.
CHUẨN BỊ BỆNH NHÂN
Bệnh sử và khám thực thể là những thành phần quan trọng của bất kỳ đánh giá tiền phẫu nào. Vị trí vào được chọn sau khi xem xét cẩn thận phim X-quang ngực (CXR), phim chụp tư thế nằm nghiêng, hình ảnh siêu âm (US), và chụp cắt lớp vi tính (CT). Trước khi thực hiện soi lồng ngực nội khoa, 200 đến 300 mL dịch được hút ra khỏi khoang màng phổi bằng kim, angiocath, catheter chọc dò dịch màng phổi, hoặc kim chọc dò màng phổi Boutin. Tràn khí màng phổi được tạo ra bằng cách mở kim ra không khí cho đến khi đạt được trạng thái cân bằng ổn định. Không khí làm cho phổi xẹp ra khỏi thành ngực để tạo điều kiện cho việc đưa trocar vào. Người thực hiện có thể chọn thực hiện soi lồng ngực nội khoa trực tiếp với hình ảnh siêu âm, phương pháp này đã được chứng minh là làm giảm tỷ lệ thất bại khi tiếp cận cũng như giảm nhu cầu gây tràn khí màng phổi do thầy thuốc.
VÔ CẢM
Benzodiazepines (midazolam) kết hợp với opioids (demerol, fentanyl, morphine) cung cấp khả năng giảm đau và an thần tốt. Việc gây tê tại chỗ một cách tỉ mỉ cho lớp biểu bì, cân cơ, các cơ liên sườn và màng phổi thành tại vị trí vào đảm bảo sự thoải mái cho bệnh nhân trong quá trình thao tác ống soi lồng ngực.¹⁵
Việc sử dụng propofol ngày càng tăng trong những năm gần đây để tăng cường sự thoải mái cho bệnh nhân trong quá trình gây dính màng phổi bằng bột talc. Tuy nhiên, việc sử dụng propofol đòi hỏi sự theo dõi của các bác sĩ gây mê ở nhiều quốc gia. Ở những bệnh nhân được dùng propofol điều chỉnh liều theo mức độ thoải mái, 64% bị tụt huyết áp, trong đó 9% cần các biện pháp khắc phục.¹⁶ Khi so sánh propofol với midazolam, tình trạng giảm oxy máu nhiều hơn (27% so với 4%) và tụt huyết áp (82% so với 40%) đã được quan sát thấy ở nhóm dùng propofol, điều này dẫn đến kết luận của các tác giả rằng propofol không nên là lựa chọn an thần hàng đầu cho soi lồng ngực nội khoa.¹⁷
Kiểm soát đau tốt cho việc gây dính màng phổi bằng bột talc đã đạt được bằng cách kết hợp opioids, benzodiazepines, và gây tê màng phổi với tối đa 250 mg lidocaine 1% bằng catheter phun sương.¹⁸ Vô cảm tiền phẫu nên được cá nhân hóa theo tình trạng chung và mong đợi của bệnh nhân; tuy nhiên, các bác sĩ phải nhận thức được các biến cố bất lợi tiềm ẩn liên quan đến thuốc gây mê và sẵn sàng xử trí chúng.
KỸ THUẬT
Bệnh nhân được đặt ở tư thế nằm nghiêng với bên bị ảnh hưởng hướng lên trên. Việc theo dõi liên tục điện tâm đồ, huyết áp và độ bão hòa oxy trong mạch được thực hiện trong suốt quá trình thủ thuật. Mặc dù vị trí vào phụ thuộc vào vị trí của tràn dịch hoặc tràn khí màng phổi, các vị trí nguy hiểm như ngực trước nơi có động mạch vú trong chạy qua, nách với động mạch ngực bên, vùng dưới đòn với động mạch dưới đòn, và cơ hoành nên được tránh. Một cổng duy nhất giữa khoang liên sườn thứ tư và thứ bảy của thành ngực và dọc theo đường nách giữa được ưu tiên cho soi lồng ngực nội khoa chẩn đoán. Cổng thứ hai có thể cần thiết để tạo điều kiện cho việc gỡ dính, dẫn lưu các ổ dịch phức tạp, sinh thiết phổi, hoặc lấy mẫu các tổn thương bệnh lý nằm xung quanh vị trí vào đầu tiên. Có thể cần tiếp cận hai cổng nếu sử dụng các dụng cụ cứng, đặc biệt là xung quanh các khía cạnh sau và trung thất của nửa lồng ngực không thể tiếp cận được do phổi xẹp một phần, hoặc khi nhu mô phổi dính vào thành ngực.⁴,⁸
Một cổng duy nhất thường là đủ cho ống soi lồng ngực mềm-cứng vì đầu mềm của nó cho phép di chuyển dễ dàng trong một không gian màng phổi hạn chế và xung quanh các dải dính.¹¹,¹²,¹⁸ Một ống dẫn lưu ngực được đặt vào cuối thủ thuật soi lồng ngực nội khoa chẩn đoán và khí còn lại được hút ra. Ống được rút ngay khi phổi đã nở lại, và bệnh nhân có thể được xuất viện sau một thời gian quan sát ngắn trong khu vực hồi sức. Nếu thực hiện gây dính màng phổi bằng bột talc hoặc sinh thiết phổi, bệnh nhân sẽ được nhập viện để theo dõi, dẫn lưu ống ngực và tối ưu hóa việc kiểm soát đau.⁴,¹²
Sinh thiết Màng phổi Thành có Hướng dẫn qua Nội soi lồng ngực (Bảng 17.2)
Việc thực hiện sinh thiết màng phổi thành trên một xương sườn là mong muốn để tránh bó mạch thần kinh (Hình 17.3). Kìm dò tìm xương sườn, kẹp lấy màng phổi thành phủ bên trên, và xé màng phổi ra, di chuyển gần như song song và dọc theo thành ngực thay vì “kẹp và kéo” vuông góc với thành ngực. Các mẫu bệnh phẩm thu được bằng kìm cứng lớn hơn so với các mẫu thu được bằng kim Abrams hoặc Cope. Sinh thiết bằng ống soi lồng ngực mềm-cứng nhỏ hơn vì chúng bị giới hạn bởi kích thước của kìm mềm, mà kích thước này lại phụ thuộc vào đường kính của kênh làm việc. Kìm mềm cũng thiếu sức mạnh cơ học cần thiết để lấy các mẫu màng phổi sâu, điều này có thể gây khó khăn nếu nghi ngờ u trung biểu mô. Vấn đề này có thể được khắc phục bằng cách lấy nhiều mẫu sinh thiết (8-12) ở vùng bất thường cũng như nhiều “miếng” ở cùng một khu vực để có được mô đại diện hơn.
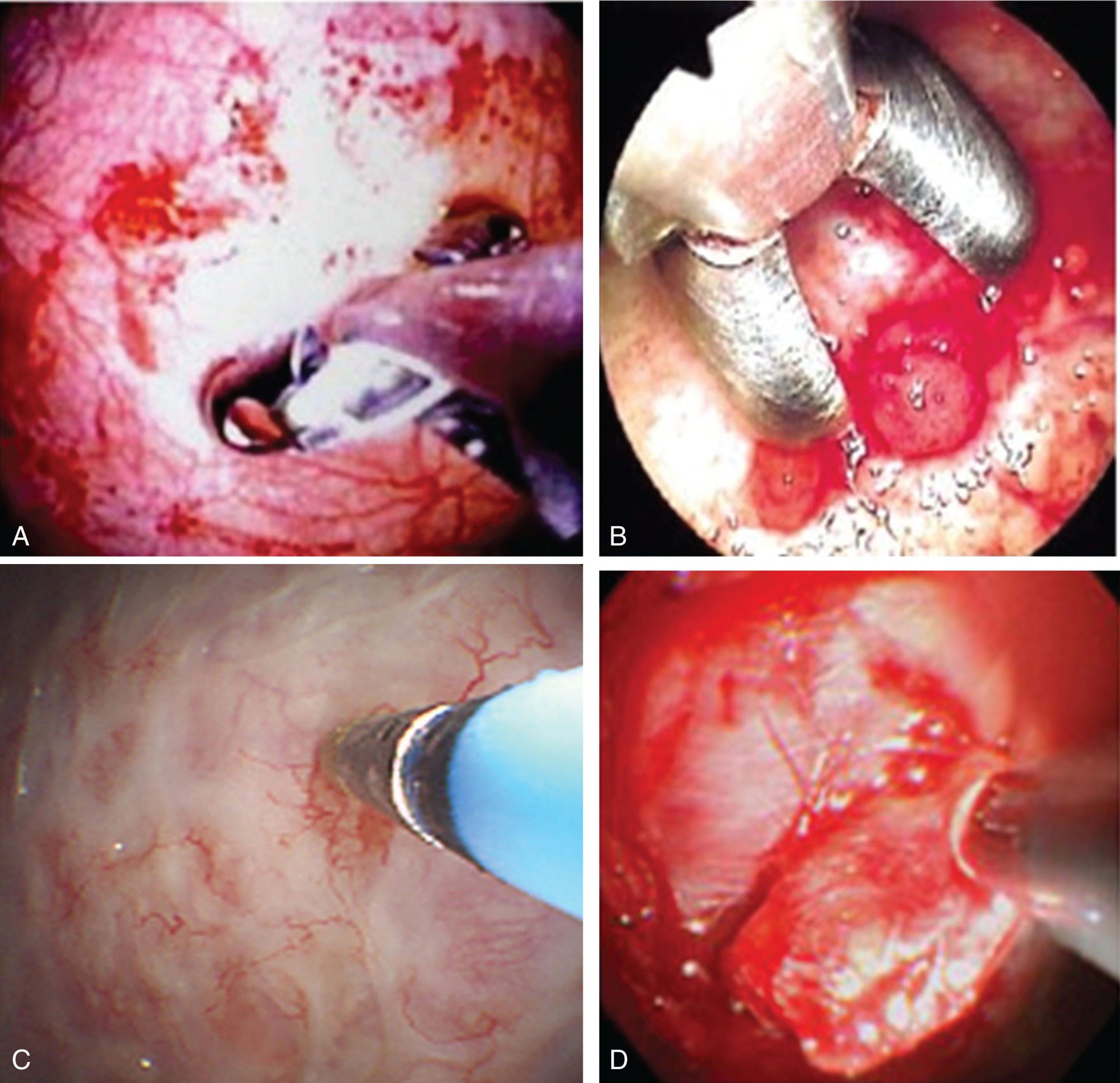
Hình 17.3 Sinh thiết màng phổi thành bằng (A) kìm mềm, (B) kìm quang học cứng, (C) đầu dò lạnh, và (D) dao đầu cách điện.
Các nghiên cứu so sánh cho thấy không có sự khác biệt về hiệu suất chẩn đoán giữa sinh thiết bằng kìm mềm và kìm cứng ngay cả trong trường hợp u trung biểu mô nếu sinh thiết màng phổi có thể được thực hiện thành công.²⁰,²¹ Sinh thiết màng phổi thành toàn bộ độ dày có thể được thực hiện bằng dao điện đầu cách điện (IT) trong quá trình soi lồng ngực bằng ống mềm-cứng. Trong một nghiên cứu, hiệu suất chẩn đoán được báo cáo là 85% và 60% tương ứng với dao IT và kìm mềm. Dao IT đặc biệt hữu ích khi gặp màng phổi thành dày, nhẵn, trong đó gần một nửa là u trung biểu mô ác tính. Sinh thiết lạnh là một phương pháp khác giúp thu được các mẫu bệnh phẩm lớn hơn và bảo tồn tốt hơn cấu trúc tế bào và sự toàn vẹn của mô.
Xử trí Xuất huyết
Nguy cơ chính là xuất huyết do vô tình sinh thiết vào một mạch máu liên sườn. Ấn ngón tay từ bên ngoài vào khoang liên sườn trên vị trí chảy máu là can thiệp đầu tiên trong khi một cổng tiếp cận khác được tạo ra. Bác sĩ sau đó sử dụng hai vị trí vào để kiểm tra và đốt cầm máu các mô cùng một lúc. Có thể dùng áp lực trực tiếp bằng gạc gắn trên kìm từ bên trong để chèn ép vị trí chảy máu. Nối ống dẫn lưu ngực với hệ thống dẫn lưu kín dưới nước cũng làm phổi nở lại, có tác dụng chèn ép vị trí chảy máu. Nếu máu không ngừng chảy với các biện pháp nêu trên, cần hội chẩn phẫu thuật lồng ngực. Các lựa chọn phẫu thuật bao gồm kẹp các mạch máu đang chảy bằng endoclips, mở rộng vết rạch để tạo điều kiện sửa chữa, hoặc thậm chí mở lồng ngực.
Gây dính Màng phổi bằng Bột Talc qua Nội soi lồng ngực
Vì tràn dịch màng phổi ác tính (MPE) có xu hướng tái phát trừ khi khối u nguyên phát nhạy cảm với hóa trị, gây dính màng phổi bằng hóa chất đóng một vai trò không thể thiếu trong việc quản lý MPE tái phát. Ngăn ngừa tái phát bằng gây dính màng phổi bằng hóa chất cũng là một mục tiêu chính đối với tràn khí màng phổi tự phát thứ phát. Gây dính màng phổi bằng hóa chất được thực hiện thông qua việc bơm chất gây dính qua ống liên sườn hoặc catheter lòng nhỏ hoặc qua việc phun bột talc trong quá trình nội soi lồng ngực. Gây dính màng phổi bằng bột talc qua nội soi lồng ngực được thực hiện sau khi hút dịch và sinh thiết màng phổi, và có thể được thực hiện bằng các thiết bị phân phối khác nhau như bình xịt bột talc hoặc bơm tiêm dạng bóng, trong đó talc được đưa vào qua trocar mà không cần quan sát nhưng được phun theo các hướng khác nhau trong khoang màng phổi (Hình 17.4).
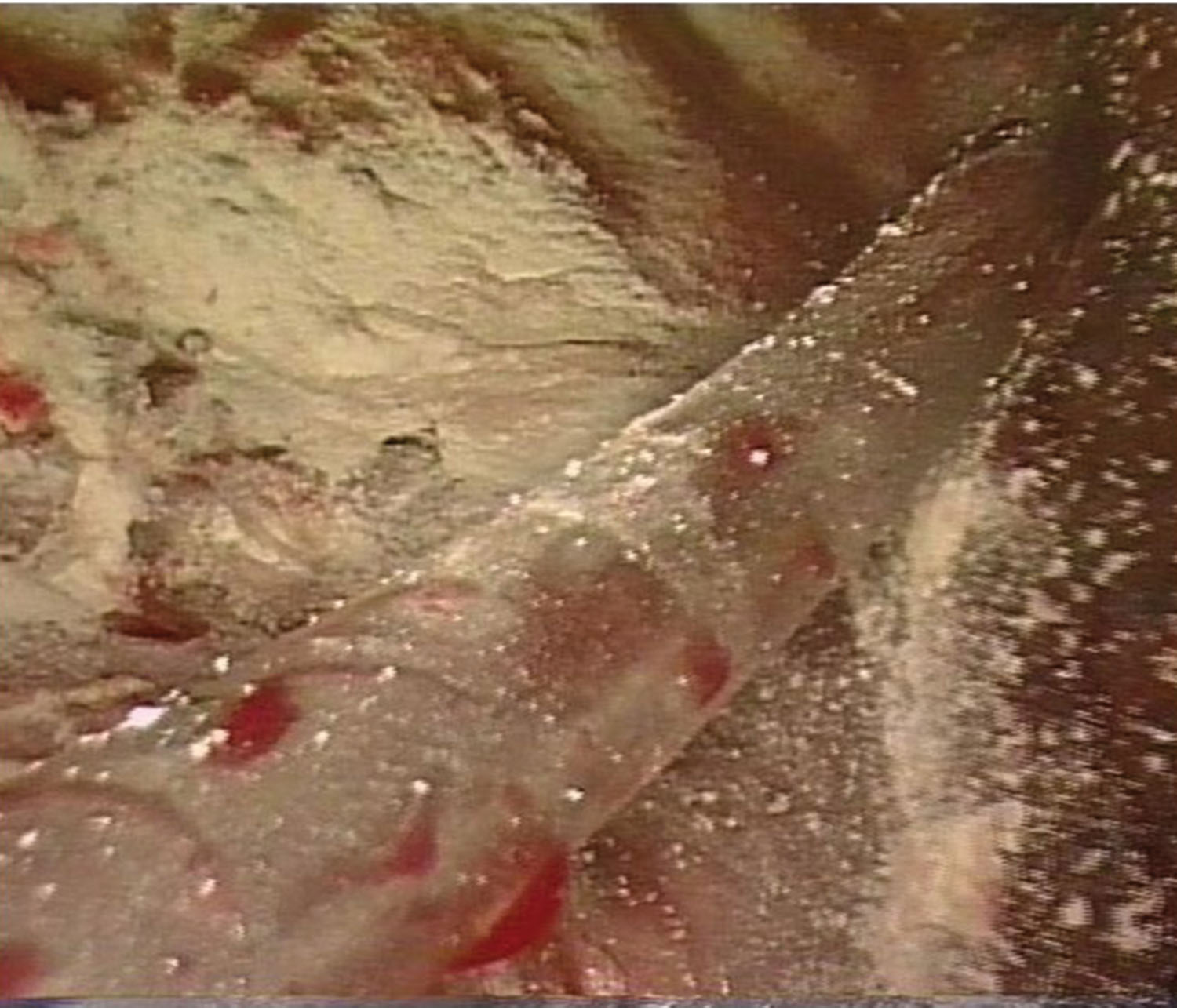
Hình 17.4 Gây dính màng phổi bằng bột talc qua nội soi lồng ngực.
BIẾN CHỨNG
Tỷ lệ tử vong do soi lồng ngực bằng dụng cụ cứng dao động từ 0.09% đến 0.34%.²⁴
Các biến chứng lớn như rò khí kéo dài, xuất huyết, tràn mủ màng phổi, viêm phổi và gieo rắc khối u tại vị trí cổng vào xảy ra ở 1.8%, trong khi các biến chứng nhỏ bao gồm tràn khí dưới da, nhiễm trùng vết mổ, sốt, tụt huyết áp và rối loạn nhịp tim được quan sát thấy ở 7.3% các ca soi lồng ngực nội khoa.²⁵,²⁶
Một biến chứng nghiêm trọng nhưng hiếm gặp liên quan đến việc gây tràn khí màng phổi là thuyên tắc khí (<0.1%).²³ Trong quá trình soi lồng ngực nội khoa, hàng lít dịch màng phổi có thể được loại bỏ với nguy cơ phù phổi do tái giãn nở ở mức tối thiểu do sự cân bằng áp suất ngay lập tức được cung cấp bởi không khí đi vào khoang màng phổi qua trocar. Sốt có thể xảy ra sau khi gây dính màng phổi bằng bột talc và tự khỏi trong vòng 48 giờ, trong khi rò phế quản-màng phổi cần dẫn lưu ngực và hút kéo dài có thể xảy ra sau khi sinh thiết phổi qua nội soi lồng ngực để chẩn đoán bệnh phổi kẽ. Nhiễm trùng vết mổ, viêm phổi và tràn mủ màng phổi có thể phát triển do dẫn lưu ống kéo dài.²⁵,²⁶ Trong các trường hợp u trung biểu mô, sự phát triển của khối u có thể xảy ra tại các vị trí rạch da và có thể được quản lý bằng xạ trị.²⁷
Các biến chứng liên quan đến ống soi lồng ngực mềm-cứng là rất hiếm. Mặc dù không có trường hợp tử vong nào được báo cáo trong một phân tích tổng hợp gần đây trên 755 bệnh nhân trải qua soi lồng ngực bằng ống mềm-cứng,¹¹,²⁸ việc đào tạo về các kỹ thuật đúng đắn không thể được nhấn mạnh quá mức. Bảng 17.2 mô tả loại bệnh nhân phù hợp cho soi lồng ngực bằng dụng cụ cứng hoặc mềm-cứng.
Bảng 17.2 Chỉ định Soi lồng ngực bằng Dụng cụ Cứng hoặc Ống soi Lồng ngực Mềm-Cứng
| Tình huống lâm sàng | Loại thủ thuật |
|---|---|
| Soi lồng ngực chẩn đoán tràn dịch màng phổi không xác định, không biến chứng, nghi ngờ u trung biểu mô không cao | Ống soi lồng ngực mềm-cứng hoặc sử dụng ống soi cứng dưới gây tê tại chỗ |
| Phổi bị kẹt với màng phổi dày trên phim X-quang | Kìm sinh thiết quang học cứng** hoặc ống soi lồng ngực mềm-cứng với kìm mềm thực hiện nhiều lần bấm ở cùng một khu vực để lấy mẫu có độ sâu đủ hoặc sử dụng kìm mềm, dao IT, hoặc sinh thiết lạnh |
| Nghi ngờ u trung biểu mô | Kìm sinh thiết quang học cứng hoặc ống soi lồng ngực mềm-cứng với dao IT hoặc sinh thiết lạnh** |
| Dính màng phổi-phổi | Dính sợi: kìm sinh thiết quang học cứng hoặc ống soi lồng ngực mềm-cứng với các phụ kiện dao đốt điện. Dính mỏng, dạng sợi tơ huyết: ống soi lồng ngực mềm-cứng với kìm mềm |
| Tràn mủ màng phổi, dấu hiệu màng phổi tách đôi, tràn dịch màng phổi khu trú | Dụng cụ cứng (VATS) hoặc chuyển sang mở lồng ngực để bóc vỏ màng phổi |
| Tràn khí màng phổi với bóng khí hoặc kén khí | Dụng cụ cứng (VATS) để cắt bóng khí bằng dập ghim |
*Chỉ định thủ thuật được ưu tiên. IT, đầu cách điện; VATS, phẫu thuật lồng ngực có hỗ trợ bằng video.
ỨNG DỤNG LÂM SÀNG
Tràn dịch Màng phổi không rõ Nguyên nhân
Chọc dò dịch màng phổi là bước đầu tiên trong việc đánh giá một ca tràn dịch màng phổi. Vì hơn một nửa số ca tràn dịch tiết là do bệnh ác tính ở các nước phát triển, xét nghiệm tế bào học dịch màng phổi có thể là một xét nghiệm xác định đơn giản. Độ nhạy chẩn đoán của chọc dò dịch màng phổi phụ thuộc vào bản chất của khối u ác tính nguyên phát và mức độ lan rộng của bệnh.²⁹ Một lần hút dịch màng phổi duy nhất có giá trị chẩn đoán bệnh ác tính trong 60% trường hợp và 30% trường hợp u trung biểu mô.³⁰,³¹ Lần lấy mẫu thứ hai làm tăng hiệu suất thêm 15% và lần lấy mẫu thứ ba không đóng góp thêm ngay cả khi gửi các thể tích lớn (>50 mL).⁵²
Sinh thiết màng phổi “mù” hay kín có kết quả dương tính trong 40% các ca MPE do sự liên quan màng phổi dạng đốm. Bệnh ác tính có xu hướng ảnh hưởng đến góc sườn hoành và cơ hoành, những nơi không thể tiếp cận bằng sinh thiết màng phổi kín, do đó việc thêm sinh thiết màng phổi kín vào xét nghiệm tế bào học dịch màng phổi chỉ làm tăng hiệu suất chẩn đoán bệnh ác tính thêm 7%-27% và 20% đối với u trung biểu mô.³³,³⁴ CT lồng ngực có cản quang vượt trội hơn CT tiêu chuẩn trong việc mô tả các MPE, và các đặc điểm như dạng nốt, không đều, và độ dày màng phổi >1 cm là rất gợi ý bệnh ác tính.³⁰,³⁵,³⁶ Chụp ảnh màng phổi bằng siêu âm tại giường hiện là tiêu chuẩn chăm sóc để lựa chọn các vị trí thích hợp cho chọc dò dịch màng phổi, mở lồng ngực đặt ống dẫn lưu và soi lồng ngực nội khoa. Vì siêu âm đã được chứng minh là cải thiện sự an toàn và giảm tỷ lệ thất bại khi tiếp cận, các hướng dẫn quốc gia khuyến nghị sử dụng siêu âm để hướng dẫn tất cả các thủ thuật màng phổi.¹²,¹³,³⁰ Các đặc điểm siêu âm như nốt màng phổi, dày màng phổi >10 mm, và dày cơ hoành >7 mm là gợi ý bệnh ác tính, với độ nhạy 73% và độ đặc hiệu 100%.³⁷ Một “dấu hiệu xoáy tăng âm”, được mô tả là nhiều hạt tăng âm trôi nổi tự do xoáy trong khoang màng phổi trong quá trình hô hấp hoặc nhịp tim, là một dấu hiệu khác gợi ý MPE.³⁸ Các đặc điểm CT và siêu âm có thể gợi ý di căn màng phổi nhưng chẩn đoán bệnh học là cần thiết, và ở những nơi không có sẵn soi lồng ngực nội khoa, sinh thiết màng phổi có hướng dẫn của CT hoặc siêu âm vượt trội hơn sinh thiết lõi kim (CNB). Trong một thử nghiệm ngẫu nhiên, sinh thiết có hướng dẫn của CT đối với màng phổi dày >5mm đã đạt hiệu suất 87% cho bệnh ác tính so với 47% với CNB sử dụng kim Abrams.³⁹ Sinh thiết có hướng dẫn của siêu âm đối với các tổn thương màng phổi >20 mm bằng kim cắt 14-gauge cho hiệu suất 85.5% cho bệnh ác tính, 100% cho u trung biểu mô ác tính, và tỷ lệ tràn khí màng phổi là 4%.⁴⁰ Loại kim dường như quan trọng; kim Tru-Cut tốt hơn kim Menghini cải tiến cho bệnh ác tính (95.4% so với 85.8%), và kim Abrams cũng vượt trội hơn cho tràn dịch do lao.⁴²
Các hình ảnh màng phổi bất thường không phải lúc nào cũng được nhìn thấy trên CT có cản quang. Trong một nghiên cứu so sánh các chẩn đoán được báo cáo trên CT với kết quả mô học bằng soi lồng ngực nội khoa, độ nhạy của báo cáo CT về bệnh ác tính là 68%, điều này ngụ ý rằng một số lượng đáng kể bệnh nhân bị bệnh ác tính mặc dù có kết quả CT âm tính. Vì vậy, chỉ riêng các phát hiện trên CT là không đủ để loại trừ bệnh ác tính, và do đó cần có các nghiên cứu xác định quy trình chẩn đoán.⁴³,⁴⁴
Khoảng 20% các ca tràn dịch màng phổi vẫn chưa được chẩn đoán mặc dù đã chọc dò dịch màng phổi nhiều lần và sinh thiết kim có hướng dẫn bằng hình ảnh. Đây là lúc soi lồng ngực nội khoa đóng một vai trò quan trọng²⁵,⁴⁵ để tăng cường khả năng chẩn đoán của chúng ta khi các xét nghiệm xâm lấn tối thiểu khác thất bại. Nếu nghi ngờ mạnh mẽ về một khối u, độ nhạy chẩn đoán của việc thăm dò và sinh thiết qua nội soi lồng ngực đạt gần 90%-100%.¹⁰,¹¹,¹⁹,²⁰,²⁵,²⁸ Các đặc điểm nội soi như nốt, khối đa polyp, và “giọt sáp nến” rất gợi ý bệnh ác tính (Hình 17.4) nhưng u trung biểu mô giai đoạn sớm có thể giống như viêm màng phổi (Hình 17.5).⁴⁵,⁴⁶
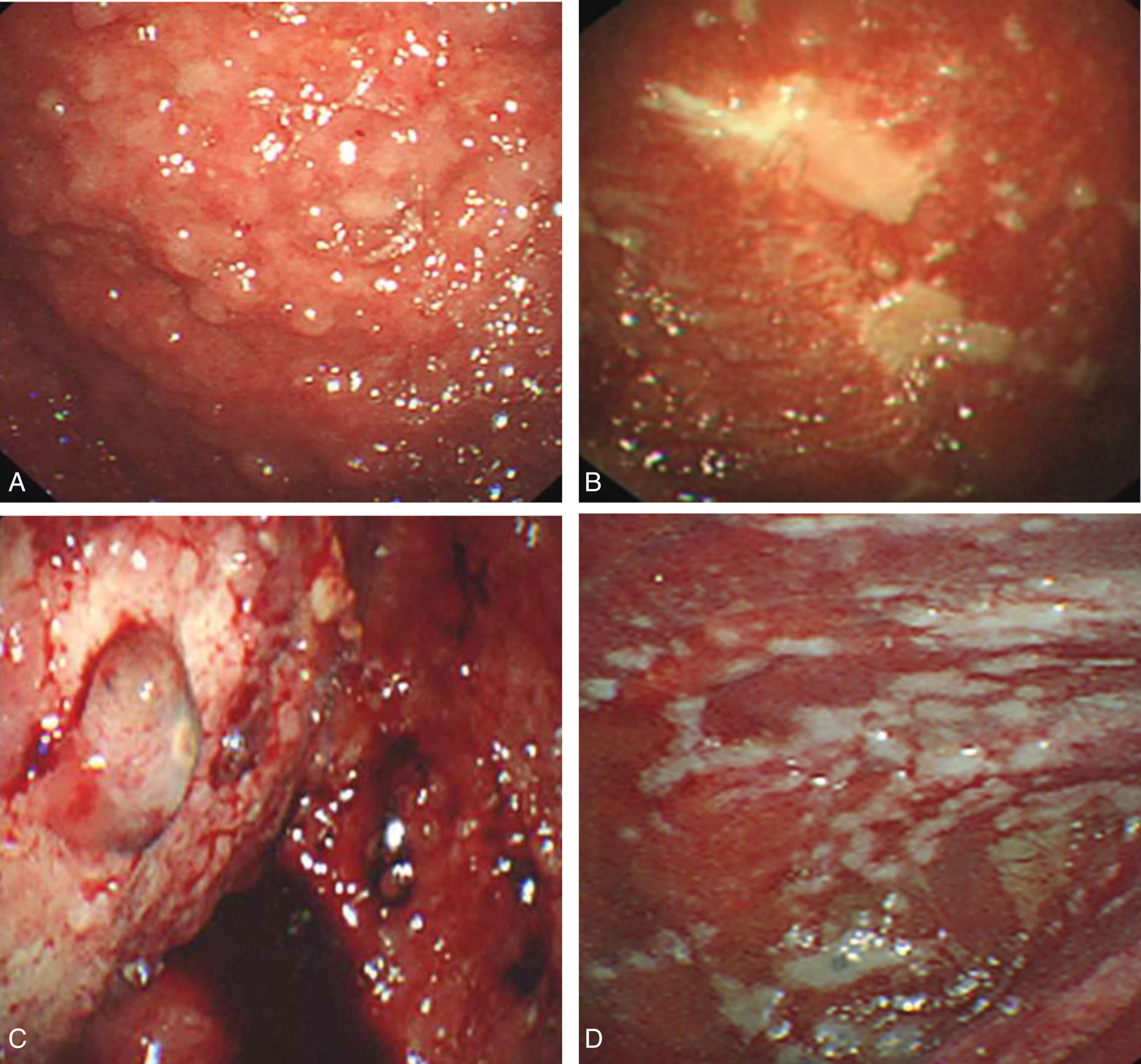
Hình 17.5 Hình ảnh nội soi các khối đa polyp (A,B) và các nốt sáp nến (C,D).
Chrysanthidis và Janssen đã tiến hành một nghiên cứu để xác định xem chế độ tự phát huỳnh quang (Richard Wolf GmbH, Knittlingen, Đức) có thể phân biệt các tổn thương ác tính giai đoạn sớm với viêm không đặc hiệu hay không để giúp nhắm mục tiêu các vị trí sinh thiết trong quá trình nội soi lồng ngực và giúp xác định ranh giới khối u để phân giai đoạn chính xác hơn. Sử dụng đèn xenon 300 W trong dải màu xanh tím (390-460 nm), sự thay đổi màu sắc từ trắng/hồng sang đỏ đã được chứng minh trong tất cả các trường hợp viêm màng phổi ác tính (độ nhạy 100%). Chúng được xác định dễ dàng và ranh giới của chúng được xác định rõ hơn với nội soi lồng ngực tự phát huỳnh quang. Tuy nhiên, sự thay đổi màu sắc từ trắng/hồng sang cam/đỏ cũng được quan sát thấy trong hai trường hợp viêm màng phổi mạn tính, do đó độ đặc hiệu của nội soi lồng ngực tự phát huỳnh quang là 75% đối với bệnh ác tính. Các tác giả kết luận rằng nội soi lồng ngực tự phát huỳnh quang có ít giá trị đối với những bệnh nhân có tổn thương màng phổi lan rộng do bệnh ác tính dễ chẩn đoán bằng nội soi lồng ngực ánh sáng trắng, nhưng chế độ tự phát huỳnh quang có thể hữu ích cho các bệnh ác tính màng phổi giai đoạn sớm.⁴⁷
NBI là một tính năng của ống soi lồng ngực mềm-cứng (Olympus LTF-160). NBI sử dụng các dải tần hẹp không lọc trong các bước sóng ánh sáng xanh (415nm) và xanh lá cây (540 nm) trùng với đỉnh hấp thụ của oxyhemoglobin và do đó tăng cường cấu trúc mạch máu của các mô. Ở 26 bệnh nhân có tổn thương ác tính ở màng phổi (chín ca u trung biểu mô), không có sự khác biệt về độ chính xác chẩn đoán giữa NBI và nội soi màng phổi bằng video ánh sáng trắng (Hình 17.6).⁴⁸ Các quan sát tương tự đã được thực hiện ở 45 bệnh nhân (dữ liệu chưa công bố, Bệnh viện Đại học Quốc gia, Singapore) trong đó 32 người bị di căn màng phổi, 12 người bị viêm màng phổi do lao, và 1 người bị viêm màng phổi không đặc hiệu. Mặc dù mạch máu màng phổi được chụp ảnh tốt bằng NBI, rất khó để phân biệt tân mạch khối u với viêm dựa trên các mẫu mạch máu. Ở những bệnh nhân bị bệnh ác tính di căn màng phổi, NBI đã xác định rõ ranh giới khối u nhưng không cải thiện được chất lượng của các mẫu sinh thiết thu được.
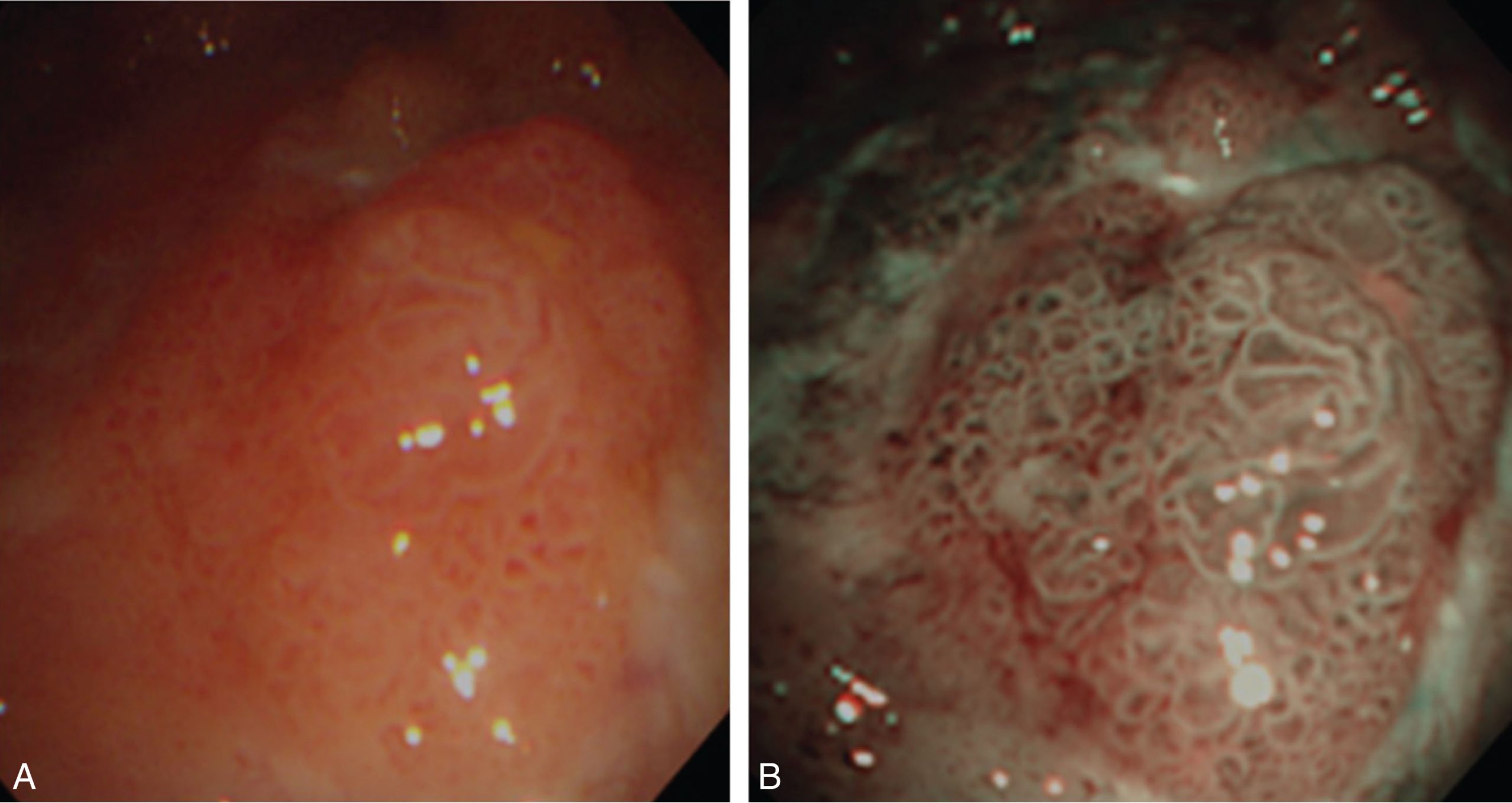
Hình 17.6 Ánh sáng trắng (A) so với hình ảnh dải tần hẹp (B) của di căn màng phổi do ung thư vú.
Baas và các đồng nghiệp đã nghiên cứu xem việc sử dụng axit 5-aminolevulinic (ALA) trước khi thực hiện VATS có thể dẫn đến việc phát hiện và phân giai đoạn bệnh ác tính lồng ngực tốt hơn hay không. 5-ALA được dùng qua đường uống 3-4 giờ trước khi thực hiện VATS và khoang màng phổi được kiểm tra trước tiên bằng ánh sáng trắng sau đó là nội soi lồng ngực huỳnh quang (Hệ thống tự phát huỳnh quang D light, Karl Storz, Tuttlingen, Đức). Lấy mẫu mô ở tất cả các khu vực bất thường đã được thực hiện, và các chẩn đoán mô học được so sánh với các phát hiện qua nội soi lồng ngực. Mặc dù nội soi lồng ngực có hướng dẫn bằng hình ảnh huỳnh quang không vượt trội hơn nội soi lồng ngực ánh sáng trắng, nó đã dẫn đến việc nâng giai đoạn ở 4 trong số 15 bệnh nhân bị u trung biểu mô do hình ảnh hóa tốt hơn các tổn thương màng phổi tạng mà không thể phát hiện được bằng ánh sáng trắng. Mặc dù có một số biến chứng sau phẫu thuật được báo cáo, các tác giả kết luận rằng nội soi lồng ngực huỳnh quang sử dụng 5-ALA là khả thi với các tác dụng phụ tối thiểu, và nó có thể có các ứng dụng tiềm năng trong chẩn đoán và phân giai đoạn u trung biểu mô.⁴⁹
Nội soi vi thể laser đồng tiêu dựa trên đầu dò (pCLE) cung cấp hình ảnh thời gian thực của đường thở, phế nang, khối u phổi, màng phổi và các hạch bạch huyết với độ phân giải 3.5 µm, độ sâu 70 µm và trường nhìn 600 µm. Nó tương thích với ống soi phế quản và ống soi lồng ngực nội khoa và có thể được đưa vào kim cho các can thiệp qua da lồng ngực dựa trên kim. Một đầu dò sợi quang được đưa qua kênh làm việc của ống soi phế quản, ống soi lồng ngực, hoặc kim (nCLE), và hướng đến khu vực quan tâm nơi nó chiếu sáng mô bằng ánh sáng laser (488 nm). Ánh sáng phản xạ trong tiêu điểm sẽ đi qua lỗ kim, tạo ra hình ảnh có độ phân giải cao. Di chuyển chùm tia laser theo chiều dọc hoặc chiều ngang cho phép tái tạo hình ảnh 3D bằng phần mềm đặc biệt.
Cả pCLE và nCLE đều đã được sử dụng để đánh giá các tổn thương màng phổi. Bonhomme và các đồng nghiệp đã cho thấy hình ảnh pCLE của màng phổi bình thường, di căn màng phổi của ung thư phổi không tế bào nhỏ, và u trung biểu mô. pCLE có thể phân biệt được sự liên quan bình thường với ác tính của màng phổi. Một nghiên cứu tiếp theo đã được thực hiện chứng minh rằng pCLE và nCLE có thể phân biệt u trung biểu mô ác tính với xơ hóa màng phổi để hướng dẫn sinh thiết.⁵¹ Một nghiên cứu ex vivo khác đã tìm thấy độ nhạy và độ đặc hiệu cao đối với bệnh ác tính màng phổi với pCLE trong tràn dịch màng phổi.⁵²
Ung thư Phổi
Tràn dịch màng phổi liên quan đến ung thư xảy ra do xâm lấn trực tiếp, thuyên tắc khối u đến màng phổi tạng với sự gieo rắc thứ phát đến màng phổi thành, lây lan theo đường máu hoặc đường bạch huyết. Nhuộm elastin và kiểm tra cẩn thận sự xâm lấn ra ngoài lớp đàn hồi của màng phổi tạng nên được thực hiện đối với các ca cắt bỏ ung thư phổi vì sự xâm lấn màng phổi tạng rất quan trọng để phân giai đoạn khi không có sự liên quan của hạch. Rất hiếm khi tìm thấy ung thư phổi có thể cắt bỏ trong bối cảnh tràn dịch màng phổi dịch tiết mặc dù xét nghiệm tế bào học âm tính. Soi lồng ngực nội khoa có thể đánh giá khả năng phẫu thuật bằng cách xác định xem tràn dịch màng phổi là cận ác tính hay do di căn.²⁵ Nếu phát hiện di căn màng phổi, chúng biểu thị bệnh lan tỏa với tuổi thọ giảm và có thể thực hiện gây dính màng phổi bằng bột talc hoặc đặt catheter màng phổi có đường hầm trong cùng một lần.⁵³
U trung biểu mô Ác tính
Thời gian sống trung bình của một bệnh nhân được chẩn đoán mắc u trung biểu mô ác tính là từ 6 đến 18 tháng, và tử vong xảy ra do suy hô hấp.⁵³ U trung biểu mô ác tính bị nghi ngờ ở một bệnh nhân có tiền sử tiếp xúc với amiăng và hình ảnh X-quang ngực đặc trưng của tràn dịch màng phổi không có sự dịch chuyển trung thất sang bên đối diện. Chẩn đoán bằng tế bào học dịch màng phổi, ngay cả với sinh thiết màng phổi kín, cũng rất khó khăn, điều này thúc đẩy một số bác sĩ ủng hộ sinh thiết mở bằng phẫu thuật mở lồng ngực nhỏ hoặc bên để có được các mẫu bệnh phẩm có kích thước và số lượng đủ cho các nhuộm hóa mô miễn dịch. Mesothelin trong dịch màng phổi và yếu tố thúc đẩy megakaryocyte , có nguồn gốc từ một protein tiền chất chung, đã cho thấy độ nhạy 65% và độ đặc hiệu 95% đối với u trung biểu mô màng phổi trong một nghiên cứu lớn trên 507 bệnh nhân.⁵⁵
Soi lồng ngực nội khoa được ưa chuộng hơn phẫu thuật mở lồng ngực vì các mẫu bệnh phẩm màng phổi thu được bằng kìm cứng 5 hoặc 7 mm tương đương với sinh thiết mở.⁵⁶ Soi lồng ngực nội khoa cho phép thực hiện phân giai đoạn một cách xâm lấn tối thiểu với độ nhạy tốt. VATS huỳnh quang với 5-ALA nên được xem là thử nghiệm nhưng có thể cải thiện độ chính xác của việc phân giai đoạn. Sự đầy đủ của việc lấy mẫu mô thu được bằng kìm mềm là một mối quan tâm trong các trường hợp u trung biểu mô, vì vậy sinh thiết bằng kìm quang học cứng 5 mm, dao IT, hoặc sinh thiết lạnh được khuyến nghị để xác định chẩn đoán.²¹,²²,⁵⁵⁻⁵⁷ Vì u trung biểu mô nổi tiếng về việc gieo rắc, các vị trí sinh thiết, soi lồng ngực nội khoa, và ống dẫn lưu ngực nên được chọn cẩn thận để tránh sự liên quan và gieo rắc của khối u. Boutin và các đồng nghiệp đã khuyến nghị xạ trị dự phòng 7 Gy trong ba ngày liên tiếp trong vòng 2 tuần sau khi soi lồng ngực nội khoa; tuy nhiên, một thử nghiệm ngẫu nhiên gần đây so sánh xạ trị ngay tại vị trí dẫn lưu (21 Gy trong ba phân liều) với chăm sóc hỗ trợ tốt nhất ở 61 bệnh nhân đã không cho thấy bất kỳ sự khác biệt nào về sự xuất hiện của di căn theo đường rạch.⁵⁹ Do đó, xạ trị dự phòng đến các vị trí soi lồng ngực nội khoa và dẫn lưu vẫn còn gây tranh cãi. Vì chỉ có 5% bệnh nhân phù hợp cho phẫu thuật chữa khỏi, một phương pháp tiếp cận giảm nhẹ hướng tới việc giảm khó thở tích cực bằng cách loại bỏ dịch màng phổi, gây dính màng phổi bằng bột talc, kiểm soát đau, và xạ trị dự phòng các vị trí rạch đã mang lại sự kiểm soát triệu chứng tốt.⁶² Trong các trường hợp tràn dịch màng phổi có triệu chứng tái phát, catheter màng phổi có đường hầm có thể là một lựa chọn khả thi.⁶⁰
Tràn dịch Màng phổi do Lao
Hiệu suất chẩn đoán của sinh thiết màng phổi kín trong tràn dịch màng phổi do lao là khác nhau. Trong một nghiên cứu tiến cứu trên 100 ca tràn dịch do lao ở Đức, chẩn đoán mô học ngay lập tức đã được xác định ở 94% bằng soi lồng ngực nội khoa so với 38% bằng sinh thiết màng phổi kín (Hình 17.7). Hiệu suất dương tính từ cấy mô cũng cao hơn với các mẫu sinh thiết có hướng dẫn của soi lồng ngực nội khoa so với mô sinh thiết màng phổi kín và dịch màng phổi kết hợp. Các kết quả tương tự đã được báo cáo bởi một nghiên cứu khác được thực hiện ở một quốc gia lưu hành bệnh lao (TB), nơi các mẫu sinh thiết màng phổi có hướng dẫn của soi lồng ngực nội khoa đạt hiệu suất vượt trội hơn sinh thiết màng phổi kín bằng kim Abrams (98% so với 80%). Nhìn chung, có vẻ như soi lồng ngực nội khoa vượt trội hơn sinh thiết màng phổi kín để chẩn đoán lao, và có thể là lựa chọn đầu tiên nếu lo ngại về lao kháng thuốc vì có thể lấy được số lượng lớn mô màng phổi qua soi lồng ngực nội khoa để cấy. Ngoài ra, gỡ dính cũng có thể được thực hiện để thúc đẩy dẫn lưu các ổ dịch khu trú.⁶⁴
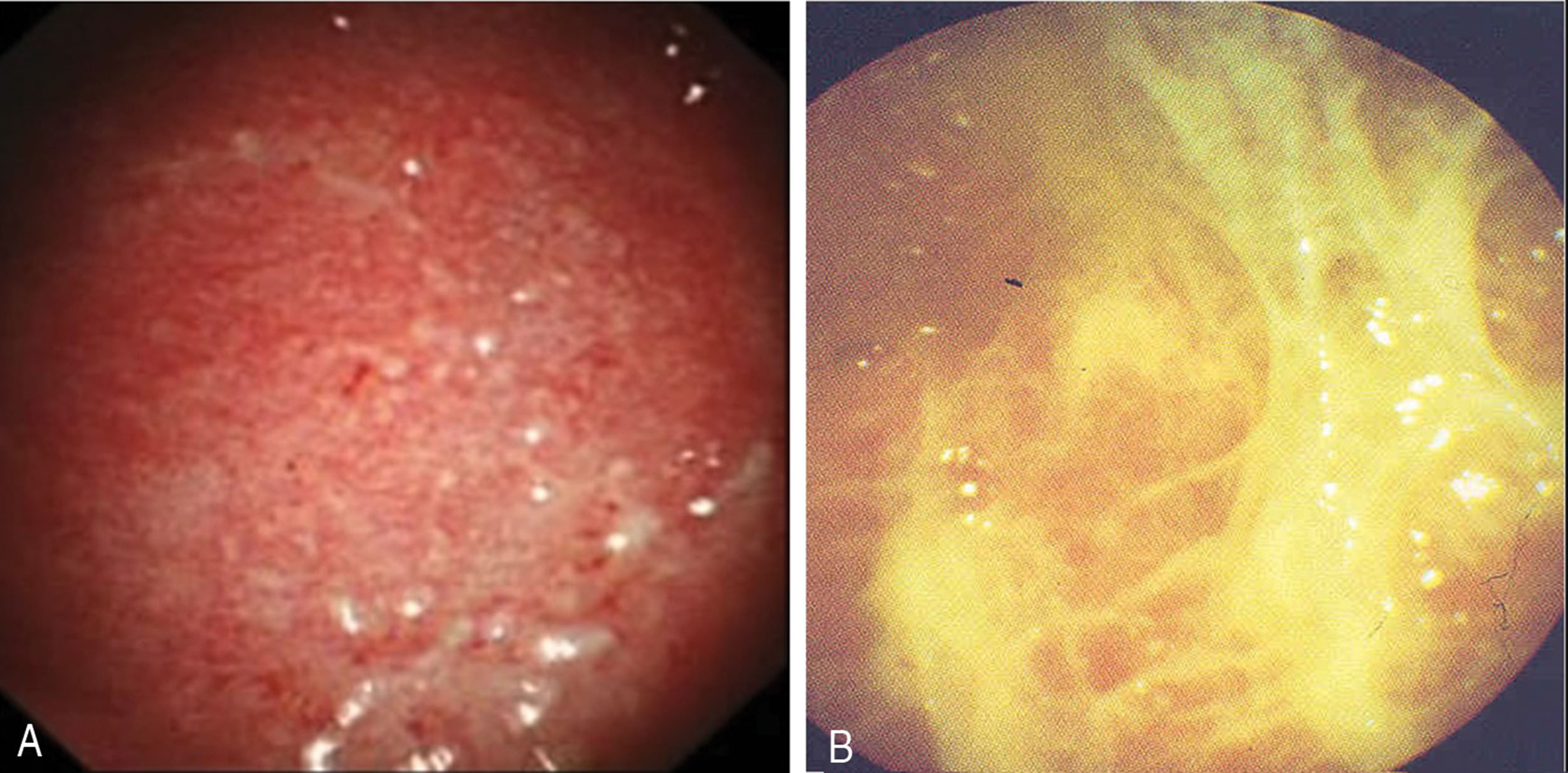
Hình 17.7 (A) Nốt sago và (B) dính dạng sợi tơ huyết trong tràn dịch do lao.
TÓM TẮT
Soi lồng ngực nội khoa chẩn đoán có hiệu quả trong việc đánh giá các bệnh lý màng phổi và phổi khi phân tích dịch thông thường và tế bào học thất bại. Ở nhiều cơ sở có sẵn phương tiện cho soi lồng ngực nội khoa, nó được sử dụng sau khi lần chọc dò dịch màng phổi đầu tiên không xác định được chẩn đoán và cho thấy một ca tràn dịch tiết không rõ nguyên nhân. Soi lồng ngực nội khoa cũng có thể được sử dụng để phá vỡ các ổ khu trú trong các ca tràn dịch cận viêm phổi phức tạp. Đối với những bệnh nhân bị MPE tái phát, soi lồng ngực nội khoa kết hợp với gây dính màng phổi bằng bột talc có thể được sử dụng để dẫn lưu dịch hiệu quả và thực hiện gây dính màng phổi. Điều này cũng hữu ích trong các trường hợp tràn khí màng phổi khi cần gây dính màng phổi.
Việc đào tạo về soi lồng ngực nội khoa là cần thiết; Hiệp hội Bác sĩ Lồng ngực Hoa Kỳ khuyến nghị thực hiện 20 thủ thuật có giám sát trước khi người thực hiện được coi là có năng lực và 10 thủ thuật mỗi năm để duy trì năng lực.⁶⁵ Ống soi lồng ngực mềm-cứng là một phát minh quan trọng trong kỷ nguyên của các thủ thuật màng phổi xâm lấn tối thiểu và có khả năng thay thế các phương pháp sinh thiết truyền thống. Tương lai của soi lồng ngực nội khoa sẽ xác định “khi nào và làm thế nào” để áp dụng các dụng cụ mềm-cứng và cứng để đánh giá các bệnh lý màng phổi-phổi.
TÀI LIỆU THAM KHẢO
- McKenna Jr. RJ. Thoracoscopic evaluation and treatment of pulmonary disease. Surg Clin North Am. 2002:80:1543-1553.
- Yim AP, Lee TW, Izzat MB, Wan S. Place of video-thoracoscopy in thoracic surgical practice. World J Surg. 2001;25:157-161.
- Lee P, Mathur PN, Colt HG. Advances in thoracoscopy: 100 years since Jacobaeus. Respiration. 2010;79:177-186.
- Tassi GF, Davies RJ, Noppen M. Advanced techniques in medical thoracoscopy. Eur Respir J. 2006;28:1051-1059.
- Moisiuc FV, Colt HG. Thoracoscopy: origins revisited. Respiration. 2007;74:344-355.
- Jacobaeus HC. Uber die Möglichkeit, die Zystoskopie bei Untersuchungen seröser Höhlungen anzuwenden. MunchMed Wschr. 1910;40:2090-2092.
- Jacobaeus HC. The practical importance of thoracoscopy in surgery of the chest. Surg Gynecol Obstet. 1922:34:289-296.
- Loddenkemper R. Thoracoscopy-state of the art. Eur Respir J. 1998;11:213-221.
- Rodriguez-Panadero F, Janssen JP, Astoul P. Thoracoscopy: general overview and place in the diagnosis and management of pleural effusion. Eur Respir J. 2006;28:409-421.
- Tassi G, Marchetti G. Minithoracoscopy: a less invasive approach to thoracoscopy- minimally invasive techniques. Chest. 2003;124:1975-1977.
- Munavvar M, Khan MA, Edwards J, Waqaruddin Z, Mills J. The autoclavable semi-rigid thoracoscope: the way forward in pleural disease? Eur Respir J. 2007:29:571-574.
- Lee P, Hsu A, Lo C, Colt HG. Prospective evaluation of flex-rigid pleuroscopy for indeterminate pleural effusion: accuracy, safety and outcome. Respirology. 2007;12:881-886.
- Marchetti G, Valsecchi A, Indellicati D, Arondi S, Trigiani M, Pinelli V. Ultrasound-guided medical thoracoscopy in the absence of pleural effusion. Chest. 2015;147:1008-1012.
- Medford AR, Agarwal S, Bennett JA, Free CM, Entwisle JJ. Thoracic ultrasound prior to medical thoracoscopy improves pleural access and predicts fibrous septation. Respirology. 2010;15:804-808.
- Migliore M, Giuliano R, Aziz T, Saad RA, Sgalambro F. Four-step local anesthesia and sedation for thoracoscopic diagnosis and management of pleural diseases. Chest. 2002;121:2032-2035.
- Tschopp JM, Purek L, Frey JG, et al. Titrated sedation with propofol for medical thoracoscopy: a feasibility and safety study. Respiration. 2011;82:451-457.
- Grendelmeier P, Tamm M, Jahn K, Pflimlin E, Stolz D. Propofol versus midazolam in medical thoracoscopy: a randomized, noninferiority trial. Respiration. 2014;88:126-136.
- Lee P, Colt HG. A spray catheter technique for pleural anesthesia: a novel method for pain control before talc poudrage. Anesth Analg. 2007;104:198-200.
- DePew ZS, Wigle D, Mullon JJ, Nichols FC, Deschamps C, Maldonado F. Feasibility and safety of outpatient medical thoracoscopy at a large tertiary medical center: a collaborative medical-surgical initiative. Chest. 2014;146:398-405.
- Rozman A, Camlek L., Marc-Malovrh M, Triller N, Kern I. Rigid versus semi-rigid thoracoscopy for the diagnosis of pleural disease: a randomized pilot study. Respirology. 2013;18:704-710.
- Dhooria S, Singh N, Aggarwal AN, Gupta D, Agarwal R. A randomized trial comparing the diagnostic yield of rigid and semirigid thoracoscopy in undiagnosed pleural effusions. Respir Care. 2014;59:756-764.
- Sasada S, Kawahara K, Kusunoki Y, et al. A new electrocautery pleural biopsy technique using an insulated-tip diathermic knife during semirigid pleuroscopy. Surg Endosc. 2009;23:1901-1907.
- Shafiq M, Sethi J, Ali MS, Ghori UK, Saghaie T, Folch E. Pleural cryobiopsy: a systematic review and meta-analysis. Chest. 2020;157(1):223-230.
- Viskum K, Enk B. Complications of thoracoscopy. Poumon-Coeur. 1981;37:25-28.
- Rahman NM, Ali NJ, Brown G, et al. Local anaesthetic thoracoscopy: British Thoracic Society Pleural Disease Guideline 2010. Thorax. 2010;65(Suppl 2):ii54-ii60.
- Colt HG. Thoracoscopy: a prospective study of safety and outcome. Chest. 1995;108:324-329.
- Kindler HL, Ismaila N, Armato 3rd SG, et al. Treatment of malignant pleural mesothelioma: American Society of Clinical Oncology Clinical Practice Guideline. J Clin Oncol. 2018;36(13):1343-1373.
- Agarwal R, Aggarwal AN, Gupta D. Diagnostic accuracy and safety of semirigid thoracoscopy in exudative pleural effusions: a meta-analysis. Chest. 2013;144:1857-1867.
- Hsu C. Cytologic detection of malignancy in pleural effusion: a review of 5, 255 samples from 3, 811 patients. Diag Cytopathol. 1987;3:8-12.
- Hooper C, Lee YC, Maskell N, BTS Pleural Guideline Group Investigation of a unilateral pleural effusion in adults: British Thoracic Society Pleural Disease Guideline 2010. Thorax. 2010;65(Suppl 2):ii4-ii17.
- Renshaw AA, Dean BR, Antman KH, Sugarbaker DJ, Cibas ES. The role of cytologic evaluation of pleural fluid in the diagnosis of malignant mesothelioma. Chest. 1997;111:106-109.
- Abouzgheib W, Bartter T, Dagher H, Pratter M, Klump W. A prospective study of the volume of pleural fluid required for accurate diagnosis of malignant pleural effusion. Chest. 2009;135:999-1001.
- Canto A, Ferrer G, Ramagosa V, Moya J, Bernat R. Lung cancer and pleural effusion: clinical significance and study of pleural metastatic locations. Chest. 1985;87:649-651.
- Whitaker D, Shilkin KB. Diagnosis of pleural malignant mesothelioma in life: a practical approach. J Pathol. 1984;143:147-175.
- Leung AN, Müller NL, Miller RR. CT in differential diagnosis of diffuse pleural disease. AJR Am J Roentgenol. 1990;154:487-492.
- Traill ZC, Davies RJ, Gleeson FV. Thoracic computed tomography in patients with suspected malignant pleural effusions. Clin Radiol. 2001;56:193-196.
- Qureshi NR, Rahman NM, Gleeson FV. Thoracic ultrasound in the diagnosis of malignant pleural effusion. Thorax. 2009;64:139-143.
- Chian CF, Su WL, Soh LH, Yan HC, Perng WC, Wu CP. Echogenic swirling pattern as a predictor of malignant pleural effusions in patients with malignancies. Chest. 2004;126:129-134.
- Maskell NA, Gleeson FV, Davies RJ. Standard pleural biopsy versus CT-guided cutting-needle biopsy for diagnosis of malignant disease in pleural effusions: a randomised controlled trial. Lancet. 2003;361:1326-1330.
- Diacon AH, Schuurmans MM, Theron J, Schubert PT, Wright CA, Bolliger CT. Safety and yield of ultrasound-assisted transthoracic biopsy performed by pulmonologists. Respiration. 2004;71:519-522.
- Tombesi P, Nielsen I, Tassinari D, Trevisani L, Abbasciano V, Sartori S. Transthoracic ultrasonography-guided core needle biopsy of pleural-based lung lesions: prospective randomized comparison between a Tru-Cut-type needle and a modified Menghini-type needle. Ultraschall Med. 2009;30:390-395.
- Koegelenberg CF, Bolliger CT, Theron J, et al. Direct comparison of the diagnostic yield of ultrasound-assisted Abrams and Tru-Cut needle biopsies for pleural tuberculosis. Thorax. 2010;65:857-862.
- Hallifax RJ, Haris M, Corcoran JP, et al. Role of CT in assessing pleural malignancy prior to thoracoscopy. Thorax. 2015;70:192-193.
- Dixon G, de Fonseka D, Maskell N. Pleural controversies: image guided biopsy vs. thoracoscopy for undiagnosed pleural effusions? J Thorac Dis. 2015;7:1041-1051.
- Boutin C, Cargnino P, Viallat JR. Thoracoscopy in the early diagnosis of malignant pleural effusions. Endoscopy. 1980;12:155-160.
- Weissberg D, Kaufman M, Zurkowski Z. Pleuroscopy in patients with pleural effusion and pleural masses. Ann Thorac Surg. 1980;29:205-208.
- Chrysanthidis MG, Janssen JP. Autofluorescence videothoracoscopy in exudative pleural effusions: preliminary results. Eur Respir J. 2005;26:989-992.
- Schönfeld N, Schwarz C, Kollmeier J, Blum T, Bauer TT, Ott S. Narrow band imaging (NBI) during medical thoracoscopy: first impressions. J Occup Med Toxicol. 2009;4:24-28.
- Baas P, Triesscheijn M, Burgers S, van Pel R, Stewart F, Aalders M. Fluorescence detection of pleural malignancies using 5-aminolaevulinic acid. Chest. 2006;129:718-724.
- Bonhomme O, Duysinx B, Heinen V, Detrembleur N, Corhay JL, Louis R. First report of probe based confocal laser endomicroscopy during medical thoracoscopy. Respir Med. 2019;147:72-75.
- Wijmans L, Baas P, Sieburgh TE, et al. Confocal laser endomicroscopy as a guidance tool for pleural biopsies in malignant pleural mesothelioma. Chest. 2019;156(4):754-763.
- Zirlik S, Hildner K, Rieker RJ, Vieth M, Neurath MF, Fuchs FS. Confocal laser endomicroscopy for diagnosing malignant pleural effusions. Med Sci Monit. 2018;24:5437-5447.
- Roberts ME, Neville E, Berrisford RG, BTS Pleural Disease Guideline Group Management of a malignant pleural effusion: British Thoracic Society Pleural Disease Guideline 2010. Thorax. 2010;65(Suppl 2):ii32-ii40.
- Ceresoli GL, Locati LD, Ferreri AJ, et al. Therapeutic outcome according to histologic subtype in 121 patients with malignant pleural mesothelioma. Lung Cancer. 2001;34:279-287.
- Hollevoet K, Nackaerts K, Thimpont J, et al. Diagnostic performance of soluble mesothelin and megakaryocyte potentiating factor in mesothelioma. Am J Respir Crit Care Med. 2010;181:620-625.
- Herbert A, Gallagher PJ. Pleural biopsy in the diagnosis of malignant mesothelioma. Thorax. 1982;37:816.
- Chan HP, Liew MF, Seet JE, Lee P. Use of cryobiopsy during pleuroscopy for diagnosis of sarcomatoid malignant mesothelioma. Thorax. 2016;72:193-195.
- Boutin C, Rey F, Viallat JR. Prevention of malignant seeding after invasive diagnostic procedures in patients with pleural mesothelioma: a randomized trial of local therapy. Chest. 1995;108:754-758.
- O’Rouke N, Garcia JC, Paul J, Lawless C, McMenemin R, Hill J. A randomized controlled trial of intervention site radiotherapy in malignant pleural mesothelioma. Radiother Oncol. 2007;84:18-22.
- Scherpereel A, Astoul P, Baas P, et al. Guidelines of the European Respiratory Society and the European Society of Thoracic Surgeons for the management of malignant pleural mesothelioma. Eur Respir J. 2010;35:479-495.
- Sugarbaker DJ, Garcia JP, Richards WG, et al. Extrapleural pneumonectomy in the multimodality therapy of malignant pleural mesothelioma. Results in 120 consecutive patients. Ann Surg. 1996;224:288-294.
- Parker C, Neville E. Management of malignant mesothelioma. Thorax. 2003;58:809-813.
- Loddenkemper R, Mai J, Scheffeler N, Brandt HJ. Prospective individual comparison of blind needle biopsy and of thoracoscopy in the diagnosis and differential diagnosis of tuberculous pleurisy. Scand J Respir Dis. 1978;102:196-198.
- Diacon AH, Van de Wal BW, Wyser C, et al. Diagnostic tools in tuberculosis pleurisy: a direct comparative study. Eur Respir J. 2003;22:589-591.
- Ernst A, Silvestri GA, Johnstone D, American College of Chest Physicians Interventional pulmonary procedures: guidelines from the American College of Chest Physicians. Chest. 2003;123:1693-1717.
- Lee P, Colt HG. Steps to flex-rigid pleuroscopy. In: Lee P, Colt HG, eds. Flex-Rigid Pleuroscopy: Step by Step. Singapore: CMP Medica Asia; 2005:77-111.
BẢNG CHÚ GIẢI THUẬT NGỮ Y HỌC ANH-VIỆT
| STT | Thuật ngữ tiếng Anh | Phiên âm IPA | Nghĩa Tiếng Việt |
|---|---|---|---|
| 1 | Medical Thoracoscopy (MT) | /ˈmɛdɪkəl ˌθɔːrəˈkɒskəpi/ | Soi lồng ngực nội khoa |
| 2 | Video-assisted thoracic surgery (VATS) | /ˈvɪdiəʊ əˈsɪstɪd θəˈræsɪk ˈsɜːrdʒəri/ | Phẫu thuật lồng ngực có hỗ trợ bằng video |
| 3 | Pleuroscopy | /plʊəˈrɒskəpi/ | Soi màng phổi |
| 4 | Minimally invasive procedures | /ˈmɪnɪməli ɪnˈveɪsɪv prəˈsiːdʒərz/ | Các thủ thuật xâm lấn tối thiểu |
| 5 | Pleural space | /ˈplʊərəl speɪs/ | Khoang màng phổi |
| 6 | Anesthesia | /ˌænəsˈθiːziə/ | Vô cảm |
| 7 | Single lung ventilation | /ˈsɪŋɡəl lʌŋ ˌvɛntɪˈleɪʃən/ | Thông khí một phổi |
| 8 | Entry ports | /ˈɛntri pɔːrts/ | Cổng vào |
| 9 | Rigid instruments | /ˈrɪdʒɪd ˈɪnstrəmənts/ | Dụng cụ cứng |
| 10 | Stapled lung biopsy | /ˈsteɪpəld lʌŋ ˈbaɪɒpsi/ | Sinh thiết phổi bằng dập ghim |
| 11 | Resection of pulmonary nodules | /rɪˈsɛkʃən əv ˈpʌlmənəri ˈnɒdjuːlz/ | Cắt bỏ các nốt phổi |
| 12 | Lobectomy | /loʊˈbɛktəmi/ | Cắt thùy phổi |
| 13 | Pneumonectomy | /ˌnjuːməˈnɛktəmi/ | Cắt toàn bộ phổi |
| 14 | Esophagectomy | /ɪˌsɒfəˈdʒɛktəmi/ | Cắt thực quản |
| 15 | Pericardial windows | /ˌpɛrɪˈkɑːrdiəl ˈwɪndoʊz/ | Mở cửa sổ màng ngoài tim |
| 16 | Parietal pleural biopsy | /pəˈraɪətəl ˈplʊərəl ˈbaɪɒpsi/ | Sinh thiết màng phổi thành |
| 17 | Pleural effusion | /ˈplʊərəl ɪˈfjuːʒən/ | Tràn dịch màng phổi |
| 18 | Empyema | /ˌɛmpaɪˈiːmə/ | Tràn mủ màng phổi |
| 19 | Pleurodesis | /ˌplʊərəˈdiːsɪs/ | Gây dính màng phổi |
| 20 | Pulmonologist | /ˌpʌlməˈnɒlədʒɪst/ | Bác sĩ chuyên khoa hô hấp |
| 21 | Endoscopy suite | /ɛnˈdɒskəpi swiːt/ | Phòng nội soi |
| 22 | Local anesthesia | /ˈloʊkəl ˌænəsˈθiːziə/ | Gây tê tại chỗ |
| 23 | Moderate sedation | /ˈmɒdərət sɪˈdeɪʃən/ | An thần mức độ vừa |
| 24 | Direct visualization | /dɪˈrɛkt ˌvɪʒuəlaɪˈzeɪʃən/ | Quan sát trực tiếp |
| 25 | Sympathectomy | /ˌsɪmpəˈθɛktəmi/ | Cắt hạch giao cảm |
| 26 | Essential hyperhidrosis | /ɪˈsɛnʃəl ˌhaɪpərhaɪˈdroʊsɪs/ | Chứng tăng tiết mồ hôi vô căn |
| 27 | Diffuse lung disease | /dɪˈfjuːs lʌŋ dɪˈziːz/ | Bệnh phổi lan tỏa |
| 28 | Internist | /ɪnˈtɜːrnɪst/ | Bác sĩ nội khoa |
| 29 | Thoracic cavity | /θəˈræsɪk ˈkævəti/ | Khoang lồng ngực |
| 30 | Cystoscope | /ˈsɪstəskoʊp/ | Ống soi bàng quang |
| 31 | Lysis of pleural adhesions | /ˈlaɪsɪs əv ˈplʊərəl ədˈhiːʒənz/ | Gỡ dính màng phổi |
| 32 | Galvanocautery | /ˌɡælvənoʊˈkɔːtəri/ | Dao đốt điện |
| 33 | Tuberculous lung | /tjuːˌbɜːrkjələs lʌŋ/ | Phổi bị lao |
| 34 | Antituberculous therapy | /ˌænti tjuːˌbɜːrkjələs ˈθɛrəpi/ | Liệu pháp kháng lao |
| 35 | Differential diagnosis | /ˌdɪfəˈrɛnʃəl ˌdaɪəɡˈnoʊsɪs/ | Chẩn đoán phân biệt |
| 36 | Tumors | /ˈtjuːmərz/ | Khối u |
| 37 | Pleurisy | /ˈplʊərɪsi/ | Viêm màng phổi |
| 38 | Unknown etiology | /ʌnˈnoʊn ˌiːtiˈɒlədʒi/ | Không rõ nguyên nhân |
| 39 | Stainless steel | /ˈsteɪnləs stiːl/ | Thép không gỉ |
| 40 | Trocars | /ˈtroʊkɑːrz/ | Trocar (dụng cụ phẫu thuật) |
| 41 | Telescopes | /ˈtɛlɪskoʊps/ | Ống soi |
| 42 | Cold xenon light source | /koʊld ˈziːnɒn laɪt sɔːrs/ | Nguồn sáng xenon lạnh |
| 43 | Endoscopic camera | /ˌɛndəˈskɒpɪk ˈkæmərə/ | Camera nội soi |
| 44 | Eyepiece | /ˈaɪpiːs/ | Thị kính |
| 45 | Video monitor | /ˈvɪdiəʊ ˈmɒnɪtər/ | Màn hình video |
| 46 | Oblique telescope | /əˈbliːk ˈtɛlɪskoʊp/ | Ống soi góc nghiêng |
| 47 | Periscope telescope | /ˈpɛrɪskoʊp ˈtɛlɪskoʊp/ | Ống soi tiềm vọng |
| 48 | Panoramic view | /ˌpænəˈræmɪk vjuː/ | Nhìn toàn cảnh |
| 49 | Disposable plastic | /dɪˈspoʊzəbəl ˈplæstɪk/ | Nhựa dùng một lần |
| 50 | Reusable | /riːˈjuːzəbəl/ | Tái sử dụng |
| 51 | Operator’s preference | /ˈɒpəreɪtərz ˈprɛfərəns/ | Sở thích của người thực hiện |
| 52 | Intercostal nerve | /ˌɪntərˈkɒstəl nɜːrv/ | Dây thần kinh liên sườn |
| 53 | Discomfort | /dɪsˈkʌmfərt/ | Khó chịu |
| 54 | Optical forceps | /ˈɒptɪkəl ˈfɔːrsɛps/ | Kìm sinh thiết quang học |
| 55 | Second port | /ˈsɛkənd pɔːrt/ | Cổng thứ hai |
| 56 | Loculated pleural effusions | /ˈlɒkjəleɪtɪd ˈplʊərəl ɪˈfjuːʒənz/ | Tràn dịch màng phổi khu trú |
| 57 | Diagnostic yield | /ˌdaɪəɡˈnɒstɪk jiːld/ | Hiệu suất chẩn đoán |
| 58 | Conventional | /kənˈvɛnʃənəl/ | Thông thường |
| 59 | Flex-rigid pleuroscope | /flɛks-ˈrɪdʒɪd ˈplʊərəskoʊp/ | Ống soi lồng ngực mềm-cứng |
| 60 | Bronchoscope | /ˈbrɒŋkəskoʊp/ | Ống soi phế quản |
| 61 | Autoclavable | /ˌɔːtoʊˈkleɪvəbəl/ | Có thể hấp tiệt trùng |
| 62 | Shaft | /ʃɑːft/ | Thân ống |
| 63 | Outer diameter | /ˈaʊtər daɪˈæmɪtər/ | Đường kính ngoài |
| 64 | Proximal | /ˈprɒksɪməl/ | Đoạn gần |
| 65 | Distal | /ˈdɪstəl/ | Đoạn xa |
| 66 | Two-way angulation | /tuː-weɪ ˌæŋɡjəˈleɪʃən/ | Gập góc hai chiều |
| 67 | Working channel | /ˈwɜːrkɪŋ ˈtʃænəl/ | Kênh làm việc |
| 68 | Biopsy forceps | /ˈbaɪɒpsi ˈfɔːrsɛps/ | Kìm sinh thiết |
| 69 | Cryosurgical accessories | /ˌkraɪoʊˈsɜːrdʒɪkəl əkˈsɛsəriz/ | Phụ kiện phẫu thuật lạnh |
| 70 | Electrosurgical accessories | /ɪˌlɛktroʊˈsɜːrdʒɪkəl əkˈsɛsəriz/ | Phụ kiện phẫu thuật điện |
| 71 | Narrow band imaging (NBI) | /ˈnærəʊ bænd ˈɪmɪdʒɪŋ/ | Hình ảnh dải tần hẹp |
| 72 | Mucosal abnormalities | /mjuːˈkoʊzəl ˌæbnɔːrˈmælətiz/ | Bất thường niêm mạc |
| 73 | Vascular patterns | /ˈvæskjələr ˈpætərnz/ | Mẫu mạch máu |
| 74 | Malignancy | /məˈlɪɡnənsi/ | Bệnh ác tính |
| 75 | Pleural lesions | /ˈplʊərəl ˈliːʒənz/ | Tổn thương màng phổi |
| 76 | Contraindication | /ˌkɒntrəˌɪndɪˈkeɪʃən/ | Chống chỉ định |
| 77 | Adhesions | /ədˈhiːʒənz/ | Dính |
| 78 | Lung sliding | /lʌŋ ˈslaɪdɪŋ/ | Dấu hiệu trượt của phổi |
| 79 | Thoracic ultrasound (US) | /θəˈræsɪk ˈʌltrəsaʊnd/ | Siêu âm lồng ngực |
| 80 | Hypoxia | /haɪˈpɒksiə/ | Thiếu oxy |
| 81 | Unstable cardiovascular status | /ʌnˈsteɪbəl ˌkɑːrdioʊˈvæskjələr ˈsteɪtəs/ | Tình trạng tim mạch không ổn định |
| 82 | Bleeding diathesis | /ˈbliːdɪŋ daɪˈæθəsɪs/ | Tạng xuất huyết |
| 83 | Refractory cough | /rɪˈfræktəri kɒf/ | Ho khó chữa |
| 84 | Allergy | /ˈælərdʒi/ | Dị ứng |
| 85 | Physical examination | /ˈfɪzɪkəl ɪɡˌzæmɪˈneɪʃən/ | Khám thực thể |
| 86 | Chest radiographs (CXR) | /tʃɛst ˌreɪdiəˈɡræfs/ | X-quang ngực |
| 87 | Decubitus films | /dɪˈkjuːbɪtəs fɪlmz/ | Phim chụp tư thế nằm nghiêng |
| 88 | Computed tomography (CT) | /kəmˈpjuːtəd təˈmɒɡrəfi/ | Chụp cắt lớp vi tính |
| 89 | Aspirated | /ˈæspəreɪtɪd/ | Hút ra |
| 90 | Angiocatheter | /ˈændʒioʊˌkæθətər/ | Angiocath (catheter tĩnh mạch) |
| 91 | Thoracentesis catheter | /ˌθɔːrəsɛnˈtiːsɪs ˈkæθətər/ | Catheter chọc dò dịch màng phổi |
| 92 | Pneumothorax | /ˌnjuːmoʊˈθɔːræks/ | Tràn khí màng phổi |
| 93 | Iatrogenic pneumothorax | /ˌaɪətroʊˈdʒɛnɪk ˌnjuːmoʊˈθɔːræks/ | Tràn khí màng phổi do thầy thuốc |
| 94 | Benzodiazepines | /ˌbɛnzoʊdaɪˈæzəpiːnz/ | Benzodiazepine (nhóm thuốc) |
| 95 | Opioids | /ˈoʊpiɔɪdz/ | Opioid (nhóm thuốc) |
| 96 | Analgesia | /ˌænəlˈdʒiːziə/ | Giảm đau |
| 97 | Epidermis | /ˌɛpɪˈdɜːrmɪs/ | Biểu bì |
| 98 | Aponeurosis | /ˌæpənʊəˈroʊsɪs/ | Cân cơ |
| 99 | Intercostal muscles | /ˌɪntərˈkɒstəl ˈmʌsəlz/ | Cơ liên sườn |
| 100 | Propofol | /ˈproʊpəfɒl/ | Propofol (thuốc gây mê) |
| 101 | Talc poudrage | /tælk puːˈdrɑːʒ/ | Gây dính bằng bột talc |
| 102 | Hypotension | /ˌhaɪpoʊˈtɛnʃən/ | Tụt huyết áp |
| 103 | Hypoxemia | /ˌhaɪpɒkˈsiːmiə/ | Giảm oxy máu |
| 104 | Spray catheter | /spreɪ ˈkæθətər/ | Catheter phun sương |
| 105 | Lidocaine | /ˈlaɪdəkeɪn/ | Lidocaine (thuốc tê) |
| 106 | Lateral decubitus position | /ˈlætərəl dɪˈkjuːbɪtəs pəˈzɪʃən/ | Tư thế nằm nghiêng |
| 107 | Electrocardiogram | /ɪˌlɛktroʊˈkɑːrdioʊɡræm/ | Điện tâm đồ |
| 108 | Pulse oximetry | /pʌls ɒkˈsɪmɪtri/ | Đo độ bão hòa oxy trong mạch |
| 109 | Internal mammary artery | /ɪnˈtɜːrnəl ˈmæməri ˈɑːrtəri/ | Động mạch vú trong |
| 110 | Lateral thoracic artery | /ˈlætərəl θəˈræsɪk ˈɑːrtəri/ | Động mạch ngực bên |
| 111 | Infraclavicular area | /ˌɪnfrəkləˈvɪkjələr ˈɛəriə/ | Vùng dưới đòn |
| 112 | Subclavian artery | /səbˈkleɪviən ˈɑːrtəri/ | Động mạch dưới đòn |
| 113 | Diaphragm | /ˈdaɪəfræm/ | Cơ hoành |
| 114 | Midaxillary line | /mɪdˈæksɪləri laɪn/ | Đường nách giữa |
| 115 | Adhesiolysis | /ədˌhiːziˈɒləsɪs/ | Gỡ dính |
| 116 | Complex fluid collections | /ˈkɒmplɛks ˈfluːɪd kəˈlɛkʃənz/ | Các ổ dịch phức tạp |
| 117 | Mediastinal aspects | /ˌmiːdiəˈstaɪnəl ˈæspɛkts/ | Các khía cạnh trung thất |
| 118 | Hemithorax | /ˌhɛmiˈθɔːræks/ | Nửa lồng ngực |
| 119 | Parenchyma | /pəˈrɛŋkɪmə/ | Nhu mô |
| 120 | Neurovascular bundle | /ˌnjʊəroʊˈvæskjələr ˈbʌndəl/ | Bó mạch thần kinh |
| 121 | Abrams or Cope needle | /ˈeɪbrəmz ɔːr koʊp ˈniːdəl/ | Kim Abrams hoặc Cope |
| 122 | Mechanical strength | /məˈkænɪkəl strɛŋθ/ | Sức mạnh cơ học |
| 123 | Insulated tip (IT) diathermic knife | /ˈɪnsjəleɪtɪd tɪp daɪəˈθɜːrmɪk naɪf/ | Dao điện đầu cách điện |
| 124 | Cryobiopsy | /ˌkraɪoʊˈbaɪɒpsi/ | Sinh thiết lạnh |
| 125 | Hemorrhage | /ˈhɛmərɪdʒ/ | Xuất huyết |
| 126 | Intercostal vessel | /ˌɪntərˈkɒstəl ˈvɛsəl/ | Mạch máu liên sườn |
| 127 | External finger compression | /ɪkˈstɜːrnəl ˈfɪŋɡər kəmˈprɛʃən/ | Ấn ngón tay từ bên ngoài |
| 128 | Cauterize | /ˈkɔːtəraɪz/ | Đốt cầm máu |
| 129 | Tamponade | /ˌtæmpəˈneɪd/ | Chèn ép |
| 130 | Underwater seal | /ˌʌndərˈwɔːtər siːl/ | Dẫn lưu kín dưới nước |
| 131 | Endoclips | /ˈɛndoʊklɪps/ | Kẹp endoclip |
| 132 | Thoracotomy | /ˌθɔːrəˈkɒtəmi/ | Mở lồng ngực |
| 133 | Malignant pleural effusion (MPE) | /məˈlɪɡnənt ˈplʊərəl ɪˈfjuːʒən/ | Tràn dịch màng phổi ác tính |
| 134 | Chemosensitive | /ˌkiːmoʊˈsɛnsɪtɪv/ | Nhạy cảm với hóa trị |
| 135 | Chemical pleurodesis | /ˈkɛmɪkəl ˌplʊərəˈdiːsɪs/ | Gây dính màng phổi bằng hóa chất |
| 136 | Secondary spontaneous pneumothorax | /ˈsɛkəndəri spɒnˈteɪniəs ˌnjuːmoʊˈθɔːræks/ | Tràn khí màng phổi tự phát thứ phát |
| 137 | Sclerosant | /sklɪəˈroʊzənt/ | Chất gây dính |
| 138 | Intercostal tube | /ˌɪntərˈkɒstəl tjuːb/ | Ống liên sườn |
| 139 | Small-bore catheter | /smɔːl-bɔːr ˈkæθətər/ | Catheter lòng nhỏ |
| 140 | Talc spray atomizer | /tælk spreɪ ˈætəmaɪzər/ | Bình xịt bột talc |
| 141 | Bulb syringe | /bʌlb sɪˈrɪndʒ/ | Bơm tiêm dạng bóng |
| 142 | Mortality | /mɔːrˈtæləti/ | Tỷ lệ tử vong |
| 143 | Prolonged air leak | /prəˈlɒŋd ɛər liːk/ | Rò khí kéo dài |
| 144 | Port site tumor growth | /pɔːrt saɪt ˈtjuːmər ɡroʊθ/ | Gieo rắc khối u tại vị trí cổng vào |
| 145 | Subcutaneous emphysema | /ˌsʌbkjuːˈteɪniəs ˌɛmfɪˈsiːmə/ | Tràn khí dưới da |
| 146 | Wound infection | /wuːnd ɪnˈfɛkʃən/ | Nhiễm trùng vết mổ |
| 147 | Cardiac arrhythmias | /ˈkɑːrdiæk əˈrɪðmiəz/ | Rối loạn nhịp tim |
| 148 | Air embolism | /ɛər ˈɛmbəlɪzəm/ | Thuyên tắc khí |
| 149 | Reexpansion pulmonary edema | /ˌriːɪkˈspænʃən ˈpʌlmənəri ɪˈdiːmə/ | Phù phổi do tái giãn nở |
| 150 | Bronchopleural fistula | /ˌbrɒŋkoʊˈplʊərəl ˈfɪstjələ/ | Rò phế quản-màng phổi |
| 151 | Interstitial lung disease | /ˌɪntərˈstɪʃəl lʌŋ dɪˈziːz/ | Bệnh phổi kẽ |
| 152 | Radiotherapy | /ˌreɪdioʊˈθɛrəpi/ | Xạ trị |
| 153 | Exudative effusions | /ɛkˈsjuːdətɪv ɪˈfjuːʒənz/ | Tràn dịch tiết |
| 154 | Cytology | /saɪˈtɒlədʒi/ | Tế bào học |
| 155 | “Blind” or closed pleural biopsy | /blaɪnd ɔːr kloʊzd ˈplʊərəl ˈbaɪɒpsi/ | Sinh thiết màng phổi “mù” hoặc kín |
| 156 | Patchy pleural involvement | /ˈpætʃi ˈplʊərəl ɪnˈvɒlvmənt/ | Liên quan màng phổi dạng đốm |
| 157 | Costophrenic recess | /ˌkɒstoʊˈfrɛnɪk rɪˈsɛs/ | Góc sườn hoành |
| 158 | Contrast-enhanced thoracic CT | /ˈkɒntræst-ɪnˈhɑːnst θəˈræsɪk siː tiː/ | CT lồng ngực có cản quang |
| 159 | Nodularity | /ˌnɒdjuːˈlærəti/ | Dạng nốt |
| 160 | Pleural thickening | /ˈplʊərəl ˈθɪkənɪŋ/ | Dày màng phổi |
| 161 | Diaphragmatic thickening | /ˌdaɪəfræɡˈmætɪk ˈθɪkənɪŋ/ | Dày cơ hoành |
| 162 | Echogenic swirling pattern | /ˌɛkoʊˈdʒɛnɪk ˈswɜːrlɪŋ ˈpætərn/ | Dấu hiệu xoáy tăng âm |
| 163 | Core needle biopsy (CNB) | /kɔːr ˈniːdəl ˈbaɪɒpsi/ | Sinh thiết lõi kim |
| 164 | Cutting needle | /ˈkʌtɪŋ ˈniːdəl/ | Kim cắt |
| 165 | Polypoid masses | /ˈpɒlɪpɔɪd ˈmæsɪz/ | Khối đa polyp |
| 166 | “Candle wax drops” | /ˈkændəl wæks drɒps/ | “Giọt sáp nến” |
| 167 | Pleural inflammation | /ˈplʊərəl ˌɪnfləˈmeɪʃən/ | Viêm màng phổi |
| 168 | Autofluorescence | /ˌɔːtoʊflʊəˈrɛsəns/ | Tự phát huỳnh quang |
| 169 | White light thoracoscopy | /waɪt laɪt ˌθɔːrəˈkɒskəpi/ | Nội soi lồng ngực ánh sáng trắng |
| 170 | 5-aminolevulinic acid (ALA) | /faɪv əˈmiːnoʊˌlɛvjuːˈlɪnɪk ˈæsɪd/ | Axit 5-aminolevulinic |
| 171 | Fluorescence thoracoscopy | /flʊəˈrɛsəns ˌθɔːrəˈkɒskəpi/ | Nội soi lồng ngực huỳnh quang |
| 172 | Probe-based confocal laser endomicroscopy (pCLE) | /proʊb-beɪst kənˈfoʊkəl ˈleɪzər ˌɛndoʊmaɪˈkrɒskəpi/ | Nội soi vi thể laser đồng tiêu dựa trên đầu dò |
| 173 | Alveoli | /ælˈviːəlaɪ/ | Phế nang |
| 174 | Lymph nodes | /lɪmf noʊdz/ | Hạch bạch huyết |
| 175 | Resolution | /ˌrɛzəˈluːʃən/ | Độ phân giải |
| 176 | Transthoracic needle-based interventions | /ˌtrænsθəˈræsɪk ˈniːdəl-beɪst ˌɪntərˈvɛnʃənz/ | Can thiệp qua da lồng ngực dựa trên kim |
| 177 | Fiberoptic probe | /ˌfaɪbərˈɒptɪk proʊb/ | Đầu dò sợi quang |
| 178 | Non-small cell lung cancer | /nɒn-smɔːl sɛl lʌŋ ˈkænsər/ | Ung thư phổi không tế bào nhỏ |
| 179 | Pleural fibrosis | /ˈplʊərəl faɪˈbroʊsɪs/ | Xơ hóa màng phổi |
| 180 | Ex vivo | /ɛks ˈviːvoʊ/ | Ngoài cơ thể sống |
| 181 | Direct invasion | /dɪˈrɛkt ɪnˈveɪʒən/ | Xâm lấn trực tiếp |
| 182 | Tumor embolization | /ˈtjuːmər ˌɛmbəlaɪˈzeɪʃən/ | Thuyên tắc khối u |
| 183 | Visceral pleura | /ˈvɪsərəl ˈplʊərə/ | Màng phổi tạng |
| 184 | Secondary seeding | /ˈsɛkəndəri ˈsiːdɪŋ/ | Gieo rắc thứ phát |
| 185 | Hematogenous spread | /ˌhiːmətəˈdʒiːnəs sprɛd/ | Lây lan theo đường máu |
| 186 | Lymphangitic spread | /ˌlɪmfænˈdʒɪtɪk sprɛd/ | Lây lan theo đường bạch huyết |
| 187 | Elastin staining | /ɪˈlæstɪn ˈsteɪnɪŋ/ | Nhuộm elastin |
| 188 | Elastic layer | /ɪˈlæstɪk ˈleɪər/ | Lớp đàn hồi |
| 189 | Paramalignant | /ˌpærəməˈlɪɡnənt/ | Cận ác tính |
| 190 | Disseminated disease | /dɪˈsɛmɪneɪtɪd dɪˈziːz/ | Bệnh lan tỏa |
| 191 | Tunneled pleural catheter | /ˈtʌnəld ˈplʊərəl ˈkæθətər/ | Catheter màng phổi có đường hầm |
| 192 | Asbestos exposure | /æzˈbɛstɒs ɪkˈspoʊʒər/ | Tiếp xúc với amiăng |
| 193 | Contralateral mediastinal shift | /ˌkɒntrəˈlætərəl ˌmiːdiəˈstaɪnəl ʃɪft/ | Dịch chuyển trung thất sang bên đối diện |
| 194 | Immunohistochemical stains | /ˌɪmjunoʊˌhɪstoʊˈkɛmɪkəl steɪnz/ | Nhuộm hóa mô miễn dịch |
| 195 | Mesothelin | /ˌmɛsoʊˈθiːlɪn/ | Mesothelin |
| 196 | Megakaryocyte potentiating factor (MPF) | /ˌmɛɡəˈkærioʊsaɪt pəˈtɛnʃieɪtɪŋ ˈfæktər/ | Yếu tố thúc đẩy megakaryocyte |
| 197 | Prophylactic irradiation | /ˌproʊfɪˈlæktɪk ɪˌreɪdiˈeɪʃən/ | Xạ trị dự phòng |
| 198 | Palliative approach | /ˈpæliətɪv əˈproʊtʃ/ | Phương pháp tiếp cận giảm nhẹ |
| 199 | Sago nodules | /ˈseɪɡoʊ ˈnɒdjuːlz/ | Nốt sago |
| 200 | Fibrinous adhesions | /ˈfaɪbrɪnəs ədˈhiːʒənz/ | Dính dạng sợi tơ huyết |
