[Sách dịch] Sổ tay Bệnh Gan – Handbook of Liver Disease – (C) NXB Elsevier, 2022 – Dịch và chú giải: Ths.Bs. Lê Đình Sáng
Chương 1. Đánh giá Chức năng Gan và Các Xét nghiệm Chẩn đoán
Assessment of Liver Function and Diagnostic Studies
Paul Martin MD, FRCP, FRCPI and Lawrence S. Friedman MD
Handbook of Liver Disease, Chapter 1, 1-17
NHỮNG ĐIỂM CHÍNH
|
Các Xét nghiệm Sinh hóa Gan Thường quy
BILIRUBIN HUYẾT THANH
- Vàng da
- Thường là bằng chứng đầu tiên của bệnh gan.
- Biểu hiện rõ trên lâm sàng khi bilirubin huyết thanh vượt quá 3 mg/dL; bệnh nhân có thể nhận thấy nước tiểu sẫm màu hoặc phân nhạt màu trước khi xuất hiện vàng da củng mạc.
- Chuyển hóa
- Bilirubin là một sản phẩm thoái giáng của hemoglobin và ở mức độ thấp hơn là từ các enzyme chứa heme; 95% bilirubin có nguồn gốc từ các tế bào hồng cầu già cỗi.
- Sau khi tế bào hồng cầu bị phá vỡ trong hệ thống võng nội mô, heme bị thoái giáng bởi enzyme heme oxygenase trong lưới nội chất.
- Bilirubin được giải phóng vào máu và liên kết chặt chẽ với albumin; bilirubin tự do hay không liên hợp tan trong lipid, không được lọc qua cầu thận và không xuất hiện trong nước tiểu.
- Bilirubin không liên hợp được gan hấp thu thông qua một quá trình qua trung gian chất mang, gắn vào các protein dự trữ nội bào (ligandin), và được liên hợp bởi enzyme uridine diphosphate (UDP)-glucuronyl transferase để tạo thành diglucuronide và, ở mức độ thấp hơn, monoglucuronide.
- Bilirubin liên hợp tan trong nước và do đó xuất hiện trong nước tiểu.
- Khi nồng độ bilirubin glucuronide trong huyết thanh tăng cao, một phần sẽ liên kết với albumin (bilirubin delta), dẫn đến không có bilirubin niệu mặc dù có tăng bilirubin liên hợp trong máu; hiện tượng này giải thích sự chậm cải thiện của tình trạng vàng da trong quá trình hồi phục từ bệnh gan cấp tính cho đến khi bilirubin liên kết với albumin được dị hóa.
- Bilirubin liên hợp được bài tiết qua màng tiểu quản mật vào trong mật bằng cơ chế vận chuyển chủ động.
- Bilirubin trong mật đi vào ruột non; ở đoạn xa hồi tràng và đại tràng, bilirubin bị thủy phân bởi các beta-glucuronidase để tạo thành bilirubin không liên hợp, sau đó bị vi khuẩn đường ruột khử thành các urobilinogen không màu; một lượng nhỏ urobilinogen được tái hấp thu qua chu trình ruột-gan và chủ yếu được bài tiết vào mật, với một tỷ lệ nhỏ hơn được thải qua nước tiểu.
- Urobilinogen hoặc các dẫn xuất có màu của chúng là urobilin được bài tiết qua phân.
- Đo lường bilirubin huyết thanh
- a. Phản ứng van den Bergh
- Bilirubin toàn phần trong huyết thanh đại diện cho toàn bộ bilirubin phản ứng với axit sulfanilic được diazo hóa để tạo thành các pyrrole sinh màu trong vòng 30 phút với sự có mặt của cồn (một chất xúc tác).
- Bilirubin trực tiếp trong huyết thanh là thành phần phản ứng với thuốc thử diazo trong môi trường nước trong vòng 1 phút và tương ứng với bilirubin liên hợp.
- Bilirubin gián tiếp trong huyết thanh đại diện cho bilirubin không liên hợp và được xác định bằng cách lấy nồng độ bilirubin toàn phần trừ đi thành phần phản ứng trực tiếp.
- b. Các phương pháp đặc hiệu hơn (ví dụ: sắc ký lỏng hiệu năng cao) cho thấy phản ứng van den Bergh thường đánh giá cao hơn lượng bilirubin liên hợp; tuy nhiên, phương pháp van den Bergh vẫn là xét nghiệm tiêu chuẩn.
- a. Phản ứng van den Bergh
- Phân loại tăng bilirubin máu
- a. Không liên hợp (bilirubin gần như luôn <7 mg/dL)
- Sản xuất quá mức (lượng bilirubin đưa đến gan vượt quá khả năng hấp thu và liên hợp của gan): Tan máu, sinh hồng cầu không hiệu quả, tái hấp thu khối máu tụ.
- Khiếm khuyết trong việc hấp thu và lưu trữ bilirubin: Hội chứng Gilbert (tăng bilirubin máu không liên hợp tự phát).
- b. Liên hợp
- Di truyền: Hội chứng Dubin-Johnson và Rotor, các khiếm khuyết protein vận chuyển mật.
- Ứ mật (Bilirubin không phải là một xét nghiệm nhạy cho rối loạn chức năng gan).
- Trong gan: Xơ gan, viêm gan, viêm đường mật tiên phát, do thuốc.
- Tắc mật ngoài gan: Sỏi ống mật chủ, hẹp đường mật, khối u, teo đường mật, viêm đường mật xơ hóa.
- c. Nồng độ bilirubin rất cao
- 30 mg/dL Thường biểu thị tình trạng tan máu kết hợp với bệnh gan nhu mô hoặc tắc mật; sự bài tiết bilirubin liên hợp qua nước tiểu có thể giúp ngăn ngừa mức tăng bilirubin máu cao hơn nữa; suy thận góp phần làm tăng bilirubin máu.
- 60 mg/dL Gặp ở những bệnh nhân có bệnh hemoglobin (ví dụ: bệnh hồng cầu hình liềm) mà có vàng da tắc mật hoặc viêm gan cấp tính tiến triển.
- d. Cách tiếp cận chẩn đoán để đánh giá một trường hợp tăng bilirubin huyết thanh đơn độc được trình bày trong Hình 1.1.
- a. Không liên hợp (bilirubin gần như luôn <7 mg/dL)
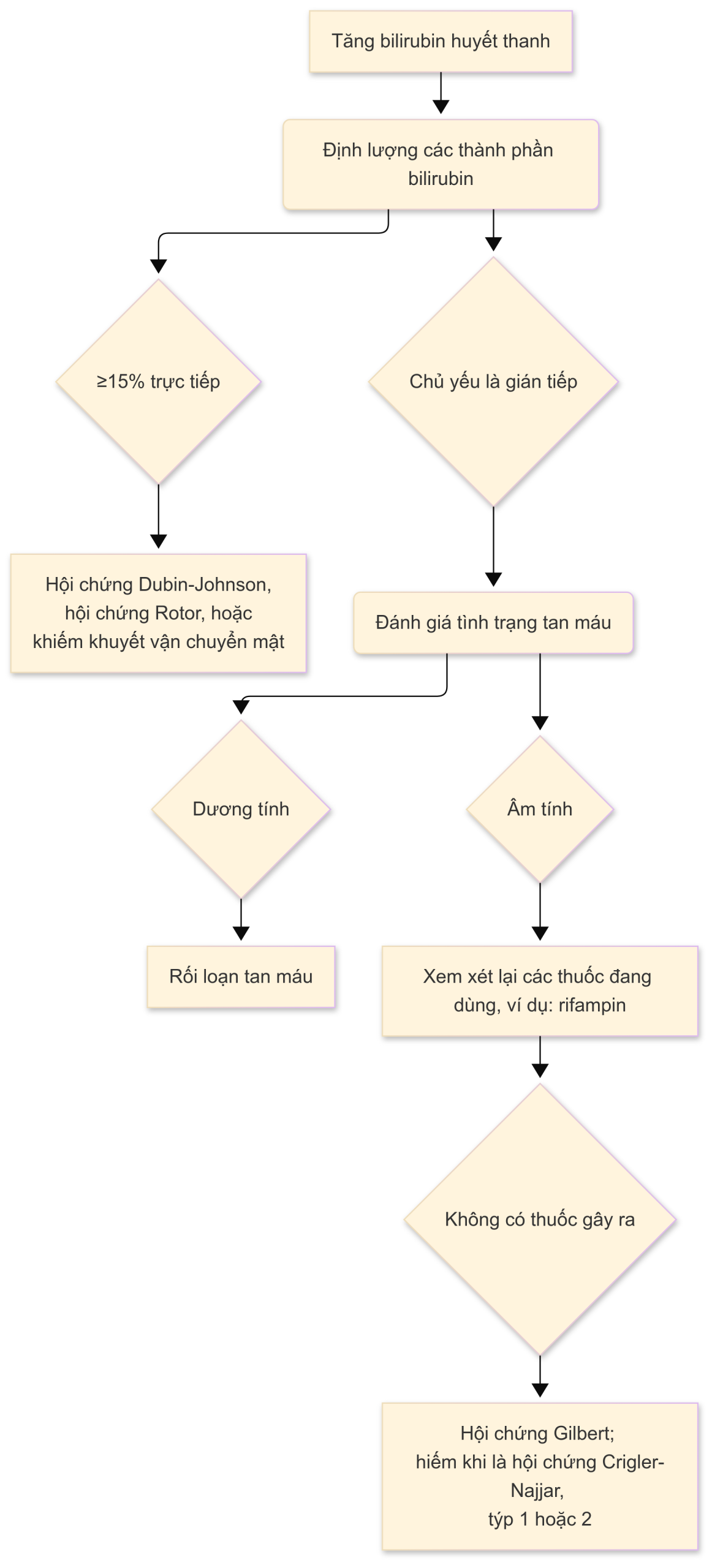
Hình 1.1 Sơ đồ tiếp cận bệnh nhân có tăng bilirubin huyết thanh đơn độc.
- Bilirubin và urobilinogen trong nước tiểu
- Bilirubin niệu cho thấy sự gia tăng bilirubin liên hợp (trực tiếp) trong huyết thanh.
- Urobilinogen trong nước tiểu (hiện nay ít được đo lường) được tìm thấy ở những bệnh nhân bị tan máu (tăng sản xuất bilirubin), xuất huyết tiêu hóa, hoặc bệnh tế bào gan (suy giảm khả năng loại bỏ urobilinogen khỏi máu).
- Sự vắng mặt của urobilinogen trong nước tiểu gợi ý sự gián đoạn chu trình ruột-gan của các sắc tố mật, như trong trường hợp tắc ống mật hoàn toàn.
- Việc phát hiện và định lượng urobilinogen không cung cấp thêm nhiều thông tin chẩn đoán cho việc đánh giá rối loạn chức năng gan.
AMINOTRANSFERASE HUYẾT THANH (Bảng 1.1)
- Các enzyme nội bào này được giải phóng từ các tế bào gan bị tổn thương và là dấu ấn hữu ích nhất của tổn thương gan (viêm hoặc hoại tử tế bào).
- a. Aspartate aminotransferase (AST, serum glutamic oxaloacetic transaminase [SGOT])
- Tìm thấy trong bào tương và ty thể.
- Tìm thấy trong gan cũng như cơ xương, tim, thận, não và tụy.
- b. Alanine aminotransferase (ALT, serum glutamic pyruvic transaminase [SGPT])
- Tìm thấy trong bào tương.
- Nồng độ cao nhất trong gan (nhạy và đặc hiệu hơn AST đối với tình trạng viêm gan và hoại tử tế bào gan).
- a. Aspartate aminotransferase (AST, serum glutamic oxaloacetic transaminase [SGOT])
Bảng 1.1 Các nguyên nhân gây tăng nồng độ aminotransferase huyết thanh
| Tăng mức độ nhẹ (<5 lần giới hạn trên của mức bình thường) | Tăng mức độ nặng (>15 lần giới hạn trên của mức bình thường) |
|---|---|
| Tại gan: ALT chiếm ưu thế | Viêm gan vi-rút cấp (A-E, herpes) |
| Viêm gan vi-rút mạn tính | DILI (Tổn thương gan do thuốc) |
| Viêm gan vi-rút cấp (A-E, EBV, CMV) | Viêm gan do thiếu máu cục bộ |
| NAFLD (Bệnh gan nhiễm mỡ không do rượu) | Viêm gan tự miễn |
| Bệnh thừa sắt mô (Hemochromatosis) | Bệnh Wilson |
| DILI (Tổn thương gan do thuốc) | Tắc ống mật cấp tính |
| Viêm gan tự miễn | Hội chứng Budd-Chiari cấp tính |
| Thiếu hụt Alpha-1 antitrypsin | Thắt động mạch gan |
| Bệnh Wilson | |
| Bệnh Celiac | |
| Bệnh gan do glycogen | |
| Tại gan: AST chiếm ưu thế | |
| Tổn thương gan liên quan đến rượu (AST/ALT >2:1) | |
| Xơ gan | |
| Ngoài gan | |
| Tập thể dục gắng sức | |
| Tan máu | |
| Bệnh cơ | |
| Bệnh tuyến giáp | |
| Macro-AST |
Ghi chú: Hầu hết mọi bệnh gan đều có thể liên quan đến nồng độ ALT tăng từ 5 đến 15 lần so với mức bình thường. ALT, Alanine aminotransferase; AST, aspartate aminotransferase; CMV, cytomegalovirus; DILI, tổn thương gan do thuốc; EBV, virus Epstein-Barr; NAFLD, bệnh gan nhiễm mỡ không do rượu.
- Giá trị lâm sàng
- Nồng độ ALT bình thường lên đến ~30 U/L ở nam và lên đến ~19 U/L ở nữ.
- Nồng độ tăng theo chỉ số khối cơ thể (và đặc biệt là với mỡ vùng thân) và tương quan với nồng độ triglyceride, glucose, insulin, và leptin trong huyết thanh và có thể tương quan nghịch với nồng độ vitamin D huyết thanh. Có nhiều tranh cãi về việc liệu nồng độ này có tương quan với nguy cơ bệnh mạch vành và tử vong hay không.
- Nồng độ có thể tăng đột ngột sau một bữa ăn nhiều calo hoặc uống acetaminophen 4 g/ngày; cà phê dường như làm giảm nồng độ này.
- Sự tăng aminotransferase thường là những bất thường sinh hóa đầu tiên được phát hiện ở những bệnh nhân bị viêm gan do vi-rút, tự miễn hoặc do thuốc; mức độ tăng có thể tương quan với mức độ tổn thương gan nhưng thường không có ý nghĩa tiên lượng.
- Trong viêm gan do rượu, AST huyết thanh thường không quá 2 đến 10 lần giới hạn trên của mức bình thường, và ALT bình thường hoặc gần như bình thường, với tỷ lệ AST:ALT >2; nồng độ ALT tương đối thấp có thể là kết quả của sự thiếu hụt pyridoxal 5-phosphate, một đồng yếu tố cần thiết cho quá trình tổng hợp ALT của gan. Ngược lại, trong bệnh gan nhiễm mỡ không do rượu, ALT thường cao hơn AST cho đến khi xơ gan phát triển.
- Nồng độ aminotransferase có thể cao hơn 3000 U/L trong viêm gan vi-rút cấp hoặc mạn tính hoặc tổn thương gan do thuốc; trong suy gan cấp hoặc viêm gan do thiếu máu cục bộ (gan sốc), có thể tìm thấy các giá trị thậm chí còn cao hơn (>5000 U/L).
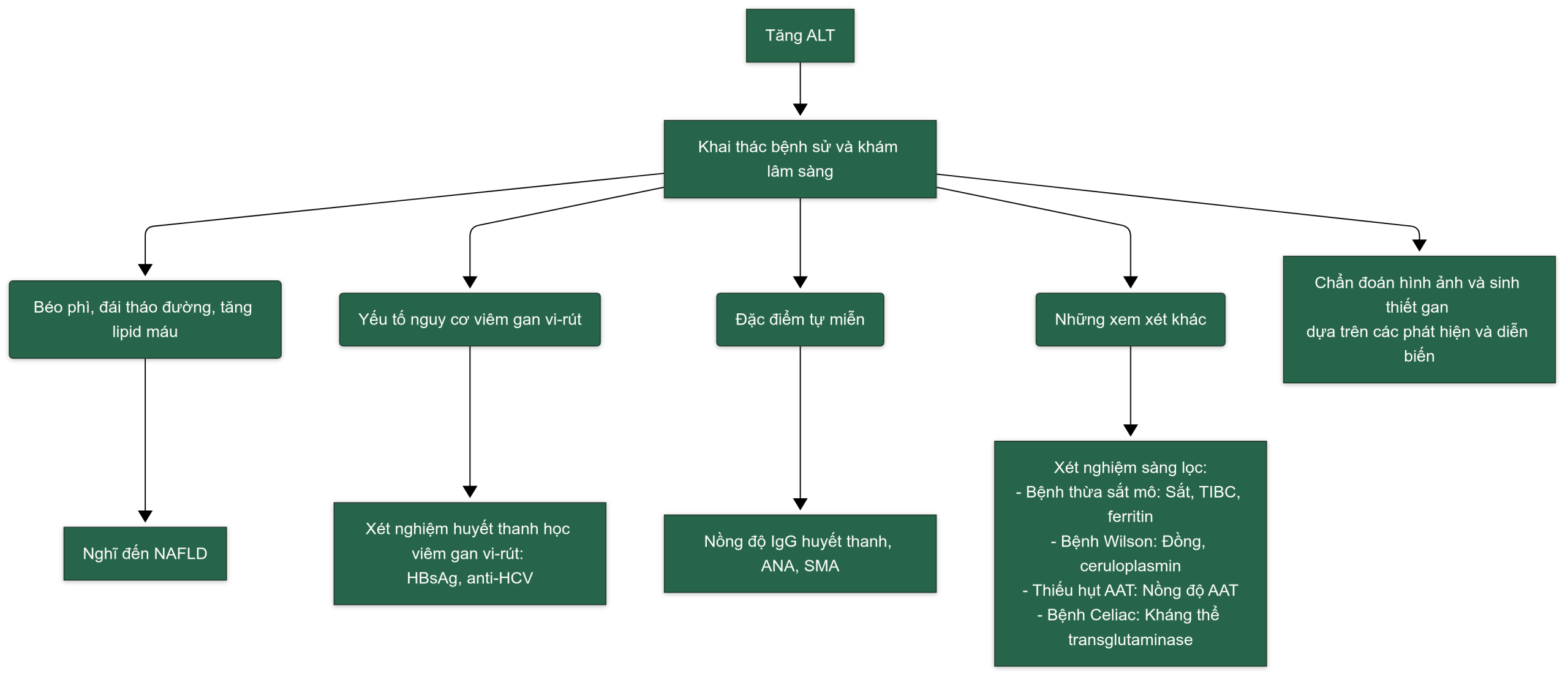
Hình 1.2 Sơ đồ tiếp cận bệnh nhân có nồng độ alanine aminotransferase huyết thanh tăng dai dẳng. AAT, Alpha-1 antitrypsin; ANA, kháng thể kháng nhân; anti-HCV, kháng thể kháng vi-rút viêm gan C; Cu, đồng; Fe, sắt; HBsAg, kháng nguyên bề mặt viêm gan B; IgG, immunoglobulin G; NAFLD, bệnh gan nhiễm mỡ không do rượu; SMA, kháng thể kháng cơ trơn; TIBC, khả năng gắn sắt toàn phần.
| * Tăng aminotransferase từ nhẹ đến trung bình là đặc trưng của viêm gan vi-rút mạn tính, viêm gan tự miễn, bệnh thừa sắt mô, thiếu hụt alpha-1 antitrypsin, bệnh Wilson và bệnh celiac.
* Trong vàng da tắc mật, giá trị aminotransferase thường thấp hơn 500 U/L; hiếm khi, giá trị có thể đạt 1000 U/L trong sỏi ống mật chủ cấp tính hoặc 3000 U/L trong viêm túi mật cấp tính, sau đó giảm nhanh về bình thường. |
- Cách tiếp cận bệnh nhân có nồng độ ALT tăng dai dẳng được trình bày trong Hình 1.2.
- Nồng độ aminotransferase thấp bất thường có liên quan đến urê huyết cao và lọc máu mạn tính; viêm gan vi-rút mạn tính ở nhóm dân số này có thể không gây tăng aminotransferase.
PHOSPHATASE KIỀM HUYẾT THANH
- ALP gan là một trong nhiều isoenzyme ALP được tìm thấy ở người và liên kết với màng tiểu quản mật của gan; có nhiều phương pháp xét nghiệm khác nhau để đo lường nó, và việc so sánh kết quả thu được bằng các kỹ thuật khác nhau có thể gây hiểu lầm.
- Xét nghiệm này nhạy trong việc phát hiện tắc nghẽn đường mật (giá trị bình thường rất hiếm gặp trong tắc nghẽn đường mật đáng kể); sự cản trở dòng chảy của mật có thể là trong gan hoặc ngoài gan.
- Sự gia tăng ALP huyết thanh là kết quả của việc gan tăng tổng hợp enzyme, chứ không phải do rò rỉ từ các tế bào ống mật hoặc không thanh thải được ALP trong tuần hoàn; vì nó được tổng hợp để đáp ứng với tình trạng tắc mật, nồng độ ALP có thể bình thường ở giai đoạn đầu của viêm đường mật cấp tính khi aminotransferase huyết thanh đã tăng.
- Nồng độ axit mật tăng có thể thúc đẩy quá trình tổng hợp ALP.
- ALP huyết thanh có thời gian bán thải là 17 ngày; nồng độ có thể vẫn tăng cao đến 1 tuần sau khi giải quyết tắc mật và nồng độ bilirubin huyết thanh trở về bình thường.
- Tăng phosphatase kiềm đơn độc
- Điều này có thể cho thấy bệnh gan thâm nhiễm: Khối u, áp xe, u hạt, hoặc bệnh amyloidosis.
- Nồng độ cao có liên quan đến tắc mật, viêm đường mật xơ hóa, viêm đường mật tiên phát, viêm đường mật liên quan đến immunoglobulin (Ig) G4, hội chứng suy giảm miễn dịch mắc phải, các phản ứng thuốc gây ứ mật, và các nguyên nhân khác của hội chứng ống mật biến mất; ở những bệnh nhân nặng bị nhiễm trùng huyết, nồng độ cao có thể là kết quả của viêm đường mật xơ hóa thứ phát do thiếu máu cục bộ với sự tiến triển nhanh chóng đến xơ gan.
- Các nguồn ALP ngoài gan là xương, ruột, thận và nhau thai (các isoenzyme khác nhau); sự tăng nồng độ được thấy trong bệnh Paget xương, di căn xương thể tạo xương, tắc ruột non và thai kỳ bình thường.
- Nguồn gốc từ gan của sự tăng nồng độ ALP được gợi ý bởi sự tăng đồng thời của gamma-glutamyltranspeptidase (GGTP) hoặc 5′-nucleotidase (5NT) huyết thanh.
- ALP gan bền với nhiệt hơn ALP xương. Mức độ chồng chéo làm cho xét nghiệm này kém hữu ích hơn GGTP hoặc 5NT.
- Cách tiếp cận chẩn đoán đối với một trường hợp tăng ALP đơn độc được trình bày trong Hình 1.3.
- Tăng nhẹ nồng độ ALP huyết thanh thường thấy trong viêm gan và xơ gan.
- Nồng độ ALP huyết thanh thấp có thể xảy ra trong suy giáp, thiếu máu ác tính, thiếu kẽm, bệnh giảm phosphatase bẩm sinh và bệnh Wilson thể tối cấp.
GAMMA-GLUTAMYLTRANSPEPTIDASE
- Mặc dù có mặt ở nhiều cơ quan khác nhau, GGTP được tìm thấy ở nồng độ đặc biệt cao trong các tế bào biểu mô lót các tiểu quản mật.
- Đây là một chỉ số rất nhạy của bệnh lý gan mật nhưng không đặc hiệu. Nồng độ tăng trong các tình trạng khác, bao gồm suy thận, nhồi máu cơ tim, bệnh tụy và đái tháo đường.
- GGTP có tính cảm ứng, và do đó nồng độ có thể tăng do uống phenytoin hoặc rượu mà không có bằng chứng lâm sàng khác về bệnh gan.
- Do thời gian bán thải dài 26 ngày, GGTP bị hạn chế trong vai trò là một dấu ấn của việc uống rượu lén lút.
- Công dụng lâm sàng chính của nó là để loại trừ nguồn gốc từ xương của một trường hợp tăng nồng độ ALP huyết thanh.
- Nhiều bệnh nhân bị tăng GGTP huyết thanh đơn độc không có bằng chứng nào khác về bệnh gan; một cuộc đánh giá sâu rộng thường không cần thiết. Bệnh nhân nên được xét nghiệm lại sau khi tránh rượu và các chất độc gan khác trong vài tuần.
5′-NUCLEOTIDASE
- 5NT được tìm thấy trong gan, liên quan đến màng sinh chất của tiểu quản mật và xoang gan.
- Mặc dù 5NT được phân bố ở các cơ quan khác, nồng độ trong huyết thanh được cho là phản ánh sự giải phóng từ gan mật do tác động tẩy rửa của muối mật lên màng sinh chất.
- Nồng độ 5NT huyết thanh tương quan tốt với nồng độ ALP huyết thanh; nồng độ 5NT huyết thanh tăng kết hợp với nồng độ ALP tăng là đặc hiệu cho rối loạn chức năng gan mật và vượt trội hơn GGTP về phương diện này.
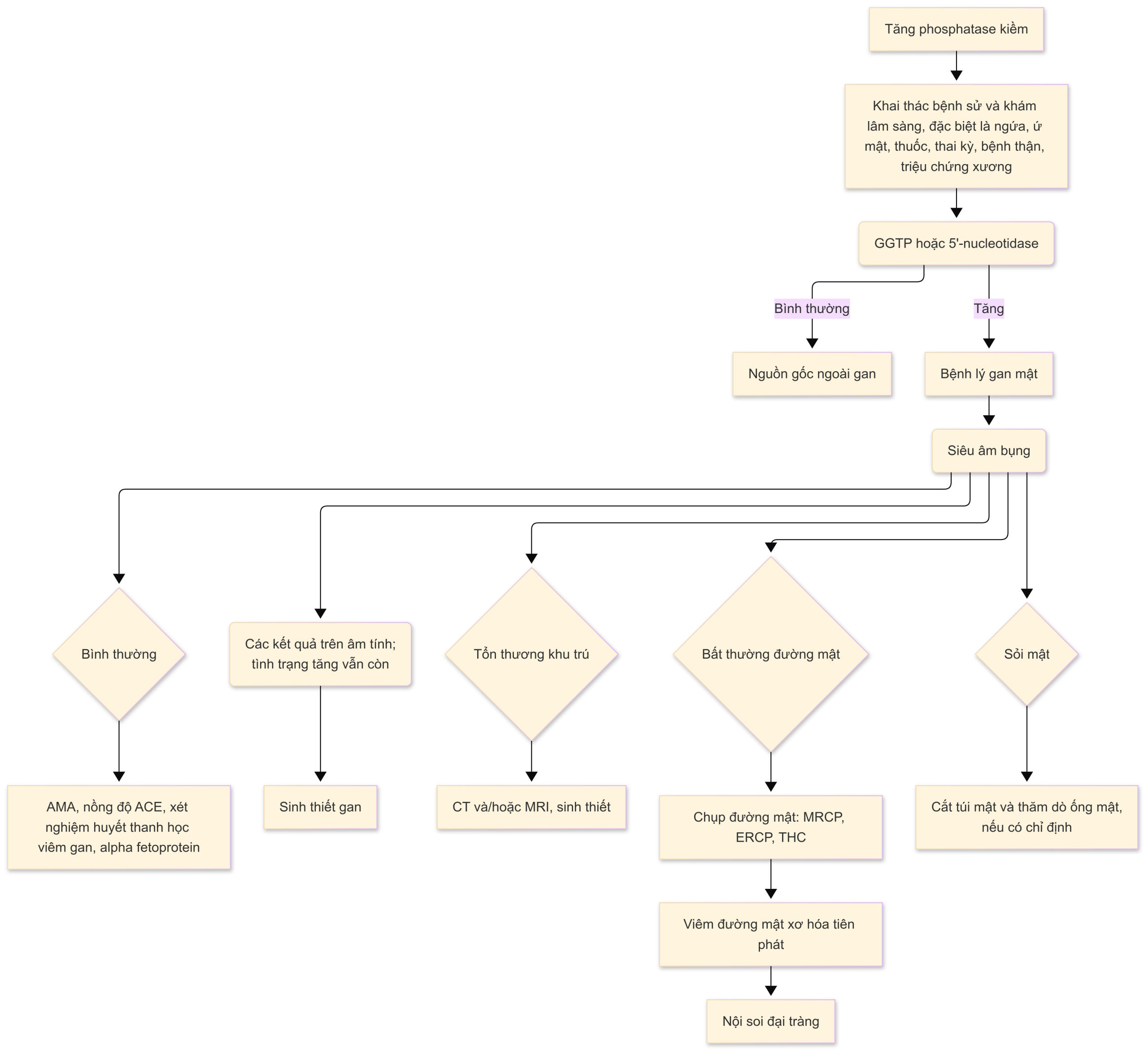
Hình 1.3 Sơ đồ tiếp cận bệnh nhân có tăng phosphatase kiềm huyết thanh đơn độc. ACE, Enzyme chuyển angiotensin; AMA, kháng thể kháng ty thể; CT, chụp cắt lớp vi tính; ERCP, chụp mật tụy ngược dòng qua nội soi; GGTP, gamma-glutamyltranspeptidase; MRCP, chụp cộng hưởng từ đường mật-tụy; MRI, chụp cộng hưởng từ; THC, chụp đường mật qua gan; US, siêu âm.
LACTATE DEHYDROGENASE
Việc đo lường lactate dehydrogenase (LDH) và isoenzyme đặc hiệu hơn là LDH5 không cung cấp thêm nhiều thông tin cho việc đánh giá nghi ngờ rối loạn chức năng gan. Nồng độ LDH cao được thấy trong hoại tử tế bào gan, viêm gan do thiếu máu cục bộ, ung thư và tan máu. Tỷ lệ ALT/LDH có thể giúp phân biệt viêm gan vi-rút cấp (≥1.5) với viêm gan do thiếu máu cục bộ và ngộ độc acetaminophen (<1.5).
PROTEIN HUYẾT THANH
Hầu hết các protein lưu thông trong huyết tương được sản xuất bởi gan và phản ánh khả năng tổng hợp của nó.
- Albumin
- Albumin chiếm 75% protein huyết thanh.
- Thời gian bán thải của nó là khoảng 3 tuần.
- Nồng độ trong máu phụ thuộc vào tốc độ tổng hợp albumin (bình thường, 12 g/ngày) và thể tích huyết tương.
- Giảm albumin máu có thể do tăng thể tích huyết tương hoặc giảm tổng hợp albumin. Nó thường liên quan đến cổ trướng và sự gia tăng của kho albumin ngoại mạch kos bằng kho albumin nội mạch. Giảm albumin máu phổ biến trong bệnh gan mạn tính (một chỉ số về mức độ nặng); nó ít phổ biến hơn trong bệnh gan cấp tính. Nó không đặc hiệu cho bệnh gan và cũng có thể phản ánh sự mất mát qua cầu thận hoặc đường tiêu hóa.
- Globulin
- a. Globulin thường tăng một cách không đặc hiệu trong bệnh gan mạn tính.
- b. Kiểu tăng có thể gợi ý nguyên nhân của bệnh gan tiềm ẩn.
- Tăng IgG: Viêm gan tự miễn
- Tăng IgM: Viêm đường mật tiên phát
- Tăng IgA: Bệnh gan do rượu
- Các yếu tố đông máu
- a. Hầu hết các yếu tố đông máu được tổng hợp bởi gan, bao gồm các yếu tố I (fibrinogen), II (prothrombin), V, VII, IX, và X và có thời gian bán thải ngắn hơn nhiều so với albumin.
- Yếu tố VII giảm đầu tiên trong bệnh gan vì có thời gian bán thải ngắn nhất, tiếp theo là các yếu tố X và IX.
- Yếu tố V không phụ thuộc vitamin K, và việc đo lường nó có thể giúp phân biệt tình trạng thiếu vitamin K với rối loạn chức năng tế bào gan ở bệnh nhân có thời gian prothrombin kéo dài. Việc đo lường nối tiếp nồng độ yếu tố V đã được sử dụng để đánh giá tiên lượng trong suy gan cấp; giá trị <20% so với bình thường báo hiệu một kết cục xấu nếu không được ghép gan.
- Việc đo lường yếu tố II (des-gamma-carboxyprothrombin) cũng đã được sử dụng để đánh giá chức năng gan. Nồng độ tăng được tìm thấy trong xơ gan và ung thư biểu mô tế bào gan (HCC) và ở những bệnh nhân dùng warfarin, một chất đối kháng vitamin K. Việc bổ sung vitamin K dẫn đến bình thường hóa des-gamma-carboxyprothrombin ở những bệnh nhân dùng warfarin nhưng không ở những người bị xơ gan.
- b. Thời gian prothrombin hữu ích trong việc đánh giá mức độ nặng và tiên lượng của bệnh gan cấp tính. Thời gian prothrombin một giai đoạn do Quick mô tả đo tốc độ chuyển đổi prothrombin thành thrombin sau khi kích hoạt con đường đông máu ngoại sinh với sự có mặt của một chiết xuất mô (thromboplastin) và các ion canxi (Ca²⁺). Sự thiếu hụt của một hoặc nhiều yếu tố do gan sản xuất dẫn đến thời gian prothrombin kéo dài.
- c. Thời gian prothrombin kéo dài trong bệnh gan ứ mật có thể do thiếu vitamin K.
- Các giải thích cho thời gian prothrombin kéo dài ngoài bệnh tế bào gan hoặc thiếu vitamin K bao gồm các bệnh đông máu do tiêu thụ, thiếu hụt di truyền của một yếu tố đông máu, hoặc các loại thuốc đối kháng phức hợp prothrombin.
- Nguyên nhân thiếu vitamin K gây kéo dài thời gian prothrombin có thể được loại trừ bằng cách tiêm 10 mg vitamin K; tiêm tĩnh mạch có thể gây ra các phản ứng nghiêm trọng, và đường uống được ưu tiên hơn, nếu có thể. (Đường tiêm dưới da không được khuyến nghị vì sự hấp thu thất thường.) Sự điều chỉnh hoặc cải thiện thời gian prothrombin ít nhất 30% trong vòng 24 giờ ngụ ý rằng chức năng tổng hợp của gan vẫn còn nguyên vẹn.
- Tỷ số bình thường hóa quốc tế (INR) được sử dụng để chuẩn hóa các phép đo thời gian prothrombin được thực hiện ở các phòng thí nghiệm khác nhau; tuy nhiên, kết quả kém nhất quán ở bệnh nhân bị bệnh gan so với những người dùng warfarin trừ khi sử dụng các mẫu chứng của bệnh gan.
- Thời gian prothrombin và INR tương quan với mức độ nặng của bệnh gan nhưng không tương quan với nguy cơ chảy máu do sự sụt giảm cân bằng của các yếu tố chống đông (ví dụ: protein C và S, antithrombin) và tăng tiêu sợi huyết ở bệnh nhân bị bệnh gan.
- a. Hầu hết các yếu tố đông máu được tổng hợp bởi gan, bao gồm các yếu tố I (fibrinogen), II (prothrombin), V, VII, IX, và X và có thời gian bán thải ngắn hơn nhiều so với albumin.
Đánh giá Khả năng Chuyển hóa của Gan
Nhiều loại thuốc trải qua quá trình chuyển hóa hoàn toàn tại gan với sinh khả dụng có thể dự đoán được đã được sử dụng để đánh giá khả năng chuyển hóa của gan. Thông thường, một chất chuyển hóa được đo trong huyết tương, nước tiểu hoặc hơi thở sau khi dùng hợp chất mẹ qua đường tiêm tĩnh mạch hoặc đường uống. Các xét nghiệm này không được sử dụng rộng rãi trong thực hành.
ĐỘ THANH THẢI ANTIPYRINE
- Antipyrine được chuyển hóa bởi cytochrome P-450 oxygenase với sự hấp thu tốt sau khi uống và được thải trừ hoàn toàn bởi gan.
- Trong bệnh gan mạn tính, có sự tương quan tốt giữa sự kéo dài thời gian bán thải của antipyrine và mức độ nặng của bệnh được đánh giá bằng thang điểm Child-Turcotte-Pugh (xem Chương 11).
- Độ thanh thải antipyrine ít bị suy giảm hơn trong bệnh gan cấp tính và vàng da tắc mật so với bệnh gan mạn tính.
- Những nhược điểm của xét nghiệm này bao gồm thời gian bán thải dài trong huyết thanh, đòi hỏi lấy nhiều mẫu máu, tương quan kém với đánh giá in vitro về khả năng của vi thể gan, và sự thay đổi chuyển hóa antipyrine do tuổi tác, chế độ ăn, rượu, hút thuốc và phơi nhiễm với môi trường.
NGHIỆM PHÁP THỞ AMINOPYRINE
- Xét nghiệm này dựa trên việc phát hiện [¹⁴C]O₂ trong hơi thở 2 giờ sau một liều uống [¹⁴C]dimethyl aminoantipyrine (aminopyrine), chất này trải qua quá trình chuyển hóa tại gan.
- Sự bài tiết giảm ở bệnh nhân xơ gan cũng như những người bị bệnh gan cấp tính.
- Xét nghiệm đã được sử dụng để đánh giá tiên lượng ở bệnh nhân viêm gan do rượu và ở bệnh nhân xơ gan đang trải qua phẫu thuật.
- Một hạn chế của nghiệm pháp thở aminopyrine là thiếu độ nhạy trong rối loạn chức năng gan do ứ mật hoặc tắc nghẽn ngoài gan.
ĐỘ THANH THẢI CAFFEINE
- Độ thanh thải caffeine sau khi uống có thể được đánh giá bằng cách đo nồng độ trong nước bọt hoặc huyết thanh; độ chính xác có vẻ tương tự như nghiệm pháp thở [¹⁴C]aminopyrine, mà không cần dùng đến đồng vị phóng xạ.
- Kết quả bất thường rõ ràng trong bệnh gan nặng trên lâm sàng, nhưng xét nghiệm không nhạy trong rối loạn chức năng gan nhẹ.
- Độ thanh thải caffeine giảm theo tuổi hoặc khi sử dụng cimetidine và tăng khi hút thuốc lá.
KHẢ NĂNG THẢI TRỪ GALACTOSE
- Độ thanh thải galactose khỏi máu do quá trình phosphoryl hóa tại gan có thể được xác định sau khi tiêm tĩnh mạch hoặc uống; nồng độ galactose huyết thanh nối tiếp được lấy từ 20 đến 50 phút sau một liều tiêm tĩnh mạch, với sự điều chỉnh cho việc bài tiết galactose qua nước tiểu.
- Ở nồng độ huyết tương >50 mg/dL, việc loại bỏ galactose phản ánh khối lượng chức năng của gan, trong khi ở nồng độ thấp hơn mức này, độ thanh thải phản ánh lưu lượng máu qua gan.
- [¹⁴C]galactose được phân bố trong nước ngoại bào và bị ảnh hưởng bởi những thay đổi về thể tích.
- Độ thanh thải galactose bị suy giảm trong bệnh gan cấp và mạn tính cũng như ở bệnh nhân có khối u di căn gan nhưng thường không bị ảnh hưởng trong vàng da tắc mật.
- Nghiệm pháp dung nạp galactose đường uống kết hợp [¹⁴C]galactose với việc đo lường [¹⁴C]O₂ trong hơi thở; kết quả của nghiệm pháp thở này tương quan với xét nghiệm [¹⁴C]aminopyrine.
- Xét nghiệm [¹⁴C]galactose không chính xác hơn các xét nghiệm sinh hóa gan tiêu chuẩn trong việc đánh giá tiên lượng ở bệnh nhân bị bệnh gan mạn tính.
CHẤT CHUYỂN HÓA LIDOCAINE
- Monoethylglycinexylidide (MEGX), một sản phẩm của quá trình chuyển hóa lidocaine tại gan, dễ dàng được đo bằng xét nghiệm miễn dịch phân cực huỳnh quang 15 phút sau khi tiêm một liều lidocaine vào tĩnh mạch.
- Xét nghiệm có thể cung cấp thông tin tiên lượng về khả năng xảy ra các biến chứng đe dọa tính mạng ở bệnh nhân xơ gan.
- Xét nghiệm cũng đã được sử dụng để đánh giá khả năng sống của các mảnh ghép gan đồng loài của người cho.
- Xét nghiệm dễ thực hiện và có ít phản ứng phụ, mặc dù nó có thể không phù hợp với một số bệnh nhân tim mạch. Kết quả xét nghiệm có thể bị ảnh hưởng bởi việc sử dụng đồng thời một số loại thuốc được chuyển hóa bởi cytochrome P-450 3A4 và nồng độ bilirubin cao; kết quả xét nghiệm bị ảnh hưởng bởi tuổi tác và chỉ số khối cơ thể và cao hơn ở nam giới so với phụ nữ.
Các Xét nghiệm Chức năng Gan Khác
AXIT MẬT HUYẾT THANH
- Axit mật được tổng hợp từ cholesterol trong gan, liên hợp với glycine hoặc taurine, và được bài tiết vào mật. Axit mật tạo điều kiện cho quá trình tiêu hóa và hấp thu chất béo trong ruột non. Chúng tái tuần hoàn qua chu trình ruột-gan; các axit mật thứ cấp hình thành do tác động của vi khuẩn đường ruột.
- Việc phát hiện nồng độ axit mật huyết thanh tăng là một dấu ấn nhạy của rối loạn chức năng gan mật.
- Có nhiều phương pháp khác nhau để xét nghiệm các axit mật riêng lẻ và tổng số; việc xét nghiệm một axit mật riêng lẻ có lẽ hữu ích như việc đo nồng độ axit mật tổng số.
- Nhiều xét nghiệm axit mật khác nhau đã được mô tả, bao gồm nồng độ lúc đói và sau ăn và xác định nồng độ sau một liều tải axit mật, qua đường uống hoặc tiêm tĩnh mạch.
- Nồng độ axit mật bình thường khi có tăng bilirubin máu gợi ý tình trạng tan máu hoặc hội chứng Gilbert.
TỔNG HỢP URÊ
- Quá trình chuyển hóa nitơ từ protein tại gan tạo ra urê. Urê được phân bố trong tổng lượng nước của cơ thể và được bài tiết qua nước tiểu hoặc khuếch tán vào ruột, nơi các vi khuẩn sản xuất urease thủy phân nó thành CO₂ và amoniac.
- Tốc độ tổng hợp urê có thể được tính toán từ lượng urê bài tiết qua nước tiểu và nitơ urê máu sau khi ước tính lượng nước trong cơ thể, với sự điều chỉnh cho quá trình thủy phân urê ở đường tiêu hóa.
- Tốc độ tổng hợp urê giảm đáng kể trong xơ gan và tương quan với thang điểm Child-Turcotte-Pugh, mặc dù nó không nhạy để phát hiện xơ gan còn bù tốt.
BROMSULPHALEIN
Độ thanh thải của bromsulphalein (BSP) sau một liều tiêm tĩnh mạch trước đây được sử dụng để đo chức năng gan. Thông tin chính xác nhất được thu thập bằng xét nghiệm lưu giữ 45 phút và tốc độ biến mất phân đoạn ban đầu. Xét nghiệm BSP không còn được ưa chuộng do có các báo cáo về phản ứng dị ứng nghiêm trọng, thiếu chính xác trong việc phân biệt vàng da do tế bào gan với vàng da tắc mật, và sự có sẵn của các xét nghiệm chức năng gan đơn giản hơn.
XANH INDOCYANINE
Thuốc nhuộm này được gan loại bỏ sau khi tiêm tĩnh mạch. Nồng độ trong máu có thể được lấy sau 20 phút kể từ khi tiêm, hoặc nồng độ có thể được xác định bằng các cảm biến trên da. So với BSP, độ thanh thải của xanh indocyanine tại gan hiệu quả hơn, và nó không độc hại. Độ chính xác của nó trong việc đánh giá rối loạn chức năng gan không tốt hơn so với thang điểm Child-Turcotte-Pugh tiêu chuẩn. Vai trò chính của nó trước đây là một thước đo lưu lượng máu qua gan.
CÁC DẤU ẤN HUYẾT THANH KHÔNG XÂM LẤN CỦA TÌNH TRẠNG XƠ HÓA
Nhiều xét nghiệm khác nhau đã được mô tả để xác định mức độ xơ hóa ở bệnh nhân bị bệnh gan mạn tính, do đó tránh được sự cần thiết của sinh thiết gan.
Các dấu ấn trực tiếp
Các dấu ấn này bao gồm hyaluronate huyết thanh, procollagen III N-peptide, và các metalloproteinase nền. Chúng thường chính xác trong việc xác nhận xơ gan và loại trừ bệnh gan nặng ở những bệnh nhân có xơ hóa tối thiểu.
Các dấu ấn gián tiếp
Nhiều công thức khác nhau đã được mô tả, kết hợp các dấu ấn xơ hóa trong huyết thanh hoặc các xét nghiệm cận lâm sàng thường quy, chẳng hạn như số lượng tiểu cầu, INR, và aminotransferase huyết thanh.
- Các ví dụ bao gồm FibroSure, Fibrospect, và chỉ số tỷ lệ AST trên tiểu cầu (APRI).
- FibroSure được sử dụng phổ biến nhất ở Hoa Kỳ và bao gồm α₂-macroglobulin, haptoglobin, apolipoprotein A1, bilirubin, và GGTP; nó hữu ích nhất để loại trừ xơ hóa (điểm thấp) hoặc gợi ý xơ gan (điểm cao); các điểm trung gian có thể phản ánh một mức độ xơ hóa khác nhau.
Sinh thiết gan
Mặc dù có những tiến bộ trong xét nghiệm huyết thanh học và chẩn đoán hình ảnh, sinh thiết gan vẫn là xét nghiệm quyết định trong một số trường hợp: để xác định chẩn đoán các bệnh gan cụ thể như bệnh Wilson, viêm đường mật xơ hóa tiên phát ống mật nhỏ, và bệnh gan nhiễm mỡ không do rượu; để đánh giá tiên lượng trong hầu hết các dạng bệnh gan nhu mô; và để đánh giá rối loạn chức năng mảnh ghép ở những người nhận ghép gan.
CHỈ ĐỊNH
Các chỉ định cho sinh thiết gan được trình bày trong Bảng 1.2.
Bảng 1.2 Chỉ định sinh thiết gan
| Đánh giá các mức xét nghiệm sinh hóa gan bất thường và gan to |
| Đánh giá và phân giai đoạn viêm gan mạn tính |
| Xác định và phân giai đoạn bệnh gan do rượu |
| Nhận biết các rối loạn viêm hoặc u hạt hệ thống |
| Đánh giá sốt chưa rõ nguyên nhân |
| Đánh giá dạng và mức độ tổn thương gan do thuốc |
| Xác định và nhận dạng bản chất của các khối trong gan |
| Chẩn đoán các rối loạn thâm nhiễm đa hệ thống |
| Đánh giá và phân giai đoạn bệnh gan ứ mật (viêm đường mật tiên phát, viêm đường mật xơ hóa tiên phát) |
| Tầm soát người thân của bệnh nhân mắc các bệnh di truyền |
| Lấy mô để nuôi cấy các tác nhân truyền nhiễm (ví dụ, mycobacteria) |
| Đánh giá hiệu quả của các liệu pháp điều trị bệnh gan (ví dụ, bệnh Wilson, bệnh thừa sắt mô, viêm gan tự miễn, viêm gan vi-rút mạn tính) |
| Đánh giá các bất thường trong xét nghiệm sinh hóa gan sau ghép tạng |
CHỐNG CHỈ ĐỊNH
Các chống chỉ định đối với sinh thiết gan được trình bày trong Bảng 1.3. Ở những bệnh nhân suy thận, rối loạn chức năng tiểu cầu do urê huyết cao nên được điều chỉnh bằng cách truyền arginine vasopressin (DDAVP), 0.3 µg/kg trong 50 mL nước muối sinh lý tiêm tĩnh mạch, ngay trước khi sinh thiết. Aspirin và các thuốc chống viêm không steroid, cũng có thể gây rối loạn chức năng tiểu cầu, bị cấm sử dụng trong 7 đến 10 ngày trước khi sinh thiết gan theo kế hoạch.
Bảng 1.3 Chống chỉ định sinh thiết gan
| Tuyệt đối | Tương đối |
|---|---|
| Tiền sử chảy máu không rõ nguyên nhân | Cổ trướng |
| Thời gian prothrombin > 3-4 giây so với chứng | Nhiễm trùng khoang màng phổi phải |
| Tiểu cầu <60.000/mm³ | Nhiễm trùng dưới cơ hoành phải |
| Thời gian chảy máu kéo dài (>10 phút) | Nghi ngờ bệnh nang sán (echinococcosis) |
| Không có sẵn hỗ trợ truyền máu | Béo phì bệnh lý |
| Nghi ngờ u máu (hemangioma) | |
| Bệnh nhân không hợp tác |
KỸ THUẬT
- Sinh thiết gan có thể được thực hiện an toàn trên cơ sở ngoại trú nếu không có chống chỉ định nào được nêu trong Bảng 1.2 và bệnh nhân có thể được theo dõi đầy đủ trong 2 đến 3 giờ sau thủ thuật, với khả năng nhập viện nếu cần (yêu cầu ở tối đa 5% bệnh nhân).
- Một loại thuốc gây tê cục bộ được tiêm dưới da và vào cơ liên sườn và phúc mạc. Một loại thuốc an thần tác dụng ngắn có thể được dùng để giảm lo lắng. Gõ để xác định điểm đục tối đa của gan.
- Việc sử dụng thường quy siêu âm để đánh dấu vị trí sinh thiết hoặc hướng dẫn kim sinh thiết đã trở thành tiêu chuẩn. Trong bệnh gan lan tỏa, sinh thiết gan dưới hướng dẫn siêu âm cho kết quả thu được mẫu tốt hơn và tỷ lệ biến chứng thấp hơn so với sinh thiết mù.
- Tiếp cận qua lồng ngực là tiêu chuẩn; tiếp cận dưới sườn chỉ nên được thử dưới sự hướng dẫn của siêu âm.
- Sinh thiết được thực hiện ở cuối thì thở ra; nhiều loại kim khác nhau (cắt [Tru-Cut, Vim-Silverman] hoặc hút [Menghini, Klatskin, Jamshidi]) được sử dụng, bao gồm cả “súng” sinh thiết.
- Vị trí sinh thiết được cầm máu bằng cách cho bệnh nhân nằm nghiêng về bên phải.
- Khi phương pháp tiếp cận tiêu chuẩn bị chống chỉ định (ví dụ, do bệnh đông máu hoặc cổ trướng), có thể thực hiện sinh thiết qua tĩnh mạch cảnh. Kỹ thuật này cũng cho phép xác định chênh lệch áp lực tĩnh mạch gan bít (xem Chương 11) để xác nhận tăng áp lực tĩnh mạch cửa, đánh giá đáp ứng với liệu pháp bằng thuốc đối kháng thụ thể beta, và xác định tiên lượng.
- Các tổn thương gan khu trú được lấy mẫu sinh thiết tốt nhất dưới sự hướng dẫn của chẩn đoán hình ảnh.
- Một mẫu bệnh phẩm đủ để giải thích mô học nên dài ít nhất 1.5 cm và chứa ít nhất sáu khoảng cửa.
BIẾN CHỨNG
- Đau sau sinh thiết có hoặc không lan đến vai phải xảy ra ở tối đa một phần ba số bệnh nhân. Phản ứng phế vị cũng phổ biến. Các biến chứng nghiêm trọng không phổ biến (<3%) và thường biểu hiện trong vòng vài giờ sau sinh thiết. Tỷ lệ tử vong là 0.03% đến 0.32%.
- Chảy máu trong ổ bụng là biến chứng nghiêm trọng nhất. Tuổi tác tăng, sự hiện diện của khối u ác tính ở gan, và số lần đâm kim là những yếu tố dự báo khả năng chảy máu, cũng như việc sử dụng kim cắt thay vì kim hút.
- Những bệnh nhân có bằng chứng lâm sàng về chảy máu có ý nghĩa huyết động, đau dai dẳng không giảm bằng thuốc giảm đau, hoặc các bằng chứng khác về biến chứng nghiêm trọng cần phải nhập viện. Tràn khí màng phổi có thể cần đặt ống dẫn lưu lồng ngực, trong khi chảy máu nghiêm trọng có thể được kiểm soát bằng cách thuyên tắc mạch chọn lọc tại phòng chụp mạch hoặc, nếu cần, phẫu thuật thắt động mạch gan phải hoặc cắt gan.
- Sinh thiết một khối u ác tính có nguy cơ 1% đến 3% gieo rắc khối u dọc theo đường kim sinh thiết.
Chẩn đoán Hình ảnh Gan
Nhiều phương thức hình ảnh có sẵn để đánh giá nhu mô gan, mạch máu và đường mật. Một trình tự hợp lý của các xét nghiệm ban đầu và tiếp theo nên được xác định bởi hoàn cảnh lâm sàng (Bảng 1.4). Sự sẵn có của các phương pháp chẩn đoán hình ảnh bụng cho các phàn nàn không liên quan như đau bụng mơ hồ đã dẫn đến việc thường xuyên phát hiện các khối u gan gần như luôn lành tính và tình cờ đối với phàn nàn của bệnh nhân nhưng đòi hỏi phải đánh giá.
Bảng 1.4 Tiếp cận sử dụng các phương pháp chẩn đoán hình ảnh
| Vấn đề lâm sàng | Hình ảnh ban đầu | Các phương pháp hình ảnh bổ sung (nếu cần) |
|---|---|---|
| Vàng da | Siêu âm | CT, nếu có giãn đường mật, một tổn thương gây tắc nghẽn, hoặc nghi ngờ một khối u ở tụy hoặc rốn gan; MRCP để xác định vị trí và nguyên nhân của giãn đường mật |
| Bệnh nhu mô gan | Siêu âm, CT, MRI | Siêu âm Doppler, siêu âm Doppler màu, hoặc MRI với chuỗi xung dòng chảy nếu nghi ngờ có bất thường mạch máu và trong một số trường hợp tăng áp lực tĩnh mạch cửa |
| Tầm soát khối u gan | Siêu âm | CT, MRI |
| Đặc điểm hóa khối u gan đã biết | CT, MRI | MRI với thuốc cản quang đặc hiệu cho gan |
| Nghi ngờ ác tính | Sinh thiết dưới hướng dẫn siêu âm hoặc CT | Siêu âm trong mổ, chụp CT động mạch cửa |
| Nghi ngờ tổn thương lành tính | Siêu âm, CT, hoặc MRI; xạ hình hạt nhân (ví dụ: xạ hình hồng cầu có đánh dấu ⁹⁹ᵐTc) đối với nghi ngờ u máu | Sinh thiết dưới hướng dẫn siêu âm hoặc CT |
| Nghi ngờ áp xe | Siêu âm hoặc CT | Hút dưới hướng dẫn siêu âm hoặc CT, Xạ hình áp xe hạt nhân (xạ hình gallium hoặc bạch cầu có đánh dấu ¹¹¹In) |
| Nghi ngờ các bất thường đường mật | Siêu âm để phát hiện giãn đường mật, sỏi mật, hoặc khối u | MRCP, ERCP, hoặc THC để xác định giải phẫu ống mật, CT hoặc siêu âm nội soi để phát hiện sỏi hoặc nguyên nhân chèn ép từ bên ngoài |
CT, Chụp cắt lớp vi tính; ERCP, chụp mật tụy ngược dòng qua nội soi; MRCP, chụp cộng hưởng từ đường mật-tụy; MRI, chụp cộng hưởng từ THC, chụp đường mật qua gan; US, siêu âm.
X-QUANG BỤNG KHÔNG CHUẨN BỊ VÀ CÁC NGHIÊN CỨU DÙNG BARIUM
- X-quang bụng không chuẩn bị ít có giá trị trong việc đánh giá bệnh gan. Đôi khi, các vôi hóa, thường là do sỏi mật, nang sán, hoặc các tổn thương cũ của bệnh lao hoặc histoplasmosis, được phát hiện. Các khối u hoặc tổn thương mạch máu cũng có thể bị vôi hóa.
- Chụp X-quang thực quản cản quang bari ít nhạy hơn đáng kể so với nội soi trong việc phát hiện giãn tĩnh mạch thực quản.
- Nội soi viên nang video không dây cũng đã được sử dụng để tầm soát giãn tĩnh mạch thực quản.
SIÊU ÂM
- Siêu âm là phương pháp chẩn đoán hình ảnh được lựa chọn ban đầu cho nhiều rối loạn gan mật. Nó tương đối rẻ, không yêu cầu bức xạ ion hóa, và có thể được sử dụng tại giường bệnh.
- Siêu âm mô tả các mặt phân cách trong mô có các đặc tính âm thanh khác nhau. Các chất cản âm đã được giới thiệu để tăng cường độ chính xác của siêu âm; chúng bao gồm kỹ thuật vi bong bóng để phát hiện các tổn thương riêng biệt và các chất cản âm dựa trên galactose để đánh giá mạch máu.
- Siêu âm không thể xuyên qua khí hoặc xương, một đặc điểm có thể ngăn cản việc kiểm tra đầy đủ các tạng. Hơn nữa, độ phân giải tăng thường đi đôi với sự giảm khả năng xuyên thấu mô.
- Siêu âm “thời gian thực” thể hiện các sự kiện sinh lý như mạch đập của động mạch.
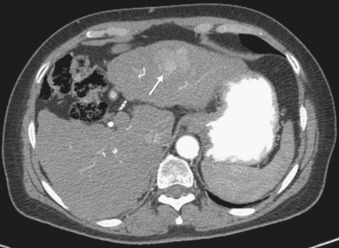
Hình 1.4 Hình ảnh chụp cắt lớp vi tính cho thấy một khối ung thư biểu mô tế bào gan (mũi tên).
- Siêu âm tốt hơn trong việc phát hiện các tổn thương khu trú so với bệnh nhu mô và là xét nghiệm lựa chọn ban đầu để phát hiện giãn đường mật.
- Các khối u gan nhỏ đến 1 cm có thể được phát hiện bằng siêu âm, và các tổn thương dạng nang có thể được phân biệt với các tổn thương đặc.
- Siêu âm cũng có thể tạo điều kiện cho sinh thiết qua da các khối u gan đặc, dẫn lưu áp xe gan, hoặc chọc dò dịch cổ trướng khu trú.
- Siêu âm Doppler được sử dụng để đánh giá sự thông suốt của các mạch máu gan và tĩnh mạch cửa ở những ứng viên và người nhận ghép gan.
CHỤP CẮT LỚP VI TÍNH
- Chụp cắt lớp vi tính (CT) thường chính xác hơn siêu âm trong việc xác định giải phẫu gan—bình thường và bệnh lý.
- Thuốc cản quang đường uống xác định lòng ruột, và thuốc cản quang tiêm tĩnh mạch làm nổi bật các cấu trúc mạch máu và tăng cường độ nét giải phẫu.
- CT xoắn ốc là một cải tiến cho phép chụp ảnh nhanh hơn ở đỉnh của sự tăng cường cản quang tiêm tĩnh mạch. Một tiến bộ gần đây hơn là CT đa dãy, cho phép chụp ảnh trong một lần nín thở và tái tạo ba chiều của mạch máu gan và đường mật.
- CT có tiêm thuốc cản quang là một cách tuyệt vời để xác định và mô tả đặc điểm của các khối u gan. Các khối u dạng nang và đặc có thể được phân biệt, cũng như các ổ áp xe. Sự tăng cường cản quang sau một liều tiêm tĩnh mạch có thể đủ chính xác để xác định các u máu dạng hang, cóลักษณะ đặc trưng. Sự xâm lấn mạch máu của khối u cũng có thể được xác định. HCC biểu hiện ngấm thuốc thì động mạch (Hình 1.4), sau đó là “thải thuốc” nhanh.
- CT cũng có thể gợi ý sự hiện diện của xơ gan và tăng áp lực tĩnh mạch cửa, cũng như những thay đổi phù hợp với gan nhiễm mỡ hoặc bệnh thừa sắt mô.
- Những hạn chế của CT là chi phí, phơi nhiễm bức xạ, và thiếu tính di động.
CHỤP CỘNG HƯỞNG TỪ
- Chụp cộng hưởng từ (MRI) có thể cung cấp hình ảnh ở nhiều mặt phẳng và cung cấp độ phân giải tuyệt vời giữa các mô chứa lượng chất béo và nước khác nhau. Chuỗi xung siêu nhanh giúp loại bỏ các ảnh giả do chuyển động. Không giống như CT, MRI không yêu cầu bức xạ ion hóa, nhưng có nguy cơ xơ hóa hệ thống do thận ở những bệnh nhân suy chức năng thận sau khi tiêm thuốc cản quang gadolinium.
Hình 1.5 Hình ảnh chụp cộng hưởng từ cho thấy một khối u máu ở gan (mũi tên).
- MRI là một phương pháp tuyệt vời để đánh giá lưu lượng máu và có thể phát hiện tình trạng quá tải sắt ở gan.
- MRI không di động, vẫn còn đắt tiền, và có thời gian chụp ảnh chậm, do đó các sự kiện sinh lý như nhu động ruột có thể dẫn đến hình ảnh bị mờ. Từ trường được sử dụng ngăn cản việc chụp ảnh ở những bệnh nhân có máy tạo nhịp tim hoặc các thiết bị kim loại khác. Những bệnh nhân mắc chứng sợ không gian hẹp cảm thấy khó chịu trong không gian kín của máy quét, và nhiều người cần dùng thuốc an thần.
- MRI là phương pháp chẩn đoán hình ảnh được lựa chọn để xác nhận sự hiện diện của các tổn thương mạch máu, đặc biệt là u máu (Hình 1.5). Nó cũng hữu ích trong việc phân biệt các nốt tái tạo với HCC; trên hình ảnh T2-weighted, cường độ tín hiệu của một nốt tái tạo tương đương với nhu mô gan bình thường, trong khi của một khối ung thư thì cao hơn.
- Việc sử dụng các thuốc cản quang đặc hiệu cho gan càng làm tăng độ chính xác trong việc đánh giá các đặc điểm của khối u gan bằng MRI.
- Chụp cộng hưởng từ đường mật-tụy (MRCP) là một phương pháp thay thế không xâm lấn cho chụp mật-tụy nội soi chẩn đoán.
- Chụp cộng hưởng từ mạch máu, giống như chụp CT mạch máu, là một phương pháp hữu ích để đánh giá các mạch máu gan trước khi cắt gan.
XẠ HÌNH HẠT NHÂN
- Các đồng vị đặc hiệu được sử dụng được hấp thu ưu tiên bởi các tế bào gan, tế bào Kupffer, hoặc các tế bào khối u hoặc viêm. Xạ hình hạt nhân đặc biệt hữu ích trong việc đánh giá nghi ngờ viêm túi mật cấp tính, mặc dù đối với bệnh gan nhu mô và khu trú, siêu âm và CT đã phần lớn thay thế các nghiên cứu y học hạt nhân.
- Các kỹ thuật bổ sung bao gồm chụp cắt lớp vi tính phát xạ đơn photon (SPECT), cho phép hình dung sự phân bố cắt ngang của một đồng vị phóng xạ, và chụp cắt lớp phát xạ positron (PET) (xem phần sau), cung cấp thông tin về lưu lượng máu và chuyển hóa mô.
CHỤP CẮT LỚP PHÁT XẠ POSITRON
- PET phát hiện sự gia tăng chuyển hóa glucose đặc trưng của khối u gan.
- Các ứng dụng lâm sàng bao gồm phát hiện và phân giai đoạn các bệnh ác tính nguyên phát ở gan, đánh giá bệnh di căn, và phân biệt các khối u gan lành tính với ác tính.
- Độ chính xác của PET trong HCC bị hạn chế bởi sự hấp thu kém của dược chất phóng xạ được sử dụng phổ biến nhất (¹⁸F-fluoro-2-deoxyglucose [FDG]) bởi các khối u biệt hóa tốt.
ĐO ĐỘ ĐÀN HỒI MÔ GAN QUA SIÊU ÂM
- Đo độ đàn hồi mô gan qua siêu âm kết hợp một đầu dò siêu âm được gắn trên một máy rung để tạo ra một sóng biến dạng đàn hồi nhằm đo độ cứng của gan, phản ánh tình trạng xơ hóa. Một kỹ thuật thường được sử dụng là đo độ đàn hồi thoáng qua, trong đó kết quả được biểu thị bằng kilopascal (kPa) và dao động từ 2.5 đến 75 kPa, với các giá trị bình thường trên khoảng 5.5 kPa.
- Đo độ đàn hồi mô gan qua siêu âm chính xác nhất để loại trừ xơ hóa tiến triển và xơ gan và để gợi ý xơ gan; tồn tại sự chồng chéo đáng kể trong kết quả khi giai đoạn xơ hóa ở mức trung gian.
- Thủ thuật này khó thực hiện về mặt kỹ thuật ở những bệnh nhân béo phì hoặc cổ trướng.
- Nó có thể bổ sung chứ không thay thế sinh thiết gan.
- Đo độ đàn hồi mô gan qua cộng hưởng từ là một kỹ thuật mới nổi khác sử dụng cộng hưởng từ để đo độ cứng của gan.
TÀI LIỆU ĐỌC THÊM
- Friedman L.S.: Controversies in liver biopsy: who, where, when, how, why?. Curr Gastroenterol Rep 2004; 6: pp. 30-36.
- Goessling W., Friedman L.S.: Increased liver chemistry in an asymptomatic patient. Clin Gastroenterol Hepatol 2005; 3: pp. 852-858.
- Green R.M., Flamm S.: AGA technical review on the evaluation of liver chemistry tests. Gastroenterology 2005; 123: pp. 1367-1384.
- Jang H.J., Yu H., Kim T.K.: Imaging of focal liver lesions. Semin Roentgenol 2009; 44: pp. 266-282.
- Kechagias S., Ernersson A., Dahlqvist O., et. al.: Fast-food-based hyper-alimentation can induce rapid and profound elevation of serum alanine aminotransferase in healthy subjects. Gut 2008; 57: pp. 649-654.
- Kim W.R., Flamm S.L., Di Bisceglie A.M., et. al.: Serum activity of alanine aminotransferase (ALT) as an indicator of health and disease. Hepatology 2008; 47: pp. 1363-1370.
- Kwo P.Y., Cohen S.M., Lim J.K.: ACG clinical guideline: evaluation of abnormal liver chemistries. Am J Gastroenterol 2017; 112: pp. 18-35.
- Lee T.H., Kim W.R., Poterucha J.J.: Evaluation of elevated liver enzymes. Clin Liver Dis 2012; 16: pp. 183-198.
- Marrero J.A., Ahn J., Reddy K.R.: ACG clinical guideline: the diagnosis and management of focal liver lesions. Am J Gastroenterol 2014; 109: pp. 1328-1347.
- Rockey D.C., Caldwell S.H., Goodman Z.D., et. al.: Liver biopsy. Hepatology 2009; 49: pp. 1017-1044.
- Ruhl C.E., Everhart J.E.: Elevated serum alanine aminotransferase and γ-glutamyltransferase and mortality in the United States population. Gastroenterology 2009; 136: pp. 477-485.
- Tapper E.B., Castera L., Afdhal N.H.: FibroScan (vibration-controlled transient elastography): where does it stand in the United States practice. Clin Gastroenterol Hepatol 2015; 13: pp. 27-36.
- Tripodi A., Mannucci P.M.: The coagulopathy of chronic liver disease. N Engl J Med 2011; 365: pp. 147-156.
- Van Beers B.E., Daire J.L., Garteiser P.: New imaging techniques for liver diseases. J Hepatol 2015; 62: pp. 690-700.
- Watkins P.B., Kaplowitz N., Slattery J.T., et. al.: Aminotransferase elevations in healthy adults receiving 4 grams of acetaminophen daily: a randomized controlled trial. JAMA 2006; 296: pp. 87-93.
