Tommaso Mauri, Marta Lazzeri, Giacomo bellani, Albert Zanelle and Giacomo Grasselli
Dịch bài: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Tóm tắt
Mục tiêu: Khi y học chính xác đang trở thành một tiêu chuẩn chăm sóc trong việc lựa chọn các phương pháp điều trị phù hợp thay vì trung bình, các phép đo sinh lý có thể là bước đầu tiên trong việc áp dụng liệu pháp cá nhân hóa trong phòng chăm sóc đặc biệt (intensive care unit − ICU). Một đánh giá có hệ thống về cơ học hô hấp ở những bệnh nhân mắc hội chứng nguy kịch hô hấp cấp tính (acute respiratory distress syndrome − ARDS) có thể là một bước tiến theo hướng này, vì hai lý do chính.
Cách tiếp cận và kết quả chính: Một mặt, cơ học hô hấp là một phương pháp sinh lý mạnh mẽ để hiểu mức độ nghiêm trọng của hội chứng này ở từng bệnh nhân. Ví dụ, giảm độ giãn nở của hệ thống hô hấp có liên quan đến thể tích phổi thở ra thấp và tổn thương phổi nghiêm trọng hơn.
Mặt khác, cơ học hô hấp có thể hướng dẫn cài đặt thông khí cơ học bảo vệ. Cải thiện độ giãn nở của phổi khu vực phụ thuộc vào trọng lực có thể hỗ trợ việc lựa chọn áp lực dương cuối thì thở ra và tối đa hóa việc huy động phế nang. Hơn nữa, mối liên quan giữa việc tăng áp lực đẩy đường thở (driving airway pressure) và tỷ lệ tử vong ở bệnh nhân ARDS có khả năng nhấn mạnh tầm quan trọng của việc định cỡ thể tích khí lưu thông đối với độ giãn nở của hệ hô hấp hơn là dựa trên trọng lượng cơ thể dự đoán.
Ý nghĩa: Bài viết đánh giá hiện tại nhằm mục đích mô tả những thay đổi chính của cơ học hô hấp trong ARDS như một công cụ đầu giường hiệu quả để hiểu mức độ nghiêm trọng và hướng dẫn cài đặt thở máy, do đó đại diện cho nguồn tài nguyên lâm sàng sẵn có cho các bác sĩ ICU.
Giới thiệu
Kể từ mô tả đầu tiên của Ashbaugh và cộng sự (1967), cơ học hô hấp (respiratory mechanics) đã được nghiên cứu rộng rãi như một công cụ theo dõi hữu ích để đánh giá mức độ nghiêm trọng của hội chứng nguy kịch hô hấp cấp tính (ARDS). Thật vậy, phổi cứng đòi hỏi áp lực thông khí cao để trao đổi khí bình thường được công nhận rộng rãi là dấu hiệu đặc trưng của ARDS (Gattinoni và Pesenti 2005). Gần đây, những tiến bộ công nghệ và hiểu biết sâu sắc về tổn thương phổi do máy thở (ventilator-induced lung injury − VILI) đã nâng cao hơn nữa kiến thức về tầm quan trọng của cơ học hô hấp toàn cục và khu vực trong ARDS (Bellani và cộng sự 2011). Các biện pháp đơn giản như áp lực đẩy đường thở đã được mô tả là yếu tố dự đoán độc lập mạnh mẽ về tỷ lệ tử vong ARDS (Amato và cộng sự 2015) và đánh giá phức tạp về các tương tác phế nang như tính không đồng nhất của thông khí động được đề xuất như một cơ chế chính nằm dưới VILI (Mauri và cộng sự 2013) .
Trong bài báo đánh giá hiện tại, chúng tôi sẽ trình bày các biện pháp cổ điển và gần đây hơn về cơ học hô hấp và chỉ ra cách chúng có thể hỗ trợ công việc lâm sàng, chẩn đoán và điều trị ARDS. Cơ học hô hấp có thể thúc đẩy sự hiểu biết về mức độ nghiêm trọng của từng cá nhân (tức là cái gọi là ‘kiểu hình’ ARDS) và trở thành mục tiêu của các cài đặt thở máy được cá nhân hóa.
Độ giãn nở hệ thống hô hấp
Phổi của bệnh nhân mắc ARDS không đồng nhất về mặt cơ học và khác nhau về kiểu thâm nhiễm và tính chất cơ học. Trong giai đoạn sớm nhất, ARDS được đặc trưng bởi phù nề có tính thấm cao và khoảng phế nang bị chiếm giữ bởi dịch protein và thâm nhiễm tế bào. Sự phá hủy tế bào phế nang loại II sản xuất chất hoạt động bề mặt (surfactant) dẫn đến giảm sản xuất cùng với tăng sức căng bề mặt và độ đàn hồi của mô, làm xẹp đường dẫn khí nhỏ, tràn ngập phế nang và xẹp phổi (Ashbaugh và cộng sự 1967).
Do đó, việc lấp đầy khoảng khí bởi các tế bào viêm và chất lỏng và sự mất mát về chức năng của chất hoạt động bề mặt dẫn đến giảm nghiêm trọng độ giãn nở của hệ thống hô hấp tĩnh (static respiratory system compliance − Crs), được định nghĩa là thể tích khí lưu thông (tidal volume − Vt) chia cho sự khác biệt giữa áp lực cao nguyên cuối thì hít vào (end-inspiratory plateau pressure − Pplat) và áp lực dương cuối kỳ thở ra tổng (total positive end-expiratory pressure − PEEP), thu được trong thủ thuật bít tắc (occlusions) (hình 1):
Crs = Vt/(Pplat – PEEPtot) phương trình (1)
Hầu hết các máy thở có sẵn trên thị trường liên tục hiển thị Crs động trong quá trình thông khí kiểm soát áp lực, được tính bằng thể tích khí lưu thông chia cho áp lực hít vào cao nhất trừ đi PEEP đã đặt. Một trong những ưu điểm của theo dõi Crs động là nó liên tục và không thay đổi kiểu thở của bệnh nhân. Tuy nhiên, Crs tĩnh và động có thể khác nhau đáng kể khi có thời gian hít vào ngắn, sức cản đường thở tăng, PEEP nội tại và thì hít vào chủ động (Stahl và cộng sự 2006, Stenqvist và cộng sự 2008).
Trong quá trình thở máy hỗ trợ, Crs được đo theo cách tương tự, mặc dù với một số bệnh nhân, có thể khó thư giãn họ và để có được giá trị Pplat và PEEP tổng chính xác.
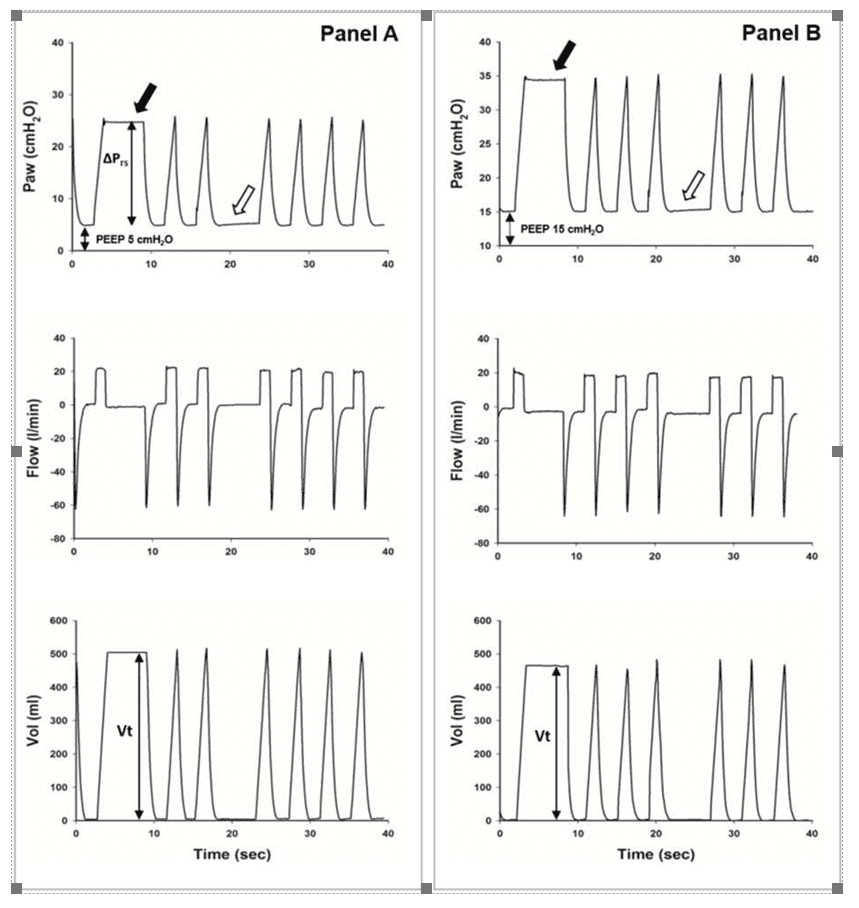

Hình 1. Ảnh hưởng của việc tăng áp lực lên độ giãn nở của hệ hô hấp. Dạng sóng áp lực đường thở, lưu lượng và thể tích khí lưu thông thu được trong quá trình thông khí kiểm soát thể tích ở hai mức PEEP khác nhau trong bộ mô phỏng phổi thụ động (Bộ mô phỏng phổi thử nghiệm kép dành cho người lớn, Dụng cụ Michigan, Grand Rapids, MI, Hoa Kỳ). Các lần giữ cuối thì hít vào và cuối thì thở ra (mũi tên đen và trắng tương ứng) được thực hiện để đo thể tích khí lưu thông (Vt) và áp lực đẩy (ΔPrs) và để tính toán độ giãn nở của hệ hô hấp (Crs). Trong hình A, Vt = 504 ml, ΔPrs = (Pplat – PEEPtot) là 20 cm H2O và Crs = Vt/ΔPrs = 25 ml cm−1 H2O ở PEEP 5 cm H2O. Trong hình B, Vt giảm xuống 464 ml (6,2 ml kg−1 IBW), ΔPrs giảm ở 19 cm H2O và Crs = Vt/ΔPrs giảm xuống 24 ml cm−1 H2O ở PEEP 15 cm H2O. Trong trường hợp mô phỏng này, tăng PEEP dẫn đến căng quá mức, giảm Crs và Vt.
Độ giãn nở giảm trong ARDS do mất khoảng khí do viêm; phế nang bị xẹp và không thể giãn ra khi hít vào. Mô hình hạn chế phổi điển hình này trong ARDS ban đầu được gọi là ‘phổi em bé’ (baby lung), được định nghĩa là một phần nhu mô phổi khỏe mạnh rõ ràng vẫn duy trì căng phồng (Gattinoni và cộng sự 2016). Gattinoni và nhóm của ông đã mô tả kích thước của phổi em bé có mối tương quan tuyến tính như thế nào với độ giãn nở của hệ hô hấp và do đó với độ cứng của phổi ARDS. Nói cách khác, họ đưa ra giả thuyết rằng độ giãn nở có thể phản ánh kích thước của phổi em bé này và họ cho rằng phổi trong ARDS thì “nhỏ” hơn là “cứng”, và các đặc tính đàn hồi của phổi khỏe mạnh còn lại gần như bình thường, như được chỉ ra bởi độ giãn nở đặc hiệu (specific compliance) (độ giãn nở/mô bình thường được sục khí), tương tự giữa các đối tượng khỏe mạnh so với ARDS.
Họ cũng mô tả khái niệm phổi em bé không phải là một khái niệm giải phẫu như thế nào: xem xét bệnh nhân nằm ngửa trên giường, các đơn vị phổi nằm ở các vùng phụ thuộc (do trọng lực) bị nén bởi trọng lượng phổi ở trên và bị đông đặc (consolidated) bởi các tế bào viêm và dịch, trong khi phần các đơn vị phổi không phụ thuộc (non-dependent lung) còn lại là gần như được bơm căng bình thường và chúng tượng trưng cho phổi em bé. Việc sử dụng tư thế nằm sấp, trong đó phổi em bé được coi là vùng giải phẫu dự kiến sẽ trở nên không phụ thuộc, được kỳ vọng sẽ cải thiện quá trình oxygen hóa bằng cách tăng tưới máu cho nó. Tuy nhiên, khi phân tích chụp CT, người ta đã mô tả cách các phế nang bị xẹp (atelectatic) và sụp xuống (collapsed) được phân phối lại cho các vùng phụ thuộc của phổi (Gattinoni và Pesenti 2005) và rằng các cơ chế cải thiện quá trình oxygen hóa trong quá trình nằm sấp có thể phức tạp hơn.
Nỗ lực đầu tiên liên quan đến mức độ nghiêm trọng của ARDS (kích thước phổi, phù nề, xơ hóa, v.v.) và các đặc tính cơ học của nó được đánh giá thông qua phương pháp đường cong áp lực-thể tích (đường cong P/V) ở bệnh nhân suy hô hấp cấp tính (acute respiratory failure − ARF) đã được báo cáo bởi Matamis và cộng sự (1984). Họ đã sử dụng phương pháp chụp X-quang ngực để theo dõi những thay đổi về mặt giải phẫu của phổi có tương quan với những rối loạn trên lâm sàng.
Vài năm sau, Gattinoni và cộng sự (Gattinoni và cộng sự 1987) đã nghiên cứu mối quan hệ giữa cấu trúc giải phẫu thu được từ chụp CT (cung cấp thông tin khu vực chính xác hơn về mật độ phổi so với chụp X quang thông thường) và cơ học phổi, thu được từ đường cong P/V ở bệnh nhân ARDS. Họ đã so sánh các đặc điểm cơ học của phổi với phân tích chụp CT chẳng hạn như thể tích khí phổi và trọng lượng mô (mô phổi được sục khí quá mức [over-aerated] hoặc bình thường, kém hoặc không được sục khí [nonaerated]) và họ phát hiện ra rằng độ giãn nở dường như phản ánh lượng mô phổi thông khí bình thường. Thật thú vị, độ giãn nở của hệ hô hấp không liên quan đến lượng mô được thông khí kém hoặc không được thông khí, thường được coi là yếu tố cho thấy mức độ nghiêm trọng của ARDS.
Tuy nhiên, các nghiên cứu quét CT chuyên đề đã chỉ ra rằng phổi của bệnh nhân ARDS không bị ảnh hưởng đồng nhất. Chủ đề này sẽ được đề cập rộng rãi hơn sau này trong bài đánh giá này. Các tác giả đã xây dựng mô hình ba vùng của phổi ARDS, với vùng H (khỏe mạnh − health), với các đặc điểm hình thái bình thường, vùng R (có thể huy động − recruitable) và vùng D (bị bệnh − diseased), bị đông đặc và không đáp ứng với sự thay đổi áp lực. Độ giãn nở dường như là một chỉ số hữu ích để chỉ ra mức độ của cả vùng H và R: vùng H và R càng nhỏ thì tổn thương phổi càng nghiêm trọng.
Một chiến lược được đề xuất để bơm lại vùng phổi bị xẹp và cải thiện độ giãn nở là tăng áp lực đường thở trong thời gian ngắn lên mức cao hơn so với thông khí bình thường: đó là thủ thuật huy động (recruitment manoeuvres − RM) và thở sâu (sigh) đã được sử dụng theo cách này để thông khí cho bệnh nhân. bệnh nhân ARDS. RM thường liên quan đến các tác động sinh lý ngắn hạn tích cực như tăng độ giãn nở của phổi và giảm shunt trong phổi (Hodgson và cộng sự 2016).
Tác động tích cực của RM đối với độ giãn nở đã được Amato và cộng sự (Amato và cộng sự 1995) chỉ ra trong một nghiên cứu trong đó bệnh nhân ARDS được chia ngẫu nhiên thành hai nhóm, nhóm đầu tiên được thở máy theo cách thông thường (Vt = 12 ml kg−1, PEEP tối thiểu được hướng dẫn bởi FiO2 và các thông số huyết động cũng như mức PaCO2 bình thường) và nhóm thứ hai được thông khí với một cách tiếp cận khác tạo huy động (PEEP trên điểm uốn dưới của đường cong áp lực-thể tích, Vt ⩽ 6 ml kg−1, áp lực đỉnh < 40 cm H2O và tăng CO2 máu cho phép [permissive hypercapnia]). Kết quả cho thấy việc sử dụng thể tích khí lưu thông cao có liên quan đến tổn thương phổi và giảm độ giãn nở do sự hiện diện của căng quá mức phế nang (alveolar overdistension) và tái mở theo chu kỳ (cycling reopening) của phế nang bị xẹp, trong khi bệnh nhân trong phương pháp huy động cho thấy sự cải thiện đáng kể về độ giãn nở, đặc biệt là trong quá trình thở máy tuần đầu tiên.
Tuy nhiên, Ranieri và cộng sự (1991) đã chỉ ra rằng nhiều bệnh nhân ARDS có thể biểu hiện của đường cong áp lực-thể tích có hình ảnh lõm hướng lên mà không có điểm uốn dưới (lower inflection point). Tình trạng này có thể phản ánh sự huy động phế nang tiến triển với mức PEEP ngày càng tăng, cho thấy sự hiện diện của bệnh phổi không đồng nhất với ‘áp lực mở’ (opening pressures) khác nhau trên phổi. Họ đã phát triển chỉ số căng thẳng (stress index), giúp phát hiện những thay đổi về độ giãn nở theo thời gian (tức là khi tăng áp lực đường thở), đây có thể là mục tiêu tốt hơn để tối ưu hóa PEEP và huy động hơn là độ giãn nở tự thân. Cần lưu ý rằng chỉ số căng thẳng chỉ có thể được đánh giá trong quá trình thông khí kiểm soát thể tích ở những bệnh nhân hoàn toàn thụ động.
Xem xét lý thuyết phổi em bé và nguy cơ đóng mở phế nang theo chu kỳ (cyclic alveolar opening and closing) trong quá trình thở máy, các khuyến nghị điều trị hiện tại bao gồm hạn chế thể tích khí lưu thông, giữ áp lực cao nguyên dưới 28–30 cm H2O và duy trì PEEP đủ cao để cải thiện quá trình oxygen hóa. Cái gọi là ‘chiến lược thông khí bảo vệ’ (protective ventilation strategy) này được cho là làm giảm căng thẳng cơ học (mechanical stress) của phổi do việc mở và đóng phế nang lặp đi lặp lại để duy trì thông khí phế nang và giảm chấn thương xẹp phổi (atelectrauma) và VILI. Cuối cùng, PEEP được chọn dựa trên độ giãn nở tốt nhất của hệ hô hấp (nghĩa là độ giãn nở liên quan đến số lượng đơn vị thông khí tối đa) trong quá trình thử nghiệm PEEP giảm dần đã được mô tả là hiệu quả và dường như là một cách sinh lý để cá nhân hóa PEEP.
Xét rằng bệnh nhân ARDS nặng không đáp ứng với điều trị thông thường với độ giãn nở thấp và/hoặc áp lực cao nguyên cực cao (tỷ lệ tử vong > 50%), họ có thể là ứng cử viên cho oxygen hóa màng ngoài cơ thể (extracorporeal membrane oxygenation − ECMO). Gattinoni và cộng sự đã áp dụng một giao thức trong đó bệnh nhân đáp ứng tiêu chí ARDS cho ECMO khi thông khí áp lực dương liên tục (continuous positive pressure ventilation − CPPV) được chuyển sang thông khí kiểm soát áp lực tỷ lệ đảo ngược (pressure-controlled inverted ratio ventilation − PC-IRV). Nếu trong vòng 4 h không có cải thiện về oxygen hóa, bệnh nhân được bắt đầu sử dụng ECMO. Thay vào đó, nếu trong quá trình trao đổi khí của bệnh nhân PC-IRV được cải thiện, họ sẽ được chuyển sang chế độ thở tự nhiên với áp lực đường thở dương liên tục (continuous positive airway pressure − CPAP). Các tác giả tuyên bố rằng giá trị tiên đoán duy nhất cho sự thành công của thông khí hỗ trợ là độ giãn nở của hệ thống hô hấp. Bệnh nhân có độ giãn nở thấp hơn 25 ml cm−1 H2O không chịu được việc chuyển sang PCIRV và CPAP, do đó kết thúc bằng ECMO. Các tác giả kết luận rằng độ giãn nở này là một trong những thông số hữu ích nhất trong việc quản lý bệnh nhân ARDS nặng không đáp ứng với điều trị thông thường (Gattinoni và cộng sự 1984).
Franchineau và cộng sự đã đề xuất cá nhân hóa việc chuẩn độ PEEP ở những bệnh nhân ARDS nặng đang trải qua ECMO bằng cách theo dõi họ trong quá trình thử nghiệm PEEP giảm dần thông qua chụp cắt lớp trở kháng điện (electrical impedance tomography − EIT). EIT có thể cung cấp một chỉ số động về tình trạng quá căng và xẹp phổi dựa trên độ giãn nở của từng khu vực (xem phần 9 bên dưới). Các tác giả, bằng cách giảm thiểu chỉ số này, đã cho thấy sự thay đổi lớn về mức PEEP tối ưu (trong khoảng 5– 20 cm H2O), nhấn mạnh nhu cầu điều chỉnh mức PEEP dựa trên sinh lý học được cá nhân hóa ở những bệnh nhân mắc ARDS nặng này (Franchineau và cộng sự 2017) .
Sức cản đường thở
Dữ liệu từ một số mô hình ARDS trên động vật cho thấy sức cản lưu lượng khí tăng lên trong trường hợp tổn thương phổi lan tỏa (Esbensahde và cộng sự 1982, Brigham và Meyrick 1986, Christley và cộng sự 2013). Sức cản đường hô hấp toàn phần ở bệnh nhân ARDS bao gồm sức cản đường thở và sức cản hô hấp ‘bổ sung’ do sự phân tán động do tính chất co giãn đàn hồi (viscoelastic properties) của hệ hô hấp (phổi và thành ngực) bị thay đổi và sự bất bình đẳng về thời gian trong nhu mô phổi (Bernasconi và cộng sự 1988, Eissa và cộng sự 1991, Antonaglia và cộng sự 2005). Do đó, sự gia tăng sức cản đường thở trong ARDS có thể được cho là do tràn ngập đường thở, giảm thể tích phổi, phản xạ phế vị và tăng hoạt tính đường thở.
Trong quá trình thông khí kiểm soát thể tích lưu lượng vuông của bệnh nhân bị liệt, sức cản của hệ hô hấp (respiratory system resistance − Rrs) được đo dễ dàng trong quá trình tắc nghẽn cuối thì hít vào (end-inspiratory occlusion) (hình 2) bằng áp lực đường thở đỉnh (peak airway pressure − Ppeak) trừ đi Pplat chia cho lưu lượng hít vào (inspiratory flow − ϕ):
Rrs = (Ppeak – Pplat)/ϕ phương trình (2)
Trong quá trình thông khí kiểm soát áp lực và hỗ trợ, sức cản đường thở khó đo hơn và thường không được theo dõi thường xuyên.
Pesenti và cộng sự (Pesenti và cộng sự 1991) đã nghiên cứu tác động cấp tính của PEEP đối với sức cản đường hô hấp ở bệnh nhân ARDS. Họ đã nghiên cứu một nhóm bệnh nhân ARDS và so sánh họ với những bệnh nhân được gây mê bình thường.


Hình 2. Đo sức cản đường thở tại giường trong quá trình thông khí kiểm soát thể tích. Đường cong áp lực đường thở, lưu lượng và thể tích thu được trong quá trình thông khí kiểm soát thể tích trong thiết bị mô phỏng phổi thụ động (Bộ mô phỏng phổi thử nghiệm kép dành cho người lớn, Dụng cụ Michigan, Grand Rapids, MI, Hoa Kỳ) ở PEEP 5 cm H2O. Giữ cuối thì hít vào (endinspiratory hold) cho phép đo chính xác áp lực đường thở đỉnh (Ppeak) và áp lực cao nguyên (Pplat). Khi đó, sức cản đường thở (Rrs) có thể được tính là (Ppeak − Pplat)/ϕ = (27–24)/0,37 = 8 cm H2O/l.s−1.
Ở cả hai nhóm, họ đã đo độ đàn hồi (tương ứng của độ giãn nở) và sức cản ở ba mức PEEP (0, 5 và 10 cm H2O) ở những người bình thường và năm mức PEEP (0, 5, 10, 15, 20 cmH2O) trong nhóm ARDS. Xem xét sức cản khi hít vào, họ nhận thấy rằng Rrs ở nhóm ARDS cao hơn đáng kể so với các đối tượng được đặt nội khí quản bình thường và nó đã thay đổi đáng kể với PEEP. Ngoài ra, các tác giả đã đo sự khác biệt giữa sức cản (difference between resistance − ΔRrs) được đo ở cuối luồng hít vào (Rrs-min) và sau khi đạt được Pplat ổn định (Rrs-max):
ΔRrs = Rrs-max – Rrs-min phương trình (3)
Cần lưu ý rằng ΔRrs khác biệt đáng kể giữa các nhóm (bệnh nhân bình thường so với bệnh nhân ARDS) và nó tăng lên ở mức PEEP cao hơn. Hơn nữa, ở cả hai nhóm (người bình thường và bệnh nhân ARDS), Rrs-max không giảm cho đến khi PEEP thấp hơn 10 cm H2O. Xem xét các kết quả này, các tác giả cho rằng Rrs-max phản ánh sự thư giãn stress của nhu mô và tính không đồng nhất liên tục theo thời gian giữa các đơn vị phổi, tức là giữa các đơn vị căng phồng quá mức với hằng số thời gian ngắn và đơn vị xẹp với hằng số thời gian dài. Mức PEEP cao hơn có thể làm căng quá mức một số vùng phổi, làm tăng tính không đồng nhất của phổi. Điều này có thể xác định hiện tượng ‘pendelluft’ tăng lên ở mức PEEP cao với Rrs-max và ΔRrs tăng lên.
Pelosi và cộng sự (Pelosi và cộng sự 1995) đã xác nhận kết quả tương tự vài năm sau đó, khi đo Rrs-max và ΔRrs ở bệnh nhân ARDS nhẹ và nặng so với người bình thường. Họ phát hiện ra rằng Rrs-max tăng rõ rệt trong ARDS, chủ yếu là do sức cản hô hấp của phổi tăng lên, trong khi sức cản của thành ngực là khá nhỏ. Đối với PEEP, họ phát hiện ra rằng việc tăng mức PEEP làm tăng đáng kể ΔRrs của phổi, dẫn đến tăng Rrs-max của phổi và Rrs-max không đổi của thành ngực. Xem xét kết quả này, vì ΔRrs sẽ phản ánh sự thích ứng với áp lực và sự bất bình đẳng về thời gian trong nhu mô phổi, họ đã suy đoán rằng PEEP có thể thay đổi các đặc tính co giãn đàn hồi của phổi bằng cách các vùng phổi bị căng phồng quá mức, do đó làm tăng sức cản tối đa và bổ sung của phổi.
Tuy nhiên, ở những bệnh nhân thở máy, Smith và Marini phát hiện ra rằng PEEP lên tới 10 cm H2O có thể xác định việc giảm sức cản đường thở như được đề xuất bằng cách giảm áp lực đẩy, tăng độ giãn nở và lưu lượng thở ra không thay đổi. Có thể giải thích rằng điều này xảy ra ở những bệnh nhân bị hạn chế lưu lượng thở ra do mức PEEP cao hơn (Smith và Marini 1988).
Eissa và cộng sự đã nghiên cứu tác động của lưu lượng hít vào và thể tích bơm vào lên các tính chất cơ học của hệ hô hấp của bệnh nhân ARDS so với những người bình thường, bằng cách sử dụng kỹ thuật làm tắc đường thở nhanh trong khi bơm vào với lưu lượng không đổi (Eissa và cộng sự 1991). Họ phát hiện ra rằng sức cản đường thở ở bệnh nhân ARDS cao hơn so với những người tình nguyện khỏe mạnh bị liệt. Ở các đối tượng bình thường, nó cũng giảm nhẹ nhưng đáng kể khi tăng thể tích. Họ cho rằng việc giảm sức cản lưu lượng khí ở những người khỏe mạnh với việc tăng thể tích phổi có thể đồng thời với việc tăng đường kính đường thở.
Xem xét rằng sức cản tăng lên có thể là do phản ứng quá mức của đường dẫn khí thứ phát do viêm, Wright và cộng sự (Wright và cộng sự 1994) đã nghiên cứu khả năng đảo ngược của việc tăng sức cản lưu lượng khí ở bệnh nhân ARDS. Họ đã thiết kế một nghiên cứu chéo ngẫu nhiên, có đối chứng với giả dược, trong đó bệnh nhân ARDS được phun khí dung chất chủ vận β2 hoặc giả dược. Họ phát hiện ra rằng chất chủ vận β2 khí dung làm giảm đáng kể sức cản lưu lượng khí so với giá trị ban đầu và giả dược. Hơn nữa, chất chủ vận β2 làm tăng cả độ giãn nở động và tĩnh của phổi. Vì vậy, họ cho rằng nó có thể làm giảm nguy cơ chấn thương nhu mô phổi trong quá trình thở máy.
Tóm lại, tất cả các nghiên cứu đã đề cập đều báo cáo rằng tổng sức cản tăng lên ở bệnh nhân ARDS so với người bình thường. Mức PEEP phù hợp có thể làm giảm sức cản khi có hạn chế lưu lượng, nhưng ngược lại, mức PEEP cao (hơn 10 cm H2O) (Pesenti và cộng sự 1991, Pelosi và cộng sự 1995) và sự thay đổi về lưu lượng và thể tích (Eissa và cộng sự 1991), có thể làm trầm trọng thêm đặc tính đàn hồi của phổi, làm tăng sức cản. Tuy nhiên, ngay cả khi sức cản hô hấp tăng ở bệnh nhân ARDS có thể được coi là dấu hiệu đặc trưng (giảm độ giãn nở), sức cản đường hô hấp hiếm khi được đo và điều trị, không giống như trong các trường hợp mắc bệnh phổi tắc nghẽn. Một cách tiếp cận đơn giản có thể là sử dụng thuốc giãn phế quản khi phát hiện thấy sức cản đường hô hấp cao hơn, đặc biệt nếu sử dụng mức PEEP cao hơn 10 cm H2O.
Thể tích phổi cuối thì thở ra và PEEP
Dung tích cặn chức năng (functional residual capacity − FRC) là thể tích khí có trong phổi khi kết thúc quá trình thở ra thụ động. Khi PEEP được áp dụng, FRC thường được đặt tên là thể tích phổi cuối thì thở ra (end expiratory lung volume − EELV). EELV là thể tích khí tối thiểu có trong phổi trong toàn bộ chu kỳ hô hấp mà thể tích khí lưu thông được thêm vào trong quá trình hít vào. EELV chủ yếu được xác định bởi sự cân bằng giữa lực đàn hồi của phổi và lực đối kháng của thành ngực và PEEP được áp dụng. EELV là tổng của thể tích dự trữ thở ra, là thể tích khí tối đa có thể được thở ra từ vị trí cuối thì thở ra, và thể tích cặn, là thể tích khí còn lại trong phổi sau khi thở ra tối đa. Thể tích dự trữ thở ra có thể được đo thông qua phép đo phế dung trong khi phép đo thể tích cặn yêu cầu các kỹ thuật như rửa trôi nitơ (nitrogen washout), pha loãng heli, đo thể tích cơ thể (body plethysmography) hoặc chụp CT.
EELV của nam giới trưởng thành có phổi khỏe mạnh thường trên 3000 ml khi áp dụng PEEP của vài centimet nước (Patroniti và cộng sự 2008). Ở phổi bị bệnh, EELV có thể giảm xuống giá trị thấp nhất là 500 ml (Patroniti và cộng sự 2010), điều này gây ảnh hưởng nghiêm trọng đến chức năng trao đổi khí của phổi và Crs. Việc giảm EELV có thể chủ yếu là do xẹp phế nang, phù phổi với tràn dịch phế nang, viêm phổi hoặc giảm độ giãn nở lồng ngực.
Các chiến lược thông khí hiện đại nhằm mục đích tối ưu hóa EELV để cải thiện quá trình trao đổi khí đồng thời ngăn ngừa VILI. EELV là thể tích khí chính góp phần trao đổi khí với máu. Nếu nhu mô phổi, không còn được thông khí và gây giảm EELV, bảo tồn sự tưới máu của nó, thì máu tưới cho nhu mô đó không tham gia vào quá trình trao đổi khí. Do đó, shunt trong phổi tăng lên, dẫn đến thiếu oxy máu. May mắn thay, có những cơ chế làm giảm tưới máu phổi ở những vùng không được thông khí, chủ yếu là co mạch do thiếu oxy, do đó làm giảm lượng shunt trong phổi. Nhưng các bệnh về phổi có thể làm thay đổi các cơ chế bảo vệ như vậy, do đó duy trì tỷ lệ shunt trong phổi tăng cao.
Số lượng phế nang được thông khí là yếu tố chính quyết định độ giãn nở của hệ hô hấp. Ví dụ, trong quá trình thông khí ở thể tích không đổi, số lượng phế nang được thông khí giảm 50 phần trăm (xấp xỉ, như xảy ra trong quá trình thông khí một phổi) sẽ dẫn đến áp lực đẩy xấp xỉ gấp đôi. Do đó, EELV giảm có thể góp phần khởi phát hoặc duy trì VILI, vì thể tích khí lưu thông được cung cấp có thể được phân phối ở một thể tích nhỏ hơn, dẫn đến chấn thương áp lực hoặc chấn thương thể tích có thể xảy ra.
Trong thời đại của y học cá nhân hóa, đo EELV dường như là một kỹ thuật đầy hứa hẹn để thiết lập máy thở cơ học đúng cách và theo dõi tiến trình của bệnh phổi. Thật không may, cho đến gần đây, không có kỹ thuật đầu giường đơn giản nào có sẵn để đo EELV. Do đó, kỹ thuật đầy hứa hẹn này chưa bao giờ được đưa vào thực hành lâm sàng và do đó thiếu dữ liệu hỗ trợ việc sử dụng nó.
Thật vậy, trong 40 năm qua chụp cắt lớp vi tính đã được sử dụng để đánh giá bệnh phổi (Gattinoni và cộng sự 1987). Chụp CT có thể được sử dụng để đo EELV, nhưng điều đó khiến bệnh nhân gặp rủi ro về bức xạ và cũng yêu cầu bệnh nhân phải được chuyển đến cơ sở CT, với các rủi ro và chi phí kèm theo.
EELV có thể được đo tại đầu giường bằng cách sử dụng một trong số các kỹ thuật dựa trên sự pha loãng khí đánh dấu (Patroniti và cộng sự 2004, Chiumello và cộng sự 2008). Một số kỹ thuật này yêu cầu thông khí cho bệnh nhân bằng một mạch kín có thể tích đã biết và nồng độ cơ bản của khí trơ, thường là helium (kỹ thuật thở lại). Trong khoảng thời gian vài hơi thở, bằng cách đo sự phối hợp cuối cùng của khí trơ đánh dấu, có thể tính toán EELV. Kỹ thuật này, được áp dụng ở những bệnh nhân thở máy, yêu cầu ngừng thông khí cơ bản hoặc điều chỉnh phức tạp mạch thở để duy trì thông khí cơ bản trong quá trình đo.
Các kỹ thuật khác, sử dụng các mạch hở (kỹ thuật không thở lại), đo EELV bằng cách thay đổi nồng độ khí được sử dụng làm chất đánh dấu trong hơi thở (có thể là oxy hoặc nitơ hoặc khí trơ như heli hoặc lưu huỳnh hexaflorua SF6) và đo lượng loại khí như vậy cần thiết để đạt đến trạng thái cân bằng mới (Richard và Guerin 2013). Một số kỹ thuật này, yêu cầu máy phân tích khí nhanh và nhạy cũng như đồng bộ hóa chính xác giữa nồng độ khí và tín hiệu lưu lượng đường thở, hiện (nhờ công nghệ cải tiến) được triển khai trong máy thở và máy theo dõi cơ học có sẵn trên thị trường. Bằng cách thay đổi tỷ lệ oxy được hít vào, các thiết bị này có thể đưa ra phép đo EELV đáng tin cậy, đặc biệt là trong quá trình thở máy kiểm soát. Người ta hy vọng rằng các thiết bị mới này có thể dẫn đến sự phổ biến rộng rãi hơn của phép đo EELV và sẽ giúp làm rõ vai trò lâm sàng của phép đo EELV.
Như đã đề cập trước đây, EELV bị giảm khi có ARDS, như được mô tả trong khái niệm ‘phổi em bé’ được giới thiệu vào giữa những năm 1980 (Gattinoni và Pesenti 2005). Các cuộc kiểm tra CT đầu tiên của bệnh nhân người lớn mắc ARDS cho thấy nhu mô phổi không đồng nhất với mô phổi có khí ước tính có kích thước bằng một em bé khỏe mạnh. Vì các đặc tính cơ học của phổi được sục khí gần như bình thường, độ giãn nở của hệ hô hấp, với sự hiện diện của độ giãn nở thành ngực bình thường, phản ánh tốt thể tích của phổi được sục khí (EELV nếu được đo vào cuối thì thở ra).
Sau đó, người ta cũng phát hiện ra rằng nhu mô có khí chủ yếu nằm ở các vùng không phụ thuộc của khoang ngực. Những dữ liệu này đã giúp phát triển khái niệm phổi ‘bọt biển’ (sponge), điều này cho thấy phổi bị bệnh có tính thấm kém dẫn đến phù kẽ. Trọng lượng phổi tăng lên gây ra sự sụp đổ của các vùng phụ thuộc, trừ khi áp lực đường thở (tức là PEEP) cao hơn áp lực chồng chất được áp dụng. Mô hình phổi xốp dường như có khả năng áp dụng cho những bệnh nhân mắc ARDS có nguồn gốc ngoài phổi (như nhiễm trùng huyết), trong khi phù kẽ dường như không đồng nhất hơn ở ARDS có nguồn gốc từ phổi (như trong viêm phổi).
Chiến lược thông khí hiện tại nhằm mục đích ngăn chặn việc giảm EELV bằng cách ngăn ngừa xẹp phổi thông qua áp dụng áp lực phù hợp (PEEP). Tuy nhiên, một khi các phế nang không được huy động, để mở chúng, cần phải tạo áp lực cao hơn mức cần thiết chỉ để giữ cho chúng mở. Áp lực huy động như vậy có thể cao tới 45 cm H2O (thủ thuật huy động). Bằng phương pháp huy động hiệu quả và mức PEEP phù hợp, có thể giảm thiểu shunt trong phổi, do đó tối đa hóa các đặc tính oxygen hóa của phổi bị bệnh. Hơn nữa, phổi được huy động có EELV cao hơn, và do đó, thể tích khí lưu thông sau đó sẽ được phân phối ở số lượng phế nang cao hơn (tức là tỷ lệ Vt/EELV thấp hơn), làm giảm nguy cơ VILI (Bellani và cộng sự 2011). Ngược lại, PEEP quá cao có thể tạo thuận lợi cho sự khởi đầu của VILI bằng cách gây ra tình trạng quá căng (hình 1).
Trong khi chọn PEEP, điều quan trọng là phải đánh giá tình trạng thể tích của bệnh nhân, vì PEEP cao hơn có thể làm tăng áp lực trong lồng ngực và có tác động tiêu cực đến cung lượng tim của bệnh nhân. Do đó, trong giai đoạn cấp tính của suy hô hấp, khi cần mức PEEP đáng kể, thông thường cần đạt được cân bằng dịch dương để duy trì cung cấp oxy đầy đủ. Khi độ giãn nở và oxygen hóa được cải thiện và PEEP có thể được hạ xuống, có thể mong muốn cân bằng dịch âm. Mức PEEP tối ưu sẽ tìm kiếm sự cân bằng phù hợp giữa mục tiêu oxygen hóa, ngăn ngừa VILI và ổn định huyết động.
Huy động phế nang
Ở PEEP không đổi và trong điều kiện trạng thái ổn định, việc áp dụng thủ thuật huy động có thể làm tăng EELV (nếu có thể tích phổi có thể huy động), điều này chủ yếu là do sự gia tăng số lượng phế nang được sục khí. Điều này đại diện cho một phương pháp chính xác để đánh giá huy động phế nang. Trong điều kiện này, nếu không có phép đo EELV, chúng ta có thể mong đợi sự gia tăng độ giãn nở của hệ thống hô hấp và oxygen hóa (nghĩa là thể tích khí lưu thông tăng lên khi thông khí áp lực không đổi hoặc giảm áp lực đẩy khi thông khí thể tích không đổi). Có thể ghi nhận khả năng thanh thải CO2 được cải thiện, nhưng không phải lúc nào cũng có.
Việc đánh giá huy động phổi ở các mức PEEP khác nhau khó khăn hơn. Sự gia tăng PEEP (và sự gia tăng liên quan đến áp lực cao nguyên) thường dẫn đến tăng EELV, nhưng EELV cao hơn như vậy có thể chỉ do sự gia tăng độ căng của các phế nang đã mở trước đó (nơi không xảy ra huy động) hoặc sự kết hợp của sự căng của các phế nang đã mở trước đó cộng với việc huy động và mở rộng các phế nang đã bị xẹp trước đó (xảy ra huy động). Cần phân biệt giữa hai tình huống này để tối ưu hóa cài đặt máy thở. Nhiều chiến lược có thể được sử dụng để đánh giá huy động phổi, mỗi chiến lược đo lường các khía cạnh cụ thể của huy động phế nang. Chụp cắt lớp vi tính có thể cho thấy lượng mô phổi chuyển từ trạng thái không có khí sang có khí (hình 3).


Hình 3. Huy động phế nang được đánh giá ở mức PEEP cao hơn bằng hình ảnh chụp CT. Hình ảnh chụp cắt lớp vi tính lồng ngực cuối thì thở ra cho thấy huy động phổi đáng kể thu được bằng cách tăng PEEP từ 12 cm H2O (hình ảnh bên trái) lên 20 cm H2O (hình ảnh bên phải) ở một bệnh nhân ARDS nặng tiêu biểu được dùng thuốc an thần và bị liệt. Lưu ý sự đảo ngược của xẹp phế nang ở PEEP cao hơn ở giữa lưng phổi, trong khi các đơn vị không phụ thuộc phía trên có nhiều nguy cơ căng phồng quá mức trong quá trình thở theo khí lưu thông.
CT khiến bệnh nhân gặp phải những rủi ro và bất tiện được liệt kê ở trên. Cần ít nhất hai lần quét và nó yêu cầu phân tích hình ảnh khá phức tạp, chưa được tiêu chuẩn hóa.
Siêu âm phổi (Lichtenstein 2014) là một công cụ động không xâm lấn áp dụng tại giường bệnh. Học kỹ thuật này cần có thời gian nhưng nó đang chứng tỏ là một công cụ đáng tin cậy, hữu ích để chẩn đoán sự hiện diện của xẹp phổi, xác định áp lực đóng và mở, cũng như đánh giá huyết động.
Bằng cách đo EELV ở hai mức PEEP và độ giãn nở của hệ hô hấp ở mức PEEP thấp hơn, có thể ước tính thể tích được huy động. Giả sử không có huy động phổi, thì độ giãn nở ở PEEP thấp hơn và cao hơn sẽ tương tự nhau (nếu không xảy ra tình trạng căng quá mức phổi). Do đó, có thể dễ dàng tính toán PEEP EELV cao hơn (EELV ở PEEP thấp cộng với độ giãn nở nhân với chênh lệch áp lực giữa PEEP thấp và cao) và nó phải tương tự như EELV đo được ở PEEP cao hơn. Nếu PEEP EELV cao đo được cao hơn con số tính toán, người ta có thể suy đoán rằng việc huy động phổi đã xảy ra.
Tương tự, huy động cũng có thể được đo bằng chênh lệch thể tích giữa hai đường cong P/V được đo ở các mức PEEP ban đầu khác nhau (Maggiore và cộng sự 2003). Hình dạng đường cong P/V hít vào có thể cung cấp thông tin về khả năng huy động của phổi. Một đường cong có độ lõm hướng lên, xác định một điểm uốn (thường được đặt tên là điểm uốn dưới) và sự hiện diện của độ trễ trong đường cong hít vào-thở ra cho thấy một phổi có thể huy động được. Phương pháp tiêu chuẩn sử dụng các đường cong P/V vẫn còn đang được tranh cãi.
Ngoài ra, EIT có thể được sử dụng để ước tính huy động phổi bằng cách đánh giá sự thay đổi của giá trị trở kháng cuối thì thở ra ở các mức PEEP khác nhau hoặc thay đổi về tính đồng nhất (xem bên dưới) (Frerichs và cộng sự 2017).
Huy động phế nang giảm thiểu căng phổi. Do đó, đo nó ở đầu giường để hướng dẫn cài đặt thông khí có thể là một chiến lược lâm sàng hiệu quả để cải thiện kết quả ARDS.
Áp lực cao nguyên
Phương trình chuyển động của hệ thống hô hấp cho biết áp lực tác dụng lên hệ thống (Prs) trong quá trình thông khí là tổng của áp lực do máy thở tạo ra (được đo tại cửa đường thở, Paw) và áp lực do các cơ hô hấp tạo ra (Pmus); áp lực này là cần thiết để vượt qua sức cản đường thở và tạo ra lưu lượng khí (Pres) và để vượt qua lực đàn hồi (Pel) (Lucangelo và cộng sự 2005). Trong quá trình thở máy kiểm soát, Pmus bằng 0 và phương trình chuyển động trở thành:
Prs = Paw + Pmus = Pres + Pel + PEEP = (Φ x Rrs) + (Vt x Ers) + PEEP phương trình (4) trong đó Rrs là sức cản đường thở, Vt là thể tích khí lưu thông và Ers là độ đàn hồi của hệ hô hấp. Pplat là áp lực được đo tại cửa đường thở khi kết thúc hít vào trong điều kiện tĩnh (tức là không có lưu lượng khí), sau khi cân bằng hoàn toàn giữa áp lực phế nang và đường thở. Trong trường hợp không có lưu lượng, Pres bằng 0 và áp lực phế nang và đường thở trùng nhau. Trong những điều kiện này, Pplat phản ánh áp lực co giãn đàn hồi của toàn bộ hệ thống hô hấp (Lucangelo và cộng sự 2005). Pplat được đo trong quá trình tắc nghẽn cuối thì hít vào, chỉ đơn giản bằng cách nhấn nút ‘giữ hít vào’ (inspiratory hold) có sẵn trên tất cả các máy thở ICU có bán trên thị trường. Trong thời gian tạm dừng, lưu lượng giảm xuống 0, thể tích được giữ lại bên trong phổi và áp lực đường thở tĩnh được đo. Điều quan trọng là phải thực hiện thủ thuật tắc ít nhất 2 giây, để cho phép cân bằng áp lực trong phế nang với các hằng số thời gian khác nhau.
Điều này đúng cho cả thông khí kiểm soát thể tích (VCV) và thông khí kiểm soát áp lực (PCV). Đáng chú ý là trong PCV, Pplat được đo bằng phương pháp tắc cuối thì hít vào có thể khác biệt đáng kể so với giá trị cài đặt của áp lực hít vào.
Cuối cùng, Pplat cũng có thể được đo trong quá trình thông khí hỗ trợ áp lực (pressuresupport ventilation − PSV), một chế độ thông khí hỗ trợ. Trong trường hợp này, Pmus không bằng 0 vì cơ hô hấp của bệnh nhân tạo ra một lượng áp lực nhất định, bệnh nhân và máy thở chia sẻ công thở. Trong thao tác tắc khi kết thúc thì hít vào, nếu bệnh nhân thả lỏng các cơ thì hít vào, có thể xác định được một cao nguyên ổn định khi theo dõi áp lực đường thở. Giống như trong quá trình thông khí cơ học kiểm soát, điều này thể hiện áp lực co giãn đàn hồi của hệ thống. Giá trị này của Pplat có thể cao hơn, bằng hoặc thấp hơn áp lực do máy thở cung cấp (là tổng của PS + PEEP); sự khác biệt được gọi là chỉ số Pmus (Pmus index − PMI) và tương ứng với áp lực do cơ hô hấp tạo ra khi kết thúc hít vào (Foti và cộng sự 1997). Tuy nhiên, thực hiện thao tác tắc nghẽn khi kết thúc thì hít vào ở bệnh nhân thở tự nhiên đòi hỏi phải chấm dứt hoàn toàn bất kỳ nỗ lực hít vào nào trong suốt thao tác. Nếu không xác định được một cao nguyên ổn định, thì giá trị này không đáng tin cậy và thao tác phải được lặp lại.
Giám sát Pplat trong quá trình thở máy là cực kỳ quan trọng vì ít nhất hai lý do.
Đầu tiên, cần đánh giá tính chất đàn hồi của hệ thống hô hấp và tính độ giãn nở của hệ thống (Crs). Ai cũng biết rằng Crs ở bệnh nhân ARDS có liên quan trực tiếp đến kích thước của ‘phổi em bé’ (phần nhu mô phổi có sẵn để thông khí), do đó có liên quan đến mức độ nghiêm trọng của bệnh.
Thứ hai, vì trong điều kiện tĩnh, áp lực đường thở và phế nang ở trạng thái cân bằng, Pplat được coi là một ước tính đáng tin cậy về áp lực làm căng phổi và do đó là mức độ căng thẳng của phổi (lung stress), yếu tố chính quyết định VILI.
Điều này đã được chứng minh rõ ràng bằng thử nghiệm ARMA đầu tiên, trong đó 861 bệnh nhân ARDS được chọn ngẫu nhiên để thông khí Vt thấp (6 ml kg−1 trọng lượng cơ thể dự đoán hoặc được điều chỉnh để giữ Pplat thấp hơn 30 cm H2O) hoặc Vt ‘truyền thống’ (12 ml kg−1 hoặc Pplat thấp hơn 50 cm H2O). Những bệnh nhân trong nhóm Pplat thấp − Vt thấp có tỷ lệ tử vong thấp hơn đáng kể (31% so với 40%, p = 0,007) (ARDSnet 2000). Dựa trên những kết quả này, việc hạn chế Vt và giữ Pplat ở mức < 30 cmH2O vẫn được coi là nền tảng của chiến lược thở máy cho bệnh nhân ARDS.
Tuy nhiên, ngưỡng 30 cmH2O đang được tranh luận. Terragni và cộng sự sử dụng hình ảnh chụp CT (Terragni và cộng sự 2007) và Bellani và cộng sự sử dụng phương pháp chụp cắt lớp phát xạ positron (Bellani và cộng sự 2011) đã chứng minh rằng có thể phát hiện ra tình trạng căng phồng phổi khi thở với Vt bình thường và viêm phổi ở một tỷ lệ đáng kể bệnh nhân, mặc dù đã sử dụng Vt và Pplat theo phương pháp ‘bảo vệ’. Dựa trên những quan sát này, một số chuyên gia đề xuất mục tiêu Pplat thấp hơn (thường thấp hơn 27 cm H2O). Hạn chế chính của việc sử dụng Pplat như một đại diện thô cho áp lực phổi phụ thuộc vào thực tế là áp lực căng phổi thực sự không phải là áp lực tĩnh của đường thở (phế nang) mà là áp lực xuyên phổi (được thảo luận trong đoạn sau), được xem như sự thay đổi áp lực màng phổi do độ đàn hồi của thành ngực. Trong thực tế, giá trị của Pplat là 30 cm H2O có thể đánh giá quá cao hoặc quá thấp mức độ căng thẳng của phổi ở những bệnh nhân có tính chất cơ học khác nhau của phổi và thành ngực.
Áp lực đẩy
Trong quá trình thở máy, áp lực đẩy đường thở qua hệ thống hô hấp (ΔPrs) được định nghĩa là áp lực do máy thở cung cấp để bơm phồng hệ thống. ΔPrs bằng với sự thay đổi áp lực khí lưu thông giữa PEEP tổng (PEEPtot, tổng của PEEP bên ngoài + PEEP nội sinh) và Pplat cuối hít vào:
Δ Prs = Pplat – PEEPtot phương trình (5)
Ở đây, ΔPrs phải được tính toán trong các điều kiện tĩnh (không có lưu lượng), bằng cách tạm dừng cuối thì hít vào và tạm dừng cuối thì thở ra. Nó có thể dễ dàng được đo tại giường ở những bệnh nhân không nỗ lực hô hấp.
Gần đây, nhiều tác giả đã khẳng định rằng, ở những bệnh nhân mắc ARDS, ΔPrs có thể được coi là đại diện tốt nhất để đánh giá mức độ căng thẳng và biến dạng của phổi (lung stress and strain) tại giường bệnh (Amato và cộng sự 2015). Vì lý do này, việc hạ thấp ΔPrs đã được đề xuất như một phương tiện để giảm nguy cơ VILI. Khái niệm về thông khí bảo vệ phổi dựa trên việc áp dụng các mức Vt thấp hơn, Pplat thấp hơn và PEEP cao hơn, để giảm lượng năng lượng bên ngoài tác dụng lên phổi, chủ yếu là do áp lực động và sức căng do bơm khí lưu thông gây ra (Slutsky và Ranieri 2013). Để đạt được mục tiêu này, Vt nên được chia tỷ lệ theo tỷ lệ phổi có sẵn để thông khí, tương ứng với thể tích phổi cuối thì thở ra (EELV) và được biết là giảm đáng kể ở bệnh nhân ARDS (‘phổi em bé’). Vì các phép đo EELV không có sẵn thường xuyên, nên không nên vượt quá giới hạn Vt là 6 ml kg−1 trọng lượng cơ thể lý tưởng (ideal body weight − IBW). Tuy nhiên, tỷ lệ Vt theo IBW không phản ánh chính xác lượng mô phổi được sục khí và không liên quan đến căng thẳng phổi.
Ngược lại, độ giãn nở của hệ thống hô hấp có liên quan tuyến tính với kích thước của ‘phổi em bé’ (Gattinoni và Pesenti 2005). Vì ΔPrs khi thở bình thường bằng tỷ lệ giữa Vt và Crs theo phương trình
Δ Prs = Vt/Crs phương trình (6)
nó có thể được xem như một cách để bình thường hóa Vt để phổi có khả năng chấp nhận nó, do đó tích hợp hai yếu tố chính của áp lực cơ học. Vì lý do này, việc giới hạn ΔPrs có thể là cách tốt hơn để chuẩn độ Vt theo kích thước thực tế của phổi được sục khí, do đó làm giảm áp lực và sức căng của phổi và có thể cải thiện kết quả của bệnh nhân.
Trong một thử nghiệm hồi cứu quan trọng gần đây, Amato và cộng sự đã phân tích tác động của ΔPrs đối với sự sống sót của bệnh nhân ARDS. Họ đã xem xét dữ liệu riêng lẻ từ 3562 bệnh nhân mắc ARDS đã tham gia vào 9 thử nghiệm ngẫu nhiên và thực hiện phân tích biến trung gian (mediation analysis) để ước tính tác động của những thay đổi ΔPrs do các cài đặt máy thở khác nhau. ΔPrs là biến thông khí có mối liên hệ chặt chẽ nhất với tỷ lệ sống sót; nguy cơ tử vong tương đối tăng đáng kể trên ngưỡng ΔPrs của 14 cm H2O, ngay cả ở những bệnh nhân được thở máy bằng Vt và Pplat ‘bảo vệ’. Thật thú vị, ở những bệnh nhân có giá trị Pplat cao hơn, tỷ lệ tử vong chỉ tăng khi Pplat cao có liên quan đến ΔPrs cao hơn; tương tự, mức PEEP cao hơn chỉ có tác dụng bảo vệ khi kết hợp với ΔPrs thấp. Cuối cùng, ở Pplat không đổi, Vt thấp hơn là một yếu tố dự đoán khả năng sống sót mạnh khi được chuẩn hóa thành Crs (tức là ΔPrs) chứ không phải IBW (Amato và cộng sự 2015).
Ngoài ra, nghiên cứu Lung Safe được công bố gần đây đã xác nhận giá trị tiên lượng mạnh mẽ của ΔPrs, với tỷ lệ tử vong tăng theo ΔPrs (Bellani và cộng sự 2016a, Laffey và cộng sự 2016) (hình 4).
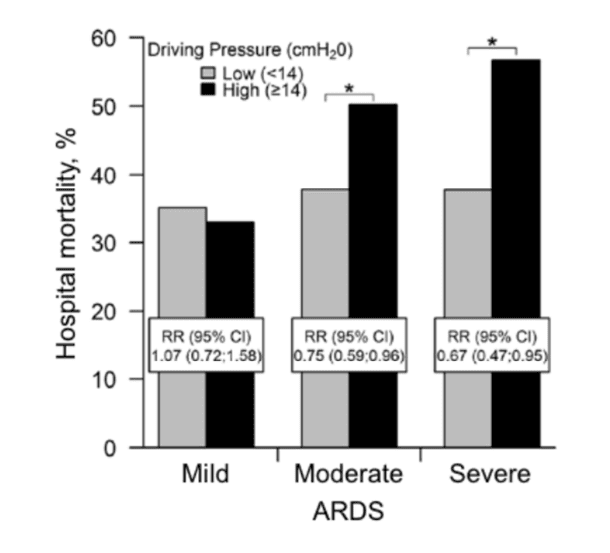

Hình 4. Mối tương quan giữa tăng áp lực đường thở và tỷ lệ tử vong trong ARDS. Trong một nhóm quốc tế lớn gồm các bệnh nhân ARDS tham gia nghiên cứu Lung Safe, áp lực đẩy cao hơn 14 cm H2O có liên quan đến kết quả tồi tệ hơn của ARDS trung bình và nặng. Phỏng theo Laffey và cộng sự (2016). Bản quyền © 2016, Springer-Verlag Berlin Heidelberg và ESICM. Với sự cho phép của Springer.
Tác động tương tự đối với tỷ lệ sống sót đã được báo cáo bởi Guerin và cộng sự, người đã xem xét lại dữ liệu từ hai nghiên cứu ngẫu nhiên lớn trên 787 bệnh nhân ARDS, trong đó Vt và Pplat được duy trì nghiêm ngặt trong giới hạn ‘an toàn’ là 6 ml kg−1 và 30 cm H2O tương ứng. Họ đã tìm thấy mối liên hệ đáng kể giữa ΔPrs và tỷ lệ tử vong, quan sát thấy nguy cơ tử vong tăng 5% đối với mỗi lần tăng 1 cm H2O trong ΔPrs và tỷ lệ tử vong giảm đáng kể khi ΔPrs thấp hơn 13 cmH2O (Guerin và cộng sự 2016). Tuy nhiên, khác với nghiên cứu của Amato, ΔPrs không vượt trội so với Pplat, Vt và Crs với tư cách là yếu tố dự báo tử vong và các tác giả kết luận rằng khi áp dụng nghiêm ngặt các cài đặt máy thở bảo vệ, ΔPrs chia sẻ thông tin tiên lượng giống như Pplat và Crs.
Một hạn chế cố hữu của khái niệm áp lực đẩy đường thở nằm ở chỗ nó thể hiện sự thay đổi áp lực trên toàn bộ hệ thống hô hấp, bao gồm hai cấu trúc nối tiếp nhau, phổi và thành ngực. Như chúng ta đã thấy trong đoạn trước, phần ΔPrs được sử dụng để mở rộng phổi và thành ngực phụ thuộc vào độ giãn nở (hoặc độ đàn hồi) tương đối của chúng.
Do đó, áp lực đẩy xuyên phổi (transpulmonary driving pressure − ΔPL) sẽ phản ánh tốt hơn sự căng thẳng của phổi so với áp lực đẩy đường thở. Ví dụ, ở một bệnh nhân có độ giãn nở phổi (lung compliance − CL) bình thường nhưng độ giãn nở thành ngực (chest wall compliance − Ccw) rất thấp, một Vt nhất định có thể tạo ra ΔPrs cao nhưng ΔPL thấp và do đó căng thẳng phổi thấp.
ΔPL là sự khác biệt giữa giá trị tĩnh của áp lực đường thở và áp lực màng phổi, với áp lực màng phổi được ước tính bằng áp lực thực quản (esophageal pressure − Pes):
ΔPL = (Pplat – end inspiratory Pes) – (PEEPtot – end expiratory Pes) phương trình (7)
Để đánh giá sự khác biệt giữa ΔPrs và ΔPL, Cortes-Puentes và cộng sự (2015) đã thực hiện một nghiên cứu thử nghiệm gây ra những biến đổi có thể đảo ngược của Ccw ở động vật mắc các bệnh lý phổi khác nhau. Đúng như dự đoán, họ phát hiện ra rằng ΔPrs bị ảnh hưởng đáng kể bởi những thay đổi trong Ccw và bởi các đặc tính cơ bản của phổi.
Tuy nhiên, Chiumello và cộng sự gần đây đã đo ΔPrs, ΔPL, áp lực phổi và độ giãn nở phân chia ở 150 bệnh nhân ARDS ở hai mức PEEP (Chiumello và cộng sự 2016). Ở cả hai mức PEEP, ΔPrs cho thấy mối tương quan đáng kể với ΔPL. Hơn nữa, những bệnh nhân có ΔPrs cao hơn có áp lực phổi cao hơn đáng kể và ΔPrs trên 15 cm H2O phát hiện chính xác căng thẳng phổi vượt quá 24 cm H2O.
Áp lực đẩy đường thở và xuyên phổi là những biện pháp đầy hứa hẹn để xác định bệnh nhân có nguy cơ mắc VILI, do mối tương quan của chúng với kết quả của bệnh nhân. Tuy nhiên, vai trò của chúng như là mục tiêu điều trị để chuẩn độ cài đặt thở máy vẫn chưa rõ ràng và cần được đánh giá trong các nghiên cứu ngẫu nhiên trong tương lai.
Áp lực xuyên phổi
Thuật ngữ “áp lực xuyên thành” (transmural pressure) dùng để chỉ áp lực bên trong một ngăn, so với bên ngoài. Trong các kết cấu rỗng, áp lực xuyên thành là áp lực tác dụng lên các vách của kết cấu và, trong điều kiện tĩnh, bằng với áp lực co giãn đàn hồi của khoang. Áp lực xuyên thành của phổi là áp lực xuyên phổi (transpulmonary pressure − PL). Vì áp lực bên trong phổi là áp lực đường thở (áp lực khi mở đường thở, Paw) và áp lực xung quanh phổi là áp lực màng phổi (pleural pressure − Ppl) (Sahetya và Brower 2016):
PL = Paw – Ppl phương trình (8)
Ở đây, PL có thể được chia thành hai phần: áp lực cần thiết để vượt qua sức cản đường thở và tạo ra lưu lượng khí giữa cửa đường thở và phế nang (áp lực trở kháng), và áp lực cần thiết để mở rộng khoang phế nang (do sự co giãn đàn hồi) của phổi và được gọi là áp lực xuyên phế nang (transalveolar pressure − PLel)) (Bellani và cộng sự 2016b). Áp lực xuyên phế nang là áp lực xuyên qua thành phế nang và thể hiện áp lực thực tế tác động lên phổi trong quá trình thông khí. Nó bằng với sự khác biệt giữa áp lực phế nang và màng phổi:
PLel = PAlv – Ppl phương trình (9)
Tuy nhiên, trong điều kiện tĩnh (tức là lưu lượng khí bằng không), áp lực đường thở và phế nang ở trạng thái cân bằng và áp lực xuyên phổi và xuyên phế nang gần như trùng khớp. Ở điều kiện thay đổi, trong điều kiện động, áp lực ở cửa đường thở và áp lực ở phế nang không giống nhau, do áp lực sức cản giảm.
Bây giờ rõ ràng là áp lực xuyên phổi (chứ không phải đường thở) là áp lực ‘thực’ làm căng phổi, gây căng thẳng phổi và VILI, và các cài đặt thông khí cơ học nên được điều chỉnh để nhắm mục tiêu các giá trị PL ‘an toàn’ hơn là Paw. Vì hệ thống hô hấp bao gồm hai cấu trúc đàn hồi nối tiếp nhau, phổi và thành ngực, nên áp lực tác dụng tại lỗ thông khí được sử dụng một phần để làm phồng phổi và một phần để mở rộng thành ngực tùy theo độ giãn nở tương đối của chúng (hoặc đàn hồi) (xem bên dưới). Do đó, áp lực xuyên phổi và đường thở có thể khác biệt đáng kể khi có bất thường thành ngực gây ra giá trị áp lực màng phổi tăng cao. Nói cách khác, cùng một Pplat 30 cm H2O có thể không gây tổn thương ở bệnh nhân có độ giãn nở phổi tương đối bình thường nhưng thành ngực rất cứng, hoặc gây chấn thương sinh học cao ở bệnh nhân có phổi cứng và độ giãn nở của thành ngực bình thường (Mauri và cộng sự 2016).


Hình 5. Áp lực đẩy xuyên phổi như một thước đo căng thẳng phổi nhạy cảm hơn. Áp lực đường thở (Paw), lưu lượng, áp lực thực quản (Pes) và dạng sóng áp lực xuyên phổi (PL) được ghi lại từ một bệnh nhân thở máy kiểm soát thể tích (Vt 500– 7,1 ml kg−1 IBW, nhịp thở 20, PEEP 8 cm H2O) với ARDS trung bình. Sự khác biệt giữa Paw và Pes là PL. Vì Pplat là 17 cm H2O và Pes-ei cuối thì hít vào là 7 cm H2O, kết quả PLei là 10 cm H2O, trong khi PEEP 8 cm H2O trừ Pes cuối thì thở ra (Pes-ee) hiện là 3 cm H2O cho nên PLee là 5 cm H2 Do đó, áp lực đẩy xuyên phổi (ΔPL = 5 cm H2O) ở bệnh nhân này nằm trong giới hạn an toàn (tức là 8–10 cm H2O) Mauri và cộng sự (2016).
Thật không may, không có kỹ thuật đơn giản và an toàn nào cho phép đo trực tiếp Ppl và phương pháp phổ biến nhất được sử dụng để ước tính nó ở đầu giường là đo áp lực thực quản. Áp lực được đo bằng một ống thông chứa đầy không khí được trang bị một quả bóng dài có thành mỏng đặt ở một phần ba dưới của thực quản (Pes) thường được coi là đại diện thay thế hợp lý cho Ppl trung bình xung quanh phổi ở những đối tượng khỏe mạnh, tư thế thẳng đứng. (hình 5).
Tuy nhiên, độ tin cậy của Pes như một ước tính của Ppl ở những bệnh nhân nằm ngửa, thở máy là một vấn đề đáng nghi ngờ, do một số lỗi có thể xảy ra (Mauri và cộng sự 2016). Một số nghiên cứu đã đánh giá PL là mục tiêu cho thở máy. Nghiên cứu phù hợp nhất được tiến hành bởi Talmor và cộng sự trên 61 bệnh nhân mắc ARDS được chỉ định ngẫu nhiên thở máy với PEEP được điều chỉnh dựa trên phép đo Pes hoặc trên bảng PEEP-FiO2 từ các khuyến nghị của Mạng ARDS (Talmor và cộng sự 2008). PL được đánh giá bằng phương pháp ‘tính toán trực tiếp’, tức là bằng cách trừ giá trị tuyệt đối của Pes cho áp lực đo được ở cửa đường thở (PL = Paw − Pes).
Trong nhóm do Pes hướng dẫn, PEEP đã được chuẩn độ để thu được giá trị dương của PL cuối thì thở ra, đồng thời duy trì PL cuối thì thở vào thấp hơn 25 cm H2O; mặt khác, bệnh nhân đối chứng thường có giá trị PL cuối thì thở ra âm tính. Bệnh nhân trong nhóm can thiệp có mức PEEP cao hơn đáng kể liên quan đến sự cải thiện đáng kể về oxygen hóa và độ giãn nở của phổi.
Do độ tin cậy không chắc chắn của các giá trị Pes tuyệt đối là ước tính của Ppl thực tế, một số tác giả đã đề xuất sử dụng phương pháp ‘có nguồn gốc từ đàn hồi’ (Chiumello và cộng sự 2016) để tính PL thay vì phương pháp tính toán trực tiếp mà Talmor sử dụng. Phương pháp này không dựa trên các giá trị Pes tuyệt đối mà sử dụng các biến thể Pes theo nhịp thở để tính toán độ đàn hồi của thành ngực:
Ecw = ΔPes/Vt phương trình (10)
Như đã giải thích ở trên, áp lực tại cửa đường thở là tổng áp lực cần thiết để làm phồng phổi (PL) và áp lực cần thiết để mở rộng thành ngực (Pcw):
Paw = PL + Pcw phương trình (11)
Vì sự thay đổi thể tích của phổi và thành ngực giống hệt nhau nên phương trình có thể được viết là:
Paw/Vt = PL/Vt + Pcw/Vt phương trình (12) là độ đàn hồi của hệ hô hấp (Ers) = Paw/Vt và độ đàn hồi của phổi (EL) = PL/Vt, phương trình có thể được viết là:
PL = Paw x (EL/Ers) phương trình (13)
Grasso và cộng sự đã áp dụng phương pháp này trong một nhóm nhỏ gồm 14 bệnh nhân mắc cúm A được đưa vào ECMO, trong đó PEEP được chuẩn độ để nhắm mục tiêu PL cuối hô hấp là 25 cm H2O, được coi là giới hạn sinh lý trên (Grasso và cộng sự 2012) .
Gulati và cộng sự đã so sánh hồi cứu phép đo Pes trực tiếp và các phương pháp có nguồn gốc từ đàn hồi để ước tính Ppl ở 64 bệnh nhân ARDS. Hai phương pháp không tương quan với nhau, đưa ra các ước tính Ppl khác nhau tới 10 cm H2O đối với một bệnh nhân nhất định. Họ cũng so sánh hai chiến lược tối ưu hóa PEEP (tức là nhắm mục tiêu PL dương tính ở cuối kỳ thở ra bằng cách sử dụng các giá trị Pes tuyệt đối so với nhắm mục tiêu PL là 25 cm H2O cuối thì thở vào bằng phương pháp có nguồn gốc từ đàn hồi) và một lần nữa tìm thấy các kết quả trái ngược và không liên quan đáng kể (Gulati và cộng sự 2013). Nói chung, chúng ta có thể đưa ra giả thuyết rằng sự bất bình đẳng về giá trị Ppl trên ngực có thể đã dẫn đến những khác biệt này.
Tính không đồng nhất
Phổi khỏe mạnh là phổi đồng nhất; ở cuối kỳ thở ra, phổi không bị xẹp và phổi nở ra đều. Sau đó, trong khi hít vào, các lực làm căng nhu mô để tạo ra áp lực phế nang âm và lưu lượng khí hít vào được phân bố đồng nhất trong các cấu trúc có đặc điểm cơ học tương tự trên một đơn vị mô, tạo ra sự giãn nở đồng đều. Trong ARDS, trọng lượng phổi tăng lên do phù nề tổn thương gây ra sụp đổ cấu trúc phế nang. Hầu hết thời gian, xẹp phổi là ở các vùng phổi phụ thuộc (vùng lưng).
Tuy nhiên, sự sụp đổ của các vùng không phụ thuộc nằm trên các đơn vị được sục khí tốt cũng là phổ biến, có thể do sự phân bố không đồng nhất của các tế bào và cytokine gây viêm. Gần đây, tính không đồng nhất này ngày càng được công nhận là một chỉ số liên quan về mức độ nghiêm trọng của ARDS cũng như là yếu tố chính quyết định VILI, với hai khái niệm có thể có mối liên hệ chặt chẽ với nhau (Cressoni 2014).
Một số nhầm lẫn phát sinh do tính không đồng nhất trong các nghiên cứu đã công bố đã được gọi lẫn nhau là cả tính không đồng nhất của thông khí cuối thì thở ra tĩnh và tính không đồng nhất của thông khí thì hít vào động. Đầu tiên đề cập đến sự phân bố không đồng nhất của các vùng phổi được sục khí và xẹp xuống trong phổi ARDS ở cuối thì thở ra; nó thường được đánh giá bằng chụp CT và nó đại diện cho một bức tranh tĩnh về kiểu hình ARDS cụ thể (Cressoni và cộng sự 2014). Mối tương quan đã được chứng minh của biện pháp này với mức độ nghiêm trọng lâm sàng của ARDS có thể xuất phát từ thực tế là sự không đồng nhất về sục khí gây ra sự không đồng nhất về thông khí. Thật vậy, một nghiên cứu trên mô hình ARDS trên động vật cho thấy rằng sự đồng nhất hóa ở cuối thì hít vào với các biến thể nhỏ so với thể tích giãn nở trung bình của các đơn vị phế nang chỉ đạt được ở phổi đã đồng nhất khi thở ra (Mascheroni và cộng sự 1988, Yoshida và cộng sự 2013).
Do đó, tính không đồng nhất của sục khí cuối thì thở ra có thể là dấu hiệu của tính không đồng nhất của thông khí cụ thể hơn (tức là sự giãn nở không đồng đều của các đơn vị phế nang trong thì hít vào). Thật vậy, công trình ban đầu của Mead và cộng sự (Mead và cộng sự 1970) đã chỉ ra làm thế nào khi có sự hiện diện của lực căng (thay đổi áp lực xuyên phổi), căng thẳng cục bộ lên thành phế nang được nhân lên theo phương trình sau:
ΔPL = (V/V0)2/3 phương trình (14)
Ở đây, ΔPL là sự thay đổi áp lực xuyên phổi, V là sự tăng thể tích của các vùng xung quanh và V0 là tăng thể tích của vùng mục tiêu.
Một nghiên cứu khác được thực hiện với PET (Wellman và cộng sự 2014) cho thấy tình trạng viêm cục bộ ở phổi bị tổn thương tỷ lệ thuận với sự mở rộng vùng chia cho thể tích ban đầu, cho thấy rằng phế nang mở rộng nhiều hơn so với thể tích ban đầu có thể chịu áp lực phù hợp hơn. Điều này cho thấy tính không đồng nhất của thông khí có thể là yếu tố gây ra VILI như thế nào và giải thích mối tương quan giữa tính không đồng nhất của sục khí và thông khí với kết quả của ARDS.
Chụp CT cho phép đo chính xác độ không đồng nhất của sục khí ở cuối thì thở ra. Một nghiên cứu của Cressoni và cộng sự đã định lượng tỷ lệ giữa không khí và mô xung quanh ở cấp độ phế nang và cho thấy rằng sự phân bố rải rác hơn có tương quan với mức độ nghiêm trọng của ARDS (Cressoni và cộng sự 2014). Chụp CT cũng có thể được sử dụng để đánh giá tính không đồng nhất của thông khí, nhưng điều này sẽ yêu cầu hai lần chụp CT được thực hiện ở cuối thì thở ra và cuối thì hít vào, điều này sẽ đòi hỏi phải tiếp xúc với bức xạ đáng kể. Tính không đồng nhất của thông khí động có thể được đánh giá tại giường bệnh ở những bệnh nhân được thông khí thể tích có kiểm soát bằng cách đánh giá những thay đổi trong ΔRrs, như đã đề cập trước đây. Giá trị này càng cao, thì sự phân phối lại và phân phối lại xảy ra ở cuối thì hít vào càng nhiều, chứng tỏ sự phân bố thể tích khí lưu thông không đồng đều.
Một phương pháp đầu giường không có bức xạ khác để đánh giá tính đồng nhất của thông khí là EIT (Luepschen và cộng sự 2007, Constantin và cộng sự 2014, Frerichs và cộng sự 2017), cho phép theo dõi liên tục sự phân bố thông khí theo khí lưu thông (hình 6).


Hình 6. Ảnh hưởng của hỗ trợ thấp hơn đối với tính đồng nhất thông khí của bệnh nhân ARDS tự thở. Những hình ảnh này thể hiện sự phân bố địa hình thu được bằng EIT của thông khí ở bệnh nhân ARDS đang được thông khí hỗ trợ áp lực (PSV). Ở bên trái, PSV cao hơn (tức là 12 cm H2O) và các vùng phụ thuộc của phổi thông khí kém (vùng 3 nhận 9% thể tích khí lưu thông và vùng 4 nhận 17%) so với vùng không phụ thuộc (vùng 1 nhận được 31% và vùng 2 nhận được 42%). Ở bên phải, PSV thấp hơn (tức là 3 cm H2O) và các khu vực phụ thuộc hiện nhận được 36% thể tích khí lưu thông, trong khi khu vực không phụ thuộc giảm xuống còn 63%. Mũi tên đỏ biểu thị sự phân phối lại thể tích khí lưu thông đối với phổi phụ thuộc. Đặt PSV ở mức thấp hơn có thể tăng hoạt động của cơ hoành và cải thiện tính đồng nhất của hệ thống thông khí.
Các chỉ số không đồng nhất có nguồn gốc từ EIT dao động từ tỷ lệ đơn giản của thể tích khí lưu thông đến các vùng không phụ thuộc/phụ thuộc đến các phép đo tính không đồng nhất trong khí lưu thông động phức tạp hơn đến chỉ số không đồng nhất toàn cục ở cấp độ pixel hoặc trung tâm thông khí. Cho dù chỉ số nào được xem xét, tất cả chúng đều đề cập đến sự hiện diện của sự mất cân bằng động của sự giãn nở phổi trong khu vực, dẫn đến tăng áp lực xuyên phổi cục bộ và nguy cơ VILI.
Sau khi đo lường được tính không đồng nhất, các cài đặt thông khí nhằm giảm thiểu nó có thể được coi là một bổ sung có giá trị cho các chiến lược thông khí bảo vệ. Cho đến nay, nhiều nghiên cứu đã chỉ ra rằng PEEP điều chỉnh tính đồng nhất (Zhao và cộng sự 2010). Thật thú vị, nó không chỉ đơn giản là PEEP cao hơn mà là các cài đặt được cá nhân hóa để đạt được sự đồng nhất tốt nhất ở mỗi bệnh nhân. Trên thực tế, cả hai mức PEEP thấp với xẹp phổi quá mức và mức cao với căng phổi quá mức đều mang lại sự không đồng nhất. Bằng chứng ở động vật và gián tiếp ở người trưởng thành cho thấy tư thế nằm sấp cũng có thể liên quan đến tính đồng nhất cao hơn (Valenza và cộng sự 2005). Thay vào đó, trong quá trình thở được hỗ trợ, hỗ trợ thấp hơn (Froese 2006, Mauri và cộng sự 2013), sự hiện diện của một số mức độ thay đổi thông khí (Bellani và cộng sự 2012, Blankman và cộng sự 2013, Mauri và cộng sự 2017) và sự mở rộng theo chu kỳ của thở sâu (Mauri và cộng sự 2015) dường như có liên quan đến việc tăng tính đồng nhất.
Tính đồng nhất là yếu tố chính quyết định mức độ nghiêm trọng của ARDS và VILI, có thể thông qua việc tăng căng thẳng cục bộ ở phổi. Nhiều cài đặt được cá nhân hóa của các chế độ thông khí hỗ trợ và kiểm soát có thể giúp giảm thiểu tình trạng này.
Căng quá mức
Căng quá mức (over-distension) thường được gọi là kéo căng phổi khu vực (regional lung stretch) cho đến dung tích sống đặc hiệu (specifc vital capacity). Đối với những người khỏe mạnh, áp lực tại đó hiện tượng này xảy ra là cực kỳ cao và hầu như không bao giờ đạt được (khoảng áp lực xuyên phổi là 20 cm H2O). Tuy nhiên, trong ARDS, với sự hiện diện của xẹp phế nang gây ra shunt trong phổi đòi hỏi PEEP tăng cao và giảm đáng kể độ giãn nở làm tăng áp lực đẩy, các vùng phổi có thể đạt dung tích sống ngay cả khi thông khí lưu thông thể tích thấp (Terragni và cộng sự 2007). Sự căng quá mức gây ra chấn thương khí áp trực tiếp với vỡ nhu mô phổi, gây xuất huyết phế nang, hình thành bóng khí và tràn khí màng phổi. Hơn nữa, sự gia tăng gián tiếp không kiểm soát được chiều dài thành phế nang kích thích các thụ thể đặc hiệu và các tế bào viêm, dẫn đến giải phóng các cytokine và huy động các tế bào và làm tổn thương thêm phổi.
Vì vậy, nên cẩn thận tránh căng quá mức để hạn chế sự phát triển của VILI (Hong và cộng sự 2008, Kuipers và cộng sự 2012). Sự căng quá mức tĩnh cuối kỳ thở ra thường được định lượng bằng chụp CT là lượng đơn vị phổi được sục khí quá mức (tức là các đơn vị có giá trị đơn vị Hounsfield thấp hơn giá trị của nhu mô phổi bình thường). Các đơn vị này rõ ràng phải chịu sự mở rộng quá mức theo nhịp thở và các rủi ro nêu trên, nhưng phương pháp này có thể đánh giá thấp mức độ căng quá mức theo nhịp thở. Thật vậy, các vùng thường được sục khí ở cuối kỳ thở ra có thể bị căng quá mức ở cuối kỳ hít vào.
Đánh giá động của sự giãn nở liên quan đến thể tích khí lưu thông nên được mong muốn trong việc đánh giá sự căng quá mức. Terragni và cộng sự đã thực hiện chụp CT cuối thì thở ra và cuối thì hít vào và cho thấy rằng một phần đáng kể tình trạng căng quá mức có trong phổi của bệnh nhân ARDS ngay cả trong môi trường thông khí bảo vệ, do đó gợi ý nhu cầu về thông khí siêu bảo vệ (ultra-protective ventilation) bằng các phương pháp thay thế để loại bỏ CO2 (Terragni và cộng sự 2009). Tuy nhiên, thực hiện hai lần chụp CT có thể không khả thi trong thực hành lâm sàng hàng ngày và không thể cung cấp phương pháp theo dõi bệnh nhân theo thời gian.
Điểm uốn trên (upper inflection point) của đường cong P/V lưu lượng thấp cho thấy sự thay đổi đột ngột về độ giãn nở của phổi khi đạt đến độ căng quá mức và đó là cách cổ điển để đánh giá nó tại giường bệnh. Giữ Pplat dưới điểm uốn trên có thể là một phương pháp đơn giản và an toàn để tránh hiện tượng căng quá mức lớn. Một phương pháp khác là chỉ số căng thẳng áp lực-thời gian (pressure–time stress index), chỉ số này xác định tình trạng căng quá mức chính bằng sự xuất hiện của độ lõm hướng lên trong dạng sóng đường thở trên máy thở trong quá trình thông khí lưu lượng vuông (xem ở trên). Tuy nhiên, cả đường cong P/V toàn cục và phương pháp chỉ số căng thẳng đều xác định áp lực trung bình mà trên mức đó phổi bị căng quá mức, trong khi một số vùng có thể đã bị căng ra ở áp lực thấp hơn nhiều.
EIT hỗ trợ xác định độ căng quá mức của khu vực bằng ít nhất hai phương pháp. Đường cong P/V ở cấp độ pixel có thể được ghi lại và bản đồ các độ lõm của nó được hiển thị, để chọn áp lực liên quan đến hầu hết các pixel có xu hướng tuyến tính (Becher và cộng sự 2017). Ngoài ra, việc giảm giá trị khu vực của độ giãn nở tĩnh giữa hai điều kiện như hai mức PEEP được coi là dấu hiệu căng quá mức dựa trên EIT, đặc biệt nếu điều này xảy ra ở phổi không phụ thuộc.
Liu và cộng sự đã giới thiệu một phương pháp để phân loại hình ảnh EIT thành các khu vực được thông khí bình thường, bơm căng quá mức, huy động và huy động/mất huy động theo chu kỳ để cung cấp thông tin quan trọng bên giường bệnh (Liu và cộng sự 2016).
Trong thực hành lâm sàng hiện nay, chụp CT được coi là tiêu chuẩn vàng để xác định độ căng quá mức của phổi (nghĩa là mật độ điểm ảnh CT nhỏ hơn −850 HU), nhưng điều này thể hiện một phép đo tĩnh không tương ứng với cơ chế động dẫn đến căng thẳng và vỡ phế nang, thay vào đó, được đánh giá phù hợp hơn bằng các biện pháp EIT động.
Cuối cùng, EIT tạo điều kiện thuận lợi cho việc xác định tình trạng căng quá mức trong quá trình thở tự nhiên do hít vào gắng sức gây ra sự dịch chuyển không khí và hiện tượng pendelluft huyền bí từ phổi không phụ thuộc sang phổi phụ thuộc (Yoshida và cộng sự 2017).
Đánh giá động căng quá mức khu vực có thể là một nhiệm vụ cơ bản để thiết lập hệ thống thông khí bảo vệ và giảm áp lực xuyên phổi cục bộ. Việc giảm căng quá mức có thể thu được trực tiếp thông qua giảm thể tích khí lưu thông và PEEP, hoặc gián tiếp thông qua cải thiện cơ học cục bộ và tính đồng nhất.
Kết luận
Cơ học hô hấp đại diện cho một công cụ đầu giường cực kỳ có giá trị để đánh giá mức độ nghiêm trọng của ARDS, phân tầng bệnh nhân và hướng dẫn điều trị. Một số thông số có thể thu được ngay tại giường bệnh để đo áp lực phổi, độ căng, tính không đồng nhất và mức độ căng quá mức của phổi, cho toàn bộ hệ thống hô hấp hoặc riêng biệt cho phổi và thành ngực. Thời gian dành cho việc đo lường cơ học hô hấp không nên được coi là một bài tập thể chất dành cho các chuyên gia mà là một công việc lâm sàng cập nhật của bệnh nhân ARDS.

COMMENTS